-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Současný pohled na etiologii vysokého vzrůstu dětí a dospívajících (2): Nesyndromický vysoký vzrůst
Current perspectives on the aetiology of tall stature in children and adolescents (2): Non-syndromic tall stature
Non-syndromic tall stature can be caused by growth hormone overproduction, hyperthyroidism, obesity, hypogonadism, precocious puberty or as constitutional growth acceleration. There are conditions caused by a genetic cause as well such as non-sydromic tall stature, typically familial tall stature or, more rarely, pituitary gigantism, which includes X-linked acrogigantism (XLAG). Tall stature can rarely occur in neurofibromatosis type I or in glucocorticoid resistance. After excluding the common endocrinopathies the patients are, in clinical practice, assigned as “familial tall stature” or “constitutional growth acceleration”. Recently, there have been findings showing that non-syndromic tall stature can be caused by a monogenic cause, which can only be found by detailed genetic testing with precise clinical-genetic evaluation.
Keywords:
tall stature – growth hormone overproduction – FIPA – XLAG – familial tall stature
Autoři: Adamovičová Kateřina; Plachý Lukáš; Lebl Jan; Koloušková Stanislava; Průhová Štěpánka
Působiště autorů: 2. lékařská fakulta Univerzity ; Karlovy a Fakultní nemocnice, v Motole ; Pediatrická klinika
Vyšlo v časopise: Čes-slov Pediat 2022; 77 (Supplementum 3): 18-23.
Kategorie: Souborný referát
doi: https://doi.org/10.55095/CSPediatrie2022/054Souhrn
Nesyndromický vysoký vzrůst může vzniknout v důsledku nadprodukce růstového hormonu, hypertyreózy, obezity, hypogonadismu, předčasné puberty či jako konstituční urychlení růstu. Mezi nesyndromický vysoký vzrůst řadíme také některé stavy vzniklé na základě genetické příčiny – familiárně vysoký vzrůst či vzácněji pituitární gigantismus včetně X-vázaného akrogigantického syndromu (XLAG syndrom). Vzácně provází vysoký vzrůst také neurofibromatózu 1. typu či glukokortikoidovou rezistenci. Po vyloučení častějších endokrinopatií jsou v klinické praxi pacienti zařazeni pod popisnou diagnózu „familiární vysoký vzrůst“ či „konstituční urychlení růstu“. V poslední době se ukazuje, že i nesyndromický vysoký vzrůst může vznikat na základě monogenní příčiny, kterou lze nalézt pouze pomocí detailního genetického vyšetření s pečlivým klinicko-genetickým zhodnocením.
Klíčová slova:
vysoký vzrůst – nadprodukce růstového hormonu – FIPA – XLAG – familiárně vysoký vzrůst
Úvod
Vysoký vzrůst je definován jako tělesná výška větší než +2 směrodatné odchylky (SD) pro daný věk a pohlaví.(1) Finální výška je dána souhrou faktorů genetických, hormonálních, nutričních a enviromentálních, které v závěru vedou ke konečné výšce člověka.(2,3)
Na postnatálním růstu se nejvíce podílí růstový hormon (GH, growth hormone), který působí přímo na tkáně přes svůj receptor nebo prostřednictvím stimulace tvorby IGF-1 (inzulinu podobný růstový faktor 1). Ten se váže spolu s IGF - -BP3 (vazebný protein 3. typu pro IGF) a ALS (acidolabilní podjednotka) do ternárního komplexu, který zajišťuje jeho delší životnost.(4) Novější poznatky ukázaly, že oblast řízení růstu daleko přesahuje působení osy GH-IGF-1 a tato osa je pouze jedním z regulačních systémů, které řídí procesy v růstové chrupavce.(5) Na regulaci růstu se významně podílejí také faktory zánětu a další hormony, ale také parakrinní faktory, jako např. fibroblastové růstové faktory (FGFs),(6–9) kostní morfogenetické proteiny (BMPs),(10,11) PTHrP (parathormone related protein), signalizační kaskády WNT (wingless), IHH (indian hedgehog)(12) a CNP-NPR2 (C typ natriuretického peptidu – natriuretický peptidový receptor 2),(11–13) molekuly extracelulární matrix a intracelulární proteiny.
Nesyndromický vysoký vzrůst u dítěte může mít endokrinní příčinu, jako je hypertyreóza, hypogonadismus, předčasná puberta, nadprodukce růstového hormonu či obezita. U většiny dětí ale nedokážeme určit konkrétní příčinu vysokého vzrůstu, a tyto děti tak dostávají diagnózu „idiopatický, resp. familiární vysoký vzrůst“ či „konstituční urychlení růstu“. V poslední době se ukazuje, že i nesyndromický vysoký vzrůst může vznikat na základě monogenní příčiny, kterou lze prokázat nejlépe metodami sekvenování nové generace. Ty dokáží odhalit konkrétní patogenní varianty a pečlivým klinicko-genetickým zhodnocením posoudit jejich vztah k růstové poruše.(14) V současné době přibývá studií zaměřených na vysoký vzrůst, které podobné metody využívají a díky nimž se posunuje vnímání etiologie i u familiárních poruch růstu.(15)
Nadprodukce růstového hormonu
Nadprodukce růstového hormonu (GH) je u dětí vzácná. Bývá způsobena adenomem hypofýzy (obr. 1) produkujícím GH (tzv. somatotropinomem). Adenom může být sporadický nebo geneticky podmíněný. Nativní cirkulující hladiny GH a IGF-1 jsou vysoké.
Obr. 1. Magnetická rezonance hypofýzy u chlapce s mikroadenomem, v tomto případě se somatotropinomem. V důsledku dlouhodobé nadměrné koncentrace GH došlo k rozvoji vysokého vzrůstu, což následně vedlo k tomuto nálezu na MR hypofýzy. 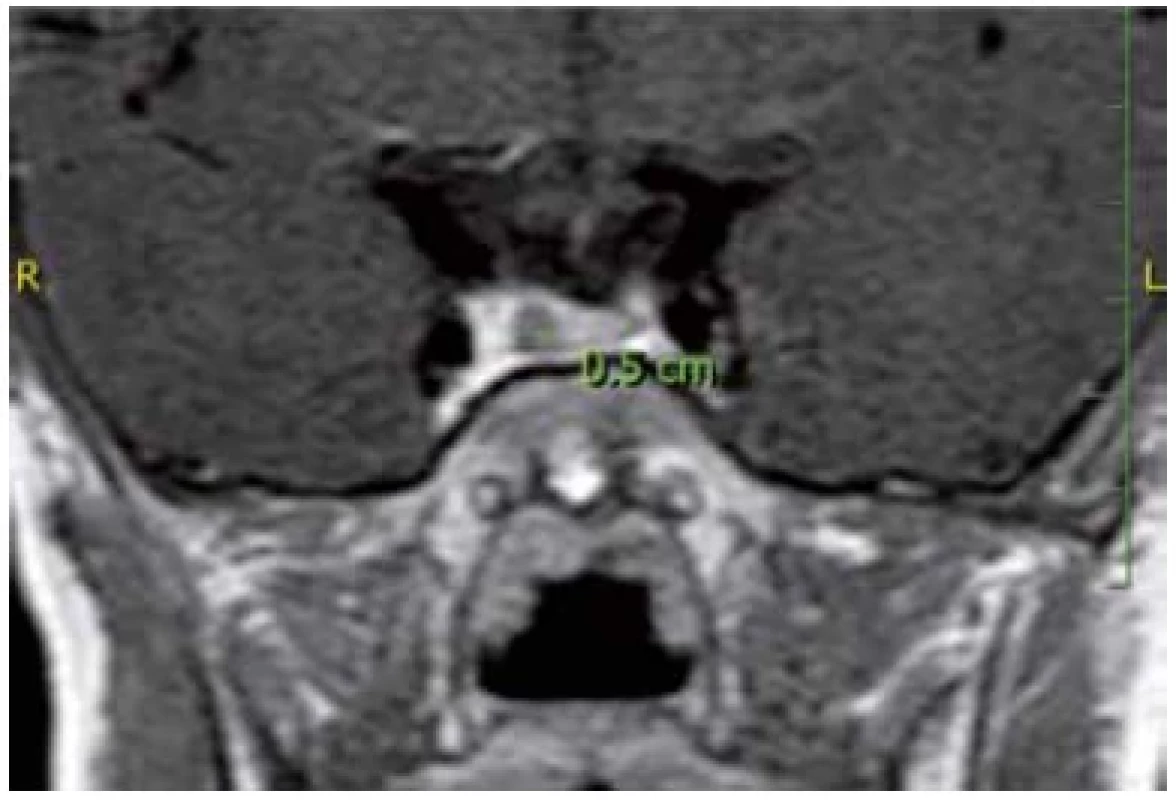
Nadprodukci GH potvrdíme nedostatečným poklesem GH v supresním orálním glukózovém testu, při kterém po dobu 5 hodin koncentrace GH v krvi neklesne pod 1 μg/l. V případě nadprodukce GH před uzavřením růstových plotének vzniká gigantismus (nadměrný, trvale se zrychlující růst), spojený často s urychleným kostním věkem (obr. 2).
Obr. 2. Růstový graf chlapce se somatotropinomem, kde můžeme dle vyznačené černé šipky sledovat urychlení kostního věku a postupné zvyšování růstové rychlosti 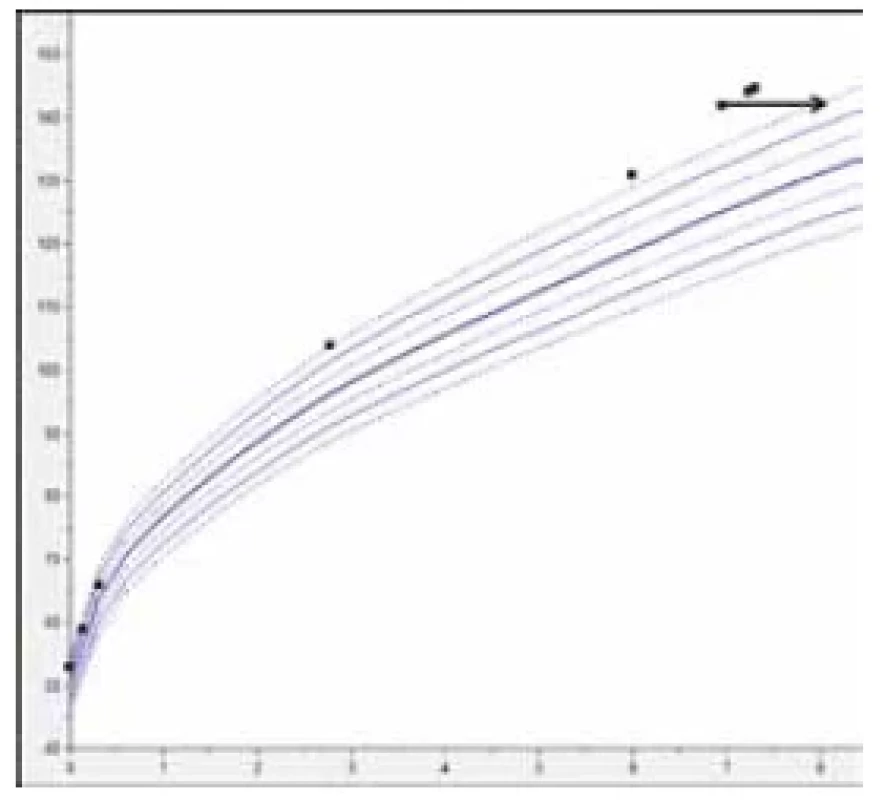
Po uzavření růstových štěrbin se nadprodukce GH projeví rozvojem akromegaloidních rysů (zvětšení rukou a nohou, hrubé rysy v obličeji – prominující nadočnicové oblouky a lícní kosti, prognacie, zvětšování nosu, uší, rtu a jazyka). Velké adenomy mohou navíc být spojeny s poruchami zraku, výpadky v zorném poli (typicky bitemporální hemianopsií), bolestí hlavy a dalšími symptomy nitrolební hypertenze.(3)
Familiární izolované pituitární adenomy (FIPA )
Stav označený jako FIPA je definován přítomností pituitárního adenomu jakéhokoli typu u alespoň dvou členů rodiny bez klinických či genetických známek syndromického onemocnění.(16) FIPA se dědí autozomálně dominantně (AD) s variabilní penetrancí. Dělí se na homogenní typ se stejným typem tumoru v rámci jedné rodiny a heterogenní typ s různým typem adenomů u různých členů rodiny. Nejčastějším typem adenomu v rámci FIPA je prolaktinom (37,5 %), následovaný somatotropinomem (35 %) s nadprodukcí GH a vysokým vzrůstem a/nebo akromegalií, popř. je také možná kombinace somatotropinoprolaktinomu (6,5 %). Asi 20 % FIPA je způsobeno mutací v genu AIP (obr. 3), v 80 % zůstává molekulárně genetická příčina zatím neznámá.(17,18) AIP gen kóduje protein důležitý v mnoha regulačních a funkčních kaskádách. Mechanismus vedoucí ke vzniku adenomů ale nebyl doposud spolehlivě objasněn. Zajímavé je, že AIP protein mimo jiné interaguje s receptorem AHR, který se účastní metabolismu xenobiotik. Dle proběhlé studie byla zjištěna asociace závažnější formy akromegalie s horší odpovědí k farmakoterapii u pacientů s genetickými variantami v genu AHR žijícími ve znečištěných oblastech oproti pacientům s akromegalií a genetickými variantami v AHR, kteří žijí v oblastech s menším znečištěním životního prostředí.( 19)
Obr. 3. Růstový graf dívky s patogenní variantou genu AIP vedoucí k vysokému vzrůstu, který je patrný na růstovém grafu setrvalým růstem nad 97. percentilem 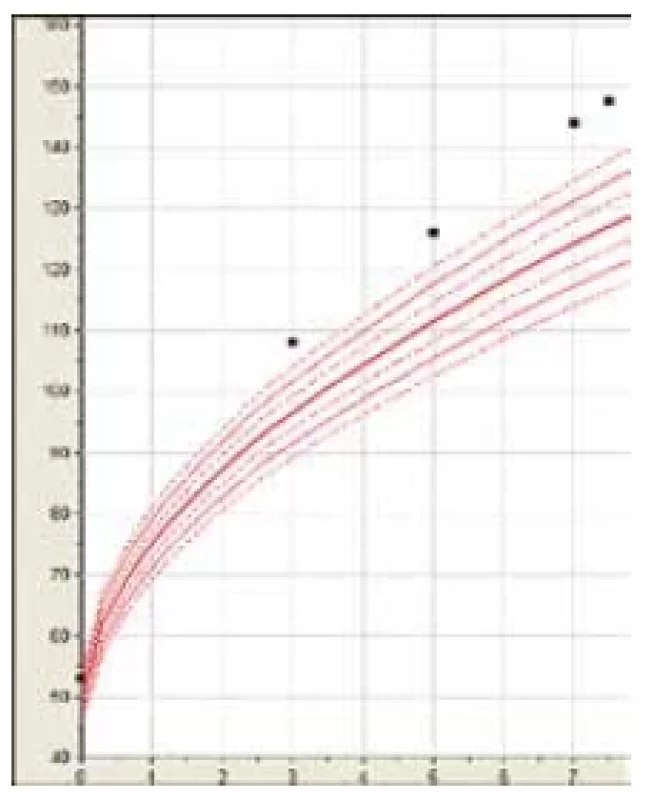
X-LAG
X-vázaný akrogigantický syndrom je velmi vzácná porucha spojená s pituitárním gigantismem. Syndrom je X-dominantně dědičný a je spojen s pituitární hyperplazií nebo s pituitárním adenomem produkujícím růstový hormon, často v kombinaci s nadměrnou sekrecí prolaktinu. Syndrom se objevuje spíše sporadicky, ale je možný také jeho familiární výskyt (poté spadá pod již zmíněný FIPA syndrom) a vykazuje X-vázanou dědičnost. X-LAG syndrom je spojen s velmi časně nastupujícím nadměrným růstem. Postižení chlapci mají od raného věku známky akromegalie.(20) X-LAG syndrom je způsoben duplikací v oblasti Xq26.3, která zahrnuje gen GPR101. Ten kóduje receptor spřažený s G-proteinem. Nadměrná exprese tohoto genu zřejmě vede ke vzniku pituitárního adenomu. Vzácně se u mužů s X-LAG syndromem nachází mozaikový duplicismus, kdy jen část buněk je postižena duplicitou na Xq26.3. U pacientů s X-LAG byla zjištěna zvýšená hladina GHRH, což vede k úvahám o možné dysregulaci na hypotalamické úrovni.(21)
Carneyův complex
Carneyův komplex je multiorgánová porucha, která je ve většině případů způsobena mutací genu PRKAR1A. Ta způsobí ztrátu funkce regulační podjednotky α 1. typu cAMP-dependentní proteinové kinázy. Důsledkem jsou charakteristické kožní léze (pihy, lentiginózní skvrny a skvrny café-au-lait), myxomy, ale také primární pigmentové nodulární onemocnění kůry nadledvin, tumory štítné žlázy, testes a hypofýzy. To je často spojené s nadprodukcí prolaktinu a GH a s následným rozvojem pituitárního gigantismu.(18)
Další endokrinní příčiny vysokého vzrůstu
Obezita
Obezita bývá spojena s urychlením růstu. Obézní děti mají zvýšenou produkci ghrelinu, který stimuluje tvorbu GH. Ghrelin se produkuje převážně ve fundu žaludku, jeho malá část ale také vzniká v hypotalamu, hypofýze, ledvinách či dalších orgánech. Funkce ghrelinu spočívá především ve stimulaci chuti, ale zároveň se účastní regulace sekrece GH pomocí GHS receptoru.(2) Předpokládá se, že na urychlení růstu se podílí i nadměrný přísun kalorií. Na druhou stranu obezita indukuje také časnější dospívání, které ve svém důsledku vede k časnějšímu uzavření růstových štěrbin a ukončení růstu. Obézní děti mohou mít proto v průběhu dětství urychlený růst spojený s urychlením kostního věku, dospělá výška ale bývá normální.(1,2)
Tyreotoxikóza
Nadměrná nabídka tyreoidálních hormonů tkáním je spojena s urychlením růstu a současně urychlením kostního věku.(2) Předpokládá se, že tyreoidální hormony působí synergicky s IGF-1.(3) V případě tyreotoxikózy dominují ostatní klinické projevy, jako je nadměrné pocení, hubnutí, zvýšená střevní motilita aj., které dovedou dítě nebo dospívajícího k lékaři. Po normalizaci hladin tyreoidálních hormonů se normalizuje také růst. Výsledná výška tedy nebývá ovlivněna.(2,3)
Hypogonadismus
Hypogonadální stavy vedou k vysokému vzrůstu v důsledku pozdějšího uzavření růstových plotének, které se uzavírají u obou pohlaví především pod vlivem estrogenů.(2) Vysoký vzrůst vzniká díky prodloužení doby růstu.(3,16) Nebývá nápadný v době dětství, ale projeví se až v době pozdní puberty a mladé dospělosti. Nicméně v současné době by měli hypogonadální jedinci být zachyceni včas na základě úplného chybění nebo nedostatečné progrese puberty.
Předčasná puberta
Centrální gonadotropin-dependentní předčasná puberta vzniká v důsledku předčasné aktivace osy hypotalamus–hypofýza – gonády a vede k rozvoji sekundárních pohlavních znaků u dívek před 8. narozeninami a u chlapců před 9. narozeninami.( 3) Periferní předčasná puberta vzniká na podkladě autonomní produkce pohlavních hormonů, která je nezávislá na ose hypotalamus–hypofýza–gonády.(3) U obou typů předčasné puberty dochází s rozvojem dospívání k pubertálnímu růstovému urychlení spojenému s urychleným kostním zráním, což vede přechodně k nadměrnému růstu (obr. 4). Finální dospělá výška u neblokované puberty však je významně snížena vlivem předčasného uzavření růstových štěrbin.(3)
Obr. 4. Růstový graf dívky s pubertas praecox. Urychlení kostního věku je vyznačeno černými šipkami. 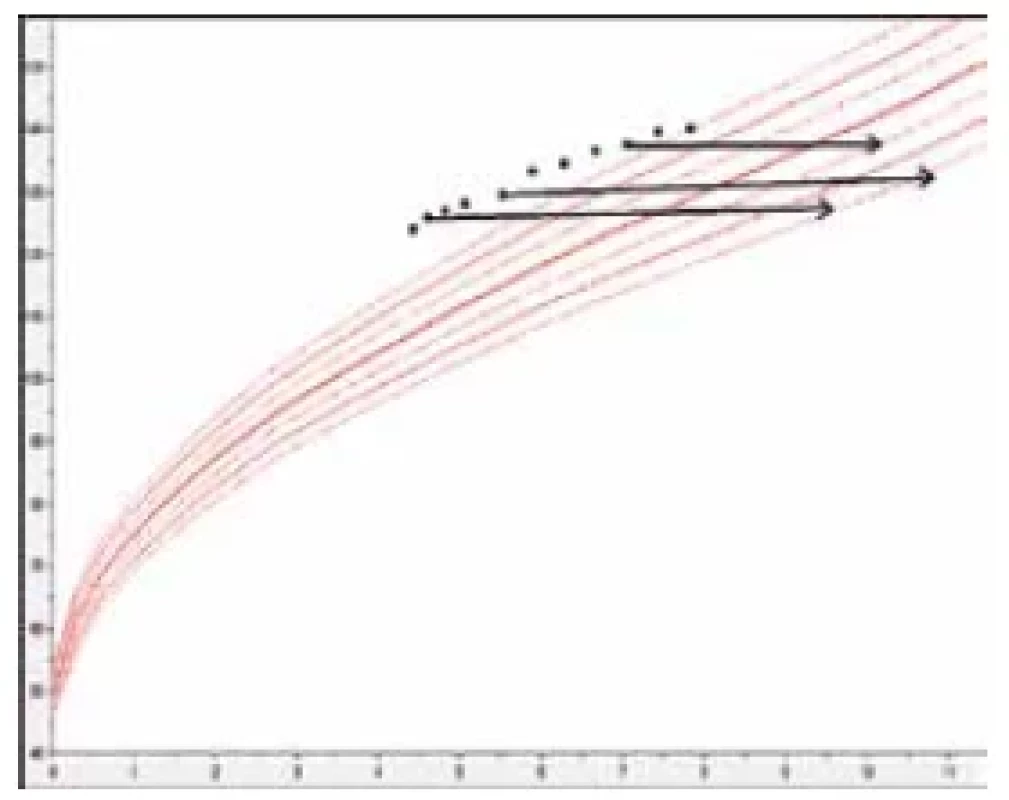
Familiárně vysoký vzrůst
Familiárně vysoký vzrůst (FVV) je dle dostupné literatury nejčastější příčinou vysokého vzrůstu.(3,16) Je definován jako kombinace vysokého vzrůstu dítěte a zároveň vysoké postavy alespoň jednoho rodiče (u muže >194,2 cm, u ženy >179,9 cm). Děti z rodin s FVV rostou v rámci rodičovské predikce, pohybují se v percentilovém grafu ve stejné pozici v rámci celého růstového období a jejich růstová rychlost bývá na horní hranici normy. Kostní věk je úměrný věku chronologickému nebo může být mírně urychlen.(16) V klasickém konceptu je FVV považován za polygenně podmíněný stav, kdy vysoký rodič i rychle rostoucí dítě nesou podobnou kombinaci variant většího množství různých genů zapojených do regulace růstu, které každá jednotlivě nemají výrazný efekt na fenotyp, ale jejich kombinace vede k vysoké postavě.
V poslední době se začínají objevovat práce, které dokládají, že heterozygotní mutace v jednotlivých genech ovlivňujících růstovou ploténku nebo různé regulační kaskády mohou v případě AD dědičnosti samy o sobě vést k FVV (jedná se o monogenně podmíněné stavy). V některých případech je monogenní vysoký vzrůst způsoben mutacemi ve stejných genech, které v případě opačného efektu způsobují vzrůst malý. Příkladem může být inaktivační heterozygotní mutace v genu FGFR3 (receptor 3 pro fibroblastový růstový faktor), jehož aktivační mutace vedou k malému vzrůstu.(11) Podobně může vysoký vzrůst způsobit nadměrná exprese natriuretického peptidu typu C (CNP), důležitého parakrinního regulátoru růstové ploténky, resp. aktivační mutace pro jeho receptor NPR2. Inaktivační mutace v tomto genu naopak vedou k malé postavě.(4) Dalším příkladem je deficit genu SHOX, vedoucí k malému vzrůstu, naopak nadměrný počet jeho kopií vede k vysoké postavě, jako je tomu i u Klinefelterova nebo triple X syndromu(3) nebo u geneticky prokázaných stavů duplikace oblastí obsahujících gen SHOX.
Konstituční urychlení růstu
Konstituční urychlení růstu je diagnóza, kterou dostává jinak zdravé rychle rostoucí dítě v případě, že je běžně dostupnými metodami vyloučena známá příčina vysokého vzrůstu. Dle literatury se jedná o druhou nejčastější příčinu vysokého vzrůstu.(3) Při narození mívají děti normální porodní délku a váhu, ale růstová rychlost se postupně začne zvyšovat. Již během 2.–4. roku se děti dostávají na vysoká percentilová pásma růstového grafu. Růstová rychlost ale dále nestoupá a děti rostou na stejném percentilu po celé růstové období. Kostní věk může být urychlen.(1,15) Na rozdíl od dětí s familiárně vysokým vzrůstem tyto děti často významně překračují rodičovskou predikci. U některých se následně vyvine časná puberta, což jejich finální výšku znormalizuje. Nicméně některé děti svoje rodiče přerostou, aniž by byla zřejmá příčina. Současné generace dětí totiž svoje rodiče již většinou nepřerůstají, protože sekulární trend se v posledních desetiletích významně zpomalil a průměrná výška dospělých se za poslední desetiletí mění již jen minimálně. Nabízí se otázka, zda by podrobnější molekulárně genetické vyšetření dokázalo odhalit změnu, která za nápadně vysokým vzrůstem těchto dětí stojí. V publikované studii Pagani et al. byla prokázána korelace mezi vysokým vzrůstem a zvýšenou expresí receptoru pro GH, který může být považován za jednu z příčin vzniku konstitučního urychlení růstu.(22)
Vzácné příčiny vysokého vzrůstu
Velmi vzácně se může vysoký vzrůst objevit u dítěte s neurofibromatózou 1. typu (NF1), AD onemocněním s multisystémovými projevy, u kterého dojde k rozvoji gliomu hypotalamu. Etiologie vysokého vzrůstu není v tomto případě úplně objasněna, protože naprostá většina pacientů s NF1 má naopak menší vzrůst nebo nižší dospělou výšku, často způsobenou časnou pubertou s malým růstovým výšvihem.(23) Další vzácnou příčinou vysokého vzrůstu je familiární glukokortikoidová rezistence. Jedná se o AR poruchu, která vede k rezistenci k ACTH v nadledvinách způsobující izolovaný deficit kortizolu s vysokými hladinami ACTH. Mechanismus vzniku vysokého vzrůstu na základě zvýšené sekrece ACTH není zatím přesně objasněn.(24,25)
Současné diagnostické algoritmy
Pacienti s vysokým vzrůstem přicházejí k odbornému vyšetření obecně méně často než pacienti s malým vzrůstem, protože vysoká výška se považuje ve společnosti spíše za benefit. Nicméně především dívky mohou vysokou výšku vnímat jako nežádoucí. Vyšetřování příčin vysokého vzrůstu je ale důležité u obou pohlaví. Ačkoli zjištění příčiny nemusí vést k zajištění léčby, je i přesto důležité k vyloučení příčin vyžadujících intervenci.(15)
Každé dítě s růstem nad 97. percentilem by mělo být vyšetřeno erudovaným dětským endokrinologem. Jak bylo popsáno výše, ani děti z rodin s FVV by neměly být vyloučeny z vyšetřovacího programu. Zvláště pozdě diagnostikované pituitární adenomy u FIPA jsou smutným příkladem zbytečně odloženého vyšetření u vysokých dětí vysokých rodičů.
Diagnostický algoritmus nyní zahrnuje tyto kroky:
1) Celkové zhodnocení růstu dítěte v percentilovém grafu, posouzení růstové rychlosti a proporcionality růstu.
2) P osouzení vývoje puberty a kostního věku.
3) Stanovení hladiny pohlavních hormonů a hormonů štítné žlázy.
4) Stanovení hladiny nativního GH a IGF-1, případně supresního orálního glukózového tolerančního testu při podezření na nadprodukci GH.
5) Vyšetření karyotypu i bez klinického podezření na syndromy spojené s abnormálním počtem chromozomů.
6) U pacientů se známkami mentální retardace, autismu, příp. s vrozenými vývojovými vadami je vhodné provedení molekulárně genetického vyšetření dle indikace klinického genetika (např. geny FMR1 a NSD1).
7) U pacientů s marfanoidním habitem vyšetření genu FBN1, oftalmologické a kardiologické vyšetření a stanovení hladin homocysteinu.
8) D alší vyšetření – např. zobrazení CNS dle předchozích výsledků.
9) Výzkumně mohou být využity některé z moderních molekulárně genetických vyšetření k podrobnějšímu stanovení genetické příčiny VV.
Diagnostické schéma je znázorněno na obr. 5.
Obr. 5. Diagnostický algoritmus u dítěte s vysokým vzrůstem v ambulanci dětského endokrinologa – upraveno dle(16) 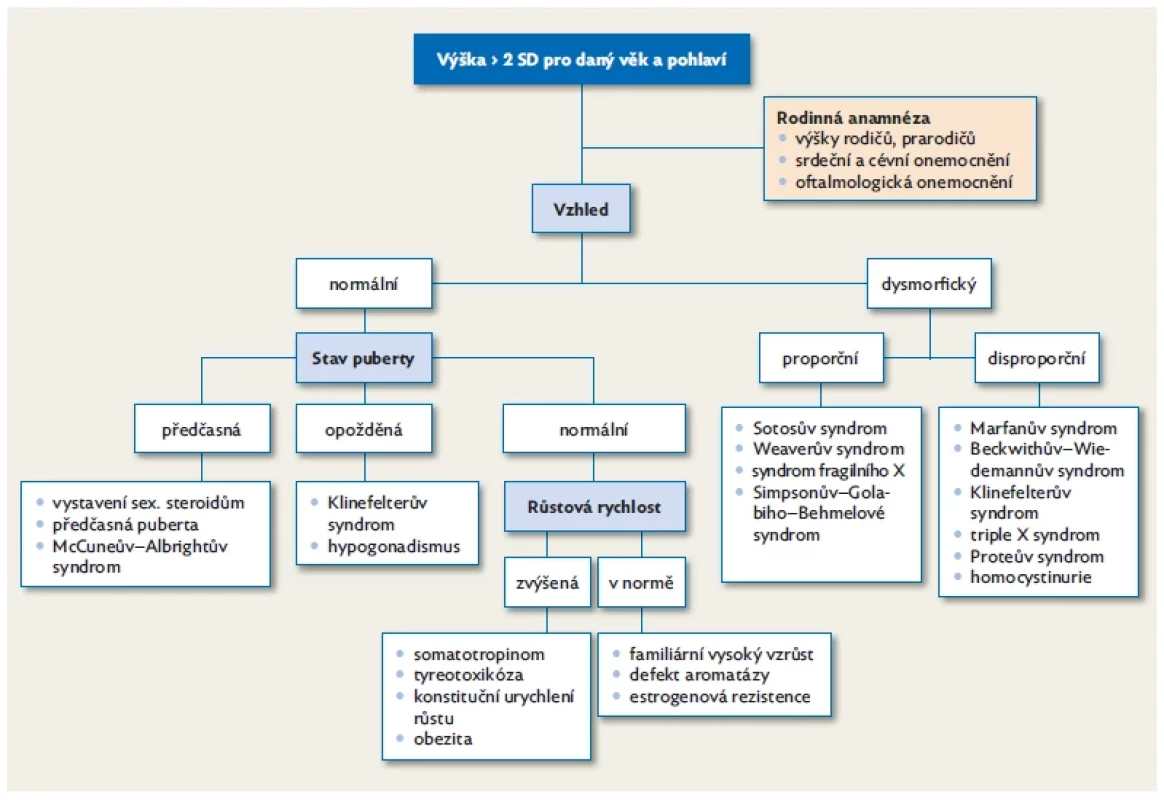
Závěr
Vysoký vzrůst je společensky přijatelnější než malý vzrůst, a je proto méně často důvodem k odbornému vyšetření. Příčiny nesyndromického vysokého vzrůstu jsou různé, některé mohou být spojeny s potenciálními riziky pro další vývoj a život dítěte. Úkolem dětského endokrinologa je tato onemocnění včas odhalit a adekvátně je řešit. Výzkum regulace dětského růstu a jeho patologií v posledních letech významně postoupil a umožňuje nám lépe pochopit nejen příčiny, ale i důsledky změn, které k nadměrnému vzrůstu vedou. Díky novým diagnostickým metodám za pomoci např. metod sekvenování nové generace máme možnost odhalit některé genetické příčiny vysokého vzrůstu a popsat detailně i jemné změny fenotypu a další rizika, která se s vysokým vzrůstem vážou.
Výzkum genetických příčin vysokého vzrůstu je podpořen grantovou agenturou AZV NU21-07-00335.
Korespondenční adresa:
MUDr. Kateřina Adamovičová
V Úvalu 84
150 06 Praha 5
katerinaadamovicova@email.cz
Zdroje
- Meazza C, Gertosio C, Giacchero R, et al. Tall stature: a difficult diagnosis? Ital J Pediatr 2017;43(1):66.
- Albuquerque E, Scalco RC, Jorge A. Management of endocrine disease: Diagnostic and therapeutic approach of tall stature. Eur J Endocrinol 2017; 176(6): 339–353.
- Leung AKC, Leung AAC, Hon KL. Tall stature in children. Adv Pediatr 2019; 66 : 161–176.
- Wei C, Gregory JW. Physiology of normal growth. Paediatrics Child Health 2009; 19(5): 236–240.
- Baron J, Sävendahl L, De Luca F, et al. Short and tall stature: a new paradigm emerges. Nat Rev Endocrinol 2015; 11(12): 735–746.
- Lazarus JE, Hegde A, Andrade AC, et al. Fibroblast growth factor expression in the postnatal growth plate. Bone 2007; 40(3): 577–586.
- Liu Z, Lavine KJ, Hung IH, Ornitz DM. FGF18 is required for early chondrocyte proliferation, hypertrophy and vascular invasion of the growth plate. Dev Biol 2007; 302(1): 80–91.
- Mancilla EE, De Luca F, Uyeda JA, et al. Effects of fibroblast growth factor-2 on longitudinal bone growth. Endocrinology 1998; 139(6): 2900–2904.
- Hung IH, Yu K, Lavine KJ, Ornitz DM. FGF9 regulates early hypertrophic chondrocyte differentiation and skeletal vascularization in the developing stylopod. Developmen Biol 2007; 307(2): 300–313.
- Nilsson O, Parker EA, Hegde A, et al. Gradients in bone morphogenetic protein–related gene expression across the growth plate. J Endocrinol 2007; 193(1): 75–84.
- De Luca F, Barnes KM, Uyeda JA, et al. Regulation of growth plate chondrogenesis by bone morphogenetic protein-2. Endocrinology 2001; 142(1): 430–436.
- Hannema SE, van Duyvenvoorde HA, Premsler T, et al. An activating mutation in the kinase homology domain of the natriuretic peptide receptor-2 causes extremely tall stature without skeletal deformities. J Clin Endocrinol Metab 2013; 98(12): 1988–1998.
- Miura K, Kim OH, Lee HR, et al. Overgrowth syndrome associated with a gain–of–function mutation of the natriuretic peptide receptor 2 (NPR2) gene. Am J Med Genet A 2014; 164 A (1): 156–163.
- Chan Y, Holmen OL, Dauber A, et al. Common variants show predicted polygenic effects on height in the tails of the distribution, except in extremely short individuals. PLoS Genet 2011; 7(12): e1002439.
- Plachy L, Dusatkova P, Maratova K, et al. Familial short stature—a novel phenotype of growth plate collagenopathies. J Clin Endocrinol Metabolism 2021; 106(6): 1742–1749.
- Corredor B, Dattani M, Gertosio C, Bozzola M. Tall stature: a challenge for clinicians. Curr Pediatr Rev 2019; 15(1): 10–21.
- Vasilev V, Daly AF, Trivellin G, et al. Hereditary endocrine tumours: current state-of-the-art and research opportunities: The role of AIP and GPR101 in familial isolated pituitary adenomas (FIPA ). Endocr Rel Cancer 2020; 27(8): T77–T86.
- Beckers A, Petrossians P, Hanson J, Daly AF. The causes and consequences of pituitary gigantism. Nat Rev Endocrinol 2018; 14(12): 705–720.
- Cannavo S, Ragonese M, Puglisi S, et al. Acromegaly is more severe in patients with AHR or AIP gene variants living in highly polluted areas. J Clin Endocrinol Metab 2016; 101(4): 1872–1879.
- Daly AF, Lysy PA , Desfilles C, et al. GHRH excess and blockade in X–LAG syndrome. Endocr Rel Cancer 2016; 23(3): 161–170.
- Beckers A, Lodish MB, Trivellin G, et al. X-linked acrogigantism syndrome: clinical profile and therapeutic responses. Endocr Rel Cancer 2015; 22(3): 353–367.
- Pagani S, Radetti G, Meazza C, Bozzola M. Analysis of growth hormone receptor gene expression in tall and short stature children. J Pediatr Endocrinol Metab 2017; 30(4): 427–430.
- Carmi D, Shohat M, Metzker A, Dickerman Z. Growth, puberty, and endocrine functions in patients with sporadic or familial neurofibromatosis type 1: a longitudinal study. Pediatrics 1999; 103(6): 1257–1262.
- Meimaridou E, Hughes CR, Kowalczyk J, et al. Familial glucocorticoid deficiency: New genes and mechanisms. Mol Cell Endocrinol. 2013; 371(1–2): 195–200.
- Savage MO, Lebrethon MC, Blair JC, et al. Growth abnormalities associated with adrenal disorders and their management. Horm Res 2001; 56 Suppl 1 : 19–23.
Štítky
Neonatologie Pediatrie Praktické lékařství pro děti a dorost
Článek vyšel v časopiseČesko-slovenská pediatrie
Nejčtenější tento týden
2022 Číslo Supplementum 3- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Fexofenadin – nesedativní a imunomodulační antihistaminikum v léčbě alergických projevů
- Efektivita kartáčku Sonicare For Kids u dětí předškolního věku
- Aktuální možnosti léčby HAE v dětském věku
-
Všechny články tohoto čísla
- Současný pohled na etiologii vysokého vzrůstu dětí a dospívajících (1): Syndromy spojené s vysokým vzrůstem
- Současný pohled na etiologii vysokého vzrůstu dětí a dospívajících (2): Nesyndromický vysoký vzrůst
- Endokrinní příčiny obezity v dětství a adolescenci
- Nesoulad rodu a pohlaví v dětství a adolescenci: současné názory a přístupy, situace v České republice
- První zkušenosti s dlouhodobě působícím růstovým hormonem
- Vážení kolegové, přátelé, pediatři z primární péče, z regionálních nemocnic i z klinik,
- Mystický Hagibor a jeho místo v historii české pediatrie
- Minipuberta – významné a dosud opomíjené období pohlavního vývoje
- Česko-slovenská pediatrie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Minipuberta – významné a dosud opomíjené období pohlavního vývoje
- První zkušenosti s dlouhodobě působícím růstovým hormonem
- Současný pohled na etiologii vysokého vzrůstu dětí a dospívajících (1): Syndromy spojené s vysokým vzrůstem
- Nesoulad rodu a pohlaví v dětství a adolescenci: současné názory a přístupy, situace v České republice
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



