-
Medical journals
- Career
Resuscitace novorozence, kardiopulmonální resuscitace dětí
Authors: Hrdlička René
Authors‘ workplace: Dětské oddělení Oblastní nemocnice Kolín a. s., nemocnice Středočeského kraje
Published in: Čes-slov Pediat 2022; 77 (2): 94-102.
Category: Chapters for Specialization in Pediatrics
Overview
Aktuální doporučené postupy pro resuscitaci vycházejí z konsenzuálních stanovisek a léčebných doporučení z roku 2020. Byly uveřejněny jako doporučení Evropské resuscitační rady v roce 2021. Resuscitace dětí představuje samostatnou kapitolu a týká se resuscitace pro věkovou kategorii 0–18 let s výjimkou novorozenců bezprostředně po porodu. Resuscitaci novorozenců po porodu je věnována samostatná kapitola. V článku jsou uvedeny postupy při základní i rozšířené pediatrické resuscitaci s důrazem na zajištění dýchání a krevního oběhu. U resuscitace novorozenců jsou probrány terapeutické postupy na porodním sále a následné zajištění péče o novorozence s poruchou poporodní adaptace. Jsou uvedena kritéria nezahájení resuscitace a jejího ukončení.
Klíčová slova:
deti – novorozenci – resuscitace – dýchání – krevní oběh
Úvod
Kardiopulmonální resuscitace (KPR) je definována jako soubor intervencí prováděných za účelem zachování dodávky kyslíku během srdeční zástavy.(1) V řadě případů je však resuscitace zahájena i při zachovaném krevním oběhu s cílem předejít asystolii. Důvodem ke kardiopulmonální resuscitaci je u dospělých pacientů nejčastěji náhlá srdeční zástava. Podle American Heart Association i v současnosti téměř 95 % dospělých pacientů zemře před přijetím do nemocnice.(2) Rozhodujícím kritériem prognózy pacientů po srdeční zástavě je časový interval mezi srdeční zástavou a zahájením resuscitace a kvalita prováděné resuscitace.(3,4) Odlišná je situace u pediatrických pacientů, kde je primární srdeční zástava relativně vzácná a je omezena hlavně na pacienty s kritickými srdečními vadami a po kardiochirurgických výkonech. Jejich zastoupení se udává mezi 4–10 % ze všech pediatrických resuscitací prováděných mimo nemocnici a ani v nemocničním prostředí není tento počet o mnoho vyšší, představuje asi 15 % pediatrických resuscitací.(5) Příčnou většiny stavů, které vedou v pediatrii k nutnosti resuscitace, je sekundární zástava při těžké hypoxii myokardu na podkladě vyčerpání kompenzačních mechanismů. Primární příčinou je respirační selhání nebo oběhové selhání při dekompenzovaném šoku. Z tohoto důvodu je pak výsledek resuscitace po srdeční zástavě u dětí uspokojivý jen v malém počtu případů. Lepší výsledky jsou při srdeční zástavě u pacientů monitorovaných na jednotkách intenzivní péče (JIP), kde počet přežití dosahuje 45 % a většina přeživších pacientů má jen minimální neurologické postižení.(6)
Historie
Snaha o obnovení základních životních funkcí má dlouhou historii a písemné prameny lze nalézt již v nejstarších kulturních artefaktech. První zdokumentovaná úspěšná resuscitace byla referována Královské společnosti v Londýně v roce 1744.(7) Přelomem v úspěšnosti resuscitace bylo zavedení dvou technik, které se s relativně malými úpravami používají dodnes. Je to asistovaná ventilace a nepřímá masáž srdeční. Techniku asistované ventilace metodou dýchání z úst do úst a její modifikaci s použitím samorozpínacího vaku popsal v 50. letech 20. století prof. Peter Safar. Následně pak byla publikována technika nepřímé srdeční masáže, kterou popsal William B. Kouwenhoven.(8) Z jejich prací vychází resuscitační postupy dosud. Prof. Safar byl významnou lékařskou osobností. Pro českou lékařskou veřejnost je určitě zajímavá skutečnost, že pocházel z rodu Šafařů z východních Čech a při svých návštěvách Československa se k českému původu hlásil.(9)
Rozdělení resuscitačních postupů
Popis a účinnost nových resuscitačních postupů byly publikovány začátkem 60. let 20. století.(10) V současné době jsou resuscitační postupy celosvětově koordinovány Mezinárodním výborem pro součinnost v resuscitaci (ILCOR). Na aplikaci resuscitačních postupů se v Evropě podílí European Resuscitation Council (ERC). ERC byl založen v roce 1989, první doporučení, představená v roce 1992, zahrnovala základní a rozšířenou resuscitaci. Pediatrická problematika byla následně doplněna v roce 1994. ERC v současné době sdružuje 33 národních resuscitačních rad, Česká republika je zastoupena Českou resuscitační radou. ERC aktualizuje resuscitační postupy každých 5 let, aktuální doporučení jsou z roku 2021 a jsou v originále publikována na https://cprguidelines. eu. Současné resuscitační postupy rozdělujeme na základní resuscitaci – basic life suppport (BLS) a rozšířenou – advanced life support (ALS). Z věkového hlediska rozdělujeme resuscitaci na resuscitaci dospělých, resuscitaci dětí a resuscitaci novorozenců. Resuscitace novorozenců představuje specifickou oblast resuscitace a týká se jen novorozenců bezprostředně po porodu. Novorozenci po ukončení poporodní adaptace spadají do skupiny dětských resuscitací. Následně uváděné resuscitační postupy vycházejí ze souhrnu doporučení ERC z roku 2021,(11) která byla doplněna i českou verzí.(12)
Organizace resuscitační péče
Resuscitaci je povinen zahájit nejen každý zdravotník, ale každý občan. Výjimkou jsou situace, kdy je zachránce vystaven nebezpečí. Neposkytnutí první pomoci může být posouzeno jako trestný čin podle zákona č. 40/2009 Sb. (trestní zákoník). Resuscitace mimo zdravotnické zařízení pak zahrnuje nejen vlastní resuscitaci, ale rovněž přivolání odborné pomoci – Zdravotnické záchranné služby (ZZS). Tu lze přivolat telefonicky na linkách tísňového volání 155 a 112 a rovněž využitím aplikace Záchranka. V tomto případě dojde nejen k automatickému vytočení čísla 155, ale také k odeslání souřadnic aktuální polohy volajícího. Při volání je vždy nezbytné zachovat hlasitý odposlech. Organizace resuscitace v nemocnici je organizována podle vnitřních směrnic zdravotnického zařízení. Resuscitací jsou obvykle pověřeny resuscitační týmy složené nejčastěji z pracovníků anesteziologicko-resuscitačních oddělení či pracovišť intenzivní medicíny. Nicméně do jejich příchodu je nezbytné, aby resuscitaci prováděl zdravotník přítomný na místě zástavy.
Základní postupy resuscitace:
- Nepřímá srdeční masáž – spočívá ve stlačování dolní poloviny sterna, u dětí je nutné stlačení do ⅓ předozadního průměru hrudníku, u dospělých pacientů je optimální stlačení 5 cm. V žádném případě by hloubka komprese neměla přesáhnout 6 cm. Frekvence kompresí se pohybuje mezi 100–120/min.
- Umělá ventilace – v některých případech vede k obnovení ventilace samotné zprůchodnění dýchacích cest. U malých kojenců je dostačující neutrální poloha hlavy vzhledem k tělu, u ostatních pacientů je nutný záklon hlavy. Dále se provede přizvednutí brady vzhůru. Pokud se spontánní dechová aktivita neobnoví, je nutné přistoupit k umělé ventilaci. Technika dýchání z úst do úst se v případě resuscitace zdravotnickým pracovníkem nahradí dýcháním samorozpínacím vakem (je-li k dispozici). Ventilaci vakem je nutno provádět přes obličejovou masku adekvátní velikosti. Pokud je zachránců více, aktuální resuscitační postupy preferují fixaci obličejové masky oběma rukama a ventilaci druhým zachráncem (obr. 1). Účinnost ventilace a přiměřenost dechového objemu kontrolujeme podle dechových exkurzí hrudníku.
Image 1. Aktuální resuscitační postupy preferují držení obličejové masky oběma rukama 
- Defibrilace – jak bylo uvedeno, nutnost defibrilace je u pediatrických pacientů relativně vzácná, konkrétní případy budou uvedeny v dalším textu. Resuscitaci vždy provádíme do obnovení příznaků spontánního krevního oběhu (restore of spontaneous circulation – ROSC).
Základní resuscitace dětí (PBLS)
Důležitou změnou v aktuálním doporučení je definice cílové skupiny v této kategorii pacientů. Jedná se o všechny pacienty do 18 let s výjimkou novorozenců resuscitovaných bezprostředně po porodu. Děti, které vypadají jako dospělí, tzn. s vyvinutými sekundárními pohlavními znaky, je však možno resuscitovat i podle souhrnu doporučení pro resuscitaci dospělých. Jedná se o racionální doporučení, kdy v řadě případů nelze v okamžiku zahájení resuscitace určit přesný věk pacienta. Základní podmínkou pro zahájení efektivní resuscitace je rychlé rozpoznání stavu indikovaného k zahájení resuscitace. V případech, kdy nutnost resuscitace není zcela jasná, je indikováno využití nástroje rychlého zhodnocení stavu (quick-look). Lze využít například pediatrický hodnoticí trojúhelník, umožňující rychlé zhodnocení stavu dítěte. Uplatňuje se zde zhodnocení celkového stavu dítěte, dechové práce a prokrvení kůže.(13) Patologie v kterémkoli bodu trojúhelníku je indikací k zahájení intenzivní léčby či resuscitace. O kritickém stavu dítěte svědčí nejen zástava oběhu či dýchání, ale rovněž další klinické známky či laboratorní hodnoty. Zahrnujeme mezi ně těžkou poruchu vědomí s absencí cílené reakce na algický podnět a prodloužení kapilárního návratu.(14) Z laboratorních hodnot pak nízká hodnota pH při těžké acidóze dokumentuje vyčerpání kompenzačních mechanismů organismu s rizikem kardiální zástavy.
Zahájení resuscitace dítěte představuje okamžité provedení pěti úvodních dechů, a pokud nadále nejsou přítomny známky života, následuje 15 stlačení hrudníku. Je-li zachránce sám, měl by před zahájením resuscitace zavolat ZZS. Pokud nemá zachránce telefon k přivolání ZZS u sebe, má provádět KPR po dobu jedné minuty a pak teprve přivolat pomoc. Při náhle vzniklém bezvědomí bez jasné příčiny je vhodné aktivovat AED, je-li snadno dostupný. Cílovou hodnotou periferní saturace O2 (SpO2) je 94–98 %. Do zavedení monitorace SpO2 je indikováno použití vysokoprůtokového kyslíku k zajištění asistované ventilace.
Souhrn resuscitačních postupů se označuje jako postup ABCDE, při zjištění patologie v jednotlivých bodech je nutné vždy adekvátně reagovat a po intervenci zhodnotit efekt intervence:
- A – dýchací cesty (airway) – zprůchodněte dýchací cesty a udržujte je průchodné. Fyziologické hodnoty ventilace jsou uvedeny v tabulce 1.
Table 1. Normální hodnoty dechové frekvence vzhledem k věku 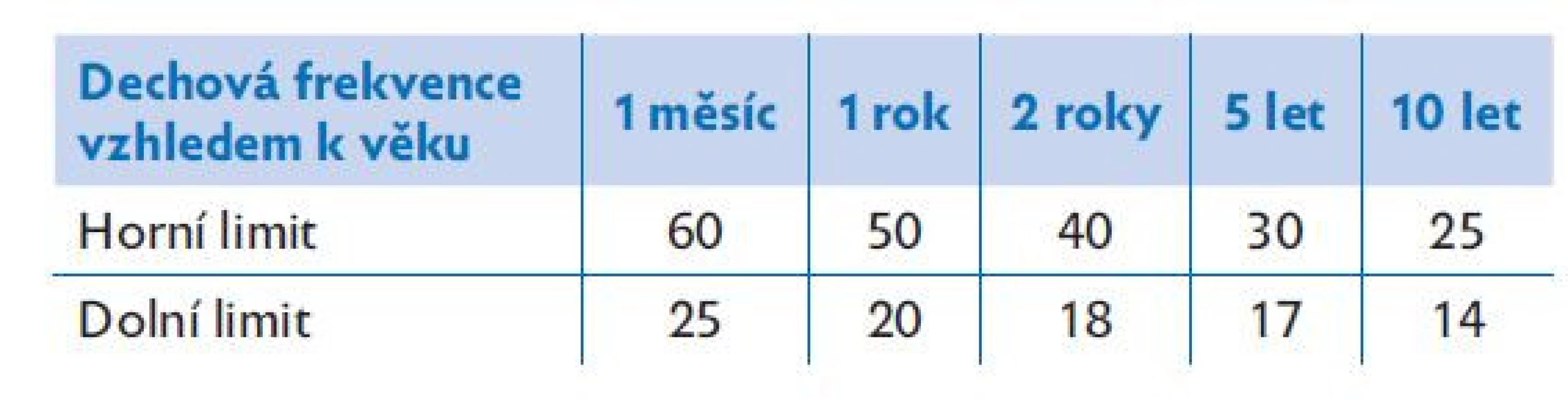
- B – dýchání (breathing) – hodnotí se dechová frekvence a její trend. Důležité je zhodnocení dechové práce (zatahování, grunting, alární souhyb) a oxygenace.
- C – krevní oběh (circulation) – do tohoto bodu patří zhodnocení tepové frekvence, krevního tlaku a periferního prokrvení. Pro zhodnocení stavu cirkulace je přínosem provedení echokardiografie. Fyziologické hodnoty tepové frekvence jsou uvedeny v tabulkách 2 a 3. K posouzení stavu krevního oběhu je vhodné doplnit opakované vyšetření laktátu.
Table 2. Normální hodnoty tepové frekvence vzhledem k věku 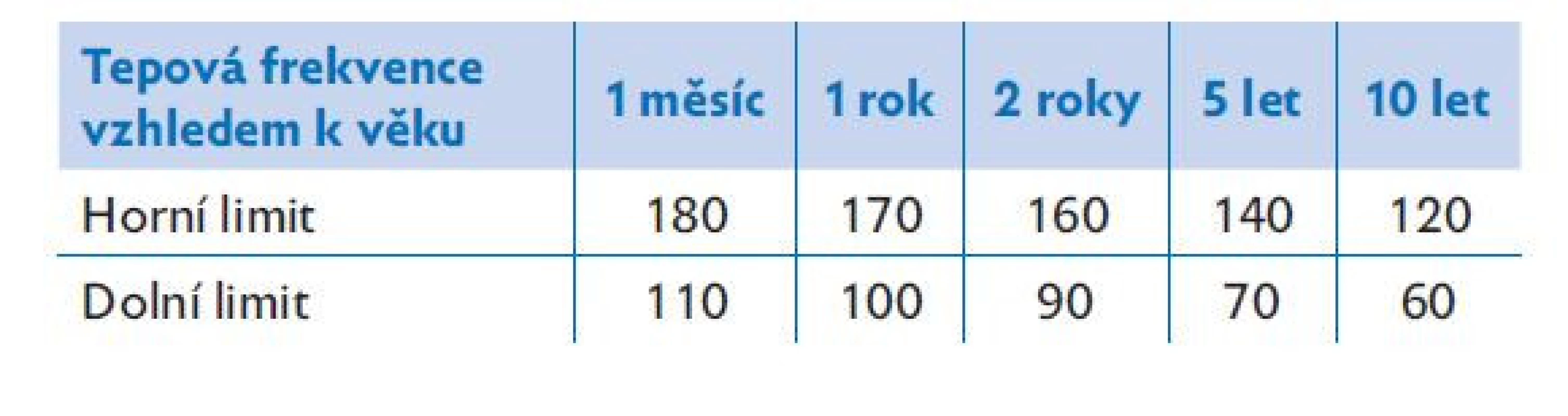
Table 3. Normální hodnoty středního arteriálního tlaku (MAP) u dětí (5. a 50. percentil) 
- D – neurologický stav (disability) – k hodnocení stavu vědomí využíváme skórovací schémata, nejčastěji používané Glasgow Coma Scale (GCS) je uvedeno v tabulce 4 včetně varianty pro malé děti. Toto vyšetření je nutné doplnit vyšetřením stavu zornic, jejich symetrie a reakce na osvit. Důležité je zaznamenat případnou neurologickou symptomatologii (přítomnost křečí, ložiskového neurologického nálezu).
Table 4. Hodnocení poruchy vědomí podle Glasgow Coma Scale 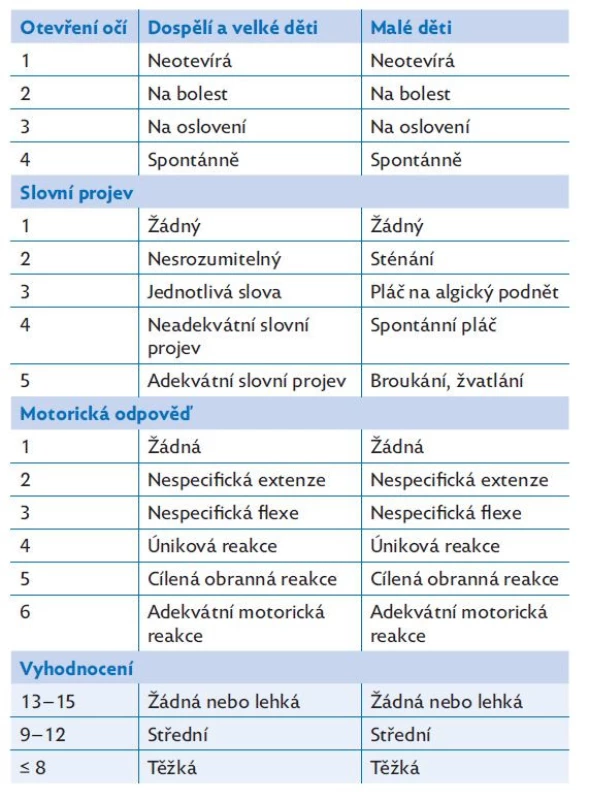
- E – celkové vyšetření (exposure) – celkové vyšetření a zhodnocení stavu pacienta k rozhodnutí o dalším léčebném postupu.
I když použití defibrilátoru je v pediatrické BLS relativně vzácné, v případě dostupnosti je nutno s jeho použitím počítat. Použití AED je nutno s maximálním omezením no-flow time a pokračováním KPR co nejdříve po podání výboje nebo po detekci nedefibrilovatelného rytmu. Pokud je u AED funkce dětského režimu s redukcí energie výboje, používá se tento výboj u dětí do 8 let. Při absenci tohoto režimu lze AED použít u dětí všech věkových kategorií.
Rozšířená resuscitace dětí (PALS )
Kromě prováděných resuscitačních postupů je u PA LS nezbytná týmová spolupráce. Pokračuje snaha o zajištění adekvátní oxygenace s použitím maximálně dosažitelné FiO2. Pokud je předpoklad déletrvající resuscitace či transportu pacienta, provede kompetentní lékař definitivní zajištění dýchacích cest (endotracheální intubace, laryngeální maska). Jako prevence hyperventilace je vhodné využít kapnometrii (EtCO2). Hyperventilace při použití nadměrného dechového objemu či dechové frekvence je spojena s rizikem cerebrální vazokonstrikce s prohloubením mozkové hypoperfuze. Přiměřený dechový objem je vhodné kontrolovat dechovými exkurzemi hrudníku, které musí být zajištěny i při kompresích hrudníku při nepřímé srdeční masáži. Při obnovení cirkulace udržujeme SpO2 v hodnotách mezi 94–98 %. Poměr kompresí hrudníku k ventilaci 15 : 2 je doporučen v případech, kdy je na to personál vyškolen.
Dalším krokem při PA LS je zajištění žilního vstupu, buď intravenózní (i.v.) kanylou, nebo intraoseálním (i.o.) vstupem. Srdeční masáž je následně doplněna aplikací adrenalinu i.v./i.o. v dávce 10 μg/kg (maximální dávka je 1 mg). Účinnost aplikace se zvýší proplachem. Uvedenou dávku adrenalinu je možné opakovat každých 3–5 minut. Tuto léčbu doplníme podáváním bolusu tekutin (krystaloidů) v dávce 10 ml/kg, v indikovaných případech je možno podání opakovat.
V případě zachycení defibrilovatelného rytmu (fibrilace komor, bezpulzová komorová tachykardie) použijeme defibrilaci výbojem 4 J/kg. Až do obnovení cirkulace je nutné minimalizovat přerušení KPR. Interval mezi poslední kompresí a podáním výboje má být maximálně 5 sekund. Při podání výboje je nutné dodržet zásady bezpečnosti. Analýzu srdečního rytmu provádíme každé 2 minuty. Při neefektivní cirkulaci se provede opakovaný výboj stejné intenzity. Bezprostředně po podání 3. výboje se aplikuje druhá dávka adrenalinu 10 μg/kg a amiodaron 5 mg/kg (max 300 mg) i.v./i.o. Po podání 5. výboje podáme další identickou dávku adrenalinu, amiodaron podáme v poloviční dávce. Každá aplikace léku musí být doplněna proplachem.
Resuscitaci vždy provádíme do obnovení příznaků spontánního krevního oběhu (restore of spontaneous circulation – ROSC) nebo do splnění kritérií pro ukončení KPR – viz níže. U každého dítěte s prolongovanou KPR s předpokladem reverzibilní etiologie zástavy je indikace ke konzultaci dětského ECMO centra (centra pro mimotělní membránovou oxygenaci).
Resuscitace dětí za specifických podmínek
Traumatická zástava oběhu – kromě PBLS a PA LS je nutno ošetřit potenciálně život ohrožující krvácení, diagnostikovat pneumotorax, ev. hemotorax, podání tekutinové resuscitace v indikovaných případech doplnit transfuzí erymasy nebo krve.
Hypotermická zástava oběhu – u pacientů s teplotou tělesného jádra 28 °C je možno KPR provádět intermitentně či odložit, je-li KPR na místě události nemožná či obtížná. U dětí s teplotou 30 °C nepodáváme adrenalin a defibrilaci odložíme až na dobu po dosažení této teploty.
Obstrukce dýchacích cest cizím tělesem – největší riziko je u dětí do 3 let. Na úplnou obstrukci je nutno myslet vždy, pokud dojde u dítěte k náhlé apnoi a cyanóze. Absence kašle svědčí pro mimořádnou závažnost stavu. Jedná se o urgentní stav vyžadující okamžitý zákrok, opakovaný úder mezi lopatky u dítěte s polohou hlavy dolů. Pokud tento postup není účinný, střídáme úder mezi lopatky a stlačení hrudníku (děti do 1 roku) nebo stlačení nadbřišku (děti > 1 rok).
Kritéria nezahájení či ukončení resuscitace
Není-li možnost zajistit bezpečnost zachránce.
Přítomnost poranění zjevně neslučitelného se životem či přítomnost známek jisté smrti.
Asystolie přetrvávající i po 20 minutách PA LS, nejsou - li přítomny reverzibilní příčiny zástavy oběhu.
U pacienta, kde riziko poškození z déle probíhající KPR převažuje nad jejím přínosem, pokud nenastává ROSC, je přítomna závažná chronická komorbidita nebo velmi nízká kvalita života před zástavou.
Souhrn resuscitace dětí
- Na rozdíl od dospělých je srdeční zástava u dětí obvykle sekundární při zástavě dechu nebo při vyčerpání kompenzačních mechanismů.
- Resuscitaci dětí lze použít pro věkové spektrum 0–18 let, s výjimkou novorozenců bezprostředně po porodu.
- Resuscitaci zahajujeme provedením 5 úvodních dechů, dále postupujeme podle doporučení pro PBLS a PA LS.
- Přehledný souhrn doporučení je uveden na obrázku 2.
Image 2. Přehledný souhrn doporučení pro základní (PBLS) a rozšířenou (PALS ) resuscitaci dětí 
Resuscitace novorozenců
Resuscitace novorozenců se týká donošených i nedonošených novorozenců bezprostředně po porodu, ve většině případů na porodním sále, případně v domácích podmínkách nebo v přednemocniční péči. Významným rozdílem proti pediatrické resuscitaci je možnost identifikace stavů, které mohou vést ke komplikacím v poporodním období. Nejčastější příčiny jsou uvedeny v tabulce 5. Z patofyziologického hlediska dochází po porodu ke dvěma významným změnám oproti intrauterinnímu životu:
- aerifikace plic, které byly do doby porodu nevzdušné a jejich perfuze neměla žádný vliv na oxygenaci;
- přestavba fetální krevní cirkulace, kdy dochází k zásadní přestavbě oběhového systému včetně uzavření Botallovy dučeje a foramen ovale.
Table 5. Rizikové faktory pro poruchu poporodní adaptace novorozence (Zdroj: Janota J, Straňák Z. Neonatologie. Praha: Mladá fronta 2013.) 
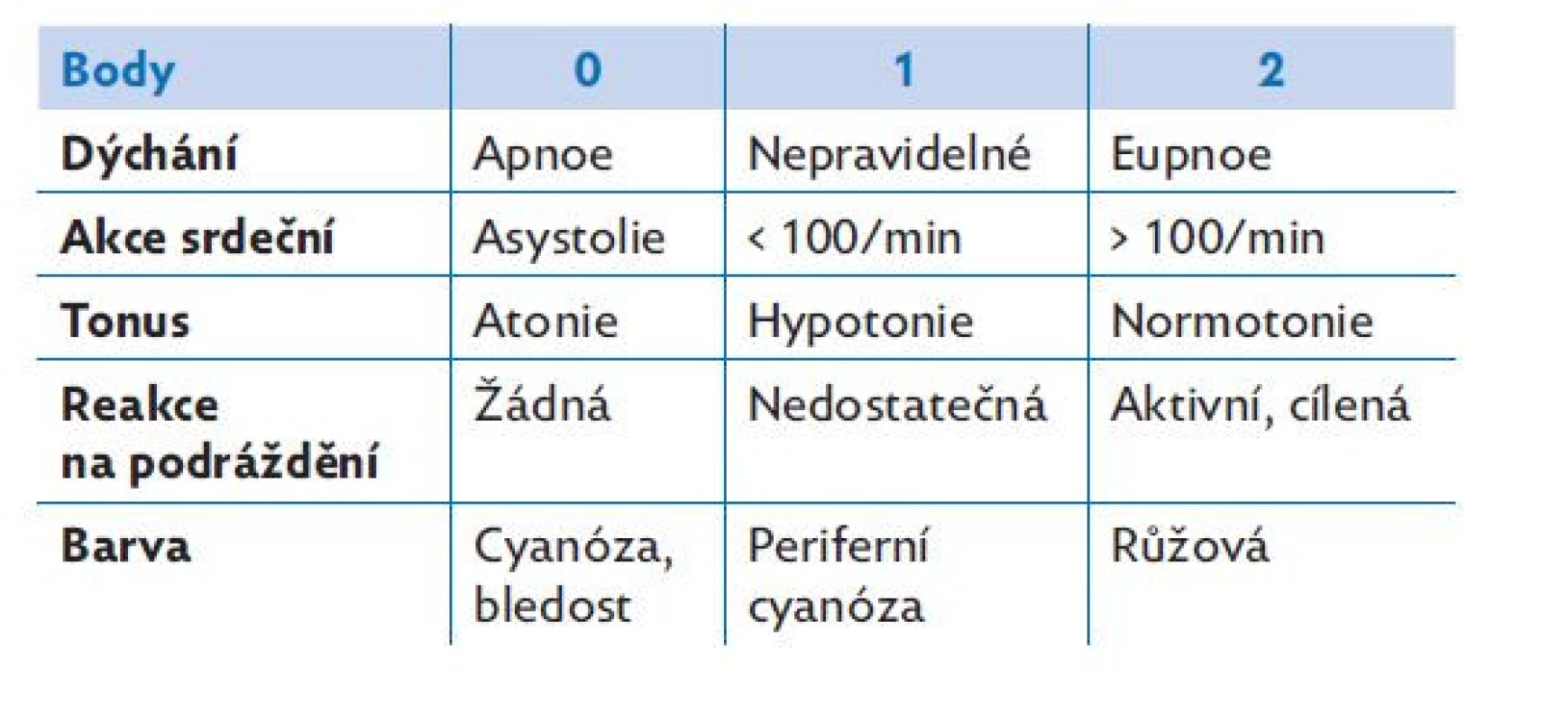
Nezbytným předpokladem kvalitní péče o novorozence s poruchou poporodní adaptace je adekvátní vybavení místa pro resuscitaci. Resuscitace musí probíhat v termoneutrálním prostředí, hypotermie je u nezralých novorozenců spojena s vyšším výskytem intraventrikulární hemoragie i vyšší úmrtností.(15) Resuscitaci je nutno provádět na vyhřívaném lůžku, cílová teplota novorozence se má pohybovat mezi 36,5 – 37,5 °C. I při maximálním výkonu vyhřívaného lůžka je nutno zabránit okolnímu proudění studeného vzduchu. Děti narozené ve 32. týdnu a mladší je doporučeno bez omytí zabalit do polyethylenové fólie (s výjimkou obličeje). Po porodu je nutno posoudit klinický stav dítěte. Dosud je standardní součástí neonatologické dokumentace Apgar skóre (tab. 6 a 7). Jedná se o jednoduchý skórovací systém, který v roce 1952 zavedla do praxe americká anestezioložka Dr. Virginia Apgar. Apgar skóre se hodnotí za 1., 5. a 10. minutu po porodu. Ve specifickém případě nutnosti resuscitace novorozence používáme zjednodušené hodnocení popisující pouze tonus, akci srdeční a dýchání. Z laboratorních hodnot využíváme k hodnocení stavu novorozence hodnotu pH z pupečníkové arterie. Těžká acidóza s pH < 7,0 poukazuje na patologii poporodní adaptace, i když nemusí vždy být predikcí závažností stavu.(16) Vždy je však vhodné mít laboratorní hodnotu k dispozici, a to pro rozhodnutí o dalším léčebném postupu. Pokud to klinický stav novorozence umožňuje, je nutno odložit podvaz pupečníku alespoň o jednu minutu po porodu. Tento postup zvýší efektivně cirkulující objem v krevním řečišti.(17)
Table 7. Hodnocení stavu novorozence po porodu dle Apgar skóre 
Počet novorozenců, kteří vyžadují po porodu intervenci, se dle údajů ERC pohybuje kolem 15 %. Většina novorozenců ale dobře reaguje na osušení a taktilní stimulaci. Tyto postupy probíhají prakticky současně a představují minimální časovou prodlevu. Následně asi 5 % novorozenců vyžaduje další léčbu.
Insuflace plic a asistovaná ventilace
Pokud je dítě apnoické, je přítomen gasping či jiná forma neefektivní ventilace, je nutno zahájit ventilaci pozitivním přetlakem, optimálně do 60 sekund po porodu. Ventilaci provádíme resuscitátorem Neo Puff (obr. 3), který umožňuje nastavit jak inspirační tlak (PIP), tak i tlak na konci expiria (PEEP). Samorozpínací vak je méně vhodný k resuscitaci novorozence, jeho použití je možné v situacích, kdy není pracoviště vybaveno resuscitačním přístrojem. K ventilaci použijeme obličejovou masku adekvátní velikosti. U donošených novorozenců zahájíme prodýchávání tlakem 30 cm H2O vzduchem (FiO2 0,21), u nezralých novorozenců na 25 cm H2O, u novorozenců ≤ 32. gestační týden se použije k ventilaci FiO2 0,21–0,30. Ventilaci vždy zahájíme provedením 5 insuflačních dechů s udržením insuflačního tlaku 2–3 sekundy. Adekvátní terapeutickou odezvou je přítomnost akce srdeční > 100/min, viditelné zvedání hrudníku a adekvátní dechový objem. Pokračujeme dále dýcháním s frekvencí 30/min a inspiračním časem 1 s. Hodnota nastavení PEEP je 5 cm H2O jako prevence kolapsu alveolů. Pokud terapeutická odezva není dostatečná, je nutno vždy zkontrolovat těsnost masky, polohu hlavičky (neutrální poloha bez záklonu), dostatečný PIP nebo přítomnost obstrukce dýchacích cest. Vždy je nutno vyloučit technický problém. Akci srdeční a dechovou frekvenci kontrolujeme po 30 s, při nutnosti prolongované ventilace a při přítomnosti kompetentního personálu provedeme následně spolehlivější zajištění dýchacích cest (endotracheální rourka). Co nejdříve je nutno monitorovat preduktální SpO2 (na pravé ruce), frakci kyslíku použitou při ventilaci je nutno přizpůsobit naměřeným hodnotám. Cílové hodnoty SpO2 jsou uvedeny v tabulce 8.
Image 3. Resuscitátor Neo Puff 
Table 8. Hodnoty uspokojivé preduktální SpO2 v poporodním období 
Masáž srdeční
Účinnost masáže srdeční je vždy podmíněna adekvátní ventilací (viz výše). Kompresi hrudníku zahájíme nejen při asystolii, ale vždy, pokud je srdeční frekvence po porodu < 60/min a nedojde k úpravě po 30 s adekvátní ventilace. V tomto případě zvýšíme FiO2 na 1,0 a provádíme 3 komprese hrudníku na 1 vdech (15 cyklů na 30 s). Pokud je to možné, používáme techniku stačování dvěma palci (ruce máme obemknuté kolem hrudníku novorozence). Efekt srdeční masáže kontrolujeme každých 30 s, kontrolujeme i účinnost ventilace, FiO2 titrujeme podle hodnot SpO2, pokud je možné ji spolehlivě měřit. Zároveň zajistíme vstup do žilního řečiště.
Zajištění žilního vstupu u novorozence
Metodou volby je zajištění vstupu do umbilikální žíly. Použijeme uzavřený systém jako prevenci vzduchové embolie. Před aplikací léků verifikujeme správné zavedení katétru aspirací krve. Alternativní cestou je zajištění intraoseálního vstupu.
Farmakoterapie
Adrenalin – je základním lékem při resuscitaci novorozence, podáváme jej, pokud adekvátní ventilace a masáž srdeční nezvýší srdeční frekvenci nad 60/min. Adrenalin je aplikován v ředění 1 : 10 000 (1 mg v 10 ml roztoku), dávka je 10–30 μg/kg. Při přetrvávání bradykardie je indikováno opakované podání vždy po 3–5 minutách. Intratracheální podání adrenalinu by mělo být použito jen v případech, kdy nelze zajistit žilní vstup, a to v dávce 50–60 μg/kg.
Glukóza – je podávána jako prevence hypoglykemie při prolongované resuscitaci, dávka je 2,5 ml/kg 10% roztoku glukózy. Hladinu glukózy je vhodné kontrolovat glukometrem.
Krystaloidy – při hypotenzi je indikováno bolusové podání krystaloidů v dávce 10 ml/kg s možností opakování. Při podezření na výraznou krevní ztrátu je indikováno podání 0 rh negativní krve.
Bikarbonát sodný – je indikován v případě déletrvající zástavy oběhu nereagující na zavedenou léčbu. Podává se dávka 1–2 mmol/kg (2–4 ml 4,2% roztoku). Výhodné je vyšetření pH při možnosti point-of-care testing (POCT).
Naloxon – jeho použití je limitováno na případy, kdy příčinou zástavy dechu a nedostatečného srdečního výdeje může být podání opioidů matce během porodu.
Řízená hypotermie
Řízená hypotermie je účinná metoda, která může zabránit závažnému neurologickému postižení po těžké perinatální asfyxii či je minimalizovat.(18) Podmínkou je gestační stáří novorozence ≥ 36. týden a zahájení řízené hypotermie do 6 hodin po porodu. Řízená hypotermie by měla být indikována na podkladě celkového stavu novorozence, případně i provedeného amplitudového EEG (aEEG). Do doby rozhodnutí o zahájení řízené hypotermie by novorozenec neměl být aktivně zahříván a je nutno zajistit optimální oxygenaci.
Indikace k ukončení či nezahájení resuscitace u novorozenců
Zahájení resuscitace není vhodné při předpokladu vysoké úmrtnosti a nepřijatelně vysoké morbidity u přeživších novorozenců. Pokud je to možné, měla by být tato situace konzultována s rodiči. Resuscitace by měla být zahájena u většiny dětí s délkou těhotenství ≥ 24. gestační týden. Resuscitaci je třeba zahájit, pokud je prognóza dítěte nejasná anebo nebyla možná konzultace s rodiči.
Pokud nelze detekovat srdeční akci po 10 minutách resuscitace, je nutno posoudit všechny klinické faktory (gestační věk, dysmorfické změny) a zvážit ukončení resuscitace. Pokud nelze detekovat akci srdeční po 20 minutách adekvátní resuscitace, je doporučeno ukončit resuscitaci novorozence vždy.
Souhrn resuscitace novorozence
- Vždy je nutné vyhodnotit průběh gravidity a rizikové faktory. Konzultace s rodiči by měla být provedena vždy, pokud je to možné.
- Resuscitace musí probíhat v termoneutrálním prostředí. Je zahájena pěti insuflačními dechy.
- Srdeční masáž zahajujeme i při bradykardii < 60/ min, pokud 30sekundová ventilace nevedla k úpravě srdeční akce.
- Přehledný souhrn doporučení je uveden na obrázku 4.
Image 4. Přehledný souhrn doporučení pro resuscitaci novorozenců 
Závěr
Resuscitace v novorozeneckém i dětském věku je vždy stav závažný nejen po odborné stránce. Kromě teoretických znalostí je pro pediatry nezbytné i získání praktických zkušeností v rámci postgraduálního vzdělávání i cíleně zaměřených kurzů. Jejich součástí musí být i adekvátní komunikace s rodiči.
Korespondenční adresa:
MUDr. René Hrdlička, Ph.D.
Dětské oddělení Oblastní nemocnice Kolín
Žižkova 146
280 02 Kolín
Sources
1. Goyal A, Sciammarella JC, Cusick AS, Patel PH. Cardiopulmonary Resuscitation. 2021 Jun 8. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing 2021. PMID: 29261985.
2. Moezzi M, Aftshari G, Rahim F, et al. Outcomes of cardiopulmonary resuscitation and its predictors in hospitalized patients. Clin Med Rev Case Rep 2020; 7 : 309. doi: 10.23937/2378-3656/1410309
3. Song F, Sun S, Ristagno G, et al. Delayed high-quality CPR does not improve outcomes. Resuscitation 2011; 82: S52 – S55.
4. Pembeci K, Yildirim A, Turan E, et al. Assessment of the success of cardiopulmonary resuscitation attempts performed in a Turkish university hospital. Resuscitation 2006; 68 : 221–229.
5. Djakow J. Neodkladná resuscitace u dětí. Pediatr Praxi 2018; 19(3): 159–165.
6. Berg RA, Nadkarni VM, Clark AE, et al.; Eunice Kennedy Shriver National Institute of Child Health and Human Development Collaborative Pediatric Critical Care Research Network. Incidence and outcomes of cardiopulmonary resuscitation in PICUs. Crit Care Med 2016; 44(4): 798–808. doi: 10.1097/CCM.0000000000001484
7. Dostál P, et al. Základy umělé plicní ventilace. Praha: Maxdorf 2005.
8. David D. Historie resuscitace. Urgentní medicína 2009; 12(3): 34–35.
9. P okorný J. Profesor Peter J. Safar, MD (1924–2003) – neuvěřitelná životní dráha. Anest Intenziv Med 2007; 18(5): 305–314.
10. Safar P, Brown TC, Holtey WJ, Wilder RJ. Ventilation and circulation with closed-chest cardiac massage in man. JAMA 1961; 176(7): 574–576. doi: 10.1001/jama.1961.03040200010003
11. Perkins GD, Graesner JT, Semeraro F, Olasveengen T, et al.; European Resuscitation Council Guideline Collaborators. European Resuscitation Council Guidelines 2021: Executive summary. Resuscitation 2021; 161 : 1–60. doi: 10.1016/j. resuscitation.2021. 02. 003. Erratum in: Resuscitation 2021; 163 : 97–98.
12. Truhlář A, Černá Pařízková R, Dizon JML, et al. Doporučené postupy pro resuscitaci ERC 2021: Souhrn doporučení. Anest Intenz Med 2021; 32(Suppl. A): 72.
13. Dieckmann RA, Brownstein D, Gausche-Hill M. The pediatric assessment triangle: a novel approach for the rapid evaluation of children. Pediatr Emerg Care 2010; 26(4): 312–5. doi: 10.1097/PEC.0b013e3181d6db37.
14. Astapenko D, Černý V. Kapilární návrat – klinické vyšetření přítomnosti cirkulační koherence? Anest Intenziv Med 2019; 30 : 190–191.
15. Miller S, Lee H, Gould J. Hypothermia in very low birth weight infants: distribution, risk factors and outcomes. J Perinatol 2011; 31: S49–S56. doi: 10.1038/jp.2010.177.
16. Větr M. Laboratorní a klinické ukazatele stavu novorozence po porodu. Čes Gynek 2010; 75(5): 447–454.
17. Gutierrez AO, Velasquez RME, Iriarte MT. Analysis of clinical course in term patients with early and delayed umbilical cord clamping after birth. Int J Pediatr Neonatol 2010.
18. Jacobs SE, Berg M, Hunt R, et al. Cooling for newborns with hypoxic ischemic encephalopathy. Cochrane Database Syst Rev 2013; 31(1).
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2022 Issue 2-
All articles in this issue
- Ze sbírky moderního českého a slovenského umění
- Co jsme psali
- Válka na Ukrajině očima kyjevské lékařky
- Editorial
- 100 let inzulinu: Příběh Elisabeth Hughesové a jednoho zázraku v medicíně
- Kompenzace diabetu 1. typu u českých dětí se dlouhodobě zlepšuje: data z národního registru ČENDA (2013–2020)
- Postiniciálna remisia u detí s diabetes mellitus 1. typu
- Technologická revoluce v léčbě diabetu 1. typu
- Glukokinázový diabetes u dětí
- Oxygenoterapie u akutních stavů v praxi
- Resuscitace novorozence, kardiopulmonální resuscitace dětí
- Pandemie covidu-19 v pediatrické populaci Ústeckého kraje
- Osobní zprávy
- Historický rozhovor s legendou: doc. MUDr. Alois Kopecký, CSc. (1920–2013)
- Pediatrická poezie
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Resuscitace novorozence, kardiopulmonální resuscitace dětí
- Oxygenoterapie u akutních stavů v praxi
- Technologická revoluce v léčbě diabetu 1. typu
- Kompenzace diabetu 1. typu u českých dětí se dlouhodobě zlepšuje: data z národního registru ČENDA (2013–2020)
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career