-
Medical journals
- Career
Interdisciplinární doporučení pro testování trombofilie
Authors: E. Drbohlavová 1; J. Gumulec 2; A. Buliková, (ČHS) 3; P. Ďulíček 4; J. Hirmerová 5; R. Malý 6; E. Zápotocká 7; J. Blatný 8; J. Václavík 9; P. Kessler 10
Authors‘ workplace: Oddělení klinické hematologie Krajské nemocnice Liberec a. s. 1; Klinika hematoonkologie LF OU a FN Ostrava 2; Oddělení klinické hematologie LF MU a FN Brno 3; IV. interní hematologická klinika FN Hradec Králové 4; II. interní klinika LF UK a FN Plzeň 5; I. interní kardioangiologická klinika FN Hradec Králové 6; Klinika dětské hematologie a onkologie 2. LF UK a FN Motol, Praha 7; Oddělení dětské hematologie a bio chemie, FN Brno 8; Interní a kardiologická klinika FN Ostrava 9; Oddělení hematologie a transfuziologie Nemocnice Pelhřimov 10
Published in: Transfuze Hematol. dnes,31, 2025, No. 2, p. 132-136.
Category:
doi: https://doi.org/10.48095/cctahd2025prolekare.cz9Overview
V předloženém mezioborovém konsenzu čtyř odborných společností zabývajících se problematikou trombofilních dispozic shrnujeme pravidla diagnostiky a péče o pacienty s vrozenými nebo získanými trombofiliemi, tj. faktory zvyšujícími riziko především žilní tromboembolické nemoci. Primárním cílem je standardizace péče o tyto nemocné s respektem k pravidlům medicíny založené na důkazech. Z doporučení vyplývá, za jakých okolností, ve kterých klinických situacích, kterým pacientům a kterými testy je užitečné ty které trombofilie vyšetřovat a jaké ne. Přes dlouhou historii a velmi dobrou dostupnost diagnostiky jednotlivých trombofilií podobné doporučení doposud nebylo v České republice publikováno.
Klíčová slova:
vrozené a získané trombofilie – žilní tromboembolizmus – arteriální trombóza – vyšetření JAK2 mutace a PNH klonu
ÚVOD
Vrozené a získané trombofilie jsou rizikovým faktorem především žilní tromboembolické nemoci. Některé z nich zvyšují riziko trombotického postižení v tepenné části řečiště nebo v mikrocirkulaci. V posledních třech dekádách významně narostly objem i kvalita zkušeností s interpretací výsledků, hodnocením významu jednotlivých trombofilií a s péčí o různé skupiny pacientů nebo asymptomatických nosičů významných trombofilií. V těchto souvislostech vznikl tento přehledný dokument, jehož cílem je standardizace péče s respektem k pravidlům medicíny založené na důkazech. Detailní informace lze dohledat v uvedených publikacích [1–12]. Srovnání mezinárodních doporučení testování trombofilií v příloze tab. 1.
Table 1. Srovnání mezinárodních doporučení testování trombofi lií. 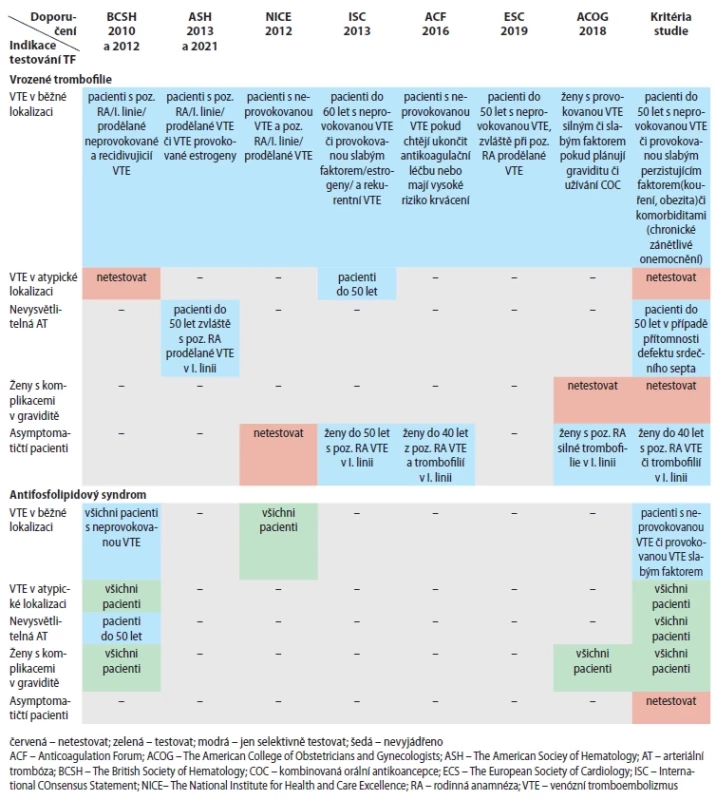
KLINICKY VÝZNAMNÉ TROMBOFILIE
Vrozené – FV Leiden a FII protrombin, deficit proteinu C, proteinu S nebo antitrombinu.
Získané – APS (LA, aCL a antiB2-GPI protilátky):
vysoce rizikové trombofilie: FV Leiden homozygot, FII protrombin homozygot, kombinovaný heterozygot FV Leiden a heterozygot FII protrombin, deficit proteinu C, proteinu S nebo antitrombinu, APS;
nízce rizikové trombofilie: FV Leiden heterozygot, FII protrombin heterozygot.
Vyšetření indikovaná ve specifických situacích, např. na základě doporučení hematologa.
Průkaz PNH klonu, mutace JAK2 V617F a JAK2 v exonu 12.
FAKTORY, KTERÉ NEJSOU KLINICKY VÝZNAMNĚ ASOCIOVÁNY S VTE [2,10,12]
Interdisciplinární expertní tým nedoporučuje pro posuzování rizika trombózy vyšetřovat polymorfizmy a varianty genů bez vztahu k VTE (např. MTHFRs 677C®T, 1298A®C) nebo faktory bez jednoznačného průkazu asociace s VTE (např. aktivita FIX, FX, FXI, PAI-1, polymorfizmus promotoru 4G/5G PAI-1, SERPINE1 varianty, mutace haplotypu M2 v genu ANXA5, SPS apod.).
Poznámka: Rovněž aktivitu FVIII se nedoporučuje rutinně vyšetřovat, přestože vysoká aktivita FVIII je spojena s rizikem VTE i její recidivy. Aktivita však výrazně kolísá v čase a je ovlivněna různou měrou vrozenými i získanými faktory a jejich interakcí. Navíc neexistují doporučení ohledně primární či sekundární tromboprofylaxe u jedinců s vysokou aktivitou FVIII, podpořená důkazy. V úvahu přichází opakované stanovení FVIII a interpretace výsledku v klinickém kontextu.
OBECNĚ PROČ A KDY VYŠETŘOVAT [2,10]
Pokud výsledek ovlivní strategii antitrombotické léčby (omezená či dlouhodobá antikoagulace, výběr antikoagulancia) nebo profylaxi v rizikových situacích vč. gravidity.
Image 1. Kdy testujeme a kdy netestujeme hereditární trombofi lie. 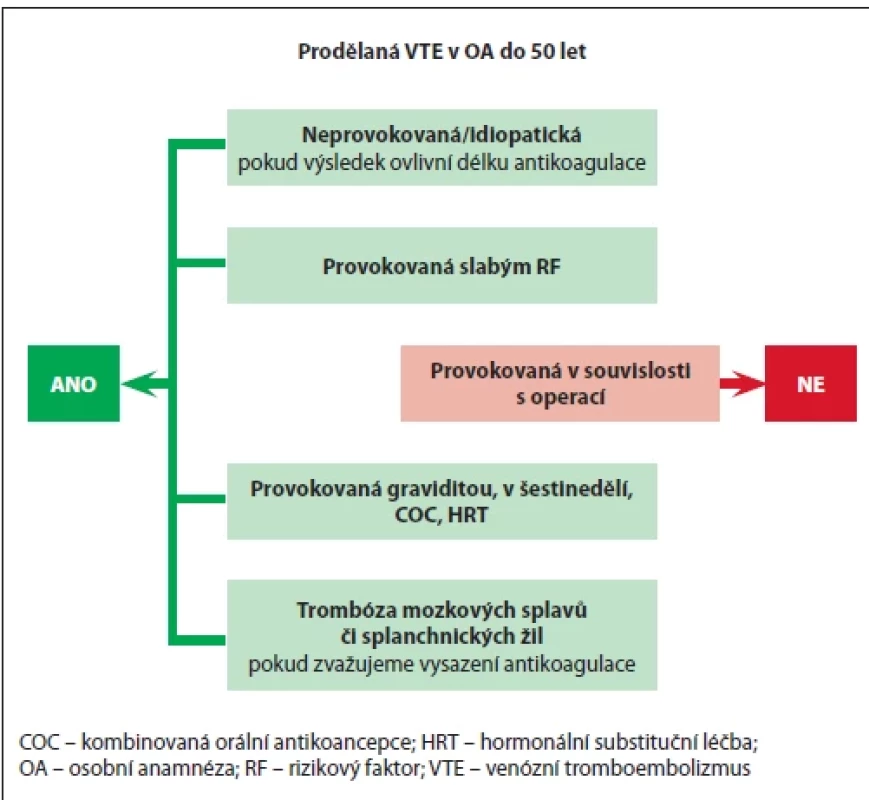
Netestovat v akutní fázi VTE (riziko zkreslení výsledků) – výjimkou je stanovení antitrombinu při podezření na rezistenci na heparin, antifosfolipidových protilátek při podezření na katastrofický antifosfolipidový syndrom, proteinu C a S u novorozenců a dětí s purpura fulminans apod.
Indikovat vyšetření TF by měl lékař se zkušeností s péčí o pacienty s trombózou nebo jinou významnou manifestací trombofilie
Poznámka: v prvních týdnech až 3 měsících po trombóze, při léčbě warfarinem, při užívání DOACs, při užívání HAK či v graviditě – je typické zkreslení výsledků proteinu C a S a LA. Genetické testy nejsou ovlivněny. Ideální čas na provedení koagulačních testů je 3 měsíce po prodělané VTE, resp. s odstupem po ukončení antikoagulační léčby. Pokud je nutné testovat během antikoagulační léčby, je nezbytné uvést na žádance k vyšetření, kterým antitrombotikem je pacient léčen. U krevních vzorků pacientů léčených DOACs může laboratorní pracovník použít tzv. DOACs stop tablet.
KDY TESTUJEME HEREDITÁRNÍ TROMBOFILIE [1,2,9,10] (obr. 1 a 2)
OA neprovokované VTE vzniklé do 50 let, pokud výsledek ovlivní délku antikoagulační terapie.
OA VTE provokované tranzientním nechirurgickým nebo slabým vyvolávacím momentem (např. trombóza po imobilizaci nebo drobném poranění, přechodné nemoci/infekci, upoutání na lůžko po dobu nejméně 3 dnů apod.) – výsledek může např. pomoci v rozhodnutí o délce sekundární profylaxe.
OA VTE provokované graviditou, v šestinedělí, při užívání COC nebo HRT – výsledek upřesní rozhodnutí o délce sekundární profylaxe a další strategie péče (následná gravidita apod.).
OA trombózy mozkových splavů či splanchnických žil – pokud zvažujeme vysazení antikoagulace a pro upřesnění strategie péče (např. průkaz PNH klonu nebo stanovení mutace JAK2 V617F).
U asymptomatických osob do 50 let, u jejichž příbuzných I. linie je prokázána vysoce riziková trombofilie, vyšetříme jen v rodině prokázanou mutaci (profylaxe v rizikových situacích, zajištění v graviditě…).
U žen před nasazením COC, HRT, plánujících graviditu/gravidních s pozitivní RA VTE a při známé přítomnosti vysoce rizikové trombofilie u příbuzných I. linie.
OA rekurentní VTE bez ohledu na přítomnost RF.
U pacientů s warfarinem indukovanou kožní nekrózou.
Image 2. Kdy testujeme a kdy netestujeme hereditární trombofi lie. 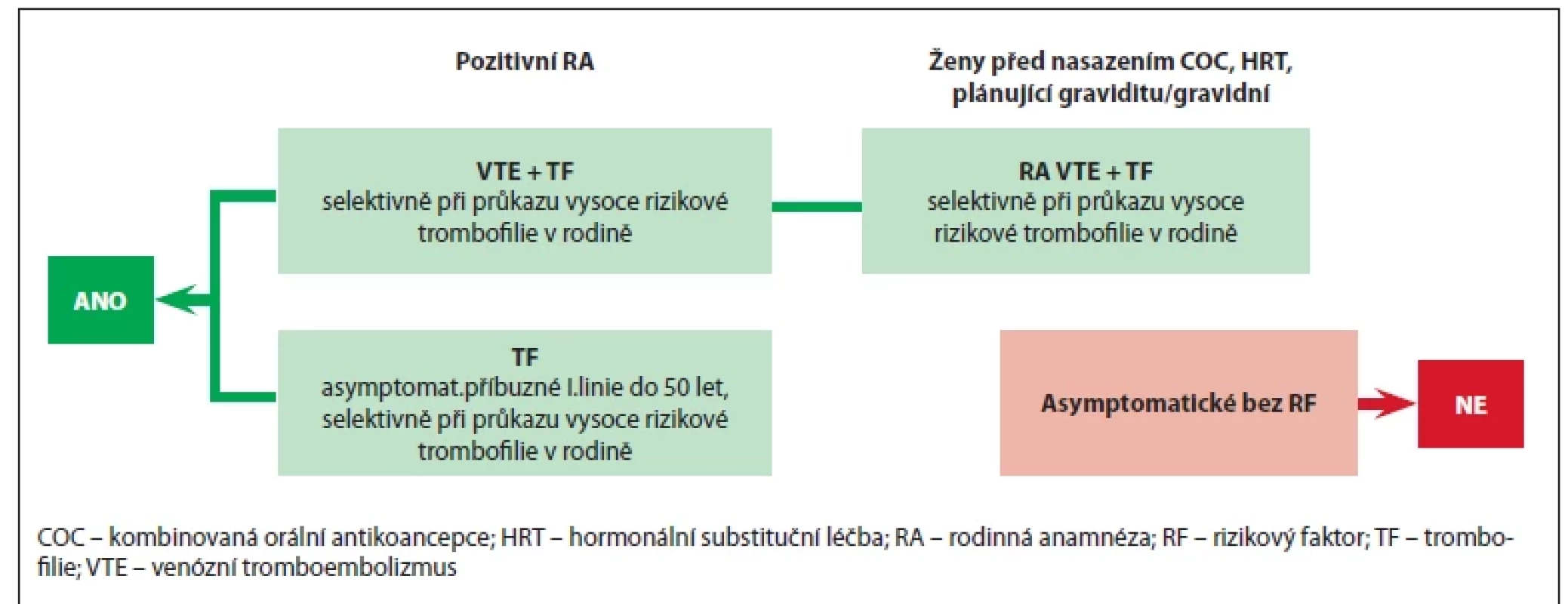
Image 3. Co vyšetřit po CMP a kdy myslet na APS. 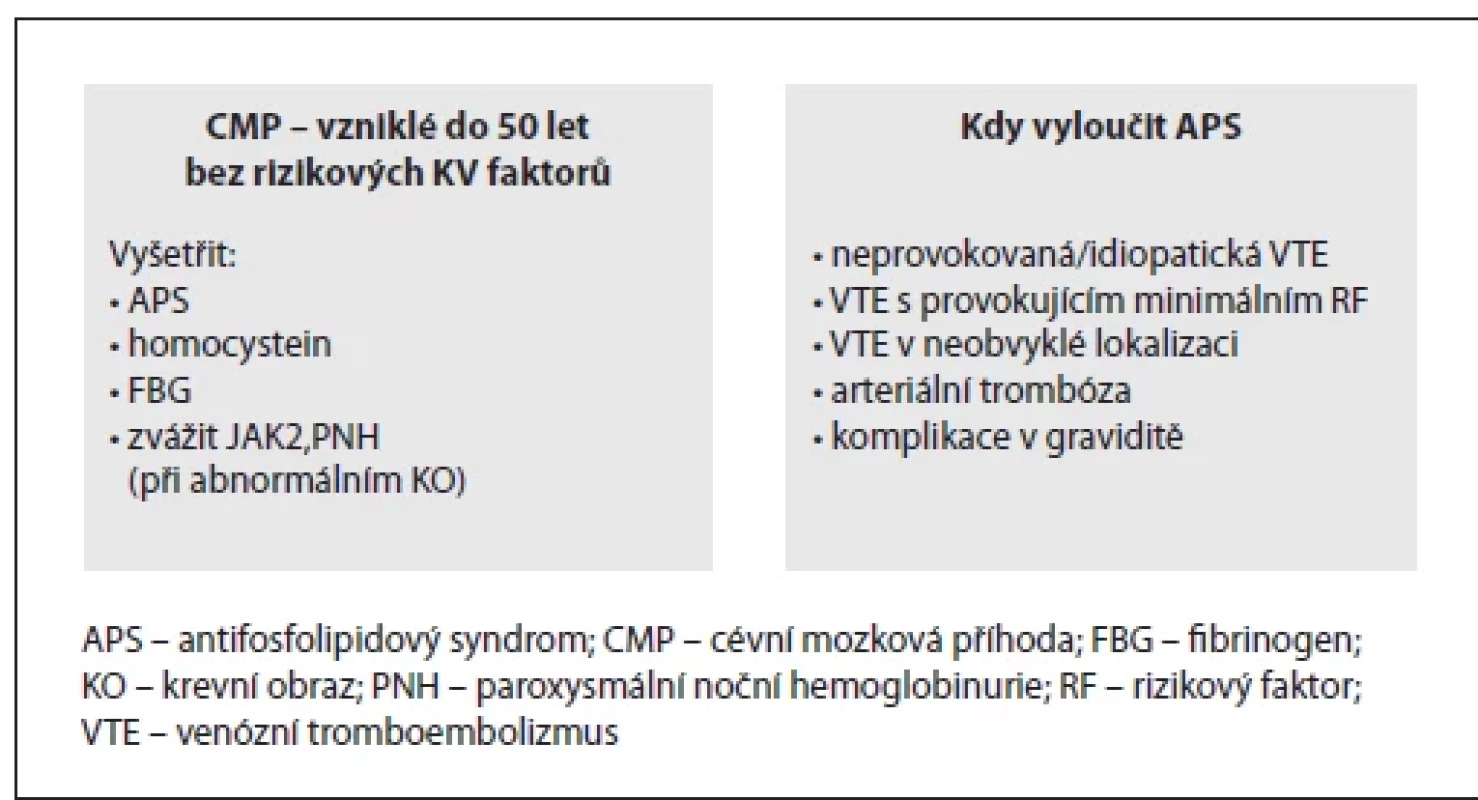
KDY RUTINNĚ NETESTUJEME HEREDITÁRNÍ TROMBOFILIE [1,2,6,9,10] (obr. 1 a 2)
Asymptomatické osoby k predikci rizika trombózy.
Pacienty s potřebou nepřetržité antikoagulační léčby.
Pacienty s OA blíže neurčeným typem trombózy (není určeno zda provokovaná či neprovokovaná).
Pacienty s OA arteriální trombózy vč. iCMP s průkazem PFO, okluze retinálních cév apod.
Ženy s OA časných ztrát plodu, preeklampsie, HELLP syndromu apod.
Asymptomatické ženy s negativní RA nosičství vysoce rizikové trombofilie před plánovanou asistovanou reprodukcí.
Asymptomatické ženy s negativní RA nosičství vysoce rizikové trombofilie před nasazením COC.
Vzdálené příbuzné pacientů s OA VTE.
Pacienty s OA pooperační VTE.
Pacienty po první trombóze asociované s CVK.
VYŠETŘENÍ JAK 2, PNH [2,4,9,10]
Vždy zvažujeme u pacientů s OA trombózy mozkových splavů a splanchnických žil (nemá-li pacient jaterní cirhózu nebo aktivní nádorové onemocnění…), dále u pacientů s arteriální trombózou vč. iCMP vzniklé do 50 let bez rizikových kardiovaskulárních faktorů a/nebo s abnormalitami v krevním obraze.
VYŠETŘENÍ ANTIFOSFOLIPIDOVÝCH PROTILÁTEK [2,4,9,10]
Vždy u pacientů s OA neprovokované/idiopatické VTE nebo VTE s provokujícím minimálním RF nebo VTE v neobvyklé lokalizaci nebo arteriální trombózy (vzniklé do 50 let a při absenci klasických kardiovaskulárních RF) a/nebo u žen s OA komplikací v graviditě (obr. 3).
U pacientů s trombotickou příhodou a se spontánně prodlouženým APTT a/nebo s trombocytopenií, s rychle progredujícím (multi) orgánovým selháním k vyloučení CAPS.
U pacientů s prokázaným revmatickým či jiným autoimunitním onemocněním.
Není indikováno vyšetření rodiny, jde o získané onemocnění.
SPECIFICKÉ MEZIOBOROVÉ SITUACE [2,4,9,10]
U pacientů s OA iCMP vzniklé do 50 let bez rizikových kardiovaskulárních faktorů doporučujeme vyšetření testů na APS, homocystein, fibrinogen a při podezřelých změnách v krevním obraze je na zvážení vyšetření JAK 2 a PNH klonu (obr. 3).
U ambulantních pacientů s malignitou na léčbě v nízkém či středním riziku VTE a s pozitivní RA VTE je doporučováno vyšetření vrozených trombofilií.
Vyšetření vrozených a získaných trombofilií zvážit také u pacientů s recidivující trombózou na nevarikózních povrchových žilách, není-li jasná souvislost s malignitou.
U pacientů se současným výskytem arteriálních a žilních trombóz doporučujeme vyšetřit antifosfolipidové protilátky, fibrinogen, zvážit vyšetření JAK 2 a PNH (při podezřelých změnách krevního obrazu), FV Leiden a FII protrombin, protein C, protein S a antitrombin.
PEDIATRICKÁ POPULACE [2,4]
Novorozenci a malé děti s purpura fulminans by měly být testováni neodkladně na deficit PC a PS.
Dále je vhodné vyšetřovat i zatím asymptomatické děti, kde u příbuzných 1. stupně byla diagnostikována vysoce riziková trombofilie. Věk vyšetření dítěte je individuální, podle hloubky deficitu a manifestace v rodině, rozhodně ale vždy prepubertálně. Je tedy nutné rodiče o této skutečnosti informovat cestou ambulantních hematologů pro dospělé, kteří se touto problematikou zabývají.
Neexistují jasná doporučení stran testování trombofilie u dětí, nicméně i v pediatrické populaci je cílem testovat vrozenou trombofilii racionálně a ne rutinně. Detailní konsenzus doporučení týkající se pediatrické populace v ČR bude publikován separátně Pracovní skupinou pro dětskou hematologii ČPS a ČHS.
ZKRATKY
aCL – antikardiolipinové protilátky
antiB2-GPI – anti-beta-2 glykoprotein I
APS – antifosfolipidový syndrom
AT – arteriální trombóza
CAPS – katastrofický antifosfolipidový syndrom
COC – kombinovaná orální antikoncepce
CVK – centrální venózní katetr
DOACs – direct oral anticoagulants
FBG – fibrinogen
HRT – hormonální substituční léčba
iCMP – ischemická cévní mozková příhoda
KO – krevní obraz
LA – lupus antikoagulant
OA – osobní anamnéza
PC – protein C
PNH – paroxysmální noční hemoglobinurie
PS – protein S
RA – rodinná anamnéza
RF – rizikový faktor
SPS – syndrom lepivých destiček
TF – trombofilie
VTE – venózní tromboembolizmus
Sources
1. Middeldorp S, Nieuwlaat R, Baumann Kreuziger L et al. American Society of Hematology 2023 guidelines for management of venous thromboembolism: thrombophilia testing. Blood Adv 2023; 7 (22): 7101–7138. doi: 10.1182/bloodadvances.2023010177.
2. Arachchillage DJ, Mackillop L, Chandratheva A et al. Guidelines for thrombophilia testing: A British Society for Haematology guideline. Br J Haematol 2022; 198 (3): 443–458. doi: 10.1111/bjh.18239.
3. Parakh RS, Sabath DE. Venous thromboembolism: role of the clinical laboratory in diag - nosis and management. J Appl Lab Med 2019; 3 (5): 870–882. doi: 10.1373/jalm.2017. 025734.
4. Baglin T, Gray E, Greaves M et al. Clinical guidelines for testing for heritable thrombophilia. Br J Haematol 2010; 149 (2): 209–220. doi: 10.1111/j.1365-2141.2009.08022.x.
5. Vrotniakaite-Bajerciene K, Tritschler T, Jalowiec KA et al. Adherence to thrombophilia testing guidelines and its influence on anticoagulation therapy: a single-center cross-sectional study. Thromb Res 2023; 223 : 87–94. doi: 10.1016/j.thromres.2022.12.001.
6. Quenby S, Booth K, Hiller L et al. Heparin for women with recurrent miscarriage and inherited thrombophilia (ALIFE2): an international open-label, randomised controlled trial. Lancet 2023; 402 (10395): 54–61. doi: 10.1016/s0140-6736 (23) 00693-1.
7. Schulman S, Konstantinides S, Hu Y, Tang LV. Venous thromboembolic diseases: diagnosis, management and thrombophilia testing: observations on NICE guideline [NG158]. Thromb Haemost 2020; 120 (8): 1143–1146. doi: 10.1055/s-0040-1712913.
8. National Institute for Health and Care Excellence: Clinical Guidelines. In: Venous thromboembolic diseases: diagnosis, management and thrombophilia testing. National Institute for Health and Care Excellence (NICE) Copyright © NICE 2023. London 2023.
9. Connors JM. Thrombophilia testing and venous thrombosis. N Engl J Med 2017; 377 (23): 2298. doi: 10.1056/NEJMc1713797.
10. Nicolaides AN, Fareed J, Spyropoulos AC et al. Prevention and management of venous thromboembolism. International Consensus Statement. Guidelines according to scientific evidence. Int Angiol 2024; 43 (1): 1–222. doi: 10.23736/s0392-9590.23.05177-5.
11. Kearon C, Ageno W, Cannegieter SC et al. Categorization of patients as having provoked or unprovoked venous thromboembolism: guidance from the SSC of ISTH. J Thromb Haemost 2016; 14 (7): 1480–1483. doi: 10.1111/jth.13336.
12. Lowe G, Wu O, van Hylckama Vlieg A et al. Plasma levels of coagulation factors VIII and IX and risk of venous thromboembolism: systematic review and meta-analysis. Thromb Res 2023; 229 : 31–39. doi: 10.1016/j.thromres. 2023.06.026.
Do redakce doručeno dne: 23. 4. 2025.
Přijato dne: 9. 5. 2025.
Eva Drbohlavová
Oddělení klinické hematologie
Krajské nemocnice Liberec a. s.
Baarova 526 /15
460 01 Liberec
e-mail: eva.drbohlavova@nemlib.cz
Labels
Haematology Internal medicine Clinical oncology
Article was published inTransfusion and Haematology Today
2025 Issue 2-
All articles in this issue
- Myelomem indukované kardiovaskulární poruchy
- Automatizovaná digitální cytomorfologie zvyšuje spolehlivost diagnostiky kostní dřeně
- Výsledky 1. linie léčby non-Hodgkinových a Hodgkinových lymfomů v reálné praxi – analýza pacientů léčených na Klinice hematoonkologie Fakultní nemocnice Ostrava v období od 2013 do 2022
- Trendy v alogenních transplantacích krvetvorných buněk – analýza činnosti transplantačního centra Fakultní nemocnice Plzeň v období 2001– 2021
- A byla tam trombotická mikroangiopatie?
- Úspěšná léčba myelodysplastického syndromu se zvýšeným počtem blastů (MDS-IB2) a chronické lymfocytární leukemie venetoklaxem
- Diagnostika a léčba peripartálního krvácení, konsenzus mezioborové pracovní skupiny modifikovanou metodou ACCORD
- Interdisciplinární doporučení pro testování trombofilie
- MUDr. Věra Vozobulová slaví 70 let
- Aktualita z Olomouckých hematologických dnů. Liso-cel jako nová CAR-T terapie v léčbě lymfomů v ČR
- Aktualita z Olomouckých hematologických dnů. Role avapritinibu v léčbě pokročilé systémové mastocytózy
- Transfusion and Haematology Today
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Interdisciplinární doporučení pro testování trombofilie
- Diagnostika a léčba peripartálního krvácení, konsenzus mezioborové pracovní skupiny modifikovanou metodou ACCORD
- Automatizovaná digitální cytomorfologie zvyšuje spolehlivost diagnostiky kostní dřeně
- Myelomem indukované kardiovaskulární poruchy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

