-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaMožnost ovlivnění duševního zdraví u pacientů s farmakorezistentní schizofrení – augmentace klozapinu dlouhodobě působícími parenterálními antipsychotiky: série případů
Potential impact on mental health in patients with treatment-resistant schizophrenia – clozapine augmentation with long-acting parenteral antipsychotics: a case series
Introduction: The rate of pharmacoresistance among in patients diagnosed with schizophrenia is around 30%. Clozapineis the drug of choice for these patients; however, an adequate response to treatment doesn’t always occur. One of the possible augmentation approaches, specifically for non-adherent patients, is the administration of long-acting parenteral antipsychotics. Our goal was to evaluate previous experiences of administering a combination of the atypical antipsychotic clozapine and long-acting injectable antipsychotics to pharmacoresistant patients at the Department of Psychiatry the Czech Republic and to assess the safety and effectiveness of such administration.
Methods: A retrospective evaluation of patient case studies was conducted for those who were hospitalized in the Ward for the therapy of Psychotic disorders between 2016 and 2020 and had a medication history of combining clozapine and depot antipsychotics.
Results: Over half of the patients had no illness relapses during the observed period. The clinical manifestation of adverse effects from combination therapy appears low in our patient sample, primarily involving mild and pharmacologically manageable side effects (tachycardia). Only one of the cases recorded neutropenia, which led to discontinuation of clozapine; the patient was maintained on long-acting injectable antipsychotics medication.
Conclusion: From our findings, it can be inferred that augmenting clozapine with depot antipsychotics is a potential therapeutic intervention that pharmacoresistant patients could benefit from. However, it is essential to emphasize that this therapeutic approach should only be administered after carefully considering the patient’s existing treatment. It should be strictly individualized based on the treating physician’s or clinical pharmacist’s sufficient professional experience.
Keywords:
pharmacoresistance – Schizophrenia – clozapine – long-acting antipsychotics – nonadherence
Autoři: M. Nováková 1,2*; T. Hammer 1,3*; E. Nováková 1; M. Mayerová 4; L. Ustohal 1,4; PharmDr. Bc. Hana Kotolová, Ph.D. 1
Působiště autorů: Ústav farmakologie a toxikologie, Farmaceutická fakulta, Masarykova univerzita, Brno Palackého třída 1946/1, 612 00 Brno e-mail: kotolovah@pharm. muni. cz 1; Ústav aplikované farmacie, Farmaceutická fakulta, Masarykova univerzita, Brno 2; Farmakologický ústav, Lékařská fakulta, Masarykova univerzita, Brno 3; Psychiatrická klinika Lékařské fakulty Masarykovy Univerzity a Fakultní nemocnice Brno 4
Vyšlo v časopise: Čes. slov. Farm., 2023; 72, 277-287
Kategorie: Původní práce
doi: https://doi.org/10.5817/CSF2023-6-277Souhrn
*hlavní autoři
Úvod: Míra farmakorezistence se u pacientů s diagnózou schizofrenie pohybuje okolo 30 %. U těchto pacientů je léčivemvolby klozapin, ovšem ne vždy dochází k adekvátní odpovědi na léčbu. Jedním z možných augmentačních přístupůspecificky u nonadherentních pacientů je aplikace dlouhodobě působících parenterálních antipsychotik. Našim cílem bylozhodnotit dosavadní zkušenosti z podání kombinace atypického antipsychotika klozapinu a dlouhodobě působících injekčních antipsychotik farmakorezistentním pacientům na Psychiatrické klinice FN Brno v České republice a zhodnotit bezpečnost a účinnost takového podání.
Metody: Byla provedena retrospektivní evaluace kazuistik pacientů, kteří byli vletech 2016–2020 hospitalizováni na Oddělení pro terapii psychotických poruch a měli v lékové anamnéze kombinaci klozapinu a depotního antipsychotika.
Výsledky: U více než u poloviny pacientů nedošlo během sledovaného období k relapsu onemocnění. Klinická manifestace nežádoucích účinků kombinační léčby se jeví na našem vzorku pacientů nízká, manifestovaly se především mírné a farmakologicky řešitelné nežádoucí účinky(tachykardie). Pouze u jedné z kazuistik byla zaznamenána neutropenie, která vyústila k vysazení klozapinu a pacientovibyla ponechána medikace dlouhodobě působícího injekčního antipsychotika.
Závěr: Z našeho zjištění vyplývá, že augmentace klozapinu depotními antipsychotiky je možnou terapeutickou intervencí,ze které by mohli mít farmakorezistentní pacienti vysoký profit. Nicméně je nutné zdůraznit, že tento terapeutický přístup by měl být podán pouze po důkladném zvážení dosavadní terapie, a tedy striktně individualizovaný, vázaný na dostatečnou odbornou zkušenost ošetřujícího lékaře, popř. klinického farmaceuta.
Klíčová slova:
farmakorezistence – schizofrenie – klozapin – dlouhodobě působící antipsychotika – nonadherence
Úvod
Schizofrenie náleží mezi závažná devastující chronická duševní onemocnění významně narušující kvalitu života pacientů. Ovlivňuje nejen osobní a rodinný, ale i pracovní život, a zasahuje také do oblasti mezilidských vztahů. Prevalence se podledostupných dat pohybuje okolo 0,5 %1, 2).
Pro terapii schizofrenie je stěžejní nastavení medikace léčivy ze skupiny antipsychotik, jejichž společným mechanismem účinku je blokování rodiny D2 postsynaptických dopaminových receptorů. Tyto léky redukují zejména pozitivní příznaky, do určité míry i negativní příznaky onemocnění a zlepšují sociální fungování pacientů3). Terapeutický účinek antipsychotik je často nedostatečný a u přibližně 30 % pacientů se objevuje schizofrenie rezistentní na léčbu/treatment-resistant schizophrenia (TRS). O TRS hovoříme v případě, kdy dochází k nepřiměřené odpovědi na ≥ dva různé neklozapinové antipsychotické léky jak z 1., tak 2. generace antipsychotik, každé užívané v přiměřené dávce a délce trvání, přičemž je známo, že byl pacient kterapii adherentní4).
I přes úvahy o jiných možnostech terapie TRS a nutnosti individualizace léčebných strategií, je za léčivo volby stálepovažován klozapin5, 6). Klozapin byl zařazen do terapie v sedmdesátých letech 20. století jako atypické antipsychotikum 2. generace, které vykazovalo oproti antipsychotikům 1. generace nižší tendencí k extrapyramidovým nežádoucím účinkům7).Léčivo ale bylo od poloviny sedmdesátých let stahováno z některých evropských trhů kvůli výskytu závažného nežádoucího účinku – agranulocytózy, který byl hlášen ve Finsku v roce 19758). Nedůvěra v klozapin byla zvrácena přelomovou studií Kanea zroku 1988, ve které klozapin přinesl zlepšení u přibližně 30 % pacientů, kteří splnili přísná kritéria pro rezistenci na léčbu. Studie prokázala superioritu klozapinu v parametru účinnosti oproti chlorpromazinu9). Tento milník vedl v devadesátých letech 20. století k znovuuvedení klozapinu na většinu světového trhu a k jeho návratu k terapii konkrétně TRS7, 10).
Vyšší účinnost klozapinu u TRS oproti jiným antipsychotikům 1. a 2. generace byla opakovaně potvrzena, navíc o jeho významu hovoří i skutečnost, že je zařazen v seznamu WHO Model List of Essential Medicines9, 11, 12). Klozapin je spojovántaké s dalšími benefitními vlastnostmi, jako je náladu stabilizující efekt, snížení rizika sebevražedných pokusů, u pacientů také dochází ke zlepšení kognitivních funkcí13). Vykazuje nízkou tendenci k extrapyramidovým nežádoucím účinkům, a proto ho lze využít u pacientů s Parkinsonovou chorobou s manifestovanou psychózou. Využívá se i jeho efektu při léčbě klidového a posturálního třesu u této diagnózy14–16).
Terapie klozapinem je specificky indikována pro pacienty s TRS17), přičemž je provázena nutností pravidelně sledovat hematologické parametry z důvodu rizika krevní dyskrazie, sledují se také plazmatické koncentrace klozapinu pronastavení optimální terapeutické dávky. Riziko neutropenie/agranulocytózy je při užívání klozapinu vyčísleno na 3,8 %(závažné u 0,9 % pacientů; mortalita se objevuje u 0,01 % pacientů) a vyskytuje se většinou v prvních 3 měsících léčby1, 18, 19).
Klozapin i přes svou schopnost postihnout více receptorových systémů (vykazuje vazebnou afinitu k dopaminergním, serotonergním, cholinergním, adrenergním a histaminergním receptorům)20, 21), není v rámci monoterapie TRS u 40–70 % pacientů dostatečně efektivní22–24). Jedná se o pacienty se schizofrenií rezistentní ke klozapinu/clozapine-resistant schizophrenia (CRS), kteří náleží vůbec k nejtěžším pacientům se schizofrenií. Dochází u nich k výraznější manifestaci pozitivních a negativních příznaků, je zde předpoklad vyššího využití zdravotnických služeb, včetně opakované a delší hospitalizace v důsledku relapsu onemocnění, které přispívají k vyšším nákladům na zdravotní péči a k nižší kvalitě života24).
Terapie CRS není v současné době uspokojivě zvládnuta a velice často jsou zkoušeny nové a odlišné strategie léčby těchto pacientů. Nejčastějším přístupem je augmentace efektu klozapinu, a to zavedením další psychotropní látky24, 25).Vedle antipsychotik zejména 2. generace, antidepresiv a stabilizátorů nálad se využívá i efektu elektrokonvulzivní a kognitivně-behaviorální terapie. Výsledky nejsou prozatím jednoznačné24, 26). Přes nedostatek publikovaných klinických důkazů, jsou i mírné přínosyaugmentačních strategií považovány za prospěšné vzhledem k rozšířenému nepříznivému dopadu CRS27–29).
Novější možnost augmentace představují dlouhodobě působící injekční antipsychotika (LAI APs). Tato možnost augmentačního přístupu vychází všeobecně z časté nonadherence pacientů se schizofrenií k antipsychotické medikaci, konkrétně při terapii klozapinem se setkáváme se zdokumentovanou nonadherencí u 10–55 % pacientů30–34).
LAI APs jsou depotní parenterální lékové formy, které byly vyvinuty s cílem zajistit terapii pacientů se schizofrenií a snížit riziko relapsu. V klinické praxi máme zástupce z 1. i 2. generace antipsychotik (např. haloperidol dekanoát, paliperidon palmitát, aripiprazol monohydrát)35). LAI APs jsou v rámci různých odborných doporučení uvedena jako terapeutická možnost u pacientů, u kterých je přítomno nebo existuje riziko nonadherence36, 37). Kromě schopnosti LAI APs předejít nonadherenci, patří k dalším výhodám léčby, oproti perorálním formulacím, určitá míra komfortu. Pacient nemusí pamatovat na každodenní užívání léčiva, dochází ke snížené frekvenci dávkování a také perorální polyfarmacie. Z pohledu lékaře se pak jedná ovčasnou identifikaci nonadherence13). Dále bylo popsáno, že LAI APs současně snižují počet hospitalizací a využití zdravotní péče, zlepšují také kvalitu života35, 38–40).
Využití depotních formulací antipsychotik k augmentaci klozapinu se nabízí zejména u nonadherentních pacientů. Doposudjsou publikované zkušenosti z augmentačního podání v rámci jednotlivých kazuistik a sérií pacientů a jejich retrospektivního zhodnocení41–46), k dispozici jsou i zrcadlové typy studií13, 47–49). Z těchto dosavadních publikačních výsledků vyplývá, že kromě snížení míry nonadherence může augmentace klozapinu pomocí LAI APs hrát roli ve zvýšení odpovědi klozapinu u CRS, objevuje se nižší riziko relapsů a snížený počet a délka hospitalizací. Kombinace klozapinu s LAI APs vede ke snížení tendence k agresivnímu chování a ke snížení míry sebevražedných pokusů, pacienti také vykazují lepší schopnost sociálního fungování. Výsledky augmentace klozapinu LAI APs naznačují, že k dosažení efektu v terapii je potřeba nižších dávek obouléčiv, což je příznivá informace z pohledu možného výskytu nežádoucích účinků24).
Dle přehledu klinických dat13, 41–49) i dostupného review24), můžeme zhodnotit, že panuje zájem odborné veřejnosti oshromáždění dalších klinických důkazů o významu augmentace klozapinu pomocí LAI APs u pacientů s CRS.
Klinická studie
Předkládáme retrospektivní zhodnocení kazuistik pacientů se schizofrenií, kteří měli v medikaci augmentaci klozapinu pomocí LAI APs.
Cílem bylo zhodnocení bezpečnosti a účinnosti kombinace klozapinu a LAI APs u pacientů s diagnózou schizofrenie neboschizoafektivní porucha. Pro analýzu dat byly použity lékařské záznamy pacientů hospitalizovaných v České republice naPsychiatrické klinice Fakultní nemocnice Brno (PK FN Brno) v letech 2016–2020.
Studovaná populace pacientů
Do studie byli zařazeni pacienti splňující kritéria definovaná na začátku sběru dat. Sběr dat probíhal na PK FN Brno, v České republice, na Oddělení pro terapii psychotických poruch. Ze všech pacientů hospitalizovaných v letech 2016-2020byl vybrán soubor pacientů, kteří měli v lékové anamnéze klozapin. V dalším kroku byli z tohoto souboru vybráni pouzepacienti, kteří měli v lékové anamnéze klozapin a LAI APs.
Přesný souhrn vylučovacích kritérií:
- hospitalizace na Oddělení pro terapii psychotických poruch krajské nemocnice pouze mimo roky 2016 až 2020
- léková anamnéza neobsahující klozapin a LAI APs
- klozapin a LAI APs v lékové anamnéze, ale ne současně
- nepřítomnost diagnózy schizofrenie a schizoafektivní porucha
- nejasná diagnóza
- věk při poslední hospitalizaci nižší než 18 let, nebo vyšší než 60 let
Kritéria retrospektivního posouzení splňovalo celkem 15 pacientů, kteří byli zařazeni do konečného souboru pacientů. Odtěchto pacientů byly získány zdravotní záznamy, které sloužily ke zpracování 15 kazuistik.
Analýza dat
Ke zpracování kazuistik byly poskytnuty řešitelům záznamy pacientů v anonymizované podobě na základě výzkumné spolupráce Farmaceutické fakulty Masarykovy univerzity, Brno (FaF MU Brno) a PK FN Brno.
Všechna potřebná data byla extrahována z elektronického zdravotního záznamu FN Brno a přenesena do textovéhoeditoru MS Word 2020. Takto získané záznamy v anonymní podobě byly zpracovány řešitelem z FaF MU Brno do kazuistik.
Záznamy pacientů byly zkoumány zpětně, aby se získal dojem o celkovém klinickém efektu augmentačního přístupu. Byly také použity ke zjištění nežádoucích účinků kombinační terapie a jejich vyhodnocení.
Kazuistiky byly vypracovány dle následujícího schématu: krátký úvod o pacientovi, jeho konečná diagnóza a věk při poslední hospitalizaci, rodinná anamnéza, osobní anamnéza a chronologicky seřazené jednotlivé hospitalizace pacienta. V kazuistikách je pak následně uvedena poslední známá hospitalizace pacienta.
Kazuistiky byly seřazeny vzestupně podle roku poslední hospitalizace od roku 2016 po rok 2020, k jednotlivým kazuistikám byla vzestupně přidělena čísla, byly zpracovány anonymně, bez údajů jasně identifikujících daného pacienta – data byla zpracovávána bez jména, adresy, rodného čísla.
V rámci práce byly zpracovány tabulky s lékovou anamnézou pacienta. Na konci kazuistiky bylo vypracováno krátké shrnutí.
Pro zpracování kazuistik nebyl použit obsah lékových záznamů, který neměl význam pro sledované parametry, popř. bylyodstraněny gramatické nepřesnosti a došlo k úpravě textu.
Vývojový diagram procesu výběru je znázorněn na obrázku 1.
Demografické údaje, zastoupení konečných diagnóz, délka léčby s konečnou diagnózou, předcházející antipsychotická léčba, LAI APs použitá v rámci augmentačního přístupu, klinická manifestace nežádoucích účinků a zaznamenaný terapeutický efekt byly tabulkově zpracovány. Tato data se stala podkladem pro zhodnocení účinnosti a bezpečnosti kombinace klozapinu a LAI APs a také dalších souvisejících výstupů.
Byly zjištěny základní statistické parametry (medián, směrodatná odchylka), výsledky byly zpracovány tabulkově, parametr účinnosti byl graficky vyjádřen.
Výsledky
V rámci retrospektivního srovnání splnilo kritéria pro zařazení celkem 15 pacientů, u kterých došlo k vypracování kazuistik dle výše uvedeného schématu, a byl zpracován lékový profil.
Primárním výsledkem našeho zhodnocení série případů bylo posouzení účinnosti kombinační terapie klozapinu a LAI APs v rámci sledovaného období (2016–2020), tedy zda u pacientů po nasazení augmentační strategie došlo k relapsu akutních psychotických příznaků a byli/nebyli hospitalizováni.
Současně, pokud v zdravotních záznamech byla zaznamenána hospitalizace, bylo posouzeno, z jakého důvodu došlo k výskytu relapsu onemocnění. Zda pacienti relabovali z důvodu pokračující nonadherence, došlo k relapsu z důvodu abúzunávykových látek anebo augmentace byla z neznámých důvodů ukončena.
Sekundárním výsledkem sledování bylo zjistit profil pozorovaných nežádoucích účinků augmentační strategie se zaměřením na míru výskytu krevní dyskrazie v podobě, která vedla k nutnému přerušení kombinační léčby.
Demografická charakteristika
V rámci posuzovaného vzorku 15 pacientů převažovali muži 60 % (n = 9), průměrný věk účastníků byl 39,07 let (± SD9,05) s rozmezím mezi 20–53 lety (max. = 53, min. = 20, nejvíce byli zastoupeni pacienti ve věkové kategorii 31–40let, osm pacientů). U pacientů převažovalo středoškolské vzdělání, většina pacientů je nezaměstnaných a pobírá invalidní důchod. Demografické údaje pacientů jsou uvedeny v tabulce 1.
Klinická data
Ze souboru 15 pacientů převažovali pacienti s diagnózou paranoidní schizofrenie, jednalo se o 86,7 % pacientů (n = 13). U jednoho pacienta byla diagnostikována katatonní schizofrenie a jeden pacient trpěl schizoafektivní poruchou. Průměrná délka antipsychotické terapie před zahájením augmentační strategie byla u pacientů v našem souboru 10,7 let (medián 9 let, ± SD 7,1), nejvíce pacientů bylo zastoupeno v kategorii 1–5 let, jednalo se celkem o pět pacientů.
Obr. 1. 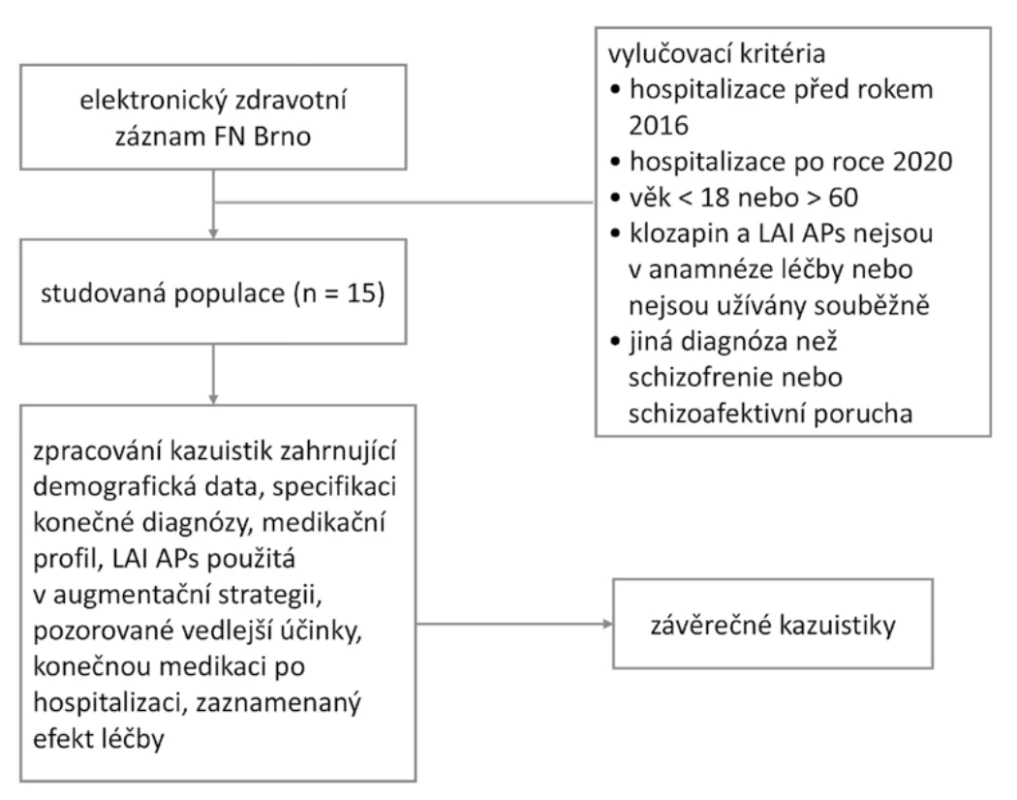
Obr. 1. Vývojový diagram procesu výběruPacienti mající kombinaci klozapinu a LAI APs odpovídali ve 13 případech (86,7 %) schizofrenii farmakorezistentní k léčbě. TRS byla zpětně posouzena/ověřena na základě lékové anamnézy zpracované pro každého pacienta tabulkově, vyplývající ze zpracovaných kazuistik. U kazuistiky 4 byla volena kombinace depotního risperidonu z důvodu nonadherence pacientak užívání léčiv a klozapinu zejména pro antiagresivní působení. U případu 15 není dostatečně znám lékový profil před zahájením augmentační strategie. TRS nebylo možné posoudit. Pacientka byla před nasazením augmentace cca 14 let léčena s diagnózou paranoidní schizofrenie, docházelo u ní k opakovaným hospitalizacím.
Noncompliantní přístup k užívání léčiv byl jako důvod nasazení LAI APs volen celkově u 13 pacientů, tedy opět u 86,7 % pacientů.
Klinické údaje pacientů jsou uvedeny v tabulce 2.
Tab. 1. Demografické údaje pacientů
Pacient
Věk*
Pohlaví
Dosažené vzdělání
Stav zaměstnání**
1
41
muž
středoškolské
?
2
35
muž
středoškolské
?
3
33
muž
středoškolské
ZM
4
31
muž
středoškolské
NZ
5
53
muž
?
?
6
47
žena
středoškolské
NZ(ID)
7
40
muž
vysokoškolské
NZ(ID)
8
34
muž
středoškolské
NZ(ID)
9
53
žena
vysokoškolské
NZ(ID)
10
32
muž
středoškolské
NZ(ID)
11
50
muž
základní
NZ(ID)
12
38
žena
vysokoškolské
NZ(ID)
13
37
žena
vysokoškolské
?
14
20
žena
?
?
15
42
žena
vysokoškolské
NZ(ID)
*Věk je stanoven k datu poslední hospitalizace.
**ZM – zaměstnaný, NZ – nezaměstnaný, ID – invalidní důchod, ? – údaj neznámýTab. 2. Klinické údaje pacientů
Pacient
Diagnóza
Antipsychotická terapie v letech předzačátkem augmentace
TRS*
Noncompliantní přístup k užíváníléčiv
1
PS
14
✔
✔
2
PS
5
✔
✔
3
PS
4
✔
✔
4
PS
2
–
✔
5
PS
24
✔
–
6
PS
8
✔
✔
7
PS
12
✔
✔
8
PS
7
✔
✔
9
KS
3
✔
✔
10
SP
9
✔
✔
11
PS
24
✔
✔
12
PS
18
✔
–
13
PS
12
✔
✔
14
PS
5
✔
✔
15
PS
14
–
✔
PS – paranoidní schizofrenie, KS – katatonní schizofrenie, SP – schizoafektivní porucha
*U pacientů došlo k nepřiměřené odpovědi na ≥ dva různé neklozapinové antipsychotické léky jak z 1., tak 2. generace, každé užívané v přiměřené dávce a délce trvání, přičemž bylo zajištěno dodržování medikace4).Posouzení účinnosti kombinační terapie klozapinu a LAI APs
Cílem terapie schizofrenie je vymizení psychotických příznaků onemocnění, prevence relapsu a navrácení pacienta doběžného života, tedy umožnění fungování v sociální i pracovní sféře. U farmakorezistentních pacientů je navození remise většinou komplikované50, 51).
K posouzení účinnosti augmentačního přístupu jsme retrospektivně hodnotili, zda ve sledovaném období (2016–2020) po nasazení kombinace klozapinu a LAI APs došlo u pacientů ke stabilizaci stavu, pacienti byli propuštěni do ambulantní péče a nebyl zaznamenán relaps psychotických příznaků onemocnění/opětovná hospitalizace a změna medikace.
Dále byla zhodnocena předchozí zkušenost s podáním LAI APs. V tabulce 3 jsou také uvedena konkrétní LAI APs použitá v rámci augmentační strategie.
Pacienti měli ve většině případů zkušenost s podáním depotní lékové formy před nasazením kombinace klozapinu a LAI APs, a to zejména z důvodu časté nonadherence k léčbě. K nejčastějším LAI APs nasazených v rámci poslední známé augmentační strategie patřil flupentixol dekanoát.
Obr. 2. 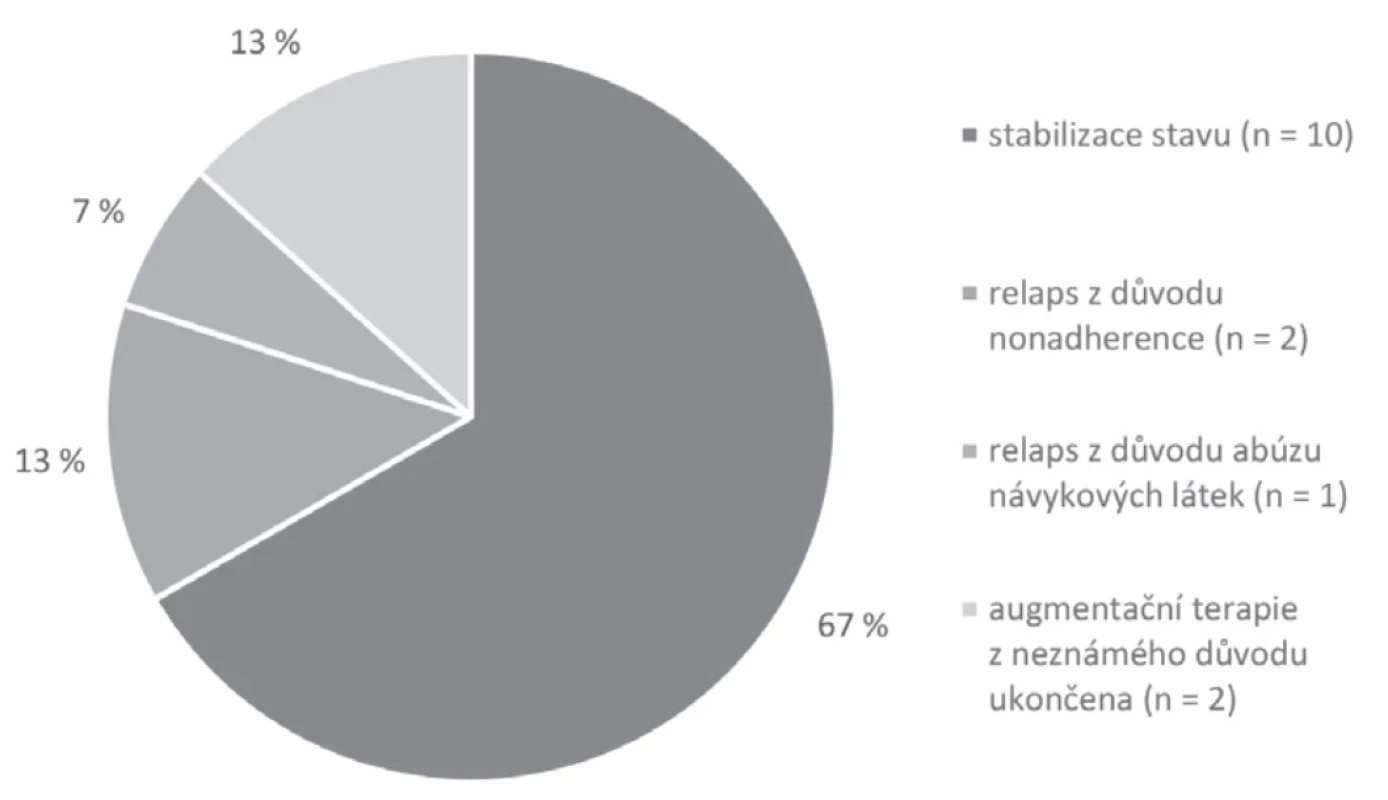
Obr. 2. Výsledky augmentační strategieTab. 3. Výstupy z retrospektivního posouzení augmentační strategie
Pacient
Předchozíterapie LAIAPs
LAI APs použitá
v rámci augmentace
Stabilizace stavu/relapsonemocnění
Pokračovala augmentacepo poslední hospitalizaci?
1
✔
flupentixol
stabilizace
ano
2
✔
haloperidol
stabilizace
ano
3
✔
zuclopentixol
stabilizace
ano
4
–
risperidon
stabilizace
ano
5
✔
zuclopentixol
stabilizace
ano
6
✔
flupentixol
stabilizace
ano
7
✔
risperidon
relaps z důvodu abúzunávykových látek
ano
8
–
paliperidon
stabilizace
ano
9
–
flupentixolhaloperidol
relaps v důsledku nonadherence
ne
10
✔
flupentixol
relaps v důsledku nonadherence
ne
11
✔
paliperidon
stabilizace (s přetrvávajícímikognitivními příznaky)
ano
12
–
zuclopentixol
stabilizace
ano
13
–
flufenazin
augmentace z neznáméhodůvodu ukončena
ne
14
–
paliperidon
stabilizace
ano
15
✔
flupentixol
augmentace z neznáméhodůvodu ukončena
ne
Ve většině případů byli pacienti po sledované období stabilní bez zaznamenané opětovné hospitalizace/ relapsu onemocnění (n = 10, 66, 7 % případů). U jednoho případu (č. 7) je popisován abúzus marihuany, kdy v průběhu augmentace došlo k prohloubení psychotických a hypomanických příznaků, pacient musel podstoupit detoxifikační pobyt, augmentační strategie mu byla ale následně ponechána. V jednom případě (č. 9) se v průběhu augmentace objevovala častá nonadherence, která vedla k relapsům onemocnění, augmentace byla nakonec ukončena z důvodu výskytu neutropenie. U kazuistiky 13. byl flufenazin dekanoát podáván pouze po krátkou dobu, vysazen byl ambulantně z neznámého důvodu, pacient byl následně hospitalizován pro další relapsy onemocnění. U případu č. 15 byla také augmentace z neznámého důvodu ukončena, při následných hospitalizacích nebyla již použita. Výsledky augmentační strategie ukazuje graf na obrázku 2.
Z našeho souboru pacientů (n = 15) více než polovina zůstala po sledované období stabilní (n = 10), 13,3 % pacientů (n = 2) relabovalo z důvodu pokračující nonadherence, u jednoho pacienta došlo k relapsu z důvodu pokračujícího abúzu návykových látek a u dvou pacientů byla augmentace ukončena z neznámého důvodu.
Nežádoucí účinky pozorované během sledování pacientů
V rámci našeho souboru pacientů jsme sledovali míru výskytu nežádoucích účinků, pozorované nežádoucí účinky jsou uvedeny v tabulce 4.
Nežádoucí účinky spojené s monoterapií klozapinem pozorované před augmentací
Klozapin byl ve většině případů podáván již před zahájením augmentačního přístupu. V rámci našeho sdělení uvádíme ipřehled nežádoucích účinků, které byly spojené právě s podáním klozapinu v monoterapii.
S podáním klozapinu se vyskytla farmakologicky řešitelná tachykardie (n = 4; 26,7 % případů), která byla zaléčena ve všech případech metoprololem a nebyla důvodem pro vysazení klozapinu. Ve dvou případech (n = 2; 13 % případů) byla pozorována obstipace, která byla zaléčena laxativy. V jednom případě (6,7 % případů) byla popsána v úvodu terapiepočáteční únava. V případě č. 9 byla již v úvodu terapie, následně i při dalších hospitalizacích, pozorována neutropenie,která však nebyla důvodem pro ukončení medikace v rámci monoterapie klozapinem.
Nežádoucí účinky související se strategií augmentace
U našeho souboru pacientů jsme hodnotili míru výskytu nežádoucích účinků, které se objevily během augmentace, abychom posoudili bezpečnost této kombinace léčiv u sledované skupiny pacientů. Zejména nás zajímalo potencionální riziko výskytu život ohrožujících nežádoucích účinků.
Tab. 4. Pozorované nežádoucí účinky v souboru pacientů
Pacient
Nežádoucí účinky spojené s monoterapiíklozapinem před augmentací
Nežádoucí účinkysouvisející s augmentační strategií
Výskytzávažnýchnežádoucích účinků
1
–
–
–
2
tachykardie (podán metoprolol)
–
–
3
–
–
–
4
–
–
–
5
–
–
–
6
–
–
–
7
mírná tachykardie (podán metoprolol) a počátečníúnava
–
–
8
mírná trombocytopénie (podán přechodněpyridoxin a kyselina listová)
–
–
9
v úvodu terapie – přechodný pokles neutrofilů(samovolně se upravil), při další aplikaci kolísavéhodnoty leukocytů a neutrofilů (podány vitamínyskupiny B a C)
neutropenie (podánpyridoxin a kyselina listová)
✔
10
obstipace (laxativa)
–
–
11
–
–
–
12
obstipace (laxativa)
–
–
13
tachykardie (podán metoprolol)
–
–
14
tachykardie (podán metoprolol), mírnýpokles v krevním obraze (podán pyridoxina thiamin)
sinusová tachykardie(podán ivabradin)
–
15
–
–
–
Z tabulky 4 vyplývá, že pouze u jednoho pacienta byla zjištěna neutropenie vedoucí k ukončení augmentační strategie – 6,7 % pacientů.
U tohoto pacienta (č. 9) se neutropenie objevila již před začátkem augmentace, kdy se v úvodu terapie samotným klozapinem samovolně upravila, v dalším průběhu terapie se ovšem objevily kolísavé hodnoty leukocytů a neutrofilů, což bylozaléčeno vitaminy skupiny B a C. Po nasazení konkrétně kombinace klozapinu a depotního haloperidolu byla při kontrolních odběrech zjištěna neutropenie, do medikace byl nasazen pyridoxin a kyselina listová. Stav pacienta se postupně zlepšil, byl propuštěn do ambulantní péče. Následně byl ale klozapin ambulantně vysazen pro neutropenii a nasazen byl nově olanzapin.
Jako další nežádoucí účinek v souvislosti s augmentací byla zjištěna sinusová tachykardie (č. 15), která byla zaléčena podáním ivabradinu. Tachykardie se v tomto konkrétním případě objevovala i při předchozí monoterapii klozapinem. Tachykardie nebyla důvodem pro vysazení kombinační léčby.
Diskuse
Z dostupných antipsychotik klozapin zaujímá nezastupitelné místo v terapii farmakorezistentní schizofrenie. Nabízí řešení pro pacienty, u kterých léčba jinými antipsychotiky nepřináší dostatečnou klinickou odpověď. V rámci naší práce jsme retrospektivně hodnotili účinnost a bezpečnost podání kombinace klozapinu a LAI APs. Vycházeli jsme z lékařskýchzáznamů poskytnutých v anonymizované podobě, které sloužily jako předloha pro zhotovení kazuistik dle předem určeného schématu.
Na základě údajů z kazuistik byla posouzena účinnost augmentační strategie. U nadpoloviční většiny pacientů bylo dosaženo stabilizace stavu bez opětovné hospitalizace ve sledovaném období. Naše výsledky odpovídají doposud publikovaným výsledkům.
Z pohledu bezpečnosti klozapinu z dosavadních zkušeností vyplývá, že díky rozsáhlému receptorovému působení je spojena terapie klozapinem s řadou nežádoucích účinků. Je známo, že přibližně 17 % pacientů užívajících klozapinnakonec léčbu přeruší52). K nejčastěji publikovaným nežádoucím účinkům klozapinu, objevujících se během prvních 3 měsíců terapie, náleží sedace, únava, neklid, závratě, hypersalivace, přírůstek hmotnosti, tachykardie, bolest hlavy, zácpa a zmatenost. Tyto nežádoucí účinky jsou většinou přechodné nebo farmakologicky řešitelné. Mezi vzácné, ale život ohrožující nežádoucí účinky, patří agranulocytóza, myokarditida, neutropenie, Steven-Johnsonův syndrom, kardiomyopatie aperikarditida. Neutropenie a agranulocytóza, které se objevují především během prvních 4 měsíců terapie, jsou častým důvodem k vysazení klozapinu. Užívání klozapinu je tedy spojeno s povinným hematologickým vyšetřením, aby se vyloučilo riziko krevní dyskrazie53). Klozapin naopak vykazuje nízký sklon k extrapyramidovým vedlejším účinkům a nezvyšuje sérový prolaktinnebo hladiny kortikotropinu54).
Při předcházejícím podání klozapinu jsme v našem souboru pacientů pozorovali častotachykardii, která byla ve všech případech úspěšně farmakologicky vyřešena. U dvou pacientů se objevila obstipace,která byla vyřešena podáním laxativ. V souvislosti s podáním klozapinu se ve třech případech objevil mírný pokles vkrevním obraze, tento nežádoucí účinek byl úspěšně stabilizován podáním pyridoxinu a kyseliny listové, popř. pyridoxinua thiaminu. Naše zjištění jsou v souladu s odbornou literaturou, neboť jsme u našeho souboru pacientů pozorovalinežádoucí účinky, které náleží k nejčastěji se vyskytujícím.
Stěžejní z pohledu zhodnocení bezpečnosti našeho podání byl výskyt nežádoucích účinků způsobených kombinačníléčbou. V přímé souvislosti se vyskytly u dvou případů. Pouze u jednoho pacienta se objevila neutropenie, běhemaugmentace nedošlo k adekvátní úpravě hematologických parametrů, proto byla nakonec kombinační terapie ukončena. Vdalším případě se jednalo o farmakologicky řešitelnou tachykardii, která nebyla důvodem k ukončení terapie.
Lze zhodnotit, že podání kombinace klozapinu a LAI APs se jeví u většiny pacientů v rámci našeho souboru kazuistik jako účinné a bezpečné. Z důvodu neutropenie došlo k ukončení augmentace pouze u jednoho pacienta. V rámci augmentační strategie po poslední zaznamenané hospitalizaci pokračovalo v terapii celkem jedenáct pacientů z celkového počtu 15.
Jelikož se jedná o retrospektivní zhodnocení kazuistik, jsou nám známy limity takového posouzení účinnosti a bezpečnosti z důvodu absence zhodnocení statistické významnosti našich zjištění. Hodnotíme účinnost a bezpečnost nazákladě výskytu nebo absence posuzovaného jevu a míry jejich zastoupení v rámci sledovaného období. Sdělení ve formězhodnocení série pacientů má tedy popisný charakter a je založeno zejména na tabulkovém zpracování získaných výsledků. Limitem je také krátký časový úsek hodnocení, pro vyšší vypovídací hodnotu našich výsledků by bylo nutné dlouhodobější sledování pacientů s přesnou komparací stavu před a na konci terapie.
I přes limity našeho zpracování výsledná data poukazují na podání klozapinu s LAI APs jako na možný terapeutický přístup u pacientů dostatečně neodpovídajících na léčbu klozapinem s častou noncompliancí k léčbě. V současné době máme na mezinárodní úrovni publikované v tomto ohledu zrcadlové typy studií, v podmínkách České republiky jsou publikovaná data tohoto typu zatím omezená, a proto má tento charakter sdělení i tak potřebnou vypovídací hodnotu. Nicméně je nutné zdůraznit, že tento terapeutický přístup by měl být podán pouze po důkladném zvážení dosavadníterapie, a tedy striktně individualizovaný, vázaný na dostatečnou odbornou zkušenost ošetřujícího lékaře, popř. klinického farmaceuta.
Střet zájmů: žádný.
Zdroje
- Jauhar S., Johnstone M., McKenna P. J. Schizophrenia. Lancet 2022; 399(10323), 473–486. doi: 10.1016/ S0140-6736(21)01730-X
- World Health Organization. Schizophrenia. WHO website. Available from: https://www.who.int/news-room/fact-sheets/detail/schizophrenia (10. 1. 2022).
- Haddad P. M., Correll C. U. The acute efficacy of antipsychotics in schizophrenia: a review of recent meta-analyses. Ther. Adv. Psychopharmacol. 2018; 8, 303–318.
- Kane J. M., Agid O., Baldwin M. L., Howes O., Lindenmayer J. P., Marder S., Olfson M., Potkin S. G., Correll C. U. Clinical guidance on the identification and management of treatment-resistant schizophrenia. J. Clin. Psychiatry 2019; 80(2), 18com12123.
- Taylor D. M. Clozapine for Treatment-Resistant Schizophrenia: Still the Gold Standard? CNS Drugs 2017; 31, 177–180. doi: 10.1007/s40263-017-0411-6
- Faden J. Treatment-Resistant Schizophrenia: A Brief Overview of Treatment Options. J. Clin. Psychiatry 2019; 80(4), 18ac12394. doi: 10.4088/JCP.18ac12394
- Crilly J. The history of clozapine and its emergence in the US market: a review and analysis. Hist. Psychiatry 2007; 18(1), 39–60.doi: 10.1177/0957154X07070335. PMID: 17580753.
- Griffith R. W., Saameli K. Letter: Clozapine and agranulocytosis. Lancet 1975; 2(7936), 657. doi: 10.1016/s0140-6736(75)90135-x. PMID: 52022.
- Kane J., Honigfeld G., Singer J., Meltzer H. Clozapine for the treatment-resistant schizophrenic. A double-blind comparison with chlorpromazine. Arch. Gen. Psychiatry 1988; 45, 789–796. doi: 10.1001/archpsyc.1988.01800330013001
- Meltzer H. Y., Alphs L., Green A. I., Altamura A. C, Anand R., Bertoldi A., Bourgeois M., Chouinard G., Islam M. Z., Kane J., Krishnan R., Lindenmayer J. P., Potkin S. International Suicide Prevention Trial Study Group. Clozapine treatment for suicidality inschizophrenia: International Suicide Prevention Trial (InterSePT). Arch. Gen. Psychiatry 2003; 60(1), 82–91. doi: 10.1001/archpsyc.60.1.82. Erratum in: Arch. Gen. Psychiatry 2003; 60(7), 735.
- Leucht S., Corves C., Arbter D., Engel R. R., Li C., Davis J. M. Second-generation versus first-generation antipsychotic drugs for schizophrenia: a meta-analysis. Lancet 2009; 373(9657), 31–41. doi: 10.1016/S0140-6736(08)-61764-X
- World Health Organization. Model List of Essential Medicines – 22nd List, 2021. Geneva: World Health Organization; 2021(WHO/MHP/HPS/EML/2021.02). Licence: CC BY-NC-SA 3.0 IGO.
- Grimminck R., Oluboka O., Sihota M., Rutherford D. L, Yeung H. Combination of Clozapine With Long-Acting Injectable Antipsychotics in Treatment-Resistant Schizophrenia: Preliminary Evidence From Health Care Utilization Indices. Prim. Care Companion CNS Disord. 2020; 22(4), 19m02560. doi: 10.4088/PCC.19m02560. PMID: 32678523
- Friedman J. H., Lannon M. C. Clozapine‐responsive tremor in Parkinson’s disease. Mov. Disord. 1990; 5, 225–229.
- Bonuccelli U., Ceravolo R., Salvetti S., D’Avino C., Del Dotto P., Rossi G., Murri L. Clozapine in Parkinson’s disease tremor. Effects of acute and chronic administration. Neurology 1997; 49, 1587–1590.
- Trosch R. M., Friedman J. H., Lannon M. C., Pahwa R., Smith D., Seeberger L. C., O’Brien C. F, LeWitt P. A., Koller W. C.Clozapine use in Parkinson’s disease: a retrospective analysis of a large multicentered clinical experience. Mov. Disord. 1998; 13, 377–382.
- Psychosis and schizophrenia in adults. The NICE guideline on treatment and management – Updated edition 2014 [online]. Available from: https://www.nice.org.uk/ guidance/cg178/evidence/full-guide-line-490503565. (4. 5. 2023).
- Myles N., Myles H., Xia S., Large M., Kisely S., Galletly C., Bird R., Siskind D. Meta-analysis examining the epidemiology of clozapine-associated neutropenia. Acta Psychiatr. Scand. 2018; 138(2), 101–109. doi: 10.1111/ acps.12898
- Couchman L., Morgan P. E., Spencer E. P., Flanagan R. J. Plasma clozapine, norclozapine, and the clozapine:norclozapine ratio in relation to prescribed dose and other factors: data from a therapeutic drug monitoring service, 1993–2007. Ther. Drug Monit. 2010; 32(4), 438–447. doi: 10.1097/FTD.0b013e3181dad1fb
- Yaw T. K., Fox S. H., Lang A. E. Clozapine in Parkinsonian Rest Tremor: A Review of Outcomes, Adverse Reactions, and Possible Mechanisms of Action. Mov.Disord. Clin. Pract. 201530; 3(2), 116–124. doi: 10.1002/mdc3.12266
- de Berardis D., Rapini G., Olivieri L., Di Nicola D., Tomasetti C., Valchera A., Fornaro M., Di Fabio F., Perna G., Di Nicola M., Serafini G., Carano A., Pompili M., Vellante F., Orsolini L., Martinotti G., Di Giannantonio M. Safety of antipsychotics for the treatment of schizophrenia: a focus on the adverse effects of clozapine. Ther. Adv. Drug Saf. 2018; 9(5), 237–256. doi:10.1177/2042098618756261
- Siskind D., Siskind V., Kisely S. Clozapine Response Rates among People with Treatment-Resistant Schizophrenia: Data froma Systematic Review and Meta-Analysis. Can. J. Psychiatry 2017; 62(11), 772–777. doi: 10.1177/0706743717718167
- Roerig J. L. Clozapine augmentation strategies. Ment. Health Clin. 2019 Nov 27; 9(6), 336–348. doi: 10.9740/ mhc.2019.11.336
- Chakrabarti S. Clozapine resistant schizophrenia: Newer avenues of management. World J. Psychiatry 2021; 11(8), 429–448. doi: 10.5498/wjp.v11.i8.429
- Muscatello M. R., Bruno A., de Fazio P., Segura-Garcia C., Pandolfo G., Zoccali R. Augmentation strategies in partialresponder and/or treatment-resistant schizophrenia patients treated with clozapine. Expert Opin. Pharmacother. 2014; 15(16), 2329–2345. doi:10.1517/14656566.2014.956082
- Buckley P., Miller A., Olsen J., Garver D., Miller D. D., Csernansky J. When symptoms persist: clozapine augmentation strategies.Schizophr. Bull. 2001; 27(4), 615–628. doi: 10.1093/oxfordjournals.schbul.a006901
- de Berardis D., Fornaro M., Anastasia A., Vellante F., Valchera A., Cavuto M., Perna G., Di Nicola M., Serafini G., Carano A.,Pompili M., Orsolini L., Tomasetti C., Di Emidio G., Martinotti G., Di Giannantonio M. When clozapine fails: Augmentationstrategies in the management of clozapine-resistant schizophrenia. In: Kim Y. K. (Eds.) Treatment resistance in psychiatry. Singapore:Springer Nature Singapore Pte Ltd, 2019; 349–367. doi: 10.1007/978-981-10-4358-1_23
- Bartoli F., Crocamo C., Di Brita C., Esposito G., Tabacchi T. I., Verrengia E., Clerici M., Carrà G. Adjunctive second-generation antipsychotics for specific symptom domains ofschizophrenia resistant to clozapine: A meta-analysis. J. Psychiatr. Res. 2019; 108, 24–33. doi: 10.1016/j.jpsychires.2018.11.005
- Miyamoto S., Jarskog L. F., Fleischhacker W. W. Schizophrenia: when clozapine fails. Curr. Opin. Psychiatry 2015; 28, 243–248. doi: 10.1097/YCO.0000000000000159
- Davis M. C., Fuller M. A., Strauss M. E., Konicki P. E, Jaskiw G. E. Discontinuation of clozapine: a 15-year naturalistic retrospective study of 320 patients. Acta Psychiatr. Scand. 2014; 130, 30–39. doi: 10.1111/acps.12233 [Epub 2013 Dec 2].
- Krivoy A., Malka L., Fischel T., Weizman A., Valevski A. Predictors of clozapine discontinuation in patients with schizophrenia. Int.Clin. Psychopharmacol. 2011; 26(6), 311–315. doi: 10.1097/YIC.0b013e32834ab34c
- Legge S. E., Hamshere M., Hayes R. D., Downs J., O’Donovan M. C, Owen M. J, Walters J. T. R, MacCabe J. H. Reasons for discontinuing clozapine: A cohort study of patients commencing treatment. Schizophr. Res. 2016; 174(1–3), 113–119. doi: 10.1016/j.schres.2016.05.002
- Pai N. B., Vella S. C. Reason for clozapine cessation. Acta Psychiatr. Scand. 2012; 125(1), 39–44. doi: 10.1111/j.160leucht0-0447.2011.01776.x
- Taylor D. M., Douglas-Hall P., Olofinjana B., Whiskey E., Thomas A. Reasons for discontinuing clozapine: matched, case-controlcomparison with risperidone long-acting injection. Br. J. Psychiatry 2009; 194(2), 165–167. doi: 10.1192/bjp.bp.108.051979
- Leucht C., Heres S., Kane J. M., Kissling W., Davis J. M., Leucht S. Oral versus depot antipsychotic drugs for schizophrenia--a critical systematic review and meta-analysis of randomised long-term trials. Schizophr. Res. 2011; 127(1–3), 83–92. doi: 10.1016/j.schres.2010.11.020
- Galletly C., Castle D., Dark F., Humberstone V., Jablensky A., Killackey E., Kulkarni J., McGorry P., Nielssen O., Tran N. Royal Australian and New Zealand College of Psychiatrists, Royal Australian and New Zealand College of Psychiatrists clinical practice guidelines for the treatment of schizophrenia and related disorders. Aust N Z J Psychiatry 2005; 39, 1–30.
- Kuipers E., Yesufu-Udechuku A., Taylor C., Kendall T. Management of psychosis and schizophrenia in adults: summary of updated NICE guidelines 2014. BMJ 2014; 348, g1173.
- Kishimoto T., Nitta M., Borenstein M., Kane J. M., Correll C. U. Long-acting injectable versus oral antipsychotics in schizophrenia: a systematic review and meta-analysis of mirror-image studies. J. Clin. Psychiatry 2013; 74(10), 957–965. doi: 10.4088/JCP.13r08440
- Kaplan G., Casoy J., Zummo J. Impact of long-acting injectable antipsychotics on medication adherence and clinical, functional, and economic outcomes of schizophrenia. Patient Prefer. Adherence 2013; 7(7), 1171–1180. doi: 10.2147/PPA.S53795
- Manchanda R., Chue P., Malla A., Tibbo P., Roy M. A., Williams R., Iyer S., Lutgens D., Banks N. Long-acting injectable antipsychotics: evidence of effectiveness and use. Can. J. Psychiatry 2013; 58(Suppl 1), 5S–13S. Long-acting injectable antipsychotics: evidence of effectiveness and use.
- Kim S. H., Jung D. CH., Ahn Y. M., Kim Y. S. The combined use of risperidone long-acting injection and clozapine in patients with schizophrenia non-adherent to clozapine: a case series. J. Psychopharmacol. 2010; 24, 981–986. doi: 10.1177/0269881109348174
- Baruch N., Das M., Sharda A., Basu A., Bajorek T., Ross C. C., Sengupta S., Larkin F., Young S. An evaluation of the use of olanzapine pamoate depot injection in seriously violent menwith schizophrenia in a UK high-security hospital. Ther. Adv. Psychopharmacol. 2014; 4, 186–192. doi:10.1177/2045125314531982
- Maia-de-Oliveira J. P., Nunes E. A., Ushirohira J. M., Machado-de-Sousa J. P., Bressan R. A., Hallak J. E. Paliperidonepalmitate for refractory and clozapine-resistant schizophrenia. J. Neuropsychiatry Clin. Neurosci. 2015; 27, e14–e16. doi: 10.1176/appi.neuropsych.13120374 [Epub 2014 Dec 12].
- Kasinathan J., Sharp G., Barker A. Evaluation of olanzapine pamoate depot in seriously violent males with schizophrenia in the community. Ther. Adv. Psychopharmacol. 2016; 6, 301–307. doi: 10.1177/2045125316656319
- Sepede G., Di Iorio G., Spano M. C., Lorusso M., Sarchione F., Santacroce R., Salerno R. M., Di Giannantonio M. A Case of Resistant Schizophrenia Successfully Treated With Clozapine/Long-acting Injectable Aripiprazole Combination. Clin. Neuropharmacol. 2016; 39, 322–324. doi: 10.1097/WNF.0000000000000191
- Oriolo G., Dominguez I., Fortea A., Bioque M., Bernardo M. Combination of clozapine with paliperidone in treatment resistant schizophrenia. Eurneuropsychopharmacol. 2016; 26, S536.
- Souaiby L., Gauthier C., Rieu C., Krebs M. O., Advenier-Iakovlev E., Gaillard R. Clozapine and long-acting injectable antipsychotic combination: A retrospective one-year mirror-image study. Schizophr. Res. 2017; 188, 89–91. doi: 10.1016/j.schres.2017.01.036
- Bioque M., Parellada E., García-Rizo C., Amoretti S., Fortea A., Oriolo G., Palau P., Boix-Quintana E., Safont G., Bernardo M. Clozapine and paliperidone palmitate antipsychotic combination in treatment-resistant schizophrenia and other psychotic disorders: A retrospective 6-month mirror-image study. Eur. Psychiatry 2020; 63, e71. doi: 10.1192/j.eurpsy.2020.72
- Caliskan A. M., Karaaslan M., Inanli I., Caliskan S., Arslan M., Esra Cicek I., Eren I. The effects of adding long-acting injectable antipsychotic drugs to clozapine on relapse and hospitalization in patients with treatment-resistant schizophrenia: a mirror-image retrospective study. Int. Clin. Psychopharmacol. 2021; 36, 30–33.
- Ustohal L., Přikryl R. Léčba rezistentní schizofrenie v praxi. Psychiat. pro Praxi 2009; 10(4), 176–179.
- Patel K. R., Cherian J., Gohil K., Atkinson D. Schizophrenia: overview and treatment options. P. T. 2014; 39(9), 638–645
- Brianne M., Newman M. D., William J., Newman M. D. Rediscovering clozapine: Adverse effects develop – what should you do now? Current Psychiatry 2016; 15(8), 40–46, 48–49.
- Iqbal E., Govind R., Romero A., Dzahini O., Broadbent M., Stewart R., Smith T., Kim C. H., Werbeloff N., MacCabe J. H.,Dobson R. J. B., Ibrahim Z. M. The side effect profile of clozapine in real world data of three large mental health hospitals. PLoS One 2020; 15(12), e0243437. doi: 10.1371/journal.pone.0243437
- Seppälä N. Clozapine-clinical studies on adverse effects and interactions. Academic dissertation. Tampere: Tampere University press, 2014. Available from: https://urn.fi/URN:ISBN:978-951-44-9565–9566 (21. 3. 2023).
Štítky
Farmacie Farmakologie
Článek Úvodník
Článek vyšel v časopiseČeská a slovenská farmacie
Nejčtenější tento týden
2023 Číslo 6- Psilocybin je v Česku od 1. ledna 2026 schválený. Co to znamená v praxi?
- Ukažte mi, jak kašlete, a já vám řeknu, co vám je
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
-
Všechny články tohoto čísla
- Úvodník
- Etické aspekty provádění klinických hodnocení humánních léčivých přípravků
- Stručný pohľad na vlastnosti in silico, vzťahy štruktúra– –aktivita a biotransformáciu fruquintinibu, protinádorovo účinkujúceho liečiva novej generácie obsahujúceho privilegované benzofuránové zoskupenie
- Možnost ovlivnění duševního zdraví u pacientů s farmakorezistentní schizofrení – augmentace klozapinu dlouhodobě působícími parenterálními antipsychotiky: série případů
- Možnosti využití komplexní farmaceutické kompozice pro farmakologickou korekci metabolického syndromu
- Zvýšení účinnosti hypolypidemické léčby kombinovaným užíváním kvercetinu u pacientů s nealkoholickou steatózou jater a souvisejícím metabolickým syndromem
- Analýza podání léčiv ve vztahu k potravě a použitým nápojům u hospitalizovaných pacientů
- K historii a vývoji některých změn v lékárenství – bezpečnost práce v lékárnách
- Krása v knihách – farmaceutická exlibris na území dnešní České republiky
- Česká a slovenská farmacie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Analýza podání léčiv ve vztahu k potravě a použitým nápojům u hospitalizovaných pacientů
- Možnost ovlivnění duševního zdraví u pacientů s farmakorezistentní schizofrení – augmentace klozapinu dlouhodobě působícími parenterálními antipsychotiky: série případů
- Etické aspekty provádění klinických hodnocení humánních léčivých přípravků
- Stručný pohľad na vlastnosti in silico, vzťahy štruktúra– –aktivita a biotransformáciu fruquintinibu, protinádorovo účinkujúceho liečiva novej generácie obsahujúceho privilegované benzofuránové zoskupenie
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



