-
Medical journals
- Career
Léčba metastatických nádorů močového měchýře, systémová chemoterapie, symptomatická léčba
Authors: J. Katolická
Authors‘ workplace: Onkologicko-chirurgické oddělení FN u svaté Anny v Brně
Published in: Urol List 2012; 10(2): 54-56
Overview
Standardním postupem v léčbě inoperabilního lokálně pokročilého nebo metastatického karcinomu je chemoterapie. Chemoterapeutickým režimem pro I. linii je doporučen gemcitabin/cisplatina, který nahradil dlouhodobě užívaný M-VAC (metotrexát, vinblastin, doxorubicin, cisplatina). Vinflunin na základě výsledků studie fáze III můžeme doporučit do druhé linie léčby uroteliálního karcinomu po selhání nebo intoleranci cisplatiny v první linii.
Klíčová slova:
chemoterapie, cisplatina, gemcitabin, vinfluninPRVNÍ LINIE LÉČBY
Standardním postupem v léčbě inoperabilního lokálně pokročilého nebo metastatického karcinomu je chemoterapie. Chemoterapeutické režimy založené na cisplatině u uroteliálního karcinomu močového měchýře dosahují vysokých odpovědí, ale medián přežití se i přes agresivní terapii pohybuje kolem 15 měsíců.
Režim M-VAC v nerandomizovaném klinické studii [1] prokázal regresi tumoru u 72 % nemocných, z toho v 36 % bylo dosaženo kompletní remise. Po dobu tří let přežívalo 55 % léčených, kteří této kompletní remise dosáhli. Následně byl M-VAC srovnáván s monoterapií cisplatinou v prospektivní randomizované studii [2]. Režimem M-VAC nebo cisplatinou v 28denním intervalu bylo léčeno do progrese nebo maximálně šesti cykly 269 nemocných. M-VAC byl spojen s vysokou toxicitou, zejména leukopenií, mukozitidou, febrilní neutropenií a také úmrtím spojeným s léčbou. Procento dosažených odpovědí, doba do progrese i celkové přežití byly u kombinace M-VAC ve srovnání s monoterapií cisplatinou vyšší (tab. 1).
Table 1. M-VAC vs monoterapie cisplatinou. 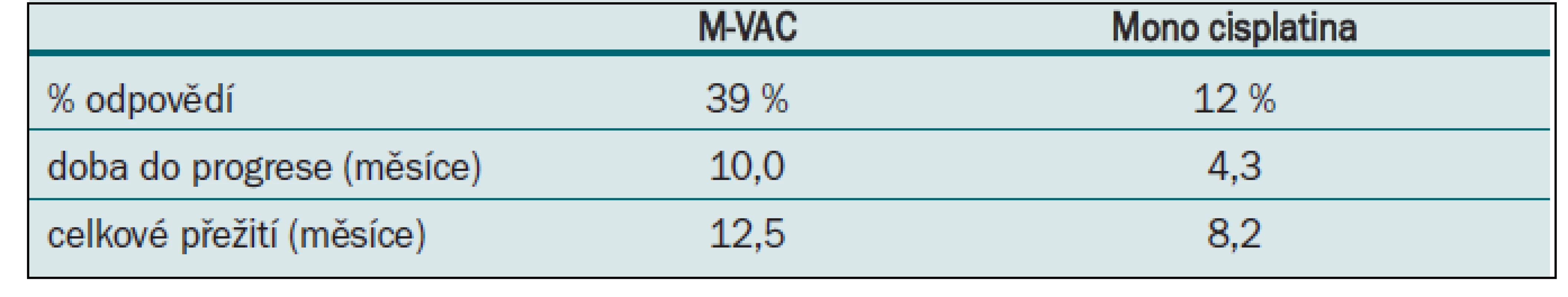
Další randomizovaná studie [3] srovnávala M-VAC s režimem CISCA (cisplatina, cyklofosfamid a doxorubicin). Léčbou M-VAC bylo dosaženo vyšší procento odpovědí a také delší přežití ve srovnání s léčbou kombinací CISCA (tab. 2).
M-VAC byl v randomizované studii EORTC fáze III (protokol #30924) srovnáván ve standardním dávkovacím režimu a ve vysokodávkovaném režimu [4]. Pacienti byli randomizováni do ramene s high-dose M-VAC podávaným každé dva týdny s podporou růstových faktorů a do ramene se standardním dávkováním podávaným každé čtyři týdny. Bylo dosaženo rozdílů v dosažení objektivních odpovědí, kompletních remisí, doby do progrese, ale nebylo dosaženo rozdílu v celkovém přežití, které bylo stanoveno jako primární cíl (tab. 3). V následné revizi po sedmi letech sledování „high-dose“ M-VAC prokázal signifikantní redukci rizika úmrtí v pětiletém sledování (21,8 vs 13,5 %; hazard ratio 0,76). Toxicita byla vyšší v rameni s M-VAC. Na základě této studie byl high-dose M-VAC zaveden v řadě center jako standardní terapeutický režim.
Table 3. High-dose M-VAC vs M-VAC. 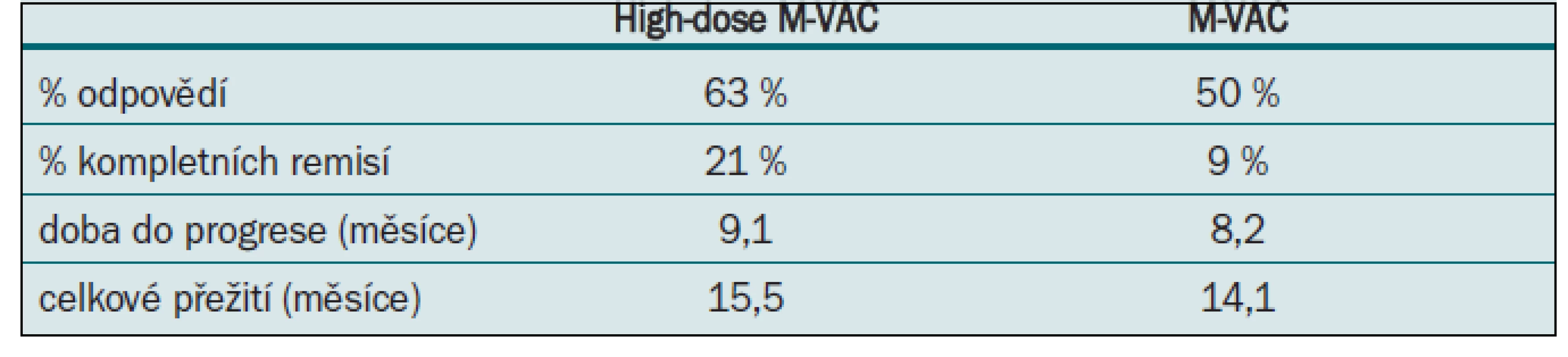
Ve studiích fáze II gemcitabin v kombinaci s cisplatinou prokázal odpověď v 50 % s mediánem přežití 14 měsíců. Na základě těchto výsledků byla provedena randomizovaná studie fáze III na 405 pacientech srovnávající čtyřkombinaci M-VAC s dvojkombinací gemcitabin/cisplatina [5]. Chemoterapie byla aplikovaná každé čtyři týdny s maximem do šesti cyklů. Většího počtu podaných cyklů za menší toxicity bylo dosaženo v dvojkombinačním režimu. Procento odpovědí, doba do progrese i celkové přežití bylo v obou ramenech stejné (tab. 4). Nežádoucí účinky léčby byly ale jednoznačně menší v rameni s gemcitabinem. Tyto výsledky posunuly kombinaci gemcitabin/cisplatina na místo standardního režimu pro pokročilý uroteliální karcinom močového měchýře.
Table 4. M-VAC vs gemcitabin/cisplatina. 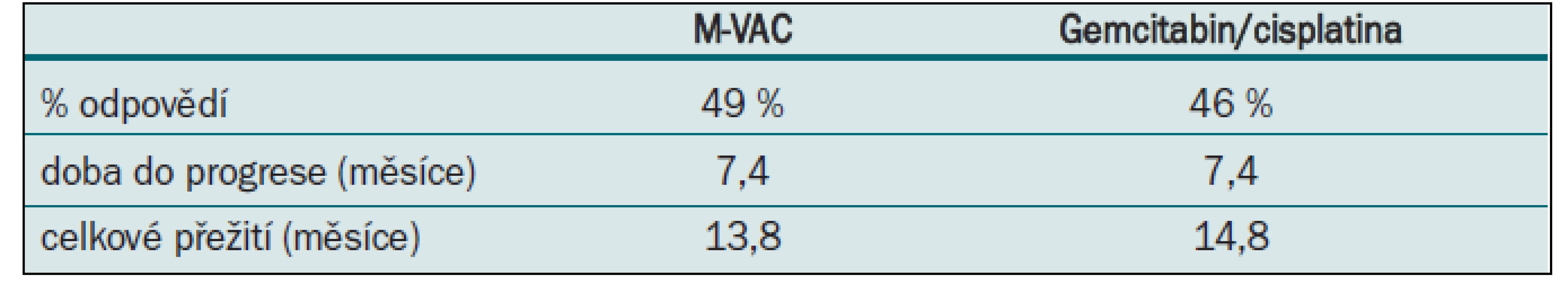
U metastatického karcinomu močového měchýře proběhla řada studií s taxany. V trial EORTC fáze III (protokol #30987) byl ke kombinaci gemcitabin/cisplatina přidán paclitaxel. V tripletu bylo sice dosaženo vyššího počtu objektivních odpovědí (57 vs 46 %) a kompletních remisí (15 vs 10 %), ale statisticky signifikantního rozdílu v celkovém přežití dosaženo nebylo (15,7 vs 12,8 měsíce) [6]. Kombinace docetaxel/cisplatina byla srovnávána s režimem M-VAC ve studii fáze III Hellenic Co-operative Oncology Group [7]. Ve všech sledovaných parametrech – odpověď na léčbu, doba do progrese, doba přežití – bylo v rameni s M-VAC dosaženo lepších výsledků. Studie EORTC (protokol #30986) srovnávala gemcitabin a carboplatinu s metotrexátem, carboplatinou a vinblastinem (M-CAVI) u pacientů s pokročilým karcinomem močového měchýře, kteří pro renální dysfunkci nebo komorbidity nemohou být léčeni cisplatinou. Zařazeno bylo 178 nemocných, objektivních odpovědí v rameni s gemcitabinem a carboplatinou bylo dosaženo u 42 % léčených a u kombinace M-CAVI u 30 %. Carboplatina je variantou pro pacienty s kontraindikacemi cisplatiny, studie také ukázala, že věk není kontraindikací pro podání cisplatiny [8]. S lepším a hlubším poznáním biologie tumorů a cest regulace nádorového růstu, např. VEGFR, EGFR, mTOR, je i u karcinomu močového měchýře testovaná biologická léčba. Probíhá řada studií s biologickou léčbou v I. linii terapie metastatického karcinomu močového měchýře.
Bevacizumab ve studii fáze II Hoosier Oncology Group (GU 04–75) byl aplikován současně s gemcitabinem a cisplatinou v dávce 15 mg/kg každé tři týdny, u 72 % léčených bylo dosaženo objektivní odpovědi, kompletní remise bylo dosaženo u 21 % pacientů, doba bez progrese onemocnění byla 8,2 měsíce a celková doba přežití 20,4 měsíce. V současné době probíhá velká studie fáze III [9]. Pozitivita Her-2/neu u pacientů s uroteliálním karcinomem močového měchýře je velmi variabilní, a to 8,5–81 %. Ve studii fáze II, kde byl trastuzumab u HER-2/neupozitivních pacientů kombinován s paclitaxelem, carboplatinou a gemcitabinem, bylo u 70 % léčených dosaženo objektivní odpovědi, doba do progrese byla 9,3 měsíce a medián přežití 14,1 měsíce. I když jsou tyto výsledky u HER-2/neupozitivních pacientů velmi slibné, není prozatím u uroteliálního karcinomu močového měchýře testování HER-2/neuexprese standardem [10].
DRUHÁ LINIE LÉČBY
Dlouhou dobu se nedařilo definovat standardní režim pro II. linii léčby uroteliálního karcinomu močového měchýře. Souvisí to především s kondicí pacientů, u kterých je po první linii prokázaná progrese onemocnění. Je poměrně těžké do klinické studie pro II. linii zařadit pacienta a po celou dobu studie ho v ní udržet. Léčebné režimy založené na monoterapii paclitaxelem, ifosfamidem a docetaxelem prokázaly 20% a menší odpověď. Kombinační režimy, např. gemcitabin s paclitaxelem, oxali-platina s fluorouracilem (FOLFOX), demonstrovaly odpovědi od 20–27 % se signifikantní hematologickou toxicitou a periferní neuropatií. Vinflunin, vinca alkaloid třetí generace, byl testován v druhé linii léčby u relabujícího nebo refrakterního pokročilého uroteliálního karcinomu močového měchýře po předchozí léčbě založené na cisplatině ve studii fáze III [11]. Studie srovnávala léčbu vinfluninem v kombinaci s nejlepší podpůrnou léčbou (BSC) vs samotná BSC. Celkem 370 pacientů bylo randomizováno do ramene vinflunin + podpůrná léčba a do ramene pouze s podpůrnou léčbou v poměru 2 : 1. V rameni s vinfluninem se z hlediska hematologické toxicity G > 3 nejvíce objevila neutropenie (50 %), febrilní neutropenie (6 %), anémie (19 %), z nehematologické toxicity únava (19 %) a zácpa (16 %). Pacienti léčení kombinací vinflunin + BSC přežívali 6,9 měsíce, nemocní léčení pouze BSC 4,6 měsíce, tento dvouměsíční rozdíl ale nebyl statisticky signifikantní (p = 0,287). Následná Cox analýza hodnotící i prognostické faktory prokázala statisticky signifikantní efekt vinfluninu na celkové přežití (p = 0,036), redukci rizika úmrtí o 23 %. Procento objektivních odpovědí (8,6 vs 0 %), procento kontroly nemoci (41,4 vs 24,8 %) a doba do progrese onemocnění (3,0 vs 1,5 měsíce) byly také statisticky signifikantní ve prospěch vinfluninu. Pokud vezmeme v úvahu ještě k tomu dobrý bezpečností profil vinfluninu, můžeme ho doporučit do druhé linie léčby uroteliálního karcinomu po selhání nebo intoleranci cisplatiny v první linii. Německá studie fáze III srovnávala krátkodobou terapii (maximálně 6 cyklů chemoterapie po 21 dnech) a dlouhodobou terapii (léčba do progrese onemocnění) v kombinaci paclitaxel + gemcitabin v druhé linii léčby u metastatického uroteliálního karcinomu po selhání prvoliniové terapie založené na cisplatině [12]. Výsledky neprokázaly rozdíl v celkovém přežití (7,8 vs 8,0 měsíce), době do progrese (4 vs 3,1 měsíce) ani počtu objektivních odpovědí (37,5 vs 41,5 %). Větší počet anémií (26 vs 6,7 %) se vyskytoval v rameni s dlouhodobou léčbou.
Symptomatická léčba metastatického karcinomu močového měchýře spočívá především v ošetření hematurie (endoskopická koagulace, embolizace větví vnitřní ilické arterie, paliativní cystektomie s derivací moči nebo samotná derivace moči), dále v zajištění derivace moči, analgetické léčbě a v případě metastatického postižení skeletu podání bisfosfonátů.
ZÁVĚR
Základem léčby metastatického uroteliálního karcinomu močového měchýře je chemoterapie. Standardním chemoterapeutickým režimem pro I. linii je kombinace gemcitabin/cisplatina. Vinflunin prokázal efekt ve II. linii léčby jak z hlediska kontroly onemocnění, tak přijatelné toxicity.
MUDr. Jana Katolická, Ph.D.
Onkologicko-chirurgické oddělení
FN u svaté Anny v Brně
jkatolicka@tiscali.cz.
Sources
1. Sternberg CN, Yagoda A, Scher HI et al. Methotrexate, vinblastine, doxorubicin and cisplatin for advanced transitional cell carcinoma of the urothelium. Efficacy and patterns of response and relapse. Cancer 1989; 64(12): 2448–2458.
2. Loehrer PJ Sr., Einhorn LH, Elson PJ et al. A randomized comparison of cisplatin alone or in combination with methotrexate, vinblastine and doxorubicin in patients with metastatic urothelial carcinoma: a cooperative group study. J Clin Oncol 1992; 10(7): 1066–1073.
3. Logothetis CJ, Dexeus FH, Finn L et al. A prospective randomized trial comparing MVAC and CISCA chemotherapy for patients with metastatic urotelial tumors. J Clin Oncol 1990; 8(6): 1050–1055.
4. Sternberg CN, de Mulder PH, Schornagel JH et al. Randomized phase III trial of high-dose-intensity methotrexate, vinblastine, doxorubicin and cisplatin (MVAC) chemotherapy and recombinant human granulocyte colony-stimulating factor versus classic MVAC in advanced urothelial tract tumors: European Organization for Research and Treatment of Cancer protocol no. 30924. J Clin Oncol 2001; 19(10): 2638–2646.
5. von der Maase H, Hansen SW, Roberts JT et al. Gemcitabine and cisplatine versus methotrexate, vinblastine, doxorubicin and cisplatin in advanced or metastatic bladder cancer: results of a large, randomized, multinational, multicenter, phase III study. J Clin Oncol 2000; 18(17): 3068–3077.
6. Bellmunt J, von der Maase H, Mead GM et al. Randomized phase III study comparing paclitaxel//cisplatine/gemcitabine (PCG) and gemcitabine//cisplatin (GC) in patients with locally advanced (LA) or metastatic (M) urothelial cancer without prior systemic therapy. American Society of Clinical Oncology Annual Meeting 2007; Chicago, IL.
7. Bamias A, Aravantinos G, Deliveliotis C et al. Docetaxel and cisplatinwith granulocyte colony-stimulatingfactor (G-CSF) versus MVAC with G-CSF in advanced urothelial carcinoma: a multicenter, randomized phase III study from Helenic Cooperative Oncology Group. J Clin Oncol 2004; 22(2): 220–228.
8. Dreicer R, Manola J, Roth BJ et al. Phase III trial methotrexate, vinblastine, doxorubicin and cisplatin versus carboplatin and paclitaxel in patients with advanced carcinoma of urotelium. Cancer 2004; 100(8): 1639–1645.
9. Hahn NM, Stadler WM, Zon R et al. Mature results from Hoosier Oncology Group GU 04-75 phase II trial of cisplatin (C), gemcitabine (G) and bevacizumab (B) as first-line chemotherapy for metastatic urothelial carcinoma (UC). American Socienty of Clinical Oncology Annual Meeting: 2010. Chicago, IL.
10. Hussain RS, Vaishampayan U, Du W et al. Combination paclitaxel, carboplatin, and gemcitabine is an active treatment for advanced urothelial cancer. J Clin Oncol 2001; 19(9): 2527–2533.
11. Bellmunt J, Theodore C, Demkov Z et al. Phase III trial of vinflunine plus best supportive care compared with best supportive care alone after a platinum-containing regimen in patients with advanced transitional cell carcinoma of the urothelial tract. J Clin Oncol 2009; 27(27): 4454–4461.
12. Albers P, Park SI, Niegisch G et al. Randomized phase III trial of 2¨nd line gemcitabine and paclitaxel chemotherapy in patients with advanced bladder cancer: short-term versus prolonged treatment (German Association of Urological Oncology (AUO) trial AB 20/99) Ann Oncol 2011; 22(2): 288–294
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2012 Issue 2-
All articles in this issue
- Denosumab rozšiřuje možnosti farmakoterapie kostního postižení pacientů s karcinomem prostaty
- Nejnovější informace v oblasti terapeutických cílů a preparátů pro léčbu karcinomu prostaty rezistentního na kastrační léčbu
- Etiologie a diagnostika nádorů horních močových cest
- Ureteroskopická biopsie tumorů horních cest močových: endoskopické a cytologické techniky
- Technické triky a tipy pro retroperitoneální laparoendoskopickou nefrektomii jedním portem (LESS)
- Chemoterapie karcinomů horních cest močových
- Léčba generalizovaných nádorů ledvin: systémová imunoterapie, paliativní léčba
- Zobrazovací metody, jejich přínos pro zjištění rozsahu onemocnění karcinomem močového měchýře
- Léčba nádorů, které neprorůstají do svaloviny: transuretrální resekce, nové postupy
- Chemoterapie a radioterapie u nádorů močového měchýře
- Léčba metastatických nádorů močového měchýře, systémová chemoterapie, symptomatická léčba
- Antimuskarinika a lékové interakce
- Extrakt ze Serenoa repens při léčbě benigní hyperplazie prostaty
- EAU Guidelines pro vazektomii
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Antimuskarinika a lékové interakce
- Zobrazovací metody, jejich přínos pro zjištění rozsahu onemocnění karcinomem močového měchýře
- Chemoterapie a radioterapie u nádorů močového měchýře
- Etiologie a diagnostika nádorů horních močových cest
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


