-
Medical journals
- Career
Paraaortální a pelvická lymfadenektomie - několik poznámek k operačním a pooperačním opatřením, komplikacím
Authors: M. Ožana; M. Mihula; M. Zubík
Authors‘ workplace: Gynekologicko-porodnické oddělení MN Ostrava
Published in: Prakt Gyn 2005; 9(5): 29-30
Overview
Pánevní a paraaortální lymfadenektomie se stala neoddělitelnou součástí diagnostického a léčebného postupu u gynekologických nádorů. Příspěvek se zabývá zhodnocením námi realizovaného operačního postupu a pooperační péčí, jež má minimalizovat rizika spojená s tímto typem operací.
Klíčová slova:
pánevní lymfadenektomie - paraaortální lymfadenektomie – pooperační postupÚvod
Provádění pánevní a paraaortální lymfadenektomie v operačním protokolu karcinomu ovaria a vybraných případů karcinomu těla děložního představuje krok, který upřesňuje prognózu a optimalizuje způsob léčby. Úloha paraaortální lymfadenektomie je v současné době nejpřesněji definována u karcinomu ovaria. U karcinomu endometria je její postavení dosud zdrojem jistých diskusí. Odstranění spádových mízních uzlin je spojeno s vyšším rizikem peroperačních i pooperačních komplikací než u operací méně radikálních, přesto se pánevní a paraaortální lymfadenektomie dnes již staly součástí komplexního chirurgického výkonu, který správně provedený významně napomáhá v určování další prognózy onemocnění a pomáhá stanovit strategii následné léčby [1]; je třeba připomenout i možný terapeutický efekt lymfadenektomie u pacientek s vyšším stadiem onemocnění po úspěšné cytoredukci [7]. Stagingová role operace plyne rovněž z faktu, že u domněle počátečních stadií ovariálního karcinomu má 10-36 % pacientek již postiženy mízní uzliny, a tedy je nutno je klasifikovat jako stadium IIIC [2,4,6,8].
Image 1. Pravé pánevní retroperitoneum, aorta a dolní dutá žíla. 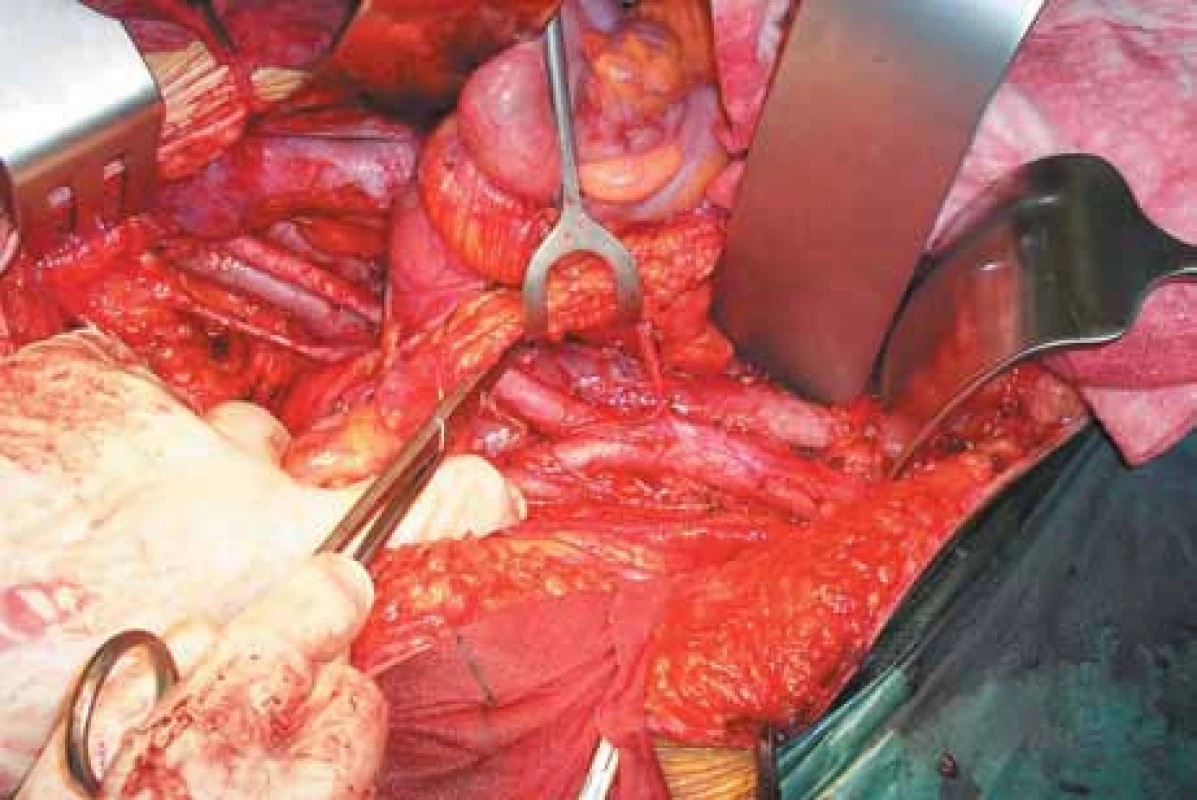
Soubor a metodika
V období 11/2003-11/2004 bylo provedení paraaortální lymfadenektomie současně s pelvickou lymfadenektomií indikováno u 16 pacientek operovaných pro karcinom ovaria či endometria na porodnicko-gynekologickém oddělení MN Ostrava. Zvolený operační přístup k odstranění vazivově tukové tkáně s mízními uzlinami z aortokaválního prostoru byl transperitoneální z vertikální incize zadního peritonea (radixu mesenteria) s následným peroperačním vyluxováním kliček tenkého střeva mimo operační ránu. Výše preparace byla dána odstupem renálních cév, tj. cca 6-7 cm nad odstupem a. mesenterica inferior, která byla při preparaci vždy pečlivě izolována (v 1 případě byla nutná její ligatura pro krvácení bez následných komplikací). Vzhledem k tomu, že v literatuře nejčastěji uváděnými peroperačními komplikacemi je poranění cév, zvláště vén, a nervů [3], operovali jsme v 7 případech - u pacientek s vysokým BMI a s očekávaným vyšším rizikem peroperačních komplikací - v přítomnosti cévního chirurga. Následně jsme zpětně analyzovali některé sledované údaje, které by měly dokumentovat úspěšnost chirurgické léčby, peroperační a pooperační opatření a eventuelní komplikace.
Image 2. Stav po odstranění uzlin podél cévních svazků. 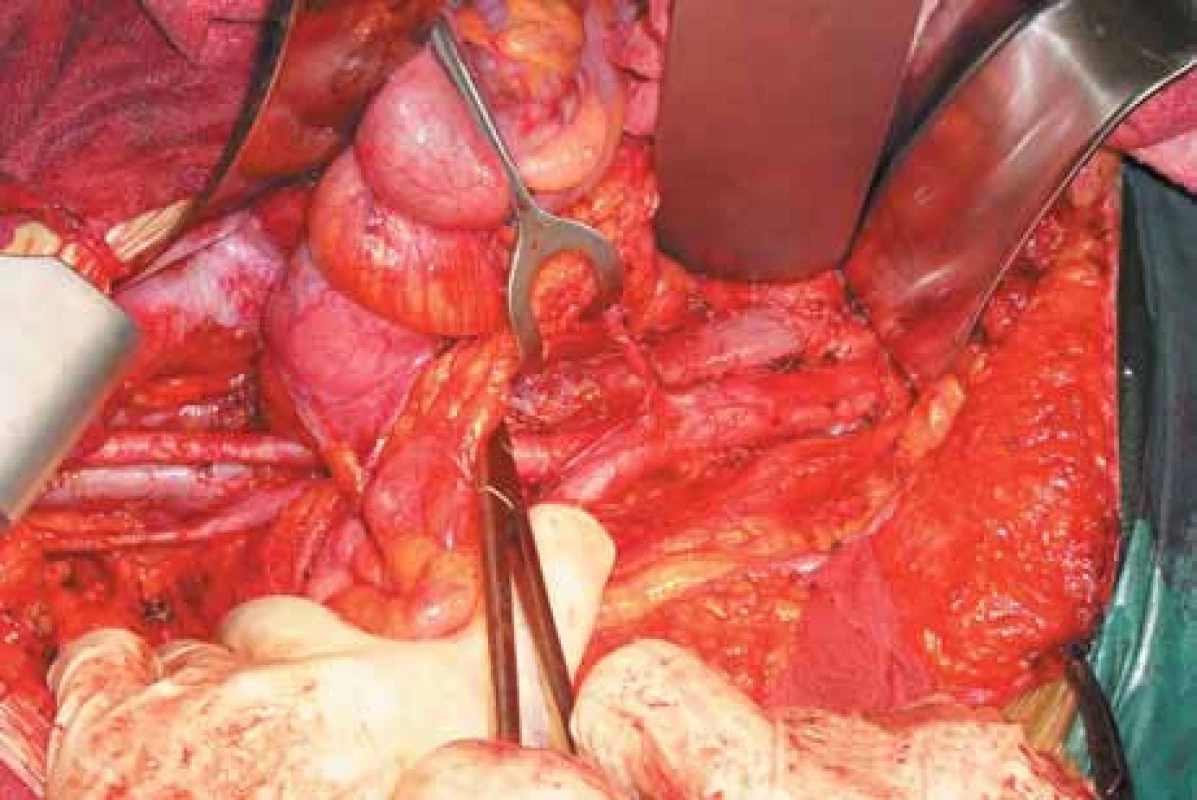
Výsledky
Počet lymfatických uzlin dle histologického vyšetření z pelvické lymfadenektomie byl v rozmezí od 10 do 44 uzlin (medián 23 uzlin) a z paraortální lymfadenektomie bylo získáno od 7 do 33 uzlin (medián 14,5 uzlin). V našem souboru jsme zaznamenali 7,69 % pacientek se současným pánevním i paraaortálním nádorovým uzlinovým postižením, pouze pánevní uzlinové postižení mělo také 7,69 % pacientek a jen paraortální uzlinové postižení se vyskytlo u 14,29 % pacientek. Délka operace se pohybovala v rozmezí 190-255 min (medián 205 min).
Přestože u všech našich pacientek byla vždy před zákrokem objednána erymasa, peroperačně ani pooperačně nebyla u žádné pacientky podána. Hodnota hemoglobinu 4 hodiny po operaci byla v souboru v rozmezí 84 g/l-146 g/l (medián 114,5 g/l). Parenterálně jsme doplňovali tekutiny a výživu ve formě krystaloidů a glukózy v rozmezí 1-4 dnů (medián 3 dny). Nazogastrickou sondu jsme zavedli u prvních 6 pacientek na dobu 2 pooperačních dnů. U dalších 10 pacientek již nazogastrická sonda zavedena nebyla. Perorální příjem v omezeném množství do 300 ml tekutin byl realizován u všech pacientek již v den operace. Standardně jsme aplikovali prokinetika k podpoře střevní peristaltiky od 1. do 4. pooperačního dne (medián 3 dny). V souboru byla slyšitelná peristaltika v rozmezí 1.-3. pooperačního dne (medián 2. pooperační den). Tomu napomáhá také včasná mobilizace pacientek od 1. pooperačního dne. Všechny operované měly aplikovány LMWH do plné mobilizace a bandáže DKK. Forsírovanou diurézu pomocí aplikace furosemidu v pooperačním období jsme použili u 1 pacientky. Permanentní močový katétr byl zaveden v rozmezí od 1.do 9.dne (medián 4 dny). ATB byla paušálně aplikována ve formě cefalosporinů I. generace do období 3 dnů afebrilie (medián podávání ATB 6 dnů). Realizujeme otevřený způsob ošetření laparotomie - od 1. pooperačního dne bez krytí. V našem souboru jsme zaznamenali jen 1krát komplikaci ve formě dehiscence laparotomie, a to u pacientky s BMI 41,45. Speciální komplikací tohoto operačního výkonu je tvorba lymfocyst. Kudela [5] udává při izolované pánevní lymfadenektomii 15% výskyt lymfocyst. V našem sledovaném souboru jsme tuto komplikaci nezaznamenali. Paušálně zavádíme 2 drény, 1 paraaortální retroperitoneálně, a druhý pelvický. Délka zavedení drénů byla v souboru v rozmezí od 3 do 4 dnů (medián 4 dny). Délka pobytu na pooperačním oddělení JIP byla v souboru v rozmezí od 2 do 5 dnů (medián 4 dny) a celková délka hospitalizace byla v rozmezí od 8 do 44 dnů (medián 8 dnů). Ze závažných komplikací jsme zaznamenali 1krát lézi ureteru a 1krát lézi močového měchýře. Hodnota BMI v našem souboru byla v rozmezí od 18,96 do 41,45 (medián 26,80).
Závěr
Námi realizovaný operační postup, peroperační a pooperační opatření i přes extenzivní operační rozsah zákroku a délku operace nevedly k výraznému vzestupu pooperačních komplikací. Nutno však podotknout, že uváděný soubor není zřejmě statisticky významný a teprve další období přinesou další podklady k přesnějšímu statistickému zhodnocení výsledků ve sledovaném souboru souboru.
MUDr. Marek Ožana,
MUDr. Michal Mihula,
MUDr. Miloš Zubík
Gynekologicko-porodnické oddělení MN Ostrava
Sources
1. Ayhan A, Celik H, Coscun F et al. Restaging in gynaecological cancers. Eur J Gynaecol Oncol 2005; 26(1): 25-30.
2. Di Re F, Paladini R, Fontanelou R et al. Surgical staging for epithelial ovarian tumor sof low malignant potential. Int Gynec Cancer1994; 4 : 310-314.
3. Freitag P, Živný J, Kužel D et al. Paraaortální lymfadenektomie v léčbě karcinomu ovaria. Čes Gynek 2001; 1 : 29-31.
4. Hoskins WJ, Perez CA, Young RC. Principles and Practice of Gynecological Oncology. Philadelphia: Lippincott Williams & Wilkins 2000 : 245-253.
5. Kudela M, Lubušký D, Jabůrek L et al. Lymfokély - komplikace po radikálních operacích dělohy. Gynekolog 1994; 3 : 168-169.
6. Leake JF, Ader JS, Woodruff JD. Retroperitoneal lymphatic involvement with epithelial ovaria tumors of low malignant potential. Gynec Oncol 1991; 42 : 124-130.
7. Scarabell C, Gallo A, Visentin MC et al. Systematic pelvic and paraaortic lymphadenectomy in advanced ovaria cancer patiens with no residua peritoneal disease. Int J Gynecol Cancer 1997; 87 : 144-149.
8. Yazigi R, Sanddstad J, Munoy AK. Primari staging in ovarian tumors of low malignant potential. Gynec Oncol 1998; 31 : 402-408.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inPractical Gynecology

2005 Issue 5-
All articles in this issue
- Podpůrná hormonální léčba v programu asistované reprodukce
- Přednosti neinvazivní diagnostiky fetální anémie – kazuistika
- Perinatální infekce GBS
- Současný pohled na vztah hormonální substituční terapie a očních nemocí
- Předoperační lokalizace nehmatných mamárních lézí
- Paraaortální a pelvická lymfadenektomie - několik poznámek k operačním a pooperačním opatřením, komplikacím
- Radioterapie v léčbě zhoubných nádorů vulvy
- Practical Gynecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Paraaortální a pelvická lymfadenektomie - několik poznámek k operačním a pooperačním opatřením, komplikacím
- Přednosti neinvazivní diagnostiky fetální anémie – kazuistika
- Perinatální infekce GBS
- Předoperační lokalizace nehmatných mamárních lézí
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

