-
Medical journals
- Career
Nové testy pro screening syfilis u dárců krve
Authors: M. Bohoněk 1; H. Zákoucká 2; L. Landová 1; E. Sládková 1
Authors‘ workplace: Ústřední vojenská nemocnice – Vojenská fakultní nemocnice Praha 1; Státní zdravotní ústav Praha 2
Published in: Transfuze Hematol. dnes,21, 2015, No. 3, p. 143-151.
Category: Comprehensive Reports, Original Papers, Case Reports
Overview
Syfilis, jejímž původcem je spirocheta Treponema pallidum, je chronické onemocnění přenášené prakticky výhradně sexuálním kontaktem, výjimečně též i transplacentárně nebo krevní transfuzí. Ojedinělost přenosu tímto způsobem je dána zejména nízkou rezistencí patogenních treponemat na pobyt v zevním prostředí, proto jsou rizikové zejména čerstvé a nezmražené přípravky. V ČR je podle vyhlášky MZ ČR č. 306/2012 Sb. stanovena povinnost vyšetření syfilis jak treponemovým, tak i netreponemovým testem, pro screening dárců krve plně postačuje provedení treponemového testu (vyhláška MZ ČR č. 143/2008 Sb.). Pro tyto účely se nejčastěji využívá TPHA testů, které mohou být manuální nebo poloautomatizované, a v poslední době i imunochemické CMIA a ELISA testy, které jsou plně automatizované. V uplynulých dvou letech byly na trh rovněž uvedeny dva zcela nové treponemové testy pro screeningové vyšetření syfilis: TPHA ScreenTM firmy Immucor a Elecsys®Syphilis firmy Roche. Cílem této práce je popis a zhodnocení těchto testů na základě provedených validačních studií se vzorky dárců krve a souborem pozitivních vzorků z Národní referenční laboratoře (NRL) pro syfilis SZÚ Praha. Na základě výsledků je možné konstatovat, že oba tyto testy jsou vhodné pro rutinní vyšetření dárců krve a krevních složek.
Klíčová slova:
syfilis, Treponema pallidum, krevní transfuze, laboratorní diagnostika syfilisÚVOD
Syfilis je chronické onemocnění přenášené prakticky výhradně sexuálním kontaktem (cca 90 %), výjimečně též i transplacentárně nebo krevní transfuzí. Vstupní branou infekce je jakákoliv oblast kůže a sliznic, nejčastěji však genitální, rektální a ústní sliznice. Inkubační doba silně kolísá mezi 9–90 dny, nejčastěji je 21 dní. Původcem onemocnění je spirocheta Treponema pallidum. Onemocnění se projevuje pestrou škálou příznaků a z hlediska infekčnosti je dělena na dvě stadia – časné (infekční) a pozdní (neinfekční).
Klinicky se u syfilis rozlišují čtyři stadia: primární stadium s kožní lézí 3–90 dní po nákaze, sekundární stadium s nejrůznějšími projevy od kožních až po orgánové 4–10 týdnů po primárním infektu, asymptomatické latentní stadium a terciární stadium, které se objevuje 3–15 let po počáteční infekci ve třech různých formách (gumatózní syfilis, pozdní neurosyfilis a kardiovaskulární syfilis), přičemž v tomto stadiu již postižené osoby nejsou infekční. Zvláštní formou je kongenitální syfilis, kdy k nákaze plodu může dojít během těhotenství nebo při porodu [1].
Ojedinělost přenosu krevní transfuzí je dána zejména nízkou rezistencí patogenních treponemat na pobyt v zevním prostředí. Skladování ≥ 72 hod. při teplotě 20 °C vede k nevratnému poškození viability bakterie a její infekčnosti, při chladničkové teplotě treponema hyne během 4 hodin, mráz treponemata hubí okamžitě (s výjimkou laboratorního uchovávání vzorků viabilních treponemat při velmi nízkých teplotách (-80 °C a méně při současném použití kryoprotektivních látek). Rizikové jsou proto z tohoto pohledu zejména krátkodobě skladované přípravky. Dalším faktorem ovlivňujícím přenos infekce krví je zpravidla krátká bakteriémie po nákaze, kdy treponemata mohou být přítomna v krevním řečišti zejména v průběhu akutní fáze onemocnění, resp. již v časném primárním stadiu – obrázek 1.
Image 1. Sérologický obraz syfilis 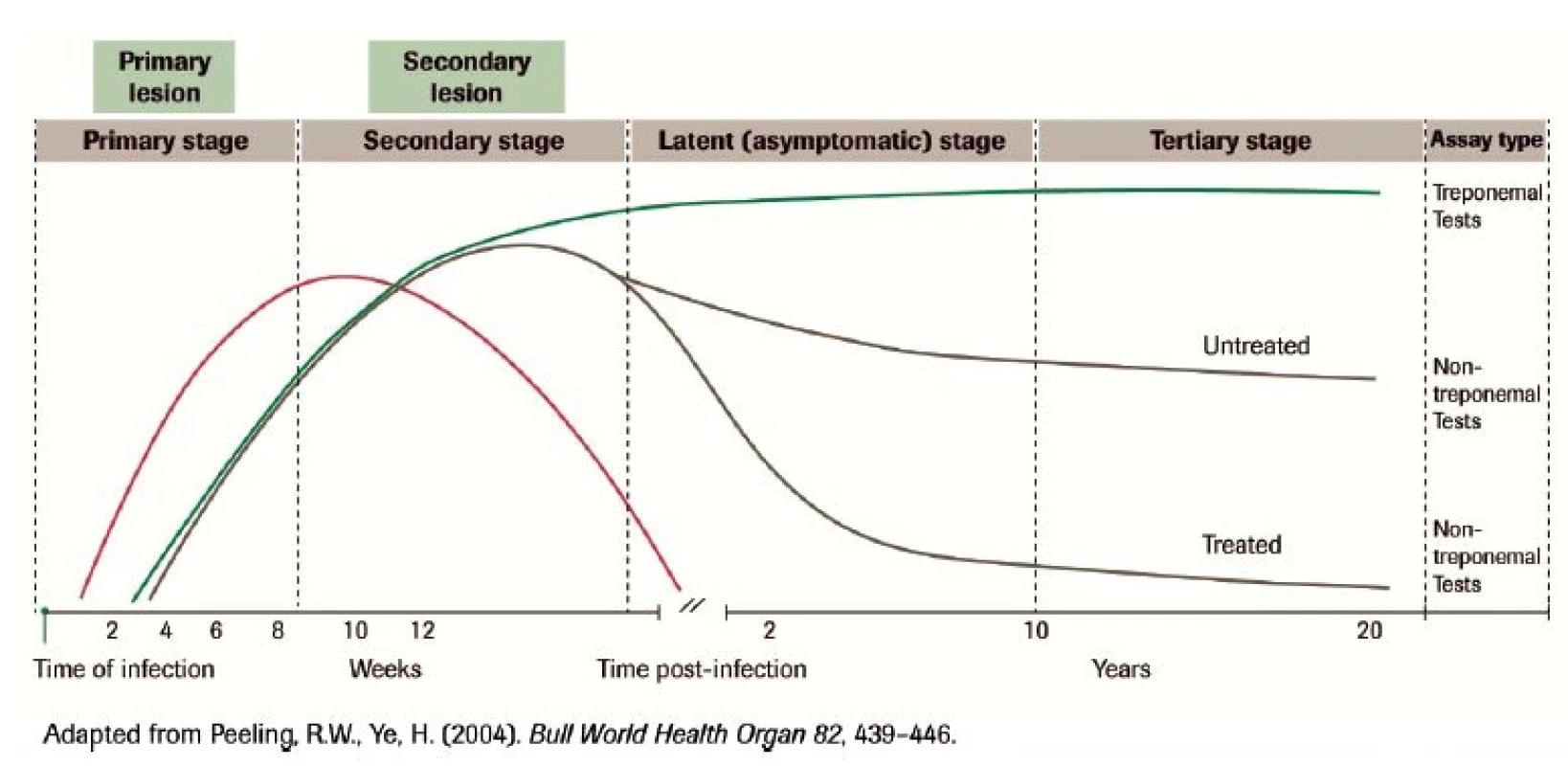
Upraveno z Peeling R.W., Ye H.: Bull World Health Organ. 2004: 82; V časných dobách transfuziologie, kdy se transfuze prováděly přímým převodem z dárce do příjemce, byla ale syfilis podstatně větší hrozbou z hlediska rizika přenosu touto cestou. Stala se tak první krví přenosnou infekcí, jejíž zjištění bylo důvodem k vyloučení dárce [2].
Laboratorní diagnostika syfilis se podle zacílení testů rozlišuje na přímou a nepřímou.
Přímá diagnostika syfilis
Základním vyšetřením při podezření na specifickou lézi na kůži nebo sliznici bylo vyšetření v zástinovém mikroskopu, které umožňuje mj. vyšetřit serózní exsudát z lézí, likvor, amniovou tekutinu apod. Metoda histopatologického vyšetření (impregnace stříbrem) je zdlouhavá a zatížená řadou artefaktů. Dnes je proto přímá diagnostika postavena především na vyšetření PCR [3, 4].
Nepřímá diagnostika syfilis
Je založena na humorální imunitní odpovědi na specifické antigeny nebo na detekci nespecifických, tzv. netreponemových protilátek.
Netreponemové testy
Tyto testy jsou založeny na detekci tzv. netrepomenových protilátek, které jsou namířeny proti antigenu kardiolipinu, který není pro treponemata specifický. Jedná se o fosfolipid, který je součástí buněčných membrán savčích buněk. Příkladem takové diagnostické reakce, jejímž výsledkem je flokulace, je VDRL (Venereal Disease Research Laboratory test, RRR (rychlá reaginová reakce) nebo RPR (rapid plasma reagin) [5].
Treponemové testy
Treponemová diagnostika detekuje specifické protilátky, které lze zachytit nejdříve ve druhém týdnu infekce ve formě IgM protilátek, následovaných během 2 týdnů protilátkami IgG. Tyto protilátky jsou namířeny proti specifickým treponemovým lipoproteinům a jejich detekce je základem různých, tzv. treponemových testů.
Základním, velmi jednoduchým a současně vysoce citlivým screeningovým testem je TPHA (Treponema pallidum hemagglutination), nebo její varianta TPPA (Treponema pallidum particle agglutination assay). Metodami ELISA (enzyme-linked immuno sorbent assay) mohou být stanovovány protilátky třídy IgG, IgM, případně celkové protilátky [6, 7].
V posledních letech jsou k dispozici imunochemické metody založené na principu chemiluminiscence (CMIA: chemiluminescent microparticle immunoassay), respektive elektrochemiluminiscence (ECLIA: electro-chemiluminescence immunoassay) [8, 9]. Imunofluorescenční reakce FTA-ABS (fluorescent treponemal antibody – absorption test), i když je zatížena jiným spektrem příčin nespecifické reakce než TPHA, se tradičně využívá jako konfirmační reakce. Může však být pozitivní již v době, kdy je TPHA ještě negativní. Odlišení zkříženě reagujících protilátek umožňuje westernblot, který detekuje protilátkovou odpověď IgM nebo IgG vůči jednotlivým vysoce specifickým antigenům odděleně. Výhodou westernblotu je jeho vysoká citlivost, umožňující zachytit nízké hladiny protilátek, např. v samém počátku infekce a zároveň vysoká specificita. Uplatňuje se jako konfirmační reakce a v diagnostice kongenitální syfilis (IgM protilátky) [10, 11].
V České republice jsou pro účely vyhledávacího testování nejčastěji zavedeny testy TPHA, prováděné ručně nebo poloautomatizovaným způsobem, plně automatické chemiluminiscenční testy a dále metody ELISA, umožňující podle použité technologie částečnou nebo plnou automatizaci při zpracování vzorku. Novými testy pro screeningové vyšetření syfilis jsou pak TPHA ScreenTM f. Immucor a Elecsys®Syphilis f. Roche. Cílem práce je popis a zhodnocení těchto testů.
SOUBORY A METODIKY
1. TPHA ScreenTM (Immucor Inc., Norcross, GA, USA)
Test je určen pro kvalitativní vyšetření IgG a IgM protilátek proti Treponema pallidum u dárců krve ze vzorků séra nebo EDTA plazmy nepřímou pasivní hemaglutinací za použití automatizovaných imunohematologických analyzátorů Galileo nebo GalileoNEO (Immucor, Inc., Norcross, GA, USA).
Nepřímá pasivní hemaglutinace je sérologická reakce, při které dochází k reakci mezi specifickými antigeny uměle navázanými na povrch erytrocytů a protilátkami proti těmto antigenům. Antigeny se na nosič – erytrocyty – navážou chemicky nebo prostou adsorpcí. Takto upravené krvinky se nazývají „senzibilizované“. Protilátka přítomná v séru nebo plazmě vyšetřovaného vzorku se pak naváže na tyto erytrocyty, způsobí jejich spojení do shluků (aglutinaci) a při následné sedimentaci jejich zachycení na stěnách jamky. Jde o velmi citlivou metodu, která umožňuje i detekci protilátek ve velmi malém množství (pg). U testu TPHA ScreenTM se k detekci protilátek používají kuřecí erytrocyty s navázaným antigenem Treponema pallidum, vlastní reakce probíhá na mikrodestičkách v jamkách tvaru V, po přidání diluentu a vyšetřovaného séra nebo plazmy s následnou 60minutovou inkubací. Krvinky s nenavázanou protilátkou sedimentují na dno V jamky a negativní výsledek je prezentován ve formě zřetelného terčíku. V případě pozitivního výsledku jsou shluky krvinek s navázanými protilátkami vzájemně zachycené a rozprostřené na stěnách jamky – obrázek 2.
Image 2. Znázornění negativního a pozitivního výsledku testu TPHA Screen<sup>TM</sup> 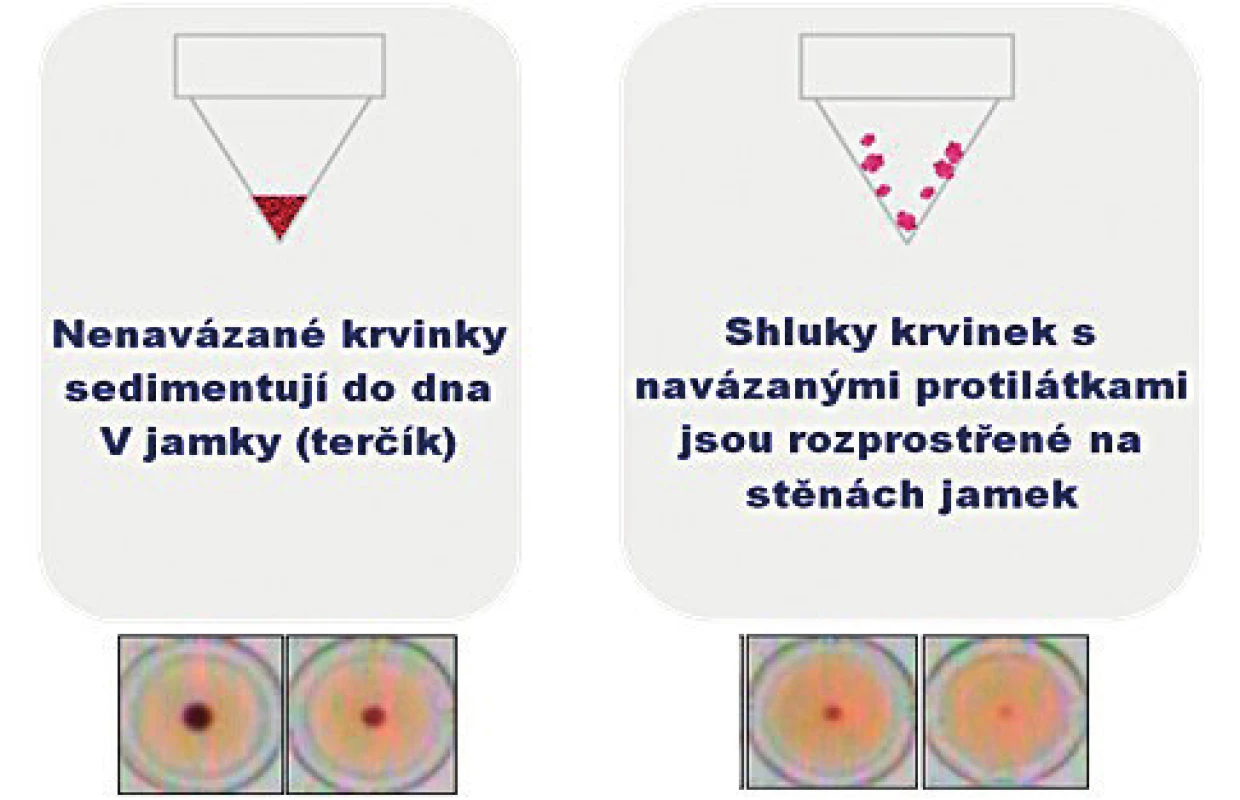
Za účelem validace a zhodnocení testu TPHA ScreenTM bylo v březnu 2013 na automatickém analyzátoru Galileo vyšetřeno 100 vzorků dárců krve, pro současné ověření případného vlivu typu vzorku byly testovány vzorky jak séra, tak i EDTA plazmy). Vzorky byly testovány dvakrát, ve dvou po sobě jdoucích dnech (D0/D1). V D0 byly vzorky séra i plazmy dárců krve současně testovány metodou Abbott Architect Syphilis TP na analyzátoru Abbott Architect i2000 (Abbott Laboratories, Abbott Park, IL, USA). Dále bylo pomocí TPHA ScreenTM vyšetřeno 124 reaktivních vzorků séra (100 vzorků pacientů s prokázanou infekcí syfilis a 24 vzorků pacientů s vyloučenou infekcí, ale reagujících pozitivně s některými treponemovými testy), které byly získány z Národní referenční laboratoře pro syfilis SZÚ v Praze. Pozitivita, respektive falešná pozitivita těchto vzorků byla deklarována panelem konfirmačních testů SZÚ: VDRL (mikroskopicky odečítaná metoda Immutrep, Omega Diagnostics Ltd) [12], TP-PA (Serodia TP-PA, FujiRebio Inc.) [13], TPHA (TPHA Immutrep, Omega Diagnostics Ltd.) [14], FTA-ABS, IgM SPHA (vlastní metody NRL pro syfilis SZÚ).
Pro srovnávání všech sledovaných primárních i sekundárních veličin mezi soubory i uvnitř souborů byly použity nepárové t-testy (Mann-Whitney U-test a Kolmogorov-Smirnov), s p < 0,05 při dvoustranném intervalu spolehlivosti. K porovnání a sledování distribuce dat byl využit Shapiro-Wilkův test s QQ grafy. Výpočty a grafy byly vytvořeny statistickým softwarem Statistica 10 společnosti StatSoft (verze 10) určeným k biostatistickým výpočtům klinických studií.
Senzitivita a specificita testu, které uvádí výrobce [15],jsou uvedeny v tabulce 1.
Table 1. Deklarovaná senzitivita a specificita testu TPHA Screen<sup>TM</sup> 
2. Elecsys®Syphilis (Roche Diagnostics GmbH, Manheim, SRN)
Jedná se o test určený pro kvalitativní vyšetření protilátek proti Treponema pallidum v krevním séru nebo plazmě dárců krve a jejích složek. Principem metody je jednokroková sendvičová analýza s dvojím antigenem (DAGS) a následnou detekcí fluorescence vyvolané elektrochemiluminiscenční reakcí pomocí fotonásobiče (ECLIA), která detekuje IgG a IgM protilátky proti treponemovým antigenům TpN15, TpN17 a TpN47 – obrázek 3.
Image 3. Princip testu Elecsys<sup>®</sup>Syphilis (Roche, 2014) 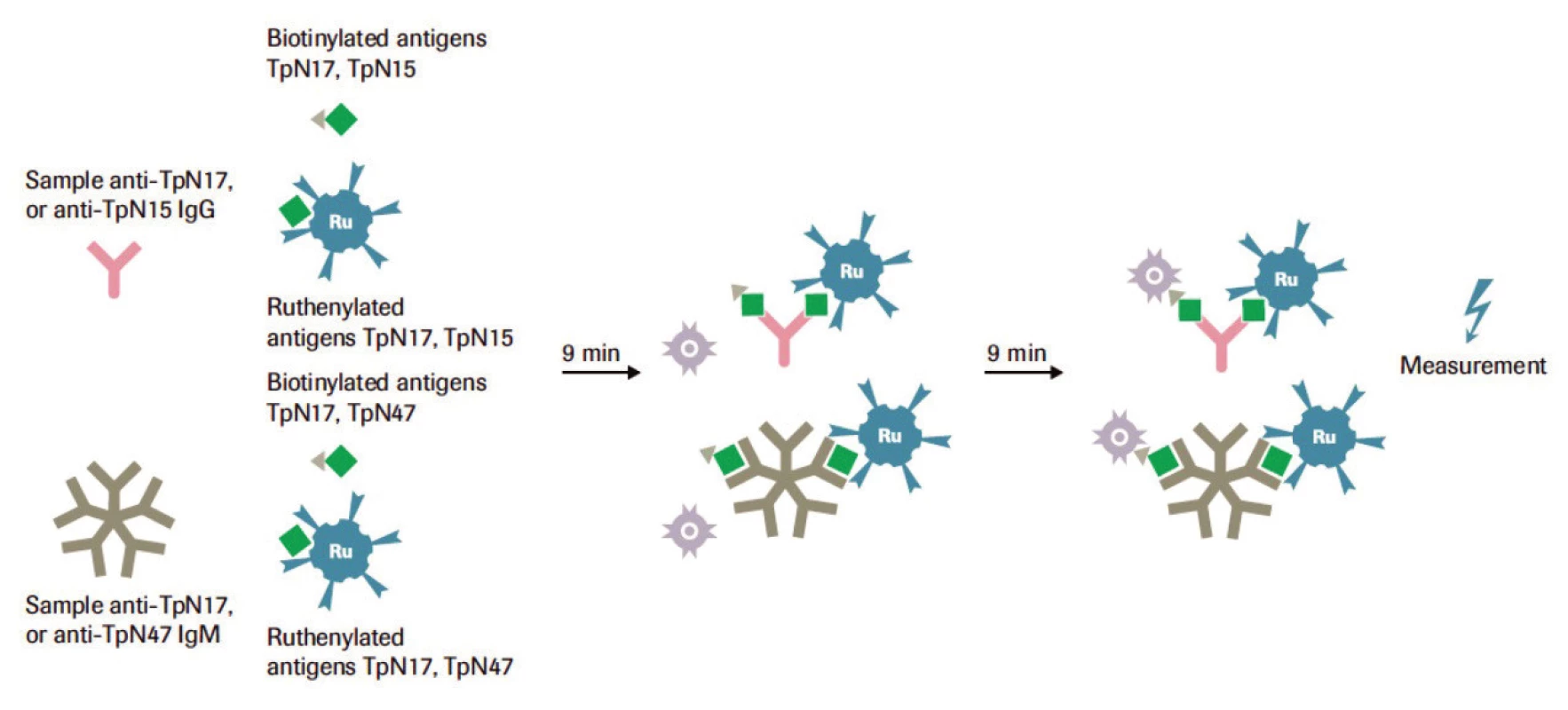
Tento test je určen pro použití na imunochemických analyzátorech Roche řady Elecsys 2010, MODULAR ANALYTICS E170 a cobas e.
Za účelem validace a zhodnocení testu bylo testem Elecsys®Syphilis na analyzátoru cobas®6000 (Roche Diagnostics GmhB, Manheim, SRN) v červnu 2014 vyšetřeno 200 vzorků dárců krve (sérum). Vzorky byly testovány dvakrát, ve dvou po sobě jdoucích dnech (D0/D1). Současně byly tyto vzorky vyšetřeny testem TPHA ScreenTM na automatickém analyzátoru Galileo a testem Abbott Architect Syphilis TP na analyzátoru Abbott Architekt i2000.
Dále bylo pomocí testu Elecsys®Syphilis na analyzátoru cobas®6000 a též srovnávacími metodami (test TPHA ScreenTM na automatickém analyzátoru Immucor Galileo a test Abbott Architect Syphilis TP na analyzátoru Abbott Architekt i2000) ve dvou následujících dnech vyšetřeno 81 reaktivních vzorků séra z Národní referenční laboratoře pro syfilis SZÚ v Praze, z toho 61 vzorků pozitivních a 20 vzorků s neprokázanou infekcí. Pozitivita, respektive falešná pozitivita těchto vzorků byla deklarována panelem konfirmačních testů SZÚ: VDRL (mikroskopicky odečítaná metoda Immutrep, Omega Diagnostics Ltd) (12), TP-PA (Serodia TP-PA, FujiRebio Inc.) [13], TPHA (TPHA Immutrep, Omega Diagnostics Ltd.) (14), FTA-ABS (vlastní metoda), IgM SPHA (vlastní metoda).
Pro srovnávání všech sledovaných primárních i sekundárních veličin mezi skupinami i uvnitř skupin byly použity nepárové t-testy (Mann-Whitney U-test a Kolmogorov-Smirnov), s p < 0,05 při dvoustranném intervalu spolehlivosti. K porovnání a sledování distribuce dat byl využit Shapiro-Wilkův test s QQ grafy. Výpočty a grafy byly vytvořeny statistických softwarem Statistica 10 společnosti StatSoft (verze 10) určený k biostatistickým výpočtům klinických studií.
Senzitivita a specificita testu, které uvádí výrobce [16], jsou uvedeny v tabulce 2.
Table 2. Senzitivita a specificita testu Elecsys<sup>®</sup>Syphilis 
VÝSLEDKY
1. TPHA ScreenTM
Výsledky testovaného souboru vzorků dárců krve metodou TPHA ScreenTM měly ve 100 % shodný interpretovaný výsledek jako výsledky testu Abbott Architect Syphilis TP. Výsledky vzorků plazmy vykazovaly mírně vyšší aglutinační hodnotu než výsledky vzorků séra, ale bez ovlivnění interpretace výsledku – tabulka 3.
Table 3. Srovnání výsledků testování vzorků dárců krve pomocí testu Syphilis TP Abbott Architect a TPHA ScreenTM 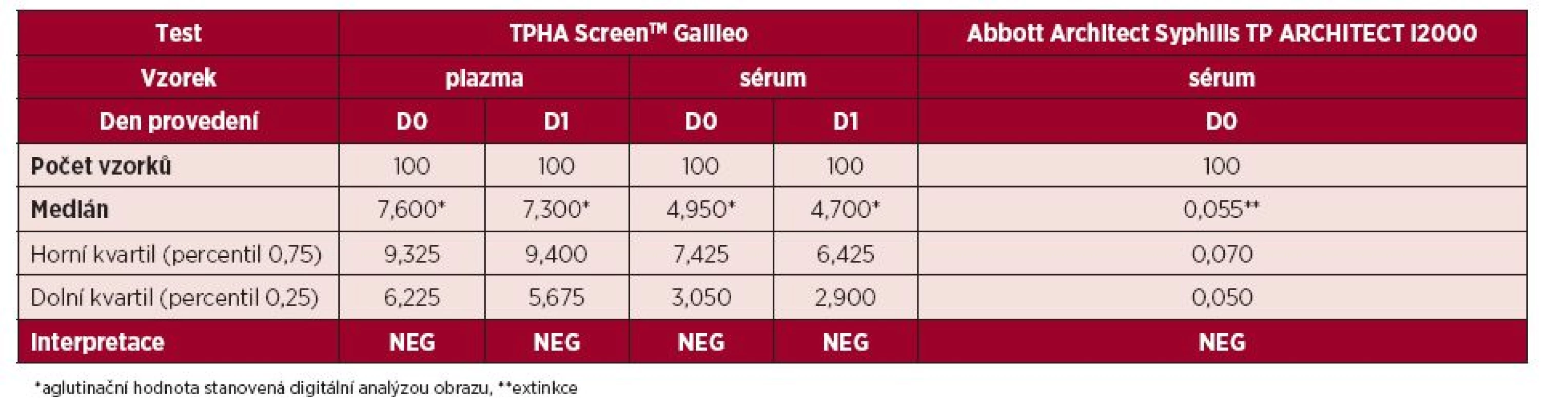
*aglutinační hodnota stanovená digitální analýzou obrazu, **extinkce V souboru 100 vzorků pacientů s detekovanou infekcí syfilis v akutní nebo léčené formě byla prokázána shoda výsledků vyšetření metodou TPHA ScreenTM a výsledků z NRL pro syfilis SZÚ u 97 z nich. U třech vzorků s diskrepantním výsledkem, tj. TPHA ScreenTM negativních, se ale ani v jednom případě nejednalo o aktivní syfilis (jednalo se o dva případy pacientů s přeléčenou infekcí v minulosti na hranici detekčního minima testů a jeden případ transplacentárně přenesených protilátek u 6měsíčního dítěte s fyziologickým poklesem mateřských protilátek). Tyto vzorky proto byly při opakovaném vyšetření v NRL SZÚ testem TPHA, tedy srovnatelnou metodikou, již nereaktivní.
V druhém souboru 24 pacientů s vyloučenou infekcí syfilis, kde byla ale prokázána nespecifická reaktivita v některých TP testech, byly pouze 3 vzorky potvrzeny jako reaktivní ve shodě s nespecifickou reaktivitou v TPHA testu provedeném v NRL SZÚ, ostatní vzorky vyšetřené na analyzátoru Galileo metodou TPHA ScreenTM byly nereaktivní, přičemž tyto vzorky byly nespecificky reaktivní v NRL SZÚ jinou metodou než TPHA. Celkový přehled vyšetřených reaktivních vzorků z NRL pro syfilis je uveden na obrázku 4.
Image 4. Srovnání klinické senzibility testu TPHA Screen<sup>TM</sup> vyšetřením reaktivních vzorků z NRL pro syfilis SZÚ Praha 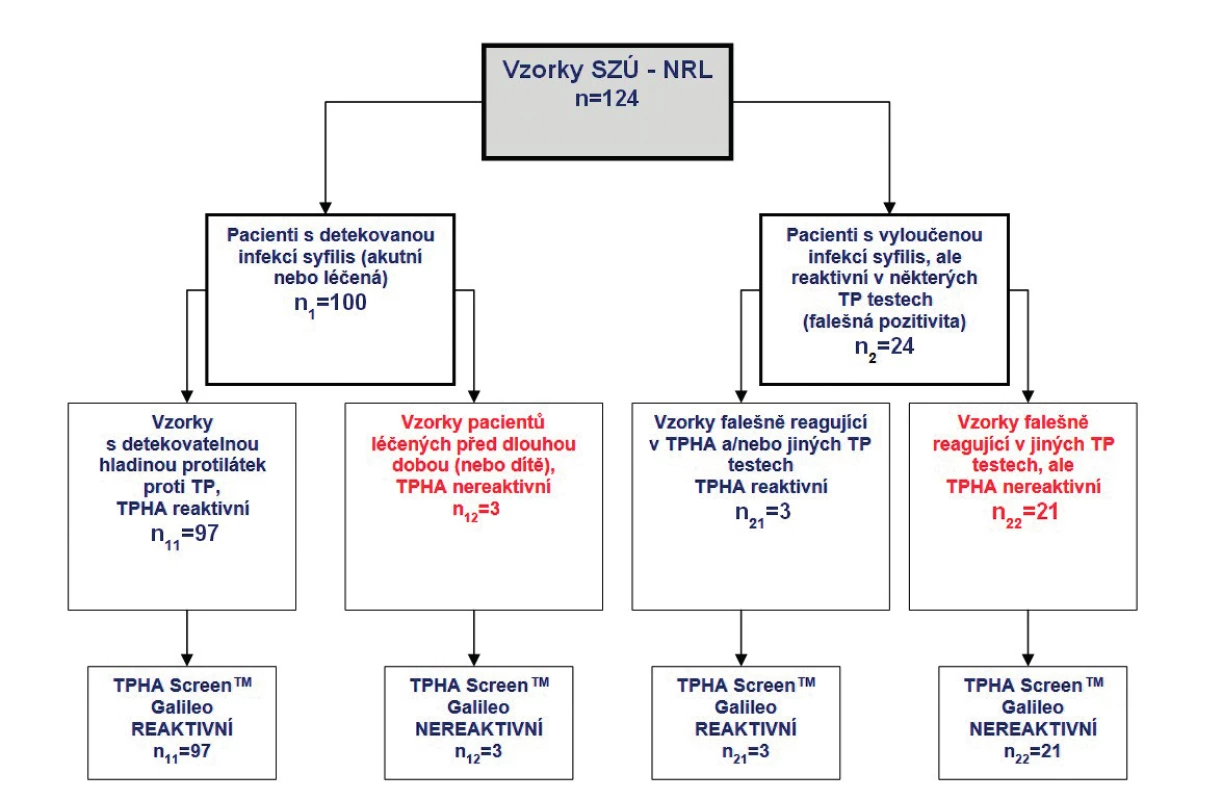
2. Elecsys®Syphilis
Výsledky u 200 vzorků dárců krve změřené metodou Elecsys®Syphilis na analyzátoru cobas®6000 byly interpretovány shodně jako výsledky naměřené na analyzátoru Galileo metodou TPHA ScreenTM a analyzátoru Architect i2000 metodou Abbott Architect Syphilis TP – tabulka 4. Vzorky změřené metodou Elecsys®Syphilis měly nejmenší rozdíly v kvantitativní interpretaci výsledků mezi D0/D1 – obr. 5–7.
Table 4. Srovnání výsledků testování vzorků dárců krve pomocí testu TPHA ScreenTM, Elecsys®Syphilis a Architect Syphilis TP 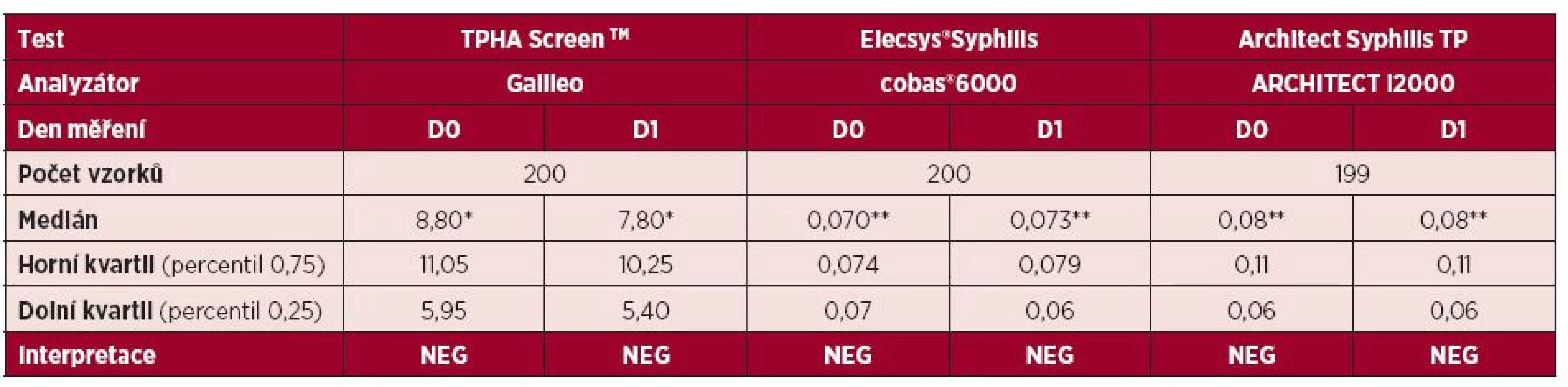
*aglutinační hodnota stanovená digitální analýzou obrazu, **extinkce Obr. 5–7 Srovnání měření negativních vzorků u jednotlivých analyzátorů 
Soubor 81 reaktivních vzorků sér pacientů z NRL pro syfilis byl při testování senzitivity testu rozdělen na dvě části: potvrzených pozitivních (61) a soubor falešně pozitivních výsledků (20). Všechny vzorky byly testovány několika testy (screeningovým testem v terénu, VDRL, TPPA, TPHA, FTA-ABS IgG, FTA-ABS IgM, 19S IgM SPHA, Abbott Architect Syphilis TP a Elecsys®Syphilis. Statistické výsledky vyšetření reaktivních vzorků z NRL pro syfilis vyšetřených testem Elecsys®Syphilis na analyzátoru cobas®6000 jsou uvedeny v souhrnné tabulce 5.
Table 5. Přehled výsledků pozitivních vzorků měřených analyzátorem cobas<sup>®</sup>6000 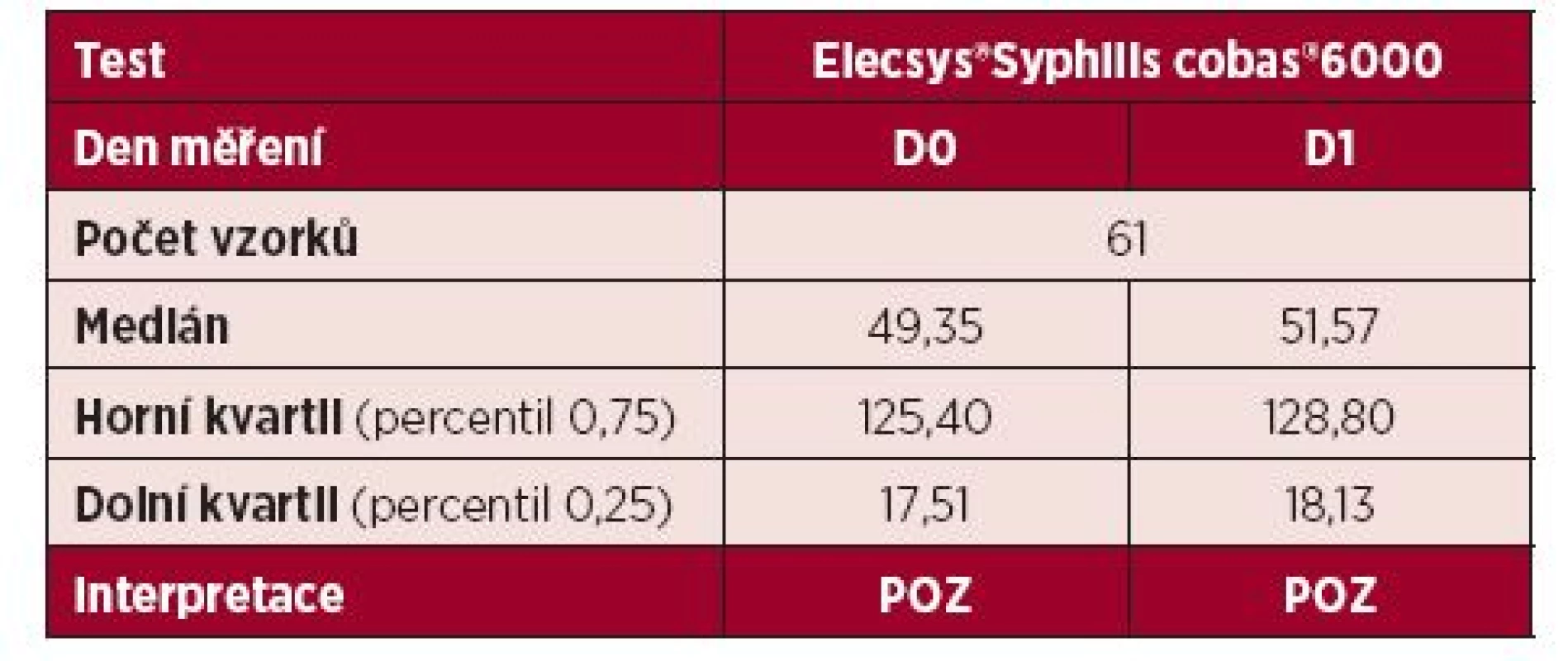
Pouze tímto testem byla potvrzena negativita všech falešně pozitivních výsledků. Při testování pomocí testu Abbott Architect Syphilis TP byly 4 vzorky z 20 reaktivní tj. opět falešně pozitivní, tři z nich i testem TPHA (1 netestován pro nedostatečné množství séra) – tabulka 6. Celkový přehled vyšetřených reaktivních vzorků z NRL pro syfilis je uveden na obrázku 8.
Table 6. Negativní testy po měření s testem Elecsys®Syphilis ve srovnání s ostatními výsledky testů 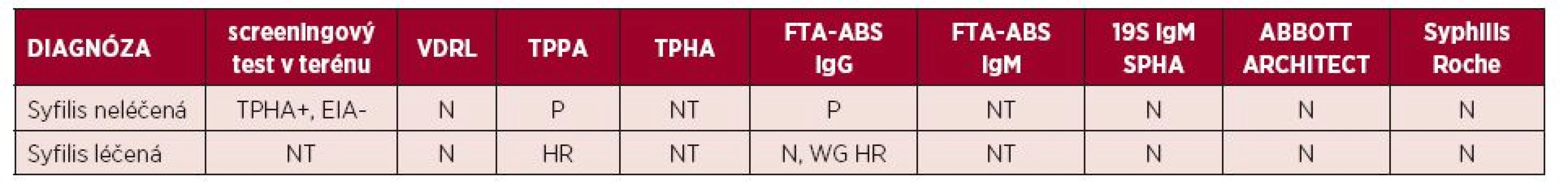
P-pozitivní (potvrzeno v NRL), NT – nedetekováno, N – negativní, HR – hraniční hodnota, WG – western blotting Image 5. Srovnání klinické senzibility testu Elecsys®Syphilis vyšetřením reaktivních vzorků z NRL pro syfilis SZÚ Praha 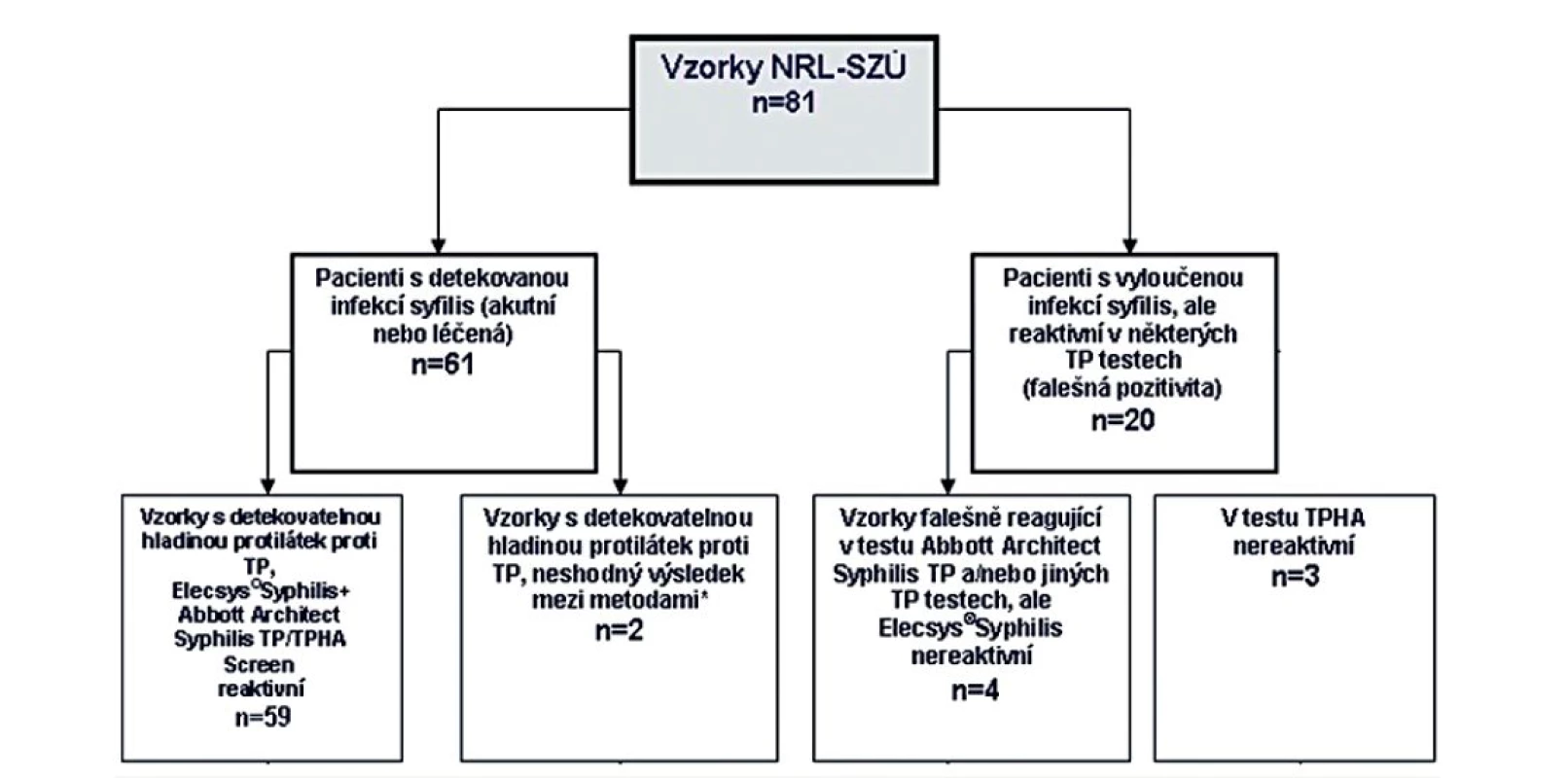
*Vysvětlení neshody: 1. vzorek byl pacienta s neléčenou syfilis: EIA/ VDRL/19S IgM SPHA/Abbott Architect Syphilis TP/Elecsys®Syphlis negativní, FTA-ABS IgG reaktivní, screeningový test v terénu TPHA reaktivní – viz tab. 6, 2. vzorek byl pacienta s léčenou syfilis: VDRL/TPPAFTA-ABS IgG 19S IgM SPHA/Elecsys®Syphlis reaktivní, Abbott Architect Syphilis TP nereaktivní – viz tab. 6. Oba vzorky byly na hranici detekčního minima testů. DISKUSE
Screening syfilis v transfuzní službě u dárců krve je v ČR na základě legislativní povinnosti rutinní praxí všech zařízení transfuzní služby a je i obvyklým screeningovým testem dárců krve v zahraničí. Ačkoli podle údajů zdravotních statistik ÚZIS výskyt syfilis v posledních letech v ČR celkově stagnuje (cca 700 případů/rok), jedná se nadále o reálné riziko, a nelze ani v budoucnu jeho screening podceňovat. Kromě toho je patrný nárůst výskytu syfilis ve skupině MSM mužů a spolu s ním nárůst koinfekce s HIV, což může mít i určitý diferenciálně-diagnostický význam [17].
Moderní transfuzní služba by již neměla používat manuální testy a pokud možno i veškeré poloautomatické metody, pokud je na trhu k dispozici dostatečný výběr plně automatizovatelných metod. Uvedení nových testů pro plně automatizovaný screening syfilis je z tohoto pohledu jednoznačným přínosem.
S ukončením platnosti licenčních omezení na screening anti-HCV u dárců krve, mohou se v transfuzní službě uplatnit screeningové testy pro dárce krve od podstatně širšího spektra výrobců, zejména imunochemických metod a analyzátorů, které v případě kompletní sady potřebné pro sérologický screening dárců krve (anti-HIV 1/2 + Agp24, HBsAg, anti-HCV a syfilis) mohou nabídnout plně automatizované a uživatelsky komfortní laboratorní vyšetření.
Hemaglutinační metody byly prováděny buď ryze manuálním způsobem, nebo poloautomatizovaně, kdy automaticky, robotem rozpipetované vzorky na mikrotitrační destičky, jsou ručně přenášeny a vkládány do readerů. Plně automatizovaný systém hemaglutinačního vyšetření syfilis na zařízení Olympus (respektivě nově Beckman-Coulter) PK 7200 byl pro malá česká ZTS příliš veliký a kapacitně nepoužitelný.
Popisovaná plně automatizovaná metoda TPHA ScreenTM pro zařízení Galileo nebo GalileoNEO je vhodná i pro menší a střední ZTS, zejména ta, která mají tyto automaty již instalované pro imunohematologická vyšetření. Metoda zatím není dostupná pro menší automaty Immucor Echo, pro které dosud nejsou k dispozici mikrojamkové stripy s „V“ tvarem mikrotitrační jamky. Pro úplnost je potřeba ještě dodat, že metoda TPHA ScreenTM je zatím CE certifikována pouze pro použití v transfuzní službě, je ale pouze otázkou času její CE certifikace i pro klinické použití pro vyšetření syfilis u pacientů. Metoda je klasickým TPHA testem využívajícím kuřecí krvinky s navázaným antigenem a má vlastnosti shodné s jinými TPHA testy, které jsou plně dostačující pro screening dárců krve.
Vzájemná statistická srovnání vzorků krve pomocí testů TPHA ScreenTM neprokázala žádný signifikantní rozdíl mezi měřením v jednotlivých dnech (D0/D1), ani mezi použitým testovaným odběrovým materiálem tj. sérem a plazmou (p < 0,05). Vzájemné srovnání, vzhledem k odlišným výstupním hodnotám (extinkce a aglutinační hodnota), nebylo prováděno mezi jednotlivými analyzátory a bylo využito grafického znázornění boxploty u negativních vzorků (viz obr. 5–7).
Vyšší medián pozitivních vzorků u druhého testovaného dne (metoda Elecsys®Syphilis Roche D1) je způsoben vyšší extinkcí vysoce pozitivního vzorku u opakovaně testovaného pacienta, který ale na interpretace pozitivních vzorků neměl žádný vliv a všechny výsledky byly shodně označeny jako pozitivní v obou testovaných dnech.
V případě hodnocení testu TPHA ScreenTM jsme testovali současně vzorky plazmy i vzorky séra, protože na automatickém analyzátoru Galileo je prováděn imunohematologický screening (stanovení krevní skupiny a nepravidelných protilátek proti erytrocytům), pro který jsou vzorky nabírány do zkumavek s K3EDTA.
V případě logisticky výhodnějšího použití jedné zkumavky pro imunohematologický a sérologický screening je výchozím materiálem plazma, v případě použití zkumavky pro ostatní sérologická vyšetření je výchozím materiálem sérum. Při hodnocení testu Elecsys®Syphilis jsme testovali pouze vzorky séra, které se v běžné praxi používají při vyšetřování infekčních markerů.
Srovnání jednotlivých sérologických metod u dárců krve provedli Sommese et al. 2014, když vyhodnotili výsledky testů u více než 17 tisíc vzorků dárců krve na analyzátoru Architect i2000 s konfirmací pomocí EIA [18]. Sami autoři konstatují, že vzhledem k vysoké specificitě použitých testů lze dosáhnout shodných výsledků s tím, že se dají ovlivnit pouze faktory do analýzy vstupující (preanalytika atd.) s tím, že testy by měly být doplněny o výsledky PCR (tam, kde je to vhodné). Další retrospektivní studii komparace jednotlivých metod pro stanovení syfilis provedli Maragoni et al. 2009, kteří srovnávali procento reaktivity, senzitivitu a specificitu na základě výsledků získaných na analyzátoru Abbott Architect, Enzygnost Syphilis, WB, TPHA a RPR [19]. Prokázali téměř shodnou specificitu (99,2 %) i senzitivitu (98,5 %) u testů Enzygnost Syphilis a Syphilis TP a podobné stanovení reaktivity mezi TPHA a Syphilis TP (> 97 %). Výsledky našich validačních studií tyto závěry doplňují o srovnání mezi dvěma novými testy Elecsys®Syphilis a TPHA ScreenTM. Prezentované výsledky potvrzují vysokou specificitu i senzitivitu obou testů, a to ve shodě i s podstatně většími soubory vyšetření [15, 16].
ZÁVĚR
Oba hodnocené testy splňují požadavky na moderní, plně automatizované metody, s dostatečnou specificitou i senzitivitou.
Výsledky testu TPHA ScreenTM se plně shodují se současnými TPHA specifickými testy. Metoda je vhodná pro rutinní vyšetření dárců krve a krevních složek; test mj. přináší novou možnost automatizovaného screeningu dárců krve na protilátky proti Treponema pallidum v séru a plazmě.
Výsledky získané na základě testu Elecsys®Syphilis jsou plně srovnatelné s dosud používanými specifickými IgG a IgM testy určenými pro screening syfilis, a přináší nové možnosti pro automatizaci testování protilátek proti syfilis. Metoda pro stanovení protilátek syfilis Elecsys®Syphilis na analyzátoru cobas®6000 je vhodná pro rutinní vyšetření dárců krve a krevních složek.
Použité zkratky
CMIA – Chemiluminescent Microparticle Immuno-assay
ECLIA – Electro-Chemiluminescence Immunoassay
ELISA – Enzyme-Linked Immuno Sorbent Assay
FTA-ABS – Fluorescent Treponemal Antibody-Absorp-tion test
NRL – Národní referenční laboratoř
PCR – Polymerase Chain Reaction
RPR – Rapid Plasma Reagin
RRR – rychlá reaginová reakce
SZÚ – Státní zdravotní ústav
TPHA – Treponema Pallidum Hemagglutination Assay
TPPA – Treponema Pallidum Particle Agglutination Assay
VDRL – Venereal Disease Research Laboratory Test
Podíl autorů na rukopisu
MB – hlavní autor, zpracování textu rukopisu
HZ – provedení a vyhodnocení testů v NRL pro syfilis SZÚ, podíl na textu rukopisu
LL – statistické zpracování, vyhodnocení výsledků, podíl na textu rukopisu
ES – vlastní provedení validačních studií, sběr dat
Prohlášení autorů
Prohlašuji, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsem ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou firmou z oboru. Toto prohlášení se týká i všech spoluautorů.
Doručeno do redakce: 20. 10. 2014
Přijato po recenzi: 12. 6. 2015
pplk. MUDr. Miloš Bohoněk, Ph.D.
primář Oddělení hematologie, biochemie a krevní transfuze
Ústřední vojenská nemocnice – Vojenská fakultní nemocnice Praha
U Vojenské nemocnice 1200
169 02 Praha 6
e-mail: milos.bohonek@uvn.cz
Sources
1. Poláčková Z. Pohlavní choroby I. díl. Dermatologie pro praxi [online]. 2008;2 : 74–76.
2. McCluskie, et al. The Transmission of Syphilis by Blood Transfusion. British Med. Journal, 1939.
3. Centurion-Lara A, Castro C, Shaffer JM, van Voorhis WC, Marra CM, Lukehart SA. Detection of Treponema pallidum by a sensitive reverse transcriptase PCR. J Clin Microbiol, 1997; 35 : 1348–1352.
4. Servant A, Laperche S, Lallemand F, et al. Genetic diversity within human Erythroviruses: identification of three genotypes. J Virol, 2002; 76 : 9124–9134.
5. Harris A, Rosenberg AA, Riedel LM. A microflocculation test for syphilis using cardiolipin antigen: Preliminary report. J Vener Dis Inform, 1946;27 : 159 –172.
6. Pedersen NS, Orum O, Mouritsen S. Enzyme-linked immunosorbent assay for detection of antibodies to venereal disease research laboratory (VDRL) antigen in syphilis. J Clin Microbiol, 1987;25 : 1711–1716.
7. White TJ, Fuller SA. Visuwell Reagin, a nontreponemal enzyme-linked immunosorbent assay for the serodiagnosis of syphilis. J Clin Microbiol, 1989;27 : 2300–2304.
8. Larsen SA. Current status of laboratory tests for syphilis. In Rippey J, Nakamura R. (eds.) Diagnostic immunology technology assessment. American College of Pathologist, Skokie, Ill 1983;162–170.
9. Zhonghua S, Yan H, Lin ChL, Du Xue Za Zhi. Evaluation of specific antibodies of blood receiver sera to Treponema pallidum by chemiluminescence immunoassay. 2013;27(1):70–72.
10. Meyer MP, Eddy T, Baughn RE. Analysis of Western blotting (Immunoblotting) technique in diagnosis of congenital syphilis. J Clin Microbiol, 1994;32 : 629–633.
11. Hunter EF, McKinney RM, Maddison SE, Cruce DD. Double-staining procedure for the fluorescent treponemal antibody absorption (FTA--ABS) test. Br J Vener Dis, 1979;55 : 105–108.
12. Datasheet of method online link. Dostupné na www: http://www.omegadiagnostics.pl/templates/_editor/kcfinder/upload/images/omega/od051_1.pdf
13. Datasheet of method online link. Dostupné na www: http://www.transplantation.com/Portals/0/docs/Laboratory%20Inserts/TP-PA_KitInsert_101606%20Serodia.pdf
14. Datasheet of method online link. Dostupné na www: http://static.omegadiagnostics.com.s3.amazonaws.com/product-downloads/ifu/Immutrep_TPHA_CE_Globe_A5_V5_including_850T.pdf
15. Datasheet of method online link. Dostupné na www: http://www.fda.gov/downloads/BiologicsBloodVaccines/BloodBloodProducts/ApprovedProducts/SubstantiallyEquivalent510kDeviceInformation/UCM327234.pdf
16. Datasheet of method online link. Dostupné na www: https://pim-services.roche.com/eLD/%28S%28bg05u3ygg1dgu2m35ndikpip%29%29/cz/cs/Documents/GetDocument?documentId=2bfcc24d-25f5-e311-98a1-00215a9b0ba8&referrer=Dialog
17. Zdravotnická statistika ČR, Vydává Ústav zdravotnických informací a statistiky ČR, Praha 2, Palackého nám. 4. Dostupné na www: www.uzis.cz
18. Sommese L, Iannone C, Cacciatore F, De Iorio G and Napoli C. Comparison Between Screening and Confirmatory Serological Assays in Blood Donors in a Region of South Italy. J Clin Lab Anal, 2014; 28 : 198–203.
19. Marangoni A, Moroni A, Accardo S, Cevenini, R. Laboratory diagnosis of syphilis with automated immunoassays. J Clin Lab Anal, 2009; 23 : 1–6.
Labels
Haematology Internal medicine Clinical oncology
Article was published inTransfusion and Haematology Today

2015 Issue 3-
All articles in this issue
- Protinádorové účinky klinicky používaných chelátorů železa – přehled literatury a vlastní zkušenosti
- Získaná uniparentální disomie v buňkách kostní dřeně nemocných s myelodysplastickými syndromy a komplexním karyotypem
- Kazuistika (ne)chelatovaného polytransfundovaného pacienta s 5q minus syndromem
- Nové testy pro screening syfilis u dárců krve
- Transfusion and Haematology Today
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nové testy pro screening syfilis u dárců krve
- Protinádorové účinky klinicky používaných chelátorů železa – přehled literatury a vlastní zkušenosti
- Získaná uniparentální disomie v buňkách kostní dřeně nemocných s myelodysplastickými syndromy a komplexním karyotypem
- Kazuistika (ne)chelatovaného polytransfundovaného pacienta s 5q minus syndromem
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

