-
Medical journals
- Career
Nezapomínáme na možnost biologické terapie hypercholesterolemie pomocí PCSK9-inhibitorů?
Authors: Vladimír Soška 1,2; Ondřej Kyselák 1,3
Authors‘ workplace: Oddělení klinické biochemie, FN u sv. Anny v Brně 1; II. interní klinika, Lékařská fakulta MU, Brno 2; Katedra laboratorních metod, Lékařská fakulta MU, Brno 3
Published in: Vnitř Lék 2021; 67(3): 138-142
Category: Review Articles
Overview
U mnoha pacientů je obtížné dosahovat současné velmi nízké cílové hodnoty LDL-cholesterolu, doporučené k prevenci aterosklerotických kardiovaskulárních komplikací. Pokud nestačí terapie statiny, ev. statiny v kombinaci s ezetimibem, má být zváženo přidání PCSK9-inhibitorů. PCSK9-inhibitory snižují LDL-CH v průměru o 50–60 % a redukují riziko aterosklerotických kardiovaskulárních příhod. V současné době jsou vyhrazeny pro pacienty s manifestním aterosklerotickým kardiovaskulárním onemocněním a pro pacienty s familiární hypercholesterolemií, u kterých nelze ani intenzivní terapií statiny s ezetimibem dosáhnout cílových hodnot LDL-cholesterolu. U těchto pacientů mohou být PCSK9-inhibitory indikovány i v případě statinové intolerance.
Klíčová slova:
aterosklerotické kardiovaskulární onemocnění – familiární hypercholesterolemie – LDL-cholesterol – statiny – PCSK9-inhibitory
Úvod
Jedním z hlavních rizikových faktorů pro rozvoj aterosklerózy a následně i aterosklerotických kardiovaskulárních onemocnění (AS KVO) je zvýšená koncentrace cholesterolu, neseného v nízkodenzitních lipoproteinech (LDL, low density lipoproteins) (1, 2). Intervenční klinické studie jednoznačně prokázaly, že snížením koncentrace cholesterolu v LDL (LDL-CH) o 1 mmol/l dosáhneme zásadního zlepšení prognózy pacientů se snížením jejich rizika AS KVO o 20–25 % (3). Doporučené cílové hodnoty LDL-CH se postupně snižují v souvislosti s výsledky intervenčních studií s hypolipidemiky, především se statiny, ale také s novými hypolipidemiky ze skupiny inhibitorů PCSK9 (proprotein konvertáza subtilisin-kexin typ 9). Současné cílové hodnoty LDL-CH, uvedené v nejnovějších doporučeních pro management dyslipidemií a redukci kardiovaskulárního rizika, jsou uvedeny v Tab. 1; kategorizace pacientů dle jejich rizika je uvedena v Tab. 2 (4).
Table 1. Cílové hodnoty LDL-cholesterolu (4) 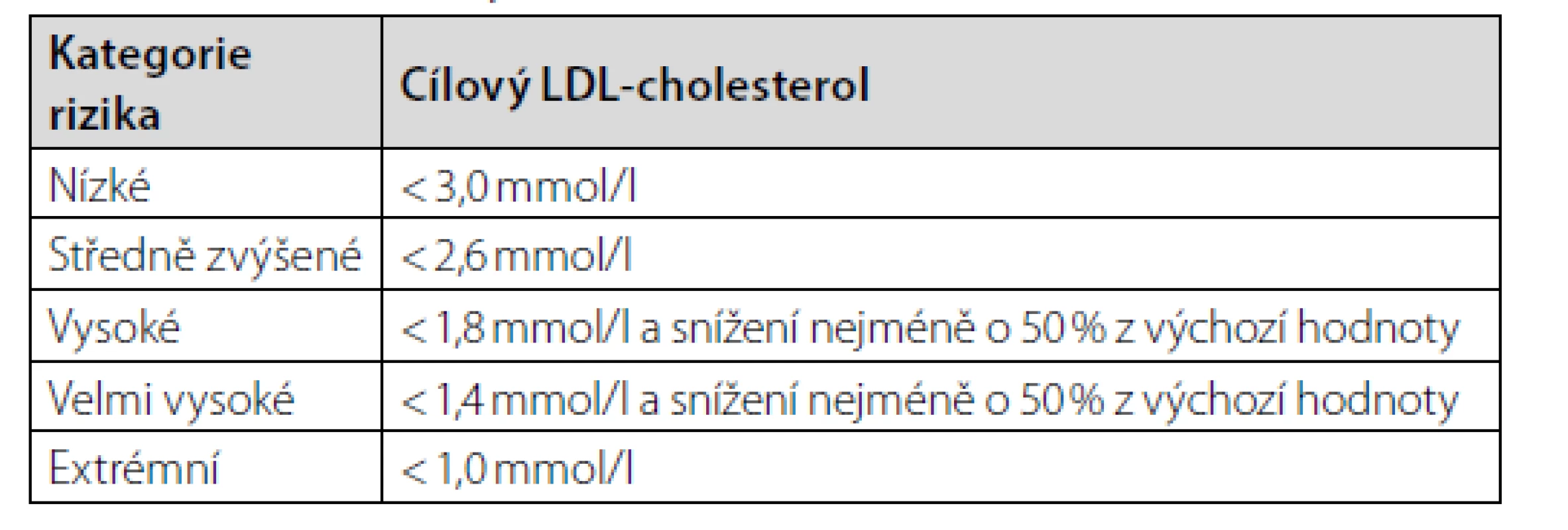
Table 2. Kategorizace rizika pacientů (4) 
Legenda: SCORE (Systematic Coronary Risk Estimation) – odečet 10letého kumulativního rizika vzniku první fatální kardiovaskulární příhody; DM – diabetes mellitus; RF – rizikový faktor Dosahování velmi nízkého cílového LDL-CH
Základními léky pro snižování LDL-CH a tím i pro prevenci AS KVO jsou statiny, především atorvastatin a rosuvastatin, jejichž maximálními dávkami můžeme snížit LDL-CH o 50–55 %. Pokud monoterapie statiny nestačí, je dalším krokem přidání ezetimibu, které obvykle vede k aditivnímu poklesu LDL-CH o dalších asi 20–25 % (4). Takovéto celkové snížení LDL-CH o 50–60 % stačí pro dosažení cílových hodnot u velké části osob v kategoriích mírného, středního či vysokého rizika za předpokladu, že: a) tuto terapii dobře tolerují, b) nemají velmi vysoké výchozí hodnoty LDL-CH. Obtížnější bývá dosahování cílového LDL-CH u pacientů s manifestním AS KVO v kategorii velmi vysokého rizika, protože k dosažení cílových hodnot pod 1,4 mmol/l, nebo dokonce pod 1,0 mmol/l, nestačí často ani maximální dávky statinů v kombinaci s ezetimibem. Obdobným problémem je dosahování cílových hodnot LDL-CH u pacientů s familiární hypercholesterolemií (FH), kteří spadají do kategorie vysokého nebo velmi vysokého rizika (viz Tab. 2). Jejich výchozí LDL-CH je typicky nad 5 mmol/l (často v rozmezí 6–10 mmol/l), a jeho snížením o 50–60 % tak nelze dosáhnout cílový LDL-CH < 1,8 mmol/l, nebo < 1,4 mmol/l. U těchto dvou skupin pacientů (pacienti s manifestním AS KVO, pacienti s FH) je proto potřeba vždy zvážit možnost přidat do terapie také PCSK9-inhibitory (PCSK9-i), které jsou pro tyto pacienty určeny.
Mechanismus snižování LDL-CH pomocí PCSK9-inhibitorů
PCSK9 (proprotein konvertáza subtilisin-kexin like, typ 9) je protein, syntetizovaný v hepatocytech, který reguluje (snižuje) počet funkčních LDL-receptorů (LDLR) na povrchu hepatocytů. LDLR fyziologicky cirkulují mezi povrchem hepatocytů, kde naváží částici LDL, a přenesou ji do nitra buňky, kde je částice LDL v lysozymu degradována. LDLR se potom vracejí zpět na povrch hepatocytu. Počet těchto cyklů ale limituje protein PCSK9, který se také může vázat na LDLR. Komplex LDLR + LDLčástice + PCSK9 je ale v lysozymech degradován celý včetně LDLR, takže LDLR již nemůže recyklovat zpět na povrch hepatocytu. Výsledkem je snížení počtu LDLR a tím i zvýšení LDL-CH (5).
Pokud zabráníme vazbě PCSK9 na LDLR, zvýší se počet funkčních LDLR, urychlí se vychytávání a degradace částic LDL a hladina LDL-CH klesá. To je také princip terapie PCSK9-i. PCSK9-i je monoklonální protilátka proti bílkovině PCSK9, která se na ni naváže, inaktivuje ji a zabrání tak vazbě PCSK9 na LDLR. Výsledkem je zvýšení počtu LDLR a pokles LDL-CH. Ke klinickému použití jsou v ČR od roku 2018 k dispozici dvě tyto monoklonální protilátky schválené Evropskou lékovou agenturou: evolocumab (Repatha®) firmy Amgen a alirocumab (Praluent®) firmy Sanofi.
Dávkování PCSK9-inhibitorů
Alirocumab i evolocumab jsou léky pro parenterální použití a jsou aplikovány ve formě jedné podkožní injekci s frekvencí 1× za 2 týdny. Jsou dodávány v předplněných perech na jedno použití a jejich aplikace je velmi jednoduchá, takže po krátkém nácviku si je již pacienti aplikují sami doma. Repatha je v ČR k dispozici v dávce 140 mg. Registrovaná je i Repatha v dávce 420 mg s indikací homozygotní forma FH v dávkovacím režimu 1× za 2–4 týdny, tento preparát však v ČR nemá úhradu a není k dispozici. Praluent je nabízen v dávce 75 mg a 150 mg s tím, že dávku 150 mg lze indikovat při nedostatečném účinku základní dávky 75 mg. Od dubna 2021 je Praluent v ČR k dispozici i v dávce 300 mg v režimu 1× za 4 týdny. Oba PCSK9-i jsou velmi dobře tolerovány a jsou prakticky bez jakýchkoliv nežádoucích účinků (6, 7). Terapie PCSK9-i je léčbou centrovou. Seznam center, ve kterých lze tuto terapii podávat, je k dispozici na webových stránkách Všeobecné zdravotní pojišťovny a některých odborných společností, např. České kardiologické společnosti, České společnosti pro aterosklerózu nebo České internistické společnosti.
Účinek PCSK9-i na krevní lipidy, lipoproteiny a kardiovaskulární příhody
Koncentrace LDL-CH se po aplikaci alirocumabu i evolocumabu snižuje většinou o 50–60 % (8, 9). Podrobnější informace o efektu PCSK9-i na jednotlivé frakce krevních lipidů a lipoproteinů jsou uvedeny v tabulce 3. Za velmi cenný je považován také vliv PCSK9-i na snížení lipoproteinu(a), který je nezávislým rizikovým faktorem pro rozvoj AS KVO (10). Hladinu lipoproteinu(a) nelze ovlivnit statiny ani jinými dostupnými hypolipidemiky. Klinické studie s PCSK9-i prokázaly, že oba PCSK9-i mohou snižovat hladinu lipoproteinu(a) až o 30 %. Pro oba PCSK9-i máme z klinických studií také důkazy o tom, že jejich přidání ke statinům u pacientů v sekundární prevenci dále snižuje kardiovaskulární mortalitu a morbiditu (11, 12). Nejnovější analýza výsledků studií s alirocumabem naznačuje, že s vysokou pravděpodobností dochází i ke snížení úmrtnosti ze všech příčin (13). Při interpretaci této analýzy je ale nutné vzít v úvahu fakt, že zmíněné studie nebyly koncipovány k průkazu změn celkové mortality.
Table 3. Průměrné změny hladiny krevních lipidů po podání PCSK9-inhibitorů (16–18) 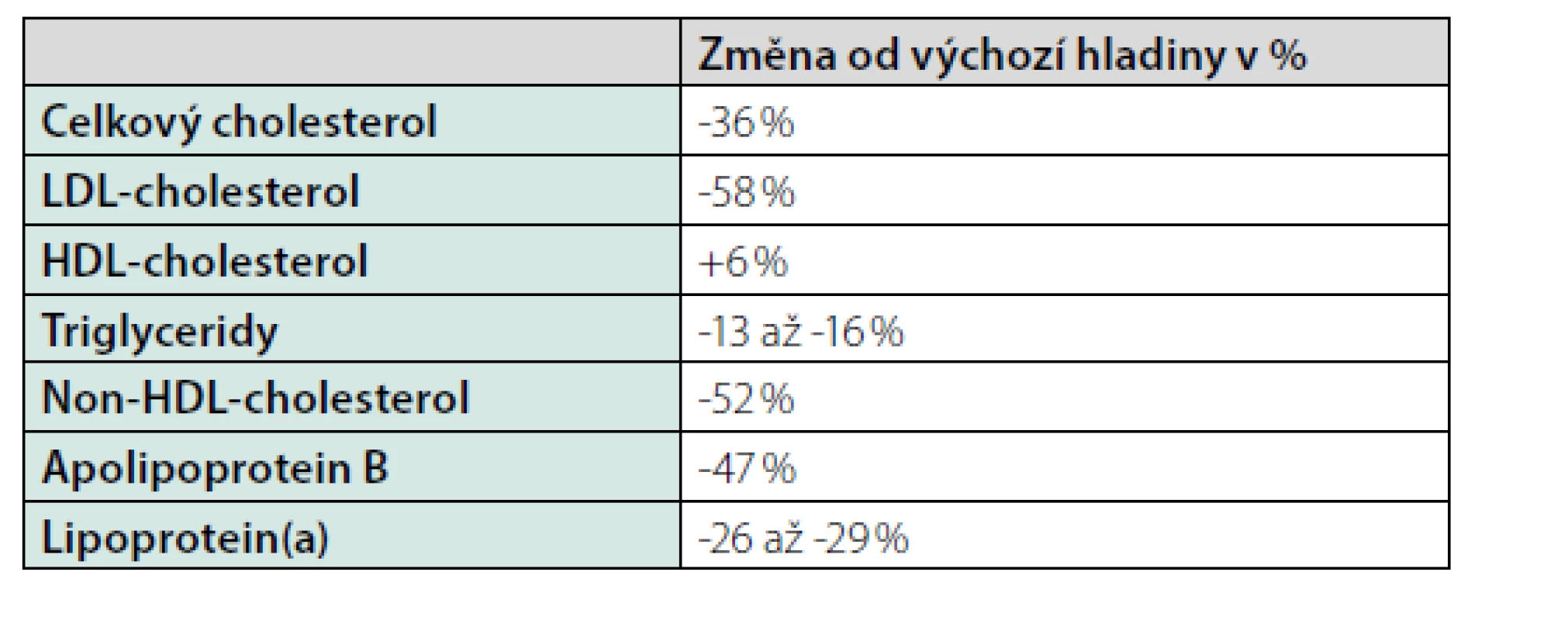
Indikační kritéria pro přidání PCSK9-inhibitorů ke stávající terapii statiny
Pro úhradu této terapie z veřejného zdravotního pojištění musejí být splněna kritéria stanovená Státním ústavem pro kontrolu léčiv (14, 15). Jak již bylo zmíněno výše, je tato terapie hrazena z veřejného zdravotního pojištění pouze u 2 skupin pacientů ve velmi vysokém riziku AS KVO:
1. pacienti s manifestním AS KVO (ischemická choroba srdeční, ischemická cévní mozková příhoda nebo tranzitorní ischemická ataka, ischemická choroba dolních končetin, stav po arteriální revaskularizaci);
2. pacienti s heterozygotní formou FH. Kritéria pro diagnostiku FH lze nalézt na webu České společnosti pro aterosklerózu (www.athero.cz), přičemž nejčastěji je pro diagnostiku používán nizozemský systém skórování DLNC (Dutch Lipid Network Criteria) (viz Tab. 4). Pacienty s podezřením na FH je možné odeslat k diagnostice do některého z center MedPed, specializovaného na tuto problematiku (seznam center je také uveden na www.athero.cz).
Table 4. Dutch Lipid Network Criteria pro diagnostiku Familiární hypercholesterolemie 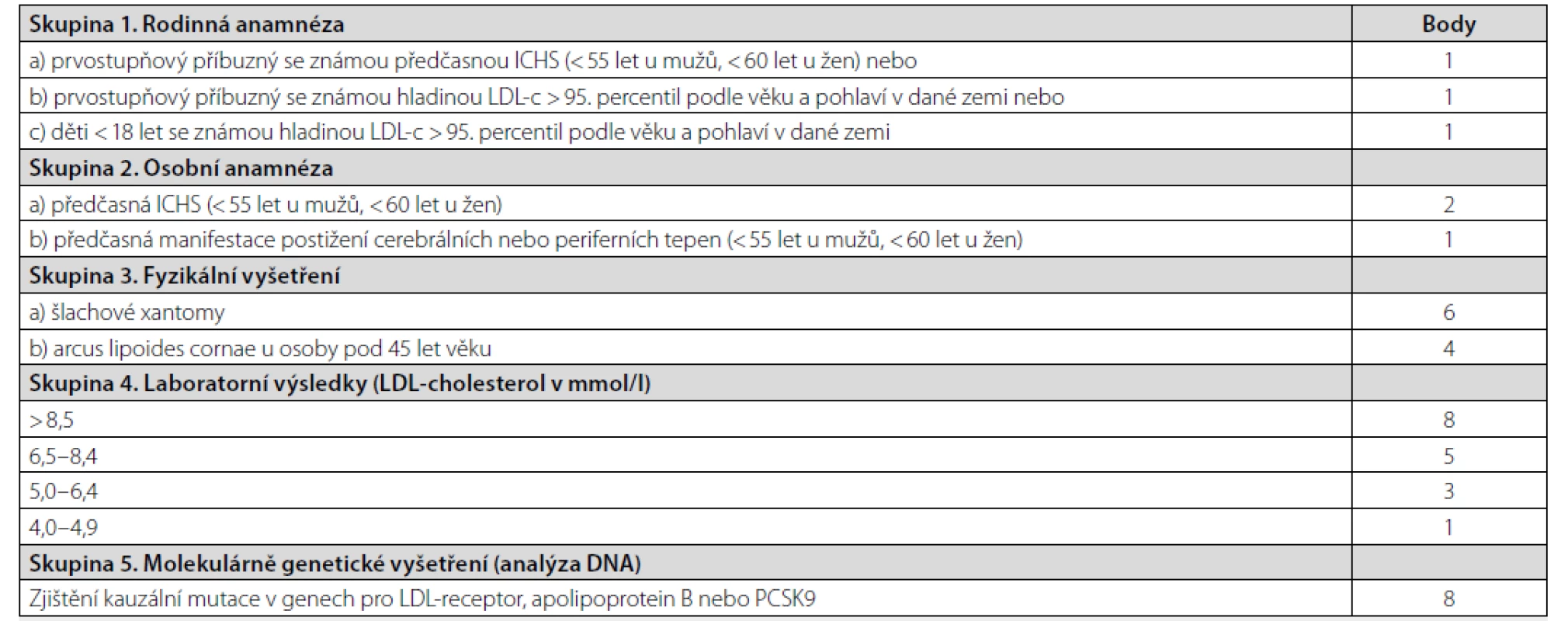
ICHS – ischemická choroba srdeční. Z každé skupiny lze použít k bodování pouze jednu položku. Hodnocení: skóre nad 8 bodů = jistá FH; skóre 6–8 bodů = pravděpodobná FH; skóre 3–5 bodů = možná FH; 0–2 body = nepravděpodobná FH Tito pacienti mají být léčeni vysoce intenzivní hypolipidemickou terapií, kterou se rozumí maximální tolerovaná dávka atorvastatinu nebo rosuvastatinu v kombinaci s ezetimibem. Pokud má pacient při max. tolerované terapii statiny LDL-CH vyšší, než je níže uvedená regulačním orgánem (SÚKL) stanovená hodnota, má být přidán do terapie PCSK9-i. Původně (v době příchodu PCSK9-i na trh v ČR) byla tato hodnota LDL-CH pro pacienty s FH > 4,0 mmol/l, pro pacienty s manifestním AS KVO > 3,0 mmol/l. V roce 2021 již platí mírnější kritéria: pro pacienty s FH > 3,1 pro pacienty s s manifestním AS KVO > 2,5 mmol/l (14, 15). Pokud má pacient s FH manifestní AS KVO, platí pro něj samozřejmě hodnota LDL-CH > 2,5 mmol/l. Je nutné zdůraznit, že tyto stanovené hladiny LDL-CH nejsou hodnotami cílovými, definovanými odbornými doporučeními, ale jde o „cutt-off“ hodnoty, při kterých má být ke stávající hypolipidemické terapii přidán PCSK9-inhibitor. Intolerance statinů sama o sobě není indikací k terapii PCSK9-i, pokud nejde o intoleranci u pacienta spadajícího do jedné ze dvou výše uvedených skupin.
Kdo by měl být odeslán do centra pro biologickou terapii PCSK9-i?
a) Všichni pacienti s manifestním AS KVO, kteří jsou na max. tolerované terapii statiny (ev. i v kombinaci s ezetimibem) a kteří mají při této terapii LDL-CH nad 2,5 mmol/l. Ti jsou indikováni k přidání inhibitorů PCSK9 k jejich stávající hypolipidemické terapii. U naprosté většiny z nich pak lze dosáhnout cílové hodnoty LDL-CH < 1,4, ev. i < 1,0 mmol/l.
b) Všichni pacienti s FH, kteří jsou na max. tolerované terapii statiny (ev. i v kombinaci s ezetimibem) a kteří mají při této terapii LDL-CH nad 3,1 mmol/l.
Upřesnění k postupu u pacientů s FH nebo s manifestním AS KVO, kteří netolerující statiny: pokud pacient netoleruje atorvastatin ani rosuvastatin, má být léčen maximální tolerovanou dávkou jiného statinu (fluvastatin, simvastatin) v kombinaci s dalším hypolipidemikem, jako je ezetimib, v případě průkazu úplné statinové intolerance pak jiným hypolipidemikem v monoterapii (ezetimib). Případné nevyužití ezetimibu v rámci stávající hypolipidemické terapie má být medicínsky zdůvodněno ve zdravotnické dokumentaci (intolerance, nedostatečná účinnost…). Informaci stran intolerance jednotlivých statinů je třeba konkrétně uvést ve zdravotnické dokumentaci. Indikační omezení SÚKL pak dále uvádí, že: „intolerance atorvastatinu a rosuvastatinu má být prokázána jako ústup klinické symptomatologie nebo normalizace CK po jejich vysazení a opětovný návrat myalgie nebo zvýšení CK po jejich znovu nasazení. Izolované zvýšení CK, nepřesahující 4násobek horních mezí, bez klinické symptomatologie, není považováno za statinovou intoleranci“.
V případě nejasnosti, zda je pacient indikován k terapii PCSK9-i, lze pacienty s kompletní zdravotní dokumentací odeslat ke konzultaci do některého z center této biologické terapie. Všechny potřebné informace k terapii PCSK9-i jsou také k dispozici např. na webu České společnosti pro aterosklerózu (www.athero.cz). V současné době je na terapii PCSK9-i pravděpodobně jen část pacientů, kteří jsou k této léčbě indikováni.
Samoplátci
Výše uvedená limitující indikační kritéria pro preskripci PCSK9-i se nevztahují na samoplátce. Pokud je pacient ochoten si terapii PCSK9-i hradit, může být léčen PCSK9-i, aniž by spadal do některé z výše uvedených rizikových skupin pacientů, nemusí být léčen maximálně tolerovanou dávkou statinů, ani jeho LDL-CH nemusí být nad uvedené „cut-off“ hodnoty.
Závěr
PCSK9-i představují velmi účinnou a bezpečnou metodu nejen pro dosažení velmi nízkých cílových hodnot LDL-CH, ale především pro zlepšení prognózy pacientů s velmi vysokým rizikem AS KVO. Tato moderní a vysoce efektivní terapie by proto měla být nabídnuta všem pacientům, kteří splňují příslušená indikační kritéria.
KORESPONDENČNÍ ADRESA AUTORA:
prof. MUDr. Vladimír Soška, CSc.
Oddělení klinické biochemie, FN u sv. Anny v Brně
Pekařská 664/53, 656 91 Brno
Článek přijat redakcí: 21. 2. 2021
Článek přijat po recenzích: 26. 4. 2021
Sources
1. Ference BA, Ginsberg HN, Graham I et al. Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J 2017; 38 : 2459–2472.
2. Boren J, Chapman MJ, Krauss RM et al. Low-density lipoproteins cause atherosclerotic cardiovascular disease: pathophysiological, genetic, and therapeutic insights: a consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J 2020; 41 : 2313–2330.
3. Piepoli MF, Hoes AW, Agewall S et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Atherosclerosis 2016; 252 : 207–274.
4. Mach F, Baigent C, Catapano AL et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J 2019; 41 : 111–188.
5. Awan Z, Baass A, Genest J. Proprotein convertase subtilisin/kexin type 9 (PCSK9): lessons learned from patients with hypercholesterolemia. Clin Chem 2014; 60 : 1380–1389.
6. Navarese EP, Kolodziejczak M, Schulze V et al. Effects of Proprotein Convertase Subtilisin/ Kexin Type 9 Antibodies in Adults With Hypercholesterolemia: A Systematic Review and Meta-analysis. Ann Intern Med 2015; 163 : 40–51.
7. Ling H, Burns TL, Hilleman DE. An update on the clinical development of proprotein convertase subtilisin kexin 9 inhibitors, novel therapeutic agents for lowering low-density lipoprotein cholesterol. Cardiovasc Ther 2014; 32 : 82–88.
8. Koren MJ, Giugliano RP, Raal FJ et al. Efficacy and safety of longer-term administration of evolocumab (AMG 145) in patients with hypercholesterolemia: 52-week results from the Open-Label Study of Long-Term Evaluation Against LDL-C (OSLER) randomized trial. Circulation 2014; 129 : 234–243.
9. Li C, Lin L, Zhang W et al. Efficiency and safety of proprotein convertase subtilisin/kexin 9 monoclonal antibody on hypercholesterolemia: a meta-analysis of 20 randomized controlled trials. J Am Heart Assoc 2015; 4 : 1–14.
10. Raal FJ, Giugliano RP, Sabatine MS et al. Reduction in lipoprotein(a) with PCSK9 monoclonal antibody evolocumab (AMG 145): a pooled analysis of more than 1,300 patients in 4 phase II trials. J Am Coll Cardiol 2014; 63 : 1278–1288.
11. Schwartz GG, Steg PG, Szarek M et al. Alirocumab and Cardiovascular Outcomes after Acute Coronary Syndrome. N Engl J Med 2018; 379 : 2097–2107.
12. Sabatine MS, Giugliano RP, Keech AC et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. N Engl J Med 2017; 376 : 1713–1722.
13. Labos C, Brophy JM, Sniderman A et al. Mortality Benefit of Alirocumab: A Bayesian Perspective. J Am Heart Assoc 2019; 8(20): e013170.
14. Praluent. https://www.sukl.cz/modules/medication/detail.php?code=0186946&tab= - prices.
15. Repatha. https://www.sukl.cz/modules/medication/detail.php?code=0186946&tab= - prices.
16. Lipinski MJ, Benedetto U, Escarcega RO et al. The impact of proprotein convertase subtilisin-kexin type 9 serine protease inhibitors on lipid levels and outcomes in patients with primary hypercholesterolaemia: a network meta-analysis. European Heart Journal 2016; 37 : 536–U103.
17. Robinson JG, Farnier M, Krempf M et al. Efficacy and Safety of Alirocumab in Reducing Lipids and Cardiovascular Events. New England Journal of Medicine 2015; 372 : 1489–1499.
18. Sabatine MS, Giugliano RP, Wiviott SD et al. Efficacy and safety of evolocumab in reducing lipids and cardiovascular events. N Engl J Med 2015; 372 : 1500–1509.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2021 Issue 3-
All articles in this issue
- Nezapomínáme na možnost biologické terapie hypercholesterolemie pomocí PCSK9-inhibitorů?
- Co nového přináší aktualizace CEAP klasifikace chronického žilního onemocnění z roku 2020?
- Možnosti léčby myelodysplastického syndromu v roce 2021
- Léčba tří pacientů s Erdheimovou-Chesterovou chorobou kladribinem, případně kombinací kladribinu a cyklofosfamidu a přehled léčby této nemoci
- Rivaroxaban v léčbě a prevenci recidivy žilního tromboembolismu u dětí
- Postavení moxonidinu v léčbě hypertenze
- Podkožní krvácení při hypotyreóze indukované pembrolizumabem
- Vericiguat u nemocných se srdečním selháním a sníženou ejekčí frakcí – studie VICTORIA
- Komentáře k analýze složení směsi flavonoidů v tabletách Diozen 500 mg metodou UHPLC
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Co nového přináší aktualizace CEAP klasifikace chronického žilního onemocnění z roku 2020?
- Vericiguat u nemocných se srdečním selháním a sníženou ejekčí frakcí – studie VICTORIA
- Postavení moxonidinu v léčbě hypertenze
- Možnosti léčby myelodysplastického syndromu v roce 2021
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

