-
Medical journals
- Career
Kryokonzervace oocytů pro zachování ženské plodnosti
Authors: A. Nesvadbová 1,2; Š. Machač 1; J. Bezdíček 2
Authors‘ workplace: IVF Clinic, a. s., Olomouc 1; Přírodovědecká fakulta, UP v Olomouci 2
Published in: Ceska Gynekol 2026; 91(2): 96-101
Category: Original Article
doi: https://doi.org/10.48095/cccg202696Overview
Cíl: Cílem studie je získat informace o úspěšnosti kryokonzervace lidských oocytů. Social freezing je metoda pro uchování plodnosti i v pozdějším věku, díky němuž mají ženy větší flexibilitu a možnost plánovat rodinu podle individuálních potřeb. Nicméně z důvodu nízké informovanosti a vysokým nákladům je tato metoda využívána v České republice minimálně. Soubor a metodika: V období od ledna 2018 do srpna 2024 bylo provedeno 93 odběrů oocytů u žen podstupujících hormonální stimulaci v rámci programu social freezing. Klientky byly rozděleny podle věku do dvou skupin: do 35 let a nad 35 let. Každá věková skupina byla dále rozdělena do dvou kategorií podle počtu vitrifikovaných oocytů: do 4 oocytů a nad 4 oocyty. Porovnali jsme úspěšnost metody vitrifikace oocytů klientek s úspěšností vitrifikace oocytů u zdravých anonymních dárkyň. Výsledky: V každé kategorii jsme vyhodnotili procento přežitých oocytů po ohřátí, tzv. survival rate (SR), procento oplozených oocytů, tzv. fertilization rate (FR), a procento získaných kvalitních blastocyst z oplozených zygot, tzv. utilization rate (UR). SR byl 61,5–89,3 %. Nejnižší hodnota je ve skupině klientek nad 35 let se ziskem oocytů do 4. FR byl 50,0–80,0 %. Nejnižší hodnota je opět ve skupině klientek nad 35 let se ziskem oocytů do 4. UR byl 34,9–75,0 %. Nejnižší hodnota je ve skupině klientek nad 35 let se ziskem oocytů nad 4. Závěr: Prokázali jsme, že věk ženy v době zmrazení oocytů a počet zamrazených oocytů zůstávají dvěma klíčovými faktory, které určují pravděpodobnost úspěšnosti dosažení možnosti mít vlastní dítě v budoucnosti.
Klíčová slova:
oocyt – plodnost – vitrifikace – kryokonzervace
V posledních dvou desetiletích vedou společenské požadavky ženy k postupnému odkládání porodu tak, aby se snažily otěhotnět po třicítce nebo čtyřicítce, kdy problémy související s věkem významně snižují šanci na úspěch [1,2]. Nedávné pokroky v reprodukční medicíně, zejména v kryobiologii a zmrazování oocytů, otevřely nové možnosti těmto ženám, které mohou v mladším věku podstoupit ovariální stimulaci vyvolávající produkci více gamet a zmrazit získané zralé oocyty pro budoucí použití [1,3].
Zmrazení oocytů bylo převážně v minulých letech nabízeno ženám před zahájením onkologické léčby [4]. V současnosti je již možné mrazení oocytů nabídnout pacientkám s hrozícím předčasným ovariálním selháním, ženám patřícím do skupiny „poor ovarian responders“ nebo pacientkám s endometriózou, která zhoršuje ovariální rezervu a může být spojena se snížením výtěžnosti oocytů po ovariální stimulaci [1,4]. Tyto ženy si během několika menstruačních cyklů mohou nastřádat větší množství zralých oocytů a později mohou vstoupit do léčby in vitro fertilizace (IVF), při níž se v jednom cyklu oplodní všechny nastřádané oocyty. Mrazení oocytů může být také nabídnuto pacientkám, u nichž v den odběru oocytů není možnost získat partnerské spermie nebo bylo odebráno velké množství oocytů [4]. Tato metoda může být také využívána při léčbě neplodnosti za použití dárcovských oocytů. Tvorba bank s dárcovskými oocyty nabízí výhodu pacientkám ve zkrácení čekací doby a větší možnosti při hledání nejlepší kompatibility dárkyně s léčeným párem [5].
V roce 2005 byla představena metoda vitrifikace oocytů a v mnoha publikacích se podařilo prokázat, že vitrifikace oocytů je z hlediska míry přežití a výsledků těhotenství lepší než pomalé zmrazování/rozmrazování [1,3] neboť prokázala vyšší počet živě narozených dětí (LBR – low birth rate).
V roce 2018 American Society for Reproductive Medicine (ASRM) popsala plánovanou kryokonzervaci oocytů jako eticky přípustnou léčbu, která může posílit reprodukční autonomii žen a podpořit sociální rovnost. Stárnutí vaječníků je přirozený a fyziologický proces, který se vyznačuje úbytkem množství a kvality oocytů. S přibývajícím věkem ženy jsou tyto základní procesy nevratně narušeny a ženy starší 35 let se v důsledku tohoto s věkem souvisejícího poklesu kvality oocytů potýkají s nižší šancí na otěhotnění a porodu živého dítěte a vyšším rizikem potratů a vrozených vad [3]. Důležitým faktorem je optimální počet oocytů, které je třeba zmrazit, aby bylo možné po zahřátí a oplodnění oocytů, kultivaci a transferu embrya dosáhnout těhotenství.
Různé odborné skupiny se obávaly zdravotních problémů u dětí počatých metodou asistované reprodukce (ART) po kryokonzervaci oocytů. První studii, která poskytla odpověď, provedli Noyes et al. v roce 2009, kteří nezaznamenali žádný významný rozdíl ve výskytu vrozených anomálií u dětí narozených po kryokonzervaci oocytů v porovnání s přirozeným početím. Jiná studie nezaznamenala žádný významný rozdíl v míře aneuploidií u embryí vzniklých z kryokonzervovaných oocytů ve srovnání s embryi získanými z čerstvých oocytů [1].
Vitrifikace je technika ultrarychlého chlazení [6]. Jde o ztuhnutí roztoku, který se rychle ochladí a z kapalné fáze se zformuje do sklovitého, vitrifikovaného stavu při nízké teplotě, a to nikoli krystalizací ledu, ale extrémním zvýšením viskozity během chlazení [7]. Cílem je v oocytech rychle nahradit většinu molekul vody kryoprotektanty. Po dehydrataci následuje velmi rychlé ochlazení (> 10 000 °C/min), které vede ke ztuhnutí obsahu buňky jako skla, při němž je plně zachována strukturální a funkční integrita oocytu [3]. Tato rychlost je závislá na typu nosiče a objemu a koncentraci kryoprotektiva [8]. Čím vyšší je koncentrace kryoprotektiv, tím vyšší je teplota při vitrifikaci (Tg), a tím se snižuje šance na tvorbu ledových krystalů, které následně poškozují samotné buňky. Každý typ kryoprotektiva má rozdílnou toxicitu, penetraci a Tg. Kombinace různých kryoprotektiv vedla ke zvýšení Tg a snížení toxicity. Další velkou roli hraje potřebný objem kryomédia při mrazení. Čím nižší je objem, tím vyšší je rychlost vitrifikace. Menší objemy umožňují lepší přenos tepla, a tím usnadňují chlazení. Snížení objemu a zvýšení rychlosti chlazení umožňuje mírný pokles koncentrace kryoprotektiv, a tím snižuje toxicitu a nebezpečné osmotické účinky [9].
Zralé oocyty ve stadiu metafáze II jsou obzvláště citlivé na ochlazení, které může způsobit nevratné poškození membrány, ztvrdnutí zóny v důsledku předčasného uvolnění kortikálních granulí nebo abnormálního zvýšení cytoplazmatických volných vápenatých iontů či dezorganizaci vřeténka se ztrátou nebo shlukováním mikrotubulů během procesu kryokonzervace [10]. Jejich citlivost je způsobena především jejich velikostí a vysokým obsahem vody [11].
Hlavní ochranu před možným poškozením představují specifické chemické sloučeniny, tzv. kryoprotektanty (CPA), které se přidávají do vitrifikačního média. CPA se dělí se na dva typy – penetrující a nepenetrující přes buněčnou membránu. Do skupiny penetrující patří nejčastěji používané ethylenglykol (EG), dimethylsulfoxid (DMSO), propylenglykol nebo 1,2-propandiol (PROH). Do skupiny nepenetrujících patří např. trehalóza, sacharóza, glukóza, polyvinylpyrrolidon (PVP) [2].
Pokud jde o vitrifikaci oocytů, bylo v průběhu let vyvinuto několik roztoků a protokolů. Kromě protokolu založeného na DMSO byl vyvinut vitrifikační systém sestávající z fosfátového pufrovaného média doplněného 20 % lidského sérového albuminu (HSA) a glycerolu ve zvyšujících se koncentracích. Pro vitrifikaci lidských oocytů a embryí jsou oba systémy dobře zavedeny a představují současné a nejlepší životaschopné možnosti lišící se především přítomností, nebo nepřítomností DMSO. Nepřítomnost DMSO např. umožňuje pomalejší rychlost chlazení, větší objemy mikrokapiček a různé nosiče. Oocyty vyžadují rychlou manipulaci (< 1 min) a tento úkol mohou úspěšně provést pouze dobře vyškolení embryologové.
V současné době bylo popsáno více než 30 různých nosných nástrojů [5]. Povrchové nosiče se využívají při otevřeném systému, např. Cryoloop a Cryotop. Tento systém využívá minimální velikost kapky kryoprotektiva s vysokou rychlostí ochlazení a oteplení [12]. Slámkové nosiče byly vyvinuty pro uzavřené systémy. Mezi tento typ nosičů patří CryoTip, Rapid I nebo Cryopette. Při porovnání Cryotopu s CryoTipem bylo zjištěno, že uzavřené zařízení vykazuje lepší míru přežití, ale u vitrifikovaných oocytů se objevila ooplazmatická vakuolizace, zduřelé mitochondrie a vysoký počet rozptýlených vezikul, což bylo pravděpodobně způsobeno méně rychlým poklesem teploty v uzavřeném nosiči.
Přestože existují důkazy, že riziko křížové kontaminace je zanedbatelné a na teoretické úrovni, stále se vedou diskuze na toto téma. Zatímco Antonouli et al. udávají, že screening kultivačního média a tekutého dusíku (LN2) na přítomnost virů HIV, hepatitidy B a hepatitidy C neprokázal přítomnost příslušných virů ve všech studovaných vzorcích, které byly vitrifikovány pomocí otevřeného zařízení Cryotop a také nebyla po 1–2 letech skladování materiálu pozorována kontaminace bakteriemi nebo plísněmi [5], Cai et al. uvádějí, že stále přetrvávají obavy v souvislosti s otázkami možné křížové kontaminace a přenosu nemocí zprostředkovaných LN2 a alternativou je uzavřená vitrifikace, u níž některé studie zaznamenaly snížení míry přežitelnosti oocytů. Někteří autoři naznačují, že „otevřená“ vitrifikace je lepší než „uzavřená“, pokud jde o míru přežití po rozmrazení. Jiní nezjistili mezi těmito dvěma metodami žádné statistické rozdíly [13].
Během zahřívání jsou vitrifikované oocyty vyjmuty z místa uložení a ponořeny do předehřátého média s vysokým obsahem sacharózy, po kterém následuje promytí v médiu s postupně nižší koncentrací sacharózy. Cílem zahřívání je rehydratace oocytů osmózou a postupná náhrada kryoprotektiv vodou. Pro mnohé je proces zahřívání důležitější než chlazení, protože během zahřívání může docházet také k tvorbě krystalů ledu, které mohou způsobit smrt buněk. Očekávaná míra obnovy po zahřátí oocytů se pohybuje od 80 do 90 % [3]. Dle autorů společnosti Alpha je minimální doporučení přežití oocytů 70 % [14].
Dalším ovlivňujícím faktorem vitrifkace je vliv osmotického stresu na buňku, který může vyvolat peroxidaci lipidů, poškození DNA a oxidaci proteinů. To vede k poškození plazmatické membrány a organel, převážně mitochondrií, kdy dojde k vyčerpání adenosintrifostátu (ATP) a spuštění vnitřní apoptické dráhy. Bylo prokázáno, že různé antioxidanty (glutathion, kyselina askorbová nebo koenzym Q10) přidané do kryomédií zmírňují oxidační stres spojený s vitrifikací oocytů u myší, ovcí i skotu [10].
Vitrifikace oocytů je vhodnou možností pro klientky, které chtějí chránit a zachovat svou budoucí plodnost [1]. Bohužel zmrazování vajíček pro sociální účely zůstává vzhledem k vysokým ekonomickým nákladům stále vhodnou volbou jen pro několik málo žen [15].
V procesu vitrifikace existuje mnoho proměnných, které mohou zásadně ovlivnit její účinnost a potenciál zlepšit míru přežití vitrifikovaných buněk [6]. Úspěch kryokonzervace nepřímo závisí na kvalitě kryokonzervovaných gamet, která zase závisí na odpovědi na léčbu ovariální stimulací [5]. Ve své práci zmiňuje Ursula Eischenlaub-Ritter řadu faktorů, které ovlivňují funkčnost stárnoucích oocytů, a potvrzuje, že mírnější hormonální stimulace snižuje aneuploidii oocytů [16]. U žen nad 35 let je patrné zhoršení kvality oocytů, které mají nižší schopnost opravy DNA ve srovnání s mladšími oocyty. Neúplná oprava DNA ve stárnoucích oocytech vede k poškození integrity a dělení chromozomů, čímž se zhoršuje kvalita oocytů.
Oocyty patří mezi nejdéle žijící buňky v těle a musí si zachovat svou cytoplazmu, aby podporovaly správný embryonální vývoj [17]. Z toho důvodu jsou věk v době zmrazení a počet uskladněných oocytů dvěma klíčovými faktory, které určují výsledky. Odhaduje se, že k dosažení těhotenství je zapotřebí v průměru 20 oocytů, přičemž minimální navrhovaný počet je osm až deset. U žen podstupujících uchování plodnosti před 35. rokem věku se očekává vyšší výtěžnost oocytů s menším počtem cyklů ovariální stimulace a vyšší počet živě narozených dětí oproti ženám starším 35 let [3].
Materiál a metodika
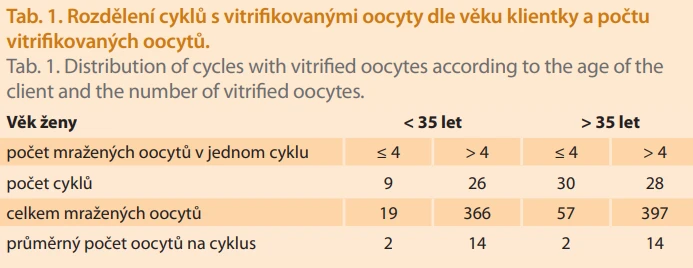
V období od ledna 2018 do srpna 2024 jsme zamrazili metodou vitrifikace Kitazato 839 oocytů od 85 klientek ve věku 18–48 let. U osmi klientek jsme vitrifikovali oocyty z více cyklů. V jednotlivých cyklech bylo zmrazeno 1–39 zralých oocytů. Pro vyhodnocení úspěšnosti zisku a vitrifikace oocytů jsme rozdělili klientky do dvou věkových skupin: do 35 let a nad 35let.
U žen ve věku do 35 let bylo celkem zamrazeno 385 oocytů z 35 cyklů. Z těchto cyklů bylo 9 cyklů s vitrifikací 1–4 oocytů a 26 cyklů s vitrifikací 5–38 oocytů.
U žen ve věku nad 35 let bylo celkem zamrazeno 454 oocytů z 58 cyklů. Z těchto cyklů bylo 30 cyklů s vitrifikací 1–4 oocytů a 28 cyklů s vitrifikací 5–39 oocytů (tab. 1).
Výsledky
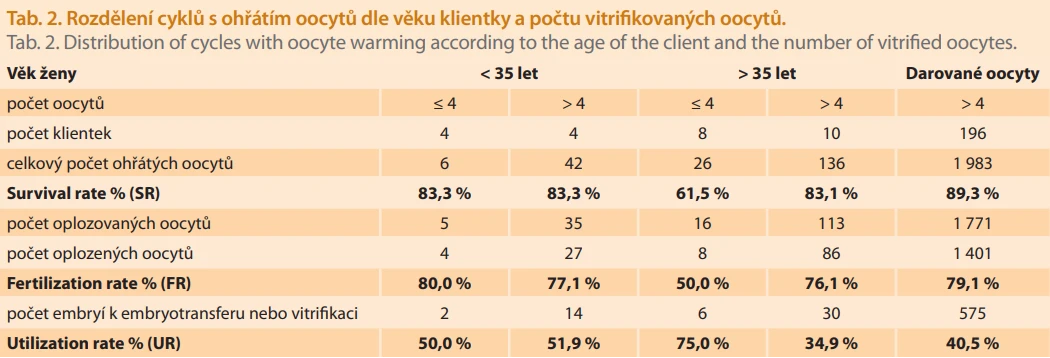
Celkem jsme rozmrazili 210 oocytů z 32 cyklů od 26 klientek. Celkově přežilo 169 oocytů, tzn. survival rate (SR) byl 80,5 %. Všechny přeživší oocyty byly oplozeny metodou intracytoplazmatické injekce spermie (ICSI) za použití partnerských či dárcovských spermií. Celkově bylo oplozeno 125 oocytů, tzn. fertilization rate (FR) byl 74,0 %. Embrya byla kultivována do 3.–6. dne kultivace a všechna získaná kvalitní embrya byla transferována nebo zamrazena. Celkově bylo získáno 52 kvalitních embryí, tzn. utilization rate (UR) byl 41,6 %.
Ve sledovaném období bylo provedeno jedenáct čerstvých embryotransferů, z nichž otěhotněly tři klientky. Jedna klientka porodila zdravé dítě a u dvou klientek došlo k těhotenské ztrátě. Dále bylo provedeno 18 kryoembryotransferů, z nichž otěhotnělo šest klientek. Čtyři klientky porodily zdravé dítě a u dvou klientek došlo k těhotenské ztrátě.
Sedm klientek požádalo o ukončení uchovávání vitrifikovaných oocytů, a to v době 11–33 měsíců od vitrifikace. Dvě klientky požádaly o export jejich vitrifikovaných oocytů do jiné IVF kliniky. V tab. 2 jsou uvedeny výsledky SR, FR a UR v jednotlivých věkových skupinách (do 35 let a nad 35 let). Každá věková skupina byla dále rozdělena do dvou kategorií podle počtu vitrifikovaných oocytů: do 4 oocytů a nad 4 oocyty. Porovnali jsme úspěšnost metody vitrifikace oocytů klientek s úspěšností vitrifikace oocytů u zdravých anonymních dárkyň za stejné časové období.
Z výsledků úspěšnosti metodiky vitrifikace oocytů plyne, že nejnižší úspěšnost SR a FR byla ve skupině pacientek > 35 let s 1–4 vitrifikovanými oocyty. Nejnižší úspěšnost UR byla ve skupině pacientek > 35 let s > 4 vitrifikovanými oocyty.
Dosažené výsledky úspěšnosti SR, FR a UR u skupiny zdravých dárkyň oocytů odpovídají doporučením odborných společnosti ESHRE a Alpha. SR minimálně 70 %, FR minimálně 65 % [14,18].
Ze získaných dat SR, FR a UR u skupin pacientek s vlastními oocyty vyplývá, že úspěšnost metodiky vitrifikace oocytů je nejen závislá na věku ženy, ale také na počtu zamrazených oocytů.
Diskuze
Z praxe vyplývá, že mnoho žen nadhodnocuje možnosti přirozeného početí ve vyšším věku i úspěšnost asistované reprodukce. Pro zamražení oocytů se často ženy rozhodnou až poté, co zjistí, že se snižuje jejich reprodukční zdraví, např. při výskytu endometriózy nebo nízké ovariální rezervy, zpravidla kolem 37. roku [19]. To podporuje nutnost včasné edukace a zavedení preventivních screeningových programů reprodukčního zdraví.
Při klinickém rozhodování je nezbytné zohlednit nejen věk, ale také charakter ovariální odpovědi. Kvalita gamet i spermií významně ovlivňuje výslednou kvalitu embryí, přičemž rozmražení může tento parametr dále zhoršit [3]. U žen se špatnou ovariální rezervou je vhodné zvážit kumulaci oocytů z více stimulačních cyklů.
Naše dosažené výsledky odpovídají výsledkům studie prof. Garratta: SR 84 %, FR 71 % a UR 37 % [20], přičemž nejvyšší úspěšnosti bylo dosaženo u skupiny žen, které podstoupily vitrifikaci před 35. rokem věku (SR 83 %, FR 78 %, UR 51 %). Cobo et al. ve své práci potvrzují, že se zvyšujícím se počtem MII oocytů roste i pravděpodobnost živě narozeného dítěte, zejména u mladších žen [19]. Chatziparasidou očekává u žen podstupujících tzv. social freezing před 35. rokem věku vyšší výtěžnost oocytů s menším počtem cyklů ovariální stimulace a vyšší počet živě narozených dětí, což posiluje význam věku pro uchování plodnosti [3].
Z biologického hlediska zůstává vitrifikace v mladším věku optimální strategií nejen pro dosažení jednoho, ale potenciálně i druhého dítěte. U žen starších 40 let je nutné zohlednit vyšší podíl aneuploidií embryí (až 80 %) a diskutovat také možnost použití darovaných oocytů.
Chang et al. uvádějí, že věk ženy v době kryokonzervace je klíčovým faktorem úspěchu, nikoli samotný protokol vitrifikace či hormonální stimulace [21]. To koresponduje s našimi zjištěními, že věk a počet uchovaných MII oocytů představují hlavní prediktory klinického výsledku.
Chatziparasidou odhaduje, že k dosažení jednoho živě narozeného dítěte je průměrně zapotřebí 20 oocytů, přičemž minimální počet se pohybuje mezi 8 a 10 [3]. Kavasen et al. dále specifikují, že u žen mladších 38 let postačuje 10–15 oocytů, zatímco u žen ve věku 38–40 let doporučuje mít uchováno 25–30 oocytů. V souladu s literaturou klesá LBR s rostoucím věkem, zatímco potřebný počet rozmražených oocytů pro dosažení porodu se zvyšuje [22–24]. Jak upozorňují Kasaven et al. [23], přeceňování šancí na úspěch může vést k emočním a psychologickým následkům, zejména u žen s nízkým počtem uchovaných oocytů.
V souladu s doporučeními odborných společností (ESHRE, Alpha) dosahovala skupina s darovanými oocyty hodnot FR nad doporučenou hranicí 65 %. Výsledky skupin s vlastními oocyty však mohly být ovlivněny menším počtem případů a variabilitou mezi pacientkami.
Technická variabilita mezi laboratořemi a embryology i nadále představuje rizikový faktor, zejména u starších žen, u kterých i malá ztráta životaschopných oocytů může výrazně snížit šanci na těhotenství [3]. Navzdory těmto omezením zůstává kryokonzervace oocytů v mladším věku efektivní strategií pro zachování reprodukčního potenciálu.
Mezi omezení naší studie patří retrospektivní charakter, analýza z jednoho centra a nízký počet klientek, které zatím použily své uchovávané oocyty, což je běžný jev i v mezinárodním kontextu. Rovněž nebyla provedena kontrola některých proměnných, jako jsou přidružené diagnózy ovlivňující plodnost. Také postupy při rozmrazování se u našich pacientek značně lišily. Některé rozdělily oocyty do více cyklů, jiné kombinovaly oocyty z více cyklů do jednoho rozmrazování. U některých byl plánován čerstvý transfer, u jiných bylo v plánu provedení preimplantační genetické testování (PGT).
Závěr
Vitrifikace oocytů nabízí ženám efektivní nástroj pro zachování reprodukčního potenciálu, který však není zárukou budoucího mateřství. Výsledky musí být vždy interpretovány v kontextu věku ženy, její ovariální rezervy a celkové výtěžnosti oocytů.
Sources
1. Sciorio R, Pluchino N, Fuller BJ. Review of human oocyte cryopreservation in ART programs: current challenges and opportunities. Cryobiology 2023; 113 : 104590. doi: 10.1016/ j.cryobiol.2023.104590.
2. Fouks Y, Sakkas D, Bortoletto PE et al. Utilization of cryopreserved oocytes in patients with poor ovarian response after planned oocyte cryopreservation. JAMA Netw Open 2024; 7 (1): e2349722. doi: 10.1001/jamanetworkopen. 2023.49722.
3. Chatziparasidou A. Improving oocyte freezing for advanced maternal age. J Reprod Med Embryol 2024; 1 (1): 10–17. doi: 10.21608/jrme.2024.261045.1003.
4. Cobo A, Domingo J, Pérez S et al. Vitrification: an effective new approach to oocyte banking and preserving fertility in cancer patients. Clin Transl Oncol 2008; 10 (5): 268–273. doi: 10.1007/s12094-008-0196-7.
5. Antonouli S, Di Nisio V, Messini C et al. A comprehensive review and update on human fertility cryopreservation methods and tools. Front Vet Sci 2023; 10 : 1151254. doi: 10.3389/fvets. 2023.1151254.
6. Liebermann J, Nawroth F, Isachenko V et al. Potencial importance of vitrification in reproductive medicine. Biol Reprod 2002; 67 (6): 1671–1680. doi: 10.1095/biolreprod.102.006833.
7. Fahy GM, MacFarlane DR, Angell CA et al. Vitification as an approach to cryopreservation. Cryobiology 1984; 21 (4): 407–426. doi: 10.1016/0011-2240 (84) 90079-8.
8. Yavin S, Arav A. Measurement of essential physical properties of vitrification solutions. Theriogenology 2007; 67 (1): 81–89. doi: 10.1016/j.theriogenology.2006. 09.029.
9. Arav A, Natan Y, Levi-Setti PE et al. New methods for cooling and storing oocytes and embryos in a clean environment of –196°C. Reprod Biomed Online 2016; 33 (1): 71–78. doi: 10.1016/j.rbmo2016.03.010.
10. Olexiková L, Dujíčková L, Makarevich AV et al. Glutathione during post-thaw recovery culture can mitigate deleterious impact of vitrification on bovine oocytes. Antioxidants 2022; 12 (1): 35. doi: 10.3390/antiox120 10035.
11. Arav A, Natan Y. Vitrification of oocytes: from basic science to clinical application. Adv Exp Med Biol 2013; 761 : 69–83. doi: 10.1007/978 - 1-4614-8214-7_6.
12. Aye M, Di Giorgio C, De Mo M et al. Assessment of the genotoxicity of three cryoprotectants used for human oocyte vitrification: dimethyl sulfoxide, ethylene gylocol and propylene glycol. Food Chem Toxicol 2010; 48 (7): 1905–1912. doi: 10.1016/j.fct.2010. 04.032.
13. Cai H, Niringiyumukiza JD, Li Y et al. Open versus closed vitrification system of human oocytes and embryos: a systematic review and meta-analysis of embryologic and clinical outcomes. Reprod Biol Endocrinol 2018; 16 (1): 123. doi: 10.1186/s12958-018-0440-0.
14. Alpha Scientists in Reproductive Medicine. The Alpha consensus meeting on cryopreservation key performance indicators and benchmarks: proceeding of an expert meeting. Reprod Biomed Online 2012; 25 (2): 146–167. doi: 10.1016/j.rbmo.2012.05.006.
15. Katsani D, Paraschou N, Panagouli E et al. Social egge freezing – a trend or modern reality? J Clin Med 2024; 13 (2): 390. doi: 10.3390/jcm13020390.
16. Eichenlaub-Ritter U. Oocyte ageing and its cellular basis. Int J Dev Biol 2012; 56 (10–12): 841–852. doi: 10.1387/ijdb.120141ue.
17. Sharma N, Coticchio G, Borini A et al. Changes in DNA repair compartments and cohesin loss promote DNA damage accumulation in aged oocytes. Curr Biol 2024; 34 (22): 5131.e6–5148.e6. doi: 10.1016/j.cub.2024. 09.040.
18. ESHRE Special Interest Group of Embryology, Alpha Scientists in Reproductive Medicine. The Vienna consensus: report of an expert meeting on the development of art laboratory performance indicators. Reprod Biomed Online 2017; 35 (5): 494–510. doi: 10.1016/ j.rbmo.2017.06.015.
19. Cobo A, García-Velasco JA, Coello A et al. Oocyte vitrification as an efficient option for elective fertility preservation. Fertil Steril 2016; 105 (3): 755.e8–764.e8. doi: 10.1016/ j.fertnstert.2015.11.027.
20. Garratt J, Shah T, McLaughlin A et al. Clinical outcomes of vitrified-warmed autologous oocyte cycles with 15-year follow-up at a single UK centre: consistent and predictable results. Reprod Biomed Online 2025; 50 (1): 104376. doi: 10.1016/j.rbmo.2024.104376.
21. Chang CC, Shapiro DB, Nagy ZP. The effects of vitrification on oocyte quality. Biol Reprod 2022; 106 (2): 316–327. doi: 10.1093/biolre/ioab 239.
22. Cobo A, García-Velasco JA, Remohí J et al. Oocyte vitrification for fertility preservation for both medical and nonmedical reasons. Fertil Steril 2021; 115 (5): 1091–1101. doi: 10.1016/ j.fertnstert.2021.02.006.
23. Kasaven LS, Jones BP, Heath C et al. Reproductive outcomes from ten years of elective oocyte cryopreservation. Arch Gynecol Obstet 2022; 306 (5): 1753–1760. doi: 10.1007/s00404-022-06711-0.
24. Kawwass JF, Crawford S, Hipp HS. Frozen eggs: national autologous oocyte thaw outcomes. Fertil Steril 2021; 116 (4): 1077–1084. doi: 10.1016/j.fertnstert.2021.05.080.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inCzech Gynaecology

2026 Issue 2-
All articles in this issue
- Impact of angiogenic factors and maternal endothelial dysfunction on pregnancy outcome
- Cryopreservation of oocytes to preserve female fertility
- vNOTES hysterectomy reduces laparotomy conversion rates in class III obesity – a retrospective comparative study
- Perinatal outcomes in severe preeclampsia with peritoneal ascites – a single tertiary center experience
- Epidemiology of obesity in pregnancy in the Czech Republic – demographic context and clinical implications
- Endometrioma of Bartholin’s gland
- Vulvodynia and persistent vulvar pain – diagnosis, treatment, and the role of laser vaporization
- Clinically relevant histopathological features and biomarkers in endometrial cancer
- Limits of preeclampsia screening and prevention in a population of women after assisted reproductive technologies
- Impact of selected dimensions of pelvic floor structures on the process of delivery – a review of the literature
- ESGO/ISUOG guidelines for needle biopsies in gynecologic oncology – the adapted version
- Assoc. Prof. MUDr. Jaroslav Feyereisl, MD, CSc. – former director of the Institute for Mother and Child Care, has passed away
- Czech Gynaecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Impact of angiogenic factors and maternal endothelial dysfunction on pregnancy outcome
- Impact of selected dimensions of pelvic floor structures on the process of delivery – a review of the literature
- Cryopreservation of oocytes to preserve female fertility
- Perinatal outcomes in severe preeclampsia with peritoneal ascites – a single tertiary center experience
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career