-
Medical journals
- Career
Neurohypofyzární peptidy v lékařství z pražských a švédských laboratoří. Část 2: Desmopressin, terlipressin, carbetocin – farmakologie a klinické aplikace
Authors: V. Pliska 1; A. Pařízek 2; M. Flegel †3*
Authors‘ workplace: Department of Biology, Eidgenössische Technische Hochschule (ETH), Wofgang-Pauli-Strasse 27, CH-8093 Zürich 1; Gynekologicko-porodnická klinika 1. lékařské fakulty UK a VFN v Praze, Perinatologické centrum, Apolinářská 18, 128 51 Praha 2 2; Ústav chemie přírodních látek, Vysoká škola chemicko-technologická v Praze, Technická 5, 166 28 Praha 6 3
Published in: Ceska Gynekol 2025; 90(2): 173-181
Category: Review
Overview
Chem. Listy 2022; 116 : 101−109. doi: 10.54779/ chl20220101
vladimir.pliska@biol.ethz.ch, parizek@porodnice.cz Došlo 12. 10. 2021, přijato 1. 11. 2021.
Klíčová slova:
Oxytocin – Vasopressin – dDAVP – neurohypofyzární hormony – peptidová léčiva – deamino-D-arginin-vasopressin – Glypressin – Terlipressin – Ferring compan
Výroba léčiv založená na dohodách ÚOCHB ČSAV – Ferring AB
Licenčními dohodami, zmíněnými v předcházejících sděleních [1,2], získala v průběhu 70. a 80. let od Ústavu organické chemie a biochemie Československé akademie věd (ÚOCHB ČSAV) švédská farmaceutická firma Ferring AB Malmö práva na výrobu řady analogů a na jejich distribuci na světovém trhu mimo státy sdružené v RVHP (zkratka pro Radu vzájemné hospodářské pomoci) a. Tři z nich nalezly použití jako úspěšné léky.
dDAVP: 1-deamino-8-D-arginin vasopressin (Desmopressin)
Design tohoto analogu, jímž započala spolupráce ÚOCHB s Ferringem [1,2], vycházel ze starších známých faktů o vlivech vypuštění N-terminální aminoskupiny a D-enantiomerní substituci v pozici 8 na antidiuretickou a vasopressorickou aktivitu u peptidů vasopressinového typu. 1-Deamino - L-arginin-vasopressin (dAVP) popsali v již roce 1966 Huguenin a Boissonnas (SANDOZ S.A., Basel) [3] a později (1974) Sawyer se spolupracovníky [4]; obě laboratoře nalezly shodné antidiuretické (1 300 a 1 390 IU/mg) a vasopressorické (370 IU/mg) aktivityb proti původnímu L-arginin-vasopressinu, tedy podstatně zvýšený antidiuretický účinek při stejné vasopressorické aktivitě. Substituce D-argininem v poloze 8 arginin-vasopressinu vedla sice k mírnému snížení antidiuretické aktivity (z 332 na 257 IU/mg [5], resp. 114 IU/mg [6], ale zároveň k podstatnému poklesu aktivity vasopressorické (mezi 1,1 a 4,1 IU/mg). Kombinace obou naznačovala, že by mohlo jít o zajímavý peptid pro substituční terapii neurogenní formy žíznivkyc (diabetes insipidus). Přesto, že kumulace strukturních modifikací v individuálních peptidech obvykle nevede k předpokládané kumulaci aktivit spojených s těmito modifikacemi, pověřil ředitel ÚOCHB František Šorm skupinu Milana Zaorala, aby peptid s kombinacemi obou strukturních změn syntetizovala [7]. Výsledek byl více než překvapivý. Již v prvních antidiuretických testech provedených farmakologickou skupinou ÚOCHB vykazoval kombinovaný peptid ve srovnání s 8-L-arginin-vasopressinem (AVP) antidiuretickou aktivitu nejméně padesátinásobně vyšší, aktivitu vasopressorickou testovanou skupinou Ivana Krejčího z Výzkumného ústavu přírodních léčivd menší něž 3 %. Standardní farmakologické testy antidiuretické aktivity nejsou při tak velkých rozdílech mezi standardem a testovaným peptidem jednoznačné a dostatečně spolehlivé [8]: jednotlivé laboratoře udávaly hodnoty pro dDAVP mezi 870 IU/mg [7] a zhruba 50 000 IU/mg [9,10]e. Hodnotu dolní meze, později znovu citovanou [5], uvádějí autoři první (předběžné) publikace [6], aniž zmiňují podstatně vyšší aktivity nalezené v tehdy dosud neukončených testech z ÚOCHB. Tyto pozoruhodné diskrepance lze snad částečně vysvětlit citlivostí dDAVP na i poměrně malé rozdíly v použitých testech, především však použitím často zcela rozdílných testů a v neposlední řadě nejednotnou numerickou formulací aktivit. Údaje antidiuretických aktivit z jednotlivých laboratoří pocházejí z testů na neastetizovaných krysách hydratovaných jednorázovou perorální dávkou izotonického hydratačního media [11] (s 1–2 % ethanolu, nebo bez alkoholu), nebo krys s trvale udržovanou hydratací odpovídající 8–10 % tělesné váhy zvířete [12,13]. Antidiuretický efekt je vztažen na celkový objem či váhu vyloučené moči, tedy veličinu definovanou ve farmakologických měřeních jako AUC (area-under-the-curve), hodnotu časového integrálu diuretické křivky. V případě, kdy aktivita je definována jako podíl k danému standardu (zde tedy AVP), musí AUC být vztažen na definovanou časovou limitu [14]. Není-li tomu tak, postrádá konečný údaj spolehlivou srovnávací hodnotu. (Tak je tomu např. u některých výše citovaných dat [10]).
V případě nerovnoběžných závislostí dávka–účinek je tudíž pojem relativní specifické aktivity neadekvátní a dovoluje jen srovnání ekvipotentních dávek (dávek dvou látek působících stejný účinek) na různých úrovních účinku.
Obr. 1 znázorňuje spektrum publikovaných antidiuretických a vasopressorických aktivit jednotlivých „mezistupňů“ vývoje dDAVP a zároveň i index preference pro antiduretickou aktivitu (čísla mezi svislými šipkami), zde ad hoc definovaný jako produkt poměru antidiuretická/vasopressorická aktivita × relativní antidiuretická aktivita. Jeho vysoké hodnoty pro udávané meze antidiuretické aktivity dokumentují jeho přednost mezi analogy potenciálně použitelné v substituční terapii žíznivky.
Image 1. Schéma designu dDAVP předpokládajícího kumulaci požadovaných aktivit peptidů s izolovanou strukturní změnou. 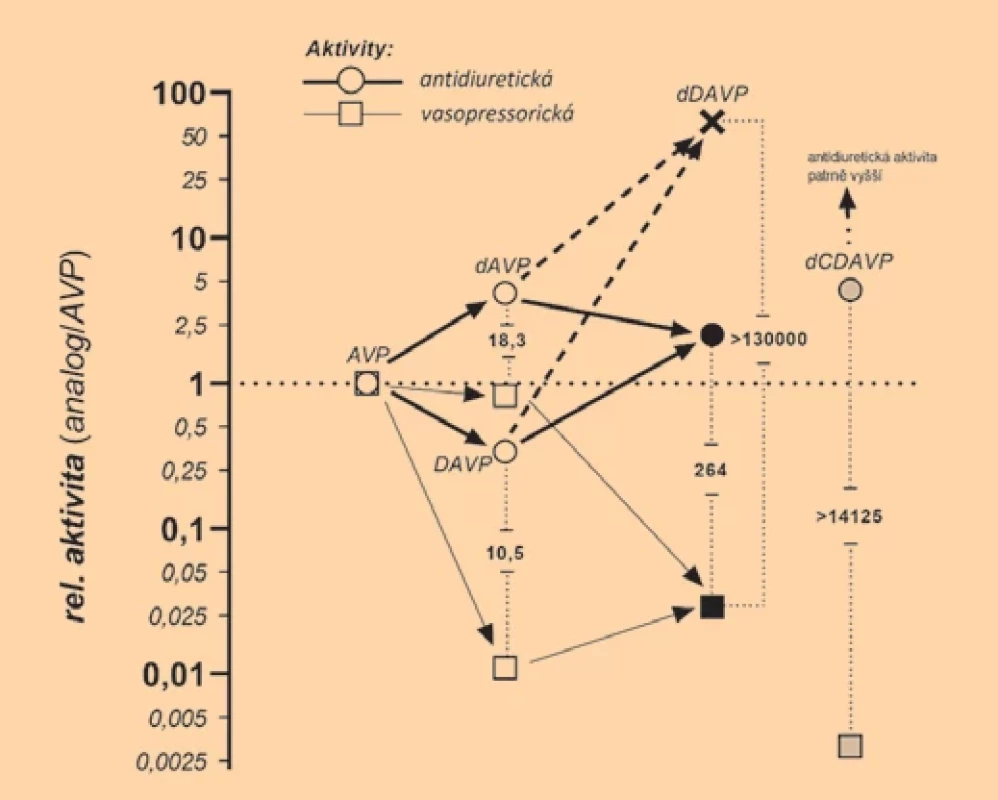
Antidiuretická (kroužky) a vasopresorická (čtverce) aktivita analogů arginin-vasopressinu (AVP), deamino-arginin-vasopressinu (dAVP), D-arginin-vasopressinu (DAVP) a kombinovaného peptidu deamino-D-arginin-vasopressinu (dDAVP, černé symboly). Rozdíly obou aktivit jsou označeny svislými tečkovanými spoji, čísla mezi nimi udávají „ad hoc index preference“ pro antiduretickou aktivitu: produkt poměru antidiuretická/vasopresorická aktivita × relativní antidiuretická aktivita (analog/ AVP). Dva údaje antidiuretických aktivit pro dDAVP odpovídají rozdílným údajům z různých zúčastněných laboratoří, používajících často rozdílné antidiuretické testy (viz text); nižší hodnota se vztahuje k extrapolované (prahové) dávce peptidu, specifi cká aktivita pro vyšší dávky [10] není jednoznačně defi nována (× označuje přibližnou horní hranici dat uváděných v literatuře). Schéma naznačuje, že v případě dDAVP byl předpoklad kumulace strukturních modifi kací v různých polohách peptidového řetězce do značné míry splněn. Pro srovnání jsou uvedeny aktivity dCDAVP (šedé symboly; viz text). Antidiuretická aktivita (2 200 IU) byla testována na neanastetisované kryse [21]; její hodnota v testu (krysa v ethanolové narkóze) je podle autorů velmi vysoká a standardní metodou neměřitelná. Index preference je tudíž ve srovnání s dDAVP mnohem vyšší. Pokud jde o délku trvání účinků dDAVP: prodloužený účinek byl jeden z parametrů, který byl již od plánované syntézy předpokládán a požadován. Autoři první klinické publikace [10] udávají pro dDAVP 12,75krát pomalejší eliminaci účinku ve srovnání s pituitárním standardem (tj. AVP), což by svědčilo o vysoké metabolické stabilitě analogu v cílových tkáních. Jejich údaje (obr. 1 v citované publikaci) však svědčí o tom, že nešlo o kinetickou analýzu a udávaná vysoká charakteristika perzistence není důvěryhodná. Srovnání směrnic lineárních částí závislostí dávka účinek [14] naznačuje přibližný index perzistence (Ip) v mezích 2,5 a 3,9. Rovněž údaje poločasu diurézy v následující publikaci [9] dovolují hrubý údaj inexu perzistence (použitím např. přepočtu podle Kimury a Yokoyamy [15]), v důsledku volby neadekvátních experimentálních podmínek však neumožňují detailní analýzu. Nicméně, přepočet naznačuje Ip = ~2, tedy hodnotu blízkou předpokladu. Ačkoliv v pracích T. Bartha a jeho skupiny na ÚOCHB byla kinetická analýza různých řad neurohypofyzárních peptidů prováděna velmi důkladně, dDAVP do těchto studií zahrnut nebyl. Zvýšenou perzistenci a s ní spojený prodloužený účinek je patrně spojen s hydrolýzou N-terminální peptidové vazby (cystein-tyrosin), která v analogických případech vede k dvoj - až čtyřnásobnému zvýšení indexu perzistence. Udávané extrémní hodnoty perzistence v citované publikaci [10] jsou tedy patrně důsledkem předávkování tohoto velmi účinného antidiuretika v citovaných pokusech.
Terapeutický potenciál dDAVP byl ovšem rychle odhadnut a substance sama byla kryta americkým patentem [16] (US 3,497,491; Feb. 24, 1970; obr. 2). Eventuální další patenty se tedy mohly týkat pouze produkčního postupu, případně nových aplikací. V tomto směru měl Ferring v době udělení patentu již vybudovanou potřebnou infrastrukturu a licenční podmínky byly tudíž pro obě strany – ČSAV a Ferring – výhodné. Licenční dohoda mezi Československou akademií věd (podpis na dohodě: K. Friml, Secretary General), Polytechnouf (dva nečitelné podpisy) a Ferringem (S. Matarasso, Managing Director; J. Mulder, Research Director) byla uzavřena v Praze v roce 1971.
Image 2. U.S. patent chránící dDAVP jako substanci a původní postup její syntézy, únor 1970. 
Klinické využití dDAVP bylo pak v druhé polovině 70. let rozšířeno o hematologické aplikace, vycházející ze studií o hemostatickém účinku vasoaktivních peptidů. Cash a spol. [17] (Regional Blood Transfusion Centre, Royal Infimary, Edinburgh) poukázali na zvýšené vyplavování aktivátoru plasminogenu a koagulačního faktoru VIII po intravenózní aplikaci neurohypofyzárních hormonů vasopressinového typu, včetně dDAVP. Později rozšířili tuto studii o další zajímavá analoga [18]. Pozoruhodně vysokou hemostatickou aktivitu nalezli u 6-karba-analogu dDAVP (dCDAVP); naproti tomu zcela neúčinný byl 8-arginin-vasotocin. Použití dDAVP ke zvýšení koncentrace faktoru VIII u pacientů s lehčí formou hemofilie A, von Willebrand-Jürgensova syndromu a trombocytárních dysfunkcích popsal pak hematolog Pier Mannuccio Mannucci z milánské univerzity se spolupracovníky [19,20]. Prevalence těchto poruch hemostáze, zpravidla dědičných, je zjevně vyšší než prevalence diabetes insipidus; dDAVP (Minirin® Ferring, Desmopressin INN) nalezl tak širší uplatnění při akutních lehčích spontánních krváceních a při menších chirurgických zásazích (ku příkladu ve stomatologii) g. To vše velice podstatně zvýšilo význam licence, kterou Ferring dohodou s ÚOCHB získal.
Případ dDAVP zároveň demonstruje časté rozdíly v úplnosti farmakologických a klinických dat. Zatímco klinická dokumentace dDAVP je obsáhlá a detailní, spolehlivé farmakologické údaje jsou nedostatečné. Ne zcela vysvětlitelné jsou zmíněné rozpory v údajích aktivit mezi jednotlivými laboratořemi, chybějící farmakokinetická data a ostatně i doklad o tom, že dDAVP představuje pro klinické účely optimální volbu ve skupině analogů s velmi podobným spektrem aktivit. Publikovaná data naznačují, že pro stejné terapeutické aplikace by takovým mohl být ku příkladu později syntetizovaný karba-6-analog dDAVP [21], 1-deamino-8-D-arginin-6-karba-vasopressin (dCDAVP, obr. 1). S ohledem na úspěch, který dDAVP v klinickém použití doznal, není ovšem tato akademická kritika zcela podstatná.
Table 1. Carbetocin a inhibitory uterotonické aktivity oxytocinu. 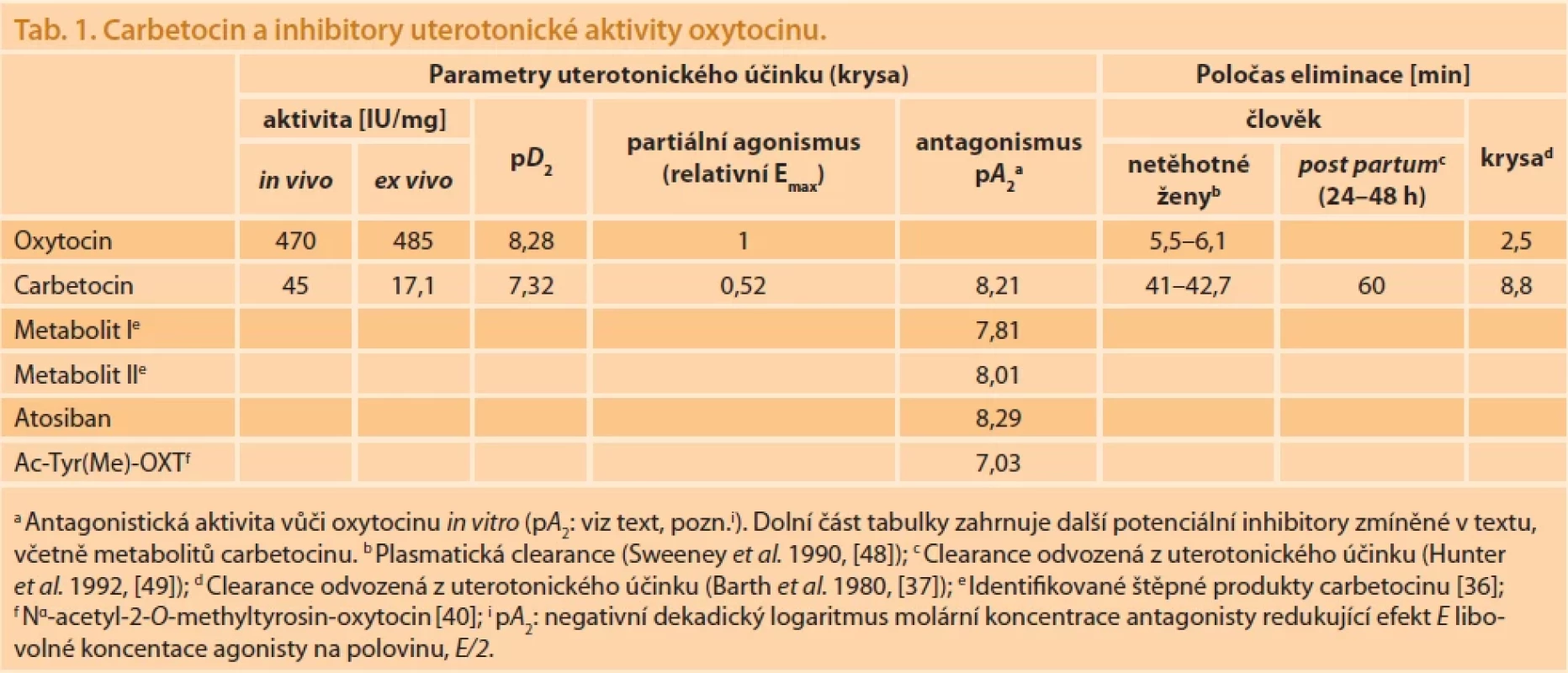
Triglycyl-8-lysin-vasopressin (Terlipressin)
V počáteční fázi licenčních dohod ÚOCHB s Ferringem figurovala vedle dDAVP také skupina analogů neurohypofyzárních hormonů s prodlouženým peptidovým řetězcem na Na-koncové aminoskupině, pro něž se ujalo (původně pracovní) označení „hormonogeny“ [22]. Jejich syntéza byla motivována představou, že převládající inaktivační proces oxytocinu a vasopressinu vzniká štěpením peptidové vazby mezi 1-hemicystinem a 2-tyrosinem aminopeptidasami, patrně enzymem leucin-amino-peptidasového typu [23]. Od prodloužení N-konce amidopeptidasami štěpitelnou aminokyselinou či krátkým peptidovým řetězcem se očekávalo postupné (a dočasné) uvolňování aktivního hormonu a tudíž prodloužení příslušného biologického účinku in vivo [24]. Tento předpokládaný mechanismus byl postupně potvrzen syntézou řady analogů 8-lysin-vasopressinu [22,25–27] a oxytocinu [28,29] s výrazně prodlouženými účinky antidiuretickými, vasopresorickými a uterotonickými, s indexem perzistence Ip mezi 1 (pro lehce štěpitelné aminoacidové substituenty – leucin, tyrosin) až 5. Na - (Gly) 3-[Cys1,Lys8]vasopressin, jehož standardní biologické aktivity na kryse jsou sice nízké (antidiuretická 2,7, vasopressorická 2,1 IU/μmol, t.j. kolem 0,5 % aktivit lysin-vasopressinu), index perzistence ale vysoký (Ip ≈ 5) [22], naznačoval ve farmakologických testech možnost klinického využití jako vasokonstričního spazmolytika zvyšujícího periferní vaskulární rezistenci při hrozícím hemoragickém šoku. Prodloužený terapeutický účinek je výhodou především v akutních stavech ezofageálním a jiném gastrointestinálním krvácení [30], traumatickém a septickém šoku, u cirhotických pacientů s portální hypertensí [31] a s tzv. hepatorenálním syndromem [32]. (Stručný přehled klinického použití publikovali v roce 2004 Kam a spol. [33]).
Analoga 8-lysin-vasopressinu acylované glycinovými peptidy na N-koncové aminoskupině byly původně chráněny československým patentem CS 4,399/64 (1. 8. 1964), později patenty v dalších zemích včetně Spojených států (US 3,558,590; July 30,1968). Patenty kryjí, velmi obecně, deriváty lysin-vasopressinu N-acetylované „krátkými peptidy obsahujícími glycin“, tedy rozsáhlou skupinu peptidů včetně meziproduktů jejich syntézy uváděné spolu s diglycyl - a triglycyl-analogem jako příklady. Licenci na jejich produkci získal Ferring již v první fázi spolupráce s ÚOCHB a registroval druhý z nich pod názvem Terlipressin (INN, Glypressin®). Z četných publikací po roce 1974 lze vyvodit jeho rychlé rozšíření v četných klinikách, i když v omezeném rozsahu aplikací.
V klinickém zkoušení byla také případná možnost použití triglycyl-vasopressinu jako kontraceptiva. Tento peptid hormonogenového typu má značně protrahovaný presorický účinek a nízký, vasopressinu podobný uterotonický efekt. Předpokládalo se, že peptid během I. trimestru těhotenství způsobuje kontrakční činnost hladké svaloviny dělohy a tím smrt plodu. Odhlížeje od etické stránky testování podobných hypotéz, naráží zde fyziologický výzkum na téměř nepřekonatelné potíže: průběh decidualizace a struktura placenty jsou u jednotlivých savců zásadně odlišné a tudíž data získaná v pokusech na zvířeti nelze v tomto specifickém případě v humánní medicíně použít. Pokud je nám známo, další kroky v tomto směru nebyly podniknuty.
Image 3. Potenciální metabolity carbetocinu identifi kované in vitro a jejich antagonistické vazby (pA2) na oxytocinovém receptoru (krysa) [36]. ![Potenciální metabolity carbetocinu identifi kované in vitro a jejich antagonistické vazby (pA2) na oxytocinovém receptoru (krysa) [36].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/0b4fe68866ac159efa28401d32e7c163.png)
V prvním stupni se předpokládá paralelní štěpení C-terminální peptidové vazby leucin-glycinamid („chymotrypsin-like enzyme“ [50–52], bílý trojúhelník; metabolit I) a enzymem hydrolyzujícím vazbu Pro7-Leu8 („postproline cleavage enzyme“ [53,54], černý trojúhelník; metabolit II), v dalším stupni následné štěpení metabolitu I na konečný metabolit II. Carbetocin: veterinární a humánní uterotonikum
Motivace syntézy a farmakologické závěry
Carbetocin (INN) h, deaminokarba1-2-O - -methyltyrosin-oxytocin, dnes rozšířené uterotonikum, byl syntetizován před rokem 1971 v laboratoři Karla Jošta v rámci výzkumu potenciálních antagonistů oxytocinu. Ohlášen byl k patentování v Československu v únoru 1971; udělení čs. patentu (CS-149028 B1; 15. 6. 1973) [34] následovalo v červnu 1973. Jak je zřejmé, nešlo o ochranu látky samotné – to nebylo v československém patentním řízení té doby přípustné, nýbrž o postup její přípravy. Bližší popis tehdy použité syntézy spolu s údaji o biologických aktivitách byl popsán v roce 1974 v publikaci o fyzikálně-chemických vlastnostech karba-analogů oxytocinu [35]. Tato publikace poprvé zahrnující též carbetocin je z různých hledisek pozoruhodná, uvedené biologické aktivity carbetocinu (zmíněné spíše na okraj) nevzbudily však z farmakologického hlediska zvláštní pozornost: uterotonická aktivita v pokuse na krysí děloze byla zhruba 3,5 % (ex vivo) a 7 % (in vivo) aktivity oxytocinu; výrazný antagonismus ex vivo zprvu prokázán nebyl. Byl však dokumentován v pozdějších pokusech na izolovaných buněčných membránách krysího myometria [36]. Stejná studie prokázala, že jde o parciálního agonistu oxytocinu (maximální kontrakce dělohy ex vivo dosáhla 50 % kontrakce inicializované oxytocinem), patrně v důsledku inhibice části oxytocinových receptorů carbetocinem samotným a jeho postupně vznikajícími metabolity (tab. 1, obr. 3). Inhibici oxytocinu in vivo a s ní spojený tokolytický účinek nebylo tudíž možné předpokládat, peptid vykazoval zhruba 10× nižší uterotonickou aktivitu oxytocinu (tab. 1). Poločas uterotonického účinku in vivo u krysy je relativně k oxytocinu několikanásobně delší [37] (poměr rychlostních konstant eliminace je 3,5), především patrně v důsledku vypuštění N-terminální aminoskupiny (farmakologická data jsou shrnuta v tab. 1). V souhrnu se tedy carbetocin ve srovnání s oxytocinem jevil jako dlouhodobě působící agonista se slabším uterotonickým efektem. V té době však byla antagonisticky působící oxytocinová analoga jedním z prioritních zájmů pražského ÚOCHB [38] a tímto zájmem byla též motivována syntéza carbetocinu. K tomu několik poznámek: antagonismem uterotonických účinků oxytocinu v širším smyslu se v druhé polovině 60. let zabýval především Josef Rudinger na ÚOCHB a skupina Ivana Krejčího na VÚFB. Jejich studie byly shrnuty v řadě publikací [23,38,39]. Zájem o antagonisty oxytocinu na této bázi byl podnícen rovněž možností jejích použití v klinické praxi při hrozícím spontánním potratu (abortus imminens) a trval i po odchodu Josefa Rudingera do Švýcarska v roce 1968. Koncem 60. let syntetizoval Karel Jošt 1-Na-acetyl-cystein-2-Ο-methyltyrosin-oxytocin [40], jeden z prvních inhibitorů uterotonického účinku oxytocinu, chráněný patenty ve více než dvou desítkách zemí (ve Spojených Státech US 3,752,799; Aug. 14, 1973, US 260-112.5, Int. Patent No. 3,752,799 [41]). Ještě před publikací projevil zájem o toto potenciální tokolytikum Jan Mulder a spolu s jedním z nás (V.P.) připravoval v říjnu 1969 podklady pro klinickou registraci ve Švédsku. Doklady o dalším licenčním jednání s ÚOCHB nejsou známy; pravděpodobné je, že licence byla udělena, ale další vývoj analogu ve Švédsku nepokračoval. Možné je, že další kroky v klinických zkouškách byly odloženy v očekávání, že nově syntetizované látky budou případně mít výhodnější antagonistické vlastnosti než stávající peptid s poměrně nízkou inhibiční konstantou – na krysí děloze ex vivo se udává pA2 = 7,03 [42]i. Zajisté byly další kroky v tomto směru ovlivněny i náhlým úmrtím Jana Muldera v roce 1976. Intenzivní vývoj nových antagonistů v Malmö pokračoval po nastoupení nového ředitele výzkumu Hanse Vilhardta, převážně pod vedením farmakologa Per Melina. Jeho výsledkem byl v druhé polovině 80. let analog 1-deaminocystein-8-ornitin-oxytocin s dalšími změnami v poloze 2 (D-O - -ethyltyrosin) a 4 (threonin) [43], který se stal postupně standardním inhibitorem v experimentální farmakologii a fyziologii neurohypofyzárních peptidů (pA2 = 8,29) a jako Atosiban (INN) rozšířeným klinickým tokolytikem [44]j.
Zdá se, že neprokazatelnost antagonismu u carbetocinu byla pro pražskou peptidovou skupinu zklamáním a ani jeho agonistické účinky neslibovaly výrazné výhody ve srovnání s jinými uterotoniky. Vysvětlovalo by to okolnost, proč tento analog, resp. jeho původní syntéza, nebyl chráněn v zemích, jejichž farmaceutický průmysl byl schopen v krátkém čase zajistit jeho produkci. Jeho patentové krytí nebylo tudíž příliš důsledné a řada firem má carbetocin ve svých nabídkách. Podmínky, za jakých převzal Ferring v této situaci carbetocin do svého výrobního programu (patrně opět v licenci Čs. akademie věd), nemohli autoři tohoto sdělení zjistit.
Carbetocin jako veterinární léčivo
Jeho první klinické použití ve veterinární medicíně spadá do druhé poloviny 70. let. Patrně z popudu Karla Jošta (ÚOCHB) převzal veterinární klinický vývoj carbetocinu a jeho zavedení do veterinární praxe Výzkumný ústav pro biofaktory a veterinární léčiva v Pohoří-Chotouni u Jílového (jeho ředitelem byl Bohumil Ševčík; ústav byl v červnu 1994 zakoupen firmou FATRO SPA, Bologna). Dokumentace pro FDA (Food and Drug Administrationk) ve formě „Drug Master File“ (DMF) l pro léčivou látku (Depotocin®) byla sestavena v pražské společnosti PolyPeptide Laboratories s. r. o. (PPL, viz níže) pro firmu Veyx-Pharma GmbH, Sachwarzenborn (Hessen). Deklarovaným cílem bylo usnadnění a vedení porodu u krav a prasnic, především ale snaha dosáhnout synchronizovaného porodu ve velkochovech, v nichž zvířata byla uměle inseminována ve stejný den. Očekávalo se též omezení nutné asistence veterinárních lékařů při porodech – tedy charakteristické cíle zkolektivizovaného chovu užitkových zvířat. Ukázalo se však, že zatímco porod mláďat bylo možno prakticky synchronizovat, porod placenty probíhal nezávisle a měl odlišný průběh. Přesto se stal carbetocin ve veterinární medicíně běžně užívaným prostředkem k indukci a vedení porodu; jevil se jako obecně šetrnější ve srovnání s oxytocinem už tím, že snižoval frekvenci porodních a poporodních komplikací. Zdůrazňovanou předností bylo bezpečnější vedení porodu u krav [45] a zvláště u (multiparitních) prasat [46] m, absence tetanické kontrakce uteru (časté při použití oxytocinu), zamezení poporodní hypoxie/asfyxie selat a urychlení involuce dělohy post partum u krav [47].
Zde je nutno podotknout, že výzkum prováděný ve jmenovaném ústavu nebyl in extenso publikován. Prvé publikace z jiných laboratoří pocházejí z let 1977–1979. Výzkum ve veterinární medicíně však později usnadnil zavedení carbetocinu v humánní medicíně, především v porodnické praxi.
Carbetocin, humánní klinická aplikace
V humánní medicíně se carbetocin stal v posledním desetiletí celosvětově používaným lékem pro prevenci a léčbu poporodního krvácení, z hlediska matky nejčastější a nejnebezpečnější komplikací porodu.
K fyziologické zástavě porodního krvácení dochází po porodu dítěte ve III. době porodní v důsledku redistribuce v cirkulaci krve a současně k aktivaci hemostatických faktorů. Tato závěrečná část porodu je časově přesně klinicky ohraničena: začíná porodem dítěte (plod přestává být plodem a stává se novorozencem) a končí porodem placenty. Při oddělování placenty od stěny dělohy je hemostáza řízena kombinací dvou mechanismů:
retrakcí hladké svaloviny dělohy (myometrium). Tím vzniká komprese cévního řečiště, kterým byla zásobena vedle myometria i placenta. Výsledkem je mechanická hemostáza;
hemostatickými faktory z děložní sliznice v těhotenství (deciduan), kdy působí tkáňový faktor, inhibitor aktivátoru plazminogenu typu 1, systémové koagulační faktory (fibrinogen apod.), které způsobují srážení krve.V patologických případech dochází k poruše alespoň jednoho ze čtyř zúčastněných faktorů označovaných také jako 4T (tonus – trauma – tkáň – trombin); následkem může být závažné, až život ohrožující krvácení. Peripartální krvácení (peripartum/postpartum hemorrhage, dále také PPH) patří mezi pět nejčastějších příčin úmrtí žen v souvislosti s těhotenstvím, porodem a šestinedělím (trombembolická nemoc, hypertenzní choroby, kardiopatie, sepse a PPH). Je tomu tak jak v zemích s vysokými, tak i nízkými příjmy na obyvatele, i když absolutní riziko úmrtí na peripartální krvácení v zemích s vysokými příjmy je mnohonásobně nižší.
Pro snížení rizika PPH u všech vaginálních porodů ve III. době porodní a po vybavení plodu při porodu císařským řezem, byl dosud lékem první volby intravenózně nebo intermuskulárně aplikovaný oxytocin. Od druhé poloviny 90. let minulého století se v klinické medicíně ke stejným účelům stále častěji uplatňuje carbetocin. Mechanismus účinku obou peptidů je stejný, ve III. době porodní (porod placenty) zvyšují stažení (retrakci) dělohy, a tím působí proti hypotonii nebo dokonce atonii dělohy, což bývá až v 80 % příčinou peripartálního život ohrožujícího krvácení (podle definice se jedná o krevní ztrátu vyšší než 1 500 ml krve matky). Ve srovnání s oxytocinem je výraznou předností carbetocinu, jako uterotonika v této kritické porodnické situaci, jeho podstatně delší eliminační poločas (přibližně 8krát u netěhotných žen [48], 10 - až 20krát 24–48 hodin post partum [49]). Má tudíž mnohem delší účinek než oxytocin. Podává se pouze intravenózně, rychlostí 100 μg během jedné minuty. V případě carbetocinu nejsou přitom popisovány závažné vedlejší účinky.
V důsledku neúplného patentového chránění carbetocinu jako substance produkuje od počátku 21. století několik firem na jeho bázi i veterinární léčiva (Depotocin®: Veyx Pharma, Germany; WDT, Germany; Veyx-Pharma, Netherlands a Tettnang, Baden-Württemberg, BRD; Decomoton®: Calier Polska; Laboratorios Calier SA, Barcelona; atd.) o. Ferring AB však zůstává nejvýznamnějším distributorem jeho lékových forem (pod různými jményp) pro humánní medicínu.
Carbetocin, navržený a poprvé syntetizovaný v laboratoři Karla Jošta na pražském Ústavu organické chemie a biochemie, se tak stal dík úzké spolupráci se švédskou firmou účinným, často používaným lékem v kritických porodnických stavech.
Sources
1. Pliska V., Pařízek A., Flegel M.: Chem. Listy 116, 19 (2022).
2. Pliska V., Pařízek A., Flegel M.: Chem. Listy 113, 675 (2019).
3. Huguenin R. L., Boissonnas R. A.: Helv. Chim. Acta 49, 695 (1966).
4. Sawyer W. H., Acosta M., Balaspiri L., Judd J., Manning M.: Endocrinology 94, 1106 (1974).
5. Manning M., Balaspiri L., Moehring J., Haidar J. H. S. W.: J. Med. Chem. 19, 842 (1976).
6. Zaoral M., Kolc J., Šorm F.: Collect. Czech. Chem. Commun. 32, 1242 (1967).
7. Zaoral M., Kolc J., Šorm F.: Collect. Czech. Chem. Commun. 32, 1250 (1967).
8. Pliška V., Krejčí I.: Arch. Int. Pharmacodyn. 161, 289 (1966).
9. Vávra I., Machová A., Krejčí I.: J. Pharmacol. Exp. Ther. 188, 241 (1974).
10. Vávra I., Machová A., Holeček V., Cort J. H., Zaoral M., Šorm F.: Lancet 291, 948 (1968).
11. Burn J. H.: Quart. J. Pharm. Pharmacol. 4, 517 (1931).
12. Pliška V., Rychlík I.: Acta Endocrinol. 54, 129 (1967).
13. Sawyer W. H.: Endocrinology 63, 694 (1958).
14. Pliška V.: Arzneim. Forsch. 16, 886 (1966).
15. Kimura T., Yokoyama R.: Tohoku J. Exp. Med. 109, 281 (1973).
16. Zaoral M., Vavra I., Machova A., Sorm F.: US Patent: US 3497491 DA (1970).
17. Cash J. D., Gader A. M., da Costa J.: Br. J. Haematol. 27, 363 (1974).
18. Prowse C. V., Sas G., Gader A. M. A., Cort J. H., Cash J. D.: Br. J. Haematol. 41, 437 (1979).
19. Mannucci P. M., Ruggeri Z. M., Pareti F. I., Capitanio A.: Lancet 310, 1171 (1977).
20. Mannucci P. M., Ruggeri Z. M., Pareti F. I., Capitanio A.: Lancet 309, 869 (1977).
21. Jošt K., Procházka Z., Cort J. H., Barth T., Škopková J., Prusík Z., Šorm F.: Collect. Czech. Chem. Commun. 39, 2835 (1974).
22. Kynčl J., Řežábek K., Kasafirek E., Pliška V., Rudinger J.: Eur. J. Pharmacol. 28, 294 (1974).
23. Rudinger J., Pliška V., Krejčí I.: Rec. Prog. Hormone Res. 28, 131 (1972).
24. Pliška V., Chard T., Rudinger J., Forsling M. L.: Acta Endocrinol. 81, 474 (1976).
25. Kasafirek E., Rábek V., Rudinger J., Šorm F.: Collect. Czech. Chem. Commun. 31, 4581 (1966).
26. Zaoral M., Pliška V., Řežábek K., Šorm F.: Collect. Czech. Chem. Commun. 28, 747 (1963).
27. Zaoral M., Šorm F.: Collect. Czech. Chem. Commun. 30, 2812 (1965).
28. Jošt K., Rudinger J., Šorm F.: Collect. Czech. Chem. Commun. 28, 2021 (1963).
29. Beranková-Ksandrová Z., Bisset G. W., Jošt K., Krejčí I., Pliska V., Rudinger J., Rychlík I., F. Š.: Br. J. Pharmacol. 26, 615 (1966).
30. Cort J. H., Hammer J., Ulrych M., Píša Z., Douša T., Rudinger J.: Lancet 284, 840 (1964).
31. Rabøl A., Juhl E., Schmidt A., Winkler K.: Digestion 14, 285 (1976).
32. Döhler K. D., Meyer M.: Best Pract. Res., Clin. Anaesthesiol. 22, 335 (2008).
33. Kam P. C. A., Williams S., Yoong F. F. Y.: Anaesthesia 59, 993 (2004).
34. Jošt K., Barth T., Krejčí I., Šorm F.: CS Patent: CS-149028 B1 (1973).
35. Frič I., Kodíček M., Jošt K., Bláha K.: Collect. Czech. Chem. Commun. 39, 1271 (1974).
36. Engstrøm T., Barth T., Melin P., Vilhardt H.: Eur J. Pharmacol. 355, 203 (1998).
37. Barth T., Slaninová J., Lebl M., Jošt K.: Collect. Czech. Chem. Commun. 45, 3045 (1980).
38. Rudinger J., Krejčí I., v knize: Neurohypophysial Hormones and Similar Polypeptides (Berde B., ed.), str. 748. Springer Verlag, Berlin 1968.
39. Krejčí I., Poláček I., Rudinger J.: Br. J. Pharmacol. Chemotherapy 30, 506 (1967).
40. Jošt K., Šorm F.: Collect. Czech. Chem. Commun. 36, 297 (1971).
41. Jost K., Pliska V., Krejcí I., Sorm F.: US Patent: US 3,752,799 (1973).
42. Krejčí I., Kupková B., Barth T., Jošt K.: Physiol. Bohemoslov. 22, 315 (1973).
43. Melin P., Trojnar J., Johansson B., Vilhardt H., Åkerlund M.: J. Endocr. 111, 125 (1986).
44. Åkerlund M., Carlsson A. M., Melin P., Trojnar J.: Acta Obstet. Gynecol. Scand. 64, 499 (1985).
45. Věžník Z., Holub A., Zralý Z., Kummer V., Holčák V., Jošt K., Cort J. H.: Am. J. Vet. Res. 40, 425 (1979).
46. Cort N., Einarsson S., Viring S.: Am. J. Vet. Res. 40, 430 (1979).
47. Bajcsy Á. C., Szenci O., van der Weijden G. C., Door-nenbal A., Maassen F., Bartyik J., Taverne M. A. M.: Theriogenology 65, 400 (2006).
48. Sweeney G., Holbrook A. M., Levine M., Yip M., Alfredsson K., Cappi S., Ohlin M., Schulz P., Wassenaar W.: Curr. Ther. Res. 47, 528 (1990).
49. Hunter D. J. S., Schulz P., Wassernaar W.: Clin. Pharmacol. Ther. 52, 60 (1992).
50. Barth T., Pliška V., Rychlík I.: Collect. Czech. Chem. Commun. 32, 1058 (1967).
51. Barth T., Hütter H. J., Pliska V., Šorm F.: Experientia 25, 646 (1969).
52. Glass J. D., Dubois B. M., Schwartz I. L., Walter R.: Endocrinology 87, 730 (1970).
53. Walter R., Schlank H., Glass J. D., Schwartz I. L., Kerenyi T. D.: Science 173, 827 (1971).
54. Yoshimoto T., Orlowski R. C., Walter R.: Biochemistry 16, 2942 (1977).
* † 15. 7. 2021. Nekrolog dr. Flegela viz Drašar P.: Chem. Listy 115, 575 (2021).
a Po likvidaci RVHP počátkem 90. let bylo toto omezení bezpředmětné a firma FERRING rozšířila činnost celosvětově.
b Mezinárodní jednotka (IU) oxytocinu je nově definována jako uterotonická aktivita 1,68 μg mezinárodního standardu NIBSC (National Institute for Biological Standards and Control); viz https: //www.nibsc.org/documents/ifu/76-575.pdf. V přepočtu: 1 mg (nového) mezinárodního standardu (ca. 10–6 mol oxytocinu) = 595 IU. Starý standard (lyofilizované hovězí neurohypofýzy) uváděl 500 IU.
c U klinických případů popsaných v tehdejších sděleních šlo velmi pravděpodobně o neurogenní (centrální) formu žíznivky (d.i.centralis). U její renální formy (d.i. renalis), nezávislé na plasmatické koncentraci vasopressinu, jde zpravidla o mutaci genu vasopressinového receptoru V2R či jeho celulární signální dráhy.
d Později Výzkumný ústav pro farmacii a biochemii (VÚFB); na testování se podílela Laboratoř endokrinologie III. interní kliniky všeobecné fakultní nemocnice v Praze.
e Přepočteno z dat ve zmíněných publikacích. Data z VÚFB pro anestetizovanou krysu jsou vztaženy na tehdejší mezinárodní standard, pituitrin (extrakt z hovězí neurohypofýzy), po přepočtu ~31 560 IU/mg; v pokusech na neanestetizovaných krysách (standard: syntetický 8-lysin-vasopressin – LVP) ~25 000 až 50 000 IU/mg.
f Polytechna (dnes: Polytechna Consulting, a. s.) byl státní podnik zahraničního obchodu, který zprostředkovával též výměnné zdravotnické služby, včetně lidské síly v zahraničí. Jeden z autorů (A.P.) upozorňuje na údaje kolegů-lékařů, kteří zprostředkováním Polytechny odjížděli pracovat např. na Maltu nebo do severní Afriky: Polytechna si přivlastňovala velkou část jejich výdělků. Na druhé straně bylo známo, že ten, kdo vyjel prostřednictvím Polytechny, byl podezřelý ze spolupráce s vládními a stranickými špionážními složkami (KSČ a STB).
g Pro zajímavost: dDAVP pronikl, byť epizodicky, i do současné anglické beletrie; viz Barbara Vine: The Blood Doctor, Viking – Penguin Random House, London 2002.
h Generikum pod názvem DURATOCIN.
i pA2: negativní dekadický logaritmus molární koncentrace antagonisty redukující efekt E libovolné koncentace agonisty na polovinu, E/2.
j Tractocile®, FERRING Pharmaceuticals A/S.
k Státní orgán povolující užití léčiv a poživatin v U.S.A. Její rozhodnutí jsou téměř universálně přebírána i mimo U.S.A..
l https: //de.wikipedia.org/wiki/Drug_Master_File.
m Autor tohoto sdělení není totožný s J. H. Cortem (Joseph Henry Cort): Nicholas Cort, PhD, DVM, Department of Obstetrics & Gyneacology, College of Veterinary Medicine, Swedish University of Agricultural Sciences, Uppsala, je uváděn jako Senior research scientist ve FERRING Pharmaceuticals. Autorům není známo, zda je v příbuzenském poměru s J. H. Cortem.
n https: / / www.wikiskripta.eu/ w/ Decidua.
o Přehled firem: https: / / www.drugs.com/ international/ carbetocin.html.
p Lonactene®, Duratocin®, Pabal®, Duratobal®.
128 08 Praha 2
michael.fanta@vfn.cz
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inCzech Gynaecology

2025 Issue 2-
All articles in this issue
- Porovnání perinatálních výsledků u porodů indukovaných pomocí perorálního misoprostolu, vaginálního misoprostolu a intracervikálního dinoprostonu
- Ergoterapie v onkogynekologii – pilotní studie
- Vyšetření sérových hladin fénixinu-14 a fénixinu-20 u těhotných žen s preeklampsií
- Analýza epidemiologického, klinického, laboratorního, ultrasonografi ckého a anatomicko-patologického profilu žen s hydatidiformní molou ve dvou referenčních centrech v severovýchodní Brazílii
- Řešení různých typů ektopické gravidity – dotazníková studie
- Spokojenost pacientek s novou metodou elektronického vyplňování validovaných urogynekologických dotazníků
- Nodul sestry Marie Josefy – vzácná kožní metastáza v umbiliku
- Nízkoobjemové postižení regionálních lymfatických uzlin u karcinomu endometria – 2024 update
- Skleroterapie endometriomu a její vliv na ovariální rezervu – narativní přehled
- Molekulární mechanizmy účastnící se rozvoje fibrózy u endometriózy
- Neurohypofyzární peptidy v lékařství z pražských a švédských laboratoří. Část 2: Desmopressin, terlipressin, carbetocin – farmakologie a klinické aplikace
- Czech Gynaecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Porovnání perinatálních výsledků u porodů indukovaných pomocí perorálního misoprostolu, vaginálního misoprostolu a intracervikálního dinoprostonu
- Nodul sestry Marie Josefy – vzácná kožní metastáza v umbiliku
- Ergoterapie v onkogynekologii – pilotní studie
- Skleroterapie endometriomu a její vliv na ovariální rezervu – narativní přehled
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


