-
Medical journals
- Career
Súčasný výskyt BCR:: ABL1 pozitívnej chronickej myelocytovej leukémie a Ph-negatívneho myeloproliferatívneho ochorenia
Authors: K. Slezáková 1; Z. Sninská 1; A. Bátorová 1; A. Žákovičová 2; R. Lukačková 2; Ľ. Majerová 2; J. Marcinek 3; P. Szépe 3; L. Plank 3; K. Rejleková 4
Authors‘ workplace: Klinika hematológie a transfúziológie LFUK a UNB 1; Medirex a. s. 2; Univerzitná nemocnica Martin 3; II. onkologická klinika LF UK a NOÚ 4
Published in: Transfuze Hematol. dnes,32, 2026, No. 1, p. 48-53.
Category: Case Reports
doi: https://doi.org/10.48095/cctahd202607Overview
Chronická myelocytová leukémia (CML) sa vďaka liečbe inhibítormi tyrozinkináz (TKI) stala za posledné dve desaťročia dobre liečiteľným onkohematologickým ochorením pre väčšinu našich pacientov. Ich celkové prežívanie je porovnateľné s prežívaním tzv. bežnej populácie a CML je príčinou úmrtia len malej skupiny pacientov, ktorí sú rezistentní na viaceré TKI. Priaznivú prognózu pacientov s CML však môže okrem rezistencie na TKI negatívne ovplyvniť sekundárne malígne ochorenie alebo duplicitné klonálne ochorenie kostnej drene. V našom príspevku prezentujeme tri prípady pacientov s CML, u ktorých bolo diagnostikované aj Ph negatívne myeloproliferatívne ochorenie. Okrem našich skúseností s manažmentom týchto pacientov sa v článku zaoberáme aj prehľadom literatúry s touto problematikou.
Klíčová slova:
myelofibróza – chronická myelocytová leukémia – inhibítory tyrozinkinázy – ruxolitinib – splenomegália
ÚVOD
Myeloproliferatívne neoplázie (MPN) sú klonálne ochorenia kostnej drene, ktoré pochádzajú z kmeňovej krvotvornej bunky a prejavujú sa zvýšenou proliferáciou buniek myeloidnej línie [1]. Podľa WHO klasifikácie z roku 2022 patria medzi MPN chronická myelocytová leukémia, esenciálna trombocytémia (ET), polycytémia vera (PV), primárna myelofibróza, (PMF) ako aj zriedkavé ochorenia ako chronická neutrofilová leukémia, chronická eozinofilová leukémia, juvenilná myelomonocytová leukémia a inak nešpecifikované myeloproliferatívne neoplázie [2]. Diagnostika myeloproliferatívnych ochorení sa okrem klinického a hematologického laboratórneho nálezu opiera o molekulovo-genetické, cytogenetické a histologické vyšetrenie kostnej drene.
Pre definíciu BCR:: ABL1 pozitívnej chro - nickej myelocytovej leukémie (CML) je nevyhnutné potvrdenie Ph chromozómu a/alebo BCR:: ABL1 fúzneho génu. Najčastejšími príznakmi CML sú bolesti brucha pri splenomegálii, únava, zhoršenie fyzickej kondície, chudnutie a v zriedkavých prípadoch pri extrémnej hyperleukocytóze aj prejavy hyperviskozity (zhoršenie videnia, bolesti hlavy, dýchavičnosť). Incidencia CML sa pohybuje od 0,7–1,0 prípadov na 100 000 obyvateľov [3]. CML predstavuje približne 15 % leukémií. Prevalencia CML stúpa s úspešnosťou liečby inhibítormi tyrozinkináz (TKI). Vďaka liečbe TKI sa v priebehu posledných dvoch desaťročí prognóza pacientov s CML dramaticky zlepšila. Ich prežívanie je podobné prežívaniu tzv. bežnej populácie. Hoci v súčasnosti dochádza k progresii CML do blastovej fázy len u cca 5 % pacientov, naďalej ide o situáciu s mimoriadne nepriaznivou prognózou [4]. Dobrú prognózu a kvalitu života pacientov s CML však môže negatívne ovplyvniť vznik duplicitného malígneho ochorenia či sekundárnej klonálnej evolúcie v kostnej dreni.
Ph negatívne MPN sú vo väčšine prípadov charakterizované prítomnosťou mutácie v tzv. driver génoch JAK2, CALR alebo MPL, pričom u väčšiny pacientov dokazujeme len jednu z týchto mutácií. Pre diagnózu Ph negatívnej MPN však nie je stanovenie mutácie v tzv. driver géne nevyhnutným diagnostickým kritériom [2]. Približne 10 % pacientov totiž nemá prítomnú ani jednu z týchto MPN špecifických driver mutácií a označujeme ich ako tzv. triple negatívnych [5]. Mutácia v géne JAK2 je prítomná u viac ako 95 % pacientov s diagnózou PV, pričom najčastejšie ide o mutáciu V617F v exóne 14 (97 % pacientov) [6]. Mutácia V617F býva prítomná aj u cca 50 % pacientov s diagnózou ET a PMF. U približne 30 % pacientov s ET a PMF bez mutácie v JAK2 géne dokazujeme prítomnosť mutácie CALR génu a u 4–8 % pacientov mutáciu v onkogéne MPL [7,8]. Prognostický význam môže mať vyšetrenie tzv. non driver mutácií, ktoré nie sú špecifické len pre Ph negatívne myeloproliferatívne ochorenia, ale aj pre manažment pacientov s akútnou myeloblastovou leukémiou. Vyšetrujú sa metódami sekvenovania novej generácie (NGS) a medzi tie, ktoré sú asociované s horšou prognózou patria mutácie v géne pre ASXL1, EZH2, IDH1 a IDH2, SRSF2 a U2AF1. Ich vyšetrenie je súčasťou aj prognostických kalkulátorov pacientov s myelofibrózou (MIPPS70 a MIPPS70+) a prispieva napr. k indikácii vysokorizikového pacienta do alogénnej transplantácie krvotvorných kmeňových buniek [9,10].
Súčasný výskyt BCR:: ABL1 pozitívnej CML a Ph negatívneho MPN je zriedkavý. V literatúre však boli publikované prípady Ph pozitívnej CML a JAK2-mutovaného myeloproliferatívneho ochorenia vo frekvencii 0,2–2,5 % [11]. Retrospektívnej analýze a prehľadu literatúry pacientov s diagnózou BCR:: ABL1 pozitívnej CML a MPN s mutáciou CALR sa venuje kolektív autorov v práci publikovanej v roku 2024 v časopise Frontiers in Cell and Developmental Biology [12]. Okrem prezentácie vlastného prípadu pacienta s CALR typ 1 pozitívnou primárnou myelofibrózou v prefibrotickom štádiu, u ktorého sa po 11 rokoch cytoredukčnej liečby diagnostikovala BCR:: ABL1 pozitívna CML, sa autori podrobne venujú ďalším 23 prípadom získaným z prehľadu literatúry. Pri diagnostike kladú okrem stanovenia BCR:: ABL1 fúzneho génu a mutácií v génoch JAK2, CALR a MPL dôraz aj dôležitosť podrobného histologického vyšetrenie kostnej drene. V rámci histologického zhodnotenia je okrem posúdenia stupňa fibrózy, zastúpenia blastických elementov dôležité aj zhodnotenie morfológie megakaryocytov. Pri CML pozorujeme menšie, tzv. trpaslíčie formy, kým u pacientov s Ph negatívnou MPN sa v kostnej dreni vyskytujú skôr väčšie zhluky megakaryocytov. Problémom pacientov so súbežným výskytom Ph pozitívnej CML a Ph negatívnej MPN môže byť aj genetická nestabilita a tendencia k progresívnemu vývoju fibrózy s nie priaznivou prognózou.
Existujú tri možné „scenáre“ tejto situácie: vývoj Ph negatívneho myeloproliferatívneho ochorenia u pacienta so známou CML, stanovenie diagnózy CML v priebehu liečby myeloproliferatívneho ochorenia alebo súčasné diagnostikovanie oboch ochorení. V dostupnej odbornej literatúre sú publikované práce menších súborov pacientov, ale väčšinou len kazuistík takýchto prípadov. Spracovali sme prehľad literatúry s touto problematikou a uvádzame tri kazuistiky pacientov so súčasným výskytom BCR:: ABL1 pozitívnej CML a Ph negatívneho myeloproliferatívneho ochorenia z pracoviska Kliniky hematológie a transfúziológie LFUK a UNB.
KAZUISTIKA 1
V prvej kazuistike uvádzame prípad pacienta s diagnózou CML, ktorá mu bola stanovená v roku 2006 ako 58 ročnému v nízkom riziku podľa Sokala s transkriptom e14a2 (zlom b3a2). Cytogenetický nález kostnej drene okrem dôkazu Ph chromozómu bol v norme. Histologické vyšetrenie kostnej drene ani vyšetrenie mutácie V617F v JAK2 géne nebolo v úvode diagnózy realizované. Pacient mal v krvnom obraze leukocytózu 64×109/l s typickým posunom k mladším vývojovým elementom granulopoézy a bazofíliou (8 %). Zastúpenie blastov v periférnej krvi bolo 2 %. Pacient mal aj anémiu (Hb 83 g/l) a miernu trombocytózu (514×109/l). Pacient bol liečený imatinibom v štandardnej dávke 400 mg denne s dosiahnutím kompletnej hematologickej remisie s normalizáciou anémie a následne aj stabilnej optimálnej liečebnej odpovede až na úroveň MR5 (BCR:: ABL1 0 % IS). Po ôsmich rokoch efektívnej terapie imatinibom sme však zaznamenali postupný vznik normocytovej normochrómnej anémie, ktorá sa prehĺbila až na úroveň ťažkého stupňa s potrebou podávania transfúzií erytrocytov. Spočiatku sme ako príčinu anémie predpokladali hematologickú toxicitu dlhodobej liečby imatinibom a liečbu sme preto v roku 2014 prerušili, avšak bez zlepšenia parametrov červeného krvného obrazu. Po vylúčení sekundárnych príčin anémie (krvácanie zo zažívacieho traktu, urologické vyšetrenie) sme v rámci diferenciálnej diagnostiky realizovali v roku 2017 histologické vyšetrenie kostnej drene so záverom myelofibrózy ťažkého stupňa. Dokázali sme prítomnosť mutácie V617F v JAK2 géne na úrovni 33,3 %. BCR:: ABL1 fúzny gén nebol zistený. Cytogenetickým vyšetrením kostnej drene sme dokázali t (8; 9) v 17 metafázach bez dôkazu Ph chromozómu. V roku 2020 došlo u pacienta k vzniku symptomatickej splenomegálie a preto sme zahájili liečbu ruxolitinibom v dávke 15 mg 2× denne (s ohľadom na trombocytopéniu 102×109/l) s dosiahnutím parciálnej regresie veľkosti sleziny. Podávaním nízkych dávok prednizónu (20 mg denne) a erytropoetínu sme dočasne dosiahli nezávislosť pacienta na podávaní transfúzií erytrocytov. Klinický stav ako aj kvalita života pacienta sa výrazne zlepšili. CML zostávala naďalej v pásme hlbokej molekulovej odpovede na úrovni MR5 (BCR:: ABL1 0 % IS) bez liečby TKI.
V júli roku 2023 bol pacientovi diagnostikovaný karcinóm kože z Merkelových buniek v oblasti zápästia pravej hornej končatiny (obr. č. 1, archív autorky) s metastatickými ložiskami v oblasti axily. Pacientovi bola na pracovisku Národného onkologického ústavu zahájená liečba monoklonálnou protilátkou avelumabom. Absolvoval 11 podaní. V septembri roku 2024 došlo k pomerne náhlemu zhoršeniu klinického stavu pacienta: výrazná progresia splenomegálie, vznik až tenzného ascitu s nutnosťou opakovaných punkcií, prehĺbenie anémie (hemoglobín 70 g/l) a trombocytopénie (48×109/l) na úroveň ťažkého stupňa a vzniku leukocytózy (18×109/l) s vyplavovaním blastov (3 %) a typickým leukoerytroblastovým obrazom. Okrem pretrvávania mutácie V617F v géne JAK2 sme pacientovi v čase progresie ochorenia dokázali aj mutáciu v géne ASXL1. Pacient zomrel v októbri 2024 na akceleráciu myelofibrózy 18 rokov od stanovenia diagnózy CML s pretrvávaním BCR:: ABL1 negativity.
KAZUISTIKA 2
Druhá kazuistika popisuje prípad pacienta, ktorému sme v roku 2017 vo veku 55 rokov diagnostikovali CML vo vysokom riziku podľa Sokala aj ELTS so zlomom e13a2 (b2a2), bez nepriaznivých cytogenetických aberácií v karyotype kostnej drene a súčasne aj myelofibrózu s mutáciou v géne CALR v strednom-2 riziku podľa skórovacieho systému DIPPS plus. Z dôvodu vstupnej stratifikácie pacienta do skupiny pacientov s vysokým rizikom a pri neprítomnosti zásadnej prekážky zo strany pridružených ochorení, sme sa v 1. línii priklonili k liečbe nilotinibom v štandardnej dávke pre 1. líniu 300 mg dvakrát denne. Dasatinib v tom čase nemal úhradu do terapie 1. línie pacientov s CML. Pacient dosiahol podľa ELN odporúčaní pre monitoring liečby pacientov s CML optimálnu liečebnú odpoveď vo všetkých požadovaných míľnikoch a aktuálne v čase písania tohto článku je na úrovni hlbokej molekulovej odpovede MR4. V auguste roku 2022 sme pre progresiu splenomegálie pri myelofibróze zahájili liečbu ruxolitinibom v dávke 10 mg dvakrát denne a súčasne sme redukovali dávku nilotinibu na 300 mg jeden krát denne s udržiavaním molekulovej odpovede v pásme MR3 až MR4. K redukovaným dávkam sme sa priklonili z dôvodu obáv rizika možnej hematologickej toxicity pri súbežnom podávaní nilotinibu a ruxolitinibu. Žiaľ od júla 2024 došlo u pacienta k progresii myelofibrózy v zmysle prehĺbenia anémie na úroveň ťažkého stupňa (Hb < 80 g/l) so vznikom transfúznej závislosti na podávaní erytrocytov ako aj rastu veľkosti sleziny. Počet leukocytov aj trombocytov bol v norme. Blasty v nátere periférnej krvi neboli prítomné. Liečba ruxolitinibom začala strácať efekt. Pacient vzhľadom na novo nadobudnuté pridružené ochorenia (artériová hypertenzia, pľúcna artériová hypertenzia na rozhraní ľahkého až stredne závažného stupňa, anamnéza abúzu alkoholu) nie je vhodným kandidátom na realizáciu alogénnej transplantácie kmeňovými krvotvornými bunkami. Na zváženie je zmena liečby na fedratinib alebo momelotinib, ktoré však v čase písania tohto článku nemajú v Slovenskej republike určenú úhradu zo strany zdravotného poistenia. Vzhľadom na osciláciu molekulovej odpovede medzi úrovňou MR3 a MR4 nezvažujeme u pacienta vysadenie liečby nilotinibom a pokračujeme v podávaní zníženej dávky 300 mg denne.
KAZUISTIKA 3
V tretej kazuistike prezentujeme prípad pacientky s diagnózou CML, ktorá bola stanovená v roku 2012 vo veku jej 60 rokov v nízkom riziku podľa Sokala so zlomom e13a2 (b2a2). Vstupne bola prítomná leukocytóza 54,49×109/l s typickou bazofíliou (3 %), s vyplavovaním myelocytov a metamyelocytov do periférnej krvi, bez prítomnosti blastických buniek. Hemoglobín a počet trombocytov bol v norme. Splenomegália prítomná nebola. Pacientka bola liečená v 1. línii imatinibom v dávke 400 mg denne s dosiahnutím optimálnej liečebnej odpovede vo všetkých míľnikoch odporúčaní. V roku 2020 sme pre opakovaný záchyt miernej trombocytózy (okolo 500×109/l) realizovali diferenciálne diagnostický proces a zistili prítomnosť mutácie V617F v JAK2 géne. Počet leukocytov, erytrocytov a hemoglobínu bol v norme ako aj enzýmu LDH a erytropoetínu (12,70 mU/ml). BCR:: ABL1 transkript vo vzorke periférnej krvi nebol detekovaný (BCR:: ABL1 0 %). Karyotyp kostnej drene bol v norme. Doplnili sme histologické vyšetrenie kostnej drene so záverom myeloproliferatívneho ochorenia typu ET. Pacientka okrem antiagregačnej profylaxie doposiaľ nevyžaduje cytoredukčnú liečbu. Je v observácii bez akýchkoľvek symptómov a komplikácií zo strany ET.
V roku 2022 sme v štádiu hlbokej molekulovej odpovede na úrovni MR4,5 liečbu imatinibom prerušili v rámci pokusu o remisiu bez liečby (treatment free remission – TFR). Po necelých 2 mesiacoch prerušenia terapie došlo k včasnému vzostupu BCR:: ABL1 transkriptu v periférnej krvi na úroveň MR3. Vrátili sme sa preto k liečbe imatinibom s rýchlym dosiahnutím molekulovo nedetekovateľnej leukémie (BCR:: ABL1 0 % IS).
DISKUSIA
Do skupiny myeloproliferatívnych ochorení patrí BCR:: ABL1 pozitívna CML a Ph negatívne MPN. Pre diagnózu BCR:: ABL1 pozitívnej CML je kľúčový Ph chromozóm a BCR:: ABL1 fúzny gén, ktorý je zodpovedný za konštitutívnu tyrozinkinázovú aktivitu. V patogenéze Ph negatívnych MPN je zásadná prítomnosť mutácie v génoch JAK2, CALR alebo MPL. Ich súčasná prítomnosť u jedného pacienta je veľmi vzácna. Približne 10 % pacientov s ET a myelofibrózou môže byť tzv. triple negatívnych (mutácie v géne JAK2, CALR a MPL nie sú prítomné). U malého percenta pacientov s Ph negatívnym myeloproliferatívnym ochorením sa môžeme stretnúť s koexistenciou mutácie v géne pre CALR a MPL. Tzv. „duálne“ myeloproligeratívne ochorenie (BCR:: ABL1 pozitívna CML + Ph negatívna MPN) zatiaľ nie je súčasťou WHO klasifikácie myeloproliferatívnych ochorení a v literatúre sú dostupné údaje prevažne malých súborov a kazuistík. BCR:: ABL1 fúzny gén a mutácia v génoch JAK2, CALR a MPL môžu byť súčasťou jedného klonu alebo nezávislých klonov buniek a môžu sa prejaviť v sekvencii v rámci komplexného procesu [13]. V klinickom a hematologickom laboratórnom náleze sa môžu následne „prekrývať“ črty CML a Ph negatívnej MPN. V literatúre boli publikované aj nálezy mutácie V617F génu JAK2 ako súčasť CHIP (clonal hematopoiesis of indeterminate potential), bez klinických či laboratórnych prejavov Ph negatívneho myeloproliferatívneho ochorenia. Prevalencia CHIP u ľudí vo veku 50–60 rokov je okolo 5 % [14].
Podľa údajov z registra MPN pacientov v Johns Hopkins Hospital v Baltimore bol zaznamenaný 0,6% výskyt BCR:: ABL1 pozitívnej CML u pacientov s Ph negatívnym myeloproliferatívnym ochorením. CML sa u týchto pacientov diagnostikovala v rozpätí od 10 do 36 rokov od stanovenia diagnózy Ph negatívnej MPN (15). V práci kolektívu autorov z univerzity v Pensylvánii sa uvádza 0,4% frekvencia súčasnej pozitivity BCR:: ABL1 fúzneho génu a mutácie V617F v géne JAK2 pozitivity pri analýze 1570 pacientov s diagnózou MPN. Išlo o 11 pacientov, z ktorých u siedmych sa potvrdila myelofibróza [11].
Zaujímavý klinický prípad bol publikovaný kolektívom autorov z hematologického pracoviska v Gdansku. Zdieľajú kazuistiku pacienta s diagnózou primárnej myelofibrózy s mutáciami génov CALR a AXL1, u ktorého vznikla CML 13 rokov od stanovenia diagnózy PMF [16]. Pacient bol súčasne liečený TKI inhibítorom a ruxolitinibom podobne ako náš pacient z druhej kazuistiky.
Retrospektívnej analýze súčasného výskytu MPN s mutáciou génu CALR pozitívnej a BCR:: ABL1 pozitívnej CML sa venuje práca talianskeho kolektívu autorov z univerzity v Bologni, ktorí spracovali 23 prípadov z literatúry a podrobnejšie sa venujú prípadu pacienta s pozitívnou myelofibrózou v prefibrotickom štádiu s mutáciou génu CALR, ktorému bola diagnostikovaná BCR:: ABL1 pozitívna CML po 11 rokoch od stanovenia prvotnej diagnózy [12]. Pacient bol liečený nilotinibom a súčasne aj ruxolitinibom, podobne ako náš pacient z kazuistiky č. 2.
Ruxolitinib je selektívny inhibítor JAK 1 a JAK 2 kináz. Je indikovaný u pacientov so symptomatickou PMF a u pacientov s PV, ktorým zlyhala liečba hydroxykarbamidom. Jeho benefit v manažmente pacientov s týmito diagnózami je nepopierateľný a dokázali to viaceré medzinárodné randomizované klinické štúdie (napr. klinická štúdia RESPONSE, COMFORT-I a COMFORT-II) ako aj retrospektívne analýzy súborov pacientov z tzv. bežnej klinickej praxe [17–19]. Kľúčovým benefitom liečby ruxolitinibom je nielen zmenšenie splenomegálie a ústup príznakov ochorenia, ale aj zlepšenie celkového prežívania a kvality života pacientov. Úskalím liečby ruxolitinibom je okrem známej a väčšinou dobre manažovatelnej myelosupresie aj zvýšený výskyt nemelanómových kožných nádorov. V klinickej štúdii COMFORT-II bol 17,1 % výskyt nemelanómových kožných karcinómov u pacientov v ramene s ruxolitinibom v porovnaní 2,7 % výskytom v ramene pacientov liečených podpornou terapiou [20]. Najčastejšie ide o bazocelulárny a skvamocelulárny karcinóm [21]. Pred zahájením liečby, ako aj v pravidelných intervaloch počas terapie ruxolitinibom, sa odporúčajú pravidelné dermatologické prehliadky a edukácia pacienta.
Karcinóm z Merkelových buniek (Merkel cell carcinoma – MCC) je primárny neuroendokrinný nádor kože, ktorého výskyt je relatívne vzácny. Najčastejšie postihuje tie oblasti kože, ktoré sú vystavené intenzívnejšej expozícii slnečnému žiareniu, ako napr. tvár, krk a končatiny [22, 23]. Ide o nádor s agresívnym správaním a rýchlym rastom, a je druhou najčastejšou príčinou úmrtí zo skupiny kožných nádorových ochorení. Klinicky sa prejavuje ako nodulárny útvar červenofialovej farby, ktorý môže na povrchu exulcerovať (viď obr. 1, archív autorky). V tejto forme sme ho pri pravidelnej kontrole „zachytili“ u nášho pacienta z kazuistiky č. 1. Ide o prvý prípad MCC u pacienta liečeného ruxolitinibom na našom pracovisku. Podľa údajov z odbornej literatúry sa MCC vyskytuje častejšie u imunosuprimovaných pacientov a imunosupresia je jeden z hlavných rizikových faktorov vzniku tohto kožného nádoru [24].
Image 1. Karcinóm kože z Merkelových buniek (archív autorky). 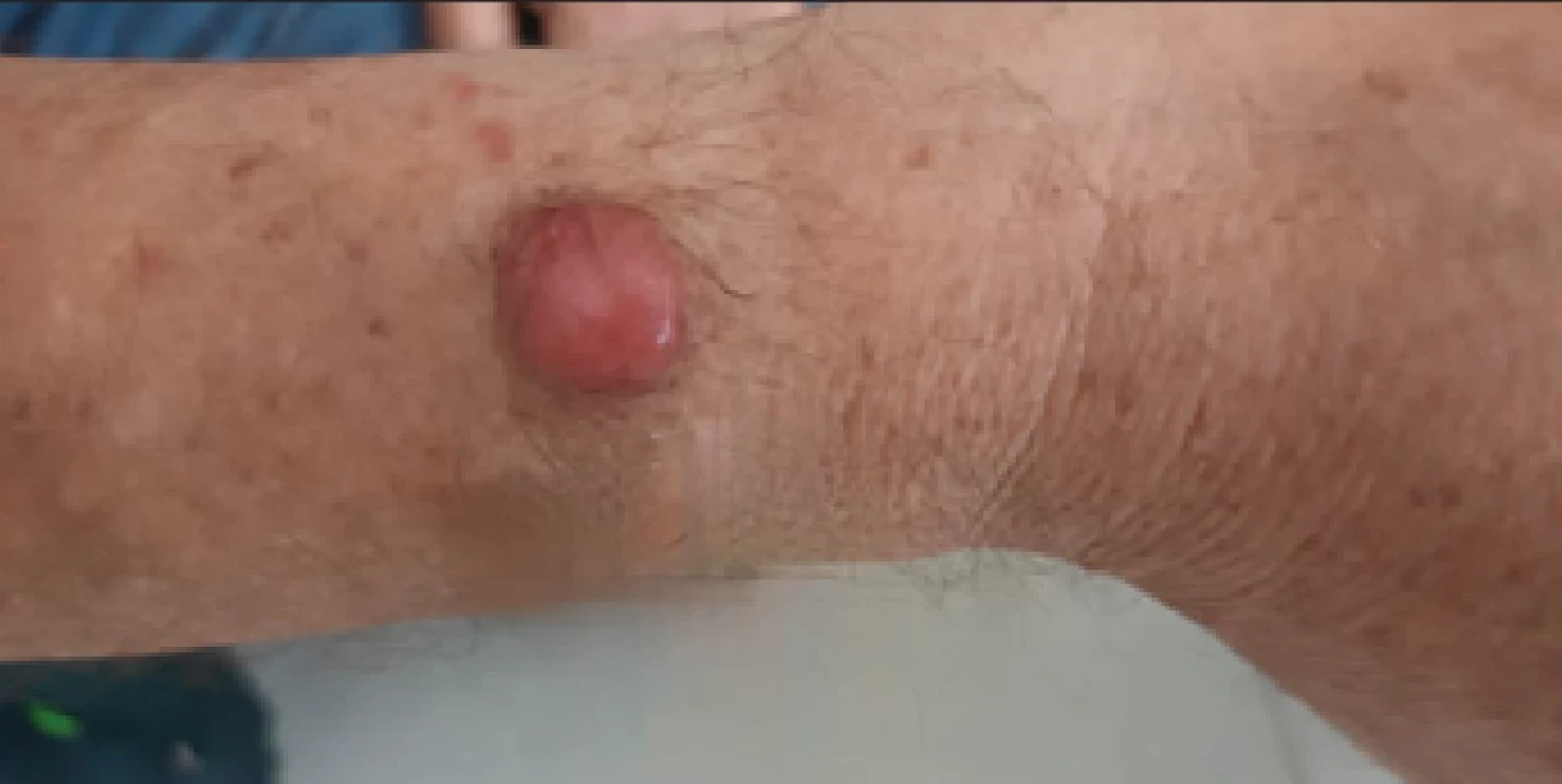
Pacientom s CML a myelofibrózou je možné podávať TKI v kombinácii s ruxolitinibom. Pri súbežnom podávaní inhibítorov tyrozínkinázy a ruxolitinibu však nesmieme zabúdať na možné liekové interakcie. Interakcia medzi imatinibom, nilotinibom a ruxolitinibom však nie je klinicky signifikantná (podľa Drug Interaction Checker, k dispozícii na www.drugs.com) [25]. Klinicky významnejšia je lieková interakcia medzi dasatinibom, ponatinibom a ruxolitinibom, najmä v súvislosti so zvýšeným rizikom možného krvácania pri trombocytopénii, ktorá sa môže pri tejto kombinácii liekov objaviť ako prejav hematologickej toxicity. Na zvýšenom riziku krvácania sa môže podieľať aj dysfunkcia trombocytov, ktorá bola dokázaná in vitro pri terapii dasatinibom [26]. Za účelom redukcie rizika farmakologickej toxicity je na zváženie modifikácia dávky ruxolitinibu alebo TKI v závislosti na konkrétnom prípade a aktuálnych parametroch krvného obrazu. Pri užívaní týchto liekov nesmie pacient konzumovať grapefruit ani produkty či nápoje s obsahom tohto ovocia.
ZÁVER
Súčasný výskyt CML a Ph negatívneho MPN je zriedkavý. Na túto situáciu však treba myslieť najmä u pacientov s CML, ktorí počas liečby TKI vyvinú nezvyčajne dlhú cytopéniu, alebo u nich napriek dôkazu optimálnej molekulovej odpovede zaznamenáme vznik splenomegálie, erytrocytózy, trombocytózy, alebo prítomnosť menej zrelých foriem granulocytov v periférnej krvi. Pacientom, ktorí spĺňajú kritériá na remisiu bez liečby, môžeme navrhnúť prerušenie terapie TKI za podmienok pravidelného monitorovania krvného obrazu a BCR:: ABL1 transkriptov v periférnej krvi [27]. V ich ďalšom manažmente sa tak môžeme zamerať na liečbu Ph negatívneho MPN.
Pokročilá fibróza kostnej drene môže negatívne ovplyvniť priebeh liečby CML. Problémom sú najmä anémia a trombocytopénia, ktoré môžu limitovať podávanie adekvátnych dávok TKI a zhoršiť liečebnú odpoveď na TKI. Okrem skráteného prežívania dochádza aj k zhoršeniu kvality života pacienta s CML, ktorý musí navštevovať svojho hematológa častejšie ako „bežný“ CML pacient a okrem liečby CML vyžaduje liečbu duplicitného hematologického ochorenia (napr. ruxolitinib, erytropoetín, transfúzie erytrocytov). U pacientov s vysokorizikovou myelofibrózou je zvýšené riziko transformácie ochorenia do sekundárnej AML. Celkové prežívanie tejto skupiny pacientov je krajne nepriaznivé. U vybranej skupiny pacientov je potrebné zvážiť alogénnu transplantáciu krvotvorných kmeňových buniek.
Sources
1. Paz DL, Kralovics R, Skoda RC, et al. Genetic basis and molecular profiling in myeloproliferative neoplasms. Blood. 2023; 141 (16): 1909–1921.
2. Khoury JD, Solary E, Abla O, et al. The 5th edition of the World Health Organisation classification of haematolymfoid tumours: myeloid and histiocytic/dentritic neoplasms. Leukemia. 2022; 36 : 1703–1719.
3. Höglund M, Sandin F, Simonsson B. Epidemiology of chronic myeloid leukemia: an update. Ann Hematol. 2015; 94 (Suppl 2): S241–S247.
4. Brioli A, Lomaia E, Fabisch C, et al. Management and outcome of patients with chronic myeloid leukemia in blast phase in the tyrosine kinase inhibitor era – analysis of the European LeukemiaNet Blast Phase Registry. Leukemia. 2024; 38 : 1072–1080.
5. Kráľová B, Kapraľová Hlušičková K, Divoký V, et al. Nové poznatky v patofyziológii Ph-negatívnych myeloproliferatívnych neoplázií. Transfuze Hematol Dnes. 2021; 27 (3): 208–217.
6. Tefferi A, Barbui T. Polycythemia vera: 2024 update on diagnosis, risk-stratification, and management. Am J Hematol. 2023; 98 (9): 1 456–1487.
7. Elala YC, Lasho TL, Gangat N, et al. Calreticulin variant stratified driver mutational status and prognosis in essential thrombocythemia. Am J Hematol. 2016; 91 : 503–506.
8. Boyd EM, Bench AJ, Goday-Fernandez A, et al. Clinical utility of routine MPL exon 10 analysis in the diagnosis of essential thrombocytaemia and primary myelofibrosis. Br J Haematol. 2010; 149 : 250–257.
9. Vannucchi AM, Lasho TL, Guglielmelli P, et al. Mutations and prognosis in primary myelofibrosis. Leukemia. 2013; 27 : 1861–1869.
10. Tefferi A, Guglielmelli P, Lasho TL, et al. MIPSS70+ version 2.0: mutation and karyotype-enhanced International Prognostic Scoring System for primary myelofibrosis. J Clin Oncol. 2018; 36 (17): 1770–2018.
11. Soderquist CR, Ewalt MD, Czuchlewski DR, et al. Myeloproliferative neoplasms with concurrent BCR-ABL1 translocation and JAK2 V617F mutation: a multi-institutional study from the bone marrow pathology group. Modern Pathol. 2018; 31 : 690–704.
12. Zanelli M, Fragliasso V, Loscocco G, et al. Chronic myeloproliferative neoplasms with concomitant CALR mutation and BCR:: ABL1 translocation: diagnostic and therapeutic implications of a rare hybrid disease. Front Cell Dev Biol. 2024; 12 : 1391078.
13. Lorenzo M, Grille S, Stevenazzi M. Emergence of BCR-ABL1 chronic myeloid leukemia in a JAK-V617F polycythemia vera. J Hematol. 2020; 9 : 23–29.
14. McKerrell T, Park N, Moreno T, et al. Leukemia-associated somatic mutations frive patterns of age-related clonal hemopoiesis. Cell Rep. 2015; 10 : 1239–1245.
15. Hochman MJ, Smith BD, Karantanos T, et al. Chronic myeloid leukemia (CML) evolves from Philadelphia chromosome-negative myeloproliferative neoplasms (MPNs) with unexpected frequency. Int J Hematol. 2023; 117 : 456–462.
16. Sobieralski P, Bieniaszewska M, Leszczyńska A, et al. Secondary chronic myeloid leukemia in a patient with CALR and ASXL1-mutated primary myelofibrosis. Int J Hematol. 2022; 116 (3): 442–445.
17. Verstovsek S, Vanucchi AM, Griesshammer M, et al. Ruxolitinib verzus best available therapy in patients with polycythemia vera: 80-week follow up from the RESPONSE trial. Haematologica. 2016; 101 (7): 821–829.
18. Vestovsek S, Gotlib J, Mesa RA, et al. Long-term survival in patients with myelofibrosis treated with ruxolitinib for myelofibrosis: COMFORT-I and COMFORT-II pooled analyses. J Hematol Oncol. 2017; 10 : 156.
19. Weinbergerová B, Čičátková P, Palová M, et al. Zkušenosti s léčbou ruxolitinibem u pacientů s myelofibrózou a pravou polycytémií na českých hematologických pracovištích. Transfuze Hematol Dnes. 2017; 23 (1): 30–40.
20. Harrison CN, Vannucchi AM, Kiladjian J-J, et al. Long-term findings from Comfort-II, a phase 3 study of ruxolitinib vs best available therapy for myelofibrosis. Leukemia. 2016; 30 : 1701–1707.
21. Rampotas A, Carter-Brzezinsky L, Somervaille T, et al. Outcomes and characteristics of nonmelanoma skin cancers in patients with myeloproliferative neoplasms on ruxolitinib. Blood. 2024; 143 (2): 178–182.
22. Pilotti S, Rilke F, Lombardi L, et al. Neuroendocrine (Merkel cell) carcinoma of the skin. Am J Surg Pathol. 1982; 6 : 243–254.
23. Ratner D, Nelson B, Brown MD, et al. Merkel cell carcinoma. J Am Academ Dermatol. 1993; 29 : 143–156.
24. Paulson KG, Iyer JG, Blom A, et al. Systemic immune suppresion predicts diminished Mercel cell carcinoma-specific survival independent of stage. J Invest Dermatol. 2013; 133 (3): 642–646.
25. Drug Interaction Checker – Find Unsafe Combinations; www.drugs.com
26. Cardama-Quintas A, Han X, Kantarjian H, et al. Dasatinib-induced platelet dysfunction. Blood. 2007; 110 (11): 2941.
27. Hochhaus A, Baccarani M, Silver RT, et al. European LeukemiaNet 2020 recommendations for treating chronic myeloid leukemia. Leukemia. 2020; 34 (4): 966–984.
PODIEL AUTOROV NA PÍSANÍ RUKOPISU
SK – liečba pacientov, písanie rukopisu
SZ – liečba pacientov
BA – revízia rukopisu
ŽA, LR, MĽ – laboratórna diagnostika, monitoring liečby
MJ, SP, PL – histologická diagnostika
ČESTNÉ PREHLÁSENIE
Autori práce prehlasujú, že v súvislosti s témou, prípravou a písaním tohto rukopisu nie sú v konflikte záujmov a práca nebola finančne podporená farmaceutickou spoločnosťou.
Do redakce doručeno dne: 15. 3. 2025.
Přijato po recenzi dne: 12. 8. 2025.
MUDr. Katarína Slezáková, PhD
Klinika hematológie a transfúziológie LFUK
a Univerzitnej nemocnice Bratislava
Antolská 11
851 07 Bratislava
Slovensko
e-mail: slezakova@pe.unb.sk, slezak.katarina@gmail.com
Společnost pro transfuzní lékařství, Česká hematologická společnost, Sekce dětské hematologie České pediatrické společnosti*, Česká společnost pro trombózu a hemostázu, Česká společnost anesteziologie, resuscitace a intenzivní medicíny, Česká společnost intenzivní medicíny, Česká chirurgická společnost, Česká internistická společnost, Česká společnost pro ortopedii a traumatologii, Česká neonatologická společnost, Společnost urgentní medicíny a medicíny katastrof ČLS JEP České lékařské společnosti J. E. Purkyně
Labels
Haematology Internal medicine Clinical oncology
Article was published inTransfusion and Haematology Today
2026 Issue 1-
All articles in this issue
- Venetoklax – základ neintenzivní cílené léčby akutní myeloidní leukémie
- Akutní myeloidní leukémie – jak se změnil přístup v diagnostice, stratifikaci rizika a možnostech léčby
- Venetoklax plus azacitidin jako přemosťující terapie k alogenní transplantaci krvetvorných buněk u nemocných s akutní myeloidní leukémií
- Co můžeme očekávat od léčby venetoklax + azacitidin (VEN+AZA) u pacientů s akutní myeloidní leukémií (AML) – výsledky studie VIALE-A a post-hoc analýz
- Antimykotická profylaxe u pacientů s akutní myeloidní leukémií léčených venetoklaxem s azacytidinem
- Léčba mnohočetného myelomu s projevy choroby z ukládání lehkých řetězců; kompletní remise s negativitou minimální reziduální nemoci po léčbě daratumumabem, dexametazonem a lenalidomidem – popis případu a přehled literatury
- Súčasný výskyt BCR:: ABL1 pozitívnej chronickej myelocytovej leukémie a Ph-negatívneho myeloproliferatívneho ochorenia
- Zásady účelné hemoterapie. Mezioborové konsensuální stanovisko
- Doporučení Společnosti pro transfuzní lékařství ČLS JEP č. STL_20 Vyšetřování chladových protilátek proti erytrocytům u pacientů před kardiochirurgickou operací v mimotělním oběhu
- 18. Střešovický transfuzní den
- Zanubrutinib čtyřikrát jinak v klinické praxi
- Hodgkinův lymfom – klíčová sdělení z ASH 2025
- Transfusion and Haematology Today
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Zásady účelné hemoterapie. Mezioborové konsensuální stanovisko
- Léčba mnohočetného myelomu s projevy choroby z ukládání lehkých řetězců; kompletní remise s negativitou minimální reziduální nemoci po léčbě daratumumabem, dexametazonem a lenalidomidem – popis případu a přehled literatury
- Akutní myeloidní leukémie – jak se změnil přístup v diagnostice, stratifikaci rizika a možnostech léčby
- 18. Střešovický transfuzní den
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

