-
Medical journals
- Career
- Contact
Souhrn doporučení 2023: Diagnostika a léčba mnohočetného myelomu
Published in: Transfuze Hematol. dnes,29, 2023, No. Supplementum 2, p. 10-23.
Category:
A. Diagnostika
Table 1. Přehled vyšetření využívaných v rámci diagnostiky pacienta s mnohočetným myelomem. 
Upraveno a doplněno (dle Kumar, 2016; Munshi, 2017). Table 2. Doporučené formy zápisu výsledků z průtokové cytometrie. 
Table 3. Diagnostická kritéria monoklonální gamapatie nejasného významu (MGUS) (IMWG, 2003; Rajkumar, 2014). 
Table 4. Diagnostická kritéria monoklonální gamapatie nejasného významu s lehkými řetězci (light chain MGUS) (Rajkumar, 2014). 
Table 5. Kritéria solitárního kostního (medulárního) plazmocytomu (modifi kováno dle IMWG, 2003; Rajkumar, 2014). 
Table 6. Kritéria solitárního mimokostního (extramedulárního) plazmocytomu (modifi kováno dle IMWG, 2003; Rajkumar, 2014). 
Table 7. Kritéria solitárního plazmocytomu s minimálním postižením kostní dřeně (Rajkumar, 2014). 
Table 8. Monoklonální gamapatie s klinickým významem (MGCS): mechanizmus vzniku a orgánové postižení (modifi kovaná tabulka dle Stern, 2023). 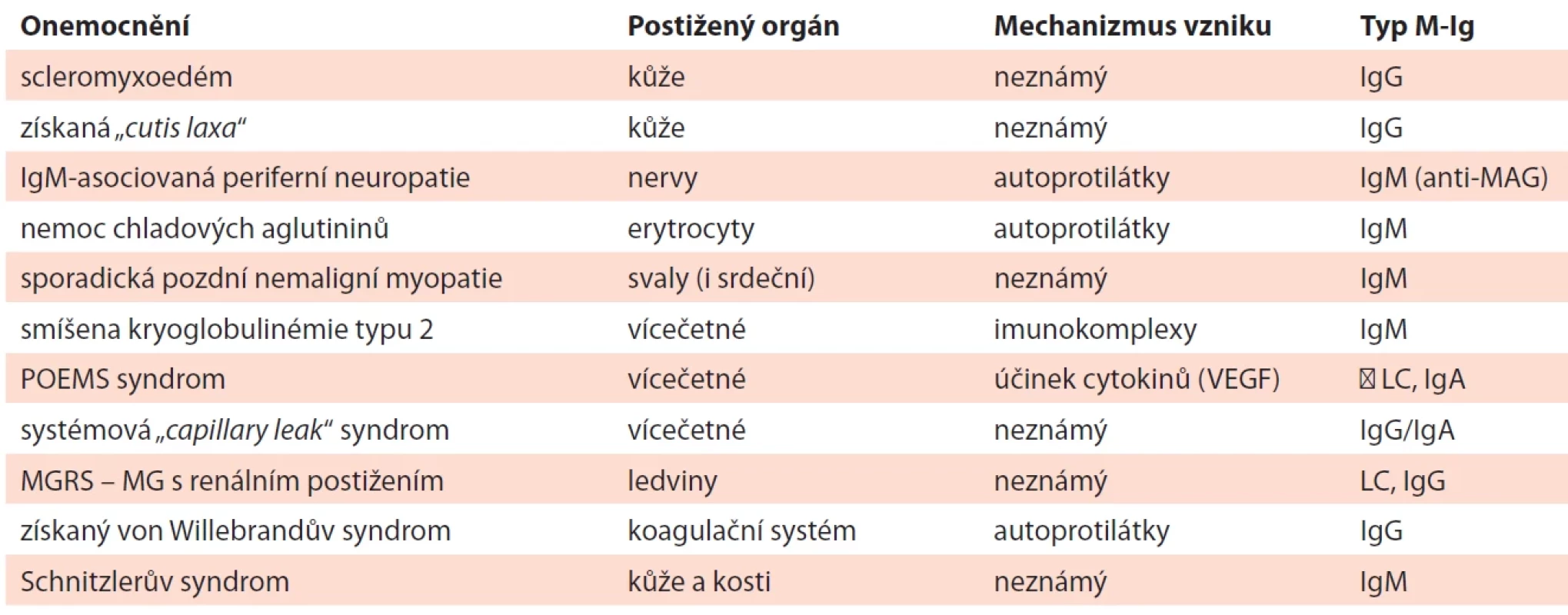
Table 9. Revidovaná diagnostická kritéria mnohočetného myelomu (Rajkumar, 2014). 
Table 10. Revidovaná diagnostická kritéria smoldering (doutnajícího, asymptomatického) mnohočetného myelomu (Rajkumar, 2014). 
Table 11. Mezinárodní prognostický index (ISS) pro mnohočetný myelom (Greipp, 2005). 
Table 12. Revidovaný mezinárodní prognostický index (R-ISS) mnohočetného myelomu (Palumbo, 2015). 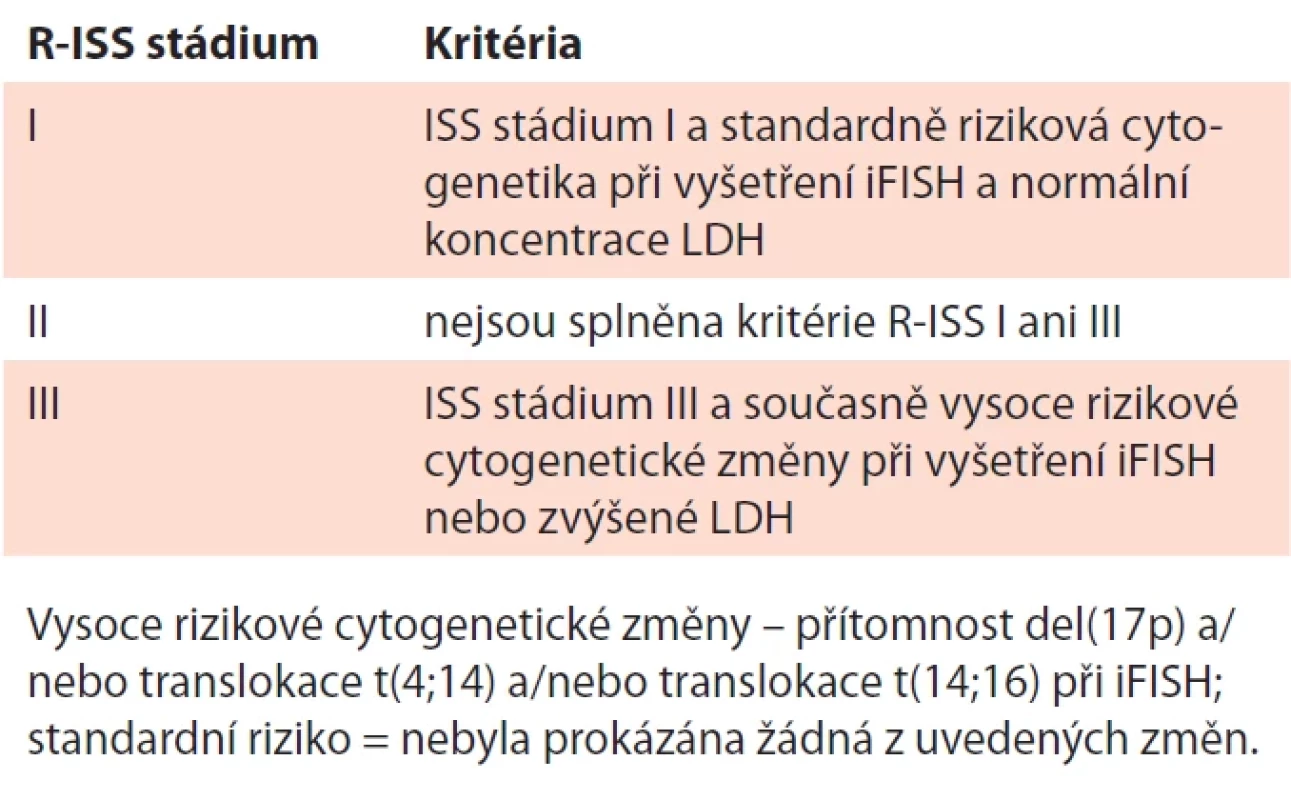
Table 13. Druhá revize mezinárodního prognostického indexu (R2-ISS) MM (D’Agostino, 2022). 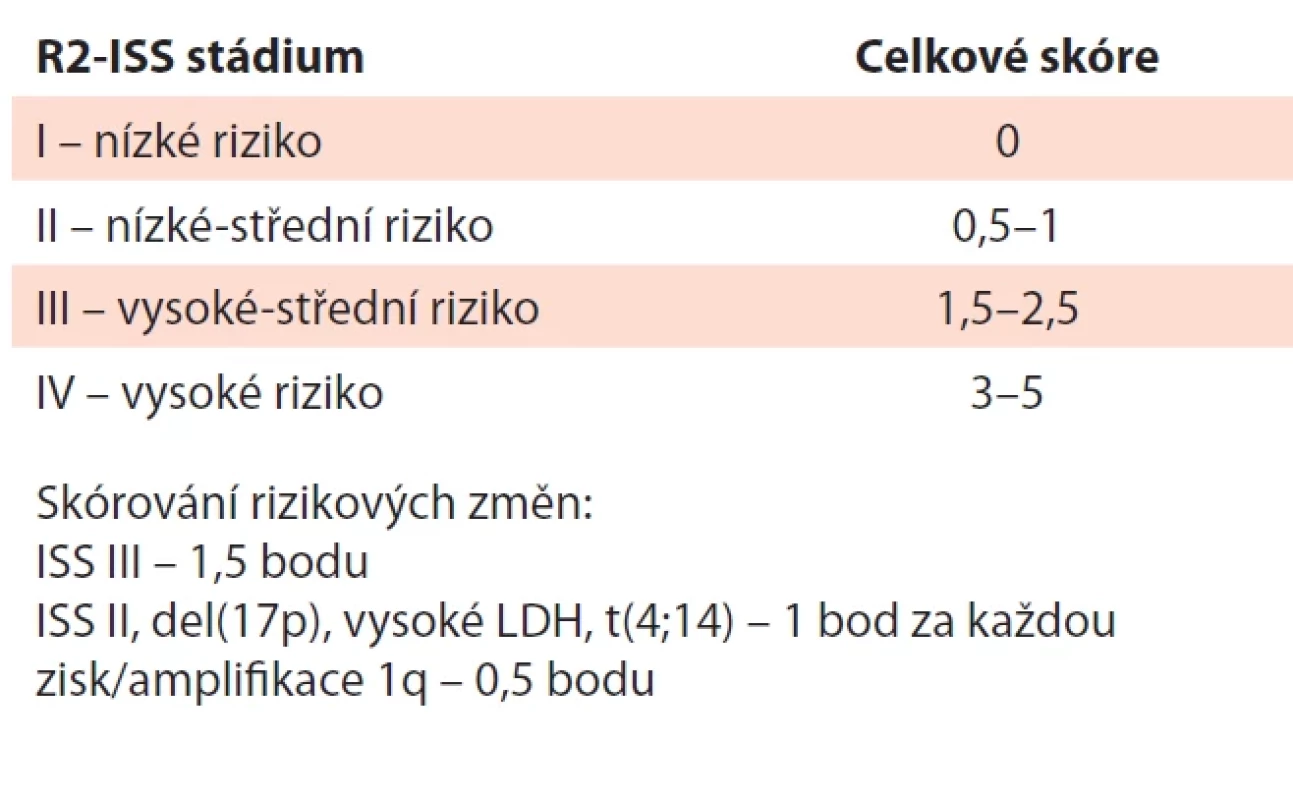
Table 14. Klasifi kace monoklonálních gamapatií neurčeného významu (Kyle, 2010). 
Table 15. Riziková stratifi kace smoldering MM – 20/20/20 IMWG model (Mateos, 2020). 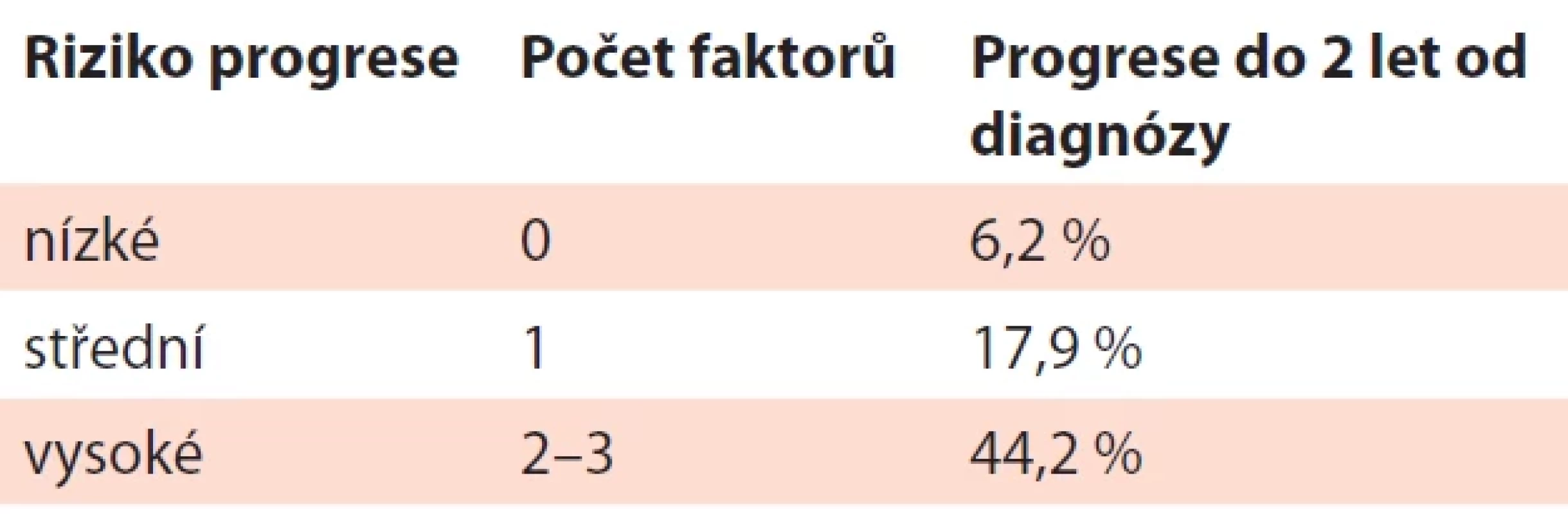
B. Zápis diagnózy
Správným diagnostickým výstupem je dnes např. následný vzorový zápis:
Smoldering MM IgA-kappa; ISS I, R-ISS I (event. R2-ISS I) datum dg.
= léčba není indikovaná
nebo
Mnohočetný myelom IgG-lambda (poškození ledvin, mnohočetná osteolytická ložiska); ISS III, R-ISS II (event. R2-ISS II) (poz. del 13, translokace neg., del 17 neg., amplifikace 1q21 neg.); 0,52 % CTC (cirkulujících plazmocytů v periferní krvi)
datum dg.
= indikováno zahájení léčby.
C. Doporučení pro hodnocení léčebné odpovědi a dlouhodobých intervalů
Table 16. Standardní defi nice dosažených léčebných odpovědí u MM dle IMWG (Durie, 2006; Rajkumar, 2011 a 2022). 
Table 17. Defi nice minimální reziduální choroby dle IMWG (Kumar, 2016). 
Table 18. Defi nice léčebných intervalů doporučených pro hodnocení dlouhodobého léčebného efektu dle IMWG (Durie, 2006; Kumar, 2016). 
Jsou stanoveny kategorie sCR, CR, VGPR, PR, MR, SD, PD a nověji MRD-negativní resp. MRD-pozitivní pro hodnocení léčebné odpovědi (Kumar, 2016).
Jsou stanoveny dlouhodobé léčebné intervaly TTP, PFS, EFS, DOR a OS.
Zhodnocení léčebné odpovědi je vyžadováno průběžně. Vždy však před změnou léčby a při ukončení léčby s následnými kontrolami v intervalu 1–3 měsíců.
Je doporučeno provést hodnocení MRD u všech pacientů s NDMM D+100 po provedení ASCT, dále vždy kdy je ošetřujícím lékařem indikován odběr KD k potvrzení CR. V případě negativity MRD je doporučeno zopakovat toto vyšetření s odstupem 12 měsíců k potvrzení tzv. sustained MRD negativity.
Léčebná odpověď musí být zaznamenána v dokumentaci nemocného.
Pro stanovení CR je nezbytné provedení imunofixace jakmile M-Ig klesne pod detekční limit používané vyšetřovací metody.
Stanovení stringent CR dnes není dle doporučení předsednictva CMG nutné, jako nejlepší dosažená léčebná odpověď bude uváděna CR, která původní kategorii sCR zahrnuje.
Biochemické stanovení musí být potvrzeno druhým odběrem, což se samozřejmě netýká odběru kostní dřeně, kde je nutný pro zhodnocení aktuálního stavu pouze jeden odběr.
Při nové aktivitě onemocnění je nutné dodržet platná kritéria pro relaps/progresi onemocnění. Je vhodné stanovit interval TTP, tj. dobu do progrese onemocnění, pokud tento nelze použít, pak stanovit interval PFS a přihlédnout k nim při volbě další léčby.
U oligosekrečních a nesekrečních forem MM je nutný monitoring pomocí stanovení volných lehkých řetězců v séru. Prozatím nezbytné je zde pravidelné opakování vyšetření kostní dřeně. Zásadní význam má i opakování a vzájemné srovnání zobrazovacích metod (dnes zejména CT/PET event. CT/MR vyšetření).
Doporučení pro diagnostiku a léčbu vysoce prognosticky rizikové skupiny („high-risk“) nemocných s mnohočetným myelomem
Pro identifikaci podskupiny nemocných s vysokým rizikem pro krátké celkové přežití (tzv. high-risk MM) je vhodné vstupně vyšetřit na myelomových buňkách všechny dostupné rizikové translokace IgH (t (4; 14), t (14; 16), t (14; 20), del (17p), zisk (1q21) a stanovit, zda jde o hyperdiploidní karyotyp. Za nezbytné minimum lze považovat (t (4; 14), t (14; 16) a del (17p) a zisk (1q21). (stupeň doporučení A, úroveň důkazu Ia)
Ultra-high-risk skupinu identifikují komplexní změny karyotypu.
Změny se v čase vyvíjejí, proto je vhodné vyhodnotit tyto změny i před léčbou relapsu onemocnění.
U high-risk podskupiny nemocných s MM by neměly být používány dvojkombinace léků, naopak by měly být použity nejméně nejúčinnější dostupné trojkombinace. Toto platí pro novou diagnózu i relaps onemocnění. (stupeň doporučení A, úroveň důkazu Ia)
V primoléčbě při přítomnosti t (4; 14) by měl být součástí léčebné strategie bortezomib a v indikovaných případech tandemová autologní transplantace. (stupeň doporučení A, úroveň důkazu Ia)
D. Léčba mnohočetného myelomu
Doporučení pro léčbu thalidomidem
Thalidomid je lékem u MM, který je dnes nahrazen účinnějšími a lépe snášenými léky ze stejné skupiny imunomodulačních léků v kombinovaných režimech (stupeň doporučení A, úroveň důkazu Ia). Jeho stávající využití je velmi limitované.
Je indikován v primoléčbě i relapsu onemocnění v kombinovaných režimech (stupeň doporučení A, úroveň důkazu Ia).
Mezi klíčová profylaktická opatření patří profylaxe žilní trombózy po dobu léčby (stupeň doporučení A, úroveň důkazu Ia).
Polyneuropatie je nejzávažnějším nežádoucím účinkem thalidomidu. Časná redukce dávky a zastavení léčby jsou vhodným opatřením. Rozvoj polyneuropatie do stupně dva by měl být signálem k zastavení léčby, existují-li jiné dostupné léčebné možnosti (stupeň doporučení A, úroveň důkazu Ib).
Thalidomid je teratogenní lék a při jeho použití je nezbytné dodržet přesně stanovený bezpečnostní program daný regulačními úřady (stupeň doporučení A, úroveň důkazu Ia).
Doporučení pro léčbu lenalidomidem
Lenalidomid je vysoce účinný lék u MM. Je indikován k léčbě relapsu i k léčbě nově diagnostikovaného onemocnění nejméně v kombinaci s dexametazonem (stupeň doporučení A, úroveň důkazu Ia); je indikován k udržovací léčbě po provedení autologní transplantace (stupeň doporučení A, úroveň důkazu Ia).
Kombinované režimy na bázi lenalidomidu s přidáním nového léku s biologickým mechanizmem účinku prokázaly u předléčených nemocných (karfilzomib, daratumumab, elotuzumab, ixazomib) i u nově diagnostikovaného onemocnění (bortezomib) zásadní zlepšení léčebného účinku i prognózy. Trojkombinace léků mají vyšší účinnost než dvojkombinace Len/Dex (stupeň doporučení A, úroveň důkazu Ib). Dle doporučení myelomové sekce ČHS by měly být proto kombinované režimy upřednostňovány.
Mezi klíčová profylaktická opatření patří profylaxe žilní trombózy po celou dobu léčby a použití růstových faktorů v případě myelosuprese. (stupeň doporučení B, úroveň důkazu IIa).
Před zahájením léčby lenalidomidem je doporučeno vyšetřit nemocného na přítomnost hepatitidy B. V případě pozitivního nálezu a rovněž u nemocných s předcházející infekcí v anamnéze je doporučené realizovat monitorování příslušných antigenů a případně zvážit vhodnou profylaxi (stupeň doporučení C, úroveň důkazu IV).
Kombinace lenalidomidu s perorálním melfalanem u pacientů s NDMM je relativně kontraindikovaná, neboť zvyšuje riziko vzniku sekundárních primárních malignit (stupeň doporučení A, úroveň důkazu Ia).
Lenalidomid je teratogenní lék a při jeho použití je nezbytné dodržovat Program prevence početí (stupeň doporučení C, úroveň důkazu IV).
Doporučení pro léčbu pomalidomidem
Pomalidomid je v kombinaci nejméně s dexametazonem indikován k léčbě dospělých pacientů s RRMM, kteří absolvovali alespoň jedno předchozí léčebné schéma zahrnující lenalidomid (stupeň doporučení A, úroveň důkazu Ib).
Kombinované režimy na bázi pomalidomidu s přidáním nového léku s biologickým mechanizmem účinku (bortezomib, daratumumab, isatuximab, elotuzumab) prokázaly u předléčených zásadní zlepšení léčebného účinku i prognózy. Trojkombinace léků mají vyšší účinnost než dvojkombinace Pom/Dex (stupeň doporučení A, úroveň důkazu Ib). Dle doporučení myelomové sekce ČHS by měly být proto kombinované režimy upřednostňovány.
Mezi klíčová profylaktická opatření patří profylaxe žilní trombózy po celou dobu léčby a použití růstových faktorů v případě myelosuprese (stupeň doporučení B, úroveň důkazu IIa).
Před zahájením léčby pomalidomidem je doporučeno vyšetřit nemocného na přítomnost hepatitidy B. V případě pozitivního nálezu a rovněž u nemocných s předcházející infekcí v anamnéze je doporučeno realizovat monitorování příslušných antigenů a případně zvážit vhodnou profylaxi (stupeň doporučení C, úroveň důkazu IV).
Pomalidomid je teratogenní lék a při jeho použití je nezbytné dodržovat Program prevence početí (stupeň doporučení C, úroveň důkazu IV).
Doporučení pro léčbu bortezomibem
Bortezomib je účinný lék u MM. Je indikován v primoléčbě i relapsu onemocnění, ve vstupní indukční a konsolidační části indukční fáze léčby u všech nemocných (stupeň doporučení A, úroveň důkazu Ib).
Kombinované režimy na bázi bortezomibu s glukokortikoidem a imunomodulační látkou (zvláště režim VRD) lze považovat za účinné, dostupné a dobře tolerované režimy nemocnými v primoléčbě. Jde současně o účinné režimy v relapsu onemocnění (stupeň doporučení A, úroveň důkazu Ib pro primoléčbu).
Kombinované režimy na bázi bortezomibu s glukokortikoidem a alkylační látkou (melfalan, cyklofosfamid) patří mezi účinné režimy v primoléčbě, ale v roce 2023 již nejde o léčbu první volby (stupeň doporučení A, úroveň důkazu Ia).
Bortezomib v kombinovaném režimu je doporučen jako u nemocných s renálním selháním, u kterých může být použit bez nutnosti redukce dávky (stupeň doporučení B, úroveň důkazu IIa).
Bortezomib částečně překonává negativní prognostický vliv tzv. nepříznivých chromozomálních aberací, zvláště translokací IgH a může být proto jedním z léků u těchto nemocných (stupeň doporučení A, úroveň důkazu Ib).
Bortezomib nezvyšuje riziko tromboembolické nemoci. U nemocných s anamnézou či vysokým rizikem tromboembolické nemoci je jeho aplikace upřednostněna (stupeň doporučení A, úroveň důkazu Ib).
Mezi klíčová profylaktická opatření patří použití acykloviru v dávce nejméně 200–400 mg 1× denně.
Neuropatie je nejzávažnějším nežádoucím účinkem bortezomibu. Subkutánní aplikace, časná redukce dávky nebo prodloužení intervalů mezi dávkami na 1× týdně a případně časné zastavení léčby jsou vhodným opatřením. Rozvoj polyneuropatie do stupně dva by měl být signálem k zastavení léčby, existují-li jiné dostupné léčebné možnosti (stupeň doporučení A, úroveň důkazu Ib).
Doporučení pro léčbu karfilzomibem
Karfilzomib je indikován k léčbě dospělých pacientů s relabujícím nebo refrakterním MM po nejméně 1 léčebné linii v kombinaci s lenalidomidem a dexametazonem nebo v kombinaci s dexametazonem (stupeň doporučení A, úroveň důkazu Ia).
Karfilzomib je indikován k léčbě dospělých pacientů s RRMM po nejméně 1 léčebné linii v kombinaci s anti-CD38 monoklonální protilátkou a dexametazonem (stupeň doporučení A, úroveň důkazu Ia).
U pacientů je doporučena profylaxe herpetických infekcí (stupeň doporučení A, úroveň důkazu Ia).
Při použití karfilzomibu je doporučeno aktivně řešit problematiku hypertenze a hypervolemie vstupně i v průběhu léčby, neboť se mohou podílet na vzniku srdečního selhání u predisponovaných jedinců a starších nemocných (stupeň doporučení A, úroveň důkazu Ia).
Doporučení pro léčbu ixazomibem
Ixazomib je indikován k léčbě dospělých pacientů s relabovaným a refrakterním MM po 1–3 léčebných liniích v kombinaci s lenalidomidem a dexametazonem (stupeň doporučení A, úroveň důkazu Ib).
U pacientů je doporučena profylaxe herpetických infekcí (stupeň doporučení A, úroveň důkazu Ib).
Ixazomib v kombinovaném režimu Ixa/Len/Dex významně zlepšuje výstupy u prognosticky nepříznivé skupiny nemocných (tzv. vysoké riziko na základě definice chromozomálních abnormalit vč. skupiny nemocných s amplifikací 1q21) (stupeň doporučení A, úroveň důkazu Ib).
Ixazomib je vhodnou alternativou k bortezomibu v léčbě dospělých pacientů s nově diagnostikovaným MM s lenalidomidem a dexametazonem (stupeň doporučení C, úroveň důkazu III).
Doporučení pro léčbu daratumumabem
Daratumumab v monoterapii je indikován u pacientů s relabovaným a refrakterním MM, kteří absolvovali léčbu obsahující, jak proteasomový inhibitor, tak immunomodulační látku, a u kterých došlo k progresi onemocnění při poslední léčbě (stupeň doporučení B, úroveň důkazu IIA).
Daratumumab v kombinaci s lenalidomidem a dexametazonem nebo bortezomibem a dexamethasonem nebo pomalidomidem a dexamethasonem nebo karfilzomibem a dexamethasonem je indikován u pacientů s MM, kteří absolvovali alespoň jednu předchozí léčebnou linii (stupeň doporučení A, úroveň důkazu Ib).
Daratumumab v kombinaci s lenalidomidem a dexamethasonem nebo v kombinaci s bortezomibem, melfalanem a prednisonem je indikován u pacientů s nově diagnostikovaným MM, nevhodných k autologní transplantaci hemopoetických buněk (stupeň doporučení A, úroveň důkazu Ib).
Daratumumab v kombinaci s bortezomibem, thalidomidem a dexamethasonem (stupeň doporučení A, úroveň důkazu Ib) nebo v kombinaci s bortezomibem, lenalidomidem a dexamethasonem (stupeň doporučení B, úroveň důkazu IIb) je indikován u pacientů s nově diagnostikovaným MM vedených k autologní transplantaci hemopoetických buněk.
Vzhledem k interferenci daratumumabu v rámci předtransfuzního vyšetření je doporučeno provést vstupní imunohematologická vyšetření ještě před zahájením léčby, a tak dopředu zajistit dostupnost antigenně kompatibilních erytrocytových transfuzních přípravků (stupeň doporučení C, úroveň důkazu IV).
Je doporučena profylaxe pomocí antivirotik v rámci prevence reaktivace herpes zoster a to po dobu léčby a minimálně ještě 3 měsíce po ukončení léčby (stupeň doporučení C, úroveň důkazu IV).
Doporučení pro léčbu elotuzumabem
Elotuzumab v kombinaci s lenalidomidem a dexametazonem je indikován u pacientů s mnohočetným myelomem, kteří absolvovali 1–3 předchozí léčebné linie (stupeň doporučení A, úroveň důkazu Ib).
Elotuzumab v kombinaci s pomalidomidem a dexametazonem je indikován u pacientů s mnohočetným myelomem, kteří absolvovali 2–4 předchozí léčebné linie obsahující lenalidomid a inhibitor proteasomu (stupeň doporučení B, úroveň důkazu IIb).
Elotuzumab lze bezpečně podávat u pacientů s mnohočetným myelomem a renálním selháním bez nutnosti redukovat dávku (stupeň doporučení B, úroveň důkazu IIa).
Doporučení pro léčbu isatuximabem
Isatuximab v kombinaci s pomalidomidem a dexametazonem nebo karfilzomibem a dexamethasonem je indikován u pacientů s MM, kteří absolvovali alespoň jednu předchozí léčebnou linii a jsou předléčení a/nebo refrakterní na lenalidomid (stupeň doporučení A, úroveň důkazu Ib).
IRRs jsou typickým a nejčastějším nežádoucím účinkem spojeným s podáním isatuxumabu. K doporučeno aplikovat premedikaci v podobě kortikoidů, antihistaminik a paracetamolu 30–60 min před podáním isatuximabu (stupeň doporučení A, úroveň důkazu Ib).
Vzhledem k interferenci isatuximabu v rámci předtransfuzního vyšetření je doporučeno provést vstupní imunohematologická vyšetření ještě před zahájením léčby, a tak dopředu zajistit dostupnost antigenně kompatibilních erytrocytových transfuzních přípravků (stupeň doporučení C, úroveň důkazu IV).
Je doporučena profylaxe pomocí antivirotik v rámci prevence reaktivace herpes zoster a to po dobu léčby a minimálně ještě 3 měsíce po ukončení léčby (stupeň doporučení A, úroveň důkazu Ib).
Doporučení pro léčbu CAR-T lymfocyty a bispecifickými protilátkami
Léčba CAR-T lymfocyty (Ide-cel nebo Cilta-cel) je indikována u pacientů s RMMM, kteří prodělali minimálně 3 předchozí linie léčby obsahující imunomodulační léky, proteasomové inhibitory a anti-CD38 monoklonální protilátku a vykázali progresi na poslední linii léčby (úroveň důkazu IIa, stupeň doporučení B).
Léčba teclistamabem je indikována u pacientů s RMMM, kteří prodělali minimálně 3 předchozí linie léčby obsahující imunomodulační léky, proteasomové inhibitory a anti-CD38 monoklonální protilátku a vykázali progresi na poslední linii léčby (úroveň důkazu IIa, stupeň doporučení B).
Elranatamab je indikován u pacientů s RMMM, kteří prodělali minimálně 3 předchozí linie léčby obsahující imunomodulační léky, proteasomové inhibitory a anti-CD38 monoklonální protilátku a vykázali progresi na poslední linii léčby (úroveň důkazu IIa, stupeň doporučení B).
Talquetamab je indikován u pacientů s RMMM, kteří prodělali minimálně 3 předchozí linie léčby obsahující imunomodulační léky, proteasomové inhibitory, anti-CD38 monoklonální protilátku a vykázali progresi na poslední linii léčby (úroveň důkazu IIa, stupeň doporučení B).
Doporučení pro léčbu alkylačními a jinými cytostatiky, glukokortikoidy
Léčba vysokými dávkami dexametazonu v monoterapii je vhodná pro iniciální léčbu pacientů, u nichž je jiná léčba kontraindikována, to znamená u pacientů s těžkou pancytopenií (stupeň doporučení C, úroveň důkazu IIa). Neprodleně, jak to stav nemocného umožní, by měl být režim doplněn na standardně používanou léčebnou kombinaci. Tato léčba je vhodná i pro pacienty s renální insuficiencí, nelze-li použít jiný silnější režim (stupeň doporučení B, úroveň důkazu IIa).
Kombinace melfalanu s prednisonem nebo kombinace cyklofosfamidu či bendamustinu s nejméně glukokortikoidy dnes nejsou optimální léčebnou volbou v primoléčbě ani v relapsu onemocnění. Možným využitím kombinace cyklofosfamidu s prednisonem je paliativní léčba. Opatrnosti je třeba při podávání pacientům s renální insuficiencí u melfalanu (stupeň doporučení A, úroveň důkazu Ia).
Doporučení pro léčbu belantamabem mafodotinem, venetoclaxem, selinexorem a melflufenem
Léčba belantamabem mafodotinem, venetoclaxem, selinexorem, melflufenem je indikována u pacientů s RMMM, kteří prodělali minimálně 3 předchozí linie léčby obsahující imunomodulační léky, proteasomové inhibitory a anti-CD38 monoklonální protilátku a vykázali progresi na poslední linii léčby. Jejich použití je možné individuálně zvážit, pokud nejsou dostupné účinnější léky (úroveň důkazu IIa, stupeň doporučení B).
Při léčbě venetoclaxem je potřeba důrazně uplatnit dostupná profylaktická opatření při zvýšeném riziku infekčních komplikací (úroveň důkazu IIa, stupeň doporučení B).
Při léčbě belantamabem mafodotinem je potřeba spolupráce s oftalmologem při významné frekvenci oční toxicity. Její monitorování a následná úprava dávek a frekvence použití léku jsou nezbytná opatření (úroveň důkazu IIa, stupeň doporučení B).
Melflufen by neměl být použitý u nemocných s předchozím využití myeloablativní dávky melfalanu (úroveň důkazu IIa, stupeň doporučení B).
Doporučení pro léčbu vysokodávkovanou chemoterapii s autologní transplantací kmenových buněk
Vysokodávkovaná chemoterapie s autologní transplantací kmenových buněk (AT) by měla být součástí primární léčebné strategie u pacienta s nově diagnostikovaným onemocněním ve věku do 70 let či vhodného biologického věku (stupeň doporučení A, úroveň důkazu Ia).
Optimálním předtransplantačním režimem je melfalan 200 mg/m2 (stupeň doporučení A, úroveň důkazu Ib).
Opakovaná (tandemová) AT může být použita jako konsolidace u nemocných s cílem dosáhnout maximální léčebné odpovědi a dlouhodobého trvání remise a je doporučována ke zvážení u vysoce rizikových pacientů (vysoké cytogenetické riziko) a u nemocných s nedostatečnou léčebnou odpovědí (stupeň doporučení A, úroveň důkazu Ia).
Pacienti starší 70 let v dobrém celkovém stavu mohou být také vhodnými kandidáty pro tento postup s možností využítí melfalanu v dávce 100–200 mg/m2 (stupeň doporučení A, úroveň důkazu Ib). V rozhodnutí o způsobu léčby musí být zvážena všechna možná rizika a přínosy tohoto postupu u konkrétního pacienta (stupeň doporučení C, úroveň důkazu IV).
Vysokodávkovaná chemoterapie u pacientů s těžkým poškozením ledvin (clearence < 50 ml/min) je proveditelná, ale vyžaduje vždy redukci dávky melfalanu a měla by být prováděna pouze ve specializovaných centrech (stupeň doporučení B, úroveň důkazu IIa).
Retransplantace v relapsu u nemocných s MM je možnou efektivní léčebnou strategií, zvláště pokud je použita v kombinaci s reindukcí zahrnující nové cílené léky (stupeň doporučení A, úroveň důkazu Ib).
Doporučení pro léčbu alogenní transplantaci krvetvorných buněk
Alogenní transplantace má omezenou roli v terapii MM, a to především z důvodů značné toxicity kombinované etiologie a také malého množství pacientů s myelomem, kterým lze tuto léčebnou alternativu nabídnout (stupeň doporučení A, úroveň důkazu Ib).
Alogenní transplantace by měly být prováděny u nemocných s MM nejlépe v rámci klinických studií, v primoléčbě výhradně v rámci klinických studií (stupeň doporučení C, úroveň důkazu IV).
Za možné kandidáty lze považovat nemocné ve věku do 55 let s HLA identickým sourozencem, kteří nejsou rezistentní na indukční léčbu před provedením alogenní transplantace. Pacient však musí být plně obeznámen s možnými riziky tohoto postupu (stupeň doporučení B, úroveň důkazu IIa).
Za možnou indikaci v dnešní době lze považovat časný první senzitivní relaps onemocnění u vysoce rizikových nemocných, za optimální léčebný postup využití kombinace auto-alo transplantace s použitím RIC režimů (stupeň doporučení C, úroveň důkazu IV).
Doporučení pro udržovací léčbu mnohočetného myelomu
Lenalidomid je doposud nejúčinnějším lékem v UL MM (stupeň doporučení A, úroveň důkazu Ia).
UL lenalidomidem je doporučena v dávce 10 mg denně (stupeň doporučení A, úroveň důkazu Ib).
Délka UL je doporučena až do relapsu či progrese onemocnění (stupeň doporučení A, úroveň důkazu Ia).
Optimální délka podávání UL lenalidomidem není doposud známa. U nemocných v kompletní remisi s MRD negativitou je podávání léku déle než 3 roky diskutabilní s ohledem na průměrnou délku UL v klinických studiích a bezpečnost podávaní (doporučení C, úroveň důkazu IV).
Jakákoliv nová udržovací či konsolidační léčba měla probíhat výhradně v rámci klinických studií (stupeň doporučení A, úroveň důkazu Ib).
Doporučení pro léčbu nemocných s MM a renálním selháním
Základní podmínkou pro úspěšnou záchranu funkcí ledvin je hlavně časná diagnostika a použití známých standardních opatření, jako jsou dostatečná hydratace a obrat tekutin s měřením centrálního žilního tlaku, řešení minerální dysbalance, zvláště pak rychlé dosažení normokalcémie, pokud se na renálním selhání podílí hyperkalcémie.
Pro iniciální léčbu MM u pacientů s poškozenou funkcí ledvin se doporučuje režim s rychlým nástupem účinku, s dobrou tolerancí, a především s vysokou šancí na léčebnou odpověď s využitím plné dávky léku. Důležité je však především zahájit léčbu rychle, ať už je použit jakýkoliv léčebný režim (stupeň doporučení B, úroveň důkazu IIa).
Nezbytná je důsledná monitorace nežádoucích účinků, vstupní redukce dávek dle doporučení a včasné snížení dávky či následně vysazení léků při zvýšené toxicitě (stupeň doporučení B, úroveň důkazu III).
Je nezbytná opatrnost při používání nesteroidních antiflogistik a úprava dávek řady léků, např. derivátů morfinu a bisfosfonátů (stupeň doporučení B, úroveň důkazu III).
Při rozvaze o vysokodávkované chemoterapii je nutno zvážit potenciální přínos a podstatně vyšší počet komplikací, než je obvyklé u pacientů s normální funkcí ledvin. Nefrotický syndrom s hypoalbuminémií je dalším rizikovým faktorem pro léčbu vysokodávkovaným melfalanem. Proto by vysokodávkovaná chemoterapie u pacientů s poškozenou funkcí ledvin, případě s nefrotickým syndromem a hypoalbuminémií, měla být prováděna jen v centrech s dostatkem zkušeností se zvládáním závažných potransplantačních situací (stupeň doporučení C, úroveň důkazu IV).
E. Vybraná doporučení pro komplexní podpůrnou léčbu mnohočetného myelomu
Radioterapie je standardní léčebnou metodou pro solitární plazmocytom i extramedulární plazmocytom (stupeň doporučení B, úroveň důkazu IIa).
Adjuvantní chemoterapie není doporučena u solitárního plazmocytomu po provedení radioterapie nebo chirurgickém zákroku z důvodu nedostatečného množství dat k vyhodnocení účinnosti postupu. Výjimkou je stále aktivní ložisko po radioterapii zhodnocené PET/CT (stupeň doporučení C, úroveň důkazu IV).
Konzultace a případná stabilizace problematických osteolytických fraktur je nezbytnou součástí komplexní péče. Akutní neurologické příznaky vyžadují rovněž akutní konzultaci a zpravidla i akutní odstranění příčiny (stupeň doporučení C, úroveň důkazu IV).
Pacienti se vzniklou PN by měli mít redukovanou dávku léku, při stupni > 2 nebo progredující PN by se měla neurotoxická léčba vysadit (stupeň doporučení C, úroveň důkazů IV).
Pacientům s neuropatickou bolestí by se měla nasadit léčba blokátory iontových kanálů, SNRI nebo opiáty (stupeň doporučení A, úroveň důkazů Ib).
Povrchová neuropatická bolest může byť léčená náplastmi s lokálním 5% lidokainem (stupeň doporučení A, úroveň důkazů Ib).
Doporučení pro léčbu inhibující osteolýzu u mnohočetného myelomu
Bisfosfonáty jsou indikované u nemocných s nově diagnostikovaným, resp. relabujícím/refrakterním MM bez ohledu na to, zda je vyšetřovacími prokázáno kostní postižení (stupeň doporučení A, úroveň důkazu Ib).
Denosumab je indikován u nemocných s nově diagnostikovaným, resp. relabujícím/refrakterním MM, u kterých je zobrazovacími metodami prokázáno kostní postižení (stupeň doporučení A, úroveň důkazu Ia).
Bisfosfonáty jsou indikované v léčbě hyperkalcémie způsobené mnohočetným myelomem (stupeň A). Denosumab může být podáván u nemocných s hyperkalcémií způsobené MM, zejména při rezistenci na bisfosfonáty (stupeň doporučení B, úroveň důkazu II).
U pacientů, kteří dosáhli kompletní remisi nebo velmi dobrou parciální remisi, by léčba bisfosfonáty měla trvat nejméně 1 rok od dosažení této odpovědi, ale neměla by přesáhnout 2 roky od dosažení této odpovědi (stupeň doporučení C, úroveň důkazu III).
Pokud není dosaženo velmi dobré parciální remise, může být podávání bisfosfonátů dlouhodobé (stupeň doporučení D, úroveň důkazu IV).
Denosumab je doporučeno podávat dlouhodobě, pokud se nerozvine významná toxicita. V případě dosažení dlouhodobé léčebné odpovědi (velmi dobrá parciální remise nebo kompletní remise trvající déle než 2 roky) je možné zvážit prodloužení intervalu mezi aplikacemi nebo jeho vysazení (stupeň doporučení D, úroveň důkazu IVa).
Pokud nastane laboratorní relaps MM u nemocných, kteří ukončili terapii bisfosfonátem nebo denosumabem, je doporučeno tuto léčbu opět zahájit (stupeň doporučení B, úroveň důkazu II).
V případě významné renální insuficience je nutné upravit dávkování bisfosfonátů, event. je vysadit (stupeň doporučení A, úroveň důkazu Ia). Denosumab může být preferován před bisfosfonáty u nemocných s MM a renální insuficiencí (stupeň doporučení B, úroveň důkazu II).
Před nasazením i během léčby bisfosfonáty nebo denosumumabem je nutné dodržovat preventivní opatření snižující riziko ONJ.
V případě plánované extrakce zubu je doporučeno vysadit denosumab 30 dní před výkonem a bisfosfonáty přibližně 3 měsíce před výkonem. Antiresorbční léčbu je možné opět zahájit až po úplném zhojení rány, u bisfosfonátů nejlépe 3 měsíce po výkonu (stupeň doporučení C, úroveň důkazu III). Stomatochirurgické zákroky (vč. neodkladných extrakcí zubů) u pacientů užívající antiresorbční terapii se doporučuje provádět s antibiotickou profylaxí.
Doporučení pro léčbu anémie
U každého pacienta s anémií je třeba standardně provést diferenciální diagnostiku příčiny anémie.
Pokud není nalezena jiná příčina anémie a anémie odpovídá anémii chronických chorob při MM, je v případě klinických příznaků (obvykle při hodnotách hemoglobinu nižších než 100 g/l) možné zvážit léčbu humánním rekombinantním erytropoetinem.
Léčebný test s preparátem stimulujícím erytropoézu je na zvážení u všech nemocných s MM a symptomatickou anémií. Indikace musí korespondovat s obecnými indikacemi pro léčbu erytropoetinem vydanými Českou hematologickou společností (stupeň doporučení A úroveň důkazu 1b).
Erytropoetin je indikovaný k léčbě anémie u pacientů s myelomem a chronickým renálním selháním (stupeň doporučení A úroveň důkazu 1b).
Doporučený postup pro profylaxi trombotických komplikací u pacientů s mnohočetným myelomem
U pacientů s MM, kteří jsou hospitalizováni pro komplikace interního i chirurgického charakteru, je indikována profylaxe TEN profylaktickou dávkou LMWH odpovídající 40 mg enoxaparinu 1× denně.
U pacientů bez rizikových faktorů TEN*, kteří jsou léčeni režimy neobsahujícími IMiDy ani kombinaci antracyklinu s vysoko dávkovaným dexametazonem, není nutná žádná farmakologická tromboprofylaxe, doporučena jsou jen režimová opatření (mobilizace, cvičení, řádná hydratace, kompresní punčochy) a zvážení nejméně zatěžující profylaxe první 3–4 měsíce léčby (úroveň důkazu IV, stupeň doporučení C).
U všech ostatních pacientů je doporučena farmakologická tromboprofylaxe. Je u nich možné použít LMWH v profylaktické dávce (enoxaparin 40 mg, bemiparin 3 500 j, dalteparin 5 000 j, nadroparin u osob s hmotností do 50 kg 0,3 ml, u osob s hmotností 50–69 kg 0,4 ml, u osob s hmotností nad 70 kg 0,6 ml – vše 1× denně) nebo apixaban v dávce 2× denně 2,5 mg nebo rivaroxaban v dávce 10 mg 1× denně.
U pacientů bez dalších rizikových faktorů TEN* lze po dosažení parciální remise považovat za srovnatelně účinný postup ASA 100 mg denně (úroveň důkazu Ib, stupeň doporučení A pro 1. linii léčby, úroveň důkazu IV, stupeň doporučení C pro další linie léčby).
U pacientů s velmi vysokým rizikem (TEN v anamnéze, nově diagnostikovaný MM léčený kombinací IMiDu nejméně s pulsním dexametazonem) je možné podat intermediární dávku LMWH (nadroparin, enoxaparin, dalteparin) 100 IU/kg 1× denně (úroveň důkazu IIa, stupeň doporučení B).
U pacientů bez dalších rizikových faktorů TEN* léčených pro relaps MM IMiDy v kombinaci s nízkou dávkou kortikoidů nebo v monoterapii je možné od počátku podávat ASA místo LMWH.
U pacientů léčených warfarinem nebo některým z přímých orálních antikoagulancií (dabigatran, rivaroxaban, apixaban, edoxaban) z jiné indikace je možné tuto léčbu ponechat, neboť lze předpokládat dostatečný tromboprofylaktický efekt těchto léků během léčby MM.
Při léčbě warfarinem je třeba častěji kontrolovat INR, při léčbě přímými orálními antikoagulancii je třeba kontrolovat renální funkce a respektovat jejich kontraindikaci při renální insuficienci podle SPC. U pacientů s renální insuficiencí je bezpečná léčba apixabanem 2× denně 2,5 mg.
Za rizikové faktory TEN jsou považovány: upoutání na lůžko, imobilizace končetiny, fraktura pánve nebo femuru, akutní infekce, srdeční selhání NYHA III-IV, paréza nebo plegie končetiny, zavedený centrální žilní katétr, nadváha a obezita, známá vrozená nebo získaná trombofilní laboratorní odchylka, další aktivní nádorové onemocnění, současná léčba estrogeny, léčba erytropoetinem nebo jeho deriváty, věk nad 80 let.
Doporučení pro profylaxi infekčních komplikací
Profylaxe bakteriálních infekcí je doporučena na základě posouzení individuálního rizika (stupeň doporučení C, úroveň důkazu III).
Profylaxe proti herpetickým virům je doporučena všem pacientům léčeným PI, anti-CD38 protilátkami a po veškeré CAR-T terapii a terapii bispecifickými protilátkami (stupeň doporučení A, úroveň důkazu Ia).
Profylaxe pneumocystové pneumonie je doporučena na základě individuálního rizika a pro všechny pacienty po CAR-T terapii a terapii bispecifickými protilátkami (stupeň doporučení A, úroveň důkazu Ia).
Očkování neživými vakcínami je doporučeno všem pacientům (stupeň doporučení A, úroveň důkazu II).
Doporučené fyzioterapeutické metody u MM pacientů s postižením osového skeletu
Doporučené: individuální léčebná tělesná výchova (LTV) – škola zad, posílení hlubokého stabilizačního systému vč. dechových cvičení v domácím prostředí,
měkké techniky, fasciální techniky (jemné), techniky a metodiky na neurofyziologickém podkladě, reflexní masáž bez tlaku, vodoléčba – cvičení v bazénu, končetinové vířivé koupele, pravidelná fyzická aktivita a cvičení, v individuálních případech elektroterapie, lokální krátkodobá termoterapie.
Nedoporučené fyzioterapeutické metody: klasické masáže (velký tlak),
akupresura, manipulační techniky s nárazem, mobilizační a trakční techniky,
celotělové horké koupele a zábaly, rázová vlna, elektroterapie v místě aktivního nádoru.Doporučené léčebné fyzioterapeutické metody u polyneuropatie: střídavé šlapací koupele dolních končetin (Kneipův chodník), vířivé koupele – končetinové, lymfoterapie (manuální dle indikace lékaře), rašelinový zábal – pouze lokální, reflexní terapie plosky nohy, elektrostimulace (dle indikace RHB lékaře).
Doporučení pro diagnostiku a sledování pacientů s MGUS
Po vyloučení jiného typu monoklonální gamapatie musí být pro stanovení diagnózy MGUS splněna kritéria dle IMWG z roku 2018 (stupeň doporučení C, úroveň důkazu IV).
Optimálním diagnostickým výstupem je zápis obsahující: typ M-proteinu, určení rizika transformace s doporučenou frekvencí sledování (stupeň doporučení C, úroveň důkazu IV).
Doporučený panel vyšetření v rámci sledování zahrnuje: krevní obraz, základní biochemické vyšetření zahrnující stanovení sérových koncentrací urey, kreatinu, vápníku, celkové bílkoviny, C-reaktivního proteinu, beta2-mikroglobulinu, albuminu, laktátdehydrogenázy, jaterních enzymů, glukózy, dále kvantitativní stanovení imunoglobulinů a FLC v séru vč. stanovení jejich poměru, elektroforézu, případně imunofixaci séra a moči, proteinurii. Vyšetření kostní dřeně je doporučeno u IgG MGUS v případě sérového M-proteinu ≥ 15 g/l a u všech IgA a IgM typů MGUS. Zobrazovací vyšetření není běžně doporučováno u pacientů s M-proteinem typu IgG ≤ 15 g/l a při M-proteinu typu IgA ≤ 10 g/l bez kostních bolestí. U všech ostatních pacientů je vhodné provedení low-dose CT, případně celotělového MRI, PET/CT či PET/MRI vyšetření (stupeň doporučení C, úroveň důkazu IV).
Frekvence sledování v prvním roce upřesňuje dynamiku MGUS (interval 3–6 měsíců). Kontrolní vyšetření od druhého roku sledování z jsou v intervalech od 3 do 36 měsíců v závislosti na míře rizika transformace (stupeň doporučení C, úroveň důkazu IV).
Labels
Haematology Internal medicine Clinical oncology
Article was published inTransfusion and Haematology Today

2023 Issue Supplementum 2
Most read in this issue
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

