-
Medical journals
- Career
Optimální miniinvazivní přístup při náhradě jícnu žaludkem
Authors: J. Dostalík; P. Guňková; L. Martínek; V. Richter; I. Guňka; M. Mazur; M. Mitták
Authors‘ workplace: Chirurgická klinika FN Ostrava, přednosta: doc. MUDr. Jan Dostalík, CSc.
Published in: Rozhl. Chir., 2009, roč. 88, č. 8, s. 422-424.
Category: Monothematic special - Original
Overview
Ezofagektomie až do začátku 90. let 20. století byla standardně prováděná transhiatálně z laparotomie nebo kombinací laparotomie a torakotomie. Takto prováděné výkony jsou však spojeny s vysokou morbiditou 40–80 % a mortalitou 5–15 % a proto je snaha v chirurgii jícnu využívat co nejméně invazivního přístupu při zachování onkologické radikality. Na základě našich zkušeností s miniinvazivní ezofagektomií bychom chtěli ukázat techniku miniinvazivní náhrady jícnu žaludkem, kterou na našem pracovišti považujeme za optimální.
Klíčová slova:
miniinvazivní ezofagektomie – laparoskopie – torakoskopieÚVOD
Karcinomy jícnu patří mezi malignity se špatnou prognózou, kdy téměř 40 % pacientů po R0 ezofagektomii zemře během prvního roku po výkonu [1]. Z toho vyplývá snaha o provedení takového operačního výkonu, který by byl nejen dostatečně radikální, ale zároveň co nejméně invazivní s nízkým počtem pooperačních komplikací, možností časné rekonvalescence a dobrou kvalitou života nemocného. V roce 1992 Cuschieri [2] poprvé použil při ezofagektomii torakoskopický přístup zprava, v roce 1994 pak Sadanaga provedl první laparoskopickou transhiatální ezofagektomii. Od té doby se v chirurgii jícnu využívají kombinace techniky laparoskopie včetně manuálně asistované, torakoskopie i mediastinoskopie [3]. Speciální mediastinoskop u transhiatálního přístupu poprvé použil Bumm v Německu [4].
OPERAČNÍ TECHNIKA
Operační výkon, trvající průměrně 360 minut je prováděn v celkové anestezii, pacienti jsou intubováni biluminální endotracheální kanylou. K výkonu má pacient zajištěnou centrální a periferní žilní linku, arteriální katétr, epidurální a močový katétr. Během výkonu je udržována hemodynamická stabilita a normotermie pacienta.
Miniinvazivní ezofagektomie byla na chirurgické klinice FN Ostrava provedena u 7 pacientů. Na základě zkušeností s našim poměrně malým souborem a literárních údajů, věnujících se této problematice, je popsána technika miniinvazivní náhrady jícnu žaludkem, kterou na našem pracovišti považujeme za optimální. Za největší zlepšení považujeme změnu polohy pacienta při torakoskopické části výkonu z levého boku do polohy na břiše s elevací hrudníku.
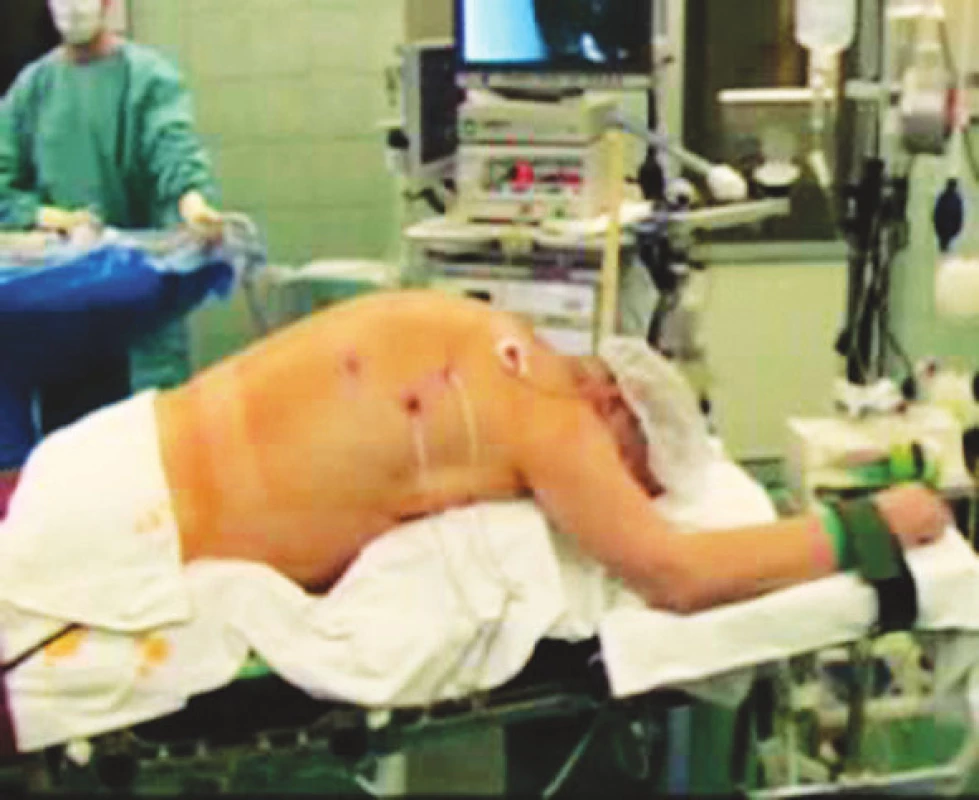
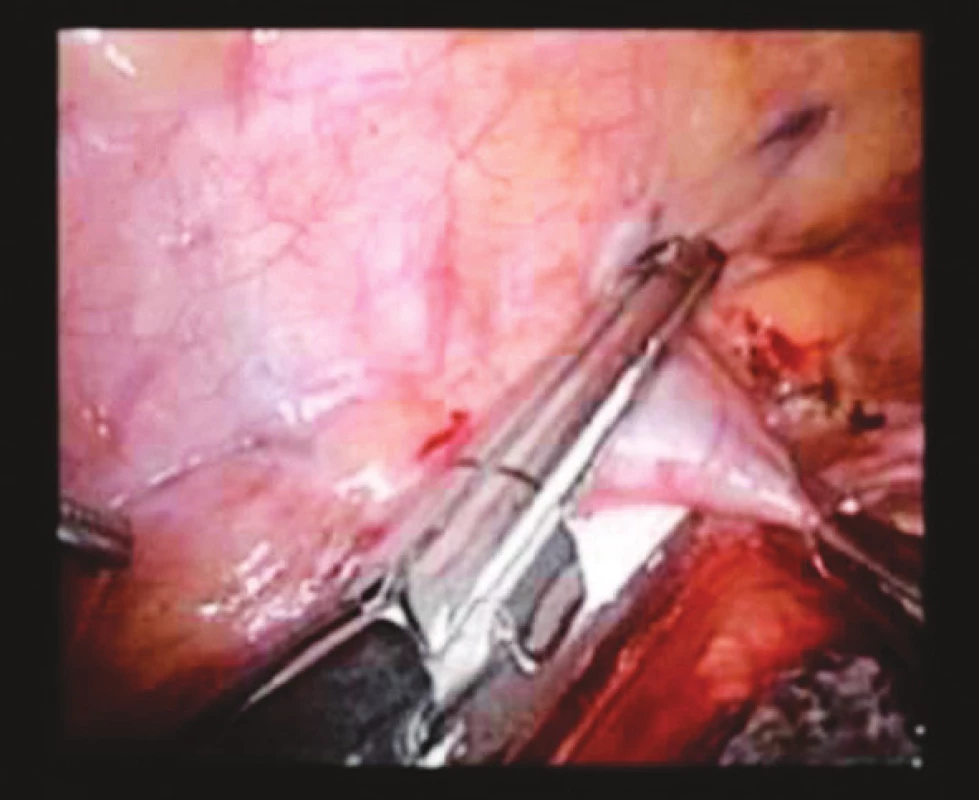
Operační výkon je zahájen v poloze pacienta na zádech s abdukovanými dolními končetinami laparoskopicky při pracovním tlaku 12 mm Hg. 11mm trokar pro optiku zavádíme nad pupkem, pracovní trokary 12 mm pak v obou mezogastriích v medioklavikulární čáře, 5mm trokar pod levým žeberním obloukem a 10mm trokar pod processus xiphoideus. Operační nález ještě doplňujeme peroperační endoskopii k ověření rozsahu tumorózního postižení. Laparoskopickou technikou je uvolněn jícen do výše 12–13 cm směrem do mediastina (Obr. 1). Kombinací harmonického skalpelu, klipovače a ligasure protínáme gastrokolické ligamentum se zachováním pravé gastroepiploické arterie. Směrem proximálním postupujeme k fundu žaludku. Na straně malé křiviny je přerušeno hepatogastrické ligamentum, klipována a. gastrica sinistra. Směrem distálním postupujeme až k okraji hepatoduodenálního ligamenta. Duodenum uvolňujeme Kocherovým manévrem. Po ukončení fáze izolace žaludku jsou odstraněny trokary, suturovány incize a pacient je polohován na břicho s elevací hrudníku (Obr. 2).
Image 1. Mobilizovaný abdominální jícen 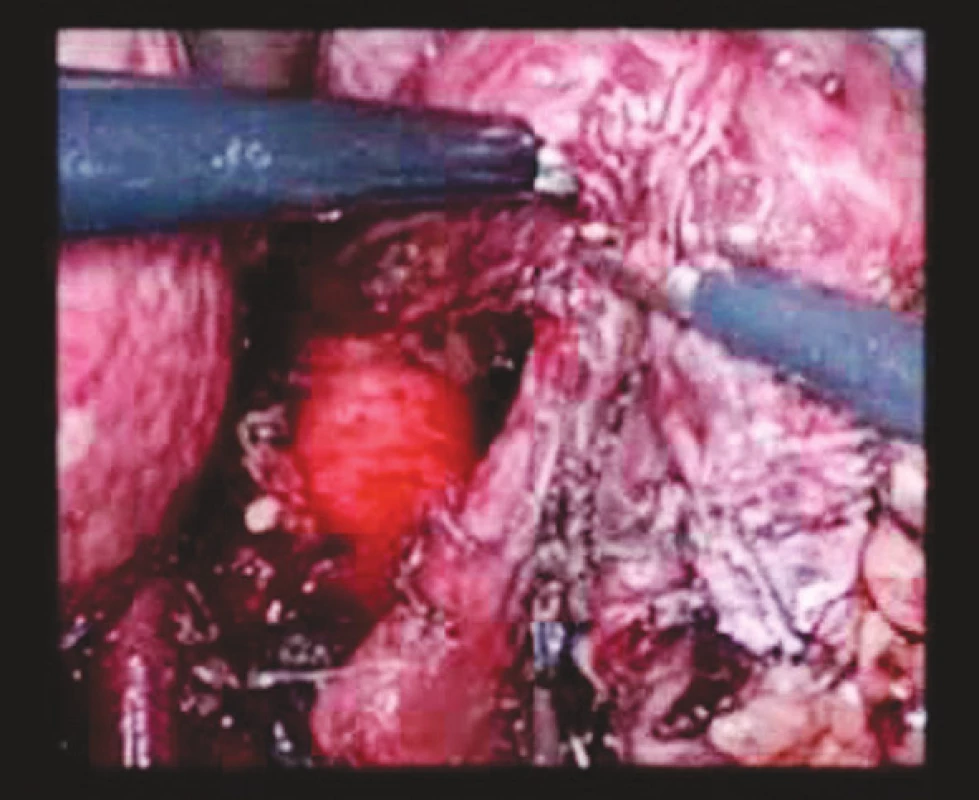
Z incize pod dolním úhlem pravé lopatky je zaveden 12mm hrudní trokar, anesteziologem je desuflována pravá plíce a za torakoskopické kontroly zavedeny zbývající trokary, a to paravertebrálně vpravo v 6. a 8. mezižebří 5mm trokary a v 8. mezižebří v zadní axilární čáře 12mm. Protínáme mediastinální pleuru nad jícnem až k v. azygos, kterou přerušujeme cévním staplerem (Obr. 3). Jícen mobilizujeme s přilehlou lymfatickou drenáži až do oblasti horní hrudní apertury. Následně provádíme hrudní drenáž, odstraňujeme trokary a suturujeme incize.
Po umístění pacienta zpět na záda vedeme řez na levé straně krku navnitř kývače a izolujeme a na úrovni laloku štítnice přerušujeme krční jícen. Na periferní část jícnu je naloženo trasovací vlákno. V pravém podžebří z minilaparotomie v délce cca 8 cm po naložení ochranné fólie žaludek a celý jícen mobilizujeme před břišní stěnu a od prepylorické části podél velké křiviny vytváříme pomocí zásobníků stapleru tubulus. Linii svorek vždy přešíváme. Na vrchol takto vytvořeného tubulu fixujeme trasovací vlákno a za manuální podpory jej vytahujeme zadním mediastinem do rány na levé straně krku. Anastomózu šijeme dvouvrstevnou konec ke konci vstřebatelným pleteným vláknem. Ještě před dokončením anastomózy zavádíme enterální a žaludeční sondu. K anastomóze ještě před suturou rány zavádíme Redonův drén. Na závěr drénujeme levý podbrániční prostor a suturujeme minilaparotomii.
DISKUSE
Až do začátku 90. let 20. století se standardně ezofagektomie prováděla buď transhiatálně z laparotomie nebo kombinovaným laparotomickým a torakotomickým přístupem. Takto prováděné výkony jsou však spojeny s vysokou morbiditou 40–80% [5] a mortalitou 5–15% [5].
S rozvojem miniinvazivní chirurgie začala tato technika se všemi svými výhodami pronikat i do chirurgie jícnu. V roce 1992 Cuschieri [2] poprvé použil při ezofagektomii torakoskopický přístup zprava, v roce 1994 pak Sadanaga provedl první laparoskopickou transhiatální ezofagektomii, malý soubor těchto výkonů pak publikoval v roce 1995 De Paula [6].
Jedna z největších evropských studií, kterou publikoval Luketich [7], prokázala statisticky významné snížení morbidity a mortality při použití kombinace torakoskopického a laparoskopického přístupu. Třicetidenní mortalita v jeho studii byla 1,4 % při zachování požadavků onkologické radikality. Srovnatelná s otevřeným výkonem byla rovněž délka přežití.
Na základě našich zkušeností ve shodě s Luketichem je optimální pro torakoskopickou fázi operace poloha pacienta na břiše, která narozdíl od polohy pacienta na levém boku umožňuje přehlednější operační pole a komfortnější přístup k jícnu pro operatéra.
Miniinvazivním přístupem jsou redukovány zejména plicní komplikace jako respirační insuficience, pneumonie, atelektázy, pleurální výpotek a perzistující pneumotorax. Torakoskopie vede rovněž ke zkvalitnění disekce v oblasti mediastina a tím pádem umožňuje díky dokonalé vizualizaci periezofageálních struktur provedení kompletní mediastinální lymfadenektomie. Rovněž je redukováno riziko poškození trachey a zvratných nervů, krvácení z velkých cév mediastina či otevření tumoru během disekce [8]. Ve srovnání s otevřeným výkonem jsou redukovány pooperační bolesti, je kratší délka hospitalizace a časnější návrat k běžným aktivitám [9].
Laparoskopickým a torakoskopickým přístupem není ovlivněna pouze jedna velká komplikace a tou je dehiscence krční anastomózy.
Fernando [10] ve své studii srovnával kvalitu života pacientů, kteří podstoupili miniinvazivní ezofagektomii se zdravou populací a nebyly nalezeny signifikantní rozdíly v polykacích funkcích, gastrointestinální symptomatologii včetně regurgitace a přítomnosti kašle.
ZÁVĚR
V práci je na základě našich zkušeností, i když bohužel s malým souborem pacientů popsána technika miniinvazivní ezofagektomie s následnou náhradou jícnu žaludkem. Torakoskopický a laparoskopický přístup k provedení ezofagektomie s lymfadenektomií je metoda na jedné straně vyhovující požadavkům onkologické radikality, na straně druhé je spojena s minimalizací operačního traumatu a dokonalým přehledem, umožňujícím přesnou preparaci i v anatomicky obtížně přístupné oblasti hiátu a dolního mediastina.
doc. MUDr. Jan Dostalík, CSc.
Rudná 55
700 30 Ostrava
e-mail: jan.dostalik@fnspo.cz
Sources
1. Muller, J. M., Erasm, H., Stelzner, M., Zieren, U., Pilchmaier, H. Surgical therapy of oesophageal cancer. Br. J. Surg., 1990, 77 : 845–857.
2. Cuschieri, A., Shimi, S., Banting, S. Endoscopic oesophagectomy through a right thoracoscopic approach. J. R. Coll. Surg. Edinb., 1992, 37 : 7–11.
3. Shichinohe, T., Hirano, S., Kondo, S. Video-assisted esophagectomy for esophageal cancer. Surg. Today, 2008, 38 : 206–213.
4. Bumm, R., Feussner, H., Bartels, H., Stein, H., Dittler, H. J., Hofler, H., Siewert, Jr. Radical transhiatal esophagectomy with two - field lymphadenectomy and endodissection for distal esophageal carcinoma. World J. Surg., 1997, 21 : 822.
5. Gockel, I., Exner, C., Junginger, T. H. Morbidity and mortality after esophagectomy for esophageal carcinoma: a risk analysis. World J. Surg. Oncol., 2005, 21 : 37.
6. De Paula, A. L., Hashiba, K., Ferreira, E. A. B., De Paula, R. A., Grecco, E. Laparoscopic transhiatal esophagectomy with esophagogastroplasty. Surg. Laparosc. Endosc., 1995, 5 : 1–5.
7. Luketich, J. D., Alvelo-Rivera, M., Buenaventura, P. O., Christie, N. A., McCaughan, J. S., Little, V. R., Schaeuer, P. R., Close, J. M., Fernando, H. C. Minimally invasive esophagectomy. Outcomes in 222 patients. Ann. Surg., 2003, 238(4): 486–495.
8. Nguyen, N. T., Schauer, P. S., Luketich, L. D. Combined laparoscopic and thoracoscopic approach to esophagectomy. J. Am. Coll. Surg., 1999, 188 : 329–332.
9. Swanstrom, L., Hansen, P. Laparoscopic total esophagectomy. Arch. Surg., 1997, 132 : 943–949.
10. Fernando, H. C., Luketich, J. D. Quality of life after esophageal surgery. Thorac. Surg. Clin., 2004, 14 : 367–374.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2009 Issue 8-
All articles in this issue
- Výsledky jednoročního přežití u nemocných po resekci hlavy slinivky břišní s resekcí žil portomezenterické oblasti (PMO)
- Optimální miniinvazivní přístup při náhradě jícnu žaludkem
- GIST jako příčina invaginace na tenkém střevě
- Význam cytokeratinového markeru TPS v pooperačním sledování nemocných s kolorektálním karcinomem
- Transarteriální chemoembolizace u hepatocelulárního karcinomu jater
- 120 laparoskopických adrenalektomií s harmonickým skalpelem
- PTA krurálnych tepien u diabetikov
- Poúrazová svalová hernia predlaktia
- Léze podkolenní jamky s neurologickou symptomatologií – kazuistiky, diagnostika a léčba
- Léčení seniorů na okresním chirurgickém oddělení
- Přínos magnetické rezonance pro diagnostiku a léčbu poranění torakolumbální páteře
- Přínos ultrasonografie břicha v diagnostice akutní apendicitidy – naše zkušenosti
- PCCP versus standardní proximální femorální hřeb při léčbě pertrochanterických zlomenin femoru
- Operační rizika a význam předoperační péče
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Operační rizika a význam předoperační péče
- Léze podkolenní jamky s neurologickou symptomatologií – kazuistiky, diagnostika a léčba
- Transarteriální chemoembolizace u hepatocelulárního karcinomu jater
- Výsledky jednoročního přežití u nemocných po resekci hlavy slinivky břišní s resekcí žil portomezenterické oblasti (PMO)
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career