-
Medical journals
- Career
Praktická doporučení pro péči o dětské pacienty po transplantaci ledviny a jater
Authors: Jakub Zieg 1; David Bauer 2; Vlasta Krejčová 1; Lucie Gonsorčíková 2
Authors‘ workplace: Pediatrická klinika 2. LF UK a FN Motol, Praha 1; Pediatrická klinika 1. LF UK a FTN, Praha 2
Published in: Čas. Lék. čes. 2022; 161: 296-302
Category: Guidelines
Overview
Počet provedených orgánových transplantací v dětském věku v čase stoupá. Tato léčba vede často ke zlepšení kvality života nemocných, ale zároveň přináší i některé specifické komplikace. Náš článek shrnuje praktická doporučení pro dlouhodobou péči o děti po transplantaci ledviny a jater. Povědomí o transplantační problematice je zásadní právě pro pediatry prvního kontaktu, jejichž spolupráce s lékaři transplantačního centra významně přispívá k správné péči o tyto pacienty.
Klíčová slova:
transplantace jater – transplantace ledviny – sport – adherence – medikace
ÚVOD
Vzhledem k nárůstu počtu transplantací (Tx) solidních orgánů v dětské populaci se nemocniční i praktičtí pediatři stále častěji setkávají s transplantovanými pacienty. Díky pokrokům v chirurgických technikách i ve vývoji nových léčiv se orgánová Tx stává obvykle optimální terapeutickou metodou umožňující vést nemocným se selhávajícím orgánem znovu kvalitní život.
Je proto velmi žádoucí, aby nemocniční i ambulantní pediatři byli s problematikou Tx dobře obeznámeni a zároveň zahrnuti do péče o tyto pacienty. Právě lékaři prvního kontaktu mají představovat další úroveň podpory pro transplantované pacienty, rozumět jejich speciálním potřebám a tím zlepšovat kvalitu života nemocných dětí i přežití transplantovaných orgánů. V našem přehledovém článku jsme se zaměřili na problematiku dětí po Tx ledvin a jater.
PŘÍPRAVA PŘED TRANSPLANTACÍ
Provedení Tx vyžaduje speciální přípravu příjemce transplantovaného orgánu. V případě Tx ledviny lze transplantovat jen jedince určité váhové kategorie (v našem centru s vahou ≥ 10 kg), hlavně vzhledem k rizikům trombotických komplikací po výkonu.
Dárce ledviny může být buď živý (např. rodič), nebo neživý (zemřelá osoba, jejíž orgán byl poskytnut za účelem provedení Tx). V případě neživého dárcovství je příjemce po splnění kritérií a po podrobném vyšetření zařazen na čekací listinu k Tx ledviny. Transplantovat lze děti v konečném stádiu chronického onemocnění ledvin, které jsou do doby Tx léčené dialýzou nebo je možné Tx ledviny provést u dítěte bez předchozí dialyzační léčby. V takovém případě hovoříme o preemptivní Tx ledviny.
Obecně přináší živé dárcovství a provedení preemptivní Tx příjemcům výhody spojené s lepším dlouhodobým přežíváním transplantované ledviny. Nejčastější indikací provedení Tx ledviny jsou vrozené vady ledvin, chronické glomerulonefritidy a hereditární/cystická onemocnění ledvin. Před provedením Tx děti podstupují řadu nezbytných vyšetření včetně urologického a psychologického posouzení. Součástí předtransplantační přípravy je i vakcinace. Většina dárců pro dětské ledvinné transplantace jsou dospělí jedinci. Živí dárci před odebráním orgánu podstupují rovněž podrobné vyšetření, kde se posuzuje jejich vhodnost i rizika odebrání orgánu pro ně samé. (1)
Indikací k Tx jater u dětí bývá nejčastěji chronické či akutní jaterní selhání, ale je to i terapeutická volba pro pacienty s vybranými dědičnými poruchami metabolismu, kdy pomocí Tx jater substituujeme geneticky podmíněný enzymatický defekt u jedince, který nemá alterované jaterní funkce. Vzhledem k nepoměru velikosti jater dospělého člověka a dítěte a omezené nabídce vhodných dárcovských orgánů vyžaduje dětská Tx jater speciální chirurgické techniky, mezi které patří transplantace redukovaného štěpu (dárcovský orgán má redukovanou svoji původní velikost) či použití splitovaného štěpu (dárcovský orgán je rozdělen mezi dva příjemce, pro dítě je to nejčastěji levostranný segment II a III). Speciální technikou je auxiliární transplantace, vhodná například pro pacienty, u kterých předpokládáme regeneraci vlastních jater, kdy je příjemci část jeho orgánu ponechána a část je nahrazena štěpem.
Tx jater lze provést dětem již od novorozeneckého věku. Po splnění indikačních kritérií a nezbytných předtransplantačních vyšetření je pacient zařazen na čekací listinu. Játra lze transplantovat také od dárce živého či neživého (2).
MEDIKACE
IMUNOSUPRESIVNÍ TERAPIE
Transplantovaní pacienti obvykle užívají celoživotně imunosupresivní medikaci, která může být zatížena různými nežádoucími účinky. Právě pravidelné užívání léků je pro dlouhodobou dobrou funkci transplantovaného orgánu naprosto zásadní. Ošetřující lékaři i pacienti by měli znát interakce užívaných medikamentů s dalšími léčivy, případně s některými potravinami.
Imunosupresivní terapii rozdělujeme na indukční, podávanou v době provedení Tx, a udržovací, jež děti užívají dlouhodobě. Většina dětí po Tx ledviny je léčena v našem centru v rámci udržovací léčby trojkombinaci imunosupresiv takrolimem, mykofenolát mofetilem a prednisonem. Takrolimus patří spolu s dříve více užívaným preparátem cyklosporinem A do skupiny kalcineurinových inhibitorů (CNI). Mykofenolát mofetil, který postupně nahradil v této indikaci azathioprin, se řadí mezi antimetabolity. Některá pracoviště používají navíc injekční indukční léčbu monoklonálními či polyklonálními protilátkami v peritransplantačním a časném potransplantačním období. Imunosupresivní léčba se může lišit v závislosti na praxi transplantačního centra a medikace i její dávky se upravují v čase podle vývoje zdravotního stavu dítěte (3).
Játra jsou ve srovnání s ledvinou imunotolerantnějším orgánem. V rámci indukční léčby po Tx jater se v našem centru podává monoklonální protilátka basiliximab a je zahajována kombinovaná imunosupresivní terapie kortikosteroidy a takrolimem, u dětí nad 15 let se přidává i mykofenolát mofetil. V týdnech následujících Tx je prednison postupně vysazen. K dlouhodobé udržovací imunosupresi se zpravidla používá takrolimus v monoterapii. Přístupy jednotlivých center se mohou lišit, alternativně se používají i léky, jako je cyklosporin A, everolimus či sirolimus (4). Nastavení imunosupresivní terapie Tx jater i ledvin je přísně individuální a dávky imunosuprese se řídí podle jejich hladiny v krvi či se vypočítávají dle tělesného povrchu pacienta. Cílem je vyvážit léčbu tak, aby byla zajištěna optimální dávka imunosupresiv a zároveň aby pacient nebyl významně zatížen jejich nežádoucími účinky.
Nejčastěji používaná imunosupresiva, jejich nežádoucí účinky i možné lékové interakce shrnuje tab. 1. Podávání řady léků mění sérové hladiny imunosupresiv, proto je při nasazování nové medikace nutno na lékové interakce pomýšlet. Známe i některé potraviny, které ovlivňují metabolismus podávaných léků. Všechna imunosupresivní léčiva jsou v porovnání s ostatní populací potencionálně spojena se zvýšenou náchylností k infekcím a vyšším rizikem vzniku některých malignit. Z toho vyplývají další režimová opatření. Obecně se u pacientů po Tx ledviny doporučuje používat nefrotoxické léky pouze v případě nutnosti a se zvýšenou opatrností, dále je nutné redukovat dávky medikace dle aktuální funkce ledvin, případně monitorovat hladiny těchto léčiv v krvi (5).
Table 1. Přehled nejčastěji předepisovaných imunosupresiv u pacientů po orgánové transplantaci 
Table 2. Nejobvyklejší látky, jež ovlivňují sérové hladiny kalcineurinových inhibitorů (CNI) (6) 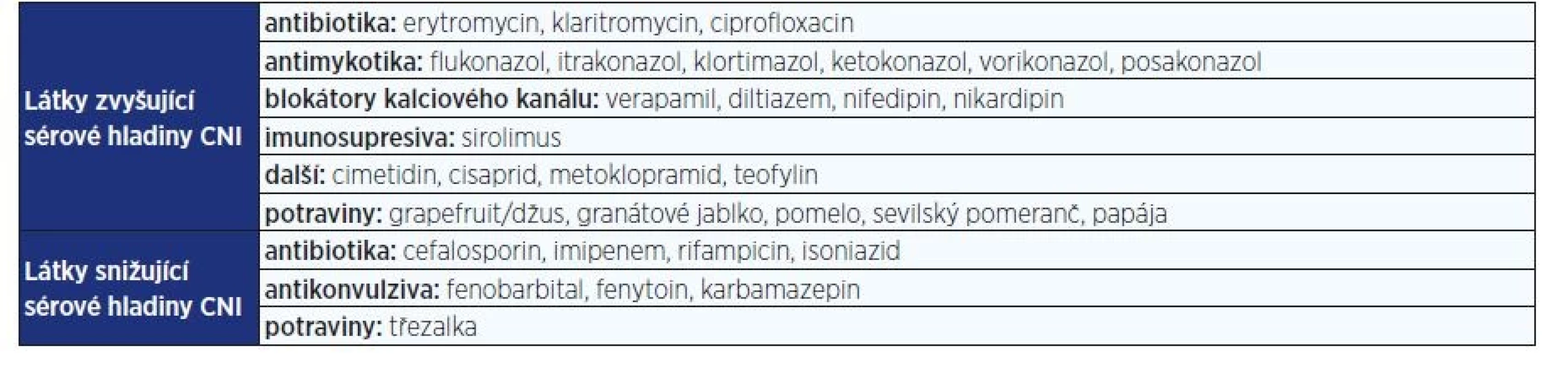
Problém s užíváním medikace může nastat v případě, že pacient zvrací. Pokud dítě zvracelo více než hodinu po požití léku, nemusí být znovu podán. Jestliže je tato doba kratší, je vhodné se řídit tab. 3.
Table 3. Doporučený postup u dítěte se zvracením (7) 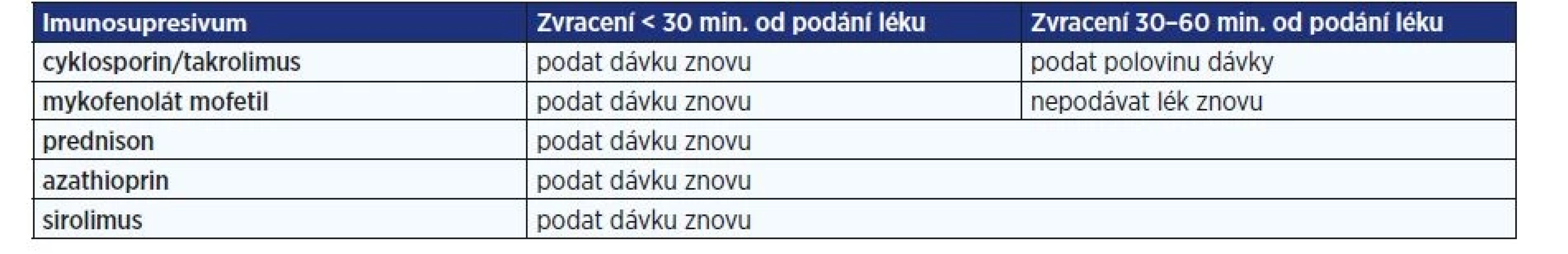
Protiinfekční terapie
K prevenci a léčbě CMV infekce se po Tx používá lék valganciklovir. Jeho indikace i doba podávání se řídí výchozí situací pozitivity/negativity dárce a příjemce z hlediska přítomnosti CMV.
K zajištění prevence zejména infekce močových cest a k ochraně před oportunní nákazou Pneumocystis jiroveci slouží sulfametoxazol/trimetoprim. Obvyklá doba jeho podávání je 6–12 měsíců po Tx, jelikož většinou se infekce objeví právě od 1.–6. měsíce po Tx a riziko jejího vzniku stoupá s intenzitou imunosupresivní léčby. Diagnostika nákazy spočívá v přímém průkazu původce v plicích (8).
Obecně také stoupá u transplantovaných pacientů incidence infekcí vyvolaných původci s vysokou mírou rezistence. Mezi rizikové faktory jejich rozvoje patří opakované podávání antibiotik, dlouhodobá antibiotická profylaxe močových infekcí či aktivní antimikrobní léčba asymptomatické bakteriurie.
Ostatní léky
Vzhledem k riziku trombotických komplikací je po Tx jater vhodné několikaměsíční zajištění antiagregační terapií pomocí kyseliny acetylsalicylové, v prvním měsíci po jaterní Tx se užívá antikoagulační terapie nízkomolekulárním heparinem. Antiagregační či antikoagulační léčba má u selektovaných příjemců transplantovaných ledvin své využití i v časném potransplantačním období (9).
Do chronické medikace transplantovaných pacientů dále často patří antihypertenziva, substituce vitamínů, elektrolytů a stopových prvků, eventuálně další léky, jako např. u dětí po Tx jater kyselina ursodeoxycholová.
ČASNÉ POTRANSPLANTAČNÍ OBDOBÍ
Po Tx ledviny i jater pacienti obvykle zůstávají hospitalizovaní 3–4 týdny k pooperační péči a k optimálnímu nastavení imunosupresivní terapie. Délka jejich hospitalizace je ovlivněna jejím průběhem a přítomností časných komplikací (mezi nejčastější patří chirurgické komplikace, jako je krvácení, prosakování ze žlučových cest či obstrukce vývodných močových cest, trombotické komplikace a primární dysfunkce štěpu).
Po propuštění do domácího ošetřování jsou naplánovány čtyři kontroly po týdnu, dále dvě kontroly v intervalu 14 dní, poté již probíhá ambulantní sledování v intervalu 4–5 týdnů. Pokud je průběh jejich hojení bez komplikací, děti se vrací zpátky do školy za 2–3 měsíce po proběhlé Tx ledviny, u dětí po Tx jater je návrat ke školní docházce zpravidla delší, cca po 6 měsících (10).
Učitelé by měli být poučeni o nutnosti časně informovat rodiče o případném rizikovém kontaktu dítěte s nakažlivou chorobou (neštovicemi, chřipkou, SARS-COV2). Ve stejném období se mohou děti začít zapojovat do pohybových aktivit – fyzická aktivita je po Tx doporučována a přispívá k lepší kvalitě života (7).
NEJČASTĚJŠÍ KOMPLIKACE U DĚTÍ PO TX
INFEKČNÍ KOMPLIKACE
Nejčastější komplikací ohrožující transplantované pacienty je infekce. Záhy po Tx (v prvních 30 dnech) jsou transplantované děti ohroženy hlavně bakteriální či mykotickou infekcí. Následně (mezi 31. a 180. dnem) jsou pacienti po Tx nejvíce v riziku vzniku latentních virových infekcí (EBV, CMV). Chronická aktivita EBV může vést k rozvoji tzv. PTLD (post-transplant lymphoproliferative disease), která se projevuje vzhledem k imunosupresivní terapii jako nekontrolovaná proliferace imunitních buněk (obvykle B lymfocytů) bez kontroly T lymfocyty.
EBV infekce může probíhat bezpříznakově nebo se projevuje nespecifickými symptomy podobnými CMV infekci (11). CMV infekce se může manifestovat systémovým i orgánovým postižením, jako je např. CMV kolitida. Z tohoto důvodu je vhodné při pravidelných kontrolách monitorovat aktivitu EBV i CMV pomocí vyšetření PCR. U dětí po Tx ledviny monitorujeme také aktivitu BK viru, jenž může ohrozit funkci štěpu. Dále se u transplantovaných pacientů objevují virové a také komunitní infekce a tyto děti mají i větší náchylnost k onemocněním vyvolávaným oportunními patogeny. Bakteriální infekce by měly být zavčas rozpoznány a léčeny antibiotiky.
Nejčastějšími bakteriálními infekcemi u dětí po Tx ledviny jsou infekce močových cest, u dětí po Tx jater cholangitida. V časném potransplantačním období se vyskytují také ranné infekce (12). Pacient s horečkou bez jaterní dysfunkce může užívat paracetamol dle zvyklého dávkování. Tomuto preparátu dáváme obecně přednost i u dětí po Tx ledviny. Pokud má dítě dobrou funkci štěpu a jeho stav to vyžaduje, lze použít i ibuprofen, ale jen po nezbytně nutnou dobu vzhledem k riziku rozvoje nežádoucích účinků. Obecně je vhodné se u dětí po Tx ledviny nesteroidním analgetikům spíše vyhýbat (7).
Při kontaktu s neštovicemi u jedince bez dostatečného titru anti-VZV protilátek je na místě podat hyperimunní imunoglobulin proti varicele co nejdříve po expozici (max. do 10 dnů) a následně pacientovi předepsat antivirotikum acyklovir. Důležité je separovat imunosuprimovaného pacienta od nemocného s kožní manifestací VZV infekce. Očkování proti neštovicím lze dětem podat již od 9 měsíců věku (13). Transplantovaní pacienti by také neměli manipulovat s plenami dětí po očkování proti rotavirům nejméně po dobu čtyř týdnů od podání vakcíny (12).
Pacienti po Tx mohou trpět častějšími mykotickými infekcemi, nejčastěji je vyvolává Candida. Mykotické afekce v dutině ústní se u imunosuprimovaných pacientů vyskytují obvykleji. U mírnějších forem postačí lokální antimykotická léčba, závažnější infekce se léčí antimykotiky podávanými perorálně či parenterálně. Řada antimykotik ale interferuje s metabolismem kalcineurinových inhibitorů, proto je nutná úprava jejich dávek (14). U dětí po Tx se mohou v dutině ústní v rámci infekce nebo v souvislosti s podávanou medikací vyskytovat ulcerace. Vzácně se můžeme setkat s infekcí Mycobacterium tuberculosis obvykle v důsledku reaktivace latentní infekce. U jedinců léčených imunosupresí probíhá toto onemocněni častěji pod obrazem diseminované formy (15).
Rejekce
Rejekce je zánětlivá reakce zprostředkovaná imunitním systémem příjemce s charakteristickými změnami v transplantovaném orgánu se známkami či bez známek jeho dysfunkce. Rozlišujeme rejekci celulární a humorální, protilátkami zprostředkovanou. U pacientů po Tx patří rejekce k častým komplikacím. U Tx jater se nejčastěji setkáváme s akutní celulární rejekcí v období prvních třech měsíců po Tx, k rejekci ale může dojít i kdykoli později.
Většina pacientů s rejekcí je asymptomatických, mezi charakteristické příznaky rejekce patří teplota nad 38 °C se zimnicí a třesavkou, slabost, nauzea a zvracení, tlak v pravém podžebří, může se objevit i ikterus a acholické stolice. Laboratorně nacházíme zvýšené hodnoty aminotransferáz i cholestatických enzymů. Diagnózu je zapotřebí potvrdit biopticky. Chronická rejekce se může vyskytnout i mnoho měsíců nebo let po Tx jater, nejčastěji vlivem nesprávného užívání imunosupresivní terapie nebo nedostatečně léčené akutní rejekce. Jejím nejčastějším příznakem je hubnutí, únava, ikterus a pruritus. Chronická rejekce je nepříznivá komplikace vedoucí často ke ztrátě jaterního štěpu. Humorálně zprostředkovaná rejekce je u pacientů po Tx jater vzácná (16).
U pacientů po Tx ledviny máme podezření na rejekci při zjištění zhoršené funkce transplantované ledviny. Rozvoj klinických příznaků v podobě horečky a bolestivosti v okolí štěpu při pozdní diagnóze v současné době již vídáme vzácně. Diagnostika rejekce je stejně jako v případě jater bioptická na základě vyhodnocení histologie renální tkáně. Dle mechanismu vzniku rozlišujeme hyperakutní rejekci, akutní celulární rejekci a akutní a chronickou protilátkovou rejekci. Léčba rejekcí se liší v závislosti na jejich typu (17).
Horečka
Horečka u dítěte po Tx může být známkou infekce, rejekce nebo přítomnosti malignity, příp. polékové reakce. Jelikož infekce představují hlavní příčinu horeček, mohou lékaři prvního kontaktu provést základní diagnostiku i terapii infekčních komplikací a v případě potřeby konzultovat transplantační centrum, eventuelně tam pacienta následně odeslat (10).
Gastrointestinální obtíže a obezita
Asi 22 % dětí prodělá v prvních třech letech po Tx ledviny průjmovité onemocnění. V diferenciální diagnostice je nutno zvažovat infekci (bakteriální, virovou, parazitární) a polékový průjem (vyvolaný mykofenolát mofetilem či takrolimem). Vyloučení infekční etiologie je nutné před stanovením diagnózy s medikací asociovaného průjmu (18).
Nemocní po Tx jsou ve zvýšené míře ohroženi vzestupem hmotnosti a obezitou – často v souvislosti s léčbou kortikoidy a při nedostatku pohybu (19). Obezita je spojena nejen s rizikem kardiovaskulárních komplikací ale i s vyšší pravděpodobností selhání transplantovaného orgánu, u jater navíc existuje riziko rozvoje steatózy až steatohepatitidy ve štěpu (20).
Hypertenze
Hypertenze je obecně častou komplikací u dětí po Tx solidních orgánů. V časném období může vzniknout díky volumovým změnám. Mezi další příčiny patří stav dárcovské ledviny, nežádoucí účinky imunosupresivní terapie (CNI, kortikoidy) či postižení transplantovaného orgánu (ledviny) de novo. V případě Tx ledviny může hypertenzi vyvolat i stenóza renální arterie, která se vyskytuje asi u 4–6 % transplantovaných dětí (21). Hypertenze je obvykle v těchto případech závažná se špatnou reakcí na podávanou léčbu. Pacientům po Tx by měl být při kontrolách pravidelně monitorován krevní tlak a dle potřeby zahájena antihypertenzní terapie. Cílový krevní tlak dle ambulantní 24hodinové monitorace tlaku je < 90. percentil. V rámci léčby se zaměřujeme na nefarmakologická opatření – omezení příjmu soli a prevenci obezity, v případě nutnosti zahájení terapie obvykle volíme blokátor kalciových kanálů případně v kombinaci s inhibitorem ACE (22).
Porucha růstu a puberty
Na růstové retardaci a opoždění puberty transplantovaných pacientů se podílí závažnost onemocnění, které vedlo k provedení Tx, malnutrice a terapie steroidy. V poslední době řada studií prokázala, že u selektované skupiny pacientů po Tx ledviny lze kortikoidy vysadit časně či s odstupem času bez zvýšeného rizika vzniku rejekce (23).
U dětí po Tx je nutné vést pečlivě růstové grafy a sledovat trend růstové rychlosti stejně tak jako popsat pubertální rozvoj dle Tannerovy stupnice. Po úspěšně provedené Tx je často patrný růstový výšvih (catch-up), většinou po 6 měsících od Tx, kdy již bývají významně snížené dávky kortikosteroidní terapie a očekává se celkové zlepšení nutričních i dalších parametrů. V případě přetrvávajícího nedostatečného růstu či opoždění puberty je vhodná konzultace dětského endokrinologa (24).
Potransplantační diabetes mellitus a dyslipidémie
Rozvoj potransplantačního diabetu mellitu a dyslipidémie (PTDM) je u dětských pacientů po transplantaci solidních orgánů poměrně častou komplikací, v případě Tx ledviny se jejich incidence udává 8–13 %, u Tx jater 13 % (25, 26). Riziko rozvoje PTDM souvisí s více faktory, mezi které patří imunosupresivní terapie (zejména steroidy a takrolimus), roli hraje také nosičství určitých kandidátních genů, přítomnost rejekce, aktivita CMV, obezita či etnikum (27). Steroidy se při vzniku PTDM uplatňují různými mechanismy, zvyšují inzulinovou rezistenci a glukoneogenezi v játrech, zvyšují apetit a s tím související výskyt obezity. V některých studiích bylo prokázáno, že takrolimus má vliv na snižování počtu β buněk tím, že indukuje jejich apoptózu. Diagnostika spočívá v provedení glukózového orálního tolerančního testu, rizikoví pacienti se odhalí skríningovým vyšetřením lačné glykémie a glykovaného hemoglobinu. Léčba PTDM se odvíjí od závažnosti stupně hyperglykémie – někdy je stav přechodný a po vysazení kortikoterapie a dietních opatřeních ustoupí, jindy je nutná dlouhodobá léčba inzulinem ve spolupráci s diabetologem (28).
Dyslipidémie je u transplantovaných dětí častá a přispívá ke kardiovaskulární morbiditě a mortalitě. Užívání cyklosporinu A a kortikoidů je spojeno s elevací hladin triacylglycerolů a non-HDL cholesterolu v séru. Také podávání inhibitorů mTOR (sirolimu, everolimu) vede ke zvýšení hladiny sérového non-HDL-c. Nutriční poradenství, případně úprava imunosupresivní terapie patří mezi hlavní léčebná opatření (21).
Malignity
Děti po orgánové Tx jsou obecně ve zvýšeném riziku vzniku malignity, jejíž kumulativní incidence stoupá s časem. Dlouhodobé riziko vzniku onkologického onemocnění u dětí po orgánové Tx je ve srovnání s obecnou populací 22–33krát vyšší (29). Mezi nejčastější patří nádory kůže, které se obvykle objevují v dospělosti – dlaždicobuněčný karcinom a bazaliom. Dlaždicobuněčný karcinom se charakteristicky vyskytuje na místech exponovaných slunečnímu záření, k jeho vzniku přispívá ultrafialové záření a infekce HPV (human papilloma virus) v kombinaci s imunosupresivní léčbou. Po Tx se setkáváme také s vyšším výskytem melanomu (30).
Vzácnou, ale obávanou malignitou vznikající po orgánové Tx je PTLD (viz výše). Představuje heterogenní skupinu onemocnění charakterizovaných nekontrolovanou proliferací B lymfocytů. Vyskytuje se nejčastěji v prvních dvou letech po Tx. Mezi hlavní rizikové faktory vzniku PTLD patří EBV pozitivní dárce / EBV negativní příjemce, trvání užívání imunosupresivní léčby a přítomnost aktivní CMV infekce. Časná forma PTLD je ve většině případů asociovaná s EBV infekcí, pozdní forma vzniká v souvislosti s dlouhodobou imunosupresí, představuje asi 10 % případů a má horší prognózu. Symptomatologie PTLD je značně variabilní a nespecifická, proto na toto onemocnění musíme pomýšlet v rámci diferenciální diagnostiky řady stavů. PTLD se může manifestovat mimo jiné pod obrazem tonzilární hypertrofie, v diagnostice využíváme řadu zobrazovacích vyšetření. Prvním léčebným opatřením je redukce imunosuprese, dle výsledků vyšetření je poté na místě podání imunoterapie, chemoterapie, chirurgická excize a další (31).
DOPORUČENÍ PRO DLOUHODOBOU PÉČI O TRANSPLANTOVANÉ PACIENTY
PSYCHOSOCIÁLNÍ RIZIKA
Tx obvykle představuje velkou psychickou zátěž jak pro pacienta, tak pro jeho rodinu. Psychické obtíže zahrnují stres, depresi, úzkosti, posttraumatickou stresovou poruchu, poruchu pozornosti s hyperaktivitou, pocit závislosti na druhých a pocity viny. Zátěž souvisí i s nutností přerušení školní docházky a s omezením kontaktu s vrstevníky. Při péči o pacienty po Tx je nutno na tuto problematiku pamatovat, přičemž praktický pediatr, který zná dobře i pacientovo rodinné zázemí, hraje v tomto významnou roli. Je důležité se ptát na to, jak se pacient cítí, jak zvládá běžnou činnost a školu, jak tráví svůj volný čas a co by si přál zlepšit. V případě potřeby je nezbytné včas vyhledat péči psychologa event. psychiatra, výhodná je též skupinová či rodinná terapie (32).
Očkování
Dětští příjemci transplantovaného orgánu by měli absolvovat věkově adekvátní očkování před Tx. Živé vakcíny by měly být podány alespoň 4 týdny před Tx, neživé vakcíny alespoň 2 týdny před výkonem. Splnění očkovacího plánu je v rukách praktického pediatra, často ve spolupráci s očkovacím centrem. Podání neživých vakcín se vzhledem k očekávané nižší postvakcinační protilátkové odpovědi v časném potransplantačním období obvykle odkládá na období tři až šest měsíců po Tx. Pokud pacient splňuje určité podmínky, zejména dostatečný časový odstup od Tx (alespoň jeden rok) a normální hodnoty při vyšetření buněčné imunity, lze očkování živou vakcínou doplnit nově i po úspěšně provedené Tx (13).
Pacienti po orgánové Tx by měli být každoročně očkováni proti influenze (lze již měsíc po Tx), v současné době je též doporučováno přeočkování proti COVID-19. Povinnou vakcinaci včetně živých vakcín by měly podstoupit také blízké domácí kontakty (13).
Dietní opatření
Pacienti s chronickým onemocněním ledvin i jater trpí často nechutenstvím a mají zároveň řadu dietních omezení, u ledvin včetně restrikce tekutin. Po transplantaci je dieta uvolněna, doporučuje se pestrá racionální strava s dostatečným zastoupením ovoce a zeleniny, vlákniny a celozrnných produktů. Vhodná je též dieta bohatá na bílkoviny, kalcium a vitamin D, žádoucí je naopak omezit potraviny s vysokým obsahem cukru, soli a nasycených mastných kyselin. Důležité je dbát na dostatečný přísun tekutin z nekontaminovaných zdrojů.
Právě pediatři hrají zásadní roli v monitoraci růstu a váhy dítěte a v zajištění jeho adekvátních nutričních potřeb. Některá transplantační centra doporučují nekonzumovat rizikové potraviny, např. nepasterizovaný sýr. Pro tato doporučení nemáme ale dostatek důkazů. Důležité je správné skladování potravin a důsledná hygiena při přípravě pokrmů (7). V případě chronického onemocnění spojeného s malnutricí je nutné i po Tx někdy přistoupit k sondové výživě či zavedení gastrostomie, přičemž je snaha postupně ve spolupráci s logopedem a fyzioterapeutem pracovat na obnově dostatečného perorálního příjmu.
Doporučení pro manipulaci s potravinami:
- Myjte si ruce často, obzvláště před kontaktem s potravinami.
- Omývejte ovoce a zeleninu pod tekoucí vodou.
- Při skladování v lednici oddělte ostatní potraviny od syrového masa.
- Pravidelně čistěte dřez i odkapávač na nádobí dezinfekčním prostředkem k tomu určeným.
- Požívejte teploměr k ozřejmění teploty vařeného masa.
- Hamburgery a tepelně upravené uzeniny musí být v rámci přípravy vystaveny dostatečné teplotě (160 ̊C).
- Snažte se vyhnout ohřívaným pokrmům, vaření a pečení je vhodnější než smažení.
Dentální péče
Péče o chrup by po Tx měla být stejná jako v případě zdravých vrstevníků, pravidelné kontroly stomatologem jsou důležité. Stomatologické vyšetření je součástí předtransplantačního vyšetření s cílem vyloučit přítomnost infekčního fokusu, který musí být před provedením Tx sanován. U dětí užívajících cyklosporin A se často rozvíjí hyperplazie gingiv, která si u některých vyžádá chirurgické ošetření (33).
Domácí zvířata
Chování domácích zvířat přináší dítěti řadu emocionálních i fyzických benefitů. Většina běžných domácích zvířat nepředstavuje pro transplantované pacienty při dodržování hygienických pravidel (důsledné mytí rukou po kontaktu se zvířaty, obzvláště před konzumací jídla, vyloučení manipulace se zvířecími exkrementy, čištění klecí, terárií apod.) a adekvátní péči veterináře o domácí mazlíčky (kontroly, imunizace, pravidelné dávky antiparazitárních medikamentů) větší riziko. Doporučováno není pro vyšší riziko nákazy salmonelou pouze chování plazů (34).
Cestování
Děti po orgánové Tx mohou cestovat do zahraničí za předpokladu dodržení několika podmínek: Vzhledem k možnému riziku zdravotních komplikací musí být dítě řádně pojištěno na cestu. S sebou musí být pacient vybaven dostatečným množstvím užívané medikace, kterou má během přepravy vždy v příručním zavazadle. Vhodné je také mít na cestu s sebou lékařskou zprávu v anglickém jazyce shrnující současný zdravotní stav dítěte a doporučení ošetřujícího lékaře. Je nutné ověřit, jaké očkování je v destinaci povinné vzhledem k tomu, že některé vakcíny nejsou po Tx vhodné. Naprosto zásadní je dodržovat hygienická opatření – mytí rukou, skladování potravin, rizika konzumace kontaminované vody. Důležité je zamezit přehřátí organismu a vyvarovat se pobytu na přímém slunci (13).
Ochrana před slunečním zářením
Nejčastější malignitou postihující pacienty po orgánové Tx jsou zhoubné kožní nádory, proto je právě u těchto jedinců velmi důležité dodržování ochrany pokožky před slunečním zářením. Rizikové faktory vzniku kožní malignity jsou bledá pokožka (fototyp I a II, kumulativní doba vystavení pokožky slunečnímu záření, intenzita a doba užívání imunosupresivní léčby) (35, 36).
Pacienty je nutné důkladně poučit o rizicích spojených s expozicí slunečnímu záření a o možnostech, jak předcházet jejím následkům. Děti s pigmentovými névy, mateřskými znaménky by měly být pravidelně sledováni dermatologem. Důležité je minimalizovat expozici slunečnímu záření v době jeho nejvyšší intenzity (10.–14. hodinou). Doporučuje se denní užívání opalovacího krému s dostatečným faktorem ochrany, nošení slunečních brýlí, oblečení z přiléhavé tkaniny s dlouhými rukávy a nošení pokrývky hlavy – klobouku, kšiltovky (37).
Doporučení pro používání opalovacího krému:
- Volte krém s dostatečnou ochranou proti UVA a UVB záření a zároveň s odolností proti otěru a vodě (faktor SPF 30 a více).
- Nanášejte opalovací krém přibližně 30 min před expozicí slunečnímu záření.
- Neopomíjejte krémem namazat všechna místa vystavená slunci rovnoměrně a v dostatečné vrstvě (2 g/cm2).
- Opalovací krém nanášejte na pokožku opakovaně – ideálně každé 2 hodiny.
- Aplikujte krém znovu po plavání či po fyzické aktivitě spojené s pocením.
- Užívejte krém v souladu s doporučením výrobce.
Fyzická aktivita a sport
Fyzická aktivita u dítěte po Tx je stejně jako u dětí zdravých žádoucí a důležitá pro jejich zdraví, motorický vývoj, fyzickou kondici i sociální rozvoj. Děti se také jako jejich vrstevníci, pokud to jejich zdravotní stav dovolí, mohou aktivně účastnit sportovních kroužků a aktivit. Volba sportu závisí na preferencích dítěte a jeho rodičů a dále na míře rizika možnosti poranění transplantovaného orgánu. Na místě je využití ochranných prostředků pro sport. Vhodná je aerobní aktivita po dobu alespoň 30–60 min 6krát týdně. Ne zcela vhodné jsou kontaktní sporty, při nichž hrozí úder do břicha (7).
Adherence a tranzice
Nejčastější příčinou ztráty transplantované ledviny či jater v adolescenci je neadherence, která se nejobvykleji projevuje neužíváním či vynecháváním medikace. Mezi další projevy neadherence patří nedodržování termínů kontrol či doporučení stran režimových opatření. K prevenci komplikací spojených s neadherencí přispívají spolu s péčí lékařů a psychologů dohled rodičů nad užíváním medikace a internetové aplikace. Pacienti v časné adolescenci by si měli sami začít připravovat medikaci pod dohledem.
K hladkému převedení transplantovaných pacientů z péče pediatrů do péče dospělého transplantačního centra napomáhá program tranzice zdravotní péče. Jedná se o proces plánované snahy připravit dětského pacienta na přechod z modelu „pečující osoba a pacient“ na model „zodpovědné péče pacienta o sebe samého“ v dospělosti. Tranzice podporuje pacientovu nezávislost, schopnost komunikovat o svých zdravotních problémech a rozhodovat se o jejich řešení. Zavedení tranzice přispělo ke zvýšení kvality i života i ke zlepšení přežívání transplantovaných orgánů (38).
Role praktického lékaře
Praktický lékař by měl při péči o transplantovaného pacienta spolupracovat s lékaři transplantačního centra. Jeho hlavní úlohou je dlouhodobá komplexní péče o děti včetně vakcinace, monitorace růstu a vývoje a prvotního posouzení zdravotního stavu v případě akutního onemocnění. Hlavním úkolem pediatra prvního kontaktu je včasná správná diagnostika a léčba interkurentních infekcí a rozpoznání situace, kdy terapie pacienta vyžaduje hospitalizaci, eventuálně konzultaci transplantačního centra. Neméně důležité je jeho dobré povědomí o transplantační problematice, režimových opatřeních a psychosociálních aspektech s ní spojených.
ZÁVĚR
Péče o transplantované pacienty je komplexní a vyžaduje spolupráci lékařů mnoha odborností a dalších odborníku zdravotnických i nezdravotnických profesí. Komunita praktických lékařů představuje u těchto dětí důležitý segment v léčbě. Správné porozumění základním aspektům transplantační problematiky přispívá ke zvýšení kvality života pacientů po Tx solidních orgánů.
Čestné prohlášení
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Adresa pro korespondenci:
doc. MUDr. Jakub Zieg, Ph.D.
Pediatrická klinika 2. LF UK a FN Motol
V Úvalu 84, 150 06 Praha 5
Tel.: 224 432 059
e-mail: jakub.zieg@lfmotol.cuni.cz
Sources
1. Zieg J, Skálová S. Dětská nefrologie do kapsy. Mladá fronta, Praha, 2019.
16. Pham YH, Miloh T. Liver transplantation in children. Clin Liver Disease 2018; 22 : 807–821.
30. Dreno B. Skin cancers after transplantation. Nephrol Dial Transplant 2003; 18 : 1052–1058.
37. Bartosh S, Dipchand A, Chavers B, Pediatric Kidney Transplantation. A Guide for Patients and Families. American Society of Transplantation, 2015. Dostupné na: www.erknet.org/patient_info/Pediatric_Kidney_Transplantation_BrochureAST__-_final_copy_2015-06-27_0.pdf
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental Hygienist
Article was published inJournal of Czech Physicians

-
All articles in this issue
- ÚVODEM
- Mezinárodní kodex lékařské etiky Světové lékařské asociace
- V roce 2022 bylo Světovou lékařskou asociací (WMA) přijato nové znění etického kodexu – co nového přináší?
- Etické zásady pro používání a sdílení genomických dat z výzkumu
- Indikace metabolické a bariatrické chirurgie – ASMBS/IFSO 2022
- Nové bariatrické postupy a etika v bariatrické chirurgii – stanovisko IFSO
- Praktická doporučení pro péči o dětské pacienty po transplantaci ledviny a jater
- Permanentní močový katétr – dobrý sluha, zlý pán: Doporučení pro prevenci, diagnostiku a léčbu močových infekci spojených s katetrizací
- Pravidla výběru hormonální léčby v klimakteriu a její alternativy
- Nízké hladiny vitaminu D v populaci exponované významnému znečištění životního prostředí
- Využití extrakorporální membránové oxygenace (ECMO) v léčbě kritického průběhu pneumonie
- Imunita po koronavirové infekci jako podle učebnice
- Trendy lázeňství v době postkovidové, dopady a perspektivy
- Spolek českých lékařů v Praze a jeho činnost v posledních desetiletích
- 160 let české medicíny prizmatem 16 jubileí Spolku českých lékařů na stránkách Časopisu lékařů českých
- Zemřel profesor Miroslav Ryska
- Journal of Czech Physicians
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Permanentní močový katétr – dobrý sluha, zlý pán: Doporučení pro prevenci, diagnostiku a léčbu močových infekci spojených s katetrizací
- Imunita po koronavirové infekci jako podle učebnice
- Pravidla výběru hormonální léčby v klimakteriu a její alternativy
- Využití extrakorporální membránové oxygenace (ECMO) v léčbě kritického průběhu pneumonie
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

