-
Medical journals
- Career
Dobutamínová záťažová echokardiografia vs SPECT pri diagnostikovaní ischemickej choroby srdca
Authors: G. Valočik 1; I. Majerčák 1; P. Mitro 1; V. Tóthová 2; I. Marin 2
Authors‘ workplace: III. interná klinika Lekárskej fakulty UPJŠ a FN L. Pasteura, Košice, Slovenská republika, prednosta doc. MUDr. Peter Mitro, Ph. D. 1; Inštitút nukleárnej a molekulárnej medicíny Košice, Slovenská republika, riaditeľ MUDr. Igor Marin 2
Published in: Vnitř Lék 2007; 53(12): 1303-1309
Category: Original Contributions
Overview
Cieľom štúdie
bolo porovnanie dobutamínovej záťažovej echokardiografie oproti scintigrafii srdca metódou SPECT pri diagnostikovaní ischemickej choroby srdca.Metodika:
Jedná sa o retrospektívnu analýzu 119 pacientov (72 žien a 47 mužov, priemerný vek 56,9 ± 10,68 rokov), ktorým bola realizovaná dobutamínová záťažová echokardiografia a SPECT. Pre nejednoznačné nálezy (BĽTR, pokles kumulácie rádiofarmaka v závislosti od polohy tela) bolo vyradených 23 pacientov.Výsledky:
V celej skupine 96 pacientov bola diagnostická citlivosť dobutamínovej záťažovej echokardiografie v porovnaní so SPECT nasledovná: senzitivita 78 %, špecificita 93 %, pozitívna prediktívna hodnota 89 %, negatívna prediktívna hodnota 85 %, hodnota κ 0,71. U žien bola senzitivita 69 %, špecificita 93 %, pozitívna prediktívna hodnota 79 %, negatívna prediktívna hodnota 89 % a hodnota κ 0,64. U mužov bola diagnostická citlivosť nasledovná: senzitivita 83 %, špecificita 92 %, pozitívna prediktívna hodnota 95 %, negatívna prediktívna hodnota 73 %, hodnota κ 0,70.Záver:
Dobutamínová záťažová echokardiografia je vysoko senzitívna a špecifická metóda pri diagnostikovaní ischemickej choroby srdca, ktorá vykazuje dobrú zhodu so SPECT. Vzhľadom na väčšiu dostupnosť a nižšiu cenu vyšetrenia v porovnaní so SPECT je to optimálna metóda pri diagnóze a manažmente pacienta s ischemickou chorobou srdca v bežnej klinickej praxi.Kľúčové slová:
dobutamínová záťažová echokardiografia - SPECT - ischemická choroba srdcaÚvod
Záťažová echokardiografia bola zavedená v roku 1979 [1]. Z rôznych variant sa najviac v klinickej praxi uplatnila najmä farmakologická záťaž dobutamínom [2]. V súčasnosti je dobutamínová záťažová echokardiografia (DZE) už rutinná a bezpečná metóda, ktorá má popredné miesto v diagnóze a manažmente pacienta s ischemickou chorobou srdca [3-6]. Existuje veľa porovnávacích štúdií, ktoré hodnotili diagnostickú senzitivitu a špecificitu DZE. Tieto štúdie však porovnávali DZE vo väčšine prípadov s koronarografickým nálezom. Ako však bolo potvrdené viacerými štúdiami za posledné 3 desaťročia, fyziologický prístup k definícii závažnosti koronárnej choroby srdca stojí nad púhym anatomickým hodnotením koronárneho riečiska pomocou angiografie, inak povedané „luminografie“ [7-10].
V nami prezentovanej štúdii sme porovnali DZE oproti metodike, ktorá relatívne presne hodnotí konečný dopad koronárnej aterosklerózy na myokard, teda poruchy perfúzie myokardu hodnotené pomocou scintigrafie srdca metódou SPECT (Single Photon Emission Computed Tomography).
Pacienti a metodika
Súbor pacientov
Jedná sa o retrospektívnu analýzu 119 pacientov (72 žien a 47 mužov, priemerný vek 56,9 ± 10,68 rokov), u ktorých bola realizovaná DZE a zároveň aj SPECT vo vzájomnom odstupe oboch vyšetrení 1 ± 1,12 mesiacov. Medzi klinické indikácie na DZE a SPECT patrila diferenciálna diagnóza ischemickej choroby srdca (97 pacientov/81,51 %), resp. diferenciálna diagnóza ischemickej choroby srdca pri BĽTR (10 pacientov/8,4 %) a BPTR (3 pacienti/2,52 %), diagnóza restenózy po revaskularizácii (3 pacienti/2,52 %) a hodnotenie viability myokardu (10 pacientov/8,4 %).
Dobutamínová záťažová echokardiografia (DZE)
DZE bola realizovaná podľa štandardného protokolu na prístrojoch Vivid Five (GE Medical Systems) alebo Sequoia (Siemens Medical Solutions) transtorakálnou 2,25 - 3,75 MHz sondou harmonickým zobrazením: dávkovanie dobutamínu 5, 10, 20, 30 a 40 μg/kg/min intravenózne v 3-minútových intervaloch [11]. Ak to stav pacienta umožnil, liečba beta-blokátormi bola pri diferenciálnej diagnostike bolestí na hrudníku prerušená 48 hod pred vyšetrením. Záťažový test bol ukončený pri dosiahnutí cieľovej pulzovej frekvencie (85 % maximálnej frekvencie pulzu podľa veku [220 – vek] × 0,85). Ak požadovaná pulzová frekvencia nebola dosiahnutá a ak pacient nemal klinické, EKG alebo echokardiografické prejavy ischémie myokardu, bol aplikovaný intravenózne atropín (po 0,5 mg do maximálnej dávky 2 mg). Na začiatku testu a pri nízkom dávkovaní, resp. na vrchole zaťaženia bolo realizované EKG a meraný krvný tlak. Medzi kritéria ukončenia testu patrilo:
- dosiahnutie požadovanej pulzovej frekvencie,
- ťažká alebo rozsiahla novovzniknutá porucha kinetiky myokardu,
- horizontálna alebo descendentná depresia segmentu ST ≥ 0,2 mV,
- symptomatický pokles krvného tlaku > 40 mm Hg alebo systolický krvný tlak ≤ 90 mm Hg,
- hypertenzná reakcia (krvný tlak > 240/140 mm Hg),
- nové, pretrvávajúce poruchy rytmu,
- ťažká angina pectoris,
- netolerované vedľajšie účinky dobutamínu alebo atropínu.
Všetky nálezy boli nahrávané na videozáznamy, resp. digitálne uložené formou slučky a hodnotené off-line zobrazením štyroch obrazov vedľa seba. Bola sledovaná regionálna porucha kinetiky 16-segmentového modelu ľavej komory. Hodnotili sa 4 stupne porúch kinetiky: normokinéza, hypokinéza, akinéza a dyskinéza [12]. Pri posudzovaní odpovede myokardu sa hodnotili ako pozitívne nálezy 4 typy odpovede:
- trvalá úprava kinetiky, ktorá bola charakterizovaná postupnou úpravou pôvodne asynergického segmentu ľavej komory,
- bifázická odpoveď, pre ktorú bola typická úprava pôvodne asynergického segmentu pri nízkom dávkovaní a následné zhoršenie kinetiky daného segmentu pri vysokom dávkovaní,
- vznik novovzniknutej poruchy kinetiky,
- nefázická odpoveď v zmysle pretrvávania poruchy kinetiky počas celého záťažového testu.
SPECT
Pri diferenciálnej diagnóze ischemickej choroby srdca bol SPECT realizovaný formou jednodňového protokolu záťaž/kľud, keď prvá dávka rádiofarmaka 99mTc-Tetrofosmín (TEF) bola aplikovaná po dosiahnutí cieľovej frekvencie na pohyblivom páse. Vyšetrenie sa realizovalo pomocou jednohlavovej scintilačnej tomografickej kamery SOPHA DSX s paralelným kolimátorom typu LEAP, matrica 64 × 64, uhol rotácie 180°, 32 krokov po 20 s z pravej prednej šikmej projekcie 45° do ľavej zadnej šikmej projekcie 45°. Dávka aplikovaného rádiofarmaka 99mTc-MYOVIEW bola spolu 600 - 1 000 MBq pri záťaži a v kľude podľa hmotnosti pacienta. Poruchy perfúzie sa hodnotili na rezoch 3D obrazom myokardiálnej perfúzie po záťaži a v pokojovej fáze 4 hod po záťaži. Zároveň sa hodnotil priebeh distribučných kriviek kumulácie rádiofarmaka v jednotlivých segmentoch myokardu ľavej komory. Pri detekcii viability myokardu bol použitý dvojdňový protokol: pokojová štúdia/záťažová štúdia. Prvá dávka rádiofarmaka (201Tl-chlorid v dávke 90 - 110 MBq podľa hmotnosti pacienta) bola aplikovaná v kľude večer, deň pred vyšetrením. Na 2. deň ráno bola vykonaná scintigrafická nahrávka perfúzie myokardu za účelom detekcie viability myokardu. Následne bol vykonaný záťažový test a pri dosiahnutí požadovanej pulzovej frekvencie na bežiacom páse bola aplikovaná druhá dávka TEF (99mTc-MYOVIEW v dávke 200 - 350 MBq podľa hmotnosti pacienta) s následnou scintigrafickou nahrávkou záťažovej perfúzie myokardu. Pri BĽTR sa použila farmakologická záťaž s adenozínom. Prvá dávka TEF bola aplikovaná v tretej minúte farmakologickej záťaže a následne bola vykonaná scintigrafická nahrávka pozáťažovej perfúzie myokardu. V kľude o 4 hod bola aplikovaná druhá dávka rádiofarmaka s následnou scintigrafickou nahrávkou kľudovej perfúzie myokardu [13-17].
Štatistická analýza
Jednotlivé údaje sú vyjadrené ako priemer ± smerodajná odchýlka (SD). Citlivosť DZE v porovnaní so SPECT bola hodnotená pomocou kontingenčnej tab. 2 × 2. Bola určená senzitivita, špecificita, pozitívna a negatívna prediktívna hodnota na základe zhody medzi týmito 2 vyšetrovacími metodikami. Pričom zhoda, resp. nezhoda sa hodnotila nielen v súvislosti s ischémiou myokardu, ale aj v súvislosti s prítomnosťou jazvy po infarkte myokardu, teda trvalej poruchy perfúzie pri SPECT a nefázickej odpovede pri DZE. Zhoda medzi dvoma vyšetrovacími metódami bola hodnotená stanovením hodnoty κ (κ). Hodnota κ < 0,2 znamenala slabú zhodu, hodnoty κ 0,2 - 0,4 znamenali uspokojivú zhodu, hodnoty κ 0,4 - 0,6 stredne silnú zhodu, hodnoty κ 0,6 - 0,8 dobrú zhodu a hodnoty κ > 0,8 veľmi dobrú zhodu medzi vyšetrovacími metódami.
Výsledky
Celkovo bolo analyzovaných 119 nálezov DZE a SPECT. Z toho 23 pacientov (19,32 %) malo nejednoznačné nálezy:
- a) u 4 pacientov s BĽTR bola pri scintigrafii myokardu zistená fixovaná porucha perfúzie (v 3 prípadoch v oblasti septa a v 1 prípade v oblasti hrotu ľavej komory). Nedalo sa jednoznačne vylúčiť, že sa jedná o falošne pozitívny nález pri BĽTR.
- b) u 11 pacientov bol po záťaži zistený pokles kumulácie rádiofarmaka, hlavne v oblasti spodnej steny ľavej komory. Pre možný arteficiálny pôvod nálezu bolo snímanie opakované na bruchu, pri ktorom sa však kumulácia rádiofarmaka upravila.
- c) u 7 pacientov (všetky ženy) bol nejednoznačný nález poruchy perfúzie myokardu v oblasti prednej steny ľavej komory. Stav sa hodnotil ako možný artefakt pri ženskom habite. Podľa priebehu distribučných kriviek kumulácia rádiofarmaka v žiadnej z oboch fáz neklesala signifikantne do oblasti patologických hodnôt.
- d) u jedného pacienta počas DZE bola zaznamenaná atypia pohybu bazálneho segmentu inferolaterálnej steny ľavej komory v zmysle tardokinézy. Na konci záťaže pretrvávala táto asynergia, ale bez pridružených porúch kinetiky ostatných segmentov.
Vzhľadom na vyššie uvedené nejednoznačné nálezy bola diagnostická citlivosť hodnotená u zvyšných 96 pacientov s jasne pozitívnym alebo negatívnym nálezom. Ich klinické charakteristiky sú uvedené v tab. 1. Z toho 31 pacientov malo pozitívnu DZE a SPECT, 52 pacientov negatívnu DZE a SPECT, 4 pacienti mali pozitívnu DZE a negatívny SPECT a 9 pacientov malo negatívnu DZE a pozitívny SPECT. Diagnostická citlivosť DZE v porovnaní so SPECT bola: senzitivita 78 %, špecificita 93 %, pozitívna prediktívna hodnota 89 %, negatívna prediktívna hodnota 85 %, hodnota κ 0,71. Podľa pohlavia boli výsledky nasledovné:
Table 1. Klinické charakteristiky študovanej skupiny pacientov (n = 96). 
- u žien malo 11 pacientov zhodne pozitívnu DZE a aj SPECT, 42 pacientov negatívnu DZE a aj SPECT, 3 pacientky mali pozitívnu DZE a negatívny SPECT a 5 pacientov malo negatívnu DZE a pozitívny SPECT. Diagnostická citlivosť bola: senzitivita 69 %, špecificita 93 %, pozitívna prediktívna hodnota 79 %, negatívna prediktívna hodnota 89 %, hodnota κ 0,64.
- u mužov malo 19 pacientov zhodne pozitívnu DZE a SPECT, 11 pacientov negatívnu DZE a SPECT, 1 pacient pozitívnu DZE a negatívny SPECT a 4 pacienti mali negatívnu DZE a pozitívny SPECT. Diagnostická citlivosť bola nasledovná: senzitivita 83 %, špecificita 92 %, pozitívna prediktívna hodnota 95 %, negatívna prediktívna hodnota 73 %, hodnota κ 0,70.
Hodnoty sú prehľadne uvedené v tab. 2.
Table 2. Diagnostická citlivosť dobutamínovej záťažovej echokardiografie (DZE) v porovnaní so SPECT. 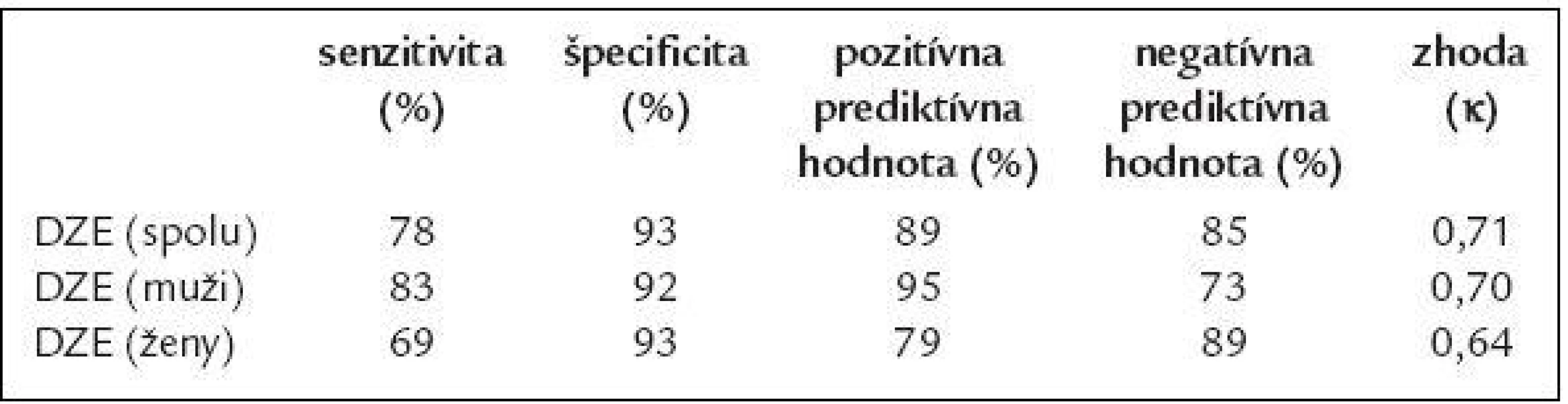
V celkovej skupine pacientov bolo 9,3 % falošne negatívnych nálezov a 4 % falošne pozitívnych nálezov. U žien bolo 5 % falošne negatívnych nálezov a 4 % falošne pozitívnych nálezov. U mužov bolo 12 % falošne negatívnych nálezov a 3 % falošne pozitívnych nálezov. V skupine 9 pacientov s falošne negatívnym nálezom (negatívna DZE a pozitívny SPECT) mal každý pacient dosiahnutých aspoň 85 % maximálnej pulzovej frekvencie podľa veku. U 4 pacientov bol v liečbe betablokátor, ale ten bol vysadený 2 - 3 dni pred vyšetrením. U jedného pacienta bol v liečbe ponechaný kalciový blokátor. Iba jeden z uvedených pacientov mal typickú anginu pectoris. Na EKG neboli zaznamenané signifikantné zmeny úseku ST-T počas DZE. Počas DZE sme nezaznamenali významnejšie komplikácie, ktoré by viedli k predčasnému ukončeniu testu. U 5 pacientov (6,6 %) bola horšia echogenita, ale ešte dovoľovala pri harmonickom zobrazení hodnotenie kinetiky.
Diskusia
V nami prezentovanej štúdii sme porovnali DZE so SPECT. V tab. 3 sú uvedené výsledky porovnávacích štúdií, ktoré hodnotili citlivosť rôznych foriem záťažovej echokardiografie a scintigrafie srdca v porovnaní s koronarografiou, pričom za signifikantnú sa považovala stenóza > 50 % [18-23]. Hodnoty senzitivity záťažovej echokardiografie sa v týchto štúdiach pohybujú od 60 do 85 %, špecificity od 83 do 95 % a v dvoch prípadoch je uvedená aj hodnota κ (0,75 a 0,51). Nami zistené výsledky diagnostickej citlivosti (senzitivita 78 %, špecificita 93 %, κ 0,71), hoci neboli korelované s koronarografickými nálezmi, sú v zhode s vyššie uvedenými štúdiami a naďalej potvrdzujú vysokú citlivosť DZE, resp. dobrú zhodu so SPECT. Vzhľadom na vysokú citlivosť DZE a na skutočnosť, že DZE je cenovo výhodnejšia ako scintigrafia srdca, je to optimálna metóda na diagnózu ischemickej choroby srdca hlavne na pracoviskách, kde nie je dostupné vyšetrenie metódou SPECT. V tejto súvislosti sa vynára otázka kombinácie oboch vyšetrovacích metód alebo využitia len niektorej z nich pri diagnóze koronárnej choroby srdca v rutinnej klinickej praxi. Marwick et al vo svojej prospektívnej štúdii, ktorá zahrňovala 217 pacientov, sa snažili odpovedať na túto otázku [24]. U pacientov so signifikantnou koronárnou chorobou srdca bola senzitivita DZE a SPECT rovnaká (72 % vs 76 %). V podskupine pacientov s negatívnou koronarografiou bola však špecificita DZE signifikantne vyššia ako špecificita SPECT (83 % vs 67 %), ale u pacientov s nedosiahnutou požadovanou pulzovou frekvenciou pri DZE (na úrovni submaxima) a negatívnym DZE nálezom bola senzitivita SPECT významne vyššia ako senzitivita DZE (59 % vs 77 %). U pacientov s hypertrofiou ľavej komory bola špecificita DZE vyššia ako špecificita SPECT (94 % vs 59 %). Autori teda konštatujú, že DZE pri hypertrofii ľavej komory je metódou voľby pri diagnostikovaní koronárnej choroby srdca. U pacientov s negatívnym submaximálnym DZE nálezom je vhodné doplniť scintigrafiu srdca, pretože sa tým zvyšuje diagnostická citlivosť. V prípade diagnózy viability myokardu je však potrebná kombinácia oboch vyšetrovacích metód [25]. Baumgarther et al zistili, že pri histopatologickom vyšetrení myokardu bolo percentuálne zastúpenie viabilných myocytov najvyššie v prípade, ak sa viabilita potvrdila pomocou DZE, SPECT a PET [26]. Najnižšie percentuálne zastúpenie viabilných myocytov bolo v prípade negatívneho nálezu pri všetkých troch vyšetreniach a intermediálne v prípade negatívneho nálezu pri DZE a pozitívnej scintigrafii. Preto na zvýšenie validity pri diagnóze viabilného myokardu je optimálna kombinácia DZE a scintigrafie srdca.
Table 3. Diagnostická citlivosť záťažovej echokardiografie a SPECT v porovnaní s koronarografiou. 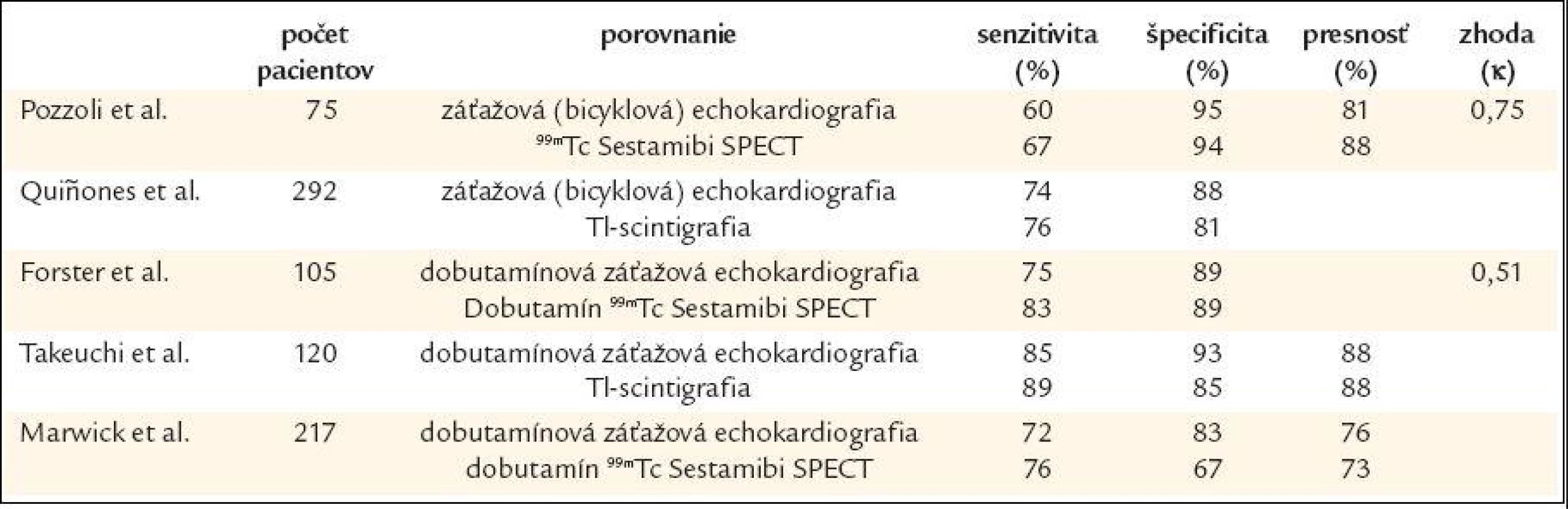
Ročne sa na celom svete vykoná niekoľko miliónov zobrazovacích vyšetrení. Z toho asi 1/3 tvoria kardiovaskulárne zobrazovacie metodiky [27]. Vzhľadom na ich vysokú ekonomickú záťaž pre spoločnosť nie je zanedbateľné ich správne využitie v klinickej praxi. K tomu je však potrebná znalosť týkajúca sa diagnostickej citlivosti danej vyšetrovacej metodiky, lebo preferovaním síce lacnejších metodík, ale s nízkou diagnostickou validitou, môže byť poškodený pacient. Pri porovnávaní nákladov, ak sa záťažovej ergometrii prisúdi hodnota 1, DZE predstavuje 2,1-krát vyššie finančné zaťaženie. V prípade SPECT je finančné zaťaženie až 5,7-krát vyššie, naviac pri DZE pacient a vyšetrujúci nie je vystavený radiačnému zaťaženiu [28].
Pre porovnávacie štúdie je charakteristická vysoká variabilita senzitivity a špecificity. Vyplýva to z viacerých metodologických problémov, ktoré sa týkajú hlavne definície pozitivity testu, druhu sledovanej populácie pacientov a manipulácie s nejednoznačnými nálezmi [29,30]. Z uvedených dôvodov sme sa snažili vylúčiť z analýzy nejednoznačné nálezy, ktoré je problematické interpretovať ako pozitívny alebo negatívny nález. Týkalo sa to hlavne pacientov s poklesom kumulácie rádiofarmaka v závislosti od zmeny polohy tela a pacientov s pozitívnym SPECT a BĽTR. Hirzel et al v skupine 19 symptomatických pacientov s BĽTR a poruchou perfúzie v anteroseptálnej oblasti potvrdili koronárnu chorobu srdca len v 4 prípadoch [31]. Pri experimente na psoch zistili, že pri elektricky indukovanom BĽTR došlo k poruche vychytávania rádiofarmaka a k zníženej perfúzii myokardu hodnotenej meraním perfúzie rádioaktívnymi mikročiasticami hlavne v oblasti septa. Autori uzatvárajú, že pri BĽTR môže dôjsť k funkčnej ischémii myokardu pri asynchrónnej kontrakcii interventrikulárneho septa aj bez signifikantnej stenózy koronárnych tepien. V celej skupine pacientov, ale aj v závislosti od pohlavia bolo 2 - 3-krát vyššie percento pacientov s falošne negatívnym DZE nálezom ako falošne pozitívnym. V skupine chorých s falošne negatívnym DZE nálezom sme nezistili, že by príčinou falošnej negativity mohla byť ponechaná liečba betablokátorom alebo nedosiahnutie požadovanej pulzovej frekvencie.
Za nedostatok nami prezentovanej štúdie by sme mohli považovať skutočnosť, že nálezy DZE a SPECT neboli porovnané s koronarografiou. Hoci koronarografia sa považuje za zlatý štandard pri hodnotení ischemickej choroby srdca, nehodnotí však perfúziu myokardu, ktorá je práve vizualizovaná pri scintigrafii srdca [32-34]. Už v minulosti bolo potvrdené, že koronarografia podhodnocuje koronárnu chorobu srdca [35]. Za posledné roky sme svedkami zavádzania nových zobrazovacích metodík, vrátane CT koronaroangiografie a intravaskulárneho ultrazvuku, pri hodnotení známej alebo podozrivej koronárnej choroby srdca [36]. Tieto nové vyšetrovacie metódy postupne menia náhľad na hodnotenie ischemickej choroby srdca pomocou angiografie. Často sa potvrdzuje diskrepancia medzi koronarografickými nálezmi a metodikami, ktoré hodnotia perfúziu myokardu. Napríklad Rodés-Cabau et al porovnali poruchy perfúzie v myokarde hodnotené pomocou SPECT s údajmi získanými pri intravaskulárnom ultrazvuku a stupňom stenózy koronárnych tepien určených kvantitatívnou angiografiou [37]. Až v 50 % prípadov stenózy hodnotené angiografiou ako nesignifikantné (< 50 % zúženie lúmenu tepny) boli spojené s ischémiou myokardu a teda by boli indikované na revaskularizáciu podľa intravaskulárneho ultrazvuku. Stupeň stenózy koronárnych tepien nie je schopný predpovedať hemodynamickú závažnosť aterosklerotického plátu, pretože poruchy perfúzie sú závislé nielen od zúženia epikardiálnych tepien, ale aj od takých faktorov, ako je mikrovaskulárna rezistencia, endoteliálna dysfunkcia a negatívna koronárna remodelácia [38-40]. Preto si myslíme, že nie je chybou, ak sa DZE porovnala so scintigrafiou srdca, pretože SPECT citlivejšie vystihuje dôsledky koronárnej choroby srdca ako koronarografia.
Hodnotenie porúch kinetiky pri DZE je limitované skúsenosťami vyšetrujúceho, zlou echogenitou pacienta a často nie optimálnou reznou rovinou dutinou ľavej komory. Tieto limitácie sa v súčasnosti postupne prekonávajú zavádzaním nových metodík. Kontrastná echokardiografia umožňuje lepšie hodnotiť kinetiku opacifikáciou dutiny ľavej komory aj u zle echogénnych pacientov. Sľubné sú výsledky aj pri hodnotení perfúzie myokardu i.v. kontrastnými látkami vyššej generácie. Trojrozmerná echokardiografia sa ukázala byť optimálnou aj pri DZE, pretože prekonáva dvojrozmernú echokardiografiu pri lokalizácii ischémie myokardu, hlavne v kombinácii s kontrastnou echokardiografiou [41].
Záver
DZE je vysoko senzitívna a špecifická metóda pri diagnostikovaní ischemickej choroby srdca, ktorá vykazuje podľa našich výsledkov dobrú zhodu so SPECT. Vzhľadom na väčšiu dostupnosť a nižšiu cenu vyšetrenia v porovnaní so SPECT je optimálnou metódou pri diagnóze a manažmente pacienta s ischemickou chorobou srdca v bežnej klinickej praxi.
Poďakovanie
Táto práca vznikla na základe vedeckého a edukačného grantu spoločnosti Siemens Medical Solutions USA, Inc. Ultrasound Division, Mountain View, CA.
doc. MUDr. Gabriel Valočik, Ph.D.
www.upjs.sk
e-mail: valocik@central.medic.upjs.sk
Doručeno do redakce: 9. 3. 2007
Přijato po recenzi: 14. 9. 2007
Sources
1. Picano E. Stress Echocardiography: A historical perspective. Am J Medicine 2003; 114 : 126-130.
2. Martin TW, Seaworth JF, Johns JP et al. Comparison of adenosine, dipyridamole, and dobutamine stress echocardiography. Ann Intern Med 1992; 116 : 190-196.
3. Biagini E, Elhendy A, Bax JJ et al. Seven-year follow-up after dobutamine stress echocardiography: impact of gender on prognosis. J Am Coll Cardiol 2005; 45 : 93-97.
4. Cheitlin MD, Armstrong WF, Aurigemma GP et al. ACC/AHA/ASE 2003 guideline update for the clinical application of echocardiography: summary article. A report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/ASE committee to update the 1997 guidelines for the clinical application of echocardiography). J Am Soc Echocardiogr 2003; 16 : 1091-1110.
5. Krivokapich J, Child JS, Walter DO et al. Prognostic value of dobutamine stress echocardiography in predicting cardiac events in patients with known or suspected coronary artery disease. J Am Coll Cardiol 1999; 33 : 708-716.
6. Marcovitz PA Prognostic issues in stress echocardiography. Prog Cardiovasc Dis 1997; 39 : 533-542.
7. Klocke FJ, Baird MG, Lorell BH et al. ACC/AHA/ASNC guidelines for the clinical use of cardiac radionuclide imaging - executive summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/ ASNC Committee to Revise the 1995 Guidelines for the Clinical Use of Cardiac Radionuclide Imaging). Circulation 2003; 108 : 1404-1418.
8. Hachamovitch R, Hayes SW, Friedman JD et al. Comparison of the short-term survival benefit associated with revascularization compared with medical therapy in patients with no prior coronary artery disease undergoing stress myocardial perfusion single photon emission computed tomography. Circulation 2003; 107 : 2900-2907.
9. Shaw LJ, Hachamovitch R, Berman DS et al. for the Economics of Noninvasive Diagnosis (END) Multicenter Study Group. The economic consequences of available diagnostic and prognostic strategies for the evaluation of stable angina patients: an observational assessment of the value of precatheterization ischemia. J Am Coll Cardiol 1999; 33 : 661-669.
10. Weiner DA, Ryan TJ, McCabe CH et al. The role of exercise testing in identifying patients with improved survival after coronary artery bypass surgery. J Am Coll Cardiol 1986; 8 : 741-748.
11. Geleijnse ML, Fioretti PM, Roelandt JR et al. Methodology, feasibility, safety and diagnostic accuracy of dobutamine stress echocardiography. J Am Coll Cardiol 1997; 30 : 595-606.
12. Armstrong WF, Pellikka PA, Ryan T et al. Stress echocardiography: recommendations for performance and interpretation of stress echocardiography. Stress Echocardiography Task Force of the Nomenclature and Standards Committee of the American Society of Echocardiography. J Am Soc Echocardiogr 1998; 11 : 97-104.
13. Farský Š, Lepej J, Bakos K. Nukleárna kardiológia. Martin: Osveta 1989 : 269.
14. Lepej J, Farský Š. Táliová scintigrafia myokardu I. Princíp a metodika. Čs Radiol 1990; 44 : 171-178.
15. Lepej J, Farský Š. Táliová scintigrafia myokardu II. Hodnotenie výsledkov. Čs Radiol 1990; 44 : 179-192.
16. Kamínek M, Mysliveček M, Škvařilová M et al. Correlation of SPECT myocardial stress scintigraphy with coronary angiography. Vnitř Lék 1998; 44 : 187-191.
17. Kamínek M, Mysliveček M, Škvařilová M et al. Myocardial perfusion tomography imaging in patients without prior myocardial infarction-comparison between 201Tl, 99mTc-tetrofosmin and dual-isotope protocol (rest 201Tl/stress 99mTc-tetrofosmin). Vnitř Lék 1999; 45 : 81-84.
18. Forster T, McNeill AJ, Salustrin A et al. Simultaneous dobutamine stress echocardiography and technetium-99m isonitrile single-photon emission computed tomography in patients with suspected coronary artery disease. J Am Coll Cardiol 1993; 21 : 1591-1596.
19. Huang PJ, Ho YL, Wu CC et al. Simultaneous dobutamine stress echocardiography and thallium-201 perfusion imaging for the detection of coronary artery disease. Cardiology 1997; 88 : 556-562.
20. Chae SC, Heo J, Iskandrian AS et al. Identification of extensive coronary artery disease in women by exercise single-photon emission computed tomographic (SPECT) thallium imaging. J Am Coll Cardiol 1993; 21 : 1305-1311.
21. Pozzoli MMA, Fioretti PM, Salustri A et al. Exercise echocardiography and technetium-99m MIBI single photon emission computed tomography in the detection of coronary artery disease. Am J Cardiol 1991; 67 : 350-355.
22. Quiñones MA, Verani MS, Haichin RM et al. Exercise echocardiography versus 201Tl single-photon emission computed tomography in evaluation of coronary artery disease. Analysis of 292 patients. Circulation 1992; 85 : 1026-1031.
23. Takeuchi M, Araki M, Nakashima Z et al. Comparison of dobutamine stress echocardiography and stress thalium-201 single-photon emission computed tomography for detecting coronary artery disease. J Am Soc Echocardiogr 1993; 6 : 593-602.
24. Marwick T, D´Hondt AM, Baudhuin T et al. Optimal use of dobutamine stress for the detection and evaluation of coronary artery disease: combination with echocardiography or scintigraphy, or both? J Am Coll Cardiol 1993; 22 : 159-167.
25. Salazar HP, Talano J Viable myocardium: How much is enough? A comparison of viability by comparative imaging techniques to assess the quantity and functionality of ischemic myocardium. Echocardiography 2005; 22 : 59-70.
26. Baumgarther H, Porenta G, Lau YK et al. Assessment of myocardial viability by dobutamine echocardiography, positron emission tomography and thallium-201 SPECT: Correlation with histopathology in explanted hearts. J Am Coll Cardiol 1998; 32 : 1701-1708.
27. Atlantic Information services: Controlling the soaring costs of medical imaging. 15 June 2004.
28. Picano E. Economic and biological costs of cardiac imaging. Cardiovasc Ultrasound 2005; 25 : 13.
29. Krenning BJ, Geleijnse ML, Poldermans D et al. Methodological analysis of diagnostic dobutamine stress echocardiography studies. Echocardiography 2004; 21 : 725-735.
30. Kaminek M, Indrakova J Quantitative gated SPECT of myocardium in detection of ischemic heart disease: validation of finding by means of coronarography. Biomed. Papers 2003; 147 : 243-244.
31. Hirzel HO, Senn M, Nuesch K et al. Thallium-201 scintigraphy in complete left bundle branch block. Am J Cardiol 1984; 53 : 764-769.
32. Lepej J, Spišiaková D, Hrnčiar J et al. Táliová SPECT scintigrafia myokardu v hodnotení pacientov so syndrómom inzulínovej rezistencie a mikrovaskulárnou anginou pectoris. Vnitř Lék 2000; 46 : 205-212.
33. Kamínek M, Mysliveček M, Škvařilová M et al. Prognostic significance of stress tomographic scintigraphy of myocardial perfusion in diabetic patients. Vnitř Lék 2001;47 : 739-743.
34. Kamínek M, Mysliveček M et al. Prognostic value of myocardial perfusion tomographic imaging in patients after percutaneous transluminal coronary angioplasty. Clin Nucl Med 2000; 25 : 775-778.
35. Arnett EN, Isner JM, Redwood DR et al. Coronary artery narrowing in coronary artery disease: comparison of cineangiographic and necropsy findings. Ann Intern Med 1979; 91 : 350-356.
36. Leber AW, Knez A, von Ziegler F et al. Quantification of obstructive and nonobstructive coronary lesions by 64-slice computed tomography: a comparative study with quantitative coronary angiography and intravascular ultrasound. J Am Coll Cardiol 2005; 46 : 147-154.
37. Rodés-Cabau J, Candell-Riera J, Angel J et al. Relation of myocardial perfusion defects and nonsignificant coronary lesions by angiography with insights from intravascular ultrasound and coronary pressure measurements. Am J Cardiol 2005; 96 : 1621-1626.
38. Meuwissen M, Chamuleau SAJ, Siebes M et al. Role of variability in microvascular resistance on fractional flow reserve and coronary blood flow velocity reserve in intermediate coronary lesions. Circulation 2001; 103 : 184-187.
39. Zeiher AM, Drexler H, Wollschlager H et al. Modulation of coronary vasomotor tone in humans: progressive endothelial dysfunction with different early stages of coronary atherosclerosis. Circulation 1991; 83 : 391-401.
40. McLeod AL, Newby DE, Northridge DB et al. Influence of differential vascular remodeling on the coronary vasomotor response. Cardiovasc Res 2003; 59 : 520-526.
41. Pulerwitz T, Hirata K, Abe Y et al. Feasibility of using a real-time 3-dimensional technique for contrast dobutamine stress echocardiography. J Am Soc Echocardiogr 2006; 19 : 540-545.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2007 Issue 12-
All articles in this issue
- Recidivující arytmie po katetrové ablaci původně paroxyzmální fibrilace síní a výsledky opakované ablace
- Bakteriální infekce ve vztahu ke vzniku a průběhu varikózního krvácení
- Stresová odezva prolaktinu u nemocných se systémovým lupus erythematodes (SLE), revmatoidní artritidou (RA) a u zdravých kontrol
- Léčba hyperglykemie u kriticky nemocných pacientů: srovnání standardního protokolu a počítačového algoritmu
- Příčiny akutního krvácení do horního trávicího traktu u pacientů s jaterní cirhózou
- Vliv etiologie syndromu diabetické nohy na lokalizaci defektů
- Sledování funkčních poruch mikrocirkulace laser dopplerem u pacientů s chronickou žilní nedostatečností třídy 2 dle CEAP klasifikace před a po operaci varixů
- Celiakia - častá príčina „idiopatickej osteoporózy“ premenopauzálnych a včasne postmenopauzálnych žien
- Dobutamínová záťažová echokardiografia vs SPECT pri diagnostikovaní ischemickej choroby srdca
- Diabetes mellitus a mikroalbuminurie
- Dnešný pohľad na riziká umelej pľúcnej ventilácie
- Waldenströmova makroglobulinemie - klinické projevy a diferenciální diagnostika a prognóza nemoci
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Dnešný pohľad na riziká umelej pľúcnej ventilácie
- Recidivující arytmie po katetrové ablaci původně paroxyzmální fibrilace síní a výsledky opakované ablace
- Waldenströmova makroglobulinemie - klinické projevy a diferenciální diagnostika a prognóza nemoci
- Diabetes mellitus a mikroalbuminurie
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

