-
Medical journals
- Career
Kongenitální adrenální hyperplazie, defekt 17α−hydroxylázy jako vzácná příčina hypertenze a hypokalemie
: V. Olšovská 1; J. Šulcová 2; A. Hondlová 1; H. Šiprová 1
: II. interní klinika Lékařské fakulty MU a FN u sv. Anny, Brno, přednosta doc. MUDr. Miroslav Souček, CSc. 1; Oddělení steroidních hormonů Endokrinologického ústavu, Praha, ředitel doc. MUDr. Vojtěch Hainer, CSc. 2
: Vnitř Lék 2005; 51(2): 226-230
: Case Reports
Autoři popisují řídce se vyskytující případ kongenitální adrenální hyperplazie, parciálního defektu 17α-hydroxylázy u pacientky s hypertenzí, hypokalemií, poruchami menstruačního cyklu a sterilitou. Diagnóza byla stanovena na základě vyšetření steroidního spektra nativně a při stimulačních a supresních testech a CT-vyšetření. Po zavedené terapii dexametazonem došlo k úpravě krevního tlaku i iontogramu. Sdělení dokládá význam vyšetření celého steroidního spektra u nemocných s touto symptomatologií k vyloučení vzácnějších příčin endokrinní hypertenze.
Klíčová slova:
kongenitální adrenální hyperplazie – endokrinní hypertenze – hypokalemie – defekt 17α-hydroxylázyÚvod
Na steroidogenezi v kůře nadledvin se podílí velké množství enzymů kódovaných příslušnými geny. Mezi nejdůležitější patří 21-hydroxyláza (P450c21, CYP 21), 11β-hydroxyláza (P450c11, CYP11B2, CYP11B1), 3β-dehydrogenáza (HSD3B2, HSD3B1), 17α-hydroxyláza (P450c17, CYP 17), desmoláza (P450scc). Při genových poruchách dochází k poškození tvorby steroidních enzymů a k rozvoji nadledvinové insuficience s deficitem cílových steroidů, především kortizolu. Tento deficit vede zpětnou vazbou ke stimulaci hypotalamu a hypofýzy s nadprodukcí ACTH. Nadbytek ACTH stimuluje sekreci steroidů kůry nadledvin před enzymovým blokem (schéma 1). Vzniká tzv. Kongenitální adrenální hyperplazie (CAH, dříve označovaná jako adrenogenitální syndrom), autozomálně recesivně dědičné onemocnění s pestrou klinickou symtomatologií, která závisí na typu a stupni (kompletní a parciální formy) enzymatického defektu. Většina steroidních prekurzorů má virilizující účinky, proto se v závislosti na míře bloku projevuje kombinace příznaků nadledvinové insuficience a virilizace (nejčastěji u deficitu 21-hydroxylázy, dále vzácněji u 3β-hydroxysteroidní dehydrogenázy). Pokud se hromadí steroidní prekurzory s mineralokortikoidními účinky, mohou navíc způsobit hypertenzi a hypokalemii (deficit 11β-hydroxylázy). V případě vzácného defektu 17α-hydroxylázy se kromě snížené tvorby kortizolu, androgenů a estradiolu uplatňuje v klinickém obraze zvýšená tvorba steroidních prekurzorů s mineralokortikoidním účinkem, zejména 11-deoxykortikosteronu, která vede k hypertenzi a hypokalemii.
Schéma 1. Schéma steroidogeneze. 
Popis případu
Dnes 42letá nemocná je sledována od 28 let pro obtížně korigovatelnou hypertenzi. Menarche byla ve 14 letech, v dospělosti byla sledována a gynekologicky léčena pro nepravidelné cykly, ovariální cysty, sterilitu, opakovaně provedena abraze pro metroragie. Dvakrát neúspěšně absolvovala pokus o graviditu v IVF programu. Vzhledem k hypertenzi a hypokalemii byla pacientka v roce 1999 odeslána na endokrinologii k vyloučení primárního hyperaldosteronizmu. Hormonální vyšetření tehdy vykazovalo suprimovanou hladinu PRA nativně i po stimulaci, aldosteron nativně i po stimulaci byl mírně snížený. Snížené byly i hladiny testosteronu a DHEAS, ostatní hormonální vyšetření bylo v normě včetně estradiolu, FSH, LH a PRL. Kortizol v séru v diurnálním profilu byl v normě, vyšetření volného kortizolu v moči lehce nad horní hranicí normy, supresibilní ve 2 mg dexametazonovém testu, ACTH v normě, odpady 17-ketosteroidů v moči za 24 hodin také v normě. Kompletní vyšetření steroidů tehdy provedeno nebylo. Vyšetření katecholaminů v moči za 24 hodin vykazovalo normální hodnoty. Vzhledem k výraznému zvětšení pravé nadledviny na CT, která byla popisována velikosti 55 × 30 × 30 mm, denzitně nehomogenní, byla doporučena adrenalektomie. Levá nadledvina byla velikosti 25 × 15 × 15 mm. Pravostranná adrenalektomie byla provedena v říjnu roku 1999, bez komplikací, histologicky byl nález popsán jako enkapsulovaný adenom s ostrůvky oxyfilních buněk. Po operaci pacientka užívala přechodně hydrokortizon, který byl v lednu roku 2001 zcela vysazen. Byla sledována v endokrinologické ambulanci v místě bydliště. Podle dokumentace byly hodnoty TK uspokojivé při terapii amlodipinem v dávce 10 mg denně. Hypokalemie byla korigována tabletami kalium chloratum. Subjektivně se cítila dobře, udávala jen sklon k mírným perimaleolárním otokům.
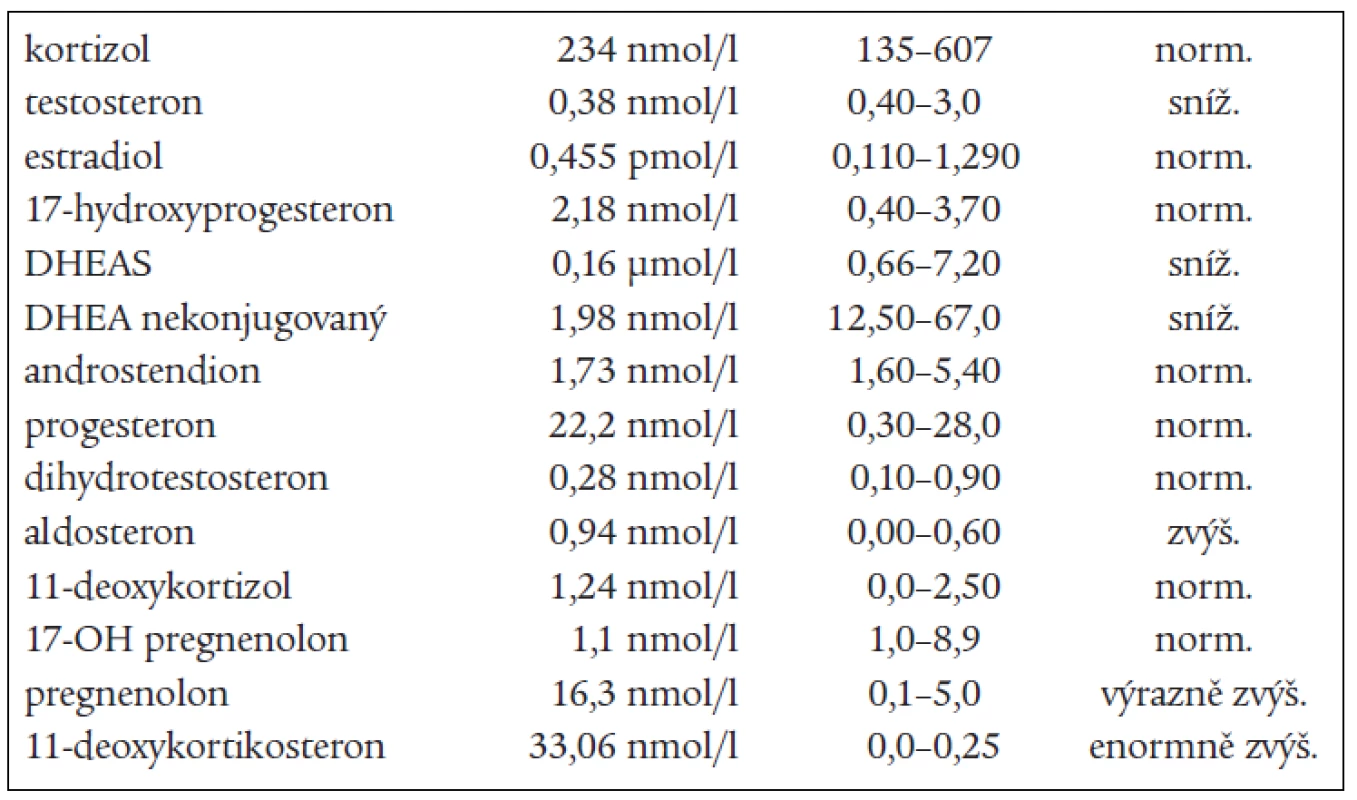
V roce 2003 byla pacientka odeslána k přešetření za hospitalizace pro trvající sklon k hypokalemii a progresi nálezu při kontrolním CT-vyšetření. Došlo ke zbytnění zbylé levé nadledviny, která byla defigurovaná s vícečetnými hypodenzními uzly o průměru 2 cm, které měly nativně lehce záporné hodnoty a po aplikaci kontrastní látky se vysycovaly asi o 20 HU. Celkový tvar byl laločnatý, rozměry 45 × 35 × 55 mm. Subjektivně byla pacientka bez výraznějších potíží, klinicky eufunkční, TK korigován monoterapií, menstruační cyklus jen lehce nepravidelný. Kalium v séru při přijetí bylo 2,9 mmol/l, ostatní základní biochemické vyšetření bylo v normě, včetně odpadů iontů v moči za 24hodin. Při hormonálním vyšetření včetně vyšetření celého steroidního spektra byly zachyceny enormně vysoké hladiny 11-deoxy-kortikosteronu a pregnenolonu, na horní hranici normy byly hodnoty aldosteronu a progesteronu, jedenkrát zachycen aldosteron mírně zvýšený. Snížené byly hladiny testosteronu,
DHEAS, DHEA, androstendionu (tab. 1 a 3). Snížená byla i hladina plazmatické reninové aktivity. Ostatní steroidy v séru i v moči byly v normě, normální byly i hladiny hypofyzárních hormonů včetně ACTH. FSH a LH byly na jaře roku 2003 hraničně zvýšené. Všechny hladiny steroidů byly supresibilní v dexametazonovém testu (tab. 2). Tyto výsledky svědčily proti diagnóze tumoru a vedly k podezření na diagnózu kongenitální adrenální hyperplazie při parciálním bloku 17α-hydroxylázy, příčinou hypertenze byly vysoké hladiny 11-deoxykortikosteronu. Na genetické vyšetření byla pacientka odeslána, ale nebylo možné provést cílené vyšetření na gen pro 17α - ydroxylázu, které se v současnosti v České republice neprovádí. Proto byla diagnóza stanovena na základě biochemického vyšetření a klinického obrazu. Byla zavedena supresní terapie dexametazonem, zpočátku v dávce 0,5 mg denně. Při této dávce došlo k úpravě TK a iontogramu, bylo možno vysadit antihypertenzní medikaci i kalium, hladina 11-DOC byla jen mírně zvýšená, pregnenolon v normě, aldosteron snížený (tab. 4). Klinicky byl při této dávce v dalším průběhu sklon k hypotenzi a hyperkalemii, proto byla dávka dexametazonu snížena na 0,25 mg a přechodně byl přidán hydrokortizon 10 mg ráno, který byl později vysazen. Pacientka je subjektivně bez potíží, normotenzní, iontogram je v normě. Vyvinula se však postupně amenorea se zvýšením hladin FSH a LH a byla za kontrol gynekologa zavedena substituční terapie. Vyšetření steroidů, kromě mírně zvýšené hladiny 11-DOC, je v normě. Při kontrolním CT vyšetření nadledvin po půl roce zůstává nález stejný, bez progrese v oblasti levé nadledviny. Pacientka zůstává v dalším sledování endokrinologické ambulance.
2. Dexametazonový test: 2 mg 3 dny. 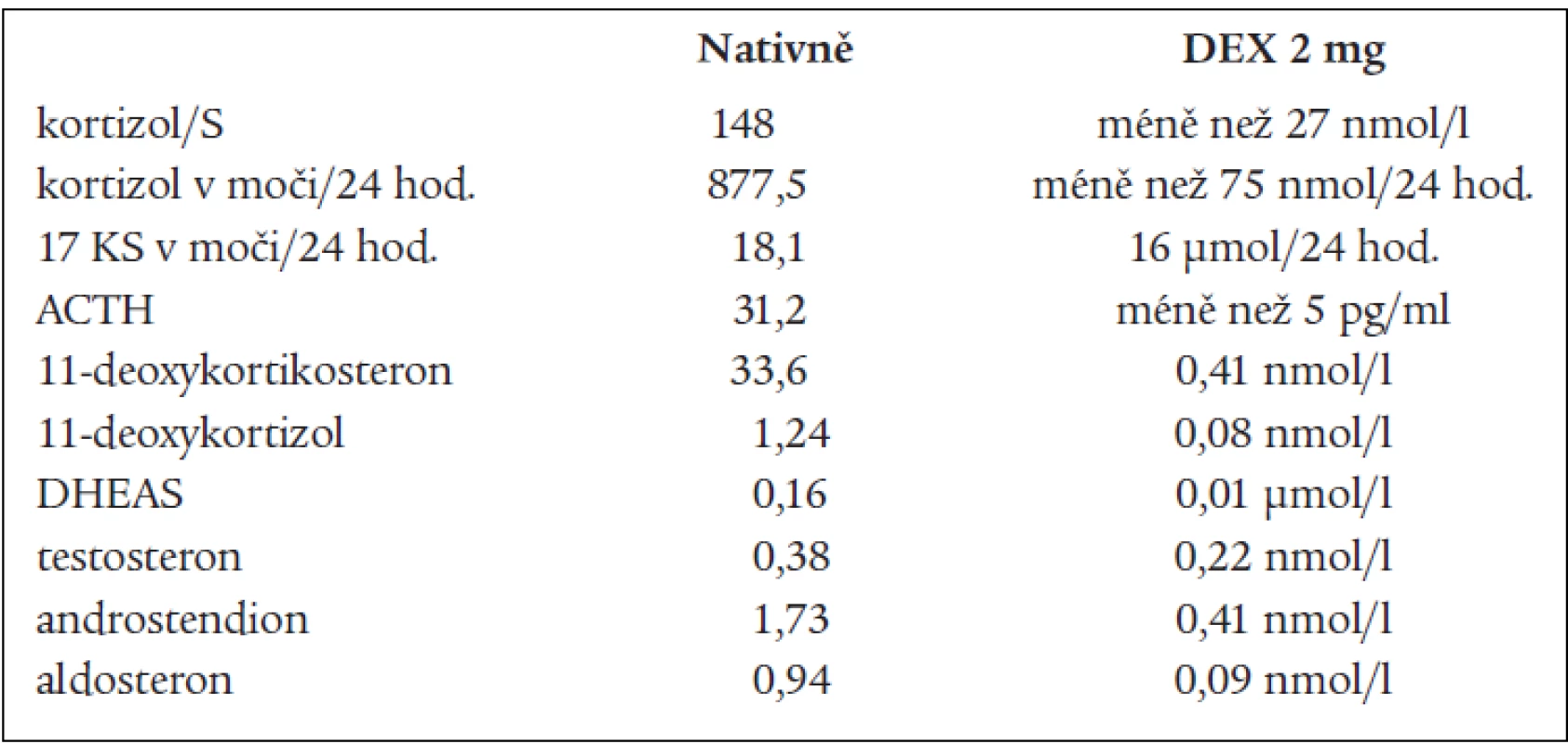
4. Steroidy po supresní terapii. 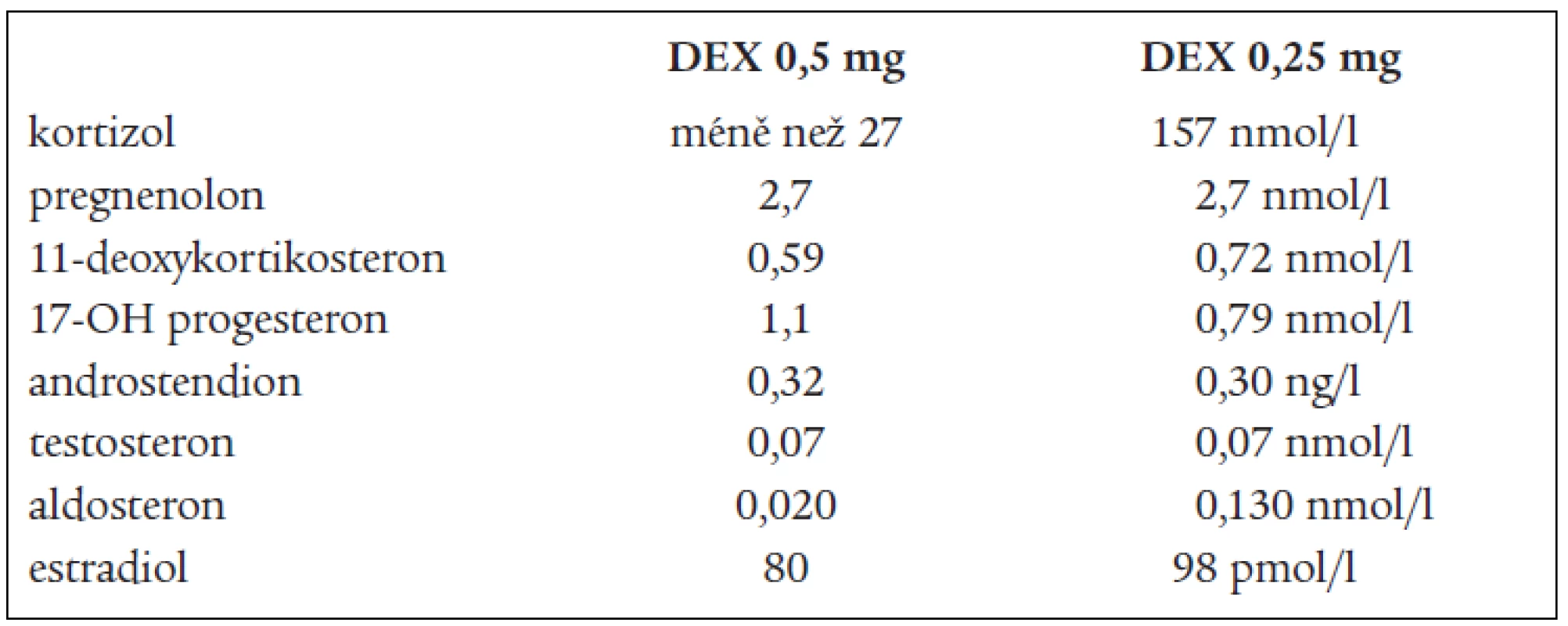
Diskuse
Blok 17α-hydroxylázy může být vzácnou příčinou hypertenze, hypokalemie a od dětství periferního hypogonadizmu, u děvčat s amenoreou, eunuchoidním habitem a vysokými hladinami FSH a LH. Jeho incidence je velmi nízká, v literatuře jsou popisovány jen ojedinělé případy. Vázne zde přeměna pregnenolonu na 17-hydroxypregnenolon a progesteronu
na 17-hydroxyprogesteron. V kůře nadledvin i v gonádách je snížená tvorba androgenů a estrogenů, v kůře nadledvin je snížená tvorba kortizolu a pod tlakem zvýšené hladiny ACTH je zvýšená tvorba 17-deoxysteroidů, které mají mineralokortikoidní účinky. Při tomto bloku by měly být 17-hydroxylované steroidy a jejich metabolity snížené, nebo při dolním okraji normy. Jsou to z C21 steroidů 17-OH-pregnenolon, 17-OH-progesteron, kortizol, 11-deoxykortizol a z C19 steroidů DHEAS, DHEA, testosteron, androstendion a 11β-OH-androstendion. Výsledky naší pacientky splňují tuto podmínku. To, že jsou některé z těchto steroidů v mezích normy, lze vysvětlit tím, že enzymové bloky nejsou většinou úplné, a hyperplastické nadledviny příslušný deficit kompenzují. Naopak steroidní hormony, které nemají 17-OH skupinu a jejich prekurzory i metabolity, by měly být zvýšené. Je to progesteron, pregnenolon, 11-deoxykortikosteron (11-DOC) a aldosteron. Z výsledků je patrné, že i tato podmínka je splněna (tab. 1). Hladina aldosteronu může být u defektu 17α-hydroxylázy snížená, protože extrémně vysoké hladiny ACTH dependentních steroidů, hlavně deoxykortikosteronu, vedou k expanzi extracelulárního volumu a hypertenzi a k potlačení plazmatické reninové aktivity, což může vést ke sníženým hladinám aldosteronu. U naší nemocné jsme zachytili v různých obdobích hladinu aldosteronu sníženou, v normě, i lehce nad normu. Konečné hormony steroidogeneze (kortizol, dihydrotestosteron a estradiol) jsou v normě, proto nejsou u pacientky výrazné známky hypogonadizmu, ale výrazný nadbytek 11-DOC způsobuje hypertenzi a hypokalemii. Pokud se týká supresních a stimulačních testů, tak všechny steroidy reagovaly snížením v dexametazonovém testu (tab. 2) a výrazným (u 11-DOC) či mírným vzestupem v testu s ACTH (tab. 3), což svědčí proti diagnóze tumoru a potvrzuje příčinu onemocnění. V terapii je důležitá správně volená dávka supresní léčby, kdy je nutno brát v úvahu klinický stav, hodnoty TK a hladiny steroidů (tab. 4). Při zahájení terapie dexametazonem mohl být počáteční sklon k hypotenzi a hyperkalemii způsoben potlačeným renin-aldosteronovým systémem, který se může navrátit k normě až za několik měsíců. U dospělých pacientek je obvykle nutné zavedení substituční kombinované terapie estrogeny a gestageny.
V kazuistice jsme chtěli upozornit na možnost vzácného výskytu defektu 17α-hydroxylázy, který může být příčinou endokrinní hypertenze a hypokalemie a poruch menstruačního cyklu. Při podezření na tuto diagnózu je nutné vyšetření celého steroidního spektra včetně testů s ACTH a s dexametazonem.
Tato práce vznikla za podpory výzkumného záměru Ministerstva zdravotnictví ČR č. MZ 000000023761.
MUDr. Věra Olšovská
www.fnusa.cz
e-mail: vera.olsovska@fnusa.cz
Doručeno do redakce: 11. 3. 2004
Přijato po recenzi: 14. 4. 2004
Sources
1. Hampl R, Stárka L. Současné možnosti steroidní laboratorní diagnostiky. DMEV 1999; 4 : 206–211.
2. Šulcová J, Stárka L. Adrenální enzymopatie s pozdním nástupem. In: Stárka L et al. Aktuální endokrinologie. Praha: Maxdorf 1999 : 540–562.
3. Procházková V, Lebl J et al. Klinická diagnostika pacientů s kongenitální adrenální hyperplazií. Česko–slovenská pediatrie 1999; 10 : 544–547.
4. Costa-Santos M, Kater CE et al. Two prevalent CYP17 mutations and genotype-phenotype correlations in
24 Brazilian patients with 17-hydroxylase deficiency. Hum Genet 2004; 89 : 95–96.
5. Van Den Akker EL, Koper JW et al. Differential inhibition of 17-hydroxylase an 17, 20-lyase activities by three movel missense CYP 17 mutations identified in patients with P450c17 deficiency. J Clin Endocrinol Metab 2002; 87. 5714–5719.
6. Biglieri EG, Herron MA et al. 17 - hydroxylation deficiency in man. J Clin Invest 1966; 45 : 1946–1954.
7. Imai T, Yanase T et al. Canadian Mennonites and individuals residing in the Friesland region of The Netherlands share the same molecular basis of 17-hydroxylase deficiency. Hum Genet 1992; 89 : 95–96.
8. Costa-Santos M., Kater, CE et al. Two intronic mutations cause 17-hydroxylase deficiency by disrupting splice acceptor sites: direct demonstration of abberant splicing and absent enzyme activity by expression of the entire CYP17 gene in HEK–293 cells. J Clin Metab 2004, 89, 43–48.
9. Kater CE, Biglieri EG. Disorders of steroid 17-hydroxylase deficiency. Endocrin Metab Clin North Am 1994; 23 : 341–357.
10. Grumbach MM, Hughes IA et al. Disorders of sex differentiation. In: Larsen PR, Kronnenberg HM et al. Wiliams textbook of endocrinology. 10th ed. Philadelphia: WB Saunders 2003; 842–1002.
11. Yanase T, Simpson ER et al. 17-hydroxylase/ 17,20 lyase deficiency: from clinical investigation to molecular definition. Endocrin Rev 1991; 12 : 91–108.
12. Mendonca BB, Inacio M et al. Male pseudohermafroditism due to 17-betahydroxysteroid dehydrogenase 3 deficiency. Diagnosis, psychological evaluation and management. Medicine 2000; 79:
299–309.
13. Rabinovici J, Blankstein J et al. In vitro fertilization and primary embryonic cleabage beta estradiol, are possible in 17-hydroxylase deficiency despite extremely intrafollicular 17-beta estradiol. J Clin Metab 1989; 68 : 693––697.
14. Votava F, Kračmar P et al. Novorozenecký screening kongenitální adrenální hyperplazie. Čes Slov pediatrie 2002; 12 : 690–696.
15. Lisá L. Nové poznatky o léčbě vrozené adrenální hyperplazie. Forum medicinae 2000; 2 : 52–57.
16. Ferrari P, Bianchetti M. Juvenile hypertension, the role of genetically altered steroid metabolism. Hormone research 2001; 5 : 213–223.
17. Widimský J. Hypertenze. Praha: Triton 2002 : 368–370.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2005 Issue 2-
All articles in this issue
- Geriatrics as an inter-disciplinary science on the threshold of the 21st century
- Stem cells: new promise in medicine
- Tumor lysis syndrome
- Adiponectin – the new adipocyte-derived hormone with relation to obesity and insulin resistance
- Congenital adrenal hyperplasia, defect of 17α-hydroxylase as a rare cause of hypertension and hypocalaemia
- Heparin-induced thrombocytopenia in a patient with left main coronary artery stenosis
- Treatment of chronic infection with hepatitis C virus with pegylated interferon and ribavirin in patient with mixed cryoglobulinaemia
- Pedal bypass in the treatment of diabetic foot ischemia – midterm results
- Pulse pressure in the young population detected by ABPM and it’s relation to metabolic and anthropometric parameters
- Apoptosis assessment in acute myeloid leukemia and B-cell chronic lymphocytic leukemia cells after in vitro cytostatics treatment and its relationship to multidrug resistance
- Personal experience with the origin and duration of spontaneous remission in adult type 1 diabetics
- The influence of combined aerobic and resistance training on left ventricle function in patients after acute myocardial infarction
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Pulse pressure in the young population detected by ABPM and it’s relation to metabolic and anthropometric parameters
- Congenital adrenal hyperplasia, defect of 17α-hydroxylase as a rare cause of hypertension and hypocalaemia
- Tumor lysis syndrome
- Personal experience with the origin and duration of spontaneous remission in adult type 1 diabetics
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career