-
Medical journals
- Career
Přínos ERG v časné diagnostice chlorochinové a hydroxychlorochinové makulopatie
Authors: M. Karkanová; V. Matušková; E. Vlková; H. Došková; R. Uhmannová
Authors‘ workplace: Oční klinika LF MU a FN Brno, přednostka prof. MUDr. E. Vlková, CSc.
Published in: Čes. a slov. Oftal., 66, 2010, No. 2, p. 62-66
Overview
Deriváty chlorochinu (Plaguenil, Delagil), využívané při dlouhodobé léčbě revmatických onemocnění, mohou způsobovat klinicky ověřenou ireverzibilní makulopatii, která může progredovat i po jejich vysazení.
Optimální časná diagnostika okulární toxicity chlorochinových nebo hydroxychlorochinových preparátů je stále kontroverzní. Cílem průřezové práce bylo zhodnotit vhodnost indikace elektroretinografického (ERG) vyšetření z důvodu časné diagnostiky kumulativní polékové makulopatie.
Fotopický, pattern a multifokální ERG (Retiscan dle metodiky ISCEV) byl vyšetřen u 10 pacientů (20 očí) léčených antimalariky, 9 pro revmatoidní artritidu (RA), 1 pro systémový lupus erythematodes (SLE). Průměrný věk pacientů byl 60 ± 15 let, doba léčby 10 ± 11 roků, medián doby léčby 5 let. Kontrolní soubor tvořilo 12 zdravých pacientů (20 očí) srovnatelného věkového průměru, bez zřejmé oční patologie. U všech bylo provedeno komplexní oftalmologické vyšetření: nejlépe korigovaná zraková ostrost (NKZO) do dálky na Snellenových optotypech, nitroční tlak (NOT) na bezkontaktním tonometru NIDEK NT-2000, Amslerův test, vyšetření předního segmentu a očního pozadí na štěrbinové lampě. Vstupní kritéria obou souborů byla NKZO do dálky 5/7,5 a lepší, NOT v normě, Amslerův test negativní, přední oční segment bez významného omezení transparence, oční pozadí fyziologické nebo s jemnými granulárními přesuny pigmentu v makule.
Signifikantní rozdíl, mezi souborem pacientů užívajících chlorochin nebo hydroxychlorochin a kontrolním souborem, se na 1% hladině významnosti prokázal v následujících parametrech, u fotopického ERG v hodnotě latence vlny b [ms], u pattern ERG v hodnotě amplitudy vlny N35–P50 [μV] a P50 – N95 [μV] a na 5% hladině významnosti u fotopického ERG v hodnotě amplitudy vlny a [μV] a u multifokálního ERG v hodnotě latence složky P1 [ms] a N1 [ms] v pericentrálním ringu.
Z výsledků vyplývá, že ERG je vyšetření vhodné pro časnou diagnostiku kumulativní polékové makulopatie způsobené deriváty chlorochinu. Ideální je ale individuální srovnání ERG hodnot u pacienta před a v určitých časových odstupech po nasazení derivátů chlorochinu.Klíčová slova:
ERG, antimalarika, kumulativní poléková makulopatieÚvod
Mezi všeobecně užívaná antimalarika patří chlorochin a hydroxychlorochin. Chlorochin (CQ) byl vynalezen v roce 1934 Hansem Andersagem pod názvem Resochin. Později byl znovu objeven v USA v roce 1946 pod názvem Chlorochin [22]. Nejdříve byl pro svoji schopnost tvořit komplexy s nukleoproteiny využíván k prevenci a léčbě malárie. Později se pro svůj specifický zásah do imunitních dějů v organismu začal využívat k léčbě autoimunitních revmatologických onemocnění (RA, SLE atd.). Chlorochin stabilizuje lysozomální membrány a tlumí buněčné dělení. V současnosti je u nás distribuován pod firemním názvem Delagil (Chloroqiuni phosphas, 250 mg v 1 tbl.). Modifikací chlorochinu s menší frekvencí systémových komplikací léčby je hydroxychlorochin (HCQ). Distribuován je pod firemním názvem Plaguenil (Hydroxychloroquini sulfas, 200 mg v 1 tbl.).
Nežádoucí účinky antimalarické léčby způsobuje především jejich vysoká afinita k melaninu a dlouhý biologický eliminační poločas (14 dní CQ, 30 dní HCQ). Toxicita je nejen oční, ale i dermatologická, gastrointestinální, hematologická a neuromuskulární. Oční toxicita byla poprvé popsána Cambiaggim v roce 1957 [3]. Antimalarika mohou způsobovat reverzibilní keratopatii, postižení ciliárního tělesa a někdy i ireverzibilní kumulativní retinopatii způsobenou akumulací CQ/HCQ solí v retinálním pigmentovém epitelu (RPE) a jejich vazbou na melaninová granula. Dochází k deficitu fagocytických funkcí RPE a následkem insuficience RPE k úbytku fotoreceptorů a buněk vnějších vrstev sítnice.
O CQ/HCQ retinopatii poprvé referovali Hobbs a kol. v roce 1959 [8]. Dřívější definice byly založeny na morfologických změnách sítnice. Funkční změny se staly součástí definic mnohem později. Easterbrook v roce 1999 definoval, že CQ/HCQ makulopatie je definována jako oboustranné, reprodukovatelné abnormality v centrálním či paracentrálním zorném poli pacienta, potvrzené dvěma rozličnými funkčními testy [5].
Pacienti s CQ/HCQ makulopatií si mohou stěžovat na potíže při čtení, světloplachost, světelné záblesky a centrální či paracentrální defekty v zorném poli. Na očním pozadí pacientů můžeme sledovat různé obrazy od fyziologického nálezu, přes granulární pigmentace makulární oblasti neodlišitelné od suché formy věkem podmíněné makulární degenerace (VPMD) až po oválné kolo depigmentace s prstýnkem zvýšené pigmentace v okolí (Bull’s eye maculopathy) (obr. 1).
Image 1. Bull’s eye maculopathy 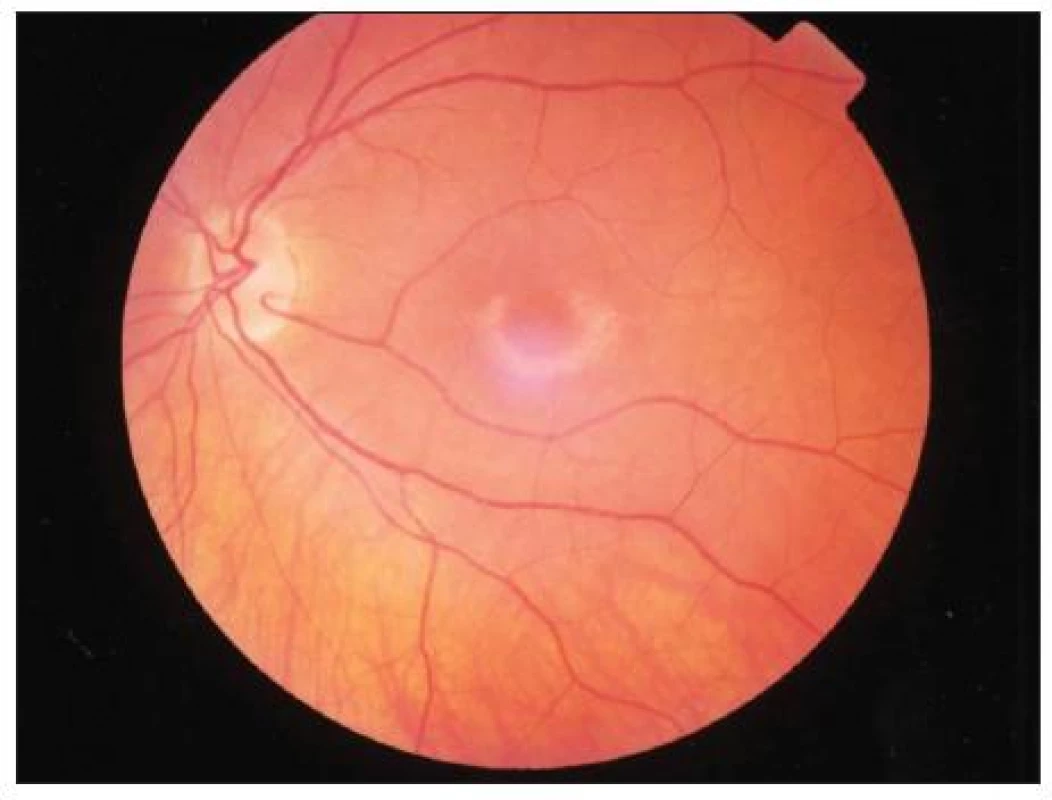
Součástí současné časné diagnostiky oční toxicity antimalarik jsou následující vyšetření: NKZO do blízka i do dálky, vyšetření NOT, vyšetření předního segmentu na štěrbinové lampě, očního pozadí nepřímou oftalmoskopií, Amslerův test, různé testy barvocitu, statická makulární perimetrie a pattern/multifokální ERG.
Riziko rozvoje retinopatie a kritéria, dle kterých je možné toto riziko stanovit, je v současnosti náplní mnoha prací. Zohledňovány jsou především tyto parametry: věk pacienta, jiné systémové postižení, dávka léku a doba léčby. Rigaudiere v roce 2004 rozdělil pacienty do 3. stadií dle rizika rozvoje retinopatie. Do stadia I. (nízké riziko) zařadil všechny pacienty, kteří splňovali následující kritéria: věk < 65 let, bez ledvinného, jaterního a retinálního onemocnění, léčba < 5 let v dávce pro HCQ ≤ 6,5 mg/kg/d., pro CQ ≤ 3 mg/kg/d. a doporučil u nich oční vyšetření každých 18 měsíců. Pacienti, kteří nesplňovali třeba jen jedno z výše zmíněných kritérií, bez fundoskopických známek retinopatie, byli zařazeni do stadia II. (v riziku) a bylo u nich doporučeno oční vyšetření každých 12 měsíců.
Pacienti s fundoskopickými známkami retinopatie byli zařazeni do stadia III. (v riziku) a oční vyšetření bylo doporučeno každých 6 měsíců [16].
Cíl
Optimální časná diagnostika okulární toxicity chlorochinových nebo hydroxychlorochinových preparátů je stále kontroverzní. Cílem průřezové práce bylo zhodnotit vhodnost indikace ERG vyšetření z důvodu časné diagnostiky kumulativní polékové makulopatie.
Materiál a metodika
Fotopický, pattern a multifokální ERG (Retiscan dle metodiky ISCEV) byl vyšetřen u 10 pacientů (20 očí) léčených antimalariky, 9 pro revmatoidní artritidu, 1 pro systémový lupus erythematodes. Průměrný věk pacientů byl 60 ± 15 let, doba léčby 10 ± 11 roků, medián doby léčby 5 let. Kontrolní soubor tvořilo 12 zdravých pacientů (20 očí) srovnatelného věkového průměru, bez zřejmé oční patologie. U všech bylo provedeno komplexní oftalmologické vyšetření: nejlépe korigovaná zraková ostrost (NKZO) do dálky na Snellenových optotypech, nitrooční tlak (NOT) na bezkontaktním přístroji NIDEK NT-2000, Amslerův test, vyšetření předního segmentu a očního pozadí na štěrbinové lampě. Vstupní kritéria obou souborů byla NKZO do dálky 5/7,5 a lepší, NOT v normě, Amslerův test negativní, přední oční segment bez významného omezení transparence, oční pozadí fyziologické nebo s jemnými granulárními přesuny pigmentu.
ERG vyšetření jsme provedli dle směrnic mezinárodní organizace ISCEV – německý přístroj RETIport32 od firmy ROLAND CONSULT. Používali jsme DTL elektrody. Testovací parametry jednotlivých elektroretinografických vyšetření byly následující: u fotopického ERG GF LED Flash 0 dB (3,00 cds/m2) BL 25 cd 0,5Hz, u pattern ERG Patt.Rev. CB, 0°48’ full field, CTR: 97% 4,304 Hz, u multifokálního ERG 61 segments, view angle 27 deg.
Výsledky
Ke statistickému zhodnocení jsme použili Mann – Whitney U test. Signifikantní rozdíl, mezi souborem pacientů užívajících CQ/HCQ a kontrolním souborem, se na 1% hladině významnosti prokázal v následujících parametrech, u fotopického ERG (F ERG) v hodnotě latence vlny b [ms], u pattern ERG (P ERG) v hodnotě amplitudy vlny N35 – P50 [μV] a P50 – N95 [μV] a na 5% hladině významnosti u F ERG v hodnotě amplitudy vlny a [μV] a u multifokálního ERG (Mf ERG) v hodnotě latence složky P1 [ms] a N1 [ms] v pericentrálním ringu.
P ERG je vyšetření vhodné pro časnou diagnostiku kumulativní polékové makulopatie. Hodnota amplitudy vlny N35 – P50 [μV] a P50 – N95 [μV] byla na 1% hladině významnosti statisticky signifikantně snížena u souboru léčených pacientů oproti kontrolní skupině (obr. 2). U f ERG u souboru CQ/HCQ léčených byla, statisticky signifikantně na 1% hladině významnosti, prodloužena latence vlny b [ms] a na 5% hladině významnosti došlo k prohloubení negativní složky fotopického ERG záznamu, vlny a [μV] (obr. 3). V rámci jednotlivých vyšetření je ale posouzení pozitivity výsledku stran rozvoje makulopatie u F ERG složitější. P ERG je z hlediska našich dosavadních výsledků a zkušeností výrazně vhodnější metoda. U Mf ERG byly na 5% hladině významnosti, u léčených pacientů, statisticky signifikantně prodlouženy hodnoty latence komponent N1 [ms] a P1 [ms] v pericentrálním ringu oproti kontrolnímu souboru (obr. 3). Vzhledem k rozložení hodnot v souboru, výraznému rozptýlení hodnot u jednotlivých pacientů, považujeme zatím Mf ERG v rámci časné diagnostiky kumulativní polékové makulopatie za doplňkové.
Image 2. Srovnání amplitud vln N35 - P50 a P50 - N95 u P ERG mezi souborem pacientů léčených CQ/HCQ a kontrolním souborem pacientů 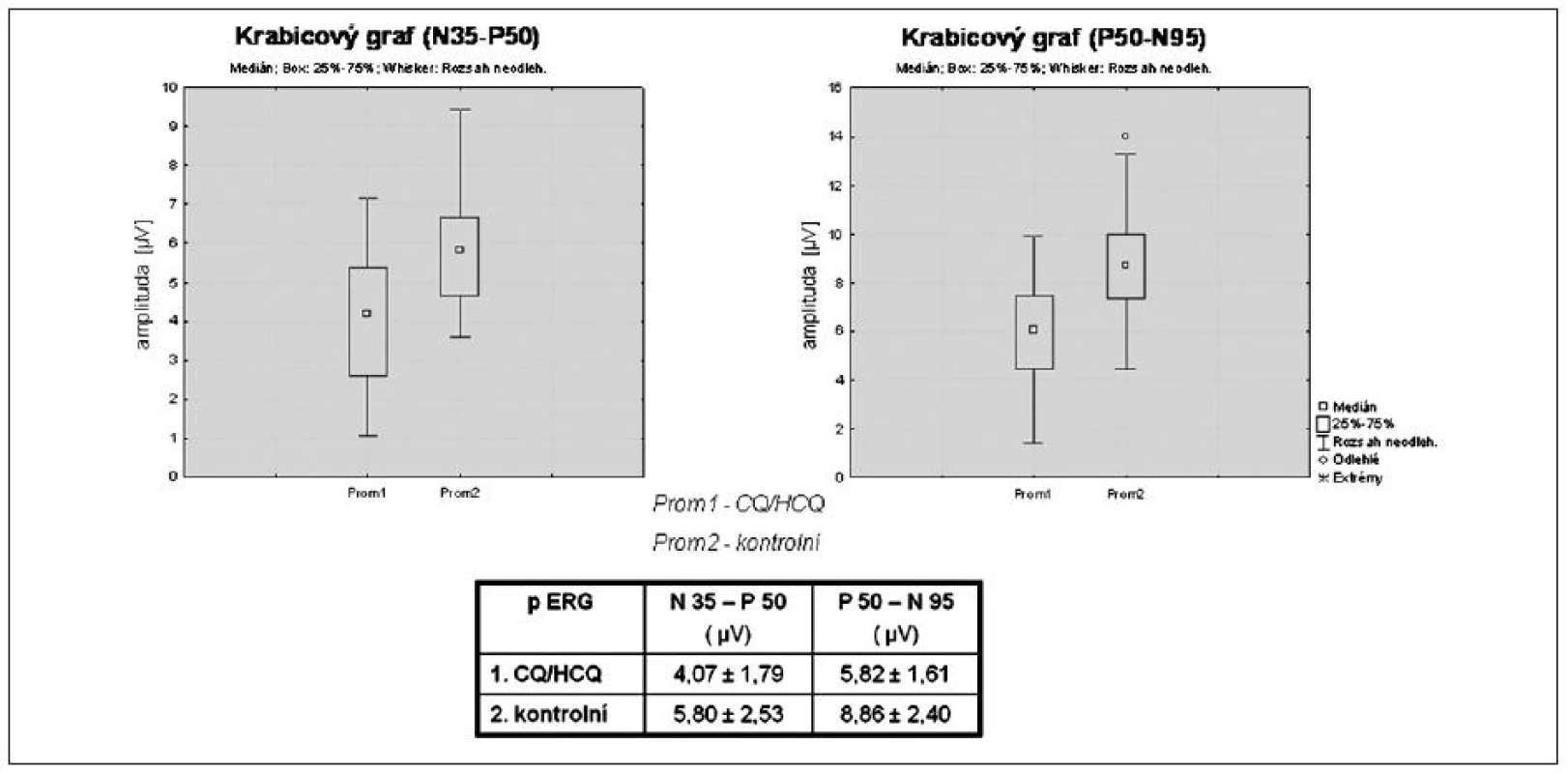
Image 3. Srovnání amplitudy vlny a a latence vlny b u F ERG a latence vln N1 a P1 u Mf ERG mezi souborem pacientů léčených CQ/HCQ (Prom 1) a kontrolním souborem pacientů (Prom 2) 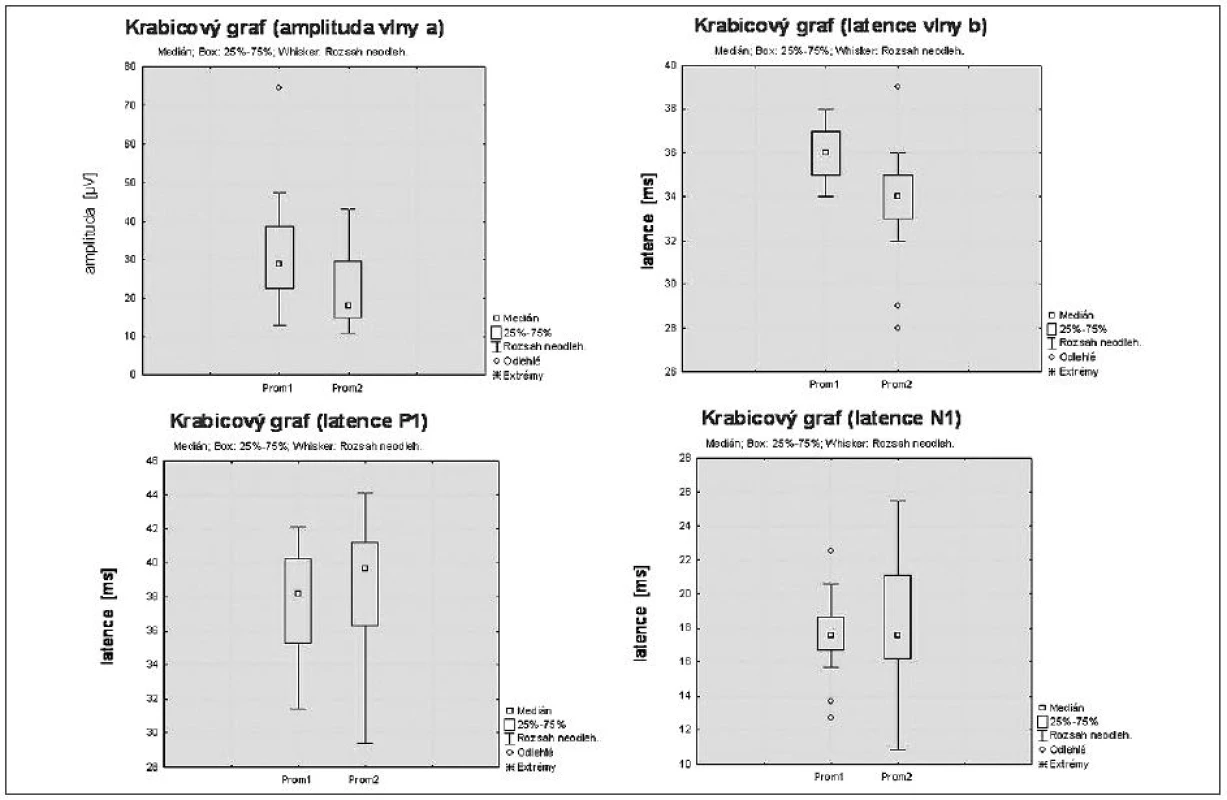
Při zhodnocení výsledků P ERG jsme doporučili vysazení antimalarik u 4 pacientů, u kterých byly hodnoty amplitudy vlny N35 – P50 [μV] nebo P50 – N95 [μV] menší než u kontrolního souboru od průměru odečtená směrodatná odchylka. Při srovnání ERG výsledků pacientů, u kterých bylo doporučeno vysazení antimalarik, s rizikem rozvoje retinopatie dle Rigauldiera nebyla nalezena významná souvislost. 1 z pacientů byl zařazen dle výše uvedených podmínek do stadia I., 1 do stadia II. a 2 do stadia III. Ideální je individuální srovnání ERG hodnot před nasazením a v určitých časových odstupech po nasazení derivátů chlorochinu. Interval mezi oftalmologickým vyšetřením pacienta, včetně funkčních testů (barvocit, makulární mikroperimetrie, ERG), je nadále diskutovanou otázkou.
Diskuse
V 70. letech studovali u nás přínos ERG při diagnostice kumulativní CQ/HCQ retinopatie Svěrák, Peregrin. a kol. [19, 20]. Popisovali u F ERG prohloubení vlny a a snížení vlny b, zřetelnější při zvyšující se intenzitě světelného podnětu a u EOG snížení Ardenova indexu u CQ/HCQ léčených pacientů v důsledku primárního poškození RPE. Ještě neměli možnost vyšetřovat P ERG, ale zkoumali i vliv CQ/HCQ makulopatie na pattern vizuální evokované potenciály (P VEP). K podobným výsledkům dospěli i světoví autoři [22]. V 80. až 90. letech, kdy prošlo ERG vyšetření standardizací, byly tyto výsledky potvrzeny v mnoha světových prácích. Po zavedení P ERG a později Mf ERG do elektrofyziologické diagnostiky, bylo studium ERG změn v rámci CQ/HCQ makulopatie zaměřeno spíše tímto směrem, neboť tyto metodiky se ukázaly mnohem specifičtější. Ve světové literatuře je v současnosti popisována významná úloha P a Mf ERG při časné diagnostice kumulativní CQ/HCQ makulopatie [2, 10, 11, 12, 13, 15]. Dle mnohých prací se zdá, že ERG detekuje časné změny dříve než jiné funkční testy, jako makulární perimetrie, testy barvocitu nebo Amslerův test. Stejně jako v naší práci popisují charakteristické snížení amplitud vln N35 - P50 a P50 - N95 u P ERG, při vyšetření Mf ERG některé práce udávají snížení amplitud N1 a P1 v centrálním a více v paracentrálním ringu. Tyto výsledky zatím naše práce nepotvrzuje. V naší práci byl sledován významný rozptyl hodnot jednotlivých komponent v centrálním i paracentrálním ringu, jak u léčených pacientů, tak u kontrolního souboru.
Řada prací se v současnosti věnuje také míře rizika rozvoje retinopatie. Většina prací popisuje riziko rozvoje retinopatie podobně jako Rigaudiere [1, 4, 6, 7, 14, 16, 17, 21]. V naší práci při srovnání ERG výsledků pacientů, u kterých bylo doporučeno vysazení antimalarik, s rizikem rozvoje retinopatie dle Rigauldiera nebyla nalezena významná souvislost. 1 z vyřazených pacientů byl dokonce zařazen dle výše zmíněných kritérií do stadia I. (nízké riziko).
Byla již publikována řada prací, které potvrdily možnost ireverzibilní progresivní ztráty zraku v důsledku rozvinuté CQ/HCQ retinopatie [9, 23]. Proto je třeba ve spolupráci s revmatology, při pozitivitě ERG výsledků (event. dalších funkčních testů), vždy zvážit přínos a rizika této léčby a možnost záměny za jiný lék.
Závěr
Pattern ERG je funkční vyšetření vhodné pro časnou diagnostiku kumulativní polékové makulopatie způsobené deriváty chlorochinu. I když u fotopického ERG byly nalazeny také statisticky významné rozdíly mezi léčenými pacienty a kontrolním souborem, v rámci jednotlivých vyšetření je posouzení pozitivity výsledku stran rozvoje makulopatie složitější. Vyšetření multifokálního ERG, přes statisticky významné rozdíly mezi soubory, považujeme zatím vzhledem k velkému rozptylu hodnot v obou souborech pro praxi za doplňkové.
Ideální je individuální srovnání ERG hodnot před nasazením a v určitých časových odstupech po nasazení derivátů chlorochinu. Interval mezi oftalmologickým vyšetřením pacienta, včetně funkčních testů (barvocit, makulární mikroperimetrie, ERG), je nadále diskutovanou otázkou.
MUDr. Michala Karkanová
Oční klinika MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: mkarkanova@fnbrno.cz
Sources
1. Araiza-Casilas, R., Cárdenas, F., Morales, Y.: Factors associated with chloroguine-induced retinopathy in rheumatic diseases. Lupus. 2004, 13, s. 119–124
2. Bui Quoc, E., Ingster-Moati, I., Rigolet, MH.: Ophthalmologic prevention of chloroguine and hydroxychloroguine induced retinopathy. Annales de Dermatologie et de Venerologie. 2005, 132, 4, s. 329–337
3. Cambiaggi, A.: Unusual ocular lesions in case of systemic lupus erythematodes. AMA Arch. Ophthalmol. 1957, 57, s. 451–453
4. Easterbrook, M., Bernstein, H.: Ophthalmological monitoring of patients taking antimalarials: preferred practice pattern. The Journal of Rheumatology. 1997, 24, 7, s. 1390–1392
5. Easterbrook, M.: An ophthalmological view on the efficacy and safety of chloroguine versus hydroxychloroquine. J. Rheumatol. 1999, 26, s. 1866–1868
6. Fardet, L., Revuz, J.: Synthetic antimalarials. Annales de Dermatologie et de Venereologie. 2005, 132, 8–9, s. 665–674
7. Grierson, DJ.: Hydroxychloroguine and visual screening in a rheumatology outpatient clinic. Annals of Rheumatic Diseases. 1997, 56, 3, s. 188–191
8. Hobbs, HE., Sorsby, A., Freedman, A.: Retinopathy following chloroguine therapy. Lancet. 1959, 2, s. 478
9. Ingster-Moati, I., Bui Quoc, E., Crochet, M.: Severe chloroquine and hydroxychloroquine induced retinopathy. Journal Francais d Opthalmologie. 2006, 29, 6, s. 642–650
10. Ingster-Moati, I., Crochet, M., Albuisson, E.: Electroretinogram b wave varies with the posology of the antimalarial treatment. Journal Francais d Opthalmologie. 2004, 27, 12, s. 1007–1012
11. Karkanová, M., Polanská, V., Vícha, I. et al.: Přínos ERG při screeningu chlorochinové a hydroxychlorochinové makulopatie, 55, In: Sborník abstrakt XV. výročního sjezdu České oftalmologické společnosti s mezinárodní účastí v Brně. Ed. Nucleus HK, 2007, s. 187, ISBN 978-80-87086-01-08.
12. Lai, T.Y., Ngai, J.W., Chan, W.M.: Visual field and multifocal electroretinography and their correlations in patients on hydroxychloroguine therapy. 2006, 112, 3, s. 177–187
13. Maturi, R.K., Yu, M., Weleber, R.G.: Multifocal electroretinographic evaluation of long-term hydroxychloroguine users. Archives of Ophthalmology. 2004, 122, 7, s. 973–981
14. Mavrikakis, I. et al.: The incidence of irreversible retinal toxicity in patients treated with hydroxychloroguine: a reappraisal. Ophthalmology. 2003, 110, 7, s. 1321–1326
15. Neubauer, AS., Stiefelmeyer, S., Berninger, T.: The multifocal pattern electroretinogram in chloroguine retinopathy. Ophthalmic Research. 2004, 36, 2, s. 106–113
16. Rigaudiere, F., Ingster-Moati, I., Hache, J.C.: Up-dated ophthalmological screening and follow-up management for long-term antimalarial treatment. Source Journal Francais d Ophthalmologie. 2004, 27, 2, s. 191–199
17. Scherbel, A.L., Mackenzie, A.H., Nousek, J.E.: Ocular lesions in rheumatoid arthritis and related disorders with particular reference to retinopathy. The New England Journal of Medicine. 1965, 12, 8, s. 360–366
18. Svěrák, J., Erbenová, Z., Peregrin, J.: ERG and EOG potentials after 6 years rescoring treatment. Sborník vědeckých prací Lékařské fakulty UK v Hradci Králové. 1971, 14, 2, s. 209–213
19. Svěrák, J., Peregrin, J., Salavec, M.: Electrophysiological methods of examination during prolonged administration of synthetic antimalarial drugs. Sborník vědeckých prací Lékařské fakulty UK v Hradci Králové. 1976, 19, 3–4, s. 427–434
20. Svěrák, J., Salavec, M., Peregrin, J.: Vliv antimalarik na činnost sítnice. Čs. Oftal. 1965, 21, 5, s. 370–378
21. Tokumaru, G.K.: New considerations in monitoring for hydroxychloroguine retinopathy. Clinical Eye and Vision Care. 1996, 8, s. 99–104
22. Tzekov, R.: Ocular toxicity due to chloroquine and hydroxychloroquine: electrophysiological and visual function correlates. Documenta Ophthalmologica. 2005, 110, s. 111–120
23. Wei, L.C., Chen, S.N., Ho, C.L.: Progression of hydroxychloroguine retinopathy after discontinuation of therapy. Chang Gung Medical Journal. 2001, 24, 5, s. 329–334
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2010 Issue 2-
All articles in this issue
- Využití moderních vyšetřovacích metod k časné diagnostice pigmentového glaukomu a syndromu pigmentové disperze
- Přínos ERG v časné diagnostice chlorochinové a hydroxychlorochinové makulopatie
- Implantace stenopeické aniridické zadněkomorové nitrooční čočky u poúrazových stavů – ano či ne?
- Liečba Angioid streaks (lakové trhliny) pomocou anti-VEGF
- Význam vitrektomie u diabetického makulárního edému a morfometrie chirurgicky odstraněné vnitřní limitující membrány
- Vliv operace idiopatické makulární díry s peelingem MLI a plynnou tamponádou na elektrickou funkci sítnice
- Využití intravitreální aplikace ranibizumabu v léčbě pozánětlivých neovaskulárních membrán – kazuistické sdělení
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Využití moderních vyšetřovacích metod k časné diagnostice pigmentového glaukomu a syndromu pigmentové disperze
- Přínos ERG v časné diagnostice chlorochinové a hydroxychlorochinové makulopatie
- Vliv operace idiopatické makulární díry s peelingem MLI a plynnou tamponádou na elektrickou funkci sítnice
- Implantace stenopeické aniridické zadněkomorové nitrooční čočky u poúrazových stavů – ano či ne?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

