-
Medical journals
- Career
Intrakraniální hematomy u warfarinizovaných pacientů – kazuistiky a doporučení léčby
Authors: V. Přibáň 1,2; M. Holý 3; I. Vonke 4
Authors‘ workplace: Neurochirurgické oddělení, Nemocnice České Budějovice, a. s. 1; Neurochirurgická klinika LF MU a FN Brno 2; Interní oddělení, Nemocnice České Budějovice, a. s. 3; Hematologické oddělení, Nemocnice České Budějovice, a. s. 4
Published in: Cesk Slov Neurol N 2009; 72/105(6): 570-574
Category: Case Report
Overview
Intrakraniální hematomy, úrazové i spontánní, jsou u warfarinizovaných pacientů zatíženy vysokou morbiditou/ mortalitou. Postiženi jsou obvykle starší, interně nemocní pacienti. Autoři prezentují kazuistiky intrakraniálních hematomů (dvou úrazových a jednoho spontánního) u antikoagulovaných pacientů s odlišným postupem substituční terapie. Je zdůrazněna nutnost časné úpravy hemokoagulačních parametrů. Dále je navržen terapeutický protokol rychlé substituce hemokoagulačních faktorů k stabilizaci hematomu a případné chirurgické intervenci. Je zdůrazněna nutnost koncentrovat warfarinizované pacienty s intrakraniálními hematomy do center s trvalou přítomností neurochirurga. Rychlá substituce spolu s okamžitou operací v případě klinické deteriorace je předpokladem zlepšení výsledků léčby intrakraniálních hematomů u antikoagulovaných pacientů.
Klíčová slova:
intrakraniální hematomy – warfarin – chirurgická léčbaVěnováno nedožitým 80. narozeninám MUDr. Miloslava Pexy, emeritního přednosty traumatologického oddělení Nemocnice České Budějovice.
Úvod
Neurochirurg je konfrontován s krvácivými komplikacemi orální antikoagulační terapie relativně často. Příčin je více, ale tou zásadní je malá terapeutická šíře preparátu warfarinu a jeho snadné předávkování. Stárnutím populace se navíc zvyšuje počet pacientů na orální antikoagulační terapii – warfarinu. Terapeutickou indikací warfarinu je žilní tromboembolická choroba; indikace preventivní zahrnují pooperační podávání po kardiochirurgických výkonech na chlopních, pooperační prevenci tromboembolie, trombofilní stavy a chronickou fibrilaci/flutter síní [1–4]. Prevalence antikoagulační terapie v populaci je odhadována na 0,5 %. Typickou komplikací antikoagulační terapie v neurochirurgii jsou intrakraniální hematomy, a to jak úrazové, tak spontánní. Incidence velkého krvácení u pacientů na warfarinu dosahuje 3,8 %, krvácení do centrální nervové soustavy pak 1 % [5]. Hematomy mohou být lokalizovány intrakraniálně subdurálně nebo intracerebrálně, méně často pak intraspinálně v epidurálním a subdurálním prostoru. Další možností je akutní krvácení do chronického subdurálního hematomu. Intrakraniální krvácivé komplikace terapie warfarinem (hematomy úrazové i spontánní) jsou zatíženy vysokou morbiditou/mortalitou [6–9]. Rychlá úprava hemokoagulačních parametrů je nezbytnou podmínkou urgentní operace [10–13]. Dalším důvodem včasné substituce faktorů hemokoagulace je skutečnost, že intrakraniální hematomy u warfarinizovaných pacientů mají tendenci k většímu nárůstu objemu v delším časovém intervalu, než je tomu u pacientů bez antikoagulace [14]. Iniciálně malé hematomy u pacientů v dobrém neurologickém stavu mají tendenci progredovat. Výsledkem nezřídka bývá klinická deteriorace s mizivou šancí na úpravu. Z těchto důvodů je na místě identifikace warfarinizovaných pacientů s kraniotraumatem a rychlá substituce u prokázaného intrakraniálního hematomu bez ohledu na aktuální indikaci k operační léčbě. Shodný terapeutický postup je indikován i u hematomů spontánních.
Kazuistika 1
76letá pacientka byla přijata na interní oddělení nemocnice s levostrannou hemiplegií, lucidní, bazálně komunikující. V anamnéze měla operaci aortokoronárního bypassu v roce 2005, chronickou fibrilaci síní a antikoagulační léčbu. Na CT mozku se prokázalo typické hypertonické krvácení v kapsule a bazálních gangliích 5 × 3 cm (obr. 1). Operační evakuace nebyla indikována. INR hodnota byla 1,85, Quick 45 %. Substituce k úpravě hemokoagulačních parametrů provedena nebyla. Během 4 hod došlo k deterioraci stavu – hluboké kóma, bilaterální mydriáza zornic. Kontrolní CT prokazuje progresi hematomu, nyní velikosti 9 × 6 × 5 cm, s intraventrikulární extenzí a přesunem středočárových struktur o 25 mm doleva; edém kmene (obr. 2). Za další hodinu pacientka umírá.
Image 1. CT mozku: typické hypertonické krvácení v kapsule a bazálních gangliích velikosti 50 × 30 mm s minimálním přetlakem. 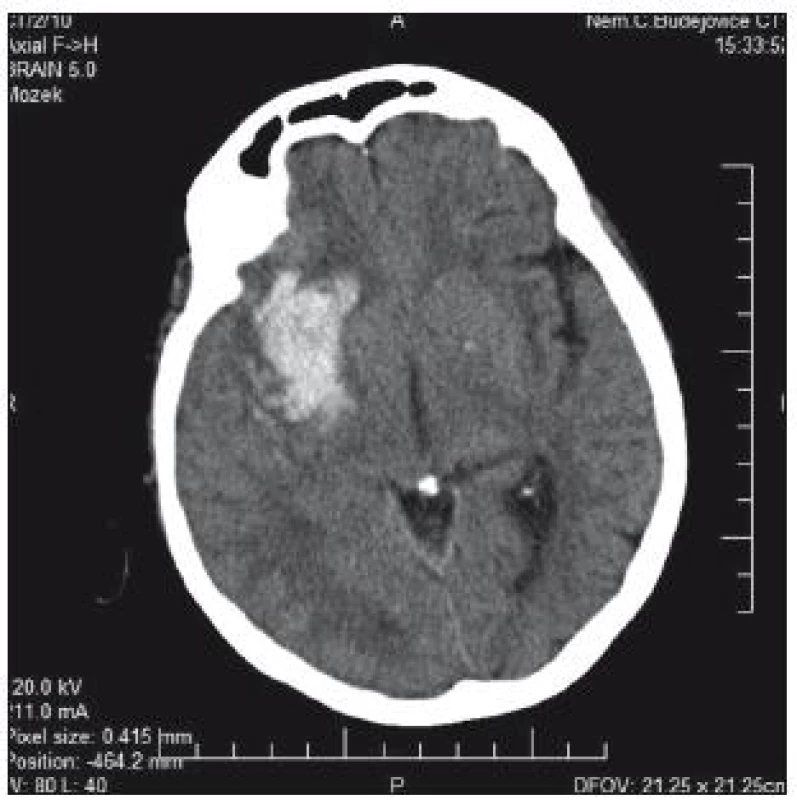
Image 2. CT mozku: výrazné zvětšení hematomu, s intraventrikulárním šířením a přesunem středočárových struktur o 25 mm doleva; edém kmene. 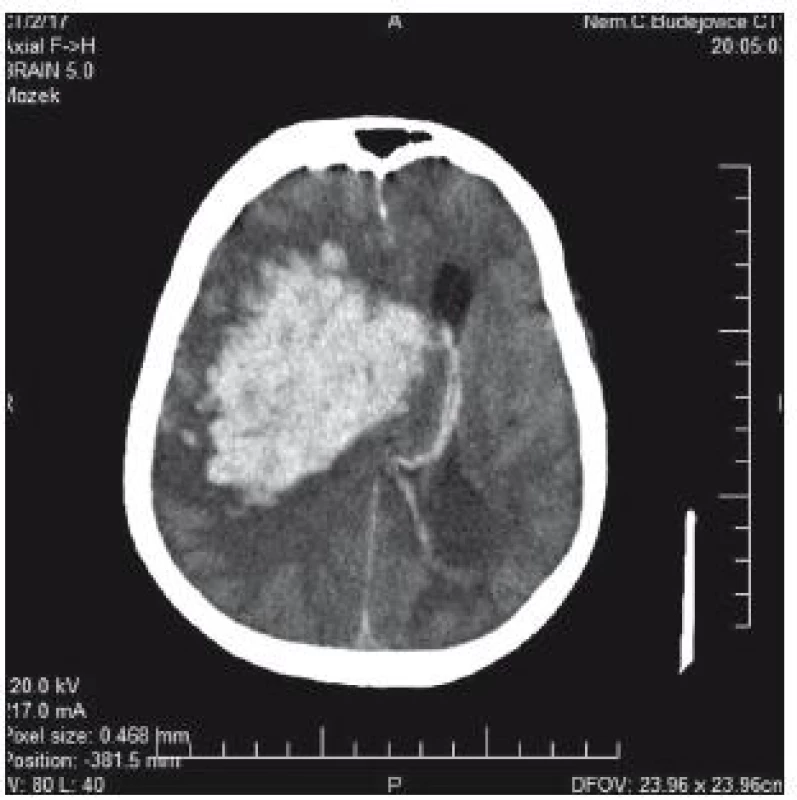
Kazuistika 2
74letý pacient byl po pádu a úderu do hlavy přijat na chirurgické oddělení okresní nemocnice. V klinickém obrazu byla cílená flexe na bolest, nesrozumitelné zvuky až jednotlivá slova, zavřené oči; GCS 8–9. CT prokazuje nález diskrétního plášťového akutního subdurálního hematomu frontotemporálně vpravo, traumatického subarachnoidálního krvácení a fisury kalvy (obr. 3). V anamnéze je patrná polymorbidita: ICHS, chronická fibrilace síní, chronická bronchitida, hypertenze a diabetes II. typu na inzulinu. Dlouhodobě je pacient warfarinizován – iniciální INR 2,57; Quick 31 %. Na základě klinického nálezu a CT byl pacient přeložen k observaci na traumatologii. Indikace k urgentní operaci nebyla. Byla zahájena substituce hemokoagulačních faktorů mraženou plazmou v kombinaci s kanavitem. Na kontrolním CT v odstupu 3 hod je zřejmý nárůst kontuzí frontobazálně vpravo a subarachnoidálního krvácení vlevo temporálně (obr. 4). Klinický stav se nemění. V odstupu dalších 4 hod na kontrolním CT (obr. 3) je nepatrná progrese kontuzí. Ani toto CT není indikací k intervenci. V tomto čase je INR 1,70 a Quick 49 %. V odstupu 20 hod od úrazu je již na CT rozsáhlá progrese kontuzních ložisek (obr. 5). INR je po 24 hod podávání kanavitu v kombinaci s mraženou plazmou (celkem 10 jednotek) 1,37; Quick 65%! V této chvíli již dochází k progresi klinického stavu a nutnosti následné intubace. Před ní je GCS 3. Pacient je následně přeložen na ARO spádové nemocnice a tam umírá druhý den po přijetí.
Image 3. CT mozku: plášťový akutní subdurální hematom frontotemporálně vpravo, traumatické subarachnoidální krvácení. 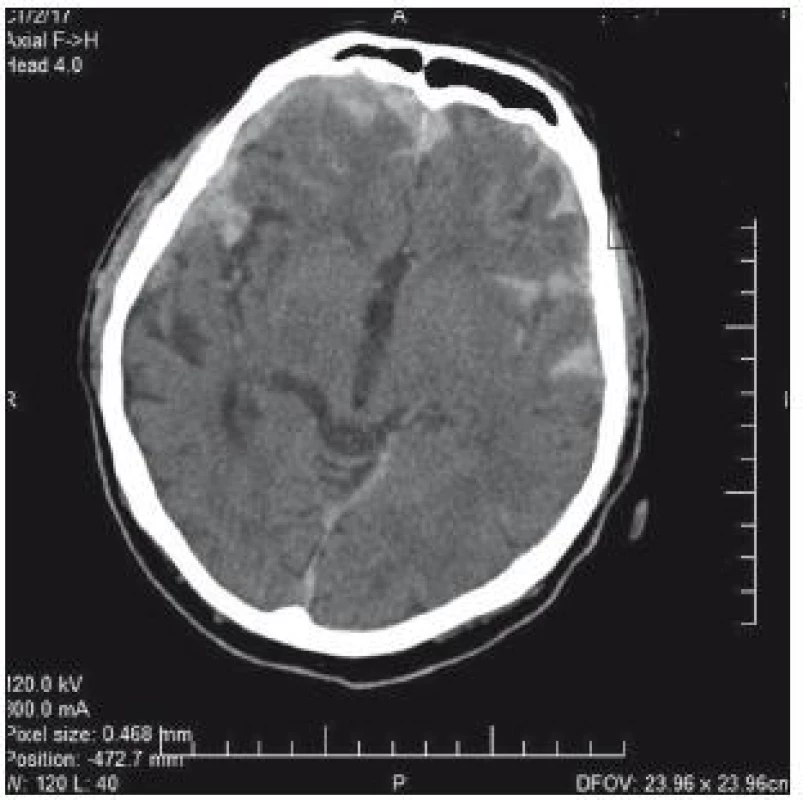
Image 4. CT mozku: progrese kontuzí frontobazálně vpravo a subarachnoidálního krvácení vlevo temporálně v odstupu 3 hod od úrazu. 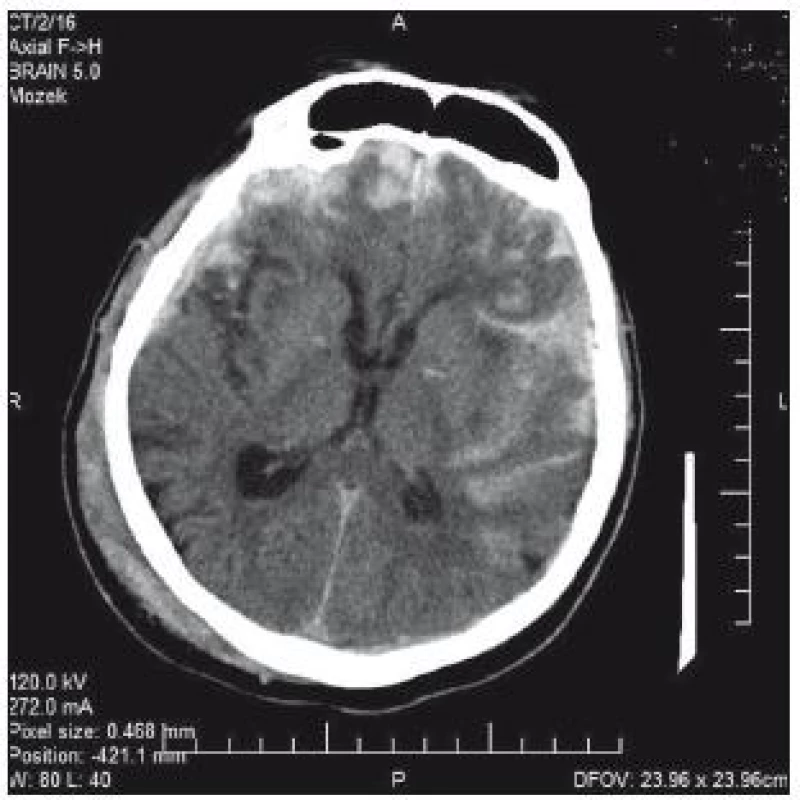
Image 5. CT mozku: výrazná progrese kontuzních ložisek 20 hod po úrazu. 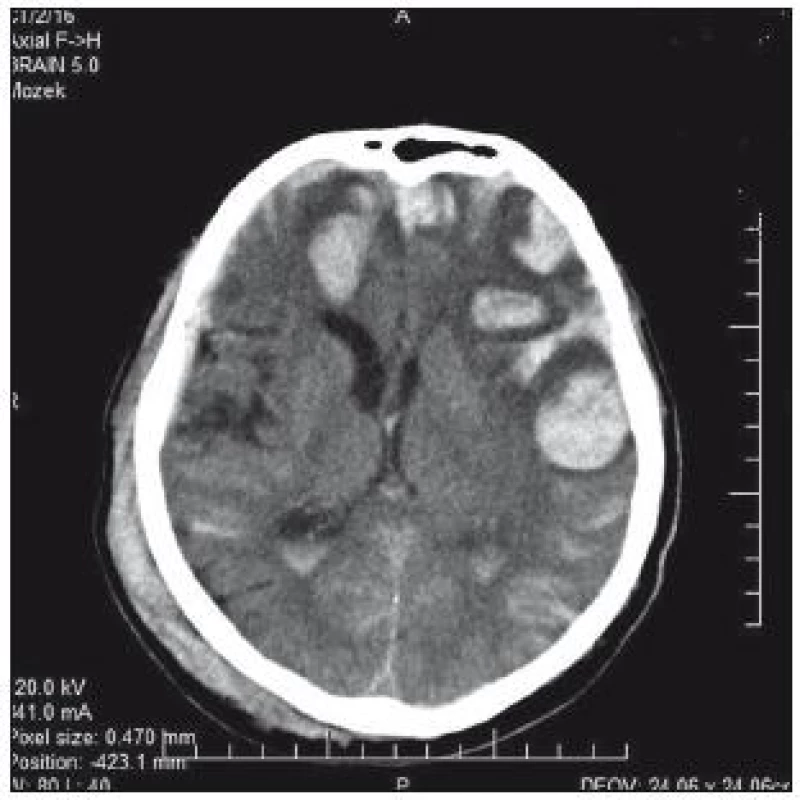
Kazuistika 3
66letý pacient byl přijat na interní oddělení okresní nemocnice pro bolesti hlavy. V anamnéze byl prokázán pád s úderem do hlavy, s přechodnou diplopií a tinitem dva dny před přijetím. CT nález: intracerebrální hematom temporálně vpravo 7 × 5 cm. Přetlak středových struktur zcela diskrétní (obr. 6). Vzhledem k anamnéze je hematom nepochybně traumatické etiologie. Pacient je lucidní, kontakt dobrý bez neurologického deficitu. Osobní anamnéza: stav po nefrektomii vpravo pro tumor, diabetes mellitus na PAD, hypertenze, chronická fibrilace síní – warfarinizace! (Quick 42 %). Během hodin dochází k zhoršení kvality vědomí, zmatenosti, GCS 13. Vzhledem k triádě progrese kliniky, CT nálezu hematomu a antikoagulaci je domluven překlad na ARO Nemocnice České Budějovice. Před transportem byl podán koncentrát protrombinového komplexu. Na transport byl pacient intubován. Akutní operace proběhla za úpravy hemokoagulačních parametrů: evakuace hematomu z kraniotomie. Kontrolní CT bylo příznivé (obr. 7). Pacient byl po extubaci bez neurologického deficitu přeložen do spádového zařízení.
Image 6. CT mozku: úrazový intracerebrální hematom temporálně vpravo. Přetlak středových struktur minimální. 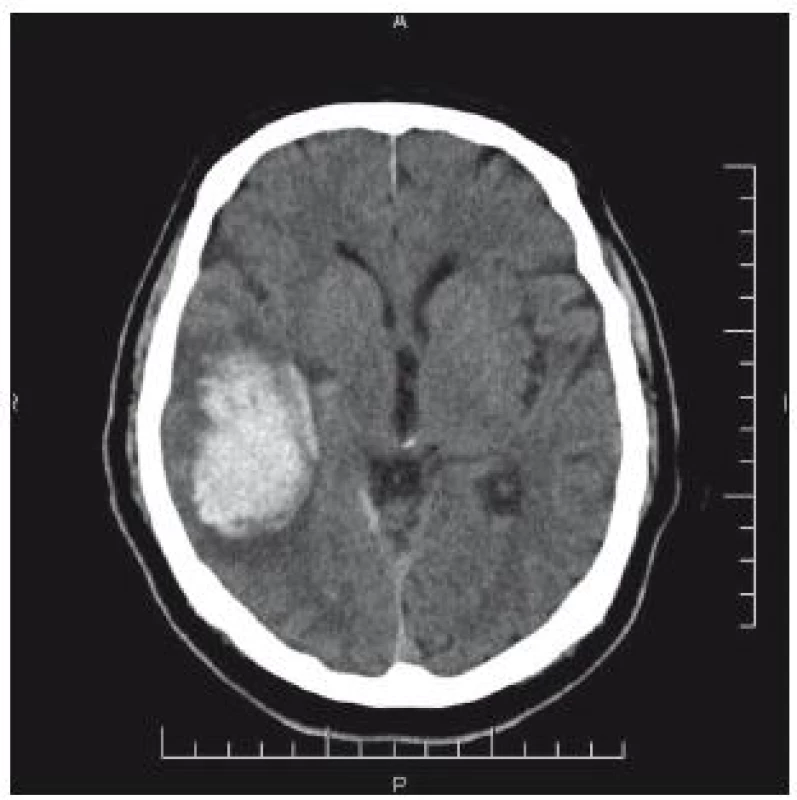
Image 7. CT mozku: příznivý nález po evakuaci hematomu z kraniotomie. 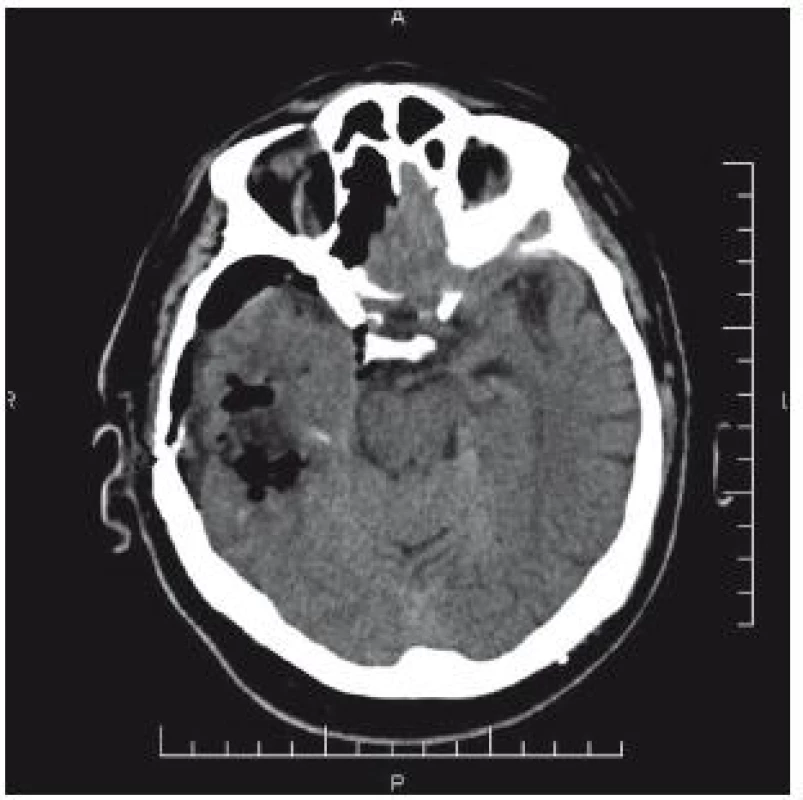
Diskuze
Warfarin je dobrý sluha, ale zlý pán. Původně prostředek na hubení hlodavců působí jako antagonista vitaminu K, nezbytného při tvorbě faktorů protrombinového komplexu (faktory II, VII, IX a X). Má postupný nástup účinku během několika dní. Jeho nevýhodou je úzké terapeutické rozpětí, nutnost monitorování účinku a potřeba spolupráce pacienta [2]. Účinek preparátu snižují barbituráty a některé potraviny (brokolice, papája). Předávkování může naopak nastat při kombinovaném podávání s nesteroidními antiflogistiky a na podkladě genetických faktorů – polymorfizmu cytochromu P 450 [15]. Terapeutická hladina je 2–3 INR. V tomto rozmezí je riziko závažného krvácení a intrakraniálního krvácení (ICH) relativně nízké – 0,5 % za rok, resp. 0,2 % u ICH [1]. Se zvyšujícím se INR dochází k závažnému zvýšení rizika krvácení. Uvádí se, že nárůst o každý stupeň škály INR zvyšuje dvojnásobně riziko krvácení proti předchozí hodnotě [7,16,17]. Riziko krvácení se liší s délkou podávání warfarinu. Nejvyšší je v prvním měsíci aplikace, kdy dosahuje 3 %. Zbytek prvního roku se snižuje na 0,8 % a následný rok pouhá 0,3 % [2]. Rizikové faktory intrakraniálního krvácení při antikoagulaci jsou: vyšší věk, opakované pády, nekorigovaná hypertenze, cévní mozková příhoda v anamnéze, intenzita antikoagulační léčby a kombinace s antiagregační terapií. Terapeutické podávání antikoagulace u žilní trombózy je obvykle 3–6 měsíců. Bohužel je běžnou praxí, že pacienti po prodělané žilní trombóze/plicní embolii jsou na antikoagulační léčbě mnohdy zbytečně roky. Dlouhodobá neodůvodněná antikoagulační léčba přináší zvýšené riziko vzniku život ohrožujícího krvácení. Nelze dostatečně zdůraznit úlohu praktického lékaře při správném sledování léčby a adekvátně načasovaném vysazení warfarinu. Chronická fibrilace/flutter síní se vyskytuje zejména u starších pacientů. Postihuje 4 % lidí nad 65 let [18]. Více než polovina pacientů s chronickou fibrilací/flutterem síní a antikoagulační léčbou je starší 75 let. Riziko ischemického iktu u pacientů s chronickou fibrilací síní není malé. Činí 5 % za rok při negativní anamnéze iktu. V případě pozitivní historie ischemické cévní mozkové příhody stoupá riziko až na 12 % [18,19]. Antikoagulace snižuje relativní riziko iktu o 68 % [20]. U 1 000 pacientů zabrání warfarin průměrně vzniku 23 ischemických iktů, na druhou stranu nastane 9 závažných krvácení [21].
Spontánní intracerebrální hematomy představují 10–15 % iktů s 30denní mortalitou 35–52 %. Rizikovými faktory vzniku hematomu u warfarinizovaných pacientů jsou vyšší věk, hypertenze a intenzita antikoagulace [10]. Výskyt spontánních intrakraniálních hematomů při antikoagulační léčbě je vzácný. Pokud ale krvácení nastane, pak je morbidita/mortalita extrémně vysoká. Fang et al uvádějí úmrtí nebo těžké poškození v 76 %, zatímco extrakraniální velké krvácení bylo zatíženo špatným výsledkem pouze ve 3% případů [9]. Hematomy u pacientů bez antikoagulace mají tendenci k rychlé expanzi objemu během 4 hod, u pacientů na warfarinu je tento proces prodloužen na 24–48 hod [22]. Flibotte uvádí nárůst objemu hematomu do týdne od počátku příhody u 54 % pacientů na warfarinu, zatímco u ostatních pouze v 16 % [23]. Tato pozorování jsou argumentem pro co nejrychlejší substituci.
Intrakraniální úrazové hematomy u warfarinizovaných jsou též zatíženy vysokou mortalitou. Mina et al udávají 4–5násobné riziko proti pacientům bez antikoagulace [6]. Významně stoupá mortalita u starých lidí [8,17,24,25]. Maligní je zejména kombinace vyššího věku s excesivní antikoagulací. Karni et al uvádějí u pacientů starších 65 let s INR nad 3,5 mortalitu 75 % [7]. Ivascu et al kladou důraz na rychlou identifikaci hematomů s okamžitou substitucí. Udávají významné snížení mortality ze 48 na 10 %. V terapeutickém protokolu použili mraženou plazmu v kombinaci s kanavitem [13]. Makris et al jako první upozornili na výhodnost užití koncentrátu protrombinového komplexu v kontrastu s mraženou plazmou [26]. Kalina et al srovnali efektivitu léčby protrombinového komplexu a mražené plazmy. Čas od podání do operace, čas do úpravy INR a procentuální úspěšnost úpravy vyzněla pro koncentrát. Mortalita byla v obou skupinách srovnatelná [12]. Problematika zvětšení hematomu v delším časovém intervalu s následnou deteriorací je známa [13]. Yasaka et al prokázali, že včasné podání koncentrátu protrombinového komplexu omezí nárůst hematomu ve srovnání s plazmou [14]. Nevýhodou při podání plazmy je nutnost aplikace poměrně velkých objemů (15–20 ml/kg ), což může vyústit v srdeční selhání. Navíc jsou tyto objemy podány v delším časovém intervalu a to může vést k výše zmíněnému zvětšení hematomu. Podávání plazmy s kanavitem upravuje INR o 0,18/hod [27]. To koresponduje s naší zkušeností z kazuistiky 2. Další nevýhodou je nepředvídatelná a nedefinovaná hladina koagulačních faktorů. Obsah faktoru IX je nízký a hemostáza tudíž inkompletní.
Koncentrát protrombinového komplexu je aplikován v dávce 25–50 j/kg v kombinaci s kanavitem 5–10 mg intravenózně.
Výhoda je podávání malých, přesně definovaných objemů s rychlým nástupem účinku a je v současných doporučeních upřednostněno [1,3,4,10,11].
Zkušenost s rekombinantním faktoremVIIa (NovoSeven) je zatím omezená [28,29]. Sami zkušenost s NovoSeven nemáme. Steinová et al na souboru 68 pacientů prokazují jak lepší terapeutický efekt, tak ekonomickou výhodnost podání FVIIa ve srovnání s mraženou plazmou [30]. Ekonomické závěry jsou z důvodů jiných vstupních podmínek v místě vzniku pochopitelně nepřenosné do našeho prostředí. Podávání potentních preparátů, jakými jsou rFVIIa a koncentrát protrombinového komplexu, je spojeno s rizikem trombogenicity [31]. V případě vyššího rizika trombózy je proto podání doplněno aplikací nízkomolekulárního heparinu. Standardním operačním postupem je při intrakraniálních hematomech u warfarinizovaných pacientů evakuace hematomu z kraniotomie. U akutních subdurálních hematomů bez přítomnosti kontuze nebo u akutního zakrvácení do chronického subdurálního hematomu je alternativou evakuace z trepanopunkce. To platí zejména při akutní deterioraci stavu vědomí. Paralelní substituce je samozřejmostí.
Naše doporučení pro pacienty na antikoagulační terapii s prokázaným intrakraniálním hematomem spontánním nebo úrazovým:
- Spontánní i úrazové hematomy na CT (byť minimální velikosti) jsou indikací pro substituci koncentrátem protrombinového komplexu v dávce 25–50 jednotek/kg společně s kanavitem v dávce 5–10mg intravenózně (výše dávky se řídí iniciálním INR).
- Pacienti s prokázaným intrakraniálním hematomem jsou indikování k překladu do centra s 24hodinovou dostupností okamžité neurochirurgické operace. Je‑li pacient v jiné nemocnici, pak je koncentrát podán před transportem do centra. Překlad je při pozitivním nálezu na CT uskutečněn vždy (i kdyby iniciální GCS bylo 15 bodů).
- Neurochirurgická intervence navazuje, pokud se hematom chová expanzivně za kontroly parametrů koagulace. Standardním výkonem je evakuace hematomu z kraniotomie. Při akutní deterioraci vědomí je u subdurálního hematomu alternativou evakuace z trepanopunkce.
- V případě rozsáhlého krvácení u pacientů v hlubokém kómatu postupujeme s přihlédnutím k dalším faktorům (věk) individuálně. Kontraindikace substituce a operačního zákroku musí být jasně zdůvodněna.
Závěr
Intrakraniální hematomy traumatické i spontánního původu u warfarinizovaných pacientů představují život ohrožující situaci. S ohledem na věkovou skladbu antikoagulovaných pacientů postihují obvykle starší pacienty. Prognóza bývá zlá. Časná úprava hemokoagulačních parametrů koncentrátem protrombinového komplexu umožní stabilizaci hematomu a v případě potřeby neodkladnou chirurgickou intervenci. To je předpokladem zlepšení výsledků léčby intrakraniálních hematomů u antikoagulovaných pacientů.
MUDr. V. Přibáň, Ph.D.
Neurochirurgické oddělení
Nemocnice České Budějovice, a.s.
B. Němcové 54
370 87 České Budějovice
e-mail: v.priban@centrum.czPřijato k recenzi: 1. 7. 2009
Přijato do tisku: 24. 8. 2009
Sources
1. Hirsh J, Fuster V, Ansell J, Halperin JL. American Heart Association/ American College of Cardiology Foundation Guide to Warfarin Therapy. Circulation 2003; 107(12): 1692 – 1711.
2. Schulman S, Beyth RJ, Kearon C, Levine MN. Hemorrhagic Complications of Anticoagulant and Thrombolytic Treatment. American College of Chest Physicians Evidence - Based Clinical Practice Guidelines (8th Edition). Chest 2008; 133 (Suppl 6): 257S – 298S.
3. Baglin TP, Keeling DM, Watson HG. Guidelines on oral anticoagulation (warfarin): third edition – 2005 update. Br J Haematol 2006; 132(3): 277 – 285.
4. Gumulec J, Kessler P, Penka M, Klodová D, Králová S,Brejcha M et al. Z. Krvácivé komplikace při léčbě warfarinem 2005 [online]. Dostupné z: http:/ / www.thrombosis.cz/ sources/ Guidelines_warfarin_krvaceni_STH_XI05.pdf.
5. Wintzen AR, de Jonge H, Loeliger EA, Bots GT. The risk of intracerebral hemorrhage during oral anticoagulant treatment: a population study. Ann Neurol 1984; 16(5): 553 – 558.
6. Mina AA, Bair HA, Howells GA, Bendick PJ. Complications of preinjury warfarin use in the trauma patient. J Trauma 2003; 54(5): 842 – 847.
7. Karni A, Holtzman R, Bass T, Zorman G, Carter L, Rodriquez L. Traumatic head injury in the anticoagulated elderly patient: a lethal combination. Am Surg 2001; 67(11): 1098 – 1100.
8. Grandhi R, Duane TM, Dechert T, Malhotra AK, Aboutanos MB, Wolffe LG et al. Anticoagulation and the elderly head trauma patient. Am Surg 2008; 74(9): 802 – 805.
9. Fang MC, Go AS, Chang Y, Hylek EM, Henault LE, Jensvold NE et al. Death and disability from warfarin‑associated intracranial and extracranial hemorrhages. Am J Med 2007; 120(8): 700 – 705.
10. Broderick J, Connolly S, Feldmann E, Hanley D, Kase C, Krieger D et al. Guidelines for the management of spontaneous intracerebral hemorrhage in adults: 2007 update. a guideline from the American Heart Association/ American Stroke Association Stroke Council, High Blood Pressure Research Council, and the Quality of Care and Outcomes in Research Interdisciplinary Working Group. Stroke 2007; 38(6): 2001 – 2023.
11. Baker RI, Coughlin PB, Gallus AS, Harper PL, Salem HH, Wood EM. Warfarin Reversal Consensus Group. Warfarin reversal: consensus guidelines, on behalf of the Australasian Society of Thrombosis and Haemostasis. Med J Aust 2004; 181(9): 492 – 497.
12. Kalina M, Tinkoff G, Gbadebo A, Veneri P, Fulda G.A protocol for the rapid normalization of INR in trauma patients with intracranial hemorrhage on prescribed warfarin therapy. Am Surg 2008; 74(9): 858 – 861.
13. Ivascu FA, Howells GA, Junn FS, Bair HA, Bendick PJ, Janczyk RJ. Rapid warfarin reversal in anticoagulated patients with traumatic intracranial hemorrhage reduces hemorrhage progression and mortality. J Trauma 2005; 59(5): 1131 – 1139.
14.Yasaka M, Minematsu K, Naritomi H, Sakata T, Yamaguchi T. Predisposing factors for enlargement of intracerebral hemorrhage in patients treated with warfarin. Thromb Haemost 2003; 89(2): 278 – 283.
15. Aithal GP, Day CP, Kesteven PJ, Daly AK. Association of polymorphisms in the cytochrome P450 CYP2C9 with warfarin dose requirement and risk of bleeding complications. Lancet 1999; 353(9154): 717 – 719.
16. Hylek EM, Singer DE. Risk factors for intracranial hemorrhage in outpatients taking warfarin. Ann Intern Med 1994; 120(11): 897 – 902.
17. Pieracci FM, Eachempati SR, Shou J, Hydo LJ, Barie PS. Degree of anticoagulation, but not warfarin use itself, predicts adverse outcomes after traumatic brain injury in elderly trauma patients. J Trauma 2007; 63(3): 525 – 530.
18. Go AS, Hylek EM, Phillips KA, Chang Y, Henault LE, Selby JV et al. Prevalence of diagnosed atrial fibrillation in adults: National implications for rhythm management and stroke prevention: The AnTicoagulation and Risk Factors in Atrial Fibrillation (ATRIA) Study. JAMA 2001; 285(18): 2370 – 235.
19. Secondary prevention in non‑rheumatic atrial fibrillation after transitransient ischaemic attack or minor stroke. EAFT (European Atrial Fibrillation Trial) Study Group. Lancet 1993; 342(8882): 1255 – 1262.
20. Hart RG, Benavente O, McBride R, Pearce LA. Antithrombotic therapy to prevent stroke in patients with atrial fibrillation: A meta‑analysis. Ann Intern Med 1999; 131(7): 492 – 501.
21. van Walraven C, Hart RG, Singer DE, Laupacis A, Connolly S, Petersen P et al. Oral anticoagulants vs aspirin in nonvalvular atrial fibrillation: an individual patient meta‑analysis. JAMA 2002; 288(19): 2441 – 2448.
22. Steiner T, Rosand J, Diringer M. Intracerebral hemorrhage associated with oral anticoagulant therapy: current practices and unresolved questions. Stroke 2006; 37(1): 256 – 262.
23. Flibotte JJ, Hagan N, O’Donnell J, Greenberg SM, Rosand J. Warfarin, hematoma expansion and outcome of intracerebral hemorrhage. Neurology 2004; 63(6): 1059 – 1064.
24. Lavoie A, Ratte S, Clas D, Demers J, Moore L, Martin M et al. Preinjury warfarin use among elderly patients with closed head injuries in a trauma center. J Trauma 2004; 56(4): 802 – 807.
25. Franko J, Kish KJ, O’Connell BG, Subramanian S, Yuschak JV. Advanced age and preinjury warfarin anticoagulation increase the risk of mortality after head trauma. J Trauma 2006; 61(1): 107 – 110.
26. Makris M, Greaves M, Phillips WS, Kitchen S, Rosendaal FR, Preston EF. Emergency oral anticoagulation reversal: The relative efficacy of infusions of fresh frozen plasma and clotting factor concentrate on correction of the coagulopathy. Thromb Haemost 1997; 77(3): 477 – 480.
27. Boulis N, Bobek M, Schmaier A, Hoff JT. Use of factor IX complex in warfarin related intracranial hemorrhage. Neurosurgery 1999; 45(5): 1113 – 1119.
28. Lin J, Hanigan WC, Tarantino M, Wang J. The use of recombinant activated factor VII to reverse warfarin‑induced anticoagulation in patients with hemorrhages in the central nervous system: preliminary findings. J Neurosurg 2003; 98(4): 737 – 740.
29. Brody DL, Aiyagari V, Shackleford AM, Diringer MN. Use of recombinant factor VIIa in patients with warfarin‑associated intracranial hemorrhage. Neurocrit Care 2005; 2(3): 263 – 267.
30. Stein DM, Dutton RP, Kramer ME, Scalea TM. Reversal of coagulopathy in critically ill patients with traumatic brain injury: recombinant factor VIIa is more cost‑effective than plasma. J Trauma 2009; 66(1): 63 – 75.
31. Lankiewicz MW, Hays J, Friedman KD, Tinkoff G, Blatt PM. Urgent reversal of warfarin with prothrombin complex concentrate. J Thromb Haemost 2006; 4(5): 967 – 970.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2009 Issue 6-
All articles in this issue
- Korelace transkraniální barevné duplexní sonografie, CT angiografie a digitální subtrakční angiografie u pacientů s aterosklerotickým postižením mozkových tepen v běžné klinické praxi
- Neuropatie nervus mentalis jako manifestace systémové malignity
- Syndróm karpálneho tunela
- Mikrodialýza v neurochirurgii
- Varianty katatonie
- Rettův syndrom
- Resekce gliomů inzuly – volumetrické hodnocení radikality
- Intrakraniální hematomy u warfarinizovaných pacientů – kazuistiky a doporučení léčby
- Mezinárodní klasifikace funkčních schopností, disability a zdraví (ICF) – kvantitativní měření kapacity a výkonu
- Je clinical‑ diffusion mismatch sdružen s dobrým klinickým výsledkem u pacientů s akutním ischemickým iktem léčených intravenózní trombolýzou?
- Vliv léčby botulinum toxinem‑ A a redresního sádrování na délku musculus triceps surae a ekvinózní postavení nohy během chůze u pacientů s dětskou mozkovou obrnou
- Extrakraniální schwannom nervi hypoglossi – kazuistika
- Recidivující ischemická mozková příhoda při systémové skleróze – kazuistika
- Kavernózní malformace kaudy equiny – kazuistika
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Varianty katatonie
- Rettův syndrom
- Neuropatie nervus mentalis jako manifestace systémové malignity
- Syndróm karpálneho tunela
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

