-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaDiagnostika a terapie těžké akutní pankreatitidy v intenzivní medicíně
Autoři: Dr. med. Wirtz H. Theresa 1; Dr. med. Puengel Tobias 2; Dr. med. Buendgens Lukas 3; prof. Dr. med. Dde Lu Tom; Mhba 4; prof. Dr. med. Trautwein Christian 5; prof. Dr. med. Koch Alexander; Mhba 6
Působiště autorů: Assistenzärztin der Medizinischen Klinik III der Uniklinik, Aachen 1; Assistenzarzt der Medizinischen Klinik III der Uniklinik, Aachen 2; Facharzt für Innere Medizin und Funktionsoberarzt der, Medizinischen Klinik III des Universitätsklinikums Aachen, mit den Schwerpunkten Endoskopie und Intensivmedizin 3; Oberarzt der Medizinischen Klinik III der Uniklinik Aachen 4; Direktor der Medizinischen Klinik III der Uniklinik Aachen 5; Leiter des Bereichs Intensivmedizin, Leiter des, Ernährungsteams und stellvertretender Direktor der, Medizinischen Klinik III der Uniklinik Aachen 6
Vyšlo v časopise: Svět praktické medicíny, 1, 2020, č. 3-4, s. 22-28
Kategorie: Medicína ve světě: překladový článek s komentáři
Souhrn
Akutní pankreatitida patří mezi potenciálně život ohrožující onemocnění, a to především její těžké formy vyžadující léčbu na jednotce intenzivní péče. V tomto článku jsou uvedeny jak možnosti racionální diagnostiky, tak přehled terapie v závislosti na stadiu pankreatitidy. Možnosti léčby zahrnují konzervativní opatření, ale také intervenční interdisciplinární řešení.
Hlavní příčiny akutní pankreatitidy jsou uvedeny v článku s ohledem na svou diagnostiku. Cholelitiáza (asi 35 %) a alkohol (30–35 %) tvoří dohromady asi dvě třetiny případů. Asi v 15 % hovoříme o idiopatické příčině. Další klinicky významnou jednotkou je post-ERCP pankreatitida (5 %).
Hlavní příčiny pankreatitidy s odpovídající diagnostickou metodou jsou uvedeny přehledně v tabulce 1.
Tab. 1. Přehled hlavních příčin pankreatitidy s odpovídající diagnostikou 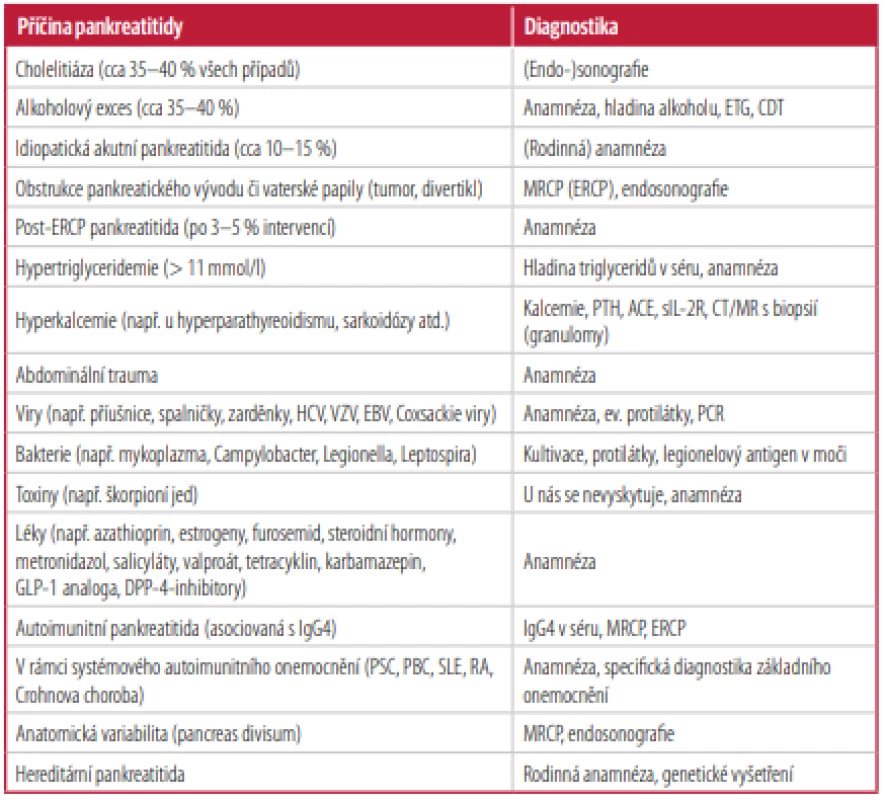
ACE – angiotenzin konvertující enzym, CDT – karbohydrát deficientní transferin, DPP-4 – dipeptidylpetidáza 4, EBV– virus Epsteina-Baarové, ERC P– endoskopická retrográdní cholangiopankreatikografie, ETG – ethylglukuronid, GLP-1 – glukagon-like peptid 1, HCV – virus hepatitidy C, IgG4 – imunoglobulin G4, MR – magnetická rezonance, MRCP – magnetická cholangiopankreatikografie, PBC – primární biliární cholangoitida, PCR – polymerase chain reaction (polymerázová řetězová reakce), PSC – primární sklerotizující cholangoitida, PTH – parathormon, RA – revmatoidní artritida, sIL-2R – solubilní interleukinový receptor 2, SLE – systémový lupus erythematodes, VZV – varicella zoster virus Poznámka
Hlavními příčinami akutní pankreatitidy jsou alkohol a cholelitiáza.
K počátečnímu hodnocení stavu pacienta by měly patřit: anamnéza, fyzikální vyšetření, odběry krve (lipáza, triglyceridy, kalcemie, jaterní testy) a také sonografické vyšetření břicha, ev. i opakovaně k bezpečnému vyloučení přítomnosti žlučových kamenů. U první epizody akutní pankreatitidy mladých pacientů (< 35 let) nebo u pacientů, kteří mají pozitivní rodinnou zátěž, můžeme po vyloučení jiných příčin pankreatitidy indikovat genetické vyšetření.1, 2
Nezávisle na příčině vzniku akutní pankreatitidy je patofyziologickým podkladem tohoto onemocnění nekontrolovatelná aktivace pankreatických enzymů, které způsobí autodestrukci slinivky a okolní tkáně. Charakteristicky dochází ke vzniku systémové zánětlivé odpovědi (SIRS) (Tab. 3) s narušením mikrocirkulace, které se může manifestovat jako multiorgánové selhání (MODS).
Tab. 2. Stanovení tíže akutní pankreatitidy [Atlanta, 2012] ![Stanovení tíže akutní pankreatitidy [Atlanta, 2012]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/44950d97ffc6cc13042ed353cdc6ef86.png)
Tab. 3. Klinická kritéria těžké akutní pankreatitidy (upravena podle doporučení American College of Gastroenterology, ACG) 
paCO2 – parciální tlak oxidu uhličitého; SIRS – systémová zánětlivá odpověď organismu Epidemiologie
Incidence akutní pankreatitidy je přibližně 5–35 nově vzniklých případů na 100 000 obyvatel za rok. V posledních letech mají tato čísla vzestupnou tendenci.3 Asi u 15–25 % pacientů s akutní pankreatitidou se rozvine těžká forma této nemoci. Ve velké americké retrospektivní studii se snížila letalita na tuto diagnózu mezi lety 1998 a 2003 z 12 % na 2 %, avšak u pacientů s těžkou formou akutní pankreatitidy tato čísla zůstávala stále vysoká.4 I z tohoto důvodu je při stanovení diagnózy velmi důležité klasifikovat závažnost onemocnění a identifikovat včas pacienty se zvýšeným rizikem komplikací a mortality.
Diagnostika
Klinická diagnóza
K diagnostice akutní pankreatitidy můžeme využít Atlantskou klasifikaci z roku 2012 (viz přehled dále).5
K dalším klinickým symptomům patří nauzea, zvracení a u těžké formy také známky systémové reakce organismu jako tachykardie, tachypnoe, horečka a hypotenze.6, 7
Laboratorní vyšetření
Při laboratorním vyšetření se jako diagnostické kritérium používá zvýšení lipázy v séru nad trojnásobek horní hranice normální hodnoty. Úvodní hodnota sérové lipázy ani dynamika jejích hodnot však nevypovídají nic o závažnosti průběhu nemoci ani prognóze pacienta. Proto není opakované sledování hodnot sérové lipázy smysluplné.
C-reaktivní protein (CRP), jako marker zánětu a imunitní odpovědi, může upozornit na rozvoj pankreatických nekróz.
Zobrazovací metody
Sonografie
Výhodou sonografického vyšetření je jeho běžná dostupnost. Slinivka se na něm v mnoha případech může jevit difuzně zvětšená a hypoechogenní. Často je vidět peripankreatický edém a eventuálně už i pankreatické nekrózy. Sonografie břicha nám pomůže v rámci diferenciální diagnostiky vyloučit cholecystitidu a nefrolitiázu. Může také identifikovat cholelitiázu jako příčinu akutní pankreatitidy. U přibližně jedné třetiny pacientů je hodnocení stavu pankreatu sonograficky obtížné kvůli jeho překrytí plynem způsobeným paralytickým subileem při probíhajícím zánětu v dutině břišní.8
Poznámka
Sonografické vyšetření břicha je standardně používáno jako první volba na počátku diagnostiky akutní pankreatitidy
Endosonografie (EUS)
EUS je díky skvělému prostorovému zobrazení okolí pankreatu zlatým standardem pro zjištění obstrukce žlučových cest.
Endoskopická retrográdní cholangiopankreatografie (ERCP)
ERCP by mělo být u pacientů s biliární pankreatitidou a zároveň probíhající cholangoitidou provedeno do 24 hodin jako sanace fokusu infektu.
Aktuálně nejsou dostupná spolehlivá data k určení vhodné doby k provedení ERCP u akutní biliární pankreatitidy bez cholangoitidy. ERCP s papilotomií a extrakcí kamenu by mělo být provedeno nejlépe současně s endosonografickým vyšetřením po stabilizaci pacienta na JIP.9
Poznámka
Při cholangoitidě by mělo být ERCP provedeno do 24 hodin.
CT vyšetření
CT na rozdíl od sonografie umožňuje rozlišení mezi edematózní a nekrotizující pankreatitidou a zhodnocení rizika. Přesto by CT nemělo být prováděno rutinně v rámci prvotní diagnostiky onemocnění, jelikož se nám nekrózy a kolekce tekutiny spolehlivě zobrazí až za 48–72 hodin po zahájení volumové substituce.9 Včasné provedení CT vyšetření je však indikováno v rámci diferenciální diagnostiky, kdy pomůže vyloučit např. absces, mezenteriální ischemii či perforaci dutých orgánů.
MR vyšetření
Při kontraindikaci vyšetření CT s kontrastní látkou můžeme zvolit jako alternativu vyšetření MR, především pokud potřebujeme vyšetřit průběh pankreatických cest.
Klasifikace a stratifikace rizika průběhu akutní pankreatitidy
Morfologicky lze podle Atlantských kritérií rozdělit akutní pankreatitidu na formu intersticiálně edematózní (80–85 % všech případů) a nekrotizující.5 První z výše uvedených forem se vyznačuje zánětem pankreatu a peripankreatické tkáně, nekrózy však neprokazujeme. Ty jsou známkami akutní nekrotizující pankreatitidy.
Další morfologické charakteristiky s důrazem na terapeutickou závažnost poskytují soubory akutní peripankreatické tekutiny (acute peripancreatic fluid collection – AFPC) a akutní nekrotické kolekce (acute necrotic collection – ANC), pro které je charakteristické, že oblasti tekutiny nebo nekrózy nejsou zapouzdřeny. ANC je typická pro akutní nekrotizující pankreatitidu a může postihnout jak tkáň pankreatu, tak i extrapankreatickou tkáň.5 Kromě toho se mohou vytvořit i útvary tekutiny či nekrózy s jasně vytvořenou stěnou, tedy pseudocysty, ohraničené nekrózy s jasně definovanou stěnou (walled-off necrosis – WON). Je pravidlem, že nekrózy s jasně prokazatelnou stěnou vznikají nejdříve po 4 týdnech od začátku bolestí břicha.
Na základě revidované Atlantské klasifikace můžeme pankreatitidu podle závažnosti jejího průběhu rozdělit na lehkou, středně těžkou a těžkou (Tab. 2). 5
Poznámka
Pomocí Atlantské klasifikace dělíme akutní pankreatitidu podle morfologie (edematózní/nekrotická) a podle klinické závažnosti (Tab. 2).
K hodnocení závažnosti akutní pankreatitidy nám mohou pomoci také laboratorní ukazatele jako CRP, urea nebo hematokrit.11 Nízký či normální hematokrit svědčí pro mírnou formu, vysoká hladina urey (> 14,3 mmol/l) je asociována s vyšší úmrtností.12, 13 Zvýšená hladina glukózy (> 11 mmol/l) může značit poškození endokrinní části pankreatu.
Možnosti léčby
Po stanovení diagnózy akutní pankreatitidy musíme ihned zvážit, zda není pacient indikován k hospitalizaci na jednotce intenzivní péče. K tomu nám mohou pomoci skórovací systémy jako Acute Physiology and Chronic Health Evaluation Score (APACHE II, např. terapie na jednotce intenzivní péče je indikována se skóre APACHE II > 8) nebo Sequential Organ Failure Assessment (SOFA).
Postupy International Association of Pancreatology (IAP) a American Pancreatic Association (APA) z roku 2013 doporučují hospitalizovat na jednotce intenzivní péče každého pacienta s těžkou formou akutní pankreatitidy podle Atlantské klasifikace.
American College of Gastroenterology (ACG) uveřejnila soubor klinických znaků, které bývají asociovány s průběhem těžké pankreatitidy (Tab. 3). 4
Poznámka
Pacienti s těžkou formou akutní pankreatitidy (podle Atlantské klasifikace) by měli být hospitalizováni na jednotce intenzivní péče.
Při ošetřování pacienta s těžkou akutní pankreatitidou musíme vzít v úvahu, zda se jedná o iniciální, či pozdní fázi onemocnění. Na počátku onemocnění musíme dbát hlavně na stabilizaci krevního oběhu, podporu orgánových funkcí a terapii bolesti (Obr. 1). V pozdější fázi je důležité dbát na léčbu infekcí a ošetření nekróz.
Obr. 1. Důležité body při ošetřování pacienta v iniciální fázi těžké akutní pankreatitidy. Důraz je kladen na objemovou resuscitaci, analgezii a brzkou enterální výživu. 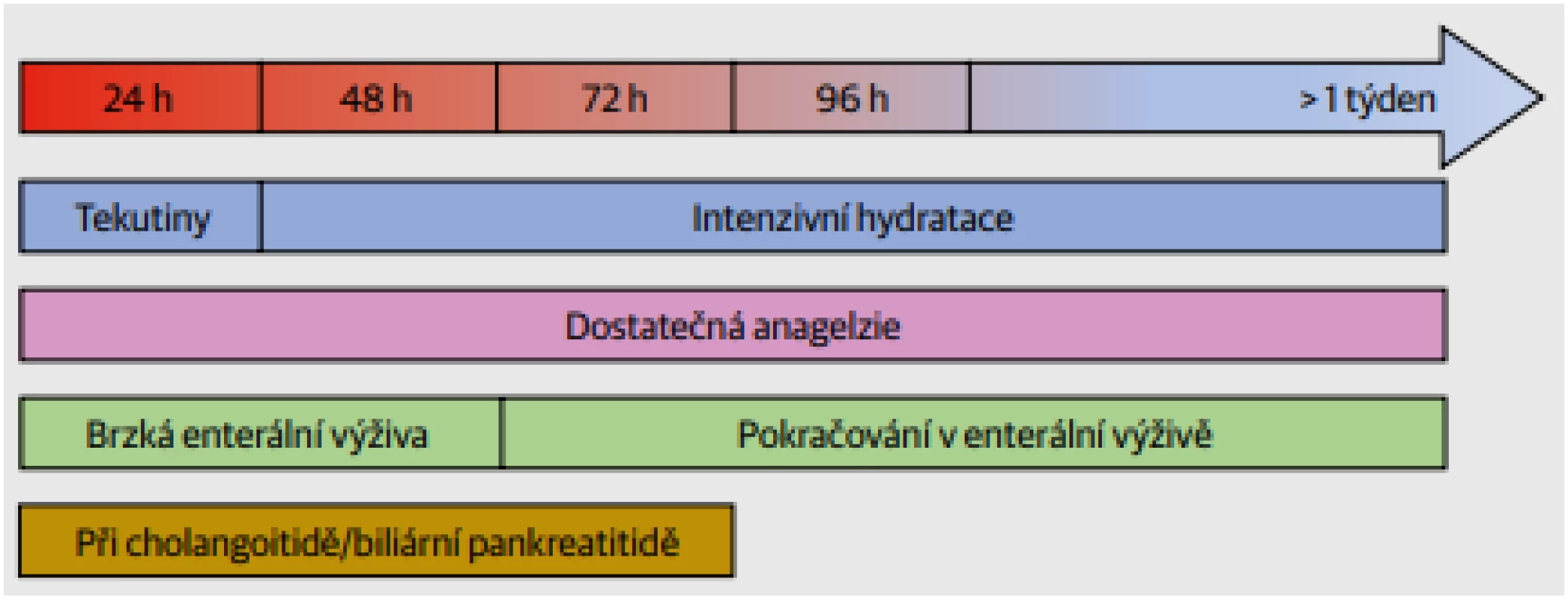
Iniciální fáze onemocnění
Volumová terapie
Pacienti s akutní pankreatitidou trpí nedostatkem intravazální tekutiny, který je způsoben zvýšenou propustností cév („kapilární leak“) v rámci systémové zánětlivé reakce organismu (SIRS). Z důvodu přerozdělení tekutin v organismu mohou vznikat pleurální výpotky, ascites, edémy až anasarka.
S ohledem na přidružené komorbidity pacienta (srdeční selhání, renální insuficience) by měla být na počátku onemocnění, tj. 12–24 hodin od vzniku příznaků, zahájena intenzivní hydratace roztoky krystaloidů (5–10 ml/kg tělesné hmotnosti/h).15 Tímto opatřením můžeme dosáhnout snížení letality a morbidity. Pokud je již na počátku léčby u pacienta přítomna tachykardie a hypotenze, lze pro rychlé doplnění objemu tekutin začít během prvních 30 minut tzv. tekutinovou výzvou 20–30 ml/kg. Avšak objemové přetížení může vést k vyššímu riziku vzniku dechové tísně s nutností invazivní dechové podpory při ARDS (acute respiratory distress syndrom) a také břišního kompartment syndromu.16
Poznámka
Včasné a agresivní doplnění tekutin může pacientovu prognózu zlepšit, ale nesmíme ho tekutinami přetížit.
V současné době probíhá několik studií, které se věnují volumové terapii u akutní pankreatitidy. Řeší se v nich otázky nastavení cílových hodnot – tepová frekvence > 120/min, střední arteriální tlak (MAP) > 65 mmHg a množství vyloučené moči > 0,5–1 ml/kg tělesné hmotnosti/h. Můžeme využít i invazivně měřené veličiny k monitoraci hemodynamické stability nebo biochemické markery (hematokrit < 44 %, laktát < 2 mmol/l, urea < 14,3 mmol/l). Předpovědět letalitu může především změna hodnoty BUN (dusíku v močovině v krvi) po rehydrataci během prvních 24 hodin.17
Analgezie
Bolesti epigastria pásovitého charakteru bývají hlavním symptomem akutní pankreatitidy. Nedostatečná analgezie vede k povrchovému dýchání, které může vyústit v rozvoj (nozokomiální) pneumonie. První volbou jsou opiáty (hydromorfon, fentanyl a další).18 Pokud bolesti přetrvávají, může být zaveden epidurální katétr. Epidurální analgezie může, díky účinné kontrole bolesti, zlepšit mikrocirkulaci v pankreatu a tím oxygenaci tkáně, což má pozitivní vliv na celkový průběh onemocnění.19
Poznámka
U terapie bolesti při akutní pankreatitidě je smysluplné zavedení epidurálního katétru.
Výživa
Dřívější, dnes již zastaralé postupy doporučovaly nihil per os, dnes se však ví, že na stav pacienta má příznivý vliv co nejčasnější zavedení enterální výživy. Pacienti s lehkou formou pankreatitidy mohou velmi brzy obnovit plný perorální příjem stravy. Při středně těžké pankreatitidě pacienti však často stravu odmítají z důvodu bolesti, nevolnosti a zvracení.
U pacientů s těžkou pankreatitidou brzké zahájení perorální výživy (do 48 hodin od přijetí do nemocnice) snižuje riziko infekce, poškození orgánů, délku léčby a letalitu.5, 20 Enterální výživu je nejvýhodnější podávat nazogastrickou sondou nebo při významném refluxu (> 400 ml/den) pomocí nazojejunální sondy. Příjem by se měl pohybovat kolem 24 kcal/kg tělesné hmotnosti, což odpovídá německým doporučením pro těžce nemocné pacienty.21 Parenterální výživa by měla být zahájena, pouze pokud nelze po 5 dnech enterální výživy zajistit dostatečný příjem kalorií.
Poznámka
U pacientů s těžkou formou akutní pankreatitidy by měla být co nejdříve zahájena enterální výživa (48 hodin po přijetí).
Kauzální léčba
V závislosti na příčině akutní pankreatitidy můžeme zvolit kauzální terapii. Biliární pankreatitida je po průkazu choledocholitiázy, cholangoitidy či cholestázy indikací k ERCP. Při lehké biliární pankreatitidě by pro riziko biliárních komplikací a recidivy pankreatitidy měla být provedena cholecystektomie, nejlépe při jednom pobytu v nemocnici.22 Pokud jsou u pacienta přítomny tekutinové kolekce a nekrózy, měla by být cholecystektomie odložena.9
Pokud se jedná o hypertriglyceridemií (> 11 mmol/l) indukovanou pankreatitidu, lze využít plazmaferézu či lipidaferézu.
Terapie infekce
Asi u 20 % všech pacientů s akutní pankreatitidou dochází k rozvoji extrapankreatických infekčních komplikací, jako je pneumonie, septikemie či cholangoitidy, které zvyšují celkovou letalitu pacientů. Je však těžké od sebe rozlišit sterilní SIRS a extrapankreatickou infekci. V zásadě platí, že při zhoršení klinického stavu ve smyslu zvýšení teploty, při stoupajících zánětlivých parametrech je důležité hledat fokus možné infekce. Odebrat hemokultury, sekret z drénů, kultivaci moči a provést zobrazovací vyšetření. Jedině tak odhalíme extrapankreatickou infekci a můžeme indikovat cílenou antibiotickou terapii.
Aktuální mezinárodní doporučené postupy nedoporučují profylaktickou antibiotickou terapii akutní pankreatitidy s prokázanými nekrózami.14 Na přítomnost infikované nekrózy pankreatu by se mělo myslet v případě, že u pacienta s akutní nekrotickou pankreatitidou dojde ke zhoršení klinického stavu (poškození orgánových funkcí, vzestup zánětlivých parametrů). Měla by být provedena CT diagnostika a zavedení drénu k zajištění fokusu. Antibiotická terapie infikovaných nekróz pankreatu by se měla skládat z antibiotik dobře pronikajících do tkání, např. karbapenemů, fluorochinolonů či metronidazolu.
Obr. 2. a) CT vyšetření u těžké akutní pankreatitidy zaměřené na okrsky nekróz; b) chirurgicky provedená laparostomická dekomprese (bílá šipka ukazuje na vloženou síťku, modré šipky ukazují na proplachovací drény) 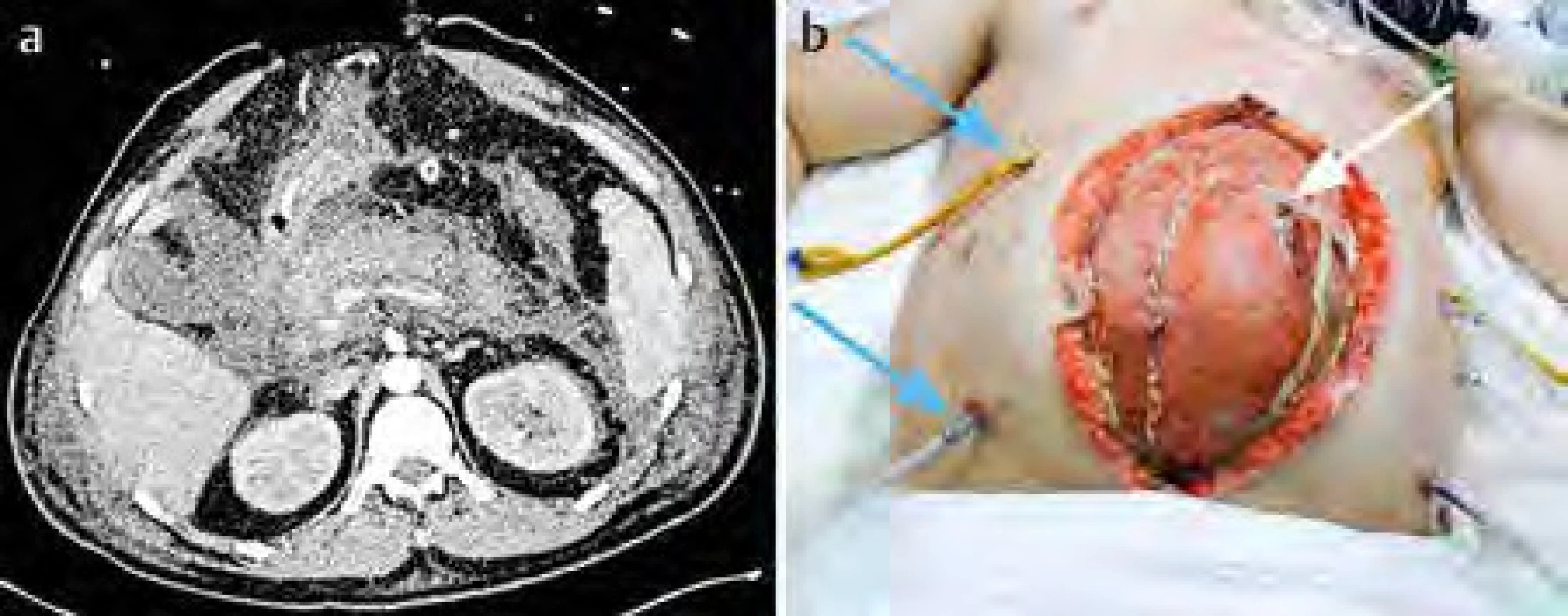
Poznámka
Karbapenemy jsou antibiotika první volby v empirické terapii infikovaných nekróz.
Pozdější fáze onemocnění – léčba komplikací
Typicky se pozdější fáze onemocnění sestává z léčby břišních komplikací, jako je infekce a ošetření nekróz (Obr. 3).
Obr. 3. Léčebný postup pozdější fáze akutní pankreatitidy. Typickými terapeutickými opatřeními jsou antibiotická terapie infikovaných pankreatických nekróz a extrapankreatických komplikací, terapie lokálních komplikací (drenáž pseudocyst) a po konsolidaci nekróz (WON – walled-off necrosis) definitivní nekrozektomie. 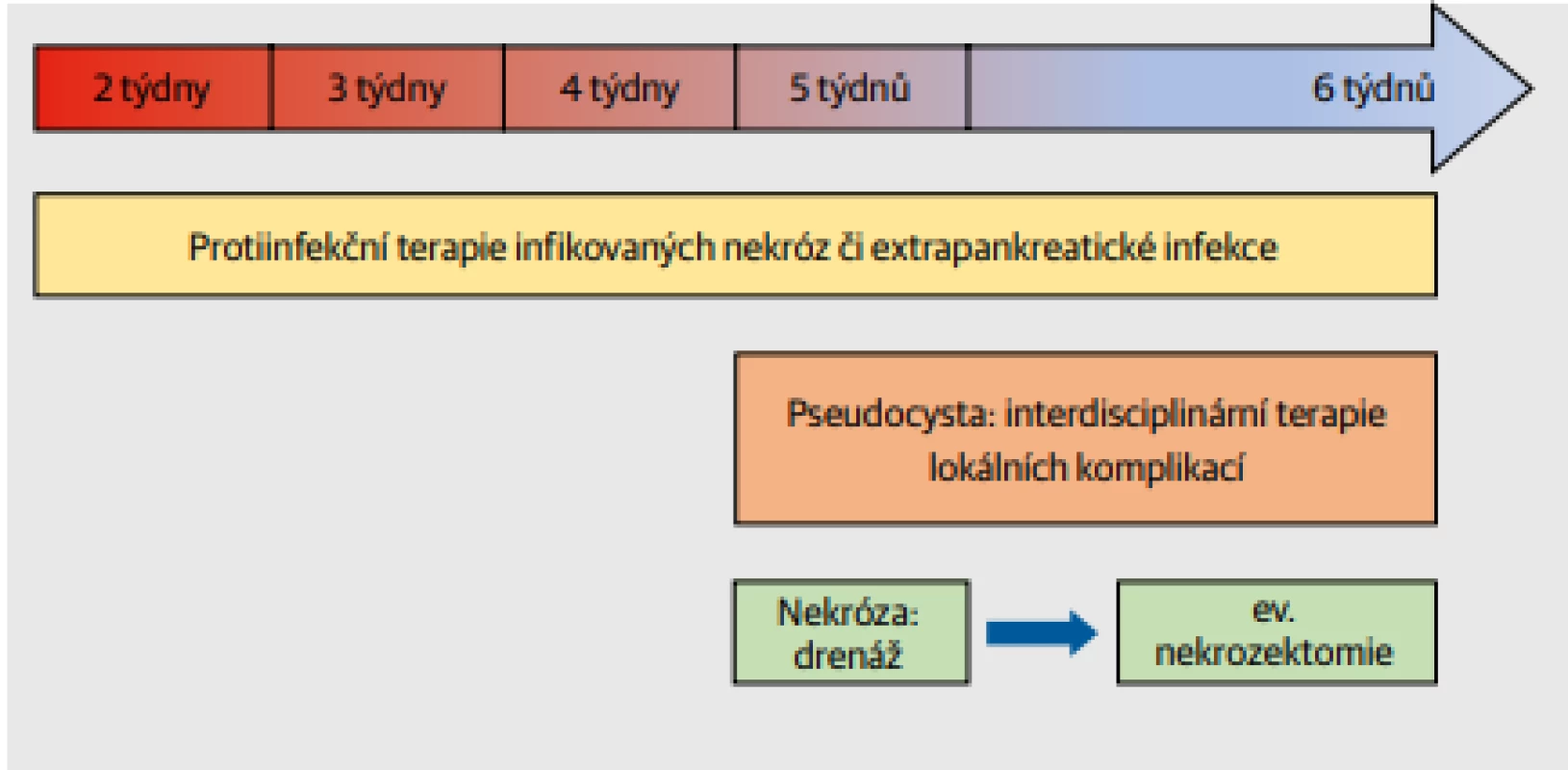
Pseudocysty a nekrózy
Těžká pankreatitida není charakterizována pouze orgánovým selháním a systémovou zánětlivou reakcí organismu. Problematická je zejména kvůli dlouhodobému průběhu lokálních komplikací, což pro pacienta znamená dlouhou hospitalizaci na lůžku. Zlatým standardem pro detekci pankreatických pseudocyst a ohraničených nekróz (WON) je CT vyšetření s kontrastní látkou.
Pankreatické pseudocysty mohou komprimovat naléhající struktury, např. duodenum. Typicky se tento stav projeví zvýšeným refluxem do nazogastrické sondy či recidivujícím zvracením. Pokud pseudocysty prorostou až k cévám, mohou způsobit významné krvácení vedoucí až k hemoragickému šoku. Další častou komplikací je bakteriální superinfekce pseudocyst, která se nejčastěji projevuje za 2 týdny od počátku onemocnění. V tomto případě je indikována (většinou) endosonografická punkce se zavedením drénu. Nekomplikovanou pankreatickou pseudocystu je nejlepší řešit konzervativním postupem, jelikož při její punkci hrozí sekundární infekce cysty.
Definitivní nekrozektomie by měla být provedena nejdříve za 4 týdny, kdy je již většinou jasně definována stěna útvaru. Pokud je zákrok proveden dříve, častěji nastávají komplikace ve smyslu krvácení či perforace.23 Proto by měla být prováděna pouze při progredující oběhové nestabilitě pacienta. Do doby, než se stěna definitivně vytvoří, je u infikované nekrózy indikována drenáž a terapie infekce. Sterilní nekrózy málokdy vyžadují intervenční řešení. Nejčastěji pouze v případě, kdy komprimují okolní orgány.
Terapeutické intervence by měly u pankreatitidy probíhat minimálně invazivním způsobem, tzv. step-up postupem.23
Nekrozektomie může být provedena endoskopicky či chirurgicky. Endoskopické řešení se sestává hlavně z endosonograficky provedené punkce se založením transgastrického nebo transduodenálního samoexpandibilního metalického stentu (SEMS). Nekrozektomii lze poté endoskopicky provádět opakovaně.
Poznámka
Definitivní nekrozektomie by měla být provedena až po vytvoření stěny.
Důležitou miniinvazivní chirurgickou metodou nekrozektomie je videoasistovaný retroperitoneální débridement (VARD).
Po zavedení perkutánního retroperitoneálního drénu (pod sonografickou či CT kontrolou) je podle step-up principu vytvořen intervenční kanál. Jím lze opakovaně provést endoskopickou či chirurgickou nekrozektomii. Postupy byly nedávno srovnány v multicentrické studii.24 Kromě zvýšeného výskytu pankreatických píštělí nebyly mezi oběma přístupy nalezeny rozdíly v morbiditě a letalitě. Vždy by mělo být o vhodném postupu rozhodováno individuálně.
Otevřená chirurgická terapie je s ohledem na vysokou morbiditu a letalitu (25–95 %) obsoletní.25
Břišní kompartment syndrom
Patofyziologickým podkladem břišního kompartment syndromu je zvýšení nitrobřišního tlaku v důsledku těžké zánětlivé reakce v dutině břišní, doprovázené ascitem, pleurálními výpotky a paralytickým ileem. Opatření pro pokles intraabdominálního tlaku jsou shrnuta v přehledu.
Obr. 4. a) Po provedení VARD (videoasistovaný retroperitoneální débridement) vznikla jako komplikace píštěl ocasu pankreatu (bílá šipka ukazuje na kanál VARD), modrá šipka ukazuje na odlehčovací drenáž píštěle ocasu pankreatu); b) zobrazení píštěle ocasu pankreatu pomocí endoskopické retrográdní cholangiopankreatikografie (ERCP) (bílá šipka ukazuje na únik kontrastní látky v okolí ocasu pankreatu) 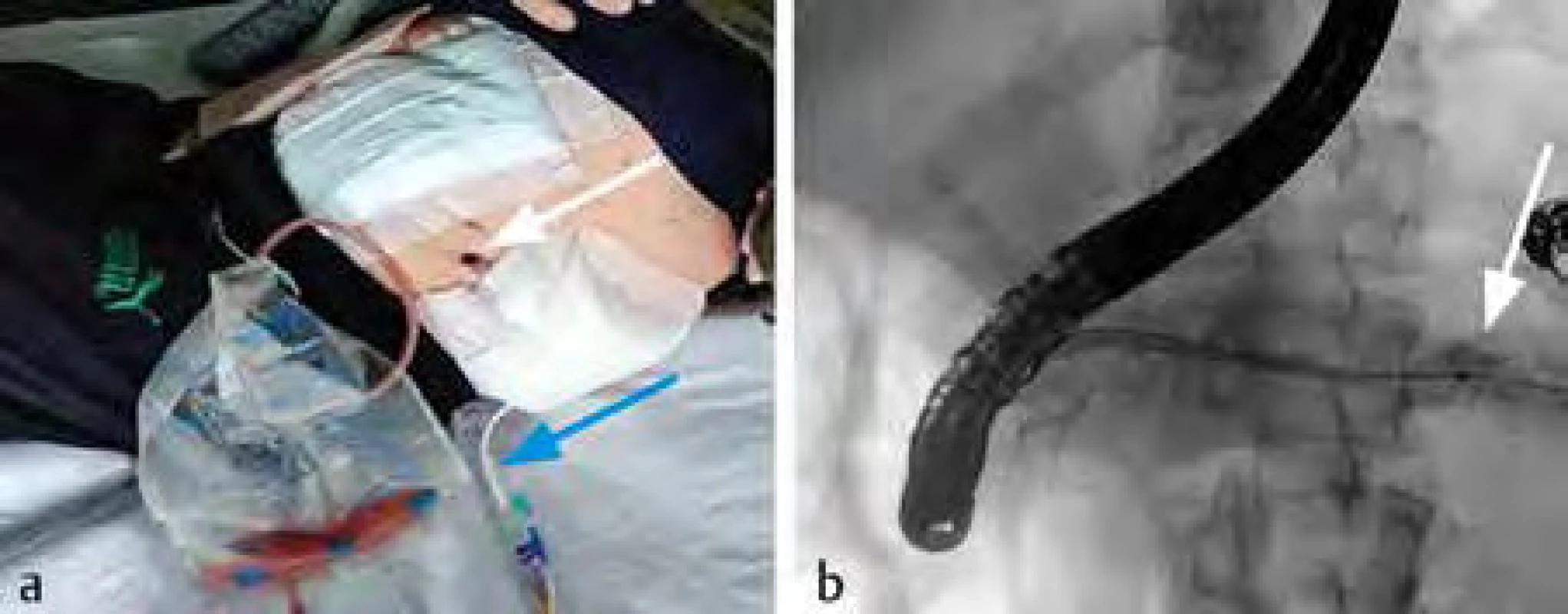
CAVE
Břišní kompartment syndrom patří mezi nejzávažnější komplikace těžké akutní pankreatitidy. Je definován vzestupem intraabdominálního tlaku nad 20 mmHg (měřeného v močovém měchýři), spolu s nově vzniklým orgánovým selháním.2
Klinicky lze zvýšení nitrobřišního tlaku sledovat pomocí měření tlaku v močovém měchýři a klinickým hodnocením (fyzikální vyšetření břicha, ventilační tlaky, potřeba katecholaminů).
Dlouhodobé komplikace
K následkům těžké akutní pankreatitidy patří exokrinní (20–30 % případů) a endokrinní poškození pankreatu s rozvojem pankreatoprivního diabetes mellitus. Chronická pankreatitida se vyvine asi v 10 % případů po alkoholem indukované akutní pankreatitidě.26
K zapamatování
- K diagnostickým kritériím akutní pankreatitidy patří zvýšení sérové lipázy (nad trojnásobek normy), typické klinické příznaky a charakteristické změny prokázané zobrazovacími metodami.
- Podle Atlantské klasifikace se akutní pankreatitida morfologicky dělí na intersticiálně-edematózní a nekrotickou.
- Klinické rozlišení mezi lehkou a těžkou akutní pankreatitidou závisí na lokálních a systémových komplikacích.
- Iniciální terapii zahajujeme intenzivní hydratací, brzy zahájíme enterální výživu a poskytneme pacientovi dostatečnou analgezii.
- U nekrotické pankreatitidy bychom měli využít step-up strategii: protiinfekční terapie (ale žádná profylaxe) – drenáž – nekrozektomie.
- Definitivní nekrozektomie může být provedena pomocí endoskopické drenáže anebo miniinvazivně díky VARD (videoasistovaný retroperitoneální débridement).
Článek v původním znění: doi: https://doi.org/10.1055/a-0949-0878 Dtsch Med Wochenschr 2020;145 : 850–862.
Překlad: MUDr. Tereza Tauerová © Georg Thieme Verlag KG, StuttgartNew York ISSN 0012-0472
Publikováno se souhlasem Thieme Gruppe. Chráněno autorským právem.
Dr. med. Theresa H. Wirtz
Assistenzärztin der Medizinischen Klinik III der Uniklinik Aachen
Dr. med. Tobias Puengel
Assistenzarzt der Medizinischen Klinik III der Uniklinik Aachen
Dr. med. Lukas Buendgens
Facharzt für Innere Medizin und Funktionsoberarzt der Medizinischen Klinik III des Universitätsklinikums Aachen mit den Schwerpunkten Endoskopie und Intensivmedizin
prof. Dr. med. Tom Lüdde, MHBA
Oberarzt der Medizinischen Klinik III der Uniklinik Aachen
prof. Dr. med. Christian Trautwein
Direktor der Medizinischen Klinik III der Uniklinik Aachen
prof. Dr. med. Alexander Koch, MHBA
Leiter des Bereichs Intensivmedizin, Leiter des Ernährungsteams und stellvertretender Direktor der Medizinischen Klinik III der Uniklinik Aachen
Za článkem následuje komentář
Zdroje
1. Rosendahl J, Landt O, Bernadova J, et al. CFTR, SPINK1, CTRC and PRSS1 variants in chronic pancreatitis: is the role of mutated CFTR overestimated? Gut 2013;62 : 582–592. doi: 10.1136/ gutjnl-2011-300645.
2. Howes N, Lerch MM, Greenhalf W, et al. Clinical and genetic characteristics of hereditary pancreatitis in Europe. Clin Gastroenterol Hepatol 2004;2 : 252–261. doi: 10.1016/ s1542-3565(04)00013-8.
3. Toouli J, Brooke-Smith M, Bassi C, et al. Guidelines for the management of acute pancreatitis. J Gastroenterol Hepatol 2002;17:S15–S39. doi: 10.1046/j.1440-1746.17.s1.2.x.
4. Fagenholz PJ, Castillo CF, Harris NS, et al. Increasing United States hospital admissions for acute pancreatitis, 1988–2003. Ann Epidemiol 2007;17 : 491–497. doi: 10.1016/j. annepidem.2007.02.002.
5. Banks PA, Bollen TL, Dervenis C, et al. Classification of acute pancreatitis–2012: revision of the Atlanta classification and definitions by international consensus. Gut 2013;62 : 102–111. doi: 10.1136/gutjnl-2012-302779.
6. Swaroop VS, Chari ST, Clain JE. Severe acute pancreatitis. JAMA 2004;291 : 2865–2868. doi: 10.1001/jama.291.23.2865.
7. Banks PA, Freeman ML. Practice Parameters Committee of the American College of Gastroenerology.Practice guidelines in acute pancreatitis. J Am Gastroenterol 2006;101 : 2379 – 2400. doi: 10.1111/j.1572–0241.2006.00856.x.
8. Dervenis C, Johnson CD, Bassi C, et al. Diagnosis, objective assessment of severity, and management of acute pancreatitis. Santorini consensus conference. Int J Pancreatol 1999;25 : 195–210. doi: 10.1007/bf02925968.
9. Working Group IAPAPAAPG. IAP/APA evidence-based guidelines for the management of acute pancreatitis. Pancreatology 2013;13:e1–e15. doi: 10.1016/j.pan.2013.07.063.
10. Arvanitakis M, Dumonceau JM, Albert J, et al. Endoscopic management of acute necrotizing pancreatitis: European Society of Gastrointestinal Endoscopy (ESGE) evidence-based multidisciplinary guidelines. Endoscopy 2018;50 : 524–546. doi: 10.1055/a-0588-5365.
11. Larvin M. Assessment of severity and prognosis in acute pancreatitis. Eur J Gastroenterol Hepatol 1997;9 : 122–130. doi: 10.1097/00042737-199702000-00004.
12. Brown A, Orav J, Banks PA. Hemoconcentration is an early marker for organ failure and necrotizing pancreatitis. Pancreas 2000;20 : 367–372.doi: 10.1097/00006676 -200005000-00005.
13. Wu BU, Bakker OJ, Papachristou GI, et al. Blood urea nitrogen in the early assessment of acute pancreatitis: an international validation study. Arch Intern Med 2011;171 : 669–676. doi: 10.1001/archinternmed.2011.126.
14. Tenner S, Baillie J, DeWitt J, et al. American College of Gastroenterology guideline: management of acute pancreatitis. J Am Gastroenterol 2013;108 : 400–1416. doi: 10.1038/ ajg.2013.218.
15. Haydock MD, Mittal A, Wilms HR, et al. Fluid therapy in acute pancreatitis: anybody’s guess. Ann Surg 2013;257 : 182–188. doi: 10.1097/SLA.0b013e31827773ff.
16. Mao EQ, Tang YQ, Fei J, et al. Fluid therapy for severe acute pancreatitis in acute response stage. Chin Med J 2009;122 : 169–173.
17. Wu BU, Johannes RS, Sun X, et al. Early changes in blood urea nitrogen predict mortality in acute pancreatitis. Gastroenterology 2009;137 : 129–135. doi: 10.1053/j.gastro. 2009.03.056.
18. Basurto Ona X, Rigau Comas D, Urrutia G. Opioids for acute pancreatitis pain. Cochrane Database Syst Rev 2013. doi: 10.1002/14651858.CD009179.pub2.
19. Task Force of the American College of Critical Care Medicine, Society of Critical Care Medicine. Guidelines for intensive care unit admission, discharge, and triage. Crit Care Med 1999;27 : 633–638.
20. Reintam Blaser A, Starkopf J, Alhazzani W, et al. Early enteral nutrition in critically ill patients: ESICM clinical practice guidelines. Intens Care Med 2017;43 : 380–398. doi: 10.1007/ s00134-016-4665-0.
21. Elke G, Hartl WH, Kreymann KG, et al. Clinical nutrition in critical care medicine – Guideline of the German Society for Nutritional Medicine (DGEM). Clin Nutrit ESPEN 2019;33 : 220 – 275. doi: 10.1016/j.clnesp.2019.05.002.
22. da Costa DW, Bouwense SA, Schepers NJ, et al. Same-admission versus interval cholecystectomy for mild gallstone pancreatitis (PONCHO): a multicentre randomised controlled trial. Lancet 2015;386 : 1261–1268. doi: 10.1016/S0140-6736(15)00274-3.
23. van Grinsven J, van Santvoort HC, Boermeester MA, et al. Timing of catheter drainage in infected necrotizing pancreatitis. Nat Rev Gastroenterol Hepatol 2016;13 : 306–312. doi: 10.1038/nrgastro.2016.23.
24. van Brunschot S, van Grinsven J, van Santvoort HC, et al. Endoscopic or surgical step-up approach for infected necrotising pancreatitis: a multicentre randomised trial. Lancet 2018;391 : 51–58. doi: 10.1016/S0140-6736(17)32404-2.
25. van Santvoort HC, Besselink MG, Bakker OJ, et al. A step-up approach or open necrosectomy for necrotizing pancreatitis. NEJM 2010;362 : 1491–1502. doi: 10.1056/ NEJMoa0908821.
26. Hollemans RA, Hallensleben NDL, Mager DJ, et al. Pancreatic exocrine insufficiency following acute pancreatitis: Systematic review and study level meta-analysis. Pancreatology 2018;18 : 253–262. doi: 10.1016/j.pan.2018.02.009.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Úvodní slovoČlánek Nový Etický kodex AIFP
Článek vyšel v časopiseSvět praktické medicíny
Nejčtenější tento týden
2020 Číslo 3-4- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Trazodon pohledem praktického lékaře
- Magnosolv a jeho využití v neurologii
-
Všechny články tohoto čísla
- Úvodní slovo
- Léčba depresí a dalších psychických nemocí nejen s ohledem na COVID-19
- Vši a svrab: Aktualizace léčby
- Komentář ke článku Vši a svrab: Aktualizace léčby
- Diagnostika a terapie těžké akutní pankreatitidy v intenzivní medicíně
- Komentář k článku Diagnostika a terapie těžké akutní pankreatitidy v intenzivní medicíně
- Možnosti antidiabetické léčby v roce 2020 – důvod ke skepsi, či optimismu?
- Bezpečnost antidiabetik v léčbě diabetu 2. typu
- Inhibitory SGLT2 v léčbě diabetu 2. typu GLIFLOZINY a jeho komplikací
- Hypoglykemie jako stále obávaná komplikace léčby diabetu a její prevence
- Profesor Miroslav Souček: Hypertenzi mám, jak jinak?
- Současná a perspektivní léčba obezity u diabetiků
- Nealkoholová tuková jaterní choroba a diabetes mellitus
- Testosteron u mužů s metabolickým syndromem, prediabetem a diabetem 2. typu Pozitivní účinky terapie testosteronem
- Nový Etický kodex AIFP
- Nemoci přenášené klíšťaty – jsou pacienti dostatečně informováni?
- Chřipka a její komplikace. Co nás čeká?
- Horké aktuality v registracích EMA
- Svět praktické medicíny
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Vši a svrab: Aktualizace léčby
- Diagnostika a terapie těžké akutní pankreatitidy v intenzivní medicíně
- Testosteron u mužů s metabolickým syndromem, prediabetem a diabetem 2. typu Pozitivní účinky terapie testosteronem
- Chřipka a její komplikace. Co nás čeká?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání











