-
Medical journals
- Career
Léčba mnohočetného myelomu s projevy choroby z ukládání lehkých řetězců; kompletní remise s negativitou minimální reziduální nemoci po léčbě daratumumabem, dexametazonem a lenalidomidem – popis případu a přehled literatury
Authors: Z. Adam 1; J. Svojanovský 2; I. Svobodová 3; A. Tkadlec 4; M. Borský 5; M. Krejčí 1; M. Štork 1; I. Boichuk 1; Z. Král 1; L. Pour 1
Authors‘ workplace: Interní hematologická a onkologická klinika (IHOK) LF MU a FN Brno 1; I. ústav patologie LF MU a FN u sv. Anny v Brně 2; II. interní klinika LF MU a FN U sv. Anny v Brně 3; Baťova nemocnice, Zlín 4; Centrum molekulární biologie a genetiky, Interní hematologická a onkologická klinika (IHOK) LF MU a FN Brno 5
Published in: Transfuze Hematol. dnes,32, 2026, No. 1, p. 37-47.
Category: Review/Educational Papers
doi: https://doi.org/10.48095/cctahd202609Overview
Light chain deposition disease (LCDD), česky nemoc z depozice lehkých řetězců, je termín používaný pro poškození ledvin depozity klonálních lehkých řetězců (FLC) kappa v amorfní neorganizované podobě. LCDD způsobuje v ledvinách pokles filtrace, nefrotický syndrom s mikroskopickou hematurií a proteinurií. Změny v glomerulech, indukované vazbou FLC kappa na struktury mezangia, způsobují ireverzibilní poškození ledvin. Podobná depozita mohou poškozovat srdce, plíce i játra. LCDD je častěji diagnostikována u pacientů s nemaligní monoklonální gamapatií, kteří, nebýt poškození ledvin, by splňovali diagnózu monoklonální gamapatie nejistého významu (MGUS), než u osob splňujících kritéria mnohočetného myelomu. V popisovaném případě byl prvním symptomem nemoci nefrotický syndrom. Biopsie ledvin vedla k průkazu poškození ledviny typu LCDD a následné hematologické vyšetření prokázalo mnohočetný myelom, i když nebyly přítomné osteolytické změny. První léčebná linie založená na bortezomibu, zakončená vysokodávkovanou chemoterapií, dosáhla 31 měsíců trvající kompletní remise nemoci. Pak bylo nutné pro narůstající koncentrace FLC kappa a zvyšující se poměr FLC kappa/lambda, čili relaps nemoci, zahájit druhou linii léčby založenou na antiCD38 protilátce. Po 24 měsících léčby daratumumabem, lenalidomidem a dexametazonem bylo dosaženo kompletní hematologické remise s negativitou minimální reziduální nemoci. Díky časnému zahájení léčby druhé linie zůstala funkce ledvin bez dalšího zhoršení. Osud ledvin pacientů s LCDD, která způsobuje ireverzibilní poškození ledvin, závisí na časné diagnostice monoklonální gamapatie lehkých řetězců, tedy na vyšetření FLC u osob s otoky nejasné etiologie či se zvyšujícími se hodnotami kreatininu. Patologická hodnota FLC a patologický poměr FLC by měl vzbudit podezření a vést k časné histologické diagnostice. Následovat musí účinná léčba vedoucí k potlačení tvorby nefrotoxických lehkých řetězců, tedy k dosažení kompletní hematologické remise a nejlépe k negativitě minimální reziduální nemoci. Zásadní je nepovažovat každou retenci tekutin za následek srdeční slabosti a vždy u těchto osob provést vyšetření, která mohou prokázat nefrotický syndrom. A pokud je nefrotický syndrom či směřování k němu prokázáno, tak je třeba požádat specialisty o diferenciální diagnostiku nefrotického syndromu, což může vést k průkazu poškození ledvin při gamapatii.
Klíčová slova:
volné lehké řetězce – light chain deposition disease
ÚVOD
Monoklonální imunoglobulin a/nebo volné lehké řetězce mohou poškozovat ledviny. Do povědomí lékařů se dostal fakt, že příčinou renální insuficience může být mnohočetný myelom. Méně známá je skutečnost, že i biologicky benigní monoklonální gamapatie může způsobit závažné poškození ledvin [1].
Moderní zobrazovací metody zvýšily bezpečnost ledvinných biopsií [2,3]. Pokrok v histopatologické diagnostice v posledních několika desetiletích vedl k prohloubení poznání jednotlivých forem poškození ledvin monoklonálním imunoglobulinem (M-Ig) a / nebo volnými lehkými řetězci imunoglobulinů (free light chain – FLC) [1].
Vznikla tak potřeba celosvětově sjednotit terminologii pro jednotlivé typy poškození ledvin volnými lehkými řetězci imunoglobulinů a/nebo kompletní molekulou monoklonálního imunoglobulinu. Tohoto úkolu se ujala mezinárodní skupina odborníků „The International Kidney and Monoclonal Gammopathy Research Group – IKMG“. Tato společnost systematicky studuje a klasifikuje všechny formy poškození ledvin monoklonálním imunoglobulinem. V roce 2012 vydala první klasifikaci. Již z názvu publikace: „Monoclonal gammopathy of renal significance: when MGUS is no longer undetermined or insignificant“ vyplývá, že velmi často je to benigní gamapatie, která by splňovala kritéria monoklonální gamapatie nejistého významu (monoclonal gammopathy of undetermined significance – MGUS), nebýt poškození ledvin. V roce 2012 uvedená skupina navrhla pro případy benigní gamapatie poškozující ledviny termín monoclonal gammopathy of renal significance (MGRS), neboli „monoklonální gamapatii renálního významu“. Biologický charakter buněčné populace, produkující M-Ig a / nebo FCL, je benigní, ale produkt těchto buněk je toxický pro ledviny a poškozuje je [4].
Poslední úprava této klasifikace byla zveřejněna v roce 2019. Pomocí klasické histologie, imunofluorescence a někdy i s pomocí elektronové mikroskopie definuje jednotlivé morfologické formy poškození ledvin etiopatogeneticky související s monoklonálním imunoglobulinem [5].
V roce 2022 byl termín „monoklonální gamapatie renálního významu“ poprvé uveden v páté verzi WHO klasifikace krevních chorob, kde monoklonální gamapatie renálního významu nyní představuje jednu jednotku ze skupiny nazvané „Plasma cell neoplasms and other diseases with paraproteins“ [6].
Skupina chorob řazených pod označením „monoklonálních gamapatií renálního významu – MGRS“ obsahuje dvě hlavní podskupiny:
- formy poškození ledvin s depozity M-Ig a / nebo FLC,
- formy poškození ledvin bez depozit M-Ig a / nebo FLC.
Podskupina s depozity M-Ig a/nebo FLC se dělí na kategorii s organizovanými depozity a kategorii s neorganizovanými (amorfními depozity) [7,8]. Klasifikaci shrnuje tab. 1.
Table 1. Klasifi kace poškození ledvin volnými lehkými řetězci (FLC) a/nebo monoklonálním imunoglobulinem (M-Ig) dle [5]. Termíny ponechány v původní anglické formě. ![Klasifi kace poškození ledvin volnými lehkými řetězci (FLC) a/nebo monoklonálním imunoglobulinem (M-Ig) dle [5]. Termíny ponechány v původní anglické formě.](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/818cf791bd1eef2b13f882d2ffe73fdf.png)
Nejznámějším zástupcem jednotky s organizovanými depozity je poškození ledvin AL-amyloidóza. Struktura amyloidu je tvořena lineárně uloženými fibrilami, jejichž základem jsou u AL-amyloidózy volné lambda řetězce [9].
Nejznámějším zástupcem jednotky s poškozením ledvin neorganizovanými (amorfními) depozity je „light chain deposition disease – LCDD“. Depozita lehkých řetězců kappa u LCDD nevykazují ani v elektronovém mikroskopu žádnou detekovatelnou strukturu, proto jsou hodnocena jako neorganizovaná na rozdíl od organizované struktury depozit amyloidových fibril.
U této jednotky se i v domácí literatuře někdy ponechává anglický termín, v jiných publikacích se používá český termín [10]. LCDD je natolik vzácná jednotka, že neexistují žádné klinické studie popisující léčbu této jednotky, ale jen popisy jednotlivých případů anebo menších souborů nemocných.
Cílem textu je připomenout tuto jednotku, která může provázet jak maligní gamapatii typu mnohočetného myelomu, tak benigní gamapatii (monoclonal gammopathy of renal significance – MGRS), a poukázat na přínos nových léků ze skupiny antiCD38 monoklonálních protilátek pro léčbu této nemoci a zdůraznit, že LCDD poškozuje ledviny nevratně, a proto cílem léčby musí být kompletní hematologická remise, optimálně s dosažením negativity minimální reziduální nemoci.
Pacient podepsal standardní informovaný souhlas v souladu s poslední Helsinskou deklarací, který byl vytvořen pro registr České myelomové skupiny. Nemocný taktéž podepsal souhlas s publikací popisu případu v časopise.
POPIS PŘÍPADU
Muž, narozený 1955, který v anamnéze neměl žádné vážnější onemocnění, měl v roce 2018 (v 63 letech) nově zjištěnou hypertenzi a také rozvíjející se symetrické otoky dolních končetin, které dříve neměl. Symetrické otoky nohou jsou někdy mylně interpretované jako následek srdeční slabosti a léčené zvyšujícími se dávkami diuretik. Přitom unikne pravá příčina, nefrotický syndrom, způsobený monoklonální gamapatií.
V tomto případě se tak naštěstí nestalo. Jeho ošetřující lékaři provedli v rámci nově zjištěné hypertenze s otoky dolních končetin (DK) kompletní vyšetření, zjistili postupně se navyšující odpad bílkoviny za 24 h a postupně se zvyšující koncentraci fibrinogenu. Ta při odeslání k dalšímu vyšetření do Brna dosáhla hodnoty 5,1 g/l (norma 1,8–4,2) v séru při nezvýšeném markeru srdeční slabosti (NTproBNP) a normálním echokardiografickém nálezu. Byl tak diagnostikováb postupně se rozvíjející nefrotický syndrom.
Pro stanovení příčiny rozvoje poškození ledvin typu nefrotického syndromu byl pacient předán do Fakultní nemocnice u sv. Anny v Brně, kde provedli biopsii ledviny. Biopsie proběhla bez komplikací a histologické vyšetření prokázalo nemoc light chain deposition disease. Punkce ledviny o délce 8 mm zastihla kůru ledviny s 10 glomeruly, z toho dva byly globálně zaniklé. Nezaniklé glomeruly vykazovaly difuzní projevy nodulární glomerulosklerózy. Noduly měly nepravidelnou velikost, malé mezangiální noduly měly v okolí zvýšenou mezangiální buněčnost. Glomerulární bazální membrány (GBM) byly zesílené, ojediněle byla subsegmentálně reduplikace GBM. Matrix nodulů byla silně PAS (periodic acid-schiff) pozitivní. Imunofluorescenční reakce, které prokazují depozita amyloidu, tedy barvení saturnovou červení, stejně jako barvení thioflavinem a kongočervení, byly negativní. Tubulární bazální membrány byly také zesílené. Artérie a arterioly měly PAS+ insudáty. Muskulární artérie měly výrazné fibrointimální zesílení a reduplikaci elastiky. Intersticium vykazovalo fibrózou asi v 25 % objemu vzorku. Tubulární atrofie měla podobný rozsah. Ložiskově v lumen tubulů byly bílkovinné válce.
Patolog nález uzavřel slovy: Histologický obraz imunofluorescenčního vyšetření je kompatibilní s diagnózou LCDD. S touto diagnózou byl pacient předán na IHOK.
Vstupní vyšetření – mnohočetný myelom bez osteolytických změn skeletu
Výsledky vyšetření, které navazovalo na průkaz LCDD, uvádí tab. 2. Pacient splňoval kritéria mnohočetného myelomu, v kostní dřeni měl poměrně masivní infiltraci abnormálními klonálními plazmocyty (kappa). V histologickém hodnocení trepanobioptického válečku jejich počet kolísal mezi 10 a 40 %, dle místa hodnocení. Biochemické vyšetření prokázalo vyšší koncentraci FLC kappa v séru (918,64 mg/l) a patologický poměr kappa/lambda, který byl 53, (normální rozmezí je 0,26–1,65). Kvantitativní vyšetření imunoglobulinů (IgG, IgM, IgA) prokázalo snížení jejich hladin. Nejvíce zřetelné bylo snížení IgG na 3,33 g/l, přičemž dolní hranice fyziologického rozmezí je 7 g/l (viz tab. 2). Tento nález se hodnotí jako imunoparéza (snížení všech hlavních tříd imunoglobulinů pod dolní hranici normy) a typicky provází mnohočetný myelom s tvorbou lehkých řetězců.
Table 2. Vstupní vyšetření v prosinci 2018 korespondující s diagnózou maligní gamapatie typu mnohočetného myelomu lehkých řetězců kappa. 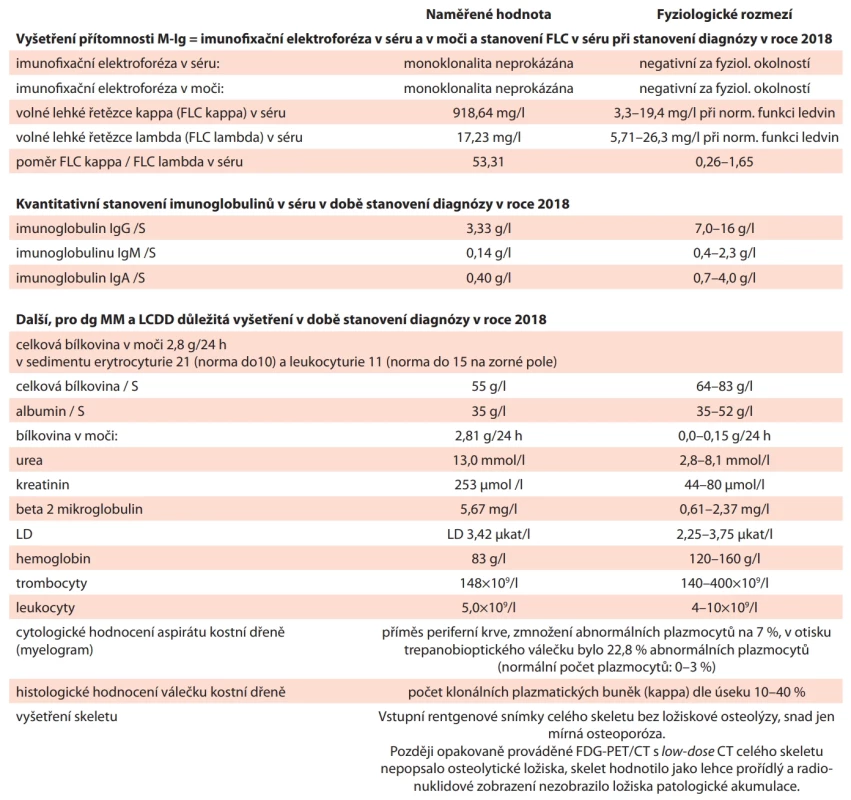
Imunofixační elektroforéza byla negativní jak v séru, tak v moči. Pacient byl anemický, koncentrace hemoglobinu dosahovala jen 83 g/l. Hodnota kreatininu byla následkem poškození ledvin zvýšená (253 µmol /l, normální hodnota do 80 µmol /l), u nás naměřená proteinurie činila 2,8 g/24 h, dle předchozích vyšetření občas přesáhla i 3,5 g/24 h, tedy hranici uvedenou v definici nefrotického syndromu. Pacient v roce 2018 neměl (a v roce 2024 stále nemá) žádná osteolytická ložiska. Je to jeden z té malé části pacientů, kteří mají mnohočetný myelom a nemají přitom osteolytické kostní postižení. Pacient byl klasifikován dle Durieho-Salmona jako stadium II a dle ISS (The Multiple Myeloma International Staging System) jako stadium III.
Léčba mnohočetného myelomu s poškozením ledvin formou LCDD
Léčba mnohočetného myelomu byla zahájena 12. 12. 2018 kombinací bortezomibu, cyklofosfamidu a dexametazonu. Celkem dostal 5 cyklů této léčby, přičemž poslední aplikace proběhla v květnu 2019. V červnu 2019 následoval sběr kmenových buněk krvetvorby z periferní krve, v září 2019 pak vysokodávkovaná chemoterapie, melfalan 100 mg/m2, a následně proběhla transplantace autologních kmenových buněk krvetvorby. Tím byla léčba ukončena a pacient byl jen sledován. Laboratorní hodnoty po ukončení léčby v září 2019 odpovídaly kompletní remisi nemoci. Hodnoty kreatininu po léčbě zůstávaly trvale zvýšené, pohybovaly se mezi 165–196 µmol/l, viz tab. 3, ale poměr FLC byl v září 2019 v normě a koncentrace polyklonálních imunoglobulinů, které byly vstupně výrazně snížené, se postupně po dosažení kompletní remise zvyšovaly, až se dostaly do fyziologického rozmezí. Dosaženou léčebnou odpověď jsme hodnotili jako první kompletní remisi. K prvnímu nepatrnému vzestupu poměru FLC nad horní fyziologickou hranici na 2,12 (norma do 1,65) a ke vzestupu absolutní hodnoty FLC došlo v dubnu roku 2022, tedy po 31 měsících od ukončení léčby. Od dubna 2024 se začala velmi pomalu zvyšovat jak koncentrace FLC kappa, tak poměr FLC kappa/lambda, jak ilustruje tabulka. Vzestup FLC kappa a poměru kappa/lambda byl velmi pomalý a hodnoty kreatininu se nijak zásadně neměnily, takže jsme jen pozorně sledovali vývoj. U pacienta byla histologicky prokázána LCDD čili nemoc způsobená nefrotoxickými lehkými řetězci kappa, což je forma poškození ledvin, která zůstává nevratná i po potlačení gamapatie. Při dosažení absolutní hodnoty FLC kappa 97 mg/l a poměru kappa/lambda 3,79 jsme tudíž naplánovali léčbu na další měsíc, únor 2023. Pro léčbu relapsu byl zvolen režim daratumumab, lenalidomid a dexametazon. Daratumumab byl podáván ve standardní dávce 1800 mg dle doporučeného schématu, dexametazon v dávce 20 mg byl podáván vždy současně s daratumumabem. Lenalidomid byl redukován na 10 mg pro renální insuficienci. Po zahájení léčby hodnoty FLC opět velmi rychle poklesly k normálním hodnotám, hodnoty kreatininu však zůstávají trvale zvýšené a pohybují se od 138 do 178 µmol /l. Pozitivní je, že je přece jen pozorována tendence ke snižování v průběhu léčby, viz tab. 3.
Table 3. Vybrané hodnoty FLC a kreatininu v séru před a v průběhu léčby pacienta s LCDD. 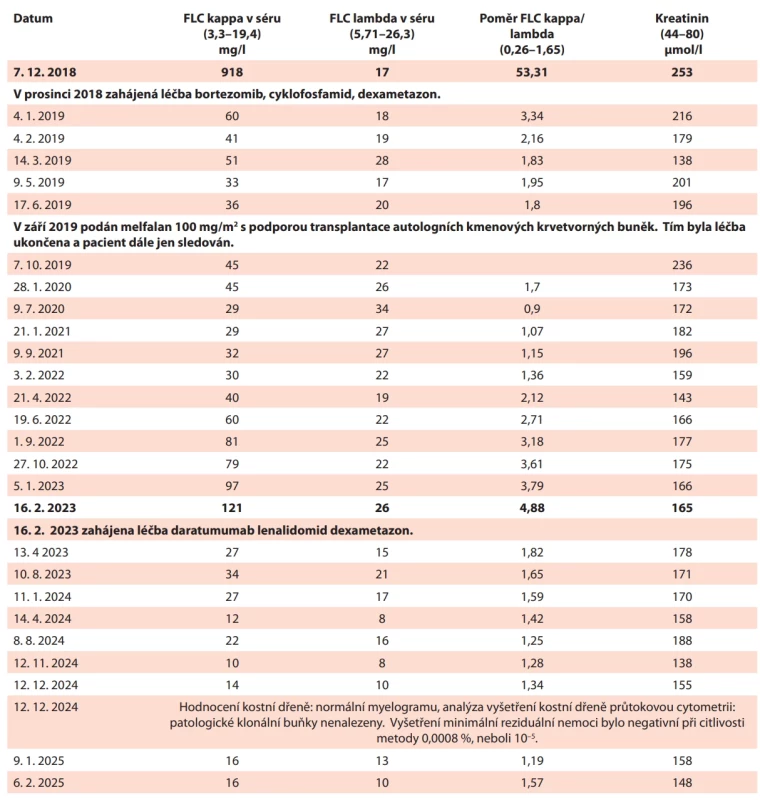
V prosinci 2024 byl aplikován 24. cyklus této léčby. Hodnoty FLC a hodnoty kreatininu dáváme do tabulky 3. V prosinci 2024 bylo provedeno vyšetření kostní dřeně. Myelogram byl bez zmnožení plazmocytů, odpovídal fyziologické hematopoéze. Hodnocení kostní dřeně pomocí průtokové cytometrie prokázalo v dodaném materiálu 0,06 % plazmocytů. Hodnocené plazmocyty byly normálního fenotypu, polyklonální. Vyšetření minimální reziduální nemoci bylo negativní při citlivosti metody 0,0008 % neboli 10–5.
V listopadu 2025 provedeno druhé kontrolní vyšetření kostní dřeně a opět prokázalo negativitu minimální reziduální nemoci při stejné citlivosti. Následně byla léčba ukončena. Pacient chodí ve 2–3měsíčních intervalech na kontroly. Po 12 měsících zkontrolujeme trvání negativity minimální reziduální nemoci.
Při poslední kontrole v lednu 2026 měl v moči nízkou koncentraci bílkoviny 0,12 g/l, hodnoty FLC byly v normě, jejich poměr je 1,19, ale kreatinin zůstává zvýšený (158 µmol /l), podobný hodnotě na počátku léčby i přes excelentní hematologickou léčebnou odpověď.
DISKUZE
Při pohledu do databáze české a slovenské odborné literatury medvik.cz jsme v posledních 20 letech napočítali jen 7 publikací na téma poškození organizmu amorfními depozity LCDD [10–16], zatímco počet publikací na téma poškození organizmu lineárními (organizovanými) depozity při AL-amyloidóze, které vyšly in extenso, výrazně přesahuje stovku. Z nich citujeme jen ty nejdůležitější [17–25].
LCDD je tedy u nás diagnostikovaná vzácně. Informace o poškozování ledvin (i celého organizmu) amorfními depozity kappa řetězů se přitom v lékařské literatuře objevují již od přelomu 60. a 70. letech minulého století. Zjistilo se, že selhání ledvin u osob s monoklonální gamapatií má v některých případech histologický obraz glomerulosklerózy, kterou nazvali kappa light chain glomerusclerosis [26,27].
Podrobný popis poškození organizmu depozity lehkých řetězců kappa zveřejnil Randall již v roce 1976 [28], a proto se v odborné literatuře spojovalo a spojuje jméno prvního autora s tímto morfologickým obrazem v názvu Randall-type monoclonal immunoglobulin deposition disease [29].
Poškození ledvin depozity klonálních lehkých řetězců v rámci LCDD
Vzhledem k tomu, že FLC jsou filtrovány v glomerulech a vstřebávány v proximálním tubulu, je poškození ledvin lehkými řetězci (LC) častější než poškození jiných tkání.
Dle patofyziologických vlastností LC je lze klasifikovat na tubulopatické, pokud poškozují proximální tubulus, anebo na glomerulopatické, pokud LC reaguje se strukturami glomerulu a s mezangiálními buňkami. Tubulopatické FLC způsobují různé formy poruch tubulů, glomerulopatické pak poruchy glomerulů. Glomerulopatické LC mohou být podkladem jak AL-amyloidózy, tak i LCDD.
To, zda LC tvořené patologickým klonem plazmocytů či lymfoplazmocytů vytvoří agregáty v ledvině či jiné tkáni, se odvíjí od toho, zda klonální evoluce v plazmocytu vedla k vytvoření struktury LC s afinitou k bílkovinám glomerulů a mezangia.
V případech LCDD mají klonální LC tendenci vázat se na struktury glomerulárních a tubulárních bazálních membrán, speciálně na sortilin-related receptor mezangiálních buněk (SORL1) s následnou transformací mezangiální buňky směrem k myofibroblastu [30].
Vazba LC na struktury glomerulárních kapilár způsobuje jejich poškození a výsledkem je proteinurie a případně erytrocyturie. Zásadním patofyziologickým mechanizmem LCDD je vazba LC kappa na struktury mezangia. Tato vazba indukuje patologické změny, expanzi mezangia s tvorbou extracelulární hmoty a abnormální kompozice s nodularitami. Tyto novotvořené hmoty, indukované depozity LC kappa, nahrazují ireverzibilně fyziologickou matrix tvořenou hlavně kolagenem IV. Zvýšená produkce patologické mezangiální matrix v okolí depozit lehkých řetězců kappa je hlavním diagnostickým znakem a hlavní příčinou selhání funkce ledvin [31].
Změna struktury mezangia je ve světelné mikroskopii patrná jako nodulární glomeruloskleróza, která velmi věrně imituje změny při diabetu [32]. Zpočátku postihuje jen část glomerulu, ale jakmile je postižena více než polovina glomerulu, vede to k jeho nevratnému zániku. Jakmile tedy již jednou vznikne závažné poškození ledvin, potlačení tvorby toxických LC již nevede k úpravě jejich funkce [33,34]. Proto jsou tak důležité včasná diagnóza a vyšetřování FLC u všech nejasných forem renálního selhání.
Biologický charakter buněk produkujících toxické LC
Přibližně 15–20 % diagnostikovaných případů LCDD souvisí s mnohočetným myelomem a zbývajících 80–85 % diagnostikovaných případů souvisí s nemaligní klonální proliferací plazmocytů.
V případě AL-amyloidózy jsou lehké řetězce produkovány myelomovými buňkami u 8–12 % osob s AL-amyloidózou, ve zbývajících případech (88–92 %) jsou produkovány nemaligní populací odpovídající MGCS [33,34].
Klinický obraz LCDD
Rychlost úbytku funkce ledvin závisí mimo jiné na kvantitě nefrotoxických lehkých řetězců kappa. V případech mnohočetného myelomu bývá jejich koncentrace vyšší než u MGRS, a tak i úbytek ledvinných funkcí bývá rychlejší. Mikrohematurie a hypertenze provázejí 75 % případů LCDD [29]. Uvedené dva fenomény u AL-amyloidózy ledvin nebývají. Cohen ve své recentní publikaci popisuje několik mírně odlišných klinických obrazů LCDD:
- Progresivně se zhoršující renální selhání se signifikantní proteinurií, která ale ne vždy naplňuje všechna kritéria nefrotického syndromu (proteinurie >3,5 g/24 hod, závažná hypoalbuminémie, hyperkoagulace a hypoproteinemické otoky). Příčinou je pozvolně narůstající poškození glomerulů.
- Progresivně se zhoršující renální selhání s nesignifikantní proteinurií (<0,5 g/24 hodin). Tento klinický obraz nejčastěji uniká diagnóze. Amorfní depozita kappa řetězců v těchto případech způsobují vaskulární poškození a extenzivní intersticiální fibrózu.
- LCDD kombinovaná s „myeloma cast nephropathy,“ neboli poškozením tvorbou odlitkových válců v ledvinných tubulech. U tohoto typu poškození prokáže biopsie ledviny jak pro LCDD typickou glomerulosklerózu, tak i poškození ledvin typu odlitkové nefropatie. Klinický obraz se v těchto případech podobá myelomové ledvině, ale je přítomna výrazná albuminurie, která u čisté formy odlitkové nefropatie nebývá. Pro správnou diagnostiku je důležité imunofluorescenční vyšetření [29].
Tyto formy lze detekovat i v popisu největšího prospektivně sledovaného souboru z Velké Británie. V centru zvaném National Amyloidosis Centre registrovali v letech 1999–2018 celkem 77 pacientů s LCDD. Medián věku při stanovení diagnózy byl 59 (26–81) let. Všech 77 pacientů mělo poškození funkce ledvin, 54 nemocných (70,1 %) mělo eGFR < 30 ml/min. 10 pacientů (13 %) mělo proteinurii < 0,5 g/24 h, 11 nemocných (14,3 %) mělo současně poškození i srdce a 10 (13 %) mělo mimo ledvin poškozená i játra. Osm pacientů (10,4 %) bylo při stanovení diagnózy dialyzováno. U žádného z popsaných pacientů se nejednalo o kombinaci LCDD a AL-amyloidózy, šlo pouze o případy LCDD.
Medián koncentrace patologického FLC v době stanovení diagnózy byl 450,8 (2,4–25 690) mg/l. Medián počtu plazmocytů v kostní dřeni byl 8 % (1–70 %).
Celkem 12 ze 77 pacientů (15,5 %) naplnilo kritéria diagnózy mnohočetného myelomu, u ostatních (84,5 %) se jednalo o nemaligní gamapatii, která, nebýt poškozených ledvin, by odpovídala diagnóze MGUS. Pro poškození ledvin však byla klasifikována jako MGCS. Medián počtu léčebných linií byl 1 (1–5). Medián celkového přežití byl 134 měsíců. Pacienti, kteří dosáhli VGPR (very good partial remission) a lepší, měli delší přežití než pacienti s menší odpovědí. U 7 ze 77 sledovaných nemocných (9,1 %) byla provedena transplantace ledvin. Přežití štěpu bylo po prvním roce 86 % po 5 letech 70 % a po 10 letech 70 %. Tato data z největší studie z Velké Británie dokládají, že osud nemocných pozitivně ovlivní včasná diagnóza a dosažení kompletní hematologické remise účinnou léčbou, jež rychle potlačí tvorbu patologických FLC. Poškození ledvin v rámci „LCDD“ je heterogenní a klinicky se projeví pomalu progredujícím renálním selháním při minimální proteinurii, přičemž 13 % nemocných mělo proteinurii < 0,5 g/24 h. Transplantace ledviny je možným řešením pouze pro pacienta s hlubokou hematologickou léčebnou odpovědí [35].
V retrospektivní analýze bylo o něco více případů asociováno s mnohočetným myelomem, jinak obě práce mají podobné výsledky [36].
V případě provedení transplantace ledvin bez potlačení tvorby nefrotoxických lehkých řetězců kappa dochází k poškození transplantované ledviny [37]. V literatuře se objevuje více popisů případů přehlédnutí LCDD před transplantací ledviny a rozpoznání této nemoci až v transplantované ledvině [38,39]. To signalizuje časté přehlédnutí této diagnózy při hledání příčin renální insuficience.
Poškození dalších orgánů v rámci LCDD
LCDD vzácně může poškodit i další orgány. V plicním parenchymu se LCDD projevuje tvorbou tenkostěnných cyst (58 %) a tenkostěnných cystických bronchiektázií. Existují minimálně dvě hematologické choroby, které způsobují cystickou přeměnu plicního parenchymu – mimo LCDD je to histiocytóza z Langerhansových buněk. Tyto cysty lze zobrazit pomocí high resolution CT (HRCT) plic. Etiopatogenetickou příčinu vzniku těchto cyst odhalí histologické vyšetření thorakoskopicky odebraného vzorku. Zcela výjimečně byla pozorována plicní forma poškození amorfními depozity bez poškození dalších orgánů. Manifestuje se jako progresivní obstruktivní choroba s tvorbou bul a cyst, které mohou vést k ventilační insuficienci. V poškozených plicích lze detekovat amorfní depozita monoklonálního LC v alveolární stěně a nejmenších bronchiolech. V těchto ojedinělých případech byla prokázána lokální tvorba kappa řetězců přímo v plicích, tedy obdoba ložiskové AL-amyloidózy [40–43].
LCDD může také způsobit hepatomegalii a jaterní selhání [44–46] anebo poškození srdce (kardiomyopatii), podobně jako vídáme u AL-amyloidózy. Současné poškození srdce je detekováno u třetiny pacientů s ledvinovou formou LCDD [47,48]. Nejčastějšími klinickými příznaky je dušnosti, arytmie, prodloužený QT interval anebo sinusová bradykardie. Echokardiografie v těchto případech prokáže hypertrofickou kardiomyopatii s diastolickou dysfunkcí, zatímco ejekční frakce levé komory bývá zachována. Klinické důsledky poškození srdce v rámci LCDD jsou méně závažné než poškození srdce depozity AL amyloidu [29].
LCDD lze diagnostikovat jedině renální biopsií (RB)
Od roku 1951, kdy byla v Dánsku provedena první RB, se postupně technika provedení zdokonalovala a v dnešní době je „zlatým standardem“ provedení RB plně automatickou odběrovou pistolí (biopsy gun) pod ultrazvukovou kontrolou. Tato technika představuje nejbezpečnější způsob provádění RB s maximální výtěžností. Transvazální metody RB (transjugulární nebo transfemorální) jsou indikovány výjimečně, a to zejména při hemokoagulačních abnormalitách.
Indikace k provedení RB lze obecně shrnout následovně: izolovaná hematurie, nefrotický syndrom, nefritický syndrom, nejasné akutní renální selhání, renální postižení v rámci systémových onemocnění, rychle progredující glomerulonefritidy.
Okruh kontraindikací se vzhledem k technickému zdokonalení při provádění RB výrazně zúžil a v dnešní době je absolutní kontraindikací RB pouze nesouhlas nemocného a nekorigovatelná porucha hemokoagulace. Mezi relativní kontraindikace RB patří: těžká trombocytopenie a porucha hemokoagulace, obezita, nespolupracující nemocný, nekorigovatelná hypertenze, anatomické odchylky ledvin (malé ledviny ≤ 8 cm, cysticky změněné ledviny, solitární ledvina, hydronefróza) nebo aktivní močová infekce.
RB je invazivní výkon a může být spojena s řadou různě závažných komplikací, které se rozvinou nejčastěji do 24 hodin po výkonu. Mezi nejčastější komplikace patří bolest (4 %), krvácení do ledviny nebo jejího okolí (drobný parenchymový nebo subkapsulární hematom až v 90 %, perinefritický hematom v 11 %, retroperitoneální hematom v 0,1–0,4 %, nutnost nefrektomie 0,01 % případů). Makroskopická hematurie se vyskytuje v 3–10 % případů a mezi vzácné komplikace RB patří i vznik arteriovenózní píštěle nebo infekční komplikace.
V současné době lze RB považovat za poměrně bezpečný výkon, který významné přispívá k diagnostice renálních onemocnění a pomáhá při rozhodování o způsobu léčby. Stále ale patří do rukou zkušeného specialisty a na pracoviště, které je schopné komplexně řešit případné komplikace [2,3,49,50].
Léčba monoklonální gamapatie renálního významu typu LCDD
Léčba MGRS, která je podkladem LCDD, má za cíl vždy kompletně potlačit tvorbu toxického FLC, a proto se používá léčba, které má největší potenciál toho účinku dosáhnout. V současnosti jsou to režimy obsahující antiCD38 monoklonální protilátky, bortezomib anebo lenalidomid. Před lety, kdy nebyly k dispozici antiCD38 protilátky, byly léčbou volby kombinace s bortezomibem. Pacientů s LCDD je podstatně méně než pacientů s AL-amyloidózou, a proto je dobrá účinnost daratumumabu u LCDD zachycena jen v popisech jednotlivých případů. Přínos antiC38 protilátky je u LCDD stejně výrazný jako u AL-amyloidózy [51], ale na rozdíl od AL-amyloidózy je doložen jen popisy jednotlivých případů či menších sérií pacientů, které zde citujeme [52–57]. Zkušenosti z těchto případů prokázaly vysoký počet kompletních hematologických remisí, tedy lepší výsledky než léčebné postupy bez antiCD38 protilátky. To platí jak pro gamapatie odpovídající maligní proliferaci typu mnohočetnému myelomu, tak pro gamapatie s nemaligní proliferací typu monoklonální gamapatie renálního významu.
V přehledovém článku o poškození depozity FLC je také zmiňována nejen léčba daratumumabem, ale i další antiCD38 protilátkou, isatuximabem [58].
V současnosti se setkáváme také s pacienty, u nichž je poškození ledvin monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci diagnostikováno až po provedení transplantace solidního orgánu od živého či mrtvého dárce. Minulý rok jsme léčili pacienta, který byl po transplantaci srdce od mrtvého dárce, u něhož recidivovala AL-amyloidóza, a dále pacientku, u níž byla diagnostikována LCDD až v transplantované ledvině [59].
U těchto pacientů se nedoporučuje podávat lenalidomid či obecně lék ze skupiny IMiDs (immunomodulatory drugs), protože tyto léky stimulují jak protimyelomovou imunitu, tak stimulují reakci dárce proti transplantovanému orgánu. To vede k rejekci transplantovaného orgánu, jak je popsáno ve více případech [60–64]. Proto při léčbě gamapatie u pacientů po alogenní transplantaci orgánu používáme daratumumab v kombinaci s bortezomibem a cyklofosfamidem, ale nikoliv s léky ze skupiny IMiDs
ZÁVĚR
LCDD je jednou z mnoha dnes dobře definovaných forem poškození ledvin spadajících pod skupinové označení monoklonální gamapatie renálního významu. LCDD se od jiných forem poškození organizmu monoklonálním imunoglobulinem liší ireverzibilitou změn i při dosažení kompletní remise s negativním výsledkem imunofixační elektroforézy a normální koncentrací volných lehkých řetězců. V případech LCDD by bylo přínosné stanovení klonálních FLC v séru, abychom při jejich opětovném vzestupu ihned obnovili léčbu gamapatie. Stanovení monoklonální lehkého řetězce zatím není dostupné, i když Kušnierová tuto metodiku popisuje [65–67].
Nevratnost poškození ledvin je imperativem pro velmi časné obnovení léčby v případě relapsu nemoci. Na rozdíl od mnohočetného myelomu, kdy se klasicky čeká s obnovením léčby až na počínající první klinické symptomy, tak u LCDD je nutno obnovit léčbu ihned při prvních laboratorních známkách progrese. Vzhledem k tomu, že zatím nemáme možnost stanovit monoklonální FLC, je důležitým vyšetřením při sledování vývoje pacientů s LCDD vyšetření kostní dřeně s vyhodnocením počtu klonálních plazmocytů v kostní dřeni s pomocí průtokové cytometrie. Vyšetření kostní dřeně průtokovou cytometrií může včas odhalit pozvolnou progresi nemoci [68,69].
Renální poškození způsobené monoklonální gamapatií bylo dříve kontraindikací provedení transplantace ledviny. Vysoký počet dlouhodobých remisí vlivem nových léků tento názor změnil. Pokud se podaří dosáhnout kompletní remise monoklonální gamapatie s negativitou minimální reziduální nemoci, které způsobila poškození ledvin LCDD, je možné zvažovat transplantaci ledviny [70]. Indikace k zařazení do transplantačního programu rozebírají autorky z Kliniky nefrologie Transplantačního centra v IKEM Praha [71].
Poškození ledvin typu LCDD může být tedy důsledkem jak mnohočetného myelomu, jako tomu bylo v tomto případě, tak i důsledkem benigní gamapatie, která se nazývá MGRS. MGRS představuje podskupinu vyšší jednotky s názvem „monoklonální gamapatie klinického významu“. Kategorie monoklonální gamapatie klinického významu sdružuje všechny formy poškození organizmu monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci, u nichž je indikována ta nejúčinnější cytotoxická léčba jako u maligních gamapatií, i když biologický charakter klonu, který produkuje tyto bílkoviny, není maligní [72,73].
Symetrické otoky nohou u starší pacientů jsou často vysvětleny srdeční slabostí a lékaři na ně reagují zvyšováním dávek diuretik. Tento zjednodušený pohled někdy vede k přehlédnutí rozvíjejícího se nefrotického syndromu. Často jsme to viděli u osob s AL-amyloidózou poškozující srdce a ledviny, kde se vše vysvětluje ischemickou nemocí srdeční a k rozpoznání AL-amyloidózy došlo až při tak značném poškození organizmu, že pacient zemřel dříve, než se mohl projevit efekt léčby. Proto je u osob se známkami retence tekutin nutné provést všechna vyšetření, která mohou odhalit nefrotický syndrom. A pokud tato vyšetření nefrotický syndrom prokáží, tak je potřeba otevřít aktuální přehled možných příčin a snažit se najít jeho etiopatogenetickou příčinu [74].
Sources
1. Ryšavá R. Postižení ledvin při monoklonálních gamapatiích a mnohočetném myelomu. Cas Lek Cesk. 2024; 163 (3): 98–105.
2. Shimamura Y, Ogawa Y, Takizawa H, et al. Light chain deposition disease diagnosed using computed tomography-guided kidney biopsy. Cureus. 2021; 13 (5): e15102. doi: 10.7759/cureus.15102.
3. Trnavský K, Svojanovský J, Nedbálková M, et al. Výsledky biopsií ledvin za posledních 5 let na II. interní klinice FN u sv. Anny. Aktual Nefrol. 2012; 18 (Suppl 1): 28–30.
4. Leung N, Bridoux F, Hutchison CA, et al. Monoclonal gammopathy of renal significance: when MGUS is no longer undetermined or insignificant. Blood 2012; 120 (22): 4292–4295.
5. Leung N, Bridoux F, Batuman V, et al. The evaluation of monoclonal gammopathy of renal significance: a consensus report of the International Kidney and Monoclonal Gammopathy Research Group. Nat Rev Nephrol. 2019; 15 (1): 45–59. doi: 10.1038/s41581-018-0077-4.
6. Alaggio R, Amador C, Anagnostopoulos I, et al. The 5th edition of the World Health Organization Classification of Haematolymphoid Tumours: Lymphoid Neoplasms. Leukemia. 2022; 36 (7): 1720–1748. doi: 10.1038/s41 375-022-01620-2.
7. Park K, Kwon SH. Monoclonal gammopathy of renal significance from the perspective of nephrologists. Blood Res. 2024; 59 (1): 28. doi: 10.1007/s44313-024-00027-5.
8. Du J, Hu Z. Systematic review and meta-analysis of the clinical features of MGRS. BMC Nephrol. 2024; 25 (1): 22. doi: 10.1186/s12882-024 - 03458-5.
9. Pika T, Flodrová P, Polcrová E. Systémová AL amyloidóza – diagnostika a léčba Onkol Rev. 2022; 9 (6): 440–447.
10. Ryšavá R, Merta M, Havrda M, et al. Light chain deposition disease in myeloma multiplex observation of 3 cases: 14th Danube Symposium on Nephrology, Prague, September 3-6, 1998. Aktual Nefrol. 1998; 4 (1): 78.
11. Ščudla, V, Minařík J. Pika T. Nemoc z ukládání lehkých řetězců imunoglobulinu (light chain deposition disease). Vnitř Lék. 2012; 58 (1): 38–43.
12. Minařík J, Tichý T, Pika T, et al. Léčba bortezomibem u pacientů s onemocněním z depozice lehkých řetězců imunoglobulinu. Vnitř. Lék. 2014; 60 (10): 821–826.
13. Honsová E. Diagnóza nemoci z ukládání lehkých řetězců imunoglobulinů (LCDD) v bioptické praxi – editorial. Vnitř Lék. 2012; 58 (1): 7–10.
14. Wohl P, Chadimová M, Engliš M, et al. Nemoc z ukládání lehkých řetězců jako příčina renálního selhání Čas Lék Čes. 1998; 137 (23): 721–724.
15. Merta M, Žabka J, Stejskalová A, et al. Postižení ledvin na podkladě nemoci z ukládání lehkých řetězců. Sbor Lék. 2002; 103 (3): 397–403.
16. Havrda M, Dvořáková JR, Gregora E, et al. Nemoc lehkých řetězců (LCDD). Postgrad Nefrol. 2011; 9 (6): 97–98.
17. Flodrová P, Pika T, Flodr P. AL amyloidóza v obrazech. Transfuze Hematol Dnes. 2014; 20 (3): 76–80.
18. Pika T. Diagnostika a léčba systémové AL amyloidózy: Doporučení vypracovaná Českou myelomovou skupinou (CMG), Myelomovou sekcí České hematologické společnosti ČLS JEP. Transfuze Hematol Dnes. 2022; 28 (Suppl 1): 6–40.
19. Pika T. Diagnostika a léčba systémové AL amyloidózy. Transfuze Hematol Dnes. 2019; 25 (Suppl 1): 37–71.
20. Chyra Z, Pika T, Jelínek T, et al. Hereditární amyloidózy – etiologie, klinický obraz a léčba. Transfuze Hematol Dnes. 2015; 21 (4): 184–192.
21. Pika T, Lochman P, Minařík J, et al. Význam stanovení sérových hladin volných lehkých řetězců imunoglobulinu u AL amyloidózy. Transfuze Hematol Dnes. 2013; 19 (3): 134–138.
22. Flodr P, Adam Z, Navrátilová M et al. Poškození způsobená depozity monoklonálního imunoglobulinu typu IgM a lehkými řetězci u Waldenströmovy makroglobulinémie – popis případu a přehled literatury. Transfuze Hematol Dnes. 2024; 30 (2): 99–111.
23. Flodr P, Minařík J, Flodrová P, et al. Plasma cell dyscrasias and bone marrow microenvironment. Transfuze Hematol Dnes. 2016; 22 (Suppl 1): 7–8.
24. Minařík J, Hrbek J, Mysliveček M, et al. Racionální algoritmus zobrazovacích vyšetření u mnohočetného myelomu v podmínkách České republiky. Transfuze Hematol Dnes. 2015; 21 (4): 200–205.
25. Navrátilová M, Flodrová P, Holub B, et al. B-buněčné nehodgkinské lymfomy asociované s amyloidózou. Transfuze Hematol Dnes. 2022; 28 (Suppl 2): 61.
26. Herdman RC, Hong R, Michael AF, et al. Light chain distribution in immune deposits on glomeruli of kidneys in human renal disease. J Clin Invest. 1967; 46 (2): 141–146. doi: 10.1172/JCI105516.
27. Seymour AE, Thompson AJ, Smith PS, et al. Kappa light chain glomerulosclerosis in multiple myeloma. Am J Pathol. 1980; 101 (3): 557–580.
28. Randall RE, Williamson Jr WC, Mullinax F, et al. Manifestations of systemic light chain deposition. Am J Med. 1976; 60 (2): 293–299. doi: 10.1016/0002-9343 (76) 90440-x.
29. Cohen C, Joly F, Sibille A, et al. Randall-type monoclonal immunoglobulin deposition disease: new insights into the pathogenesis, diagnosis and management. Diagnostics (Basel). 2021; 11 (3): 420. doi: 10.3390/diagnostics 11030420.
30. Herrera GA, Del Pozo-Yauner L, Teng J, et al. Glomerulopathic light chain-mesangial cell interactions: sortilin-related receptor (SORL1) and signaling. Kidney Int Rep. 2021; 6 (5): 1379–1396. doi: 10.1016/j.ekir.2021.02.014.
31. Ronco P, Plaisier E, Mougenot B, et al. Immunoglobulin light (heavy) -chain deposition disease: from molecular medicine to pathophysiology - driven therapy. Clin J Am Soc Nephrol. 2006; 1 (6): 1342–1350. doi: 10.2215/CJN.01730506.
32. Ryšavá R. Renální selhání u mnohočetného myelomu a jeho léčba. Vnitř Lék. 2020; 66 (7): 425–431.
33. Wang Q, Jiang F, Xu G. The pathogenesis of renal injury and treatment in light chain deposition disease. J Transl Med. 2019; 17 (1): 387. doi: 10.1186/s12967-019-02147-4.
34. Herrera GA, Teng J, Turbat-Herrera EA, et al. Understanding mesangial pathobiology in AL-amyloidosis and monoclonal Ig light chain deposition disease. Kidney Int Rep. 2020; 5 (11): 1870–1893. doi: 10.1016/j.ekir.2020.07.013.
35. Ravichandran S, Law S, Mahmood S, et al. Long-term outcomes in light chain deposition disease-analysis of a UK cohort. Am J Hematol. 2022; 97 (12): E444–E446. doi: 10.1002/ajh.26725.
36. Joly F, Cohen C, Javaugue V, et al. Randall-type monoclonal immunoglobulin deposition disease: novel insights from a nationwide cohort study. Blood. 2019; 133 (6): 576–587. doi: 10.1182/blood-2018-09-872028.
37. Kobayashi A, Takeda A, Shinjo H, et al. Light chain deposition disease recurrence in renal allograft after long-term remission. Nephron. 2023; 147 (Suppl 1): 96–100. doi: 10.1159/000529776.
38. Yue J, Xu F, Zhang Y, et al. Diagnosis of light‑chain deposition disease after renal transplantation: A case report and literature review. Exp Ther Med. 2024; 28 (3): 339. doi: 10.3892/etm.2024.12628.
39. Kuppachi S, Holanda D, Thomas CP. Light chain deposition disease after kidney transplantation with long graft survival: case report. Transplant Proc. 2016; 48 (1): 255–258. doi: 10.1016/j.transproceed.2015.12.009.
40. Wei P, Tao R, Liu Y, et al. Pulmonary light chain deposition disease: a case series and literature review. Ann Transl Med. 2020; 8 (9): 588. doi: 10.21037/atm-20-2708.
41. Pornchai A, Moua T. Dyspnea and cough in a 68-year-old female with light chain deposition disease. Respir Med Case Rep. 2023; 43 : 101839. doi: 10.1016/j.rmcr.2023.101839.
42. Baqir M, Moua T, White D, et al. Pulmonary nodular and cystic light chain deposition disease: A retrospective review of 10 cases. Respir Med. 2020; 164 : 105896. doi: 10.1016/j.rmed.2020.105896.
43. Gonzalez TV, Roden AC, Bartholmai BJ, et al. Pulmonary light chain deposition disease: Case series and review of the literature. Radiol Case Rep. 2024; 19 (9): 3763–3769. doi: 10.1016/j.radcr.2024.05.043.
44. Gandhi M, Pasha SB, Reznicek E, et al. Case of light chain deposition disease leading to acute liver failure and review of literature. Diseases. 2023; 11 (1): 24. doi: 10.3390/diseases11010024.
45. Wei C, Wang M, Li J, et al. Light chain deposition disease presenting with gastrointestinal disorder as primary manifestation: report of two cases and literature review. J Int Med Res. 2024; 52 (3): 3000605241233972. doi: 10.1177/03000605241233972.
46. Tsushima T, Suzuki T, Terao T, et al. Light chain deposition disease involving kidney and liver in a patient with IgD myeloma. BMC Nephrol. 2021; 22 (1): 40. doi: 10.1186/s12882-021-02246-9.
47. Park BE, Jang SY, Park YJ, et al. Cardiomyopathy without amyloid deposit in systemic light chain deposition disease. Korean Circ J. 2024; 54 (4): 221–222. doi: 10.4070/kcj.2024.0022.
48. Nishioka R, Yoshida S, Takamatsu H, et al. Cardiac light-chain deposition disease and hints at diagnosing: a case report. Eur Heart J Case Rep. 2023; 7 (2): ytad049. doi: 10.1093/ehjcr/ytad049.
49. Ryšavá R, Merta M. Indikace k provedení biopsie. Med Pro Praxi. 2008; 5 (5): 200–202.
50. Fuiano G, Mazza G, Comi N, et al. Current indications for renal biopsy: a questionnaire-based survey. Am J Kidney Dis. 2000; 35 (3): 448–457. doi: 10.1016/s0272-6386 (00) 70197-1.
51. Palladini G, Kastritis E, Maurer MS, et a. Daratumumab plus CyBorD for patients with newly diagnosed AL amyloidosis: safety run-in results of ANDROMEDA. Blood. 2020; 136 (1): 71–80. doi: 10.1182/blood.2019004460.
52. Bnaya A, Ganzel C, Shavit L. Successful treatment with daratumumab of a patient with monoclonal lambda light chain disease presenting as nephrotic syndrome and crescentic glomerulonephritis. Acta Haematol. 2024; 147 (5): 598–603. doi: 10.1159/000536283
53. Milani P, Basset M, Curci P et al. Daratumumab in light chain deposition disease: rapid and profound hematologic response preserves kidney function. Blood Adv. 2020; 4 (7): 1321–1324. doi: 10.1182/bloodadvances.2020001553.
54. Kastritis E, Rousakis P, Kostopoulos IV, et al. Consolidation with a short course of daratumumab in patients with AL amyloidosis or light chain deposition disease. Amyloid. 2021; 28 (4): 259–266. doi: 10.1080/13506129.2021.1971192.
55. Cassano Cassano R, Bonadio AG, Del Giudice ML, et al. Light chain deposition disease: pathogenesis, clinical characteristics and treatment strategies. Ann Hematol. 2025; 104 : 2083–2093. doi: 10.1007/s00277-024-05911-9.
56. Wang J, Lv JT, Xiao D, et al. Case report: A case of proliferative glomerulonephritis with monoclonal kappa-light chain deposits treated with daratumumab combination therapy. Front Med (Lausanne). 2024; 11 : 1462199. doi: 10.3389/fmed.2024.1462199.
57. Švabova E, Zieg J, Sukova M, et al. Proliferative glomerulonephritis with monoclonal IgG deposits in an adolescent successfullytreated with daratumumab. Pediatr Nephrol. 2024; 39 : 3455–3457. doi: 10.1007/s004 67-024-06425-2.
58. Roccatello D, Fenoglio R, Sciascia S, et al. CD38 and anti-CD38 monoclonal antibodies in AL amyloidosis: targeting plasma cells and beyond. Int J Mol Sci. 2020; 21 (11): 4129. doi: 10.3390/ijms21114129.
59. Roháľ T, Kment M, Voska L. et al. Léčba monoklonální gamapatie renálního významu s projevy choroby z ukládání lehkých řetězců (Light Chain Deposition Disease – LCDD) v transplantované ledvině. Popis případu a přehled literatury. Vnitř Lék. 2025; 71 (1): E14–E24.
60. Lum EL, Huang E, Bunnapradist S, et al. Allograft rejection precipitated by lenalidomide treatment for multiple myeloma. Am J Kidney Dis. 2017; 69 (5): 701–704. doi: 10.1053/j.ajkd.2016.11.024.
61. Qualls DA, Lewis GD, Sanchorawala V, et al. Orthotopic heart transplant rejection in association with immunomodulatory therapy for AL amyloidosis: A case series and review of the literature. Am J Transplant. 2019; 19 (11): 3185–3190. doi: 10.1111/ajt.15499.
62. Vaxman I, Eaton J, Lee HE, et al. Acute liver rejection in a multiple myeloma patient treated with lenalidomide. Case Rep Transplant. 2020; 2020 : 8894922. doi: 10.1155/2020/8894922.
63. Walavalkar V, Adey DB, Laszik ZG, et al. Severe renal allograft rejection resulting from lenalidomide therapy for multiple myeloma: case report. Transplant Proc. 2018; 50 (3): 873–876. doi: 10.1016/j.transproceed.2018.01.014.
64. Xie L, Jozwik B, Weeks P, et al. Treatment of multiple myeloma in a heart transplant recipient. Prog Transplant. 2017; 27 (1): 65–68. doi: 10.1177/1526924816679842.
65. Kušnierová P, Zeman D, Michnová O, et al. Poměr volných lehkých řetězců u pacientů s chronickým selháním ledvin. Klin Bioch Metabol. 2020; 28 (4): 144–149.
66. Kušnierová P. Laboratorní diagnostika monoklonálních gamapatií Kušnierová, Pavlína, Vydání první. Ostrava: Ostravská univerzita, 2022. 122 stran.
67. Kušnierová P, Zeman D, Revendová K. et al. Detection of monoclonal free light chains by immunofixation electrophoresis and isoelectric focusing – comparison with the quantitative method of determination. Scand J Clin Labor Inv. 2020; 80 (7): 556–561.
68. Kumar S, Paiva B, Anderson KC, et al. International Myeloma Working Group consensus criteria for response and minimal residual disease assessment in multiple myeloma. Lancet Oncol. 2016; 17: e328–e346. doi: 10.1016/S1470-2045 (16) 30206-6.
69. Awasthi NP, Mishra S, Gupta G, et al. Immunophenotypic characterization of normal and abnormal plasma cells in bone marrow of newly diagnosed multiple myeloma patients. Indian J Pathol Microbiol. 2023; 66 (2): 295–300. doi: 10.4103/ijpm.ijpm_505_21.
70. Leung N, Heybeli C. Kidney transplantation in multiple myeloma and monoclonal gammopathy of renal significance. Semin Nephrol. 2024; 44 (1): 151497. doi: 10.1016/ j.semnephrol.2024.151497.
71. Rajnochová-Bloudíčková S, Novotná A. Transplantace ledviny u pacientů s mnohočetným myelomem: současné možnosti. Vnitř Lék. 2024; 70 (8): 517–521.
72. Fermand JP, Bridoux F, Dispenzieri A, et al. Monoclonal gammopathy of clinical significance: a novel concept with therapeutic implications. Blood. 2018; 132 (14): 1478–1485.
73. Dispenzieri A. Monoclonal gammopathies of clinical significance. Hematol Am Soc Hematol Educ Program. 2020; 2020 (1): 380–388. doi: 10.1182/hematology.2020000122.
74. Wendt R, Sobhani A, Diefenhardt P, et al. An updated comprehensive review on diseases associated with nephrotic syndromes. Biomedicines. 2024; 12 (10): 2259. doi: 10.3390/biomedicines12102259.
PODÍL AUTORŮ NA PŘÍPRAVĚ RUKOPISU
A. T. včas diagnostikoval nefrotický syndrom nejasné etiologie a poslal pacienta na biopsii do FN u svaté Anny panu doktorovi Svojanovskému k provedení biopsie. Připomínkoval text z pohledu nefrologa.
J. S. prováděl biopsii ledviny a podílel se na textu z úhlu pohledu nefrologa a psal text o biopsiích ledvin, které rutinně provádí.
I. S. hodnotila bioptický vzorek z biopsie ledviny a podílela se na textu z úhlu pohledu patologa specializovaného na nefropatologii.
M. B. hodnotil kostní dřen metodou průtokové cytometrie.
Z. A., L. P., M. K., M. Š., I. B. a Z. K. se podíleli na léčbě nemoci tohoto pacienta i na textu z úhlu pohledu hematologů.
Článek vznikl složením pohledů všech spolupracujících lékařů do jednotného textu.
ČESTNÉ PROHLÁŠENÍ
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Doručeno do redakce dne: 31. 1. 2025.
Přijato po recenzi dne: 20. 2. 2025.
prof. MUDr. Zdeněk Adam, CSc.
Interní hematologická a onkologická klinika
LF MU a FN Brno
Jihlavská 20
625 00 Brno Bohunice
e-mail: adam.zdenek@fnbrno.cz
Labels
Haematology Internal medicine Clinical oncology
Article was published inTransfusion and Haematology Today
2026 Issue 1-
All articles in this issue
- Venetoklax – základ neintenzivní cílené léčby akutní myeloidní leukémie
- Akutní myeloidní leukémie – jak se změnil přístup v diagnostice, stratifikaci rizika a možnostech léčby
- Venetoklax plus azacitidin jako přemosťující terapie k alogenní transplantaci krvetvorných buněk u nemocných s akutní myeloidní leukémií
- Co můžeme očekávat od léčby venetoklax + azacitidin (VEN+AZA) u pacientů s akutní myeloidní leukémií (AML) – výsledky studie VIALE-A a post-hoc analýz
- Antimykotická profylaxe u pacientů s akutní myeloidní leukémií léčených venetoklaxem s azacytidinem
- Léčba mnohočetného myelomu s projevy choroby z ukládání lehkých řetězců; kompletní remise s negativitou minimální reziduální nemoci po léčbě daratumumabem, dexametazonem a lenalidomidem – popis případu a přehled literatury
- Súčasný výskyt BCR:: ABL1 pozitívnej chronickej myelocytovej leukémie a Ph-negatívneho myeloproliferatívneho ochorenia
- Zásady účelné hemoterapie. Mezioborové konsensuální stanovisko
- Doporučení Společnosti pro transfuzní lékařství ČLS JEP č. STL_20 Vyšetřování chladových protilátek proti erytrocytům u pacientů před kardiochirurgickou operací v mimotělním oběhu
- 18. Střešovický transfuzní den
- Zanubrutinib čtyřikrát jinak v klinické praxi
- Hodgkinův lymfom – klíčová sdělení z ASH 2025
- Transfusion and Haematology Today
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Zásady účelné hemoterapie. Mezioborové konsensuální stanovisko
- Léčba mnohočetného myelomu s projevy choroby z ukládání lehkých řetězců; kompletní remise s negativitou minimální reziduální nemoci po léčbě daratumumabem, dexametazonem a lenalidomidem – popis případu a přehled literatury
- Akutní myeloidní leukémie – jak se změnil přístup v diagnostice, stratifikaci rizika a možnostech léčby
- 18. Střešovický transfuzní den
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

