-
Medical journals
- Career
Akutní myeloidní leukémie – jak se změnil přístup v diagnostice, stratifikaci rizika a možnostech léčby
Authors: P. Žák
Authors‘ workplace: IV. interní hematologická klinika FN Hradec Králové
Published in: Transfuze Hematol. dnes,32, 2026, No. 1, p. 9-15.
Category: Review/Educational Papers
doi: https://doi.org/10.48095/cctahd202606Overview
K porozumění odlišného biologického chování u akutní myeloidní leukémie (AML) vedly především nové poznatky z molekulární biologie. Na základě molekulárních změn byla upravována klasifikace a diagnostická kritéria tak, aby odrážela biologickou podstatu AML. Přítomnost molekulárních změn umožnila též zpřesnit stanovení prognózy AML a sledování léčebné odpovědi. Současně s tím dochází k rozvoji cílené terapie. Nejvýznamnějšími léčivy z této skupiny jsou inhibitor proteinu bcl-2 (venetoklax), inhibitory FLT3 mutace a inhibitory IDH1/2. Léčba AML je komplikovaná, což zdůrazňuje potřebu odborných znalostí, aby bylo možné poskytnout optimální terapii a dosáhnout optimálních výsledků. Různé podtypy AML vyžadují odlišný léčebný přístup. V tomto přehledu jsou shrnuty důležité změny zahrnující diagnostiku, význam precizního molekulárně genetického vyšetření a nové léčebné směry.
Klíčová slova:
venetoklax – AML (diagnóza) – AML (terapie) – MRD (měřitelná reziduální choroba) u AML
ÚVOD
Akutní myeloidní leukémie (AML) je onemocnění vznikající v důsledku proliferace klonálních hematopoetických buněk. AML je nejčastěji diagnostikována u starších osob s mediánem věku 66–68 let. Zavedení řady nových léků vedlo ke zlepšení léčebných výsledků, přesto jsou výsledky léčby neuspokojivé. Odhadované 5leté přežití se pohybuje okolo 30–35 % (u mladších pacientů se pohybuje okolo 50 %, u starších pacientů nad 60 let je 5leté přežití méně než 20 %).
Molekulárně genetické metody pomohly přesněji diferencovat podjednotky AML a současně došlo k lepšímu pochopení odlišného biologického chování AML. Dobrá dostupnost molekulárně genetických metod umožnila implementaci těchto nálezů do diagnostiky, stratifikaci rizika AML a hledání nových léčebných cílů. Od roku 2017 bylo schváleno 12 nových léků nebo kombinovaných režimů pro léčbu AML. V tomto sdělení je podán přehled nejvýznamnějších změn, které se v diagnostice, stanovení prognostického rizika a vedení léčby udály.
KLASIFIKACE AML
V současné době jsou užívány klasifikační systémy 5. vydání WHO klasifikace, ICC (mezinárodní konsenzuální kritéria) a dále ELN kritéria AML [1–4]. Podstatou obou klasifikačních systémů je integrace nových poznatků z molekulární biologie a biologického chování AML. Pro definici AML je stanovena nižší prahová hodnota počtu blastů na ≥ 10 % v kostní dřeni při přítomnosti mutací definujících AML – AML1-ETO (RUNX1:: RUNX1T1) a CBFb:: MYH11 a nově přítomností mutací NPM1 u myelodysplastických syndromů. Pro AML s BCR:: ABL i nadále platí podmínka více jak 20 % blastů v kostní dřeni, aby byla odlišena akcelerovaná fáze CML. Dále byla nově zavedena kategorie MDS/AML zahrnující pacienty s 10–19 % blastů v kostní dřeni nebo periferní krvi, která je biologicky podobná AML [5]. Při stanovení diagnózy je nezbytné provést stanovení molekulárně genetických změn a rozřazení do samostatných skupin.
STRATIFIKACE RIZIKA AML NA ZÁKLADĚ MOLEKULÁRNÍCH ZMĚN
Molekulárně-genetické vyšetření implementované do klasifikace AML umožnilo vyhodnotit efekt léčby u lépe definované skupiny a současně je umožněna přesnější prognostická stratifikace. Nejdůležitější poznatky jsou tyto:
- Alelický poměr tandemové duplikace FLT3 se již nezohledňuje při klasifikaci rizika a řadí se do středně rizikové skupiny i přes přítomnost mutace NPM1 [6].
- AML s mutacemi, které souvisejí s MDS (ASXL1, BCOR1, EZH2, RUNX1, SF3B1, SRSF2, STAG2, U2AF1 a ZRSR2), je dle ICC i ELN definována jako riziková skupina. Pokud je však současně přítomna mutace s příznivým rizikem, výše uvedené mutace nepředstavují vyšší riziko [7,8].
- AML s NPM1 a nepříznivými genetickými mutacemi je klasifikována jako nepříznivé riziko [9,10].
- Nepříznivé riziko nese t (3q26.2; v) zahrnující gen MECOM a t (8; 16) (p11; p13) asociovaná s KAT6A:: CREBB [11].
- AML s hyperploidním karyotypem nejsou považovány za ekvivalent komplexního karyotypu a jsou vyřazeny z nepříznivé rizikové skupiny [12].
- AML nebo AML/MDS s mutací TP53 je častěji spojena s komplexními změnami karyotypu a pro vysoce nepříznivý průběh jsou samostatnou podskupinou.
Nový pohled přinesly i dlouhodobé výsledky studie VIALE-A, kde bylo u pacientů léčených azacytidinem (AZA) a venetoklaxem (VEN) využito 4genové rizikové skóre, které stratifikovalo pacienty do 3 skupin dle léčebné odpovědi. Pacienti s TP53 mutací vykazovali velmi nízkou nebo jen krátkodobou léčebnou odpověď. Pacienti bez TP53, ale s mutacemi FLT3-ITD, NRAS nebo KRAS měli odpověď lepší. Velmi dobrou léčebnou odpověď vykazovali ti, kteří neměli žádnou z těchto mutací [12]. V dalších retrospektivních analýzách byly použity podobné nebo podrobnější modely, které závěry této stratifikace potvrdily [13]. Tyto závěry odráží doporučení ELN pro molekulárně genetickou stratifikaci AML při použití nízce intenzivních režimů (tab. 1) [14].
Table 1. ELN molekulárně genetická riziková stratifi kace akutní myeloidní leukémie u nízce intenzivních režimů VEN+AZA [14]. ![ELN molekulárně genetická riziková stratifi kace akutní myeloidní leukémie u nízce intenzivních režimů VEN+AZA [14].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/859972278767129d5a069974079c992c.png)
HODNOCENÍ LÉČEBNÉ ODPOVĚDI
Nadále je užívána definice kompletní remise (CR), kompletní remise s neúplnou normalizací parametrů KO (CRi), parciální remise (PR) a stav bez leukémie v kostní dřeni (MLFS). Kategorie CR s částečným zotavením (CRh) se příliš neujala a je využívána ve studijních protokolech. CRh je definována počtem blastů v kostní dřeni < 5 %, absencí blastů v obvodové krvi, nepřítomností extramedulárního onemocnění a částečnou normalizací parametrů krevního obrazu (ANC ≥ 500/μl a trombocyty ≥ 50 000/μl). Zásadní význam pro posouzení léčebné odpovědi a stanovení rizika relapsu je jednotné posouzení měřitelné reziduální choroby (MRD). Do ELN klasifikace byly integrovány popis a podmínky hodnocení MRD. Je tedy vhodné popsat dosaženou odpověď jako CRMRD– nebo CRMRD+. K upřesnění by měla být uvedena metoda stanovení MRD (vícebarevná průtoková cytometrie – MFC, PCR, NGS), protože každá má odlišnou citlivost pro vybranou metodu a monitorovaný gen. U MFC je MRD negativita dosahovaná již při hodnotách < 10–3 až 10–4 pro blasty s určeným LAIP, u real time PCR je dosahovaná citlivost < 10–4 až 10–6 a u NGS hodnota < 10–3 až 10–5. U molekulárních metod je nezbytné vycházet nejméně ze 2 měření [3,6].
Image 1. Algoritmus léčby pro dnAML ve věku 60–75 let, kteří jsou vhodní pro intenzivní terapii. 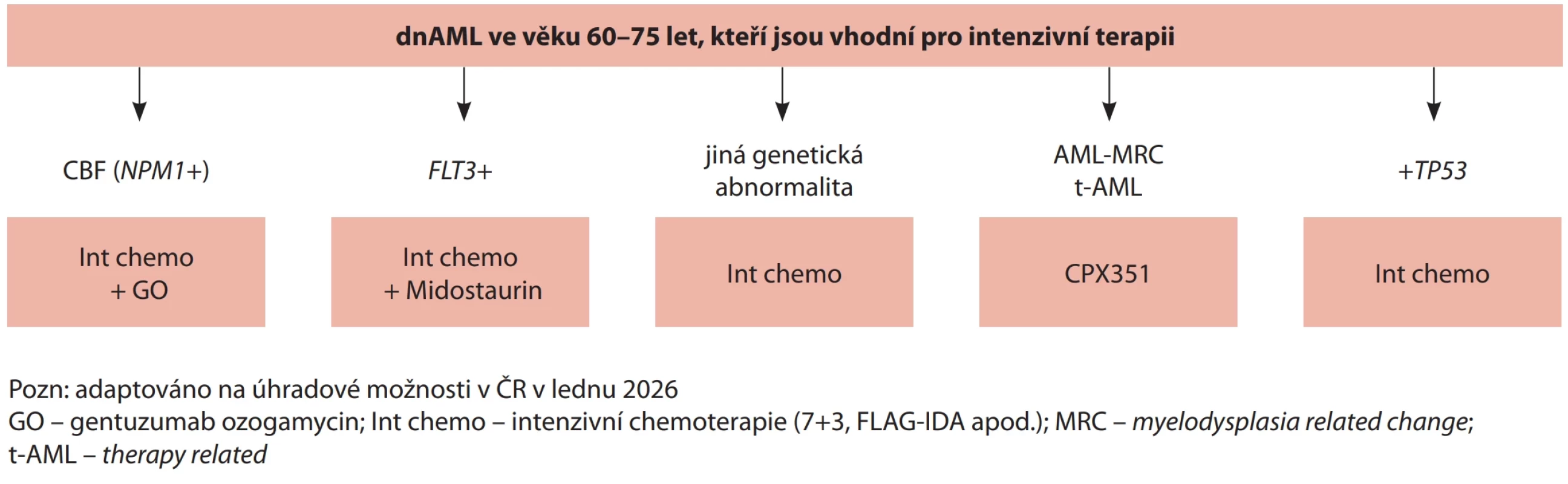
Image 2. Algoritmus léčby pro dnAML nevhodných pro intenzivní terapii nebo ve věku ≥ 75 let. 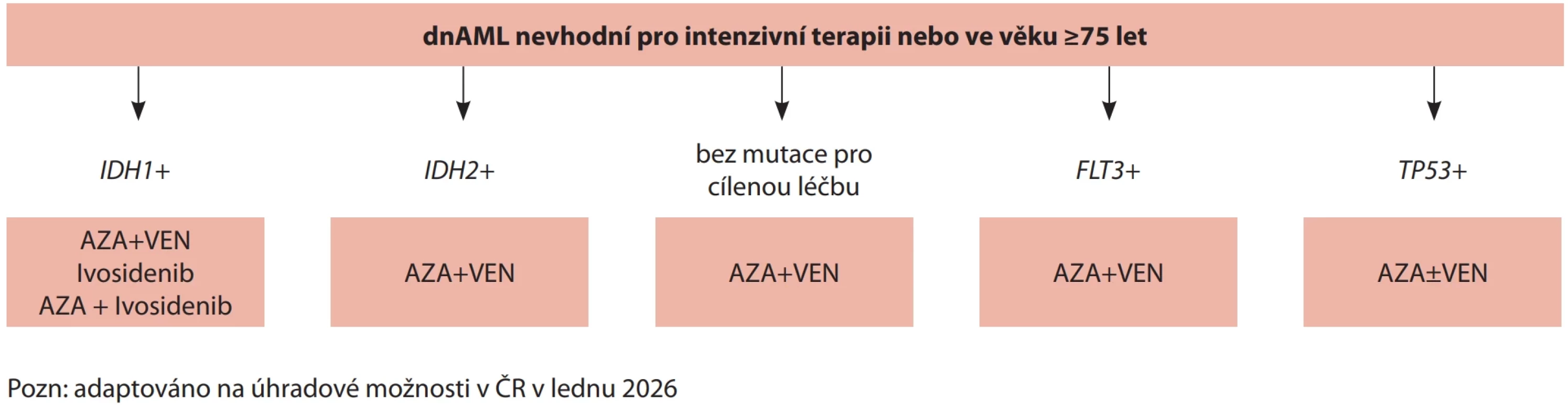
VÝZNAM MĚŘITELNÉ REZIDUÁLNÍ CHOROBY (MRD) PO LÉČBĚ
Hodnota MRD, s výjimkou mutací v DNMT3A, TET2 a ASXL1, které často provázejí klonální hematopoézu, je významným nezávislým prognostickým ukazatelem, a to jak při měření vícebarevnou průtokovou cytometrií, PCR a NGS [14]. U pacientů, kteří dosáhli MRD negativity je významně nižší riziko relapsu a delší celkové přežití (OS). Měření MRD pomocí citlivých technik se tak stalo důležitou informací při hodnocení hloubky léčebné odpovědi a pro prognózu rizika relapsu AML [4]. Otman et al. prokázali u pacientů s mutací NPM1 léčených hypometylační látkou (HMA) + VEN, že negativita NPM1 po 4 cyklech léčby byla spojena s lepším OS a EFS. Po 2letém hodnocení ve skupině s MRD negativním nálezem přežívalo 84 vs. 46 % MRD pozitivních pacientů a období bez relapsu (EFS) bylo 84 vs. 20 % [15].
SOUČASNÝ LÉČEBNÝ PŘÍSTUP U NOVĚ DIAGNOSTIKOVANÉ AML (dnAML)
V posledních 5 letech se výrazně změnil přístup k léčbě pacientů s AML. V předchozím textu byla popsaná diagnostika opřená o informace molekulárně genetických změn, která umožňuje správné zařazení AML a podání cílené léčby. Přes dostupnost molekulárních metod vyžadují tato vyšetření dostatek času (obvykle 2–10 dnů). Studie skupiny SAL prokázala, že vyčkání na výsledky genetického vyšetření nemělo vliv na celkové přežití [16]. Vyčkávat na výsledek není možné u stavů s extenzivní proliferací blastů, kde je nezbytná leukoredukční terapie leukaferézou, hydroxyureou nebo aplikací AraC z důvodu leukostázy. Naopak se znalostí imunologického a molekulárně genetického profilu lze blastické elementy zařadit a určit optimální terapii a marker pro sledování MRD. Druhou otázkou je, který pacient je vhodný k intenzivní a neintenzivní léčbě. I neintenzivní terapie má při použití HMA+VEN významný kurativní potenciál s navozením vysokého procenta CR a MRD negativity.
Základními limitacemi nadále zůstávají biologický stav pacienta, přidružená onemocnění a většinou věk nad 75 let. Z tohoto pohledu je nejvíce problematickou skupinou pacient ve věku 60–75 let, kde jsou někteří pacienti schopní podstoupit intenzivní léčbu. Před určením vhodné léčby je nezbytné vyhodnotit přidružená interní onemocnění, poznat rodinné a sociální zázemí a schopnost spolupráce pacienta. Poté je možné doporučit intenzivní či ne-intenzivní léčebný přístup. Pro skupinu dnAML 60–75 a > 75 let jsou na schématu 1 a 2 uvedeny nejčastěji používané algoritmy indukční léčby [17].
AKTUALIZACE TÝKAJÍCÍ SE INDUKČNÍ INTENZIVNÍ TERAPIE DNAML
Od roku 1973 se stal základem léčby režim 7+3 s použitím cytarabinu v dávce 100–200 mg/m2 a daunorubicinu v dávce 60–90 mg/m2 [18]. Zde je vhodné zdůraznit, že nebyl prokázán přínos zvýšené dávky daunorubicinu 90 mg/m2 v první indukci a současně nebyl prokázán benefit druhé indukce u pacientů v CR po 1. indukci [19]. Nové režimy zahrnující purinový nukleosid CLAG-M nebo FLAG-Ida dosahují vyššího počtu CR proti 3+7, ale je přítomna vyšší toxicita léčby [2,20,21]. Nadějným přístupem se jeví kombinace těchto režimů s venetoklaxem, kde probíhají randomizované studie (CAVEAT, FLAG+IDA+VEN: NCT03214562) [22].
Monoklonální protilátka anti CD33 – gentuzumab ozogamycin (GO, Mylotarg) je látka již delší dobu známá a při původním hodnocení musela být pro hepatotoxicitu z léčby AML vyřazena [23]. Ve studii ALFA 0701, kde byl GO podáván frakcionovaně a ve snížené dávce, bylo dosaženo delší OS a lepší EFS proti 7+3 bez GO [24]. Další pozitivní výsledky vycházejí ze studie AML-MRC15 a 16 [25,26]. Podrobnější post-hoc analýzy ukazují, že zásadní profit z kombinované léčby 7+3+GO nebo /FLAG-Ida + GO je u pacientů s příznivým cytogenetickým profilem. Přidání vedlo k prodloužení EFS také u AML NPM1+/FLT3-ITD negativní (nemutovaný; wt). Přidání GO má nejlepší výsledky především ve skupině pacientů s příznivým cytogenetickým rizikem [27]. U středního cytogenetického rizika je nutné zvážit celkovou terapeutickou rozvahu vzhledem k efektivitě, ceně a možnému hepatotoxickému vlivu, který může limitovat následné provedení alogenní transplantace hematopoetických buněk (HSCT).
Inhibitory FLT3 I. a II. generace byly zavedeny do intenzivní léčby u pacientů s AML s FLT3-ITD mutací nebo FLT3-TKD mutací. Studie RATIFY prokázala přínos midostaurinu (Mido, Rydapt) v OS u AML pacientů ve věku 18–59 let i 60–70 let (medián OS 22,7 vs. 8,4 měsíce; p = 0,01) [28,29]. Quizartinib (Vanflyta) je FLT3 inhibitor II. generace. Studie QUANTUM FIRST prokázala u pacientů s dnAML FLT3-ITD mutací do 60 let zlepšení OS proti 7+3 (medián 32 vs. 15 měsíců; p = 0,03) [30]. Quizartinib prokázal účinnost pro udržovací terapii u pacientů, kteří nepodstoupili alogenní transplantaci. Gilteritinib (GIL, Xospata) je specifičtější inhibitor FLT3 ve srovnání s midostaurinem. Na základě studie ADMIRAL byl schválen pro léčbu R/R AML FLT3+ AML [31]. Zařazení GIL a crenolanibu do indukční léčby dnAML je předmětem probíhajících studií [32].
CPX 351 je lipozomální formulace daunorubicinu a cytarabinu. Původní schválení FDA pro t-AML (therapy related) a AML-MRC (myelodysplasia related changes) bylo určeno pro věkovou skupinu 60–75 let a proběhlo již v roce 2017. Míra dosažené CR a OS byla vyšší u pacientů léčených CPX-351 (37 vs. 26 %; p = 0,02; medián OS 9,3 vs. 6 měsíců). Významné je zjištění, že u pacientů, kteří podstoupili alogenní HSCT po předchozí léčbě CPX-351, bylo významně delší OS ve srovnání s kontrolní skupinou léčených před transplantací režimem 3+7 nebo FLAG Ida. Bohužel výsledky u AML s TP53 mutací jsou stejné jako po terapii 7+3 [33]. Při výběru léčby pro skupinu dnAML (t-AML a AML-MRC) ve věku 60–75 let je nezbytné pečlivě vyhodnotit kondici pacienta. U fit pacientů je podání CPX-351 vhodné, ale u unfit je vhodnější neintenzivní terapie s hypometylační látkou (HMA) a venetoklaxem (VEN). Multicentrická retrospektivní studie hodnotila výsledky pacientů s AML rozčleněných dle WHO klasifikace (5. vydání), kteří byli léčeni 3+7 nebo CPX-351 nebo HMA+ VEN. Míra odpovědi byla podobná ve všech léčebných skupinách CR/CRi (56 vs. 44 vs. 56 %; p = 0,22), medián OS byl též srovnatelný (16 vs. 11 vs. 15 měsícům; p = 0,54) a i u pacientů konsolidovaných transplantační terapií byl 2letý OS 64 vs. 60 vs. 74 %; p = 0,55). V multivariantní regresní analýze byla kombinace HMA+VEN proti CPX351 prokázána jako benefitní. Dalšími důležitými faktory jsou i míra infekcí u CPX351 vs. HMA+VEN (51 vs. 20 %; p < 0,0001) a délka hospitalizace u CPX-351 (41 vs. 15 dní) [34].
Venetoklax (VEN) je schválen v kombinaci s HMA nebo LDAC pro pacienty starší 75 let nebo u mladších z důvodu nezpůsobilosti pro intenzivní terapii. Kombinace intenzivních režimů s VEN vykazuje synergický efekt [21,35]. Bezpečnost a účinnost VEN byla prokázána u režimu FLAG-Ida s VEN vs FLAG-Ida u pacientů s nově diagnostikovanou AML (ndAML), kdy bylo dosaženo CR (CR, CRi, CRh) u 89 % [21]. V další sledované skupině 33 pacientů ve věku 18–60 let byla kombinace 3+7 s VEN opět vysoce efektivní (dosaženo 94 % CR, z toho 82 % CRMRD–) [36].AKTUALIZACE TÝKAJÍCÍ SE NEINTENZIVNÍ TERAPIE U DNAML
Léčebné možnosti u starších nebo závažně komorbidních pacientů byly značně omezené z důvodu věku a přidružených onemocnění. Ve věkové skupině nad 60 let jsou častěji přítomny nepříznivé molekulárně genetické změny. Výsledky léčby hypomethylačními látkami (HMA – azacytidinem (AZA) nebo decitabinem (DEC)) nebo nízkými dávkami AraC (LDAC) jsou neuspokojivé. Zlepšení OS v této skupině pacientů přinesla kombinace synergicky fungujícího venetoklaxu s azacytidinem.
- HMA+VEN – přidání VEN k AZA vedlo ve studii VIALE-A (de novo AML > 75 let nebo u mladších pacientů s komorbiditami) ke zlepšení odpovědi a prodloužení OS ve skupině VEN+AZA vs monoterapie AZA (CR 66,4 vs. 28,3 %; p < 0,001 s mediánem OS 14,7 vs. 9,7 měsíce; p < 0,001) [37]. Při kombinaci VEN a LDAC ve studii VIALE-C nebylo primárního cíle dosaženo, ale při 6měsíčním hodnocení byla zaznamenána výhoda v OS ve skupině VEN+LDAC vs monoterapie LDAC (8,4 vs. 4,1 měsíce; p = 0,04) [38,39]. Studie neprokázala výhodu kombinace VEN+AZA u skupiny mladších 75 let, kteří byli do studie zařazeni na základě významné komorbidity.
- Nabízí se otázka srovnání, jakou léčbu zvolit u mladších pacientů bez komorbidit. Zda HMA + VEN, nebo 7+3 / FLAG-IDA, nebo 7+3/FLAG-Ida + VEN? Je skutečností, že méně toxická léčba s režimem HMA+VEN může vést k dobré léčebné odpovědi s menší toxicitou a umožní tak alogenní transplantaci [40]. Dosud však nejsou k dispozici výsledky randomizovaných studií s dlouhodobým prospektivním srovnáním HMA+VEN a klasické intenzivní chemoterapie. Určité informace poskytuje evropská multicentrická studie pro dnAML > 60 let, kdy byl k režimu 7+3 přidán 10denní DEC. Ve sledovaných parametrech OS, EFS, CR a počtu alogenních transplantací nebyl prokázán statisticky významný benefit [41,42].
- Ve studii VIALE-A u vysoce rizikových AML s mutací TP53 vedlo přidání VEN k HMA k vyšší míře dosažení CR (55,3 vs. 0 %), ale nebyl zaznamenán přínos pro celkové přežití. U vysoce rizikových AML s mutací TP53 a monocytární diferenciací je odezva léčby VEN + HMA krátká [43–45].
- Inhibitory IDH
- Inhibitor IDH1 (IVO, ivosidenib, Tibsovo) je užíván jako monoterapie u pacientů nevhodných k intenzivní terapii nebo R/R AML IDH1+ AML. Ve studii AGILE, kde byl kombinován IVO s AZA byly dosaženy výrazně lepší výsledky proti samotnému AZA (střední OS 24 vs. 7,9 měsíce). Proto byla tato kombinace schválena FDA pro léčbu pacientů starších 75 let nebo s komorbiditami [46].
- Inhibitor IDH2 (ENA, enasidenib, Idhifa) byl zkoušen v kombinaci s AZA. Přestože bylo dosaženo až 54 % CR vs. 12 % CR u AZA, celkové přežití bylo srovnatelné s režimy HMA+VEN. Problémem IDH inhibitorů byl také závažně probíhající diferenciační syndrom [47].
NOVÉ POSTUPY V LÉČBĚ dnAML
Trojkombinace v neintezivní terapii dnAML („triplet“ terapie)
U pacientů s dnAML FLT3+ mutací je v klinických studiích hodnocena kombinace FLT3 blokátoru s VEN+AZA. Daver a Short prezentovali vynikající průběžné výsledky studie NCT04140487, kdy byli pacienti s dnAML FLT3 mutací léčeni kombinací VEN+AZA+GIL. U 96 % léčených bylo dosažena CR/CRi a u 65 % MRD negativita. Při sledování v 18 měsících bylo OS 72 % a RFS 71 % [48]. Nadějné výsledky byly prezentovány i dalšími autory. V současné době probíhá randomizovaná klinická studie MyeloMATCH
ECOG-ACRIN MM20A-EA02 pro dnAML FLT3-ITD+/TKD+. Protokol odlišuje pacienty dle věku (< 70 let a ≥ 70 let) a řadí je do 3 skupin: VEN+AZA nebo VEN+AZA+GIL nebo VEN+AZA+ FLT3 inhibitor jiný než GIL [49].
Další potenciální oblastí pro triple terapii jsou pacienti dnAML s IDH1/IDH2 mutací. Ve skupině pacientů nevhodných k intenzivní terapii byl u pacientů s IDH1 mutací ke kombinaci VEN+AZA přidán ivosidenib a u IDH2 enasidenib. Tato kombinace je vysoce účinná – u IDH1 mutovaných dnAML bylo dosaženo i 86 % CR/CRi (81 % MRD neg.) a IDH2 CR/CRi 100 % (MRD 95 % neg). Při sledování v 18 měsících nebyl dosažen medián v OS a EFS.
Inhibitory meninu
Jedná se o zcela nový přístup v léčbě AML, u kterých je prokázána mutace NPM1 nebo KMT2Ar. Menin je jaderný stavební protein, který zasahuje do transkripčních mechanizmů a regulace chromatinu. U výše uvedených mutací navozuje poruchy epigenetické regulace a navozuje rozvoj AML. V současnosti jsou intenzivně zkoumány čtyři inhibitory – revumenib, ziftomenib, bleximenib a enzomenib.
ZÁVĚR – KAM SMĚŘUJE LÉČBA AML
Přístup k péči o pacienty s AML prochází dramatickým vývojem nejen v diagnostice, klasifikaci, hodnocení léčebné odpovědi, ale především v léčebném přístupu. Cílem léčby je dosažení jak kompletní remise, tak negativity MRD, a to co nejšetrnější cestou. Nová skupina léků kombinujících hypometylační látky a VEN se ukázala jako vysoce efektivní a méně toxická. Tím byla otevřena možnost léčby pacientů vyššího věku nebo pacientů se závažnými přidruženými chorobami. Další vývoj bude směřovat ke srovnání významu intenzivní a neintenzivní terapie a dále k hodnocení významu kombinovaných režimů jak při intenzivní léčbě (přidání VEN), tak neintenzivní léčbě (triple terapie). Provedení alogenní HSCT má i nadále zásadní roli pro dosažení dlouhodobé odpovědi nebo vyléčení.
Sources
1. Khoury JD, Solary E, Abla O, et al. The 5th Edition of the World Health Organizator Classification of Haematolymphoid Tumours: Myeloid and Histiocytic/Dendritic Neoplasms. Leukemia. 2022; 36 (7): 1703–1719.
2. Arber DA, Orazi A, Hasserjian RP, et al. International Consensus Classification of Myeloid Neoplasms and Acute Leukemia: Integrating Morphological, Clinical, and Genomic Data. Blood. 2022; 140 : 1200–1228.
3. Döhner H, Wei AH, Appelbaum FR, et al. Diagnosis and Management of AML in Adults: 2022 Recommendations From an International Expert Panel on Behalf of the ELN. Blood. 2022; 140 (12): 1345–1377.
4. Short NJ, Zhou S, Fu C, et al. Association of Measurable Residual Disease With Survival Outcomes in Patients With Acute Myeloid Leukemia. JAMA Oncol. 2020; 6 (12): 1890.
5. Estey E, Hasserjian RP, Döhner H. Distinguishing AML From MDS: A Fixed Blast Percentage May No Longer Be Optimal. Blood. 2022; 139 (3): 323–332.
6. Heuser M, Freeman SD, Ossenkoppele GJ, et al. 2021 Update on MRD in Acute Myeloid Leukemia: A Consensus Document From the European LeukemiaNet MRD Working Party. Blood. 2021; 138 (26): 2753–2767.
7. Papaemmanuil E, Gerstung M, Bullinger L, et al. Genomic Classification and Prognosis in Acute Myeloid Leukemia. New Engl J Med. 2016; 374 (23): 2209–2221.
8. Lindsley RC, Mar BG, Mazzola F, et al. Acute Myeloid Leukemia Ontogeny Is Defined by Distinct Somatic Mutations. Blood. 2015; 125 (9): 1367–1376.
9. Angenendt L, Röllig C, Montesinos P, et al. Chromosomal Abnormalities and Prognosis in NPM1−Mutated Acute Myeloid Leukemia: A Pooled Analysis of Individual Patient Data From Nine International Cohorts. J Clin Oncol. 2019; 37 (29): 2632–2642.
10. Chan O, Al Ali N, Tashkandi H, et al. Mutations Highly Specific for Secondary AML Are Associated With Poor Outcomes in ELN Favorable Risk NPM1-Mutated AML. Blood Adv. 2024; 8 (5): 1075–1083.
11. Kayser S, Hills RK, Langova R, et al. Characteristics and Outcome of Patients With Acute Myeloid Leukaemia and t (8; 16) (p11; p13): Results From an International Collaborative Study. Br J Haematol. 2021; 192 (5): 832–842.
12. Döhner H, Pratz RW, DiNardo CD, et al. Genetic Risk Stratification and Outcomes Among Treatment - Naive Patients With AML Treated With Venetoclax and Azacitidine. Blood. 2024; 144 (21): 2211–2222.
13. Bataller A, Bazinet A, DiNardo CD, et al. Prognostic Risk Signature in Patients With Acute Myeloid Leukemia Treated With Hypomethylating Agents and Venetoclax. Blood Adv. 2024; 8 (4): 927–935.
14. Döhner H, DiNardo CD, Appelbaum FR, et al. Genetic risk classification for adults with AML receiving less-intensive therapies: the 2024 ELN recommendations. Blood. 2024; 144 (21): 2169–2173.
15. Othman J, Tiong IS, O‘Nions J, et al. Molecular MRD Is Strongly Prognostic in Patients With NPM1-Mutated AML Receiving Venetoclax-Based Nonintensive Therapy. Blood. 2024; 143 (4): 336–341.
16. Rollig C, Kramer M, Schliemann C, et al. Does Time from Diagnosis to Treatment Affect the Prognosis of Patients with Newly Diagnosed Acute Myeloid Leukemia? Blood. 2020; 136 (7): 823–830.
17. Shimony S, Stahl M, Stone R. Acute Myeloid Leukemia: 2025 Update on Diagnosis, Risk-Stratification, and Management. Am J Hematol. 2025; 100 : 860–891.
18. Yates JW, Wallace HJ, Ellison RR, et al. Cytosine Arabinoside (NSC-63878) and Daunorubicin (NSC-83142) Therapy in Acute Nonlymphocytic Leukemia. Cancer Chemother Rep. 1973; 57 (4): 485–488.
19. Rollig C, Steffen B, Schliemann C, et al. Single or Double Induction With 7 + 3 Containing Standard or High - Dose Daunorubicin for Newly Diagnosed AML: The Randomized DaunoDouble Trial by the Study Alliance Leukemia. J Clin Oncol. 2024; 43 : 65–74.
20. Halpern AB, Othus M, Huebner EH, et al. Phase 1/2 Trial of GCLAM With Dose - Escalated Mitoxantrone for Newly Diagnosed AML or Other High-Grade Myeloid Neoplasms. Leukemia. 2018; 32 (11): 2352–2362.
21. DiNardo CD, Lachowiez CA, Takahashi K, et al. Venetoclax Combined With FLAG - IDA Induction and Consolidation in Newly Diagnosed Acute Myeloid Leukemia. Am J Hematol. 2022; 97 (8): 1035–1043.
22. DiNardo D, Wei-Ying J, Takahashi K, et al. Long Term Results of Venetoclax Combined with FLAG-IDA Induction and Consolidation for Newly Diagnosed and Relapsed or Refractory Acute Myeloid Leukemia. Leukemia. 2025; 39 (4): 854–863.
23. McKoy JM, Angelotta C, Bennett CL, et al. Gemtuzumab Ozogamicin-Associated Sinusoidal Obstructive Syndrome (SOS): An Overview From the Research on Adverse Drug Events and Reports (RADAR) Project. Leukemia Res. 2007; 31 (5): 599–604.
24. Fournier E, Duployez N, Ducourneau B, et al. Mutational Profile and Benefit of Gemtuzumab Ozogamicin in Acute Myeloid Leukemia. Blood. 2020; 135 (8): 542–546.
25. Burnett AK, Hills RK, Milligan D, et al. Identification of Patients With Acute Myeloblastic Leukemia Who Benefit From the Addition of Gemtuzumab Ozogamicin: Results of the MRC AML15 Trial. J Clin Oncol 2011; 29 (4): 369–377.
26. Burnett AK, Russell NH, Hills RK, et al. Addition of Gemtuzumab Ozogamicin to Induction Chemotherapy Improves Survival in Older Patients With Acute Myeloid Leukemia. J Clin Oncol. 2012; 30 (32): 3924–3931.
27. Ronnacker J, Muller PJ, Mikesch JH, et al. Gemtuzumab Ozogamicin in First-Line Treatment of CBF-AML: Insights From a Retrospective Multi-Center Analysis. Leukemia. 2025; 39 : 2174–2180.
28. Stone RM, Mandrekar SJ, Sanford BL, et al. Midostaurin Plus Chemotherapy for Acute Myeloid Leukemia With a FLT3 Mutation. New Engl J Med. 2017; 377 (5): 454–464.
29. Döhner H, Weber D, Krzykalla J, et al. Midostaurin Plus Intensive Chemotherapy for Younger and Older Patients with AML and FLT3 Internal Tandem Duplications, Blood Adv. 2022; 6 (18): 5345–5355.
30. Erba HP, Montesinos P, Kim HJ, et al. Quizartinib Plus Chemotherapy in Newly Diagnosed Patients With FLT3-Internal-Tandem-Duplication-Positive Acute Myeloid Leukaemia (QuANTUM-First): A Randomised, Double-Blind, Placebo-Controlled, Phase 3 Trial. Lancet. 2023; 401 (10388): 1571–1583.
31. Perl AE, Martinelli G, Cortes JE, et al. Gilteritinib or Chemotherapy for Relapsed or Refractory FLT3 - Mutated AML. New Engl J Med. 2019; 381 (18): 1728–1740.
32. Wang ES, Goldberg AD, Tallman M, et al. Crenolanib and Intensive Chemotherapy in Adults With Newly Diagnosed FLT3-Mutated AML. J Clin Oncol. 2024; 42 (15): 1776–1787.
33. Lindsley RC, Gibson CJ, Murdock HM, et al. Genetic Characteristics and Outcomes by Mutation Status in a Phase 3 Study of CPX - 351 Versus 7 + 3 in Older Adults With Newly Diagnosed, High-Risk/Secondary Acute Myeloid Leukemia (AML). Blood. 2019; 134 (Suppl 1): 15.
34. Shimony S, Bewersdorf JP, Shallis RM, et al. Hypomethylating Agents Plus Venetoclax Compared With Intensive Induction Chemotherapy Regimens in Molecularly Defined Secondary AML. Leukemia. 2024; 38 (4): 762–768.
35. Wang H, Mao L, Yang M, et al. Venetoclax Plus 3 + 7 Daunorubicin and Cytarabine Chemotherapy as First - Line Treatment for Adults With Acute Myeloid Leukaemia: A Multicentre, Single-Arm, Phase 2 Trial. Lancet Haematol. 2022; 9 (6): e415–e424.
36. Kadia TM, Reville PK, Borthakur G, et al. Venetoclax Plus Intensive Chemotherapy With Cladribine, Idarubicin, and Cytarabine in Patients With Newly Diagnosed Acute Myeloid Leukaemia or High-Risk Myelodysplastic Syndrome: A Cohort From a Single-Centre, Single-Arm, Phase 2 Trial. Lancet Haematol. 2021; 8 (8): e552–e561.
37. DiNardo CD, Jonas BA, Pullarkat V, et al. Azacitidine and Venetoclax in Previously Untreated Acute Myeloid Leukemia. New Engl J Med. 2020; 383 (7): 617–629.
38. Wei H, Montesinos P, Ivanov V, et al. Venetoclax Plus LDAC for Newly Diagnosed AML Ineligible for Intensive Chemotherapy: A Phase 3 Randomized Placebo-Controlled Trial. Blood. 2020; 135 (24): 2137–2145.
39. Wei AH, Panayiotidis P, Montesinos P, et al. 6-Month Follow-Up of VIALE-C Demonstrates Improved and Durable Efficacy in Patients With Untreated AML Ineligible for Intensive Chemotherapy. Blood Cancer J. 2021; 11 (10): 163.
40. Pollyea DA, Winters A, McMahon C, et al. Venetoclax and Azacitidine Followed by Allogeneic Transplant Results in Excellent Outcomes and May Improve Outcomes Versus Maintenance Therapy Among Newly Diagnosed AML Patients Older Than 60. Bone Marrow Transplant. 2022; 57 (2): 160–166.
41. Lübbert M, Wijermans PW, Kicinski M, et al. 10-Day Decitabine Versus 3 + 7 Chemotherapy Followed by Allografting in Older Patients With Acute Myeloid Leukaemia: An Open-Label, Randomised, Controlled, Phase 3 Trial. Lancet Haematol. 2023; 10 (11): e879–e889.
42. Kim K, Maiti A, Loghavi S, et al. Outcomes of TP53-Mutant Acute Myeloid Leukemia With Decitabine and Venetoclax. Cancer. 2021; 127 (20): 3772–3781.
43. Pei S, Pollyea DA, Gustafson A, et al. Monocytic Subclones Confer Resistance to Venetoclax-Based Therapy in Patients With Acute Myeloid Leukemia. Cancer Disc. 2020; 10 (4): 536–551.
44. DiNardo CD, Tiong IS, Quaglieri A, et al. Molecular Patterns of Response and Treatment Failure After Frontline Venetoclax Combinations in Older Patients With AML. Blood. 2020; 135 (11): 791–803.
45. Shimony S, Garcia JS, Keating J, et al. Molecular Ontogeny Underlies the Benefit of Adding Venetoclax to Hypomethylating Agents in Newly Diagnosed AML Patients. Leukemia. 2024; 38 (7): 1494–1500.
46. Lachowiez CA, Loghavi S, Zeng Z, et al. A Phase Ib/II Study of Ivosidenib With Venetoclax +/ − Azacitidine in IDH1 - Mutated Myeloid Malignancies. Blood Cancer Disc. 2023; 4 (4): 276–293.
47. Venugopal S, Takahashi K, Daver N, et al. Efficacy and Safety of Enasidenib and Azacitidine Combination in Patients With IDH2 Mutated Acute Myeloid Leukemia and Not Eligible for Intensive Chemotherapy. Blood Cancer J. 2022; 12 (1): 10.
48. Daver N, Short NJ, Macaron W, et al. Azacitidine, Venetoclax, and Gilteritinib in Newly Diagnosed and Relapsed or Refractory FLT3-Mutated AML. J Clin Oncol. 2024; 42 (13): 1499–1508.
49. Fathi A, Perl A, Fell G, et al. Results from PARADIGM – a Phase 2 Randomized Multi-Center Study Comparing Azacitidine and Venetoclax to Conventional Induction Chemotherapy for Newly Diagnosed Fit Adults with Acute Myeloid Leukemia. 2024; 146 (Suppl 1): 6.
Prohlášení o konfliktu zájmů
Příprava rukopisu byla iniciována firmou Abbvie. Jiný konflikt zájmů v souvislosti s rukopisem nedeklaruji. Poradenská činnost a konzultační činnost v posledních 5 letech: Swixx Biopharma, Abbvie, Novartis, Takeda, Roche, Astellas, Sanofi, Medac, Pfizer, Sanofi, Sobi, Sysmex
Poděkování
Práce byla podpořena programem Cooperatio – výzkumná oblast hematologie a onkologie a Agenturou pro zdravotnický výzkum MZ ČR č. NU23-03-00562.
Prohlášení o použití AI
AI byla použita k přípravě anglického souhrnu.
Do redakce doručeno dne: 10. 11. 2025.
Přijato po recenzi dne: 1. 2. 2026.
prof. MUDr. Pavel Žák, Ph.D.
IV. interní hematologická klinika
FN HK Sokolská 581
Hradec Králové
LF HK, UK Praha
Šimkova 870 Hradec Králové
e-mail: zak@lfhk.cuni.cz
Labels
Haematology Internal medicine Clinical oncology
Article was published inTransfusion and Haematology Today
2026 Issue 1-
All articles in this issue
- Venetoklax – základ neintenzivní cílené léčby akutní myeloidní leukémie
- Akutní myeloidní leukémie – jak se změnil přístup v diagnostice, stratifikaci rizika a možnostech léčby
- Venetoklax plus azacitidin jako přemosťující terapie k alogenní transplantaci krvetvorných buněk u nemocných s akutní myeloidní leukémií
- Co můžeme očekávat od léčby venetoklax + azacitidin (VEN+AZA) u pacientů s akutní myeloidní leukémií (AML) – výsledky studie VIALE-A a post-hoc analýz
- Antimykotická profylaxe u pacientů s akutní myeloidní leukémií léčených venetoklaxem s azacytidinem
- Léčba mnohočetného myelomu s projevy choroby z ukládání lehkých řetězců; kompletní remise s negativitou minimální reziduální nemoci po léčbě daratumumabem, dexametazonem a lenalidomidem – popis případu a přehled literatury
- Súčasný výskyt BCR:: ABL1 pozitívnej chronickej myelocytovej leukémie a Ph-negatívneho myeloproliferatívneho ochorenia
- Zásady účelné hemoterapie. Mezioborové konsensuální stanovisko
- Doporučení Společnosti pro transfuzní lékařství ČLS JEP č. STL_20 Vyšetřování chladových protilátek proti erytrocytům u pacientů před kardiochirurgickou operací v mimotělním oběhu
- 18. Střešovický transfuzní den
- Zanubrutinib čtyřikrát jinak v klinické praxi
- Hodgkinův lymfom – klíčová sdělení z ASH 2025
- Transfusion and Haematology Today
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Zásady účelné hemoterapie. Mezioborové konsensuální stanovisko
- Léčba mnohočetného myelomu s projevy choroby z ukládání lehkých řetězců; kompletní remise s negativitou minimální reziduální nemoci po léčbě daratumumabem, dexametazonem a lenalidomidem – popis případu a přehled literatury
- Akutní myeloidní leukémie – jak se změnil přístup v diagnostice, stratifikaci rizika a možnostech léčby
- 18. Střešovický transfuzní den
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

