-
Medical journals
- Career
Časná integrace paliativní péče v onkologii
Authors: Marek Sochor
Authors‘ workplace: Komplexní onkologické centrum, Krajská nemocnice Liberec, a. s.
Published in: Čas. Lék. čes. 2018; 157: 13-18
Category: Review Article
Overview
Paliativní péče se v posledním půlstoletí posunula od filozofie péče o umírající k samostatnému oboru, který pečuje o pacienty s nevyléčitelnými chorobami. Pacienti s pokročilými nádory trpí řadou fyzických a psychických symptomů, existenciálním a sociálním distresem a mají omezenou prognózu. V současnosti existují přesvědčivá klinická data o aplikovatelnosti a užitečnosti časné integrace paliativní péče v onkologii zlepšením kvality života, kontrolou symptomů a přežitím. Dnes není otázkou zda, ale kdy, kým a jak nejlépe integrovat paliativní péči do moderní onkologie. Následující přehledový článek uvádí klinická data ze studií, modely spolupráce pro časnou integraci a otázky, které musíme vyřešit v budoucnosti.
Klíčová slova:
onkologie, paliativní péče, časná paliativní péče, symptomy, kvalita životaÚVOD
Nádorová onemocnění představují spolu s kardiovaskulárními nejčastější příčiny nemocnosti a úmrtnosti u dospělých pacientů. Pacienti s pokročilými nádorovými chorobami trpí řadou obtěžujících fyzických a psychických symptomů, mají významné sociální a existenciální komplikace s přímým dopadem na celkovou kvalitu života, léčbu a přežití (1). Tyto problémy se přenášejí i na rodiny a blízké pacientů.
Paliativní péče (PC – palliative care) je definována jako „přístup ke zlepšení kvality života pacientů a jejich rodin čelících problémům spojeným s život ohrožujícími chorobami cestou prevence a úlevy od utrpení pomocí časné identifikace a precizního zhodnocení léčby bolesti a dalších symptomů – fyzických, psychosociálních a spirituálních“ (2). Pro lepší porozumění je vhodné definovat i péči podpůrnou. Jedná se o „poskytování nezbytné péče pacientům s nádory k naplnění jejich informačních, emočních, spirituálních, sociálních a fyzických potřeb během diagnostiky, léčby a sledování, zahrnující podporu zdraví, prevenci, péči o přežívající, paliativní péči a péči o truchlící“. Z této definice vyplývá, že paliativní péče v onkologii je podskupina podpůrné péče u pacientů s pokročilými nádory (3). Paliativní péče tvoří nezbytnou součást onkologie a její co nejčasnější zařazení do celkové péče je velmi doporučované (4). Za posledních 10–15 let byla nashromážděna přesvědčivá data, která prokázala zlepšení kvality života, kontroly symptomů, snížení zátěže pečujících a prodloužení celkového přežití při aplikaci časné paliativní péče (EPC – early palliative care) v onkologii (4–6).
Pacienti s nádorovými chorobami mohou profitovat z časné paliativní péče bez ohledu na prognózu a pokročilost stavu (7). Paliativní péče byla v onkologii poskytována v minulých desetiletích zpravidla v poslední fázi onemocnění po ukončení protinádorové léčby. Byla vnímána jako péče na konci života, podobně jako péče hospicová. Tím pádem neměla řada pacientů přístup k dobře vedené paliativní péči, případně u nich byla zahájena pozdě, bez možnosti mít z ní prospěch. Diskuse o cílech léčby, pacientových preferencích, plánování pokročilé péče a péče na konci života tak byla vedena pozdě nebo vůbec. Důsledkem je častá aplikace chemoterapie v posledních 30 dnech života, velká část onkologických pacientů umírá v nemocnicích, včetně jednotek intenzivní péče, jejich léčba není vedena podle preferencí a představ pacientů a nízká a pozdní je reference do hospicové péče.
Pro moderní onkologii dnes není otázkou, zda do svého kontinua paliativní péči zařadit, ale kdy a kým má být vedena, jaké pacienty referovat, jaké komponenty přinášejí maximální benefit, kde ji realizovat a jaké modely spolupráce paliativních specialistů a onkologů jsou pro pacienta optimální (8–10).
KLINICKÁ DATA PODPORUJÍCÍ EPC
V posledních letech byla provedena řada randomizovaných studií, které podporují časnou aplikaci paliativní péče spolu s onkologickou léčbou v domácím prostředí, za hospitalizace i v ambulantním provozu (11–18).
Studie vedené u hospitalizovaných pacientů vedly zpravidla ke zkrácení a zlevnění hospitalizace, nemocní měli častěji vedené rozhovory o péči na konci života a plánování pokročilé péče, nelišila se celková kvalita života a doba přežití. To vyvolává otázku, zda paliativní péče zahájená u takto pokročilých pacientů má potenciál zlepšit symptomy (19).
Význam domácího multidisciplinárního paliativního týmu na celkovou spokojenost a kontrolu symptomů zkoumali Brumley et al. (20). Do studie zařadili celkem 298 pacientů s předpokládanou prognózou života kratší než 1 rok a recentní hospitalizací nebo vyšetřením na pohotovosti. Pacienti vedení paliativním týmem vykazovali méně hospitalizací, návštěv pohotovostí, častěji umírali doma a byli celkově více spokojeni s péčí. Pozitivní výsledek vedl k zařazení komplexní a specializované domácí paliativní péče do běžné praxe (21, 22).
Ambulance paliativní péče představují spojovací článek mezi nemocnicemi akutní péče a domácí specializovanou paliativní péčí. Jejich roli zkoumaly projekty ENABLE (11, 17). Projekt ENABLE II zahrnoval vstupní edukaci pacientů, měsíční návštěvy v paliativní ambulanci a strukturované telefonické rozhovory vedené sestrami specialistkami paliativní péče. U intervenční skupiny byla významně lepší kvalita života, méně depresivity a symptomové zátěže a delší přežití (14 vs. 8,5 měsíce) (11). Projekt ENABLE III zkoumal optimální načasování paliativní péče po stanovení onkologické diagnózy a jeho výsledky silně podpořily co nejvčasnější zahájení. Jedna skupina pacientů byla do PC zařazena ihned, druhá 3 měsíce od diagnózy. Včasná skupina měla medián přežití 18,3 a pozdní 11,8 měsíce (p = 0,003) (17).
Nejvíce citovanou je studie Temelové et al. (18) vedená u pacientů s nemalobuněčným karcinomem plic. Autoři randomizovali pacienty s metastatickým nemalobuněčným karcinomem k běžné péči a běžné péči s časnou specializovanou PC. Do studie bylo zařazeno 151 pacientů. Po 12 týdnech měli nemocní s EPC signifikantně lepší kvalitu života (p = 0,03), byli méně depresivní a měli lepší náladu (p = 0,01). Pacienti v EPC skupině lépe porozuměli prognóze a méně často volili chemoterapii na konci života (9 vs. 50 %, p = 0,02), což může být faktor odpovědný za delší přežití. I přes menší agresivitu péče (p = 0,05) bylo přežití v intervenční skupině delší (11,6 vs. 8,9 měsíce, p = 0,02). Tato studie prokázala významný přínos EPC, kdy i přes nižší agresivitu léčby měli pacienti delší přežití při zachování vyšší kvality života a lepší nálady.
Předchozí data ukazují na to, že kvalita života a depresivita jsou nezávislé prediktory přežití u pacientů s NSCLC (23). Zajímavé bylo porovnání záznamů paliativních specialistů a onkologů s důrazem na coping a kvalitu života. Z nich vyplynula potřeba dalšího prohlubování paliativních dovedností onkologů pro správné vedení paliativní péče (24).
Zajímavá studie byla vedena v Kanadě Zimmermannovou et al. se zařazením paliativních intervencí u onkologických pacientů hospitalizovaných, ambulantních a v domácím prostředí (14). Po 3 měsících byla u intervenční skupiny významně lepší kvalita života a spokojenost s péčí, po 4 měsících přibyla významně lepší kontrola symptomů.
Bohatá klinická data jednoznačně podporují integraci paliativní péče do onkologické léčby pacientů s pokročilými nádory. Panuje shoda, že by to mělo být co nejdříve, optimální doba načasování je zpravidla do 8 týdnů od zjištění diagnózy, ale liší se podle symptomové zátěže jednotlivých pacientů. V budoucnosti je třeba definovat komponenty paliativní péče přinášející prospěch u konkrétních skupin pacientů. Ze studií je patrné, že nejlépe vycházel týmový multidisciplinární přístup. Dalším podstatným krokem je nastavení spolupráce mezi onkology a paliatry, jejich komunikace, zodpovědnost za pacienty, vedení péče a léčby. V neposlední řadě je otázkou dostupnost specializované PC. Studie prokázaly, že i v onkologických centrech s kvalitně integrovanou PC pouze přibližně 50 % pacientů obdrží specializovanou PC během své léčby (25). Další studie prokázaly limitovanou dostupnost a pozdní referenci k paliativní péči (26). Bariéry jsou na straně onkologů, paliatrů, pacientů a v celkové systémové organizaci a k jejich překonání bylo navrženo několik druhů modelů spolupráce, které se dají aplikovat na různých úrovních péče.
MODELY SPOLUPRÁCE
Na modely paliativní péče v onkologii můžeme nahlížet z hlediska konceptuálního a klinického. Konceptuální modely lze dělit podle časové osy, úrovně PC, spolupráce mezi jednotlivými odbornostmi a systémové organizace.
Model načasování paliativní péče v onkologii se v posledních letech významně změnil. Původní zahájení PC po ukončení protinádorové léčby ustoupilo modelu s postupným prolínáním obou specializací. S tím, jak se snižují možnosti protinádorové léčby, roste význam PC. V komplexním modelu je zahrnuta i hospicová péče a péče o pozůstalé (obr. 1) (27).
Image 1. Možnosti prolínání jednotlivých druhů péče (podle 27) 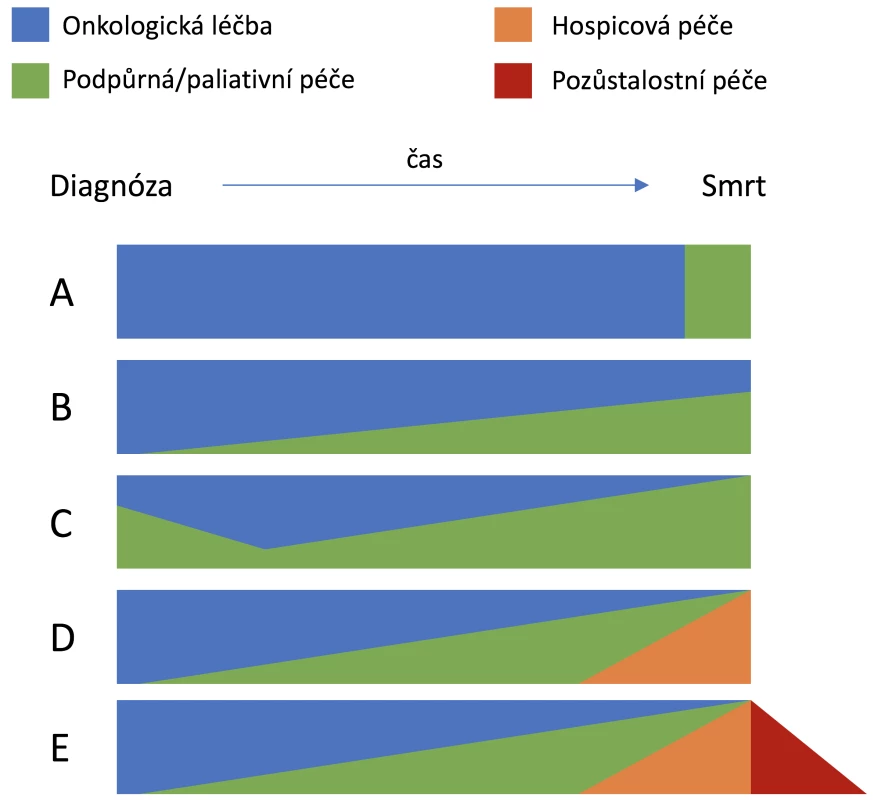
Dělení podle úrovně rozlišuje PC primární, sekundární a terciární (28). Primární je realizována základními odbornostmi, u kterých se klade důraz na zvládnutí základních fyzických a psychických symptomů. Onkologové hrají zásadní roli v kontrole symptomů v časných fázích léčby nádorového onemocnění. Je však nerealistické očekávat plné zohlednění pacientových obtíží s progresí onemocnění a symptomů z důvodů časových, dostupnosti psychosociální podpory, zkušeností a zájmu o PC. Navíc podle studií pacienti preferují, aby jejich onkolog byl více optimistický, věnoval se léčbě nádoru a fyzickým obtížím a méně řešil psychické a existenciální otázky, včetně péče na konci života (29, 30). Sekundární PC je realizována specialisty paliativní péče a je určena pacientům s potřebou komplexní multidisciplinární PC. Specialisté PC v tomto modelu fungují jako konzultanti, a to jak v případě lůžkové, tak ambulantní péče. Terciární PC je pak nejčastěji realizována ve formě paliativních jednotek pro pacienty s vysokou mírou symptomové zátěže a komplexním utrpením (31). Hierarchie úrovně PC vznáší otázky, které se týkají toho, jak široce má být primární PC realizována onkologem, jaká by měla být dostupnost sekundární a terciární PC a jak ji zajistit.
Model dělení podle spolupráce jednotlivých specializací zohledňuje většinu paliativních a podpůrných situací v každodenní onkologické praxi (9). V tomto modelu lze definovat několik podskupin podle řešení pacientových obtíží.
- V sólo modelu je onkolog zodpovědný za onkologickou i paliativní problematiku. V začátcích se jedná o ideální přístup, protože pro pacienta nezvyšuje nároky na kontroly jinými specialisty. S přibývajícími obtížemi nemusejí být komplexní obtíže pacienta zohledněny z důvodu času, znalostí a zkušeností a je nutná komplexní PP, která je optimálně realizována multidisciplinárním specializovaným týmem.
- V kongresovém modelu (congress approach) funguje onkolog jako „dispečer“, odesílá pacienta k jednotlivým specialistům podle jeho obtíží. Tento model klade na pacienta velké nároky, omezuje jeho volný čas a může často vést k jeho zmatení z důvodu různých a někdy si navzájem odporujících doporučení. Tento model obecně pro onkologické pacienty není vhodný a doporučovaný.
- Jako optimální se jeví integrovaný model, kdy onkolog odesílá pacienta do specializované PC časně po zjištění pokročilého nádoru. Onkolog tak kromě vedení protinádorové léčby řeší základní podpůrné a paliativní problémy a má jistotu okamžité spolupráce specialisty PC. Tím pádem se nároky na onkologa nezvyšují a zároveň je tento postup šetrnější pro pacienta, který nemusí být referován dalším specialistům.
Z hlediska systémového řešení jsou dva možné modely (32). Ten první je v současnosti převládající a je závislý na osobě onkologa, který dle své edukace, zaměření a zkušeností rozhoduje o tom, jaký bude další postup. Může být postupováno v sólo, kongresovém i integrovaném modelu, s jejich výhodami a nevýhodami. Druhý model využívá předem definovaná kritéria pro reference do PC, bez ovlivnění osobou lékaře. Bylo publikováno několik různých kritérií pro včasné zahájení PC (33, 34). Modely systémového řešení jsou komplementární k modelu spolupráce specializací, zvýrazňují komplexní zhodnocení a paliativní péči vedenou paliativním týmem a ukazují na to, jak standardizace procesu integrace PC do onkologie zlepšuje její dostupnost.
Výše uvedené konceptuální modely slouží k nastavení komunikace a spolupráce mezi onkology a paliatry z hlediska načasování a role jednotlivých specialistů a rozvoje skutečné integrace PC v onkologii (35). Klinická aplikace zohledňuje jejich principy a může být realizována v ambulantním provozu nebo za hospitalizace. V každém prostředí lze nalézt výhody, nevýhody, bariéry, ale také odlišné klinické výsledky integrace.
Jak již bylo řečeno, paliativní péče se postupně vyvinula z predominantně hospicové péče realizované na konci života přes konzultace a symptomové ovlivnění vysoce nemocných hospitalizovaných pacientů až po v současnosti samostatný obor realizovaný převážně ambulantně v časných fázích nevyléčitelných chorob. Vznik paliativních ambulancí (samostatných nebo navázaných na lůžková zařízení) umožňuje dosáhnout více pacientům v časnějších fázích nemoci na komplexní PC. Onkologie je v současnosti obor, který se o většinu pacientů stará ambulantně, propojení s ambulantní PC je tak zcela logické.
Uvedené klinické studie prokázaly realizovatelnost a významný prospěch ve zlepšení symptomové kontroly, snížení depresivity, zlepšení nálady, kvality života a spokojenosti s léčbou nejenom pro pacienty, ale i rodinné příslušníky. Spolu s tím se významně zlepšila informovanost o prognóze, komunikace o cílech léčby, péče na konci života, snížily se zbytné hospitalizace na akutních lůžkách včetně JIP a návštěv pohotovostí (36). Rozvoj ambulantní PC je dán změnou vnímání paliativní péče, výhodami při jejím včasném zařazení a je patrný ve všech zemích s propracovanou PC (37).
Paliativní péče za hospitalizace je dalším klinickým modelem aplikace PC. Její hlavní výhodou je možnost užší spolupráce, komunikace a koordinace péče mezi onkology a členy paliativního týmu. Dále přináší možnosti pravidelných setkání nad jednotlivými pacienty, časnější přístup k PC a ušetření času onkologa v řešení podpůrné a paliativní problematiky. Mezi hlavní výzvy patří prostorové řešení a možnost umístit členy paliativního týmu do stávajících prostor. Dále, i přes blízkost paliativního týmu, může být pacient na další konzultaci unaven, případně se mu to nehodí z časových důvodů. Mezi nejdůležitější úkoly v tomto modelu se jeví hledání a nastavení optimálního způsobu spolupráce, komunikace, předávání a vedení pacientů.
Pro specialisty paliativní péče a onkology může být zajímavé a přínosné vzdělání i ve druhém oboru, hovoříme tak o paliativní onkologii. Znalost obou specializací, jejich specifik, uvažování a možností je velkou výhodou při rozvíjení integrované paliativní péče v onkologii. Začlenění paliativního onkologa do každého komplexního onkologického centra může podpořit komunikaci, spolupráci a určitou vzájemnou „nakaženost“ obory na cestě k prohloubení a koordinaci správné a komplexní paliativní péče v onkologii (38).
Kombinované paliativně-onkologické multidisciplinární týmy přinášejí další příležitost k integraci PC v onkologii. Jejich role by měla být v komplexním zhodnocení pacienta z hlediska diagnózy, stadia nemoci, potenciálních léčebných možností, ale též předpokládané prognózy, funkčního stavu, symptomové zátěže a jeho preferencí. Takto koncipované multidiscplinární týmy přinášejí možnost lepší komunikace o pacientech, rozšiřují diskusi o adekvátní péči, spouštějí včasnou paliativní péči, podporují pacientův rozhodovací proces a obecně otevírají možnosti pro rozšíření pacientského managementu (39).
BARIÉRY A VÝZVY V INTEGRACI PALIATIVNÍ PÉČE DO ONKOLOGIE A CESTY JEJICH PŘEKONÁNÍ
Všechny výše uvedené studie prokázaly realizovatelnost a benefit současné aplikace časné paliativní péče spolu s onkologickou léčbou u pacientů hospitalizovaných, ambulantních a v domácím prostředí. Dále prokázaly, že benefit je tím větší, čím dříve jsou intervence zahájené a pokud jsou realizované multidisciplinárně. Ve studiích nedošlo u skupiny s EPC ke zhoršení jakéhokoliv parametru. Pro úspěšné zařazení efektivní EPC do klinické praxe je nutné pojmenovat a překonat některé bariéry a omezení, jež s sebou tento zcela nepochybně prospěšný koncept přináší (tab. 1) (40).
Table 1. Bariéry v integraci PC a možnosti jejich překonání 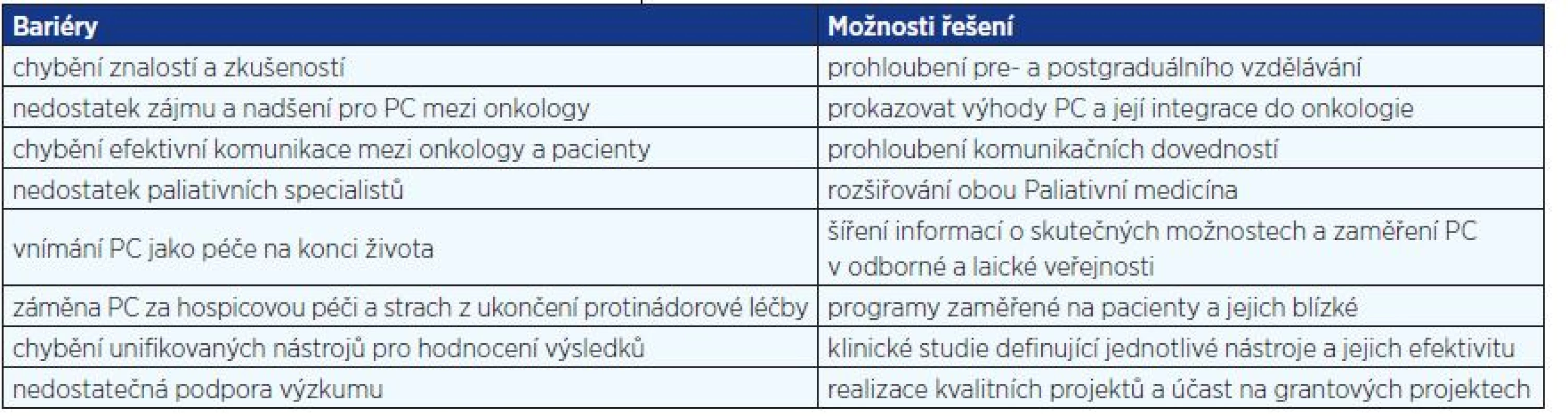
Z hlediska onkologů je hlavní bariérou vnímání paliativní péče jako přístupu, který je realizován až po ukončení onkologické léčby, a dále znalost skutečných možností multidisciplinární PC (41). Tyto překážky lze překonat dobře vedeným pre - i postgraduálním vzděláváním s důrazem na možnosti paliativní péče (42). Další možnou bariérou může být obava z významného navýšení doby nutné ke zvládnutí všech povinností. Tento fakt je důležitý, současná onkologie klade vysoké nároky na znalosti protinádorové léčby, podpůrné terapie a managementu nežádoucích účinků.
Při dobře vedeném a strukturovaném rozhovoru s pacientem lze kvalitně a efektivně vyřešit většinu stesků v relativně krátkém čase. Vhodné je následné sledování v odstupu několika dnů až jednotek týdnů ve formě krátké telefonické konzultace, vedené případně i sestrou-specialistkou paliativní péče. Předpokladem je dobrá úroveň znalosti základního ovlivnění hlavních symptomů pokročilých nádorů, zde je to opět otázka vzdělání a praxe (43–45).
Obecná paliativní péče má své limity, po jejichž dosažení je nutné zařadit do spolupráce specializovanou multidisciplinární PC. Základní paliativní dovednosti, které by měl ovládat každý onkolog, jsou uvedeny v tab. 2.
Table 2. Základní <i>curriculum</i> paliativní péče v onkologii 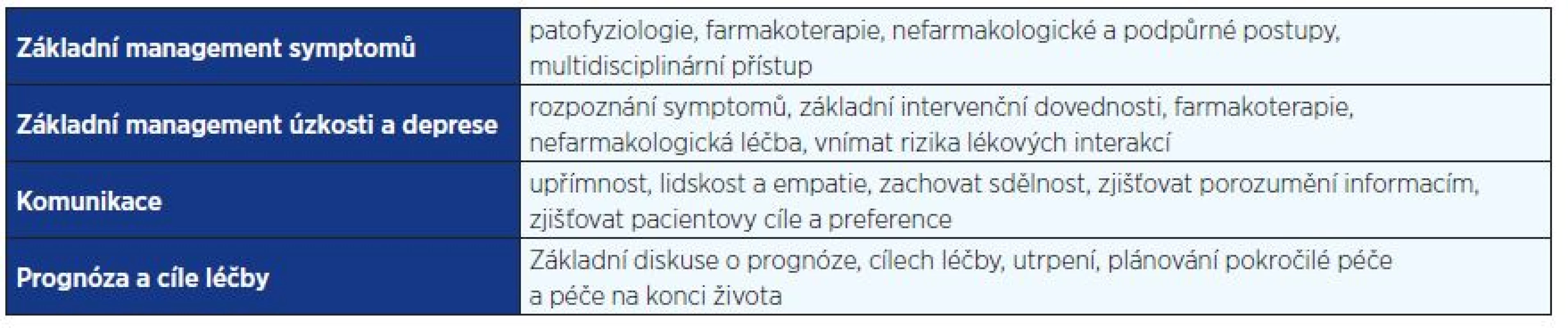
Hlavním nástrojem lékaře pro zvládnutí všech pacientových obtíží v každodenní praxi je efektivní komunikace, v onkologii pokročilých nádorů zvlášť (46). Onkologové se v komunikaci zaměřují primárně na protinádorové léčebné možnosti a jejich nežádoucí účinky. Méně je s pacientem řešena předpokládaná prognóza a možnosti paliativní péče, resp. cíle péče a léčby. Přitom u pacientů s prognózou v jednotkách měsíců u nádorů obtížně léčebně ovlivnitelných (karcinom pankreatu, žaludku, žlučových cest, plic) je přínos chemoterapie nízký nebo vůbec žádný při vysokém riziku komplikací.
Dobrá znalost reálné prognózy a ovlivnitelnosti choroby může pacientovi změnit jeho preference (47). Komunikace o prognóze, cílech léčby, možnostech terapie a paliativní péče není jednorázový krok, jedná se o proces, který je s pacientem veden po celou dobu léčby. Na jeho začátku musí být hlavní informace řečené v jasné a srozumitelné podobě, poskytneme tak pacientovi a jeho rodině delší čas na vyrovnání se s nastalou životní situací a předejdeme těžkým zklamáním s utrpení v dalším průběhu. Existuje řada důkazů o tom, že komunikace o prognóze u pacientů nezhoršuje naději a adherenci k léčbě (48, 49).
Významná bariéra na straně specializované paliativní péče je v nedostatku specialistů. Vzrůstající potřeba a konzultace specializované PC tento nedostatek dále zvyšuje. Již několik let je paliativní medicína v ČR samostatný nástavbový atestační obor, který každým rokem produkuje několik specialistů. Jejich místa působení jsou rozličná: primární péče, nemocnice, ambulantní péče, hospice. Budoucnost je v pokračování oboru paliativní medicíny jakožto samostatného nástavbového oboru.
Nezanedbatelným faktorem pro realizaci včasné paliativní péče je její celkové vnímání společností. Pacienti, jejich rodiny, pečující a laická veřejnost nerozumí tomu, co je skutečná paliativní péče. Většina laiků tento výraz nezná, a pokud ano, tak dává jej na stejnou úroveň jako hospice a péči na konci života. Zároveň vnímá konotace ukončení onkologické léčby a urychlení smrti. Opak je přitom pravdou – většina přehledů a studií jednoznačně dokumentovala, že u pacientů v paliativní a hospicové péči nedochází ke zkrácení života a jeho kvality (50, 51). Podaří-li se zlepšit porozumění tomu, co skutečně je PC, v čem spočívá její hlavní přínos a jaké jsou její reálné možnosti (lepší kvalita života a delší přežití), je to důležitý krok k EPC (10).
SHRNUTÍ A ZÁVĚR
V posledním půlstoletí se paliativní péče rozvinula od filozofie péče o pacienty v závěru života po samostatný klinický obor pomáhající pacientům s nevyléčitelnými chorobami. V minulých letech bylo podáno mnoho důkazů o tom, že časná paliativní péče v onkologii může zlepšit celkovou péči, kvalitu života, kontrolu symptomů a psychický stav a prodloužit přežití u pacientů s pokročilými nádory. Otázka dnes není, zda má být paliativní péče součástí moderní onkologie, ale kdy, kým a jak má být realizována. Základ tvoří rutinní screening symptomů a definovaná kritéria předání do paliativní péče s multidisciplinární péčí o každého pacienta (paliativně-onkologický multidisciplinární tým).
Bylo navrženo několik modelů pro realizaci EPC v nemocnicích, ambulantní a domácí péči, které prokazují přínos od stanovení diagnózy po konec života. Všechny modely vykazují omezení a bariéry ze strany onkologů, paliativních specialistů, společnosti a koncepce zdravotní péče. Do budoucna je nutné tyto bariéry překonávat pomocí propracovaného systému vzdělávání, obecné osvěty o paliativní péči a pokračujícího sbírání dat o jednotlivých parametrech EPC. Jedině tak lze očekávat skutečnou integraci kvalitní paliativní péče v onkologii.
Adresa pro korespondenci:
MUDr. Marek Sochor
Komplexní onkologické centrum
Krajská nemocnice Liberec, a. s.
Husova 357/10
460 63 Liberec
Tel.: 485 312 226
e-mail: marek.sochor@nemlib.cz
Sources
1. Davis MP, Bruera E, Morganstern D. Early integration of palliative and supportive care in the cancer continuum. Am Soc Clin Oncol Educ Book 2013; 144–150.
2. World Health Organization. WHO Definition of Palliative Care. Dostupné na: www.who.int/cancer/palliative/definition/en/
3. Hui D. Definition of supportive care: does the semantic matter? Curr Opin Oncol 2014; 26 : 372–379.
4. Ferrell BR, Temel JS, Temin S et al. Integration of palliative care into standard oncology care: American Society of Clinical Oncology clinical practice guideline update. J Clin Oncol 2016; 35 : 96–112.
5. Smith TJ, Temin S, Alesi ER et al. American Society of Clinical Oncology provisional clinical opinion: the integration of palliative care into standard oncology care. J Clin Oncol 2012; 30 : 880–887.
6. Cherny N, Catane R, Schrijvers D et al. European Society for Medical Oncology (ESMO) program for the integration of oncology and palliative care: a 5-year review of the Designated Centers’ incentive program. Ann Oncol 2010; 21 : 362–369.
7. Von Roenn JH. Optimal cancer care: Concurrent oncology and palliative care. J Natl Compr Canc Netw 2013; 11(Suppl1): S1–S2.
8. Quill TE, Abernethy AP. Generalist plus specialist palliative care-creating a more sustainable model. N Engl J Med 2013; 368 : 1173–1175.
9. Bruera E, Hui D. Integrating supportive and palliative care in the trajectory of cancer: establishing goals and models of care. J Clin Oncol 2010; 28 : 4013–4017.
10. Parikh RB, Kirch RA, Smith TJ et al. Early specialty palliative care: translating data in oncology into practice. N Engl J Med 2013; 369 : 2347–2351.
11. Bakitas M, Lyons KD, Hegel MT et al. Effects of a palliative care intervention on clinical outcomes in patients with advanced cancer: the Project ENABLE II randomized controlled trial. JAMA 2009; 302 : 741–749.
12. Higginson IJ, Bausewein C, Reilly CC et al. An integrated palliative and respiratory care service for patients with advanced disease and refractory breathlessness: a randomized controlled trial. Lancet Respir Med 2014; 2 : 979–987.
13. Grudzen CR, Richardson LD, Johnson PM et al. Emergency department-initiated palliative care in advanced cancer: a randomized clinical trial. JAMA Oncol 2016; 2 : 591–598.
14. Zimmermann C, Swami N, Krzyzanowska M et al. Early palliative care for patients with advanced cancer: A cluster-randomised controlled trial. Lancet 2014; 383 : 1721–1730.
15. Back AL, Park ER, Greer JR et al. Clinician roles in early integrated palliative care for patients with advanced cancer: A qualitative study. J Palliat Med 2014; 17 : 1244–1248.
16. Greer JA, Pirl WF, Jackson VA et al. Effect of early palliative care on chemotherapy use and end-of-life care in patients with metastatic non-small-cell lung cancer. J Clin Oncol 2012; 30 : 394–400.
17. Bakitas MA, Tosteson TD, Li Z et al. Early versus delayed initiation of concurrent palliative oncology care: patient outcomes in the ENABLE III randomized controlled trial. J Clin Oncol 2015; 33 : 1438–1445.
18. Temel JS, Greer JA, Muzikansky A et al. Early palliative care for patients with metastatic non-small-cell lung cancer. N Engl J Med 2010; 363 : 733–742.
19. Gade G, Venohr I, Conner D et al. Impact of an inpatient palliative care team: a randomized control trial. J Palliat Med 2008; 11 : 180–190.
20. Brumley R, Enguidanos S, Jamison P et al. Increased satisfaction with care and lower costs. Results of a randomized trial of in-home palliative care. J Am Geriatr Soc 2007; 55 : 993–1000.
21. Jang RW, Burman D, Swami N et al. Impact of an oncology palliative care clinic on access to home care services. Am J Hosp Palliat Care 2013; 30 : 425–431.
22. Porzio G, Aielli F, Verna L et al. Integrating oncology and palliative home care in Italy: the experience of the "L’Aquila per la Vita" Home Care Unit. Tumori 2013; 99 : 225–228.
23. Maione P, Perrone F, Gallo C et al. Pretreatment quality of life and functional status assessment significantly predict survival in elderly patients with advanced non-small-cell lung cancer receiving chemotherapy: a prognostic analysis of the Multicenter Italian Lung Cancer in the Elderly study. J Clin Oncol 2005; 23 : 6865–6872.
24. Yoong J, Park ER, Greer JA et al. Early palliative care in advanced lung cancer: a qualitative study. JAMA Intern Med 2013; 173 : 283–290.
25. Hui D. Access to palliative care among patients treated at a comprehensive cancer center. Oncologist 2012; 17 : 1574–1580.
26. Beccaro M, Constantini M, Merlo DF et al. Inequity in the provision of and access to palliative care for cancer patients: Results from the Italian survey of the dying of cancer (ISDOC). BMC Public Health 2007; 7 : 66.
27. Hui D, Bruera E. Models of integration of oncology and palliative care. Ann Palliat Med 2015; 4(3): 89–98.
28. Weissman DE, Meier DE. Identifying patients in need of a palliative care assessment in the hospital setting: a consensus report from the Center to Advance Palliative Care. J Palliat Med 2011; 14 : 17–23.
29. Tanco K et al. Patient perception of physician compassion after a more optimistic vs a less optimistic message: A randomized clinical trial. JAMA 2015; 1 : 176–183.
30. Dow LA et al. Paradoxes in advance care planning: the complex relationship of oncology patients, their physicians, and advanced medical directives. J Clin Oncol 2010; 28 : 299–304.
31. Payne R. The integration of palliative care and oncology: the evidence. Oncology (Williston Park) 2011; 25 : 126.
32. Bruera E, Hui D. Conceptual models for integrating palliative care at cancer centers. J Palliat Med 2012; 15 : 1261–1269.
33. Levy MH, Adolph MD, Back A et al. Palliative care. J Natl Compr Canc Netw 2012; 10 : 1284–1309.
34. Gaertner J, Wolf J, Hallek M et al. Standardizing integration of palliative care into comprehensive cancer therapy – a disease specific approach. Support Care Cancer 2011; 19 : 1037–1043.
35. Hui D, Kim Yj, Park JC et al. Integration of oncology and palliative care: a systematic review. Oncologist 2015; 20 : 77–83.
36. Hui D, Kim SH, Roquemore J et al. Impact of timing and setting of palliative care referral on quality of end-of-life care in cancer patients. Cancer 2014; 120 : 1743–1749.
37. Davis MP, Strasser F, Cherny N et al. MASCC/ESMO/EAPC survey of palliative programs. Support Care Cancer 2015; 23 : 1951–1968.
38. Hui D, Finlay E, Buss MK et al. Palliative oncologists: Specialists in the Science an Art of Patient Care. J Clin Oncol 2015; 33 : 2314–2317.
39. Vergo MT, Cullinan AM. Joining together to improve outcomes: Integrating specialty palliative care into the care of patients with cancer. J Natl Compr Cancer Netw 2013; 11: S38–S46.
40. Von Roenn JH, Voltz R, Serrie A. Barriers and approaches to the successful integration of palliative care and oncology practice. J Natl Compr Cancer Netw 2013; 11(Suppl. 1): S11–S16.
41. Schenker Y, Crowley-Matoka M, Dohan D et al. Oncologist factors that influence referrals to subspecialty palliative care clinics. J Oncol Practice 2014; 10: e37–44.
42. Ross DD, Shpritz D, Alexander CS et al. Development of required postgraduate palliative care training for internal medicine residents and medical oncology fellows. J Cancer Educ 2004; 19 : 81–87.
43. Rangachari D, Smith TJ. Integrating palliative care in oncology. The oncologist as a primary palliative care provider. Cancer J 2013; 19(5): 373–378.
44. Gaertner J, Weingartner V, Wolf J, Voltz R. Early palliative care for patients with advanced cancer: how to make it work? Curr Opin Oncol 2013; 25 : 342–352.
45. Quill TE, Abernethy AP. Generalist plus specialist palliative care-creating a more sustainable model. N Engl J Med 2013; 368 : 1173–1175.
46. Gilligan T, Coyle N, Frankel RM, Berry DL et al. Patient-clinician communication: American Society of Clinical Oncology consensus guideline. J Clin Oncol 2017; 35 : 3618–3632.
47. Johnson LA, Gorman C, Morse R et al. Does communication skills training make a difference to patients’ experiences of consultations in oncology and palliative care services? Eur J Cancer Care 2013; 22 : 202–209.
48. Mack J, Wolfe J, Cook EF. Hope and prognostic disclosure. J Clin Oncol 2007; 25 : 5636–5642.
49. Wright AA, Zhang B, Ray A et al. Associations between end-of-life discussions: Patient mental health, medical care near death, and caregiver bereavement adjustments. JAMA 2008; 300(14): 1665–1673.
50. Connor SR, Pyenson B, Fitch K et al. Comparing hospice and nonhospice patient survival among patients who die within a three-year window. J Pain Symptom Manage 2007; 33(3): 238–246.
51. El-Jawahri A, Green JA, Temel JS. Does palliative care improve outcomes for patients with incurable illness? A review of the evidence. J Support Oncol 2011; 9 : 87–94.
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental Hygienist
Article was published inJournal of Czech Physicians

-
All articles in this issue
- Výrobci cigaret a jejich opravné prohlášení – corrective statement
- Hospic – pokračující péče během života pacienta
- Péče o nevyléčitelně nemocné a umírající v domácím prostředí
- Časná integrace paliativní péče v onkologii
- Paliativní péče v kardiologii
- Paliativní péče v nefrologii
- Perioperační paliativní péče: role mezioborového konziliárního týmu v perioperačním období a v prostředí intenzivní péče
- Geriatrická paliativní péče
- Dětská paliativní péče
- Přehled dotazníků a škál hodnotících pacienty s amyotrofickou laterární sklerózou
- Journal of Czech Physicians
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Paliativní péče v nefrologii
- Péče o nevyléčitelně nemocné a umírající v domácím prostředí
- Přehled dotazníků a škál hodnotících pacienty s amyotrofickou laterární sklerózou
- Dětská paliativní péče
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

