-
Medical journals
- Career
Neurostimulace v léčbě refrakterní anginy pectoris
Authors: P. Neužil 1; D. Urgošík 2; M. Táborský 1
Authors‘ workplace: Kardiologické oddělení Kardiocentra Primář: doc. MUDr. Miloš Táborský, CSc., FESC, MBA 1; Oddělení stereotaktické a radiační neurochirurgie Neurocentra Primář: doc. MUDr. Roman Liščák, CSc. Nemocnice Na Homolce Ředitel: MUDr. Vladimír Dbalý, MBA 2
Published in: Prakt. Lék. 2009; 89(2): 85-88
Category: Of different specialties
Overview
Úvod:
Neurostimulace jako symptomatická léčba refrakterní anginy pectoris (AP) je v současné době kromě laserové revaskularizace jednou z mála dostupných možností léčby tohoto jinak neřešitelného a kvalitu života negativně ovlivňujícího onemocnění. K této léčbě může být indikovaný nemocný s pokročilým stupněm AP III.-IV. CCSC klasifikace, u kterého není možný chirurgický nebo perkutánní revaskularizační výkon (PCI, AKB) a ani při maximální antianginózní terapii nedochází k ústupu symptomů.Metodika:
V tomto sdělení popisujeme způsob provedení míšní stimulace (spinal cord stimulation SCS), zahraniční a naše vlastní zkušenosti v České republice. Tato léčba je soustředěna do center bolesti, které se zabývají algickým syndromem a je velmi specifická svým interdisciplinárním rozsahem. Vlastní výkon je prováděn neurochirurgem nebo anesteziologem, za asistence kardiologa, který také nemocné sleduje ve specializované ambulanci vybavené programerem, který umožňuje komunikaci a programaci neurostimulačního přístroje implantovaného nemocnému. V další části sdělení diskutujeme mechanismy pozitivního účinku míšní stimulace přes placebo efekt, ovlivnění b endorfínů snížením nociceptivních podnětů, redistribuce a „homogenizace“ myokardiální perfuze snížením účinků adenozinu, nicméně základní princip účinku spočívá nejspíše v přímém ovlivnění bolesti stimulací nízkoprahových A vláken, která zprostředkovávají přenos nebolestivých podnětů. Použití SCS tlumí tedy senzitivitu vysokoprahových tenkých C vláken, která spinothalamickou drahou přenášejí bolestivé podněty a znemožňují tedy tento bolestivý podnět vnímat.Závěry:
Naše vlastní zkušenosti a výsledky publikované v zahraniční literatuře jasně prokazují, že u přísně indikované skupiny nemocných tato symptomatická léčba přináší především produktivním nemocných výraznou úlevu a umožňuje jim se zapojit zpět do aktivního života.Klíčová slova:
refrakterní angina pectoris, neuromodulační léčba, míšní stimulaceNemocní s vysokým stupněm anginy pectoris (AP) refrakterní na maximalizovanou medikamentózní léčbu, kteří zároveň nejsou vhodnými kandidáty k revaskularizační intervenci buď pro nevhodný koronarografický nález, nebo neúnosné riziko zákroku, trpí obvykle výrazně sníženou kvalitou života s minimální možností zásadnějšího zlepšení další medikamentózní léčbou. Protože ani transmyokardiální a perkutánní revaskularizace s využitím laseru nepřinesla očekávaný efekt, ukazuje se, že stimulace míchy představuje dnes jedinou existující možnost, jak ovlivnit symptomy refrakterní anginy pectoris.
Míšní stimulaci (SCS – spinal cord stimulation) jako způsob léčby refrakterní anginy pectoris poprvé použili Murphy a Giles v roce 1987 (1), kteří navázali na výsledky práce Mannheimera z počátku osmdesátých let, který použil k redukci atak anginy pectoris transkutánní nervovou stimulaci (transcutaneous electrical nerve stimulation – TENS) (2). K obecnému rozšíření metodiky pak přispěly práce především De Jongsteho skupiny, ve kterých autoři prokázali snížení celkového počtu epizod AP, spojené s redukcí ischemických příhod za období 48 hodin, proti kontrolní skupině (3), s využitím tří hodinových sérií neurostimulace během 24 hodin. Murray dále prokázal významné snížení počtu hospitalizací během jednoho roku sledování pacientů (4).
Základní námitky, že trvalá stimulace míchy vede k maskování akutních ischemických příhod včetně nestabilní angíny pectoris (NAP) nebo akutního infarktu myokardu a že působí arytmogenně, nebyly prokázány (3, 4, 5, 6). Mechanismus účinku neurostimulace zatím není zcela jasně prokázán, uvažuje se o přímém ovlivnění bolesti stimulací nízkoprahových A vláken, která zprostředkovávají přenos nebolestivých podnětů. Jejich stimulace (použitím SCS) tlumí senzitivitu vysokoprahových tenkých C vláken, která spinothalamickou drahou přenášejí bolestivé podněty, takže původně bolestivý vjem je vnímám spíše jako parestezie (7, 8, 9) (obr. 1). Dalším efektem, který může ovlivnit vnímání anginózní bolesti, je stimulace b endorfínů a tzv. homogenizace myokardiální perfuze ovlivněním aktivace adenozinu a snížením „steal fenomenu“ (10, 11, 12), takže výsledkem SCS je zlepšení tolerance zátěže a zároveň redukce myokardiální ischemie (13).
Image 1. Schéma působení neurostimulátoru 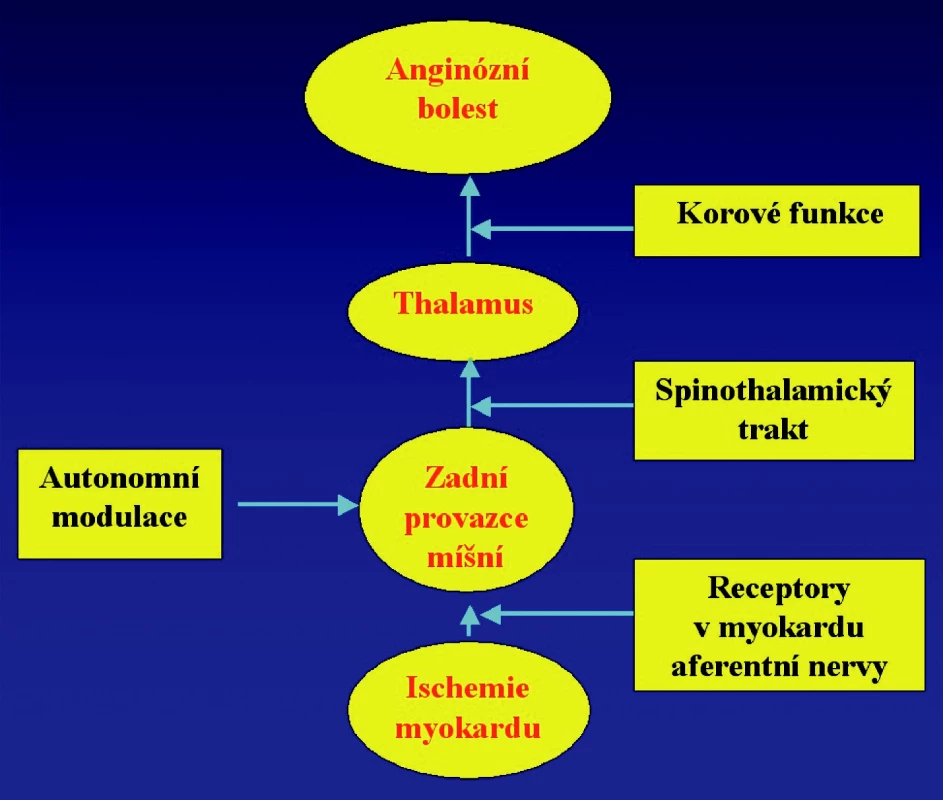
Pacienti s chronickou refrakterní anginou pectoris mají výrazně horší kvalitu života vlivem zásadně snížené snášenlivosti tělesné námahy i se zhoršením psychiky, které jsou také ovlivněny častou rehospitalizací a opakováním intervenčních vyšetření, bez možného odstranění symptomů.
Popis metody
Vlastní implantace neurostimulátoru spočívá v zavedení čtyř nebo osmipolární stimulační elektrody do oblasti epidurálního vaku provedením punkce Tuohyho jehlou, a to převážně mezi obratlovými těly Th 4 a Th 5. Punkční jehlou se zavádí vodící drát pod fluoroskopickou kontrolou, a stejnou cestou se zavádí i stimulační elektroda, která se pak umisťuje obvykle do oblasti C7 – Th 1 páteře (obr. 2).
Image 2. Schéma implantace neurostimulátoru 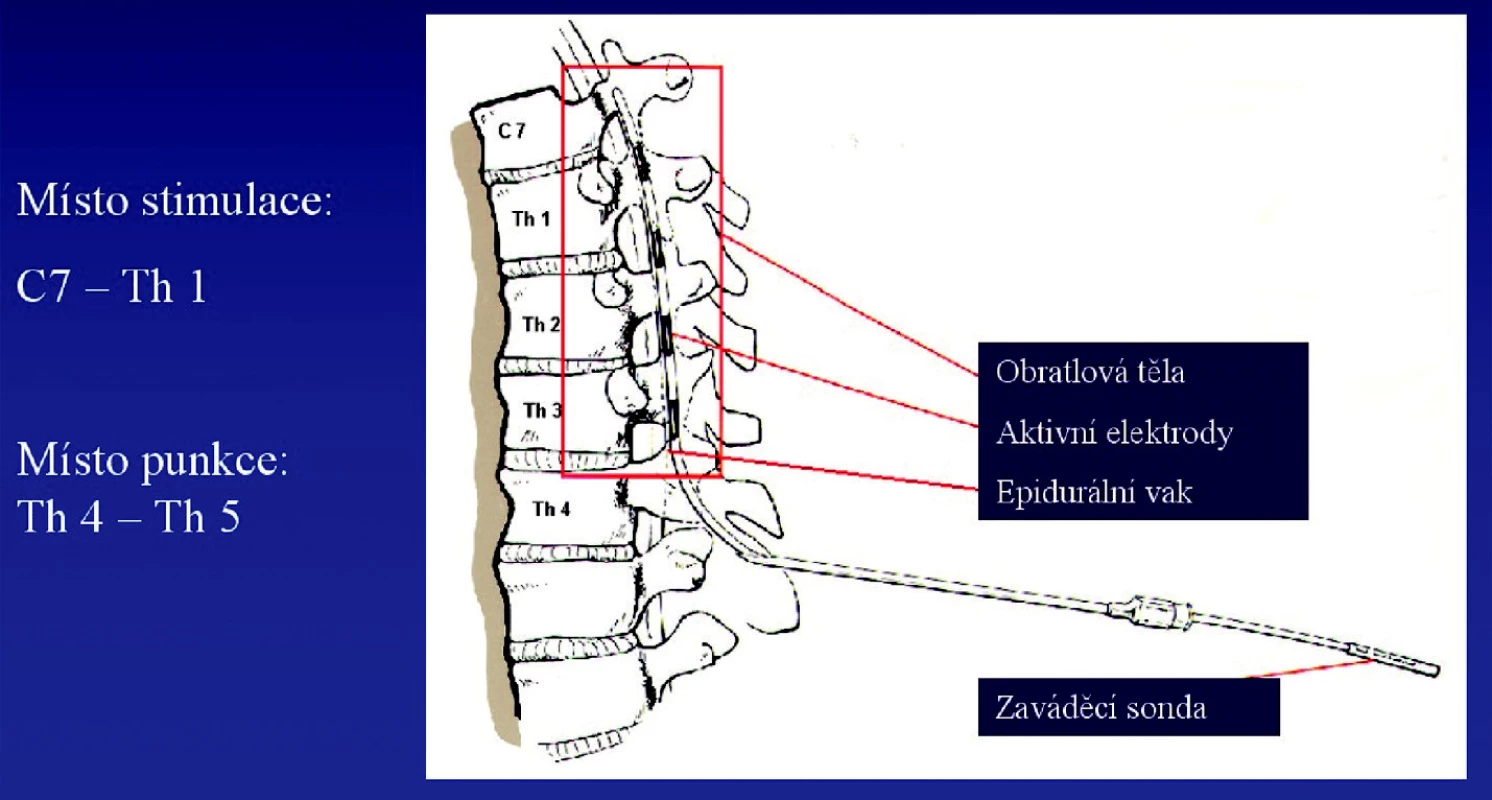
Elektroda není fixována. Po testování polohy elektrody, stimulační amplitudy, délky stimulačního pulzu a frekvence se proximální konec spojí s prodlužovacím kabelem, který se vyvádí podkožním tunelem. Pak následuje testování efektu parestézie, nastavením a úpravou parametrů neurostimulace. Je možné vybrat kombinace elektrod v různých etážích, kde je neurostimulace nejefektivnější. Důležitý je kontakt nemocného při testování rozsahu parestezie při spuštěné neurostimulaci. On musí určit, zda ložisko vnímané parestezie je shodné s ložiskem vnímané bolesti při epizodách AP. Pokud jsou parametry neurostimulace optimální, provádí se buď v jedné době, nebo odloženě implantace vlastního neurostimulátoru (v našem souboru jsme použili neurostimulátor Medtronic Itrel™ III model 7425), který se následně implantuje do podkoží v abdominální oblasti.
Chirurgický zákrok se provádí v lokální anestezii, pacient zůstává v klidu na posteli pouze 2–3 hodiny. Neurostimulátor se programuje v několika automatických režimech buď jako kontinuální, nebo cyklická neurostimulace nezávislá na záchvatech anginózních obtíží. Dále má nemocný vlastní aktivátor, kterým si sám spouští stimulaci volným přiložením nad generátor. V našem případě se jednalo o aktivátor Itrel® EZ model 7434. (obr. 3)
Image 3. Aktivátor Itrel<sup>®</sup> EZ model 7434 
Obvyklý automatický režim stimulace je třikrát až čtyřikrát za den v jedno až dvouhodinových cyklech stimulace . Některá centra začínají po implantaci s nepřetržitou stimulací 24 hodin denně a po několika týdnech dobu stimulace omezují. Pacientem aktivovaná stimulace by měla být spouštěna ještě před očekávaným nástupem AP nebo alespoň s jejím začátkem.
Podle potřeby je možné ovlivnit výši amplitudy a dobu trvání stimulačního impulzu (0–8,6V/60–210 μsec), který vede k omezení anginózních příhod. Frekvence stimulace je nastavitelná od 50 do 100 Hz.
Další kontroly je vhodné provádět ve tří až šestiměsíčních intervalech v závislosti na obtížích nemocného. Mezi potenciální komplikace léčby patří dislokace elektrody (velmi zřídka, po 1. roce od implantace není popsána) a infekce.
Hlavními indikačními kritérii jsou:
- a) pacient se syndromem anginy pectoris III. nebo IV. stupně (klidové noční bolesti),
- b) dokumentovaná ischemie myokardu,
- c) koronarograficky dokumentovaná ischemická choroba srdeční (ICHS) nebo spastická forma AP,
- d) pacient již není vhodným kandidátem revaskularizace myokardu (PCI, AKB),
- e) pacient s maximalizovanou medikamentózní terapií,
- f) pacient rozumí principu metody a souhlasí s jejím provedením.
Za kontraindikace lze považovat situaci kdy:
- není schůdné provedení metody,
- pacient má již implantovaný kardiostimulátor či implantabilní kardioverter – defibrilátor,
- relativním je pak dramatické snížení systolické funkce levé komory, ejekční frakce pod 20 % s potenciální nutností zavedení resynchronizační terapie.
Vlastní zkušenosti
První implantaci neurostimulátoru pro refrakterní AP jsme provedli na našem pracovišti v červenci 2000 a od té doby jsme provedli tuto léčbu u 17 nemocných (13 mužů, 4 žen), průměrný věk nemocných byl nižší než v obvyklých souborech, a to 59, 8 let ± 11 let s průměrnou hodnotou EF LK 54,4 ± 14 %.
Všichni nemocní měli poměrně závažný stupeň obtíží, jejich stupeň dle funkční klasifikace CCSC (Canadian Cardiology Society Classification) byl v průměru 3,8. Průměrný počet výskytu atak anginy pectoris během dne činil u této skupiny nemocných průměrně 5,4, přičemž všichni nemocní měli alespoň dvě epizody klidové anginy pectoris a u 8 z nich klidové bolesti převažovaly. Průměrný počet aplikací nitroglycerinu byl 4,2.
U každého nemocného byla před implantací neurostimulátoru provedena alespoň jedna angiografie věnčitých tepen, přičemž u 12 z nich byla provedena alespoň jednou perkutánní koronární intervence (PCI), a u 9 z nich pak aortokoronární bypass (AKB) s přetrvávajícími projevy refrakterní AP při technicky neřešitelném nálezu na zbylých větvích věnčitých tepen.
Jeden nemocný ze souboru měl farmakologicky prokázanou vazospastickou formu AP s intolerancí farmakoterapie, jak kalciových antagonistů, tak nitrátů (otoky nohou a kruté bolesti hlavy).
U jednoho nemocného, u kterého byla v rámci kardiochirurgického výkonu kromě revaskularizace provedena současně i resekce aneuryzmatu, jsme nacházeli výrazné zlepšení EF LK na 45 % a neprokazovali jsme během programované stimulace komor inducibilitu život ohrožujících komorových tachyarytmií. Proto jsme se také pak přiklonili k indikaci neurostimulace (prakticky každou noc se probouzel pro bolesti na hrudi). U všech dalších nemocných po většinou pro difúzní stenotický proces na věnčitých tepnách nebylo schůdné provedení aortokoronárního by-passu, ani paliativní PCI nebyla shledána jako schůdná, nebo byla ukončena technickým nezdarem.
Po implantaci neurostimulátoru výskyt epizod AP významně ustoupil u 16 nemocných, došlo také k zásadnímu poklesu aplikací nitroglycerinu; při optimální programaci neurostimulátoru pouze 2 nemocní uváděli požití nitroglycerinu více jak 1x za měsíc. Jeden nemocný uváděl sice mírný pokles výskytu zvláště klidových bolestí, přesto u něj dál bylo nutné aplikovat vyšší dávky nitroglycerinu, tj. cca 2x denně.
U 13 nemocných bylo možné již po 6 měsících od zavedení SCS nastavit cyklický režim stimulace s trvajícím příznivým efektem neurostimulace (převážně se jednalo o dvě hodiny aktivní neurostimulace střídané čtyřhodinovou pauzou. Nemocný je však schopen sám si aktivovat přístroj, například v době předpokládané vyšší fyzické nebo psychické zátěže).
U první nemocné došlo dvakrát k dislokaci zavedené elektrody vždy s úspěšnou repozicí (nemocná sama rozpoznala nárůst epizod AP při ne příliš optimální projekci parestezií), jeden nemocný přes zavedený a dobře fungující režim neurostimulace rozpoznal příznaky akutního infarktu myokardu (častá výhrada, že by neurostimulace svojí funkcí blokovala rozpoznání bolestí provázející akutní IM, a tím zabránila optimální a zvláště včasné léčbě).
Dva nemocní zemřeli 1 a 2 roky od zavedení SCS na terminální formu vleklého srdečního selhání
Diskuse
Počet nemocných, kterým byla provedena neurostimulace míchy pro refrekterní AP, se celosvětově odhaduje na 3 500 osob. Stále více klinických dat prokazuje její účinnost a bezpečnost. Greco referoval výrazný ústup anginózních obtíží při použití SCS oproti skupině nemocných bez použití neurostimulace (4,2 epizod AP/2 dny vs. 9,2 epizod AP/2 dny) (14), metaanalýza 4 studií prokázala snížení epizod na 2,2 / 2 dny vs. 5,5 / 2 dny (15).
De Jongste prokázal zvýšení tolerance zátěže o 25 %, prodloužení doby do nástupu AP o 40 % (3), Andersen dále prokázal 20% redukci ST depresí na Holterovských záznamech EKG a 70% redukci nutnosti hospitalizace v období ročního sledování (6). Tyto výsledky potvrdila i randomizovaná studie z roku 1998 publikovaná Hautvastem (16).
Velmi významné je snížení počtu epizod AP o 80 % (17). Zároveň TenVaarwerk zjistil ve skupině 517 nemocných zajištěných SCS v letech 1987 až 1997 v 21 evropských centrech za průměrnou dobu 128 měsíčního sledování jednoroční kardiální mortalitu 3,5–5 %, celková jednoroční mortalita byla 7–8 %. Jednalo se o nemocné s postižením tří a více věnčitých tepen (18). Nebylo tedy prokázáno zvýšení mortality u srovnatelných nemocných z jiných studií. To ostatně potvrzuje studie ESBY (Electrical stimulation versus coronary artery bypass surgery in severe angina pectoris) z roku 1998, ve které bylo randomizováno 104 nemocných (53 s SCS a 51 s AKB), kde v první skupině bylo za jeden rok sledování pozorováno jedno úmrtí, zatímco ve druhé skupině s AKB bylo dokumentováno 7 úmrtí.
Tolerance zátěže při ergometrii byla ovšem vyšší u nemocných po AKB (15).Ve prospěch SCS hovoří i doposud ojedinělé studie prokazující prostředníctvím pozitronové emisní tomografie (PET) tzv. homogenizaci myokardiální perfuze („Robin Hood efekt“). Při provedení PET mozkové perfuze bylo sledováno zvýšené prokrvení nociceptivních oblastí mozku a oblastí kardiovaskulárních (11). Norssell prokázal snížení obratu norepinefrinu při použití SCS (18 % vs 47 %), což by svědčilo pro snížení adrenergní aktivity u nemocných s míšní neurostimulací (10).
Eliasson dále prokazuje výrazný efekt i u nemocných se syndromem X, u kterých došlo k výraznému zlepšení tolerance zátěže, a během Holterovského monitorování EKG neprokazoval ani jedinou epizodu AP (12)! Velmi přínosné jsou i práce Andersena a De Jongsteho publikované v roce 1994, kteří neprokazují nárůst četnosti infarktu myokardu nebo maskování IM a NAP (tedy ve shodě s naším vlastním pozorováním). V referovaných souborech 50, respektive 22 osob nedošlo k jedinému úmrtí v důsledku akutní koronární příhody. Nemocní zároveň charakterizovali bolest při IM nebo NAP zcela odlišně oproti běžným atakám AP (3, 6).
Závěr
Závěrem je možné shrnout, že použití SCS u refrakterní AP by měl indikovat a nemocné s provedenou neurostimulací refrakterní AP sledovat kardiolog, který úzce spolupracuje s odborníky na léčbu bolesti a neuromodulační léčbu. Tato metoda nemá ambice a jistě nikdy ani nebude dominantní léčbou tohoto klinicky velmi obtížně léčitelného syndromu, ale u takových nemocných, kde je kauzální reperfuzní léčba technicky neschůdná nebo vysoce riziková, se míšní stimulace stává jednou z hlavních způsobů terapie, jak ovlivnit kvalitu života nemocných, která je i podle rozboru našeho souboru nemocných nezaviděníhodná. Dosažené výsledky jasně dokumentují, že námi zavedená neuromodulační léčba u nemocných, kteří jsou jinak „odsouzeni k přežívání“, zásadním způsobem změní jejich denní aktivitu směrem k nesrovnatelně kvalitativnějšímu „aktivnímu životu“.
doc. MUDr. Petr Neužil, CSc.
Kardiologické oddělení
Nemocnice Na Homolce
Roentgenova 2,
150 30 Praha 5
E mail: petr.neuzil@homolka.cz
Sources
1. Murphy, D.F., Giles, K.E. Dorsal column stimulation for pain relief from intractable angina pectoris. Pain 1987, 28, p. 365-368.
2. Mannheimer, C., Carlsson, C.A., Emanuelsson, H. et al. The effects of transcutaneous electrical nerve stimulation in patients with severe angina pectoris. Circulation 1985, 71, p. 308-316.
3. De Jongste, M.J.L., Haaksma, J., Hautvast, R.W.M. et al. Effects of spinal cord stimulation on myocardial ischaemia during daily life in patients with severe coronary artery disease. A prospective ambulatory electrocardiographic study. Br. Heart J. 1994, 71, p. 413-418.
4. Murray, S., Carson, K.G.S., Ewings, P.D. et al. Spinal cord stimulation (SCS) significantly decreases the need for acute hospitalization due to chest pain in patients with refractory angina pectoris. Heart 1999, 82, p. 89-92.
5. Sanderson, J.E. Ibrahim, B., Waterhouse, D. et al. Spinal electrical stimulation for intractable angina - long term clinical outcome and safety. Eur. Heart J. 1994, 15, p. 810-814.
6. Andersen, C., Hole, P., Oxhoj, H. Does pain relief with spinal cord stimulation for angina conceal myocardial infarction? Br. Heart J. 1994, 71, p. 413-418.
7. Shealey, C.N., Mortimer, J.T., Reswick, J.B. Electrical inhibition of pain by stimulation of the dorsal columns. Anesth. Analg. 1967, 46, p. 45-47.
8. Jacobs, M.J., Jorning, P.J., Joshi, S.R. et al. Epidural spinal cord electrical stimulation improves microvaskcular blood flow in severe limb ischaemia. Ann. Surg. 1988, 207, p. 170-183.
9. Mannheimer, C., Augustinsson, L.E., Carlsson, C.A. et al. Epidural SCS in severe angina pectoris. Br. Heart J. 1988, 59, p. 56-61.
10. Norrsell, H., Eliasson, T., Manheimer, C. et al. Effect of pacing-induced myocardial stress and spinal cord stimulation on whole body norepinephrine spillover. Eur. Heart J. 1997, 18, p. 1890-1896.
11. Hautvast, R.W.M., Blanksma, P.K., De Jongste, M.J.L. et al. Effect of spinal cord stimulation on myocardial blood flow assessed by positron emission tomography in patients with refractory angina perctoris. Am. J. Cardiol. 1996, 77, p. 462-467.
12. Eliasson, T., Mannheimer, C., Waagstein, F. et al. Safety aspects of spinal cord stimulation in severe angina pectoris. Cor. Art. Dis. 1994, 5, p. 333-339.
13. Mannheimer, C., Eliasson, T., Andersson, B. et al. Effects of spinal cord stimulation in angina pectoris induced by pacing and possible mechanisms of action. Br. Heart J. 1993, 301, p. 477-480.
14. Greco, C. Spinal cord stimulation for the treatment of refractory angina pectoris: a two year follow up. PACE 1999, 22, p. 26-32.
15. Mannheimer, C., Eliason, T., Augustinsson, L.E. et al. Electrical stimulation versus coronary artery bypass surgery in severe angina pectoris: the ESBY study. Circulation 1998, 97, p. 1157-1163.
16. Hautvast, R.W.M., De Jongste, M.J.L., Stal, M.J. et al. Spinal cord stimulation in intractractable angina pectoris: A randomized controlled efficacy study. Am. Heart J. 1998, 136, p. 1114-1120.
17. Sanderson, J.E., Brooksby, P., Waterhause, D. et al. Epidural spinal electrical stimulationfor severe angina: a study of its effect on symptoms, exercise tolerance and degree of ischaemia. Eur. Heart J. 1992; 13: p. 628-633.
18. Ten Vaarwerk, I.A.M., Jessurum, G.A.J., De Jongste, M.J.L. et al. Clinical outcome of patients treated with spinal cord stimulation for therapeutically refractory angina pectoris. Heart 1999, 82, p. 82-88.
19. Murray, S., Carson, K.G., Ewings, P.D. et al. Spinal cord stimulation significantly decreases the need for acute hospital admission for chest pain in patients with refractory angina pectoris. Heart 1999, 82, p. 89–92.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2009 Issue 2-
All articles in this issue
- Posttraumatická stresová porucha u zneužívaných dětí
- Kouření a kardiovaskulární nemoci
- Zdravotní aspekty redukční mammaplastiky
- Prevence onemocnění klíšťovou encefalitidou z pohledu zdravotní pojišťovny
- Transplantace ruky
- Neurostimulace v léčbě refrakterní anginy pectoris
- Patofyziologie diabetické retinopatie
- Alergická rinitida jako nemoc z povolání
- Spokojenost pacientů s poskytovanou péčí: teoretické přístupy a modely
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Transplantace ruky
- Posttraumatická stresová porucha u zneužívaných dětí
- Spokojenost pacientů s poskytovanou péčí: teoretické přístupy a modely
- Alergická rinitida jako nemoc z povolání
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

