-
Medical journals
- Career
Metabolický profil pacientů po transplantaci jater ve vztahu k rozvoji NAFLD – výsledky pilotní studie
Authors: I. Hejlová 1; M. Dezortová 2; P. Šedivý 2; M. Drobný 2; M. Hájek 2; M. Cahová 3; H. Daňková 3; E. Sticová 4; V. Lánská 5; P. Trunečka 6
Authors‘ workplace: Klinika hepatogastroenterologie, Transplantcentrum, IKEM, Praha 1; Pracoviště radiodiagnostiky a intervenční radiologie, Komplement, IKEM, Praha 2; Centrum experimentální medicíny, IKEM, Praha 3; Pracoviště klinické a transplantační patologie, Transplantcentrum, IKEM, Praha 4; Lékařská statistika, IKEM, Praha 5; Transplantcentrum, IKEM, Praha 6
Published in: Gastroent Hepatol 2016; 70(4): 325-330
Category: Hepatology: Original Article
doi: https://doi.org/10.14735/amgh2016325Overview
Cíl:
Nealkoholická steatóza (NAFLD – non-alcoholic fatty liver disease) jaterního štěpu se vyskytuje u 31–56 % pacientů po transplantaci jater, její výskyt narůstá s dobou od transplantace. Cílem naší prospektivní studie byla analýza metabolického profilu pacientů po transplantaci jater ve vztahu k rozvoji NAFLD.Metody:
Pilotní část prospektivní studie zahrnula 31 pacientů 1 – 16 let po transplantaci jater, kteří podstoupili protokolární biopsii jater. Provedli jsme laboratorní vyšetření glukózového a lipidového metabolizmu, 1H MR spektroskopií a zobrazováním jsme stanovili obsah tuku v játrech a objem podkožního a viscerálního tuku. Metodou dynamické 31P MR spektroskopie jsme v musculus gastrocnemius stanovili maximální mitochondriální kapacitu.Výsledky:
V biopsii jater jsme prokázali steatózu stupně 2 – 3 u 12 (38,7 %) pacientů, steatózu stupně 1 u 13 (41,9 %) pacientů a šest (19,4 %) pacientů bylo bez steatózy. Se stupněm steatózy pozitivně koreloval body mass index (p = 0,002), obvod pasu (p = 0,004), objem podkožního (p = 0,023) i viscerálního tuku (p = 0,034), výskyt metabolického syndromu (p = 0,006), lačná glykemie (p = 0,043), glykovaný hemoglobin (p = 0,048) a C-peptid (p = 0,026). Podíl kuřáků ve skupině se steatózou byl významně menší (p = 0,001) než ve skupině bez steatózy. Vzestup HOMA indexu (p = 0,10) a pokles QUICKI indexu (p = 0,10) nedosahovaly statistické významnosti. Se vzrůstajícím stupněm steatózy jsme pozorovali trend k poklesu maximální mitochondriální kapacity kosterního svalstva měřené 31P MR spektroskopií, ale rozdíly nebyly statisticky signifikantní (p = 0,23). Histologický stupeň steatózy dobře koreloval se stupněm steatózy stanoveným 1H MR spektroskopií (p = 0,0002).Závěry:
V pilotní studii jsme identifikovali významné klinické, laboratorní a MR parametry, které mohou přispět k predikci NAFLD u pacientů po transplantaci jater.Klíčová slova:
inzulinová rezistence – magnetická rezonance – metabolický syndrom – mitochondriální kapacita – NAFLD – transplantace jaterÚvod
Prevalence nealkoholické steatózy jater (NAFLD – non-alcoholic fatty liver disease) se v obecné populaci západních zemí pohybuje mezi 19 a 31 % [1,2]. Pacienti s NAFLD mají dle rozsáhlých studií vyšší celkovou mortalitu [3,4]. NAFLD je spojena se znaky metabolického syndromu zahrnujícími abdominální obezitu, inzulinovou rezistenci nebo diabetes mellitus 2. typu (DM2T) a aterogenní dyslipidemií, k rozvoji NAFLD významně predisponují i genetické faktory [5]. Tématu prevalence, rizikových faktorů a významu steatózy po transplantaci jater jsme se věnovali v rozsáhlé retrospektivní epidemiologické studii hodnotící celkem 2 360 potransplantačních biopsií u 548 pacientů po ortotopické transplantaci jater (OLT – orthotopic liver transplantation) [6]. Steatóza jaterního štěpu (≥ 5 %) postihovala 56,4 % pacientů, u 10,4 % pacientů byla diagnostikována steatohepatitida (NAS ≥ 5). Výskyt steatózy narůstal s dobou od OLT (30,3 % v jednom roce, 47,6 % v 10 letech). Nezávislými před-/ peritransplantačními rizikovými faktory steatózy nad 33 % byly alkoholická cirhóza, vysoký body mass index (BMI) a nízká sérová alkalická fosfatáza, iniciálně podávaný mykofenolát mofetil měl protektivní účinek. Nezávislými potransplantačními rizikovými faktory byly vysoký BMI, vysoký obsah triglyceridů v séru, konzumace alkoholu, přítomnost DM2T a nízký obsah kreatitinu. Pacienti se steatózou nad 33 % měli tendenci k horšímu dlouhodobému přežívání [6]. Retrospektivní design studie neumožňoval hodnocení dalších potenciálně významných faktorů spojených s výskytem NAFLD, zejména stupně inzulinové rezistence.
Zlatým standardem měření inzulinové rezistence je metoda hyperinzulinického euglykemického clampu, která je však nákladná a časově i organizačně značně náročná. Pro účely větších epidemiologických studií lze bazální inzulinovou rezistenci snadno hodnotit pomocí HOMA (homeostasis assessment model) indexu nebo QUICKI (quantitative insulin sensitivity check index), které vycházejí z hodnot lačné inzulinemie a lačné glykemie, nebo z poměrů lačná glykemie/inzulinemie nebo 1/lačná inzulinemie. Markerem endogenní sekrece inzulinu je C-peptid, jehož hladina není ovlivněna exogenně podávaným inzulinem [7,8].
U pacientů s DM2T a inzulinovou rezistencí byl popsán pokles v energetickém metabolizmu kosterního svalstva [9,10]. Mitochondriální oxidativní fosforylaci lze in vivo hodnotit metodou 31P MR spektroskopie při zátěži, při které se mimo jiné měří hodnota rychlosti syntézy fosfokreatinu (VPCr), a lze vypočítat maximální mitochondriální kapacitu (Qmax) [9–11].
Kromě jaterní biopsie lze stupeň jaterní steatózy hodnotit i metodou 1H MR spektroskopie [12], jejíž výhodou je neinvazivita a použitelnost i v rozsáhlých epidemiologických studiích. Jak jsme prokázali v naší předchozí práci, je tato metoda vhodná i pro hodnocení obsahu tuku v transplantovaných játrech [13].
Cílem této pilotní prospektivní studie bylo zhodnotit metabolický profil pacientů po transplantaci jater ve vztahu k přítomnosti NAFLD hodnocené histologicky a identifikovat faktory vhodné pro predikci potransplantační NAFLD.
Metodika
Do studie byli zahrnuti pacienti, kteří podstoupili protokolární jaterní biopsii v rámci standardního sledování po OLT. Studie nezahrnovala pacienty s rekurencí hepatitidy C ve štěpu, pacienty s aktuálním známým či předpokládaným abúzem alkoholu a pacienty léčené prednisonem v dávce nad 5 mg/den. Všichni pacienti podepsali informovaný souhlas se studií a s MR vyšetřením.
Vzorek biopsie jater byl získán Menghiniho technikou a zpracován standardním způsobem v naší laboratoři. Biopsie byly klasifikovány dle Kleinera et al [14] a steatóza byla rozdělena dle procenta postižených hepatocytů na stupeň 0 u < 5 %, stupeň 1 u 5 – 33 %, stupeň 2 u 33,1–66 % a stupeň 3 u > 66 %.
V den biopsie byly pacientům odebrány vzorky krve po celonočním lačnění (min. 8 hod) a stanoveny parametry glukózového a lipidového metabolizmu.
V den biopsie po krátkodobém lačnění (min. 3 hod) jsme technikou MR získali celkový objem břicha, objem podkožního a viscerálního tuku. Metodou 1H MR spektroskopie jsme stanovili procento objemu tuku v játrech, toto měření bylo prováděno ve třech standardizovaných částech jater.
Následujícího dne podstoupili pacienti po celonočním lačnění (min. 8 hod) vyšetření dynamickou 31P MR spektroskopií. Při ní pacienti prováděli plantární flexi a extenzi jedné končetiny na mechanickém ergometru vlastní výroby s pracovní zátěží cca 10 kg. Po 6 min cvičení následovalo 6 min klidu, kdy byly opakovaně měřeny intenzity signálů z oblasti musculus gastrocnemius odpovídající signálům anorganického fosfátu, fosfokreatinu (PCr), fosfodiesterů a ATP a z nich byla vypočtena iniciální VPCr a Qmax. Vyšetření se prováděla na 3T celotělovém tomografu Trio (Siemens, Německo).
Statistické hodnocení
Kategorické proměnné jsou udávány v absolutních počtech a procentech, spojité proměnné jako průměr a směrodatná odchylka. Rozdíly mezi spojitými proměnnými byly hodnoceny pomocí analýzy rozptylu (ANOVA–analysis of variance) nebo Kruskal-Wallisova testu, rozdíly v procentuálním zastoupení byly porovnány pomocí Pearsonova χ2 testu. Všechny proměnné byly porovnávány mezi třemi skupinami pacientů, se steatózou stupně 2–3, 1 a 0. Vzhledem k malému počtu pacientů v jednotlivých skupinách nebylo možné provést multivariantní analýzu. Spearmanův korelační koeficient byl použit k měření závislosti dvou spojitých veličin. Za statisticky významnou byla použita hodnota p < 0,05. Pro statistické hodnocení jsme použili JMP 10.0.0 statistický software, SAS Institute Inc. 2012.
Výsledky
V pilotní studii bylo hodnoceno 31 pacientů, 17 (54,8 %) mužů, průměrného věku 55,5 ± 9,6 let, v průměru 5,7 ± 4,0 let (rozmezí 1 – 16 let) po OLT. Indikací k transplantaci jater byla alkoholická cirhóza u 11 pacientů (35,5 %), virová hepatitida B nebo C u 6 pacientů (19,4 %), biliární cirhóza u 5 pacientů (16,1 %), jiná diagnóza u 9 pacientů (29,0 %). Průměrný BMI v době biopsie byl 27,9 ± 5,4. V době biopsie mělo 19 pacientů (61,3 %) hypertenzi a 13 pacientů (41,9 %) DM2T. Základním imunosupresivem byl takrolimus u 28 pacientů (90,3 %), cyklosporin u 1 pacienta (3,2 %) a sirolimus u 2 pacientů (6,5 %). Devět pacientů (29,0 %) bylo léčeno prednisonem v dávce 1,25–5,0 mg/den.
Histologickým zhodnocením vzorku jaterní biopsie byla u jednoho pacienta (3,2 %) přítomna steatóza stupně 3, u 11 (35,5 %) steatóza stupně 2, u 13 pacientů (41,9 %) steatóza stupně 1 a šest pacientů (19,4 %) bylo bez steatózy (stupeň 0). Klinická (tab. 1), laboratorní (tab. 2), histologická (tab. 2) a MR data (tab. 3) jsme porovnávali mezi třemi skupinami pacientů, pacienty se steatózou stupně 2–3, 1 a 0.
Table 1. Rozdíly klinických parametrů a užívané medikace mezi skupinami pacientů s různým stupněm steatózy v biopsii jater. Tab. 1. Differences in clinical parameters and medication between groups of patients with various steatosis grade on the liver biopsy. 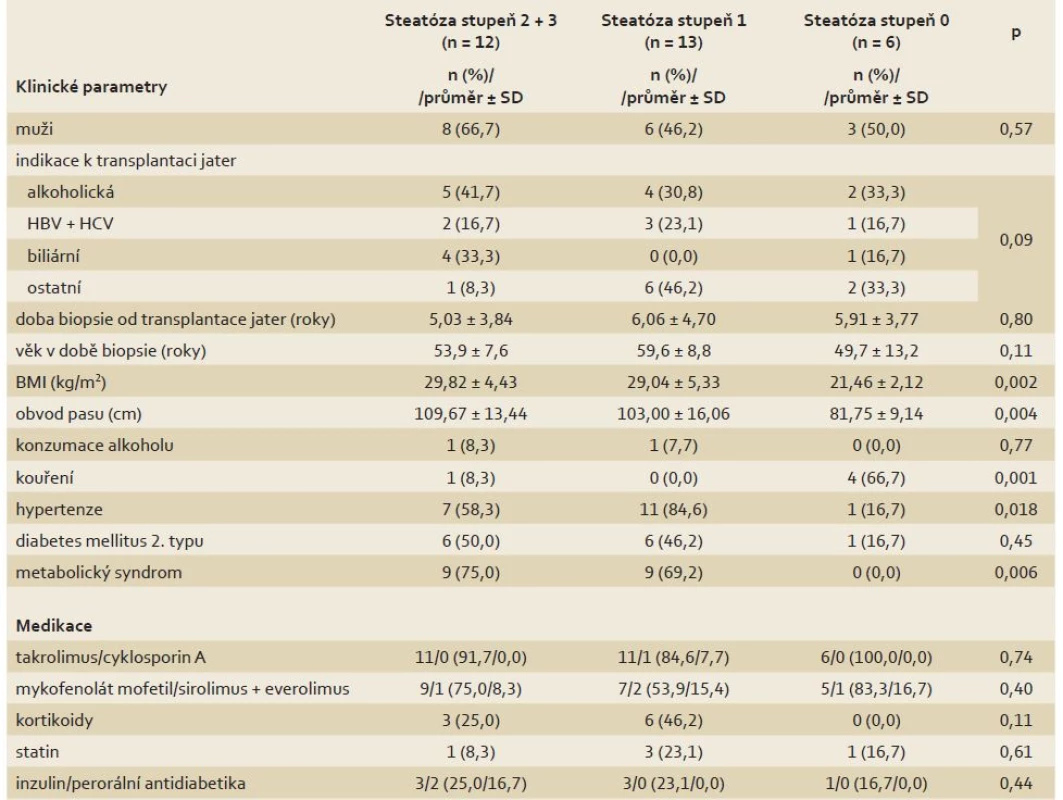
BMI – body mass index, HBV – virová hepatitida B, HCV – virová hepatitida C, SD – směrodatná odchylka Table 2. Rozdíly laboratorních a histologických parametrů mezi skupinami pacientů s různým stupněm steatózy v biopsii jater. Tab. 2. Diff erences in laboratory and histological parameters between groups of patients with various steatosis grade on the liver biopsy. 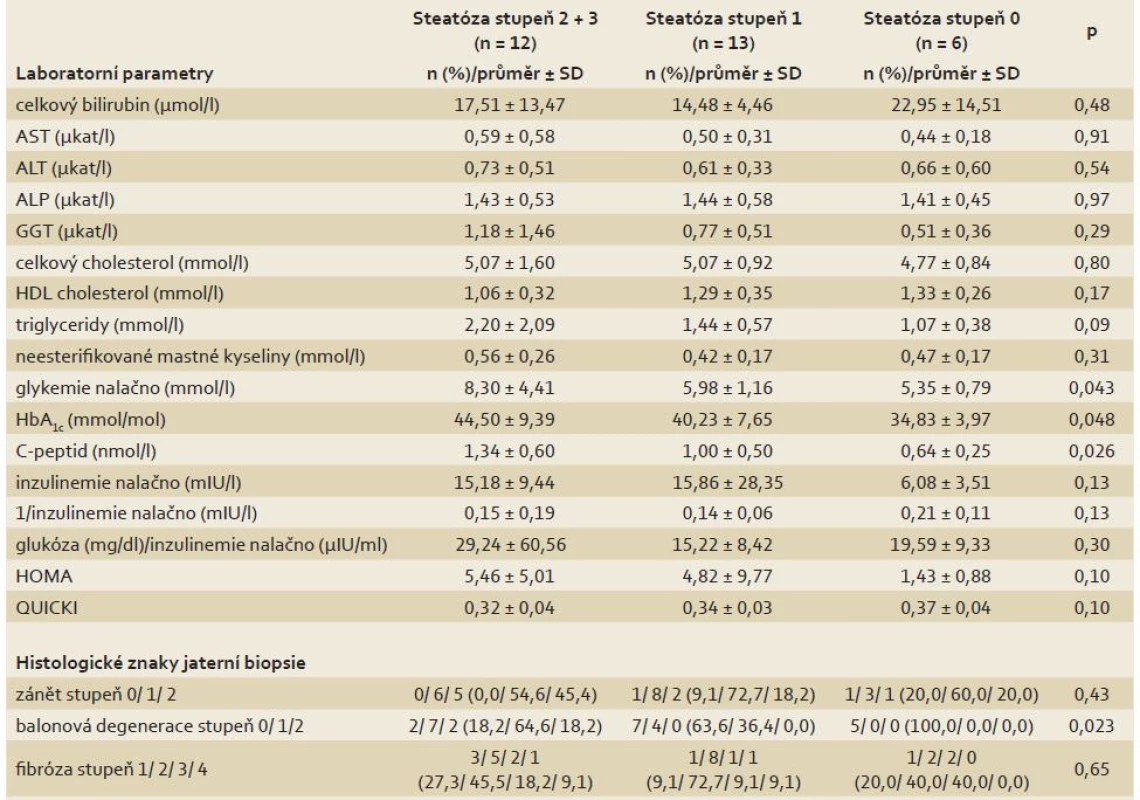
ALP – alkalická fosfatáza, ALT – alaninaminotransferáza, AST – aspartátaminotransferáza, GGT – gamaglutamyltransferáza, HbA1c – glykovaný hemoglobin, HDL – high density lipoprotein, SD – směrodatná odchylka, HOMA – homeostasis assessment model, QUICKI – quantitative insulin sensitivity check index Table 3. Rozdíly MR parametrů mezi skupinami pacientů s různým stupněm steatózy v biopsii jater. Tab. 3. Differences in MR parameters between groups of patients with various steatosis grade on the liver biopsy. 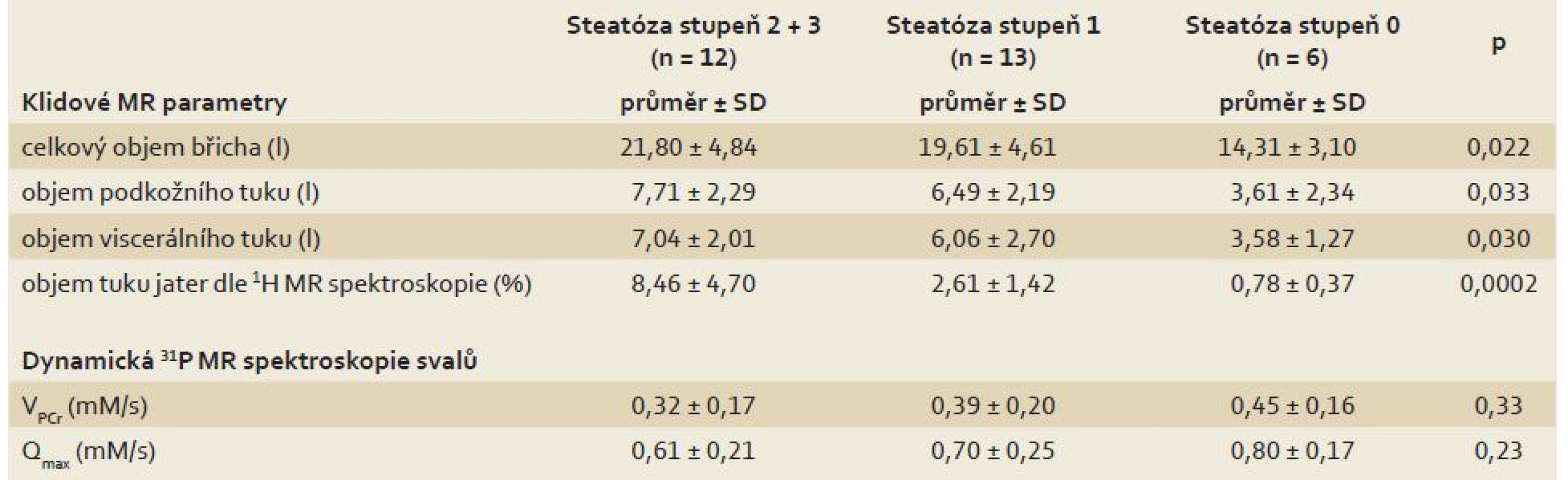
MR – magnetická rezonance, SD – směrodatná odchylka, Qmax – maximální mitochondriální kapacita, VPCr – časová konstanta regenerace fosfokreatinu po zátěži S rostoucím stupněm steatózy pozitivně koreloval BMI (p = 0,002), obvod pasu (p = 0,004), objem podkožního (p = 0,023) i viscerálního tuku (p = 0,034), výskyt metabolického syndromu (p = 0,006), lačná glykemie (p = 0,043), glykovaný hemoglobin (p = 0,048) a C-peptid (p = 0,026). Ve skupině se steatózou byl menší podíl kuřáků (p = 0,001). Mezi skupinami nebyly rozdíly v užívané imunosupresi a v hodnotách jaterních testů.
Vzestup HOMA indexu (p = 0,10), pokles QUICKI indexu (p = 0,10) a vzestup obsahu triglyceridů v séru (p = 0,09) nedosahovaly statistické významnosti.
Se vzrůstajícím stupněm steatózy jsme pozorovali trend k poklesu maximální mitochondriální kapacity (Qmax) lýtkových svalů měřené 31P MR spektroskopií, ale rozdíly nebyly statisticky signifikantní (p = 0,23). Histologický stupeň steatózy dobře koreloval se stupněm steatózy stanoveným 1H MR spektroskopií (p = 0,0002).
Z histologických parametrů s rostoucím stupněm steatózy stoupal stupeň balonové degenerace (p = 0,023), nelišil se stupeň zánětu nebo fibrózy.
V tab. 4 jsou uvedeny Spearmanovy korelační koeficienty závislosti mezi objemem jaterního tuku stanoveného 1H MR spektroskopií a parametry obezity, glukózového metabolizmu/ inzulinové rezistence a dynamické 31P MR spektroskopie. Z parametrů obezity nejlépe s objemem jaterního tuku koreloval objem viscerálního tuku a obvod pasu, dále BMI a celkový objem břicha. Z parametrů glukózového metabolizmu/ inzulinové rezistence objem jaterního tuku koreloval s lačnou glykemií, glykovaným hemoglobinem a C-peptidem. Korelace mezi objemem jaterního tuku a maximální mitochondriální kapacitou hodnocenou dynamickou 31P MR spektroskopií nebyla statisticky významná.
Table 4. Korelace mezi objemem jaterního tuku stanoveným 1H MR spektroskopií a parametry obezity, inzulinové rezistence a dynamické 31P MR spektroskopie. Tab. 4. Correlation between liver fat volume measured by 1H MR spectroscopy and parameters of obesity, insulin resistance and dynamic 31P MR spectroscopy. 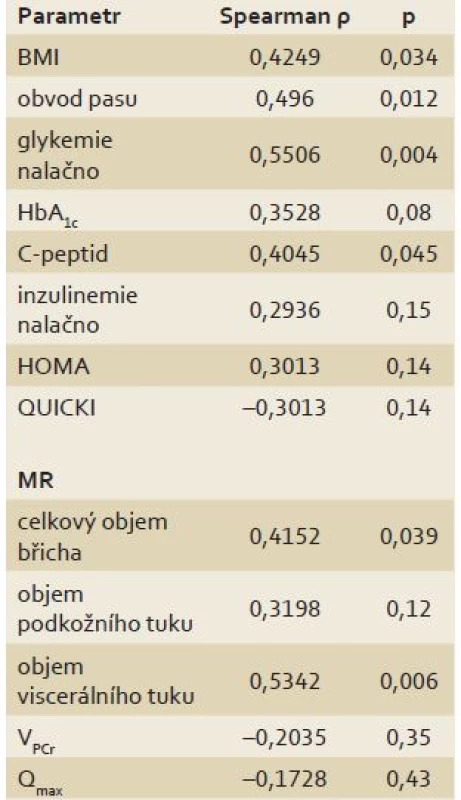
BMI – body mass index, HbA1c – glykovaný hemoglobin, HOMA – homeostasis assessment model, QUICKI – quantitative insulin sensitivity check index, MR – magnetická rezonance, Qmax – maximální mitochondriální kapacita, VPCr – časová konstanta regenerace fosfokreatinu po zátěži Diskuze a závěr
V naší předchozí retrospektivní studii [6] jsme prokázali, že steatóza jaterního štěpu se týká velkého počtu pacientů po transplantaci jater (56,4 %) a její výskyt narůstá s dobou od transplantace (30,3 % v jednom roce; 47,6 % v 10 letech). Prospektivní studií navazujeme na předchozí výsledky s cílem zpřesnit metabolický profil pacientů ve vztahu k výskytu NAFLD, výsledky pilotní části zahrnující 31 pacientů po OLT předkládáme v této práci.
Výskyt NAFLD jaterního štěpu stanovený histologicky koreloval dle očekávání s abdominální obezitou, množstvím viscerálního tuku a výskytem metabolického syndromu. Z laboratorních parametrů nejlépe se stupněm steatózy korelovaly lačná glykemie, glykovaný hemoglobin a C-peptid. C-peptid je markerem endogenní sekrece inzulinu, který není ovlivněn exogenně podávaným inzulinem, takže ve skupině pacientů s častým diabetem léčeným inzulinem dává přesnější výsledky než inzulinemie [7].
Z indexů inzulinové rezistence/ senzitivity měly v našem souboru hraniční významnost HOMA a QUICKI, ostatní indexy inzulinové rezistence (lačná glykemie/inzulinemie nebo 1/lačná inzulinemie) nebyly v našem souboru statisticky významné. Na rozdíl od literatury jsme nepozorovali vliv stupně steatózy na hladinu neesterifikovaných mastných kyselin [15,16].
S rostoucím stupněm steatózy klesala maximální mitochondriální kapacita kosterního svalstva měřená 31P MR spektroskopií, nicméně tento rozdíl nebyl v našem malém souboru statisticky signifikantní. Některé studie však naznačují, že změny v energetickém metabolizmu kosterního svalstva se mohou vyskytovat v časné fázi patofyziologie DM2T a inzulinové rezistence [9,10].
V souladu s literaturou dobře koreloval histologický stupeň steatózy s objemem jaterního tuku stanoveným 1H MR spektroskopií, což dále potvrzuje, že je tato metoda vhodná ke stanovení stupně steatózy jaterního štěpu [12,13].
Stupeň steatózy v naší studii nekoreloval s hodnotou jaterních testů a dokonce i většina pacientů se steatózou nad 33 % měla hodnoty jaterních testů v rámci normy, což zdůrazňuje nutnost hledání jiných parametrů, které mohou steatózu predikovat.
Byť má většina imunosupresiv podávaných po orgánových transplantacích nežádoucí metabolické účinky na výskyt hyperlipoproteinemie a DM2T [17], v naší pilotní studii jsme nepozorovali vliv jednotlivých imunosupresiv na stupeň steatózy jaterního štěpu. Příčinou může být delší časový odstup od transplantace u většiny nemocných (v průměru 5,7 let), kdy je snaha dávky imunosupresiv minimalizovat vždy, je-li to možné.
V naší pilotní prospektivní studii jsme prokázali, že histologický stupeň steatózy koreluje s BMI, obvodem pasu, objemem podkožního i viscerálního tuku, výskytem metabolického syndromu, lačnou glykemií, glykovaným hemoglobinem a C-peptidem. Ve skupině se steatózou byl menší podíl kuřáků. Vzestup HOMA indexu a pokles QUICKI indexu nedosahovaly statistické významnosti. Se vzrůstajícím stupněm steatózy jsme pozorovali trend k poklesu maximální mitochondriální kapacity kosterního svalstva měřené 31P MR spektroskopií, ale rozdíly nebyly statisticky signifikantní. Histologický stupeň steatózy dobře koreloval se stupněm steatózy stanoveným 1H MR spektroskopií. V dalším výzkumu je třeba pokračovat prospektivní studií na větším souboru pacientů.
Studie vznikla za podpory grantů AZV MZ ČR 15-26906A a IGA MZ ČR NT11275-6.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Doručeno: 11. 7. 2016
Přijato: 1. 8. 2016
MU Dr. Mgr. Irena Hejlová
Klinika hepatogastroenterologie
Transplantcentrum, IKEM
Vídeňská 1958/ 9
140 21 Praha 4
irhe@ikem.cz
Sources
1. Bedogni G, Miglioli L, Masutti F et al. Prevalence of and risk factors for nonalcoholic fatty liver disease: the Dionysos nutrition and liver study. Hepatology 2005; 42(1): 44 – 52.
2. Browning JD, Szczepaniak LS, Dobbins R et al. Prevalence of hepatic steatosis in an urban population in the United States: impact of ethnicity. Hepatology 2004; 40(6): 1387 – 1395.
3. Adams LA, Lymp JF, St Sauver J et al. The natural history of nonalcoholic fatty liver disease: a population-based cohort study. Gastroenterology 2005; 129(1): 113 – 121.
4. Söderberg C, Stål P, Askling J et al. Decreased survival of subjects with elevated liver function tests during a 28-year follow-up. Hepatology 2010; 51(2): 595 – 602. doi: 10.1002/ hep.23314.
5. Anstee QM, Seth D, Day CP. Genetic factors that affect risk of alcoholic and nonalcoholic fatty liver disease. Gastroenterology 2016; 150(8): 1728 – 1744. doi: 10.1053/ j.gastro.2016.01.037.
6. Hejlova I, Honsova E, Sticova E et al. Prevalence and risk factors of steatosis after liver transplantation and patient outcomes. Liver Transpl 2016; 22(5): 644 – 655. doi: 10.1002/ lt.24393.
7. Wallace TM, Matthews DR. The assessment of insulin resistance in man. Diabet Med 2002; 19(7): 527 – 534.
8. Muniyappa R, Lee S, Chen H et al. Current approaches for assessing insulin sensitivity and resistance in vivo: advantages, limitations, and appropriate usage. Am J Physiol Endocrinol Metab 2008; 294(1): E15 – E26.
9. Petersen KF, Dufour S, Befroy D et al. Impaired mitochondrial activity in the insulin-resistant offspring of patients with type 2 diabetes. N Engl J Med 2004; 350(7): 664 – 671.
10. Scheuermann-Freestone M, Madsen PL,Manners D et al. Abnormal cardiac and skeletal muscle energy metabolism in patients with type 2 diabetes. Circulation 2003; 107(24): 3040 – 3046.
11. Šedivý P, Kipfelsberger MC, Dezortová M et al. Dynamic 31P MR spectroscopy of plantar flexion: influence of ergometer design, magnetic field strength (3 and 7 T), and RF-coil design. Med Phys 2015; 42(4): 1678 – 1689. doi: 10.1118/ 1.4914448.
12. Thomsen C, Becker U, Winkler K et al. Quantification of liver fat using magnetic resonance spectroscopy. Magn Reson Imaging 1994; 12(3): 487 – 495.
13. Hájek M, Dezortová M, Wagnerová Det al. MR spectroscopy as a tool for in vivo determination of steatosis in liver transplant recipients. MAGMA 2011; 24(5): 297 – 304. doi: 10.1007/ s10334-011-0264-9.
14. Kleiner DE, Brunt EM, Van Natta M et al. Design and validation of a histological scoring system for nonalcoholic fatty liver disease. Hepatology 2005; 41(6): 1313 – 1321.
15. Zhang J, Zhao Y, Xu C et al. Association between serum free fatty acid levels and nonalcoholic fatty liver disease: a cross-sectional study. Sci Rep 2014; 4 : 5832. doi: 10.1038/ srep05832.
16. Larter CZ, Yeh MM, Haigh WG et al. Hepatic free fatty acids accumulate in experimental steatohepatitis: Role of adaptive pathways. J Hepatol 2008; 48(4): 638 – 647. doi: 10.1016/ j.jhep.2007.12.011.
17. Sorice GP, Muscogiuri G, Mezza T et al. Metabolic syndrome in transplant patients: an academic or a health burden? Transplant Proc 2011; 43(1): 313 – 317. doi: 10.1016/ j.transproceed.2010.09.099.
Labels
Paediatric gastroenterology Gastroenterology and hepatology Surgery
Article was published inGastroenterology and Hepatology

2016 Issue 4-
All articles in this issue
- Klinická a experimentální gastroenterologie
- Pankreatické cystické léze u pacientů po transplantaci jater
- První hodnocená zkušenost s testem Septin 9 v České republice
- Význam regulácie tranzientných relaxácií dolného pažerákového zvierača v patogenéze pažerákovej refluxovej choroby
- Bronchogenní cysta jícnu
- Apoptóza při vývoji kolorektální neoplazie
- Primární adenokarcinom žaludku s yolk sac diferenciací
- Metabolický profil pacientů po transplantaci jater ve vztahu k rozvoji NAFLD – výsledky pilotní studie
- Nezvyklá manifestace časného kryptogenního hepatocelulárního karcinomu
- Nedostatočná liečba tiopurínmi u pacientov s nešpecifickými zápalovými ochoreniami čreva odoslaných na anti-TNF liečbu
- Obstrukce duodena a obstrukční ikterus jako první symptomy primárního maligního duodenálního lymfomu
- Noví členové redakční rady časopisu
- Výběr z mezinárodních časopisů
- Olysio® (simeprevir)
- Flush, rosacea, alebo červenanie – pochopenie rozdielov
- Falk Symposium 202 – Evolving therapies in clinical practice in IBD
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- První hodnocená zkušenost s testem Septin 9 v České republice
- Obstrukce duodena a obstrukční ikterus jako první symptomy primárního maligního duodenálního lymfomu
- Flush, rosacea, alebo červenanie – pochopenie rozdielov
- Bronchogenní cysta jícnu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

