-
Medical journals
- Career
- Contact
Endosonografie v diagnostice choledocholitiázy
Authors: T. Chvátalová; J. Martínek; F. Závada; M. Zavoral
Authors‘ workplace: Interní klinika 1. LF UK a ÚVN Praha
Published in: Gastroent Hepatol 2012; 66(3): 160-164
Category: Digestive Endoscopy: Original Article
Overview
Choledocholitiáza je sice běžné onemocnění, které ale může mít závažné komplikace. Diagnostika konkrementů ve žlučových cestách udělala v posledním desetiletí zásadní pokrok a zcela se změnil přístup k pacientům při podezření na tuto afekci. Článek přehledně shrnuje výhody a nevýhody v současnosti používaných vyšetřovacích metod (EUS a MRCP) a uvádí návrh doporučeného postupu. Uvedené výsledky potvrzuje i závěr retrospektivní studie provedené v letech 2008–2010 v ÚVN. Při analýze souboru 109 endosonografických vyšetření v indikaci suspektní choledocholitiáza činila senzitivita EUS pro choledocholitiázu 87,9 %, specificita 94,7 %, pozitivní prediktivní hodnota 87,9 % a negativní prediktivní hodnota 94,7 %.
Klíčová slova:
choledocholitiáza – EUS-MRCPCholelitiáza je onemocnění, které postihuje 6–21 % dospělé evropské populace [1]. Choledocholitiáza s cholecystolitiázou se vyskytuje současně v 5–20 % případů [2,3], u pacientů s akutní biliární pankreatitidou je prevalence choledocholitiázy 18–33 % [3]. Choledocholitiáza má většinou původ ve žlučníku, jen malá část konkrementů vzniká přímo ve žlučovodech. Po cholecystektomii se choledocholitiáza objevuje u 1–5 % nemocných [4]. Žlučové kameny dělíme tradičně na cholesterolové (80 %), pigmentové (15 %) a smíšené (5 %). Cholesterolové konkrementy nacházíme predilekčně u žen, ve vyšším věku, u obezních, diabetiků, rizikovými faktory jsou dále gravidita, parenterální výživa, rychlé zhubnutí. Pigmentové kameny (černé a hnědé) jsou obecně vzácnější, černé se vyskytují u nemocných s hemolýzou, jaterní cirhózou a po náhradě srdečních chlopní. Hnědé kameny jsou spjaté s cholestázou a typicky s bakteriální nebo parazitární infekcí žluče, bývají mnohočetné a často je nacházíme i v intrahepatálních žlučových cestách [5]. Klinický obraz je společný všem bez ohledu na etiologii. Kolísá od zcela asymptomatického, přes biliární dyspepsii a koliku, až po akutní biliární pankreatitidu či septický stav při akutní cholangoitidě. S pestrostí klinických projevů choledocholitiázy souvisí často obtížná diferenciální diagnostika od jiných afekcí v oblasti podjaterní krajiny a epigastria.
Diagnostika
Diagnóza extra - i intrahepatální choledocholitiázy je postavena na nálezu konkrementu ve žlučových cestách při zobrazovacím vyšetření. Anamnéza, laboratorní a fyzikální nález mají pouze přídatnou hodnotu. Samotné sice pro diagnózu nestačí, ale v nejasných případech jsou důležité pro stanovení pravděpodobnosti choledocholitiázy, a tím určení dalšího postupu. Sporným „zlatým standardem“ v diagnostice choledocholitiázy jsou od konce 70. let minulého století endoskopická retrográdní cholangiopankreatikografie (ERCP) a intraoperační cholangiografie (IOC). Z dnešního pohledu sporným, protože senzitivita ani specificita cholangiografie není zdaleka 100 %, uvádí se 89–93 % [6] a zejména drobné konkrementy v dilatovaném žlučovodu mohou být přehlédnuty. Obě metody s sebou navíc přináší nezanedbatelná rizika. Při ERCP se komplikace (krvácení, akutní pankreatitida, perforace) vyskytují až v 5–10 %, mortalita je uváděna v rozmezí 0,02–0,5 % [7]. Je důležité mít na paměti, že i diagnostické ERCP může skončit fatální akutní pankreatitidou! IOC není vzhledem ke svému chirurgickému charakteru vůbec vhodná pro běžnou diagnostiku. Proto byla od počátku 90. let minulého století snaha nahradit tyto metody méně invazivními a ERCP a IOC ponechat jen k řešení již ověřené choledocholitiázy. Bylo vyvinuto několik skórovacích systémů založených na kombinaci klinických, laboratorních a zobrazovacích nálezů, nicméně jejich pozitivní prediktivní hodnota je nízká (75 %) [8]. Abdominální ultrasonografie (UZ) a výpočetní tomografie (CT) se pro diagnostiku choledocholitiázy neukázaly přínosem, ze studie Sugiyamy et al z roku 1997 vyplývá senzitivita UZ a CT pro choledocholitiázu 63 %, resp. 71 % [9]. Již v roce 1992 se ale Edmundowitz et al poprvé zmíňují o použití endosonografie (EUS) v této indikaci [10] a v roce 1999 de Lédinghen et al publikovali prospektivní studii porovnávající EUS a magnetickou cholangiografii (MRCP) [11]. EUS i MRCP jsou v diagnostice choledocholitiázy minimálně stejně senzitivní (93 %, resp. 85 %) i specifické (96 %, resp. 93 %) jako ERCP [12,13]. Selekcí nemocných významně snižují (o 50–70 %) počet zbytečných a potencionálně rizikových ERCP [14,15] a naopak u nemocných nakonec k ERCP indikovaných se dvěma vyšetřeními/endoskopiemi nijak zásadně nezvyšuje zatížení pacienta, jak by se na první pohled mohlo zdát. Za nejvýhodnější je považováno provedení EUS a případné ERCP v jednom sezení, což snižuje náklady, zkracuje hospitalizaci a je dobře tolerováno i nemocnými [16,17]. V ČR se touto problematikou jako první systematicky zabýval Tozzi et al [18] v rozsáhlé prospektivní studii porovnávající abdominální ultrasonografii (UZ), EUS a ERCP v diagnostice obstrukce extrahepatálních cest.
EUS či MRCP
Zda je v této indikaci výtěžnější MRCP či EUS, je velmi složitá otázka, na kterou v současné době neexistuje jednoznačná odpověď. Byla provedena řada studií a metaanalýz [9,10,19–25], z nichž vyplývá stejná vypovídací schopnost obou metod, avšak existují situace, při kterých upřednostňujeme jedno či druhé vyšetření (tab. 1).
Table 1. Porovnání výhod a nevýhod EUS a MRC P v diagnostice choledocholitiázy. (*) při současném provedení ERC P. Tab. 1. Comparison of advantages and disadvantages of EUS and MRCP for diagnosis of choledocholithiasis. (*) if ERCP is done immediately. 
Hlavní výhodou MRCP je její kompletně neinvazivní charakter, ale s omezením četných kontraindikací – kardiostimulátor, klaustrofobie (uvádí se 1–5 % populace), obezita [10]. MRCP dokáže kvalitně zobrazit bifurkaci a intrahepatální žlučové cesty a naopak má „Achillovu patu“ v oblasti Vaterovy papily (spasmus svěrače může imitovat konkrement, časté falešně pozitivní nálezy) (obr. 1). Dále se uvádí její horší rozlišovací schopnost pro konkrementy menší než 1,5–2 mm. Kvalita MRCP výrazně závisí na použité technice vyšetření a také na erudici hodnotícího – i MRCP je zatíženo subjektivním pohledem [19,26]. Největší nevýhodou MRCP však zůstává nemožnost okamžitého provedení terapeutického zásahu a prodlení při přesunech pacienta a při čekání na výsledek MRCP.
Image 1. Falešně pozitivní nález na MRC P nad Vaterovou papilou (šipka). Při následném ERC P nebyl konkrement nalezen. Fig. 1. False positive finding on MRCP in the area of Vater’s papilla (arrow). No lithiasis was found during the subsequent ERCP. 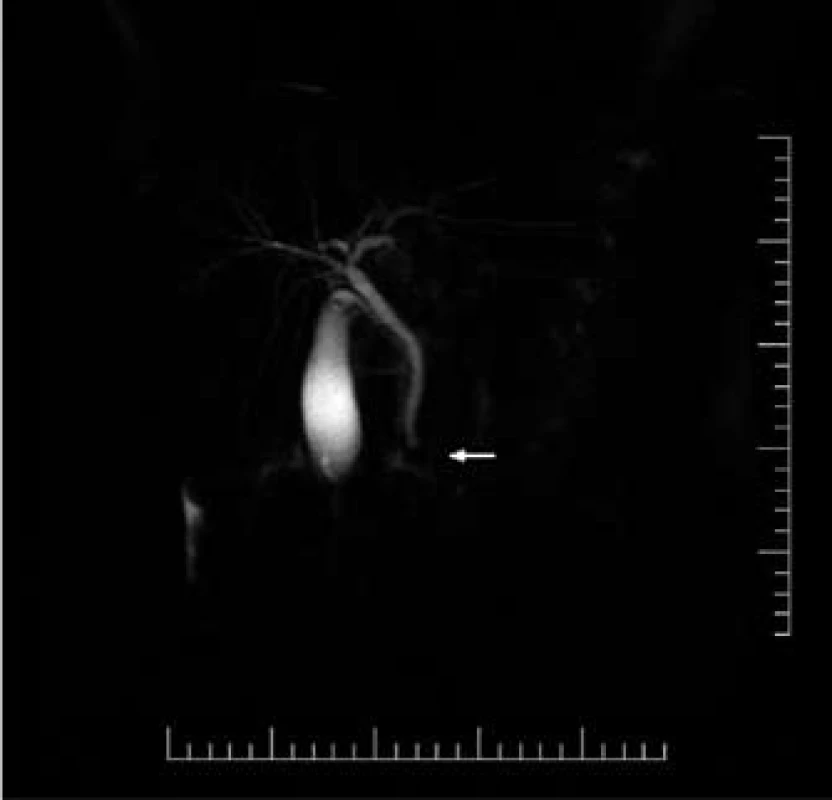
Endosonografie s sebou přináší rizika a kontraindikace shodné s diagnostickou endoskopií horní části trávicího traktu, navíc je však třeba počítat s obtížnou vyšetřitelností nemocných po operacích v horní části gastrointestinálního traktu (Billroth II, stenóza pyloru, hepatikojejunoanastomóza apod.). Limitací pro EUS je oblast hilu jater a intrahepatálních žlučových cest (mimo dosah přístroje, zdroj falešně negativních nálezů) [27,28]. Proti MRCP se uvádí vysoká senzitivita EUS pro drobné konkrementy a sludge (rozlišení 0,1 mm). Výsledek EUS sice závisí na zkušenosti vyšetřujícího, ovšem tzv. „learning curve“ je proti jiným EUS indikacím relativně krátká – do jednoho roku [29]. EUS je velmi výhodná z časového a organizačního hlediska, neboť dovoluje v případě nálezu konkrementu okamžité provedení ERCP. Ideálně v jednom sezení, na jednom sále, jedním lékařem a v takovém případě trvá celé vyšetření 30–60 min.
Naše zkušenosti
Metodika
Na Interní klinice 1. LF UK a ÚVN Praha jsme provedli retrospektivní studii, do které jsme zahrnuli 107 pacientů (68 žen, medián věku 62 let; 39 mužů, medián věku 66 let) v letech 2008–2010 vyšetřovaných pro suspektní choledocholitiázu. Jednalo se o nemocné s bolestmi břicha a s mírnou dilatací choledochu (6–10 mm) nebo laboratorními známkami cholestázy (elevace GGT a ALP). Tito nemocní byli nejprve vyšetřeni endosonograficky, v případě pozitivního nálezu ve smyslu choledocholitiázy (hyperechogenita se stínem, nebo beze stínu) bylo ihned provedeno ERCP. Pacienti, u kterých byl endosonografický nález negativní, nebylo ERCP v této fázi indikováno a byli dále sledováni do stanovení diagnózy. Na endosonografii se podíleli tři zkušení endosonografisté, používali jsme standardní radiální a lineární echoendoskopy firmy Olympus (GF UE 160 a GF UCT 140). Endoskopie probíhala za analgosedace (fentanyl, midazolam a buscopan).
Výsledky
U 107 pacientů jsme provedli celkem 109 endosonografických vyšetření žlučových cest (76 vyšetření radiálním, 30 lineárním a 3 oběma typy přístrojů). Ve 33 případech byl endosonografický nález pozitivní, v 76 negativní. Ze 33 nálezů hyperechogenity s akustickým stíenm ve žlučovodu, nebo bez něj byla choledocholitiáza při následném ERCP potvrzena ve 29 případech, zbývající 4 vyšetření byly falešně pozitivní (1× Klatskinův tumor, 3× nález zcela negativní). U 76 původně endosonograficky negativních nálezů bylo nakonec u 10 nemocných s odstupem ERCP indikováno (většinou pro neustupující cholestázu). U čtyř z nich byla zjištěna choledocholitiáza a u šesti pacientů byla pro zhoršování laboratorního nálezu jiná příčina (schéma 1). Specificita, senzitivita, pozitivní prediktivní hodnota a negativní prediktivní hodnota endosonografie pro diagnózu choledocholitiázy jsou uvedeny v tab. 2. Nezaznamenali jsme žádné komplikace spojené s endosonografií. Z výsledků vyplývá, že jsme u 66 pacientů (60 %) správně ustoupili od původně zvažovaného ERCP.
Schéma 1. Endosonografická vyšetření žlučových cest a zjištěné nálezy. Schema 1. Biliary tree endosonography and findings. 
Table 2. Výsledky studie. Tab. 2. Results of the study. 
Racionální přístup k pacientovi s choledocholitiázou
V přístupu k nemocným vycházíme ze subjektivních stesků (lokalizace a charakter bolesti, vyvolávající a ulevující faktory), fyzikálního nálezu (ikterus, palpační bolestivost břicha, známky sepse), anamnézy (známá cholelitiáza, stav po cholecystektomii, stav po pankreatitidě nejasné etiologie), laboratorního obrazu (elevace bilirubinu, GGT a ALP, transamináz), sonografického nálezu (cholecystolitiáza, dilatace žlučových cest). Na základě získaných údajů rozdělíme pacienty na dvě skupiny. Nemocní s velmi pravděpodobnou choledocholitiázou (vysokoriziková skupina) [27] (tab. 3), tj. s akutní cholangoitidou, s akutní pankreatitidou se známkami cholangoitidy, s obstrukčním ikterem s dilatací žlučových cest, nebo bez ní. U těchto nemocných je indikována ERCP. U skupiny nemocných se suspektní choledocholitiázou (skupina se středním rizikem) [27](tab. 3), tedy u těch s nejasnými bolestmi břicha či nespecifickou dyspepsií, mírnou elevací jaterních testů nebo dynamikou v jaterních testech (podezření na pasáž konkrementu) a hraniční nebo i normální šíří žlučových cest při sonografii, indikujeme nejprve EUS či MRCP. V případě pozitivního nálezu pro choledocholitiázu (hyperechogenita v hepatocholedochu při EUS či defekt při MRCP) (obr. 2) provádíme ERCP (schéma 2).
Image 2. 30letý muž přijatý pro akutní pankreatitidu biliární etiologie, na UZ břicha mnohočetná cholecystolitiáza, choledochus nebyl dilatován. Laboratorně celkový bilirubin 26 μmol/l, ALT 6,2 μkat/l, AST 2,9 μkat/l, GGT 5,2 μkat/l, ALP 5,2 μkat/l, pankreatická amyláza 16 μkat/l. Při endosonografii žlučových cest jsme nalezli hyperechogenitu s akustickým stínem 20 mm nad Vaterovou papilou (obr. 2A, šipka), při následném ERC P byla choledocholitiáza extrahována (obr. 2B, šipka). Fig. 2. 30-year old man admitted for acute biliary pancreatitis. Multiple cholecystolithiasis observed on abdominal ultrasound. Choledochus was not dilated. Laboratory tests revealed bilirubin 26 μmol/l, ALT 6.2 μkat/l, AST 2.9 μkat/l, GGT 5.2 μkat/l, ALP 5.2 μkat/l and pancreatic amylasis 16 μkat/l. During endosonography of the bile duct a small hyperechogenity with acoustic shadow was found 20 mm above the papilla vateri (fig. 2A, arrow). The choledocholithiasis was extracted during the subsequent ERCP (fig. 2B, arrow). 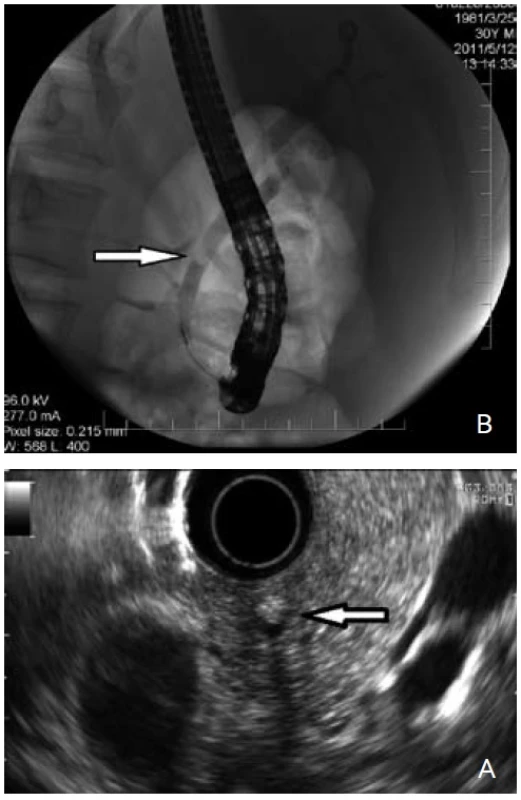
Schéma 2. Přístup k pacientovi s cholecystolitiázou a suspektní choledocholitiázou. Schema 2. Approach to patient with cholecystolithiasis and suspected choledocholithiasis. 
Table 3. Stratifikace rizika choledocholitiázy na základě anamnézy, laboratorních výsledků a UZ. Tab. 3. Establishing risk of choledocholithiasis – based on case history, laboratory results and sonography results. 
Závěr
Choledocholitiáza je relativně běžným onemocněním doprovázeným často řadou závažných komplikací, diagnostický proces proto musí být rychlý a efektivní. EUS a MRCP umožňují rychlé a bezpečné potvrzení, či vyloučení choledocholitiázy v nejasných situacích. ERCP je terapeutickou metodou jen v případech již zjištěné nebo velmi pravděpodobné choledocholitiázy. Přímé provedení ERCP bez předchozí EUS nebo MRCP u pacienta se středním rizikem choledocholitiázy je v současné době již nutné považovat za chybu a případná komplikace při ERCP je neobhajitelná.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 13. 1. 2012
Přijato: 30. 1. 2012
MUDr. Tereza Chvátalová
Interní klinika 1. LF UK a ÚVN Praha
U Vojenské nemocnice 1200
169 02 Praha 6
tereza.chvatalova@uvn.cz
Sources
1. Aerts R, Penninckx F. The burden of gallstone disease in Europe. Aliment Pharmacol Ther 2003; 18 (Suppl 3): 49–53.
2. Tse F, Barkun JS, Barkun AN. The elective evaluation of patients with supected choledocholithiasis undergoing laparoscopic cholecystectomy. Gastrointest Endosc 2004; 60(3): 437–438.
3. Maple JT, Ben-Menachem T, Anderson MA et al. The role of endoscopy in the evaluation of suspected choledocholthiasis. Gastrointest Endosc 2010; 71(1): 1–9.
4. Hermann RE. The spectrum of biliary stone disease. Am J Surg 1989; 158(3): 171–173.
5. Brodanová M, Beneš J, Dufek V et al. Onemocnění žlučníku a žlučových cest. Praha: Grada Publishing 1998.
6. Prat F, Amouyal G, Amouyal P et al. Prospective controlled study of endoscopic ultrasonography and endoscopic retrograde cholangiography in patients with suspected common bile duct lithiasis. Lancet 1996; 347(8994): 75–79.
7. Freeman ML, Nelson DB, Sherman S et al. Complications of endoscopic biliary sphincterotomy. N Engl J Med 1996; 335(13): 909–918.
8. Topal B, Fieuws S, Tomczyk K et al. Clinical models are inaccurate in predicting bile duct stones in situ for patients with gallbladder. Surg Endosc 2009; 23(1): 38–44.
9. Sugiyama M, Atomi Y. Endoscopic ultrasonography for diagnosing choledocholithiasis: a prospective comparative study with ultrasonography and computed tomography. Gastrointest Endosc 1997; 45(2): 143–146.
10. Edmundowitz SA, Aliperti G, Middleton WD. Preliminary experience using endoscopic ultrasonography in the diagnosis of choledocholithiasis. Endoscopy 1992; 24(9): 774–778.
11. De Lédinghen V, Lecesne R, Raymond JM et al. Diagnosis of choledocholithiasis: EUS or magnetic resonance cholangiography? A prospective controlled study. Gastrointest Endosc 1999; 49(1): 26–31.
12. Verma D, Kapadia A, Eisen GM et al. EUS vs MRCP for detection of choledocholithiasis. Gastrointest Endosc 2006; 64(2): 248–254.
13. Aljebreen A, Azzam N, Eloubeidi MA. Prospective study of endoscopic ultrasound performance in suspected choledocholithiasis. J Gastroenterol Hepatol 2006; 23(5): 741–745.
14. Lee YT, Chan FK, Leung WK et al. Comparison of EUS and ERCP in the investigation with suspected biliary obstruction caused by choledocholithiasis: a randomized study. Gastrointest Endosc 2008; 67(4): 660–668.
15. Buscarini E, Tansini P, Vallisa D et al. EUS for suspected choledocholithiasis: do benefits outweight costs? A prospectice controlled study. Gastrointest Endosc 2003; 57(4): 510–518.
16. Fabbri C, Polifermo AM, Luigiano C et al. Single session versus separate session endoscopic ultrasonography plus endoscopic retrograde cholangiography in patients with low to moderate risk for choledocholithiasis. J Gastroenterol Hepatol 2009; 24(6): 1107–1112.
17. Polkowski M, Regula J, Tilszer A et al. Endoscopic ultrasound versus endoscopic retrograde cholangiography for patients with intermediate probability of bile duct stones: a randomized trial comparing two management strategies. Endoscopy 2007; 39(4): 296–303.
18. Tozzi I, Procházka V, Konečný M et al. Vyhodnocení senzitivity a specificity radiální endoskopické ultrasonografie v porovnání s ERCPP v diagnostice obstrukce extrahepatických žlučových cest. Folia Gastroenterol Hepatol 2008; 6(4): 128–136.
19. Ainsworth AP, Rafaelsen SR, Wamberg PA et al. Is there a difference in diagnostic and clinical impact between endoscopic ultrasonography and magnetic resonance cholangiopancreatography? Endoscopy 2003; 35(12): 1029–1032.
20. Ledro-Cano D. Suspected choledocholithiasis: endoscopic ultrasound or magnetic resonance cholangio-pancreatography? A systematic review. Eur J Gastroenterol Hepatol 2007; 19(11): 1007–1011.
21. Materne R, Van Beers BE, Gigot JF et al. Extrahepatic biliary obstruction: magnetic resonance imaging compared with endoscopic ultrasonography. Endoscopy 2000; 32(1): 3–9.
22. Schmidt S, Chevalier P, Novellas S et al. Choledocholithiasis: repetitive thick-slab single-shot projection magnetic resonance cholangiopancreaticography versus endoscopic ultrasonograpgy. Eur Radiol 2007; 17(1): 241–250.
23. Fernándéz-Esparrach G, Gines A, Sánchéz M et al. Comparison of Endoscopic Ultrasonography and Magnetic Resonance Cholangiopancreaticography in th Diagnosis of pancreatobiliary Diseases: A prospective Study. Am J Gastroenterol 2007; 102(8): 1632–1639.
24. Romagnuolo J, Bardou M, Rahme E et al. Magnetic resonance cholangiopancreatolography: a meta analysis of test performance in suspected biliary disease. Ann Intern Med 2003; 139(7): 547–557.
25. Garrow D, Miller S, Sinha D et al. Endoscopic ultrasound: a metanalysis of test performance in suspected biliary obstruction. Clin Gastroenterol Hepatol 2007; 5(5): 616–623.
26. McMahon CJ. The relative roles of magnetic resonance cholangiopancreatography [MRCP] and endoscopic ultrasound in diagnosis of common bile duct calculi: a critically appraised topic. Abdom Imaging 2008; 33(1): 6–9.
27. Tse F, Barkun AN, Armstrong D, Moayyedi P. EUS: a meta-analysis of test performance in suspected choledocholithiasis. Gastrointest Endosc 2008; 67(2): 235–244.
28. Palazzo L, O´Toole D. EUS in common bile duct stones. Gastrointest Endosc 2002; 56 (4 Suppl): S49–57.
29. Denis BJ, Bas V, Goudot C et al. Accuracy of endoscopic ultrasonography for diagnosis of common bile duct stones [abstract]. Gastroenterology 1993; 104: A358.
Labels
Paediatric gastroenterology Gastroenterology and hepatology Surgery
Article was published inGastroenterology and Hepatology

2012 Issue 3-
All articles in this issue
- Jak kvalitní je Vaše kolonoskopie?
- Endosonografie v diagnostice choledocholitiázy
- Využití NBI v diagnostice a sledování pacientů s Barrettovým jícnem
- Endoskopický trénink na neživém zvířecím modelu zlepšuje endoskopické dovednosti
- Snížení dyskomfortu spojeného s kolonoskopií použitím kombinace vodní imerze a insuflace oxidu uhličitého
- Endosonograficky navigovaná alkoholová ablácia cystickej neoplázie pankreasu
- Pozitivita imunoglobulinu IgG4 v krevním séru u osob s karcinomem slinivky břišní
- Korelace indikace k resekci pankreatu s následným histopatologickým nálezem
- Antibiotická profylaxe u akutní pankreatitidy
- Očekávané počty nádorů jater, žlučníku a pankreatu ve světě
- Primární sklerozující cholangoitida u pacientů s idiopatickými střevnímí záněty
- Standardní diagnostický a terapeutický postup u chronické infekce virem hepatitidy C (HCV)
- Highlights of the 34th Czech and Slovak endoscopic days
- Zpráva o DDW 2012
- Ostrava Live Endoscopy
- Prof. MUDr. Julius Špičák, CSc., šedesátníkem
- Prim. MUDr. Karel Lukáš, CSc., sedmdesátiletý
- Moviprep® – moderní příprava střeva před vyšetřením
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Moviprep® – moderní příprava střeva před vyšetřením
- Antibiotická profylaxe u akutní pankreatitidy
- Primární sklerozující cholangoitida u pacientů s idiopatickými střevnímí záněty
- Snížení dyskomfortu spojeného s kolonoskopií použitím kombinace vodní imerze a insuflace oxidu uhličitého
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

