-
Medical journals
- Career
Zhodnocení onkologických výsledků pomocí prognostických modelů u pacientů operovaných pro renální karcinom – zkušenosti jednoho pracoviště
Authors: Marek Kašík; Michal Fedorko
Authors‘ workplace: Urologická klinika LF MU a FN Brno
Published in: Ces Urol 2025; 29(3): 158-163
Category: Original article
doi: https://doi.org/10.48095/cccu2025017Overview
Hlavní stanovisko práce: Práce si klade za cíl vyhodnotit výsledky operační léčby renálního karcinomu na Urologické klinice FN Brno v letech 2014–2022 pomocí prognostických modelů.
Cíl studie: Cílem této studie je vyhodnotit soubor pacientů operovaných pro renální karcinom na našem pracovišti s ohledem na prognostické faktory a s využitím prognostických modelů podle Leiboviche a GRANT skóre. Soubor pacientů a metody: Bylo provedeno retrospektivní vyhodnocení základních dat pacientů, kteří podstoupili radikální či parciální nefrektomii na Urologické klinice FN Brno mezi lety 2014 a 2022. Pacienti byly rozděleni do prognostických skupin na základě klinických a patologických charakteristik zahrnutých do běžně využívaných prognostických modelů (Leibovich 2003 a GRANT skóre). Pro jednotlivé rizikové skupiny bylo stanoveno 5leté přežití bez progrese. Jako komplikace výkonu byly hodnoceny závažné komplikace stupně Clavien-Dindo IIIb–V. Výsledky: Mezi lety 2014 a 2022 bylo na našem pracovišti operováno 482 pacientů s podezřením na tumor ledviny, z toho bylo 312 mužů (64,7 %) a 170 žen (35,3 %). V definitivní histologii byly maligní nálezy potvrzeny u 424 pacientů (87,9 %), 58 nálezů bylo histologicky benigních (12,1 %). Recidiva se vyskytla u 35 pacientů s renálním karcinomem, což odpovídá 8,3 % případů s mediánem odstupu 33 měsíců od operace. Pětileté přežití bez progrese pro skupinu s nízkým, středním a vysokým rizikem dle Leibovichova modelu bylo 94,8; 89,6; resp. 63,2 %, dle modelu GRANT 94,1; 95,0; resp. 73,6 % v případě nula, jednoho, resp. dvou přítomných faktorů. Závěr: Naše analýza potvrzuje důležitost používání zavedených prognostických modelů pro renální karcinom, jako jsou Leibovich a GRANT skóre, při hodnocení rizika recidivy a celkového přežití po chirurgické léčbě. Oba skórovací systémy prokázaly svou schopnost rozlišit mezi pacienty s příznivou a nepříznivou prognózou.
Klíčová slova:
parciální nefrektomie – prognostický model – radikální nefrektomie – renální karcinom – rizikové faktory
Úvod
Renální karcinom (RCC – renal cell carcinoma) patří mezi nejčastější malignity urogenitálního traktu, přičemž jeho incidence v posledních desetiletích narůstá. Díky rozvoji diagnostických metod je stále častěji zachycován v časných stadiích, což významně ovlivňuje možnosti léčby a prognózu pacientů.
V České republice (ČR) je incidence RCC jedna z nejvyšších na světě, dle dat Globocanu z roku 2022 mají vyšší incidenci RCC pouze Bělorusko, Uruguay a Lotyšsko [1]. Dle dat Národního onkologického registru bylo v roce 2022 v ČR diagnostikováno 3 290 zhoubných nádorů ledvin, hrubá incidence představovala více než 30 případů na 100 000 obyvatel [2]. Muži jsou postiženi častěji než ženy, a to v poměru 2 : 1. Vzhledem k populačnímu stárnutí a změnám životního stylu se očekává, že výskyt tohoto onemocnění bude i nadále růst. Mezi uznávané rizikové faktory RCC patří kouření, hypertenze, obezita a metabolický syndrom [3]. Nejvyšší počet pacientů je diagnostikován ve věku 65–74 let.
Prognóza pacientů s RCC je ovlivněna řadou klinických, patologických a molekulárních faktorů [3–5]. Mezi nejvýznamnější prognostické faktory patří:
- stadium onemocnění podle TNM klasifikace, kde přítomnost lymfatických uzlinových metastáz (N) a vzdálených metastáz (M) výrazně zhoršuje prognózu;
- velikost nádoru, přičemž nádory < 4 cm (T1a) mají podstatně lepší prognózu než větší léze;
- histologický subtyp;
- jaderný grading dle ISUP (International Society of Urological Pathology), který hodnotí jadernou atypii a je klíčový pro predikci agresivity nádoru;
- přítomnost nekrotických ložisek a vaskulární invaze, které signalizují vyšší riziko recidivy a metastáz;
- celkový stav pacienta hodnocený např. podle skóre Karnofského nebo ECOG (Eastern Cooperative Oncology Group), který ovlivňuje nejen prognózu, ale i volbu terapeutické strategie;
- biomarkery a genetické faktory, jako jsou mutace v genech VHL, PBRM1, BAP1 a další, které mohou mít prognostický a prediktivní význam.
K přesnějšímu hodnocení prognózy pacientů se využívají různé prognostické modely, které kombinují zejména klinické a patologické parametry. Nejčastěji využívané modely pro lokalizované onemocnění shrnuje tab. 1. Pro vyhodnocení naší kohorty pacientů jsme použili modely podle Leiboviche z roku 2003 [6] a GRANT skóre [7]. Hlavním cílem práce bylo stanovení 5letého přežití bez progrese (PFS – progression-free survival).
Table 1. Vybrané prognostické modely pro lokalizovaný RCC. Upraveno podle Bex et al. [3]. Tab. 1. Selected prognostic models for localized RCC. Adapted from Bex et al. [3]. ![Vybrané prognostické modely pro lokalizovaný RCC. Upraveno podle Bex et al. [3]. Tab. 1. Selected prognostic models for localized RCC. Adapted from Bex et al. [3].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/d0391dd8edc310fbbe34486368758678.png)
Metodika a soubor
Byla provedena retrospektivní analýza základních anamnestických dat pacientů, kteří byli operováni na našem pracovišti mezi lety 2014 a 2022 pro podezření na tumor ledviny dle zobrazovacích vyšetření, a to konkrétně dle počítačové tomografie nebo magnetické rezonance. Dále byly hodnoceny jednotlivé operační přístupy a základní charakteristika nádorů, tedy histologický podtyp RCC, T klasifikace a jaderný grade. Jako komplikace výkonů byly posuzovány pouze závažné komplikace stupně Clavien-Dindo IIIb–V. Pacienti s definitivní histologií světlobuněčného renálního karcinomu (ccRCC – clear-cell renal cell carcinoma) byli roztříděni dle prognózy podle Leibovichova skóre z roku 2003 a modelu GRANT a pro každou rizikovou skupinu bylo stanoveno 5leté PFS pomocí Kaplan-Meierovy křivky. Ke statistickému vyhodnocení byl použit software Stata/SE, za statisticky významné byly považovány hodnoty p < 0,05.
Výsledky
Ve sledovaném období bylo provedeno celkem 482 operací, z tohoto počtu bylo 64,7 % (n = 312) u mužů a 35,3 % (n = 170) u žen. Medián věku v době operace činil 67 let shodně pro obě pohlaví. Ze známých rizikových faktorů byla zjištěna hypertenze u 70,1 % (n = 338) jedinců, v době přijetí na kliniku kouřilo 22,6 % (n = 109) pacientů, bývalí kuřáci tvoří 19,3 % (n = 93) operovaných. Obezitu definovanou jako body mass index (BMI) ≥ 30 kg/m2 jsme zaznamenali u 173 (35,9 %) pacientů.
Pravostranný výkon byl o něco častější (n = 247; 51,2 %) než na straně levé. Resekci ledviny podstoupilo 209 pacientů (43,4 %), zbytek souboru byly radikální nefrektomie. Laparoskopický transperitoneální přístup tvoří 35,5 % (n = 171) operací, častěji byla provedena laparoskopická radikální než parciální nefrektomie (n = 101 vs. 70). Definitivní histologie maligního onemocnění byla potvrzena u 424 (87,9 %) pacientů, z toho naprostá většina ve formě RCC (n = 421), 58 nálezů bylo histologicky benigních (12,1 %), mezi které patřily nejčastěji angiomyolipomy, onkocytomy a další nezhoubné léze. Mezi jednotlivými podtypy RCC dominoval ccRCC, který byl potvrzen u 325 (77,2 %) pacientů, druhým nejčastějším subtypem byl papilární RCC (n = 58; 13,8 %), následovaný chromofobním RCC (n = 21; 5 %). Ostatní, vzácnější varianty RCC tvořily zbývající 4 % (n = 16) případů. Pooperační období bylo u většiny pacientů bez závažných komplikací. Nicméně u tří pacientů došlo k fatálním tromboembolickým komplikacím, které vedly k jejich úmrtí v časném pooperačním období. Závažné pooperační komplikace klasifikované dle systému Clavien-Dindo ve stupních IIIb–V byly zaznamenány celkem u 22 (4,5 %) pacientů. Konkrétně komplikace stupně IIIb se vyskytly u třinácti (2,7 %) pacientů, stupeň IV byl identifikován u šesti (1,2 %) pacientů a úmrtí odpovídající stupni V bylo evidováno u tří (0,6 %) pacientů.
Podle Leibovichova skóre byla většina pacientů zařazena do nízkorizikové skupiny (skóre 0–2; n = 210), středněrizikovou skupinu (skóre 3–5) tvořilo 96 pacientů, zatímco vysokorizikovou kategorii (skóre ≥ 6) s nepříznivou prognózou tvořilo 19 pacientů.
Model GRANT poskytl obdobné výsledky, přičemž nízkorizikovou skupinu (skóre 0–1) tvořilo 269 pacientů, zatímco do skupiny se zvýšeným rizikem recidivy (skóre ≥ 2) bylo zařazeno 56 pacientů. Výsledky stratifikace jsou podrobně znázorněny v grafech 1 a 2.
Detailní výsledky výpočtu 5letého PFS pomocí Kaplan-Meierovy metody jsou přehledně shrnuty v grafech 3 a 4. Hodnoty PFS v procentech jsou uvedeny v tab. 2. Pro model GRANT nebyla vytvořena Kaplan-Meierova křivka pro jednotlivé rizikové skupiny, jelikož by výsledky byly zkreslené a statisticky nevýznamné vzhledem k nízkému počtu pacientů ve skupinách GRANT 3 a 4 (pouze dva pacienti a jeden pacient). Místo toho bylo 5leté přežití určeno pro jednotlivé počty rizikových faktorů.
Graph 1. Rizikové skupiny – Leibovich skóre. Graph 1. Risk groups – Leibovich score. 
Graph 2. Rizikové skupiny – GRANT skóre. Graph 2. Risk groups – GRANT score. 
Graph 3. Pětileté přežití bez progrese – Leibovich skóre. Graph 3. Five-year progression-free survival – Leibovich score. 
Graph 4. Pětileté přežití bez progrese – GRANT skóre. Graph 4. Five-year progression-free survival – GRANT score. 
Diskuze
Výsledky našeho sledování 5letého PFS pacientů s karcinomem ledviny na základě Leibovichova skóre potvrzují jeho význam jako prognostického nástroje v klinické praxi. Ve skupině pacientů s nízkým rizikem (Leibovich skóre 0–2) jsme zaznamenali vynikající 5leté přežití ve výši 94,8 %. Tento výsledek je v souladu s publikovanými daty a potvrzuje, že pacienti v této kategorii mají velmi příznivou prognózu po radikální nebo parciální nefrektomii [8,9]. U pacientů se středním rizikem (Lei-
bovich skóre 3–5) bylo dosaženo 5letého přežití 89,6 %, což odráží relativně příznivý vývoj onemocnění, avšak s mírně vyšším rizikem relapsu či progrese. Výsledky této skupiny podporují individualizovaný přístup ke sledování podle dalších rizikových parametrů. Nejnižší přežití bylo zaznamenáno u pacientů s vysokým rizikem (Leibovich skóre > 6), kde 5leté přežití dosáhlo pouze 63,2 %. Tato hodnota zdůrazňuje potřebu intenzivnějšího sledování a v rámci studií i případné zařazení systémové léčby. V současné době je v ČR adjuvantní léčba (imunoterapie pembrolizumabem) indikována u nemetastatického ccRCC u nádorů pT2G4 nebo s přítomností sarkomatoidní složky, pT3–4 a N1 M0, tedy je doporučena i pro vybranou skupinu pacientů odpovídající střednímu riziku vzniku metastáz dle Leibovichova skóre [10]. Zároveň výsledky naznačují potřebu dalšího výzkumu a vývoje nových terapeutických strategií pro vysokorizikovou skupinu. V naší práci jsme používali Leibovichův model z roku 2003, byť je dostupný a doporučovaný i model z roku 2018 [11]. Model z roku 2018 je dokonce považován za nejpřesnější [12], je však poměrně složitý (hodnotí devět parametrů), a navíc neumožňuje rozdělení do rizikových skupin. Námi používaný model je snadno aplikovatelný v běžné klinické praxi bez potřeby složitých výpočtů nebo molekulárních dat, byl mnohokrát externě validován na různých souborech pacientů po celém světě, a má tak prokázanou robustnost při predikci rizika progrese u pacientů s ccRCC.Stratifikace pomocí GRANT skóre přinesla další pohled na prognózu pacientů. Ve skupině bez přítomnosti rizikových faktorů dosahovalo 5leté přežití 94,1 %, což potvrzuje velmi příznivý výhled této podskupiny. Je zajímavé, že u pacientů s jedním rizikovým faktorem bylo přežití mírně vyšší (95 %). To může být ovlivněno různým počtem případů v jednotlivých kategoriích nebo charakterem konkrétního rizikového faktoru. Naproti tomu u pacientů se dvěma rizikovými faktory již 5leté přežití klesá na 73,6 %, což ukazuje na významnou změnu prognózy i při relativně mírném nárůstu rizika. Pro skupinu s třemi a více rizikovými faktory nebylo možné 5leté přežití spolehlivě stanovit z důvodu nedostatečného počtu pacientů.
V porovnání s dostupnými daty jsou naše výsledky u Leibovichova modelu podobné, u nízkého rizika se PFS dle různých zdrojů pohybuje mezi 92 a 97 %, střednímu riziku odpovídá hodnota PFS 75–90 % a vysokému riziku 31–39 % [11,13].
Naše výsledky potvrzují využitelnost obou skórovacích systémů – Leibovich i GRANT – pro predikci dlouhodobého přežití. Jejich kombinované použití může poskytnout podrobnější a přesnější odhad prognózy a usnadnit rozhodování o další péči v rámci individualizované onkologické strategie. Jejich schopnost přesně predikovat prognózu je však v dnešní době omezená. Spektrum parametrů, které hodnotí, není v kontextu moderní onkologie dostatečné, protože neodráží biologickou rozmanitost RCC ani možnosti moderní léčby.
Table 2. Pětileté PFS u jednotlivých rizikových skupin v naší kohortě. Tab. 2. Five-year PFS in individual risk groups in our ohort. 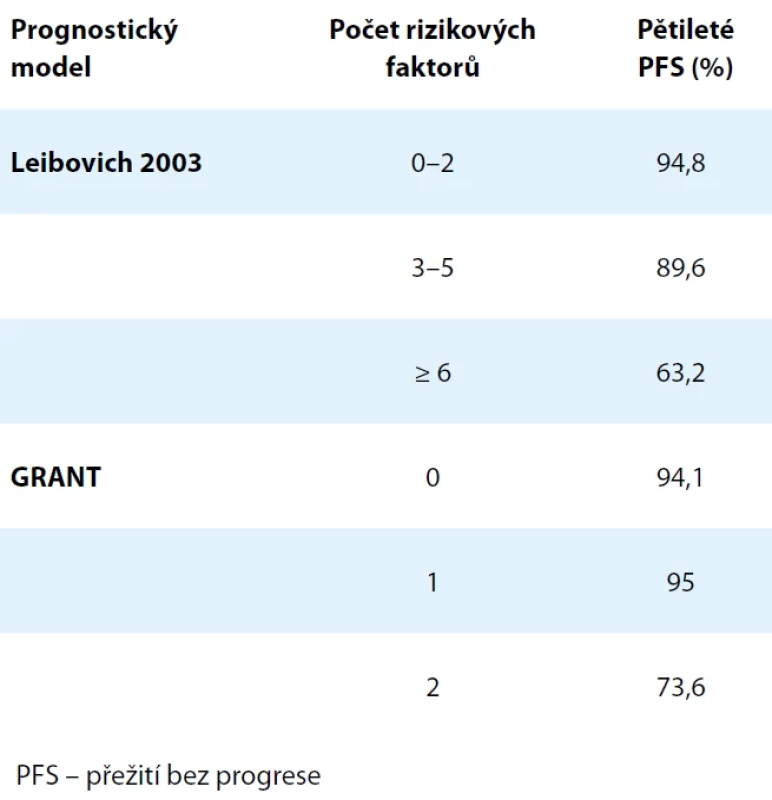
Závěr
Naše analýza 5letého PFS pacientů s karcinomem ledviny potvrzuje důležitost používání zavedených prognostických modelů, jako jsou Leibovich a GRANT skóre, při hodnocení rizika recidivy a celkového přežití po chirurgické léčbě. Oba skórovací systémy prokázaly svou schopnost rozlišit mezi pacienty s příznivou a nepříznivou prognózou, což umožňuje lépe cílit následné sledování i zvážit indikaci adjuvantní nebo systémové léčby u vysoce rizikových jedinců.
Získaná data reflektují klinické výsledky dosažené na našem pracovišti a zároveň přispívají k širší databázi poznatků o vývoji karcinomu ledviny v závislosti na klinicko-patologických parametrech. Významným přínosem této práce je i potvrzení relevance těchto modelů v každodenní praxi mimo centra, kde byly původně vyvinuty.
Zavedení standardizovaných prognostických nástrojů umožňuje lépe stratifikovat pacienty, individualizovat léčebné strategie a optimalizovat využití zdravotnických zdrojů. Do budoucna je žádoucí rozšířit sledování i na další prediktivní ukazatele, vč. molekulárních a genetických markerů, které by mohly dále zpřesnit odhad prognózy a přispět ke zlepšení výsledků léčby.
Střet zájmů: Autoři prohlašují, že v souvislosti s příspěvkem nemají žádný konflikt zájmů.
Prohlášení o podpoře: Práce nebyla podpořena žádnou společností, grantem ani jinou formou externí finanční podpory.
Sources
1. Ferlay J, Ervik M, Lam F et al. Global Cancer Observatory: Cancer Today (version 1). [online]. Lyon: International Agency for Research on Cancer 2024. Dostupné z: https://gco.iarc.who.int/today.
2. Krejčí D, Mužík J, Šnábl I et al. Portál epidemiologie novotvarů v ČR. [online]. Brno: Masarykova univerzita 2024. Dostupné z: https://www.svod.cz.
3. Bex A, Albiges L, Bedke J et al. EAU Guidelines on Renal Cancer. Edn. presented at the EAU Congress, Madrid 2025. Arnhem: EAU Guidelines Office 2025.
4. Čechová M, Chocholatý M, Babjuk M et al. Prognostické faktory renálního karcinomu. Rozhl Chir 2022; 101(10): 469–477. doi: 10.33699/PIS.2022.101.10.469-477.
5. Kašík M, Fedorko M. Prognostické faktory renálního karcinomu. Ces Urol 2023; 27(3): 139–150. doi: 10.48095/cccu2023021.
6. Leibovich BC, Blute ML, Cheville JC et al. Prediction of progression after radical nephrectomy for patients with clear cell renal cell carcinoma: a strat-
ification tool for prospective clinical trials. Cancer 2003; 97(7): 1663–1671. doi: 10.1002/cncr.11234.7. Buti S, Puligandla M, Bersanelli M et al. Validation of a new prognostic model to easily predict outcome in renal cell carcinoma: the GRANT score applied to the ASSURE trial population. Ann Oncol 2017; 28(11): 2747–2753. doi: 10.1093/annonc/mdx492.
8. Pichler M, Hutterer GC, Chromecki TF et al. External validation of the Leibovich prognosis score for nonmetastatic clear cell renal cell carcinoma at a single European center applying routine pathology. J Urol 2011; 186(5): 1773–1778. doi: 10.1016/j.juro.2011.07.034.
9. Lee HJ, Lee A, Huang HH et al. External validation of the updated Leibovich prognostic models for clear cell and papillary renal cell carcinoma in an Asian population. Urol Oncol 2019; 37(6): 356.e9–356.e18. doi: 10.1016/j.urolonc.2019.02.014.
10. Choueiri TK, Tomczak P, Park SH et al. Overall survival with adjuvant pembrolizumab in renal-cell carcinoma. N Engl J Med 2024; 390(14):
1359–1371. doi: 10.1056/NEJMoa2312695.11. Leibovich BC, Lohse CM, Cheville JC et al. Predicting oncologic outcomes in renal cell carcinoma after surgery. Eur Urol 2018; 73(5): 772–780. doi: 10.1016/j.eururo.2018.01.005.
12. Rosielo G, Larcher A, Fallara G et al. Head-to-head comparison of all the prognostic models recommended by the European Association of Urology Guidelines to predict oncologic outcomes in patients with renal cell carcinoma. Urol Oncol 2022; 40(6): 271.e19–271.e27. doi: 10.1016/j.urolonc.2021.12.010.
13. Usher Smith JA, Li L, Roberts L et al. Risk models for recurrence and survival after kidney cancer: a systematic review. BJU Int 2022; 130(5):
562–579. doi: 10.1111/bju.15673.Labels
Paediatric urologist Nephrology Urology
Article was published inCzech Urology

2025 Issue 3-
All articles in this issue
- Editorial
- Modelování lidské ledviny in vitro – potenciál renálních organoidů a tubuloidů pro urologii
- Penilní rehabilitace po radikální prostatektomii
- Náhodný nález karcinomu prostaty při výkonu pro benigní hyperplazii prostaty – jak postupovat?
- Pozitivní chirurgické okraje u renálních malignit po záchovných operacích ledvin – výsledky monocentrické retrospektivní analýzy
- Zhodnocení onkologických výsledků pomocí prognostických modelů u pacientů operovaných pro renální karcinom – zkušenosti jednoho pracoviště
- Histologické nálezy u kompletně zdvojené ledviny a močovodu po heminefrektomii
- Komplexní novinky v onkourologii – KNOU 2025
- Czech Urology Boot Camp 2025
- Czech Urology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Penilní rehabilitace po radikální prostatektomii
- Náhodný nález karcinomu prostaty při výkonu pro benigní hyperplazii prostaty – jak postupovat?
- Modelování lidské ledviny in vitro – potenciál renálních organoidů a tubuloidů pro urologii
- Komplexní novinky v onkourologii – KNOU 2025
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

