-
Medical journals
- Career
Závažné spontánní intrakraniální krvácení u 11měsíčního chlapce s vrozenou afibrinogenémií
Authors: O. Zapletal 1; J. Blatný 1; S. Köhlerová 1; V. Fiamoli 1; R. Kotlín 2; J. E. Dyr 2
Authors‘ workplace: Oddělení dětské hematologie, FN Brno primář MUDr. J. Blatný, Ph. D. 1; Ústav hematologie a krevní transfuze, Praha ředitel prof. MUDr. P. Cetkovský, Ph. D., MBA 2
Published in: Čes-slov Pediat 2014; 69 (5): 291-294.
Category: Case Report
Sdělení bylo prezentováno formou přednášky na XIX. Pařízkových dnech v Ostravě dne 20. 9. 2013.
Overview
Vrozená afibrinogenémie je velmi vzácná vrozená krvácivá choroba způsobená absencí fibrinogenu v krevní plazmě. Pacienti mohou být postiženi závažným spontánním krvácením, včetně intrakraniálního, a to v kterémkoliv věku.
Uvádíme kazuistiku chlapce s vrozenou afibrinogenémií, která je způsobena nově zjištěnou mutací v genu pro fibrinogen – homozygotní delecí Aα 6477A. Diagnóza byla stanovena po krvácení při plastice rozštěpu rtu, čelisti a patra po narození. Ve věku 11 měsíců došlo ke spontánnímu intrakraniálnímu krvácení, rozsáhlý hematom byl lokalizován okcipitálně. Akutní neurochirurgický výkon s evakuací hematomu proběhl za substituce plazmatickým derivátem fibrinogenu, stejně jako pooperační období. Poté jsme pacientovi zavedli pravidelnou profylaktickou substituci koncentrátem fibrinogenu 2krát týdně, dosud nebyla zaznamenána žádná další krvácivá epizoda.
Spontánní intrakraniální krvácení u pacientů s vrozenou krvácivou chorobou je často závažné. Rozhodujícími faktory pro přežití pacienta jsou včasná diagnostika, substituce koncentrátem a případná neurochirurgická intervence. Profylaktická substituční léčba je po takovéto příhodě doporučeným léčebným přístupem.Klíčová slova:
vrozená krvácivá choroba, děti, afibrinogenémie, intrakraniální krváceníÚvod
Fibrinogen je 47,5 nm velký rozpustný glykoprotein (molekulární hmotnost 340 kDa) produkovaný především v hepatocytech. Je obsažený v krevní plazmě v množství asi 2–4 g/l a je nezbytný pro koagulaci krve. Skládá se ze tří párů polypeptidových řetězců (označovaných Aα, Bβ a γ), které jsou kódovány každý jiným genem (FGA, FGB, FGG) na dlouhém raménku 4. chromozomu (4q31).
Vznik krevní zátky je důsledkem složitého řetězce dějů, při kterém dochází k postupné aktivaci koagulačních faktorů a krevních destiček. Fibrinogen je poslední zymogen v řadě. Přeměna fibrinogenu na fibrin je katalyzována serinovou proteázou trombinem, dochází k odštěpování N-terminálních fibrinopeptidů A a B. Následně fibrinové monomery polymerují za vzniku fibrinové sítě. Fibrinogen (Fbg) je také mediátorem agregace krevních destiček.
Při různých mutacích v genech pro Fbg může dojít ke snížení hladiny Fbg (hypofibrinogenémie), úplné absenci produkce Fbg (afibrinogenémie), nebo ke změně funkce Fbg (dysfibrinogenémie).
Vrozené chybění fibrinogenu – afibrinogenémie – je velmi vzácná vrozená krvácivá choroba. V literatuře se uvádí výskyt méně než 1 : 1 000 000. Afibrinogenémie je dědičná autozomálně recesivně. Diagnóza afibrinogenémie je stanovena laboratorním vyšetřením – aktivita Fbg i antigen Fbg jsou neměřitelně nízké [1].
Závažné samovolné krvácení se může objevit v jakémkoli věku, dokonce i prenatálně [2], dále u novorozenců [3], dětí [4] i dospělých [5]. Popisováno je krvácení z pupečníku, slizniční a podkožní krvácení, krvácení do svalů nebo do kloubů, spontánní ruptura sleziny a intrakraniální krvácení [1, 4, 5]. Krvácení se také může objevit při intervenčních výkonech nebo po úrazu. Krvácení u pacientů s afibrinogenémií léčíme substituční léčbou. K dispozici je koncentrát fibrinogenu, alternativou jsou kryoprecipitát a čerstvě zmrazená plazma (ČZP). Jako prevenci recidivy život ohrožujícího krvácení je možné podávat koncentrát fibrinogenu pravidelně a dlouhodobě. Primární profylaxe není v současnosti doporučována kvůli riziku trombotických komplikací, alergických reakcí, možnosti vzniku inhibitoru a také kvůli možnému přenosu infekce [1, 6–8].
Kazuistika
Pacient se narodil v roce 2011 nepříbuzným zdravým rodičům. Prenatálně byl ultrazvukovým vyšetřením zjištěn rozštěp rtu a patra. Třetí den života proběhla plánovaná operace, pooperačně byla komplikována krvácením z ran. Při koagulačním vyšetření byl zjištěn nízký Fbg, prodloužené aPTT (aktivovaný parciální tromboplastinový čas), PT (protrombinový čas) i TT (trombinový čas). Po substituci fibrinogenem a ČZP se laboratorní nález upravil, krvácení ustalo, rány se zhojily.
Rodičům bylo doporučeno výhledově doplnit hematologické vyšetření, které proběhlo v šesti měsících věku pacienta. Aktivita fibrinogenu byla pod 0,2 g/l (metoda podle Clausse), antigen fibrinogenu nebyl detekován (metoda EID: electro-immunodiffusion). Sekvenováním byla prokázána nová mutace v genu pro Aα řetězec fibrinogenu – homozygotní delece Aα 6477A [9]. Mutace byla pojmenována fibrinogen Poděšín podle bydliště rodiny pacienta. Tato mutace zkracuje Aα řetězec na 400 aminokyselin a mění primární strukturu od pozice 293 po 400. Oba rodiče jsou heterozygoti pro stejnou deleci, a jak bylo později při rodinné studii zjištěno, nesou ji i otec matky a otec otce probanda.
V sedmi měsících věku byl po substituci fibrinogenem (Haemocomplettan® P, CSL Behring) zaveden centrální žilní katétr – port a byla provedena další plastika patra bez komplikací. Po operaci jsme udržovali Fbg denní substitucí nad 1,6 g/l s následnou sekundární profylaxí 3krát týdně po dobu 3 týdnů, poté byla tato dočasná profylaxe ukončena.
V 11 měsících věku byl pacient přijat po několikadenních potížích (neobvyklé chování a spavost, které rodiče primárně přičítali respiračnímu infektu) na spádové dětské oddělení. Postupně progredovala porucha vědomí a po námi doporučené substituci Fbg byl hoch urgentně letecky transportován na klinické pracoviště. Na CT mozku byl prokázán rozsáhlý hematom v okcipitální oblasti, již se známkami nitrolební hypertenze (obr. 1 a 2). Za pokračující substituce koncentrátem Fbg byl proveden akutní neurochirurgický výkon: evakuace epidurálního hematomu staršího data z kraniotomie.
Image 1. CT scan mozku, v axiální rovině. Okcipitálně je patrný rozsáhlý hematom. Dále je zřejmá dilatace komorového systému a redukce zevních likvorových prostor. Fig. 1. CT scan of the brain shows large lenticular hematoma of occipital region, with dilatation of ventricular system and reduction of external liquor spaces. Axial scan. 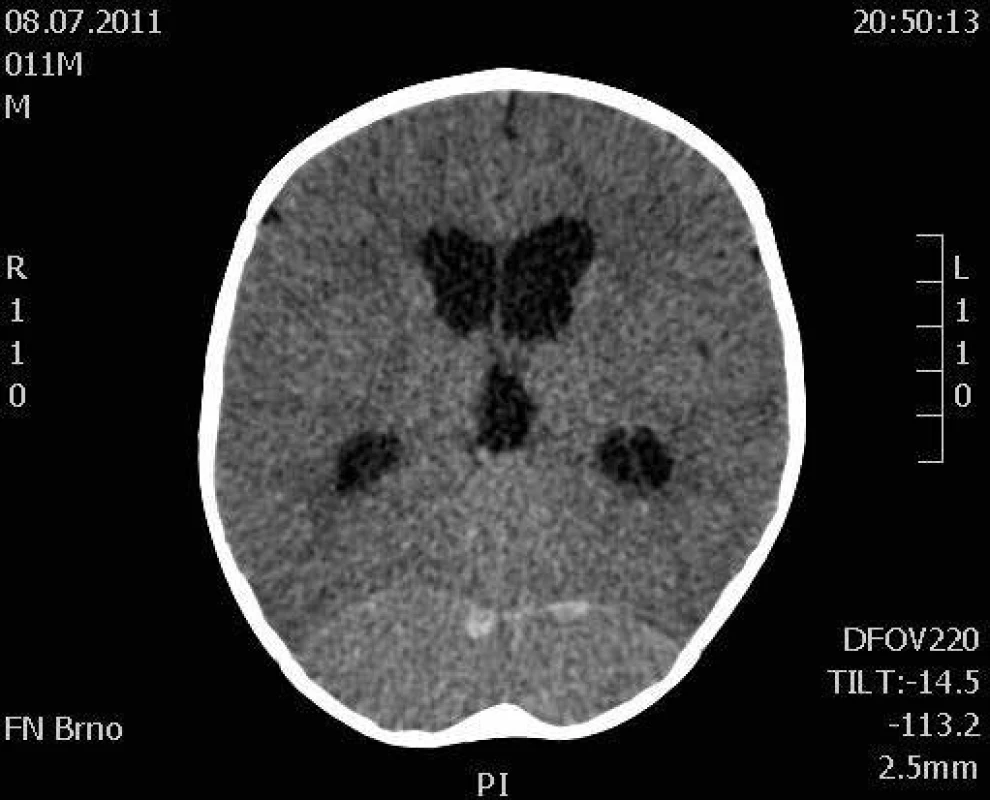
Image 2. CT scan mozku, v sagitální rovině. Okcipitálně je patrný rozsáhlý hematom. Dále je zřejmá dilatace komorového systému a redukce zevních likvorových prostor. Fig. 2. CT scan of the brain shows large lenticular hematoma of occipital region, with dilatation of ventricular system and reduction of external liquor spaces. Sagittal scan. 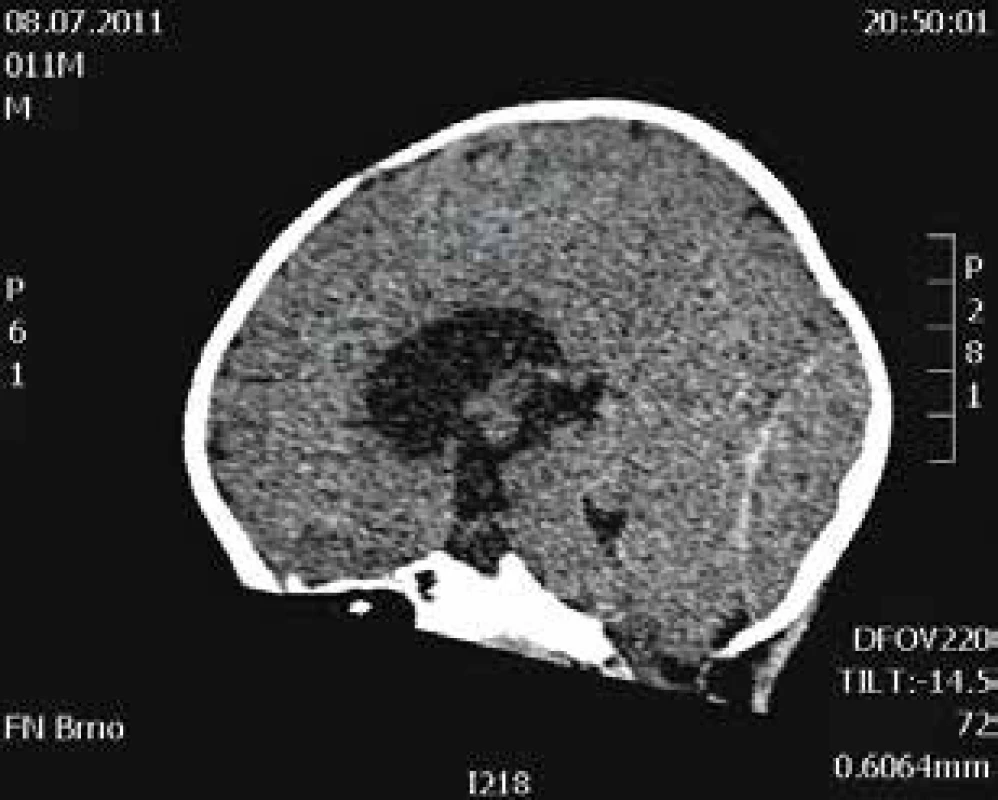
Perioperačně ani po operaci se komplikace neobjevily, do zhojení byla substitucí udržována hladina Fbg nad 1,6 g/l. Neurologický nález se upravil do původního stavu. Prevence krvácení nadále probíhá formou pravidelné profylaktické substituce koncentrátem fibrinogenu, zpočátku 3krát týdně, nyní 2krát týdně v dávce 1 g. Tato léčba udržuje hladiny Fbg nad 1 g/l před podáním následující dávky.
Závěr
Vzácné krvácivé choroby se mohou manifestovat kdykoli různě závažným krvácením i bez pozitivní rodinné anamnézy. Toto je typické pro autozomálně recesivně dědičné choroby, u kterých jsou heterozygoti asymptomatičtí.
Spontánní krvácení u pacientů s vrozenou afibrinogenémií se může manifestovat od nejútlejšího věku. Intrakraniální krvácení je vždy život ohrožující a okamžitá substituce koncentrátem fibrinogenu je zásadní, spolu s rychlou diagnózou a případným chirurgickým řešením. Preventivní substituční léčba po takovéto příhodě je doporučována ve většině případů.
Péče o pacienty s vzácnými krvácivými chorobami patří do rukou dětského hematologa.
Došlo: 24. 2. 2014
Přijato: 4. 6. 2014
MUDr. Ondřej Zapletal, Ph.D.
Oddělení dětské hematologie FN Brno
Černopolní 9
613 00 Brno
e-mail ozapletal@fnbrno.cz
Sources
1. Tziomalos K, Vakalopoulou S, Perifanis V, Garipidou V. Treatment of congenital fibrinogen deficiency: overview and recent findings. Vasc Health Risk Manag 2009; 5 : 843–848. Epub 2009 Oct 12. Review. PubMed PMID: 19851522; PubMed Central PMCID: PMC2762433.
2. Hariharan G, Ramachandran S, Parapurath R. Congenital afibrinogenemia presenting as antenatal intracranial bleed: a case report. Ital J Pediatr 2010 Jan 5; 36 : 1. PubMed PMID: 20180944; PubMed Central PMCID: PMC2841604.
3. Ataoglu E, Duru NS, Celkan T, Civilibal M, Yavuz SC, et al. Spontaneous intracranial bleeding in a neonate with congenital afibrinogenemia. Blood Coagul Fibrinolysis 2010 Sep; 21 (6): 592–594. PubMed PMID: 20445442.
4. Abdel Wahab M, de Moerloose P, Fish RJ, Neerman-Arbez M. Identification and functional characterization of a novel nonsense mutation in FGA accounting for congenital afibrinogenemia in six Egyptian patients. Blood Coagul Fibrinolysis 2010 Mar; 21 (2): 164–167. PubMed PMID: 20051841.
5. Sakai N, Akamine S, Tokuyama T, Sugiyama K, Kanayama N, Namba H. Chronic subdural hematoma in a patient with congenital afibrinogenemia successfully treated with fibrinogen replacement. Neurol Med Chir (Tokyo) 2011; 51 (11): 780–783. PubMed PMID: 22123482.
6. Bornikova L, Peyvandi F, Allen G, Bernstein J, Manco-Johnson MJ. Fibrinogen replacement therapyfor congenital fibrinogen deficiency. J Thromb Haemost2011 Sep; 9 (9): 1687–1704. doi: 10.1111/j.1538-7836.2011.04424.x. Review. PubMed PMID:21711446.
7. Peyvandi F, Palla R, Menegatti M, Siboni SM, Halimeh S, et al.; European Network of Rare Bleeding Disorders Group. Coagulation factor activity and clinical bleeding severity in rare bleeding disorders: results from the European Network of Rare Bleeding Disorders. J Thromb Haemost 2012 Apr; 10 (4): 615–621. doi: 10.1111/j.1538 - 7836.2012.04653.x. PubMed PMID: 22321862
8. Goyal SS, Bhardwaj DV, Shenoy U, Reddy B. Anaesthetic management of a child with congenital afibrinogenemia – A rare inherited coagulation disorder. Indian J Anaesth 2011 Nov; 55 (6): 605–607. PubMed PMID: 22223906; PubMed Central PMCID: PMC3249869.
9. Stikarová J, Blatný J, Kotlín R, Suttnar J, Zapletal O, et al. Novel homozygous fibrinogen Aα chain truncation causes severe afibrinogenemia with lifethreatening complications in a two-year-old boy. Thromb Res 2013 Oct; 132 (4): 490–492. doi: 10.1016/j.thromres.2013.08.022. Epub 2013 Sep 1. PubMed PMID: 24050829.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2014 Issue 5-
All articles in this issue
- Využitie zobrazovacích metód pri diagnostike intestinálnych malrotácií
- Betablokátory v léčbě hemangiomů dětského věku
- Význam klasického cytogenetického vyšetření v pediatrické praxi: zhodnocení 384 indikací
- Závažné spontánní intrakraniální krvácení u 11měsíčního chlapce s vrozenou afibrinogenémií
- Alveolární kapilární dysplazie s vychýlením plicních žil jako příčina hypoxeamického respiračního selhání donošeného novorozence
- Úloha hepcidinu v regulaci metabolismu železa
- Etické problémy péče o rizikové novorozence
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Betablokátory v léčbě hemangiomů dětského věku
- Etické problémy péče o rizikové novorozence
- Úloha hepcidinu v regulaci metabolismu železa
- Význam klasického cytogenetického vyšetření v pediatrické praxi: zhodnocení 384 indikací
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

