-
Medical journals
- Career
Péče o pacienty se zlomeninou horního konce stehenní kosti. I. Ortopedická péče. Doporučené postupy České revmatologické společnosti a Společnosti pro metabolická onemocnění skeletu
Authors: J. Vaculík; P. Dungl; T. Malkus; M. Majerníček; A. Podškubka; K. Pavelka 2; J. Štěpán 2
Authors‘ workplace: Ortopedická klinika IPVZ FN Na Bulovce Praha, 2Revmatologický ústav, 1. lékařská fakulta UK, Praha
Published in: Čes. Revmatol., 17, 2009, No. 3, p. 134-144.
Category: Recommendations for Treatment
Overview
Výsledek léčby zlomeniny proximálního femuru vedle standardně provedeného operačního výkonu závisí na dalších faktorech. Po předoperačním vyšetření má na vývoj stavu pacienta vliv časnost operačního zákroku. Standardní součástí léčby zlomeniny proximálního femuru je prevence infekce a trombózy. Z hlediska pooperačního vývoje je vhodá svodná anestezie.. Zlomeniny krčku femuru jsou podle dislokace, věku a celkového stavu pacienta řešeny chirurgicky osteosyntézou, implantací totální endoprotézy nebo cervikokapitální endoprotézy. Zlomeniny pertrochanterické, intertorchanterické a subtrochanterické jsou řešeny osteosyntézou dynamickým skluzným šroubem nebo nitrodřeňovým implantátem. Součástí péče o pacienty se zlomeninou proximálního femuru je rehabilitační léčba a řešení sociální otázky. Zhodnocení rizika vzniku další zlomeniny a doporučení sekundární prevence zlomeniny u pacientů po zlomenině horního konce stehenní kosti by mělo být též nedílnou součástí léčby.
Klíčová slova:
zlomenina horního konce stehenní kosti, chirurgická léčba, pooperační péčeV České republice utrpí každoročně zlomeninu v oblasti kyčle kolem 12 000 osob, z toho dvě třetiny jsou ženy (1–2). Průměrný věk pacientů se pohybuje kolem 77 let. Jde obvykle o nízkotraumatické zlomeniny v situaci dalších komorbidit. Letalita pacientů během dalšího roku je u těchto pacientů 15–25 % (3), letalita během 2 let po zlomenině je 36 % (4). Až polovina ostatních pacientů zůstává závislá na dopomoci a zdravotní stav pacientů je důvodem zhoršení kvality jejich života (5). Náklady na léčení zlomenin proximálního femuru představují 72 % výdajů na léčení všech zlomenin (6).
Obecně přijatým principem léčby zlomenin horního konce stehenní kosti je dosažení maximální možné kvality života a zmírnění bolesti pacienta v nejkratším možném intervalu. Léčba zlomeniny horního konce stehenní kosti zahrnuje řešení celkového stavu pacienta a klade důraz na soběstačnost, samoobslužnost a návrat do původního prostředí i v období po úrazu. Výsledek léčby závisí na mnoha faktorech. Základem úspěchu léčby je dobře provedený operační výkon, pokud je indikován, dále je to absence místních a celkových komplikací a zvládnutí komorbidit. Optimální péče o pacienty se zlomeninou horního konce stehenní kosti ve zdravotnických systémech rozvinutých zemí v prevenci a časném řešení uplatňuje nejnovější poznatky medicíny založené na důkazu ve všech navazujících fázích léčby zlomeniny.
Zlomenina proximálního femuru je ve svých důsledcích život ohrožujícím poraněním. Obvykle se jedná pouze o jednu z vícečetných morbidit starého člověka. Zatímco cílem léčby u mladších nemocných je obnova kyčelního kloubu, u starších nemocných je cílem léčby záchrana života. Komplexní péče o tyto nemocné zahrnuje práci ze strany ortopeda – traumatologa, internisty, anesteziologa (event. dalších medicínských oborů), rehabilitační péči a řešení sociální problematiky.
V první části tohoto doporučeného postupu odborných společností jsou uvedeny zásady ortopedické péče o pacienty, kteří utrpěli zlomeninu v oblasti kyčle. Ve druhé části jsou uvedena doporučená vyšetření a jsou uvedeny postupy medikamentózní sekundární prevence zlomenin u těchto pacientů.
Předoperační péče
Pacient musí být před operací celkově vyšetřen. Doba mezi úrazem a operací musí být maximálně využita ke zlepšení klinického stavu pacienta, zejména k obnovení intravaskulárního volumu a kompenzaci chronických interních onemocnění. Krátký odklad operace může být opodstatněn kompenzací interního stavu (např. korekcí hypo - či hyperkalemie, srdečního selhávání, diabetu, anémie, vyšetřením srdečních šelestů a srdečních arytmií). Je důležité nesnažit se dosáhnout nerealistických medicínských cílů za cenu delšího odkladu operace. Součástí předoperačního vyšetření je radiologické posouzení kvality kostní hmoty zaměřené na osteoporózu, osteomalacii či podíl sekundárního maligního procesu na vzniku zlomeniny.
Vliv odkladu operace na výsledek léčby
Zpoždění operačního řešení je vedle psychické zátěže spojeno s vyšší morbiditou a mortalitou pacienta a s celkově nižší úspěšností operační léčby a následné rehabilitace (7–8). Interval mezi přijetím a operačním řešením delší než 24 hodin je spojován s vyšší mortalitou. Časné operační řešení po zlomenině proximálního femuru do 24 hodin snižuje riziko hluboké žilní trombózy a plicní embolie (9–10). Odklad operace je též spojen s vyšším rizikem vzniku dekubitů (11). Z hlediska načasování výkonu byl u intrakapsulárních zlomenin krčku femuru zjištěn významně nižší podíl následné avaskulární nekrózy hlavice kosti stehenní po osteosyntéze u nemocných operovaných do 6 hodin od úrazu oproti nemocným operovaným po 24 hodinách od úrazu (61). Operace má být provedena, jakmile ji umožňuje interní stav pacienta za předpokladu, že je k dispozici příslušné technické zázemí a kvalifikovaný personál (12–13). Je třeba zároveň zohlednit skutečnost, že operační léčba prováděná v nočních hodinách prokazatelně zvyšuje mortalitu. Pacient by měl být operován co nejdříve (obvykle do 24 hodin) v denní době.
Předoperační extenze
Předoperační extenze je používána ke zmírnění bolesti a je přípravou operačního řešení k usnadnění repozice. Poslední systematický přehled Cochrane hodnotil použití extenze (jak kožní, tak skeletální) na poraněné končetině od momentu přijetí do operace v 10 studiích (14). V devíti studiích bylo hodnoceno zajištění pomocí trakcí nebo bez trakce, ve 2 studiích byla porovnávána trakce skeletální s náplasťovou. V systematickém přehledu nebyla prokázána účinnost trakce při zmírnění bolesti ani její vliv na následnou repozici. Údaje z deseti studií nejsou dostatečné k hodnocení výskytu avaskulární nekrózy hlavice femuru, k hodnocení komplikací při hojení zlomenin, ani k jednoznačnému závěru o výhodách extenze.
Ke zmírnění bolestivosti před operačním řešením je však extenze na poraněné končetině doporučována. Pokud ale má operační výkon následovat v krátké době, je ke zmírnění bolesti vhodná i antirotační botička nebo polohování končetiny na polštáři. U zlomenin krčku femuru určených k osteosyntéze může extenze zvyšovat intraartikulární tlak. Jako vhodnější je zejména v těchto případech doporučovaná pouze antirotační botička.
Prevence infekce
Pacienti se zlomeninou horního konce stehenní kosti jsou vedle rizika vzniku infekce operační rány též ohroženi infektem dýchacích cest a infektem močových cest (15).
Systematický přehled randomizovaných studií Cochrane potvrdil při profylaktickém podání antibiotik před operací pro zlomeninu proximálního femuru snížení incidence nejen povrchových a hlubokých infektů rány, ale též snížení incidence uroinfektů a respiračních infektů (16). Antibiotikum má být podáno intravenózně, 30 minut před zahájením operace buď jednorázově, nebo může profylaxe pokračovat po dobu 24 hodin. Delší profylaktické podávání antibiotika než 1 den od operace ve většině studií nedosahovalo dalšího snížení výskytu infekčních komplikací (17). U osteosyntézy zlomeniny proximálního femuru a implantace endoprotézy pro zlomeninu krčku femuru je standardně účinné cefalosporinové antibiotikum I. nebo II. generace. Lokální bakteriální flóra a její rezistence může vyžadovat změnu antibiotika podávaného v profylaxi po konzultaci s mikrobiologem. Antibiotika je vhodné preventivně aplikovat u všech starších pacientů operovaných pro zlomeninu horního konce stehenní kosti.
Prevence trombózy
Operace zlomeniny horního konce stehenní kosti bez prevence TEN je zatížena vysokým rizikem vzniku asymptomatické hluboké žilní trombózy, symptomatické žilní trombózy, rizikem symptomatické plicní embolie (3–13 %) a fatální plicní embolie (18). V ortopedii byla zaznamenána klesající incidence fatální plicní embolie v závislosti na zvyšujícím se podílu spinální nebo epidurální anestezie, časné mobilizaci a použití mechanické profylaxe (19).
Metaanalýza randomizovaných studií zaznamenala snížení výskytu asymptomatické hluboké žilní trombózy při aplikaci intermitentní pneumatické komprese nebo nožní pumpy z 19 na 6 %. Data z uvedených studií neumožňovala vyhodnotit účinky těchto opatření na symptomatické případy tromboembolické nemoci či mortalitu. Mechanické pomůcky však vyžadují aplikaci u pacienta na lůžku, jejich cena není zanedbatelná a lokálně mohou vést ke vzniku kožních erozí (20). V rámci randomizované studie hodnotící efekt antiagregační léčby oproti placebu u 13 000 pacientů se zlomeninou proximálního femuru v prevenci tromboembolické nemoci byl zároveň hodnocen efekt elastické komprese dolních končetin. V uvedené studii nebyl prokázán efekt komprese dolních končetin na snížení výskytu symptomatické tromboembolické nemoci (21). Obecně v samostatné studii vliv kompresních punčoch na snížení výskytu tromboembolické nemoci u pacientů se zlomeninou proximálního femuru testován nebyl, avšak v systematickém přehledu Cochrane zahrnujícím výsledky 16 randomizovaných studií u imobilizovaných pacientů za hospitalizace pro různé jiné chirurgické a interní diagnózy byla aplikace elastických kompresivních punčoch jako doplněk farmakologické profylaxe spojena s výskytem hluboké žilní trombózy jen ve 3 %, ve skupině bez elastické komprese dolních končetin byla hluboká žilní trombóza zaznamenána ve 14 % (22). Z uvedeného vyplývá že v praxi by měla být elastická komprese dolních končetin i při zlomenině horního konce stehenní kosti aplikována ke snížení rizika vzniku hluboké žilní trombózy jako doplněk farmakologických metod.
V již uvedené studii prevence antiagregačními preparáty (21) bylo při podávání kyseliny acetylsalicylové zjištěno snížení výskytu symptomatické hluboké žilní trombózy (z 1,5 % na 1,0 %), plicní embolizace (z 1,2 % na 0,7 %) a fatální plicní embolie (z 0,64 % na 0,27 %). Aplikace kyseliny acetylsalicylové byla spojena s krvácivými komplikacemi vyžadujícími transfuzi u 2,9 % pacientů oproti 2,4 % ve skupině s aplikací placeba. I když kyselina acetylsalicylová prokazatelně snižuje výskyt tromboembolické nemoci u pacientů se zlomeninou horního konce stehenní kosti, pro prevenci hluboké žilní trombózy je v současné době místo kyseliny acetylsalicylové doporučováno podávání nízkomolekulárního heparinu (LMWH) a warfarinu pro vyšší účinnost.
Metaanalýza podávání heparinu a nízkomolekulárního heparinu (LMWH) u pacientů operovaných pro zlomeninu proximálního femuru prokázala snížení výskytu žilní trombózy dolních končetin ze 42 % na 26 %, RR 0,60 (20).
Warfarin rovněž snižuje riziko výskytu hluboké žilní trombózy po operaci zlomeniny proximálního femuru. Jeho nevýhodou je však pomalejší nástup účinku a nutnost v počátku využít jiné prostředky prevence. V randomizované studii byl ve skupině s placebem zaznamenán výskyt hluboké žilní trombózy ve 46 %, ve skupině u níž byl aplikován warfarin ve 20 % bez zvýšení rizika vzniku krvácení (23). Podle některých studií je aplikace warfarinu prokazatelně zatížena rizikem výskytu krvácivých komplikací (24–25).
Syntetický oligosacharid fondaparinux, jehož antikoagulační účinek je dán inhibicí aktivovaného faktoru X (Xa), snížil v randomizované multicentrické studii u pacientů operovaných pro zlomeninu proximálního femuru relativní riziko vzniku hluboké žilní trombózy oproti aplikaci enoxaparinu o 56 %. Optimální doba preventivní aplikace fondaparinuxu je 28 dnů (26). Aplikace nízkomolekulárního heparinu je účinnou prevencí tromboembolické nemoci a měla by být zvážena při zlomenině proximálního femuru u každého pacienta, pokud se nevyskytuje důvod pro její kontraindikaci. Pacient má v prevenci tromboembolické nemoci pokračovat po propuštění. Může být buď nadále aplikována prevence nízkomolekulárním heparinem po dobu 5–6 týdnů u nekomplikovaných případů, či může být pacient před propuštěním převeden na prevenci warfarinizací (s cílovou hodnotou INR 1,5–2,5). Prevence tromboembolické nemoci warfarinem by měla probíhat po dobu 6 týdnů od operace. Elastická komprese dolních končetin by měla být aplikována po dobu trvání farmakologické profylaxe. Je-li nutno operační řešení zlomeniny proximálního femuru odložit, měla by být zvážena prevence hluboké žilní trombózy již v předoperačním období (27).
Úprava vnitřního prostředí
Dehydratace a odchylné koncentrace minerálů jsou častým problémem při léčbě zlomenin horního konce stehenní kosti u pacientů ve vyšším věku. Zhodnocení těchto odchylek je součástí předoperačního vyšetření. Ohroženi jsou zejména starší pacienti, u kterých byla opožděna diagnóza zlomeniny a opožděno přijetí do nemocnice. U pacientů musí být vedle klinického posouzení stavu provedeno laboratorní vyšetření s vyhodnocením hypovolemie a nerovnováhy minerálů. Odchylky musí být bezodkladně korigovány.
U pacientů se zlomeninou proximálního femuru může být přítomna hypoxemie již při přijetí a následně v peroperačním období. Hypoxemie má být korigována dle saturace.
Anestezie
Anestezie má být prováděna nebo podrobně dozorována anesteziologem s dostatečnou zkušeností vedení anestezie u pacientů ve vyšším věku. Významným faktorem ovlivňujícím výsledek léčby pacienta je ASA skóre.
Vliv zvolené metody anestezie na výsledky operací zlomeniny horního konce stehenní kosti byl hodnocen metaanalýzami (28), systematickými přehledy (29) a dalšími studiemi. Metaanalýza 13 studií převážně randomizovaných prokázala snížení mortality do 1 měsíce od operace u pacientů, u nichž byla aplikována regionální anestezie (spinální nebo epidurální) ve srovnání s pacienty, u kterých byla aplikována celková anestezie (poměr pravděpodobností mortality 0,67, 95 % CI 0,46–0,98) (28). Regionální anestezie je doporučena jako metoda volby. Podle systematického přehledu Cochrane byla u pacientů s aplikací regionální anestezie snížena mortalita do jednoho měsíce od operace ve srovnání s celkovou anestezií se stanovením relativního rizika 0,69 (95 % CI 0,50–0,95) (29).
Snížení výskytu symptomatické žilní trombózy po spinální anestezii diagnostikované venografií nebo označeným fibrinogenem bylo prokázáno několika studiemi. V některých studiích bylo prokázáno snížení výskytu tromboembolických komplikací. Podle systematického přehledu Cochrane snižuje regionální anestezie riziko symptomatické hluboké žilní trombózy ze 47 % na 30 % (29).
Konfuzní stavy
Podle již zmíněného systematického přehledu Cochrane (29) je regionální anestezie spojena s nižším výskytem zmatenosti v pooperačním období ve srovnání s celkovou anestezií. Z hlediska pooperační respirační morbidity, peroperačních ztrát, infarktu myokardu, kongestivního srdečního selhávání, renálního selhávání a cévních mozkových příhod nebyl prokázán statisticky významný rozdíl v závislosti na typu anestezie.
Konzervativní léčba
Konzervativní léčba u zlomenin proximálního femuru může být tzv. indikovaná, tj. u zaklíněných nebo nedislokovaných typů zlomenin krčku femuru nebo tzv. paliativní, v případech pokud celkový stav pacienta neumožňuje operační řešení. Konzervativní postup lze volit u inkompletní subkapitální zlomeniny krčku femuru Garden I. Přitom je vhodné se přesvědčit o stabilitě zlomeniny klinickým i rentgenovým vyšetřením. V případě konzervativní léčby je indikována odlehčující punkce kyčle k odstranění intraartikulárního hematomu. Součástí konzervativního postupu je postupná mobilizace nemocného.
Chirurgická léčba
Základním předpokladem úspěšné léčby je dobře provedený, neprotrahovaný operační výkon. Možnost vyslovit zcela jednoznačné závěry pro ošetření různých typů zlomenin je omezena. Alternativní chirurgická řešení různých typů zlomenin horního konce femuru byla porovnána v řadě menších studií. Zkušenost operatéra prokazatelně ovlivňuje délku trvání operace a výskyt pooperačních komplikací, ale nemá prokazatelný vliv na mortalitu (7, 11). Neadekvátní výkon vede k nemožnosti vertikalizace, zhoršuje možnost ošetřování, může vést ke komplikacím, pro které je nutné zvažovat reoperaci, obvykle mnohem více zatěžující.
Typy zlomenin
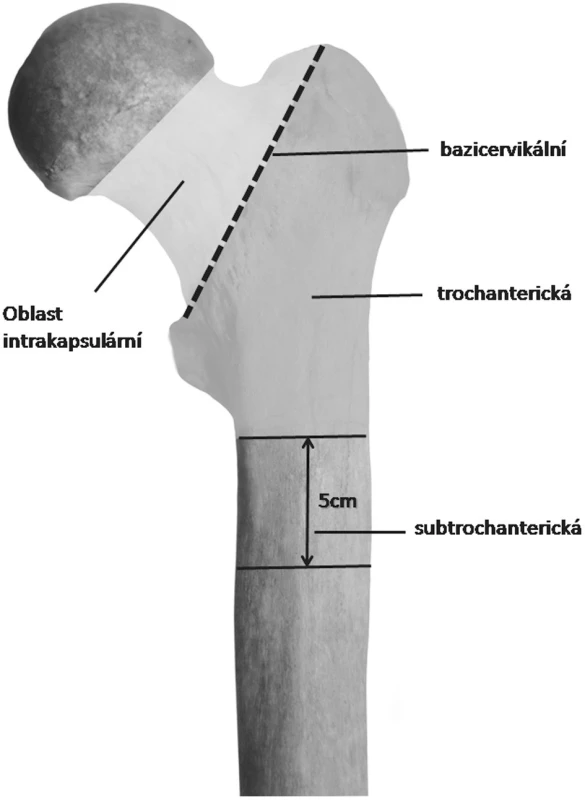
Zlomeniny horního konce stehenní kosti jsou klasifikovány jako intrakapsulární nebo extrakapsulární v závislosti na lokalizaci zlomeniny ve vztahu k úponu kloubního pouzdra kyčelního kloubu na proximálním femuru (obr. 1). Intrakapsulární zlomeniny zahrnují subkapitální a transcervikální zlomeniny a nejlépe je dělit je na nedislokované a dislokované. Starší klasifikace, jako je například klasifikace dle Gardena (I. – IV.), mají dílčí přídatný diagnostický, léčebný nebo prognostický význam oproti uvedenému dělení.
Extrakapsulární zlomeniny zahrnují per-, inter - a subtrochanterické zlomeniny. Linie bazicervikální zlomeniny se vyskytuje ventrálně přibližně v úrovni úponu kloubního pouzdra (obr. 1, přerušovaná linie). Bazicervikální zlomenina se vyznačuje vlastnostmi extrakapsulární zlomeniny a měla by tak být chápána z hlediska léčebného a prognostického. Intrakapsulární zlomeniny jsou ve srovnání se zlomeninami extrakapsulárními zatíženy rizikem vzniku avaskulární nekrózy hlavice femuru.
Léčba nitrokloubních zlomenin
Není dostatek přesvědčivých důkazů pro volbu optimálního léčebného postupu pro všechny případy, i když je léčba nitrokloubních zlomenin krčku femuru předmětem úvah již několik desetiletí. Osteosyntézu je možno indikovat u pacientů ve věku do 65–70 let, totální náhradu u pacientů starších 65 let a hemiartroplastiku podle biologického věku obvykle nad 75 let. I přes nejednoznačné výsledky randomizovaných studií a systematického přehledu Cochrane (32, 51) je k osteosyntéze zlomeniny krčku femuru při osteoporotickém skeletu upřednostňováno použití DHS s přídatným antirotačním spongiózním šroubem před použitím samotných kanylovaných šroubů, jejichž aplikace je podmíněna kvalitní spongiózní kostí zejména u mladých pacientů.
Nedislokované nitrokloubní zlomeniny krčku femuru
Chirurgická léčba umožňuje časnou mobilizaci pacienta a snižuje riziko dislokace zlomeniny v pozdějším období. Podle dosavadních poznatků byl prokázán pouze malý rozdíl mezi výsledky operačního a konzervativního léčení nedislokovaných zlomenin krčku femuru (30–31). Nedislokované zlomeniny krčku femuru, které jsou chirurgicky léčeny, je vhodné řešit vnitřní fixací.
Metaanalýza randomizovaných studií neprokázala výhodu některého z typů osteosyntéz či přednost postranní dlahy u implantátu při osteosyntéze jak u dislokovaných, tak nedislokovaných zlomenin krčku femuru (32). U velmi starých nebo biologicky starých pacientů s rizikem selhání osteosyntézy může být případně provedena hemiartroplastika místo vnitřní fixace (33). Při zavřené osteosyntéze je potřeba provést odlehčující punkci nitrokloubního hematomu.
Dislokované intrakapsulární zlomeniny
Optimální chirurgická léčba starších pacientů s dislokovanou zlomeninou krčku femuru není jednoznačná. Je nutno zhodnotit více faktorů: typ zlomeniny, stabilitu zlomeniny, věk, celkový stav a mentální stav nemocného, jeho dosavadní aktivitu a mobilitu, časový interval od úrazu, stav kosti (stupeň osteoporózy či přítomnost jiné osteopatie), stav kyčelního kloubu (stupeň osteoartrózy), vyloučit patologickou zlomeninu, posoudit schopnost spolupráce nemocného a jeho schopnost odlehčování operované končetiny, typ plánovaného implantátu při volbě chirurgického řešení. V současné době proto není k dispozici jednotný chirurgický výkon, který by zajišťoval optimální výsledky u všech pacientů s tímto typem zlomeniny s ohledem na uvedené faktory. Mezi soudobé možnosti řešení patří repozice s vnitřní fixací, hemiartroplastika nebo implantace totální endoprotézy. Randomizované studie prokazují, že jak vnitřní fixace, tak artroplastika vedou ke stejným konečným funkčním výsledkům, kdy vnitřní fixace je zatížena hraničně nižší mortalitou za cenu vyššího výskytu reoperací (33–37). Podle některých studií je otevřená repozice a vnitřní fixace zatížena reoperací až ve 42 % případů (38–39). V multicentrické prospektivní randomizované studii srovnávající vnitřní fixaci s artroplastikou u 450 pacientů starších 70 let došlo k selhání osteosyntézy ve 43 % případů po vnitřní fixaci oproti 6 % případů řešených artroplastikou (40). U biologicky starších pacientů by měla být preferována artroplastika.
Výsledky hemiartroplastiky jsou iniciálně lepší ve srovnání s implantací totální endoprotézy, ale v případě přežití pacienta dochází ke zhoršení funkce po třech až pěti letech. Implantace totální endoprotézy je však zatížena větším výskytem časných luxací (41–44). Výsledky sekundární implantace totální endoprotézy po selhání vnitřní fixace jsou lepší než výsledky hemiatroplastiky po několika letech od původního úrazu (45). Jak již bylo uvedeno, je nutné zhodnotit více faktorů než jen typ zlomeniny a typ implantátu při volbě chirurgického řešení. Je nutno zhodnotit věk pacienta, dosavadní mobilitu, dosavadní mentální stav pacienta, kvalitu skeletu a kyčelního kloubu (artróza(32). V klinické praxi v současné době přichází v úvahu repozice a vnitřní fixace dislokovaných zlomenin krčku femuru u pacientů biologicky mladších než 65–70 let a artroplastika u starších pacientů ve snaze omezit komplikace při hojení zlomeniny po vnitřní fixaci.
Komplikace při využití vnitřní fixace závisí na kvalitě repozice a kvalitě kosti (45–49). Metaanalýza 106 prací doložila procento reoperací 20–36 % po vnitřní fixaci ve srovnání s 6–18 % po hemiartroplastice. Podle některých prací jsou reoperace častější u starších pacientů (42, 50). Systematický přehled Cochrane se zabýval technikami při vnitřní fixaci, hodnotil zaklínění zlomeniny při operaci, kompresi zlomeniny, otevřenou či zavřenou repozici dislokované zlomeniny. Nebyla prokázána relativně vyšší účinnost některé z hodnocených technik (51). Stejně tak nebyla prokázána vyšší účinnost některého z fixačních prvků pro vnitřní osteosyntézu (32).
U mladých, aktivních, zdravých pacientů má být zvážena možnost vnitřní fixace. U aktivních pacientů s očekávanou dobou přežití více let má být zvážena buď vhodnost vnitřní fixace, nebo implantace totální endoprotézy v závislosti na uvedených faktorech. U pacientů s očekávanou délkou života kratší než 3 roky a u pacientů jejichž úroveň aktivity je nízká by měla být provedena hemiartroplastika. U pacientů upoutaných na vozík či lůžko může být léčba konzervativní.
Typy hemiartroplastiky
Hemiartroplastika může být buď unipolární, bipolární, či modulární. Hemiartroplastiky mohou být cementované či necementované. Použití cementu je spojováno s intraoperační morbiditou v důsledku kardiopulmonální odpovědi a tromboembolizace při jeho aplikaci. Tyto projevy lze snížit intramedulární laváží či modernějšími technikami cementování (52–53). Necementované dříky jsou spojovány s větší bolestí femuru a celkově horší funkcí (54–56).
Radiologické studie naznačily, že u mnoha pacientů dochází k pohybu bipolární hemiartroplastiky pouze na zevní kloubní ploše a fungují prakticky jako unipolární hemiartroplastiky (57). Tím se ztrácí jejich teoretická výhoda, tj. zmírnění opotřebení acetabula (58). Nebyl nalezen přesvědčivý důvod pro upřednostnění implantace bipolární hemiartroplastiky před unipolární (56, 59–60). Ve snaze upřesnit výhodnost implantace bipolární či unipolární náhrady systematický přehled Cochrane v roce 2004 zahrnul sedm prospektivních randomizovaných studií zahrnujících celkem 857 pacientů. Závěrem nebyl nalezen rozdíl s ohledem na luxaci, erozi acetabulární chrupavky, hluboký infekt, reoperace, DVT či mortalitu. Základním nedostatkem studie bylo krátkodobé sledování po dobu 2 let, kdy základní teoretická výhoda bipolární hemiartroplastiky (eroze acetabula) se má možnost projevit až v dlouhodobějším sledování. Vzhledem k 50% mortalitě do 5 let u pacientů starších 70 let bylo možno jen obtížně získat dostatečné množství informací k dosažení adekvátní síly testu. Vzhledem k neprůkaznosti výhody unipolární či bipolární hemiartroplastiky při závažnějších faktorech ovlivňujících erozi acetabula jako je věk, úroveň aktivity a délka sledování, by bipolární hemiartroplastika neměla být používána. Modulární hemiartroplastika teoreticky umožňuje akutní řešení zlomeniny krčku femuru s možností konverze na totální endoprotézu v případě potřeby při dlouhodobějším sledování pacienta (61).
Při hemiartroplastice je možný přístup anterolaterální a zadní. Luxace a trombóza je častější při využití zadního přístupu (62–63). Při využití předního přístupu je delší operační čas, vyšší krevní ztráta a je zvýšeno riziko infekčních komplikací (64–65). Všeobecně je anterolaterální přístup považován za výhodnější.
Totální endoprotéza
Totální endoprotéza jako primární výkon je v současné době léčebnou možností u staršího pacienta s dislokovanou zlomeninou krčku femuru. V minulosti byla považována za vhodnou jen u pacientů se současným onemocněním kyčelního kloubu (artróza, revmatoidní artritida). Dřívější studie prokazovaly, že pacienti léčení implantací totální endoprotézy pro zlomeninu krčku femuru mají častější luxace než pacienti léčení pro artrózu. Vyšší pravděpodobnost luxace byla připisována většímu předoperačnímu rozsahu pohybu u pacientů se zlomeninou (50). Pokud jsou vyloučeni pacienti s jednou časnou luxací do 4 měsíců od operace, pak jsou unipolární hemiartroplastika, bipolární hemiartroplastika a totální endoprotéza zatíženy obdobným výskytem luxací.
Kohortové studie poskytují protichůdné závěry o výsledcích totálních náhrad jako primární léčebné metody zlomenin krčku femuru (41–42). Luxace je možno očekávat v rozmezí 10–20 %. Po 3 letech však poskytuje totální endoprotéza lepší výsledky než hemiartroplastika (41, 56).
Totální endoprotéza jako sekundární výkon po selhání vnitřní fixace rovněž poskytuje lepší výsledky než hemiartroplastika (45). Výsledky totální náhrady kyčelního kloubu po selhání hemiartroplastiky jsou obdobné jako výsledky po revizi primární implantace totální endoprotézy, jsou však zatíženy vyšším množstvím komplikací. V nejdelším publikovaném sledování bylo 271 pacientů starších 65 let randomizováno k implantaci totální endoprotézy, hemiartroplastiky a k vnitřní osteosyntéze (66). Po jednom roce udávalo 27 % pacientů po implantaci hemiartroplastiky bolestivost kyčle. Po implantaci TEP po 1 roce nebyl výskyt bolestivosti zaznamenán. Po 13 letech ze zbývajících 10 % pacientů ve skupině s hemiartroplastikou bylo nuceno 45 % pacientů užívat analgetika pro bolesti, ze zbývajících 19 % pacientů ve skupině s TEP 6 %. Ve skupině hemiartroplastiky bylo celkově zaznamenáno 24 % reoperací, ve skupině TEP 6,8 %. Proměnným a obtížně hodnotitelným faktorem ovlivňujícím úspěšnost léčby implantací TEP ve studiích zůstává chirurgická technika a zkušenost operatérů.
Implantace totální endoprotézy je vhodná jako primární léčba u pacientů s postižením kyčelního kloubu z předchozího období a u pacientů bez mentálního omezení se středně vysokou nebo vysokou úrovní aktivity s předpokladem dlouhodobějšího přežití.
Léčba extrakapsulárních zlomenin
Extrakapsulární zlomeniny jsou léčeny operačně, pokud se nevyskytuje kontraindikace operačního řešení. Konzervativní způsob léčby je zatížen vysokou morbiditou, letalitou, dlouhodobější hospitalizací a výraznější deformitou po zhojení zlomeniny (31).
Operační léčba extrakapsulárních zlomenin je prováděna repozicí a vnitřní fixací. Vnitřní fixace může být provedena buď extramedulárním implantátem (DHS), nebo nitrodřeňovým implantátem (například PFN). Podle závěru systematického přehledu Cochrane se extramedulární osteosyntéza doposud zdá být zatížena menším množstvím komplikací než osteosyntéza nitrodřeňovými implantáty (Gamma Nail) nebo cefalokondylickými implantáty (67). Podle závěru systematického přehledu je třeba dalších studií ke stanovení výhod jednotlivých implantátů u jednotlivých typů zlomenin. Stabilní pertrochanterické zlomeniny jsou standardně a optimálně řešeny za pomoci DHS. Nestabilní pertrochanterické zlomeniny s vylomením posteromediálního fragmentu mediální kortikální opory mohou být řešeny implantátem intramedulárním i extramedulárním. Zlomeniny s porušením laterální stěny (kortikální kost od úponu m. vastus lateralis do úrovně uvažovaného vstupu krčkového šroubu implantátu), zlomeniny subtrochanterické a intertrochanterické zlomeniny s opačnou šikmostí linie lomu (reversed obliquity fractures) mají být ošetřeny intramedulárním implantátem (68–69). U pertrochanterických zlomenin je ve Spojených státech v praxi zaznamenán trend stále častějšího užívání intramedulárních implantátů, aniž by však byla jednoznačně definována a prokázána jejich výhoda podle principu medicíny založené na důkazu (70–71).
Nerandomizovaná prospektivní studie českých autorů vyhodnocující osteosyntézu trochanterických zlomenin intramedulárním implantátem prokázala dobré výsledky při léčbě nestabilních pertrochanterických zlomenin a subtrochanterických zlomenin (72). Rovněž v domácí retrospektivní studii výsledků léčby intramedulárním implantátem v souboru pacientů převážně s nestabilní pertrochanterickou zlomeninou bylo zaznamenáno 95% zhojení operovaných zlomenin (73). Ve studii vyhodnocující retrospektivně komplikace osteosyntézy intramedulárním implantátem byla zaznamenána 4 % reoperací (74). Uvedené studie nebyly randomizované, poukazují však na velmi dobré výsledky léčby nestabilních pertrochanterických zlomenin. Řešení nestabilních pertrochanterických zlomenin za pomoci osteotomie a osteosyntézy předpokládá rekonstrukci mediální kortikální opory (75). Při použití osteotomie u nestabilních extrakapsulárních zlomenin s osteosyntézou DHS nebo jiným implantátem nebyla podle některých autorů prokázána výhoda ve srovnání s běžnou repozicí osteosyntézou a kontrolovanou impakcí fragmentů dynamizací na implantátu (76).
Pertrochanterické zlomeniny včetně nestabilních typů jsou s velmi dobrými výsledky řešeny PC C.P. (percutaneous compression plate) (77–78).
Časná pooperační péče
V časném pooperačním období je monitorována bolest a je adekvátně tlumena. Účinná analgezie v pooperačním období je spojena se snížením morbidity kardiovaskulárního, respiračního a gastrointestinálního systému. Saturace kyslíkem je monitorována, dokud je zaznamenávána tendence k hypoxemii, v případě hypoxemie je aplikován kyslík. Rovněž je u pooperačních pacientů monitorováno EKG k zaznamenání pooperační ischemie. Nerovnováha minerálů, zejména hyponatremie a hypokalemie jsou v pooperačním období časté v důsledku limitovaných renálních funkcí, což může být zhoršováno skladbou diuretik a nevhodnou infuzní léčbou. Rovnováha minerálů a hydratace pacienta jsou monitorovány. Krevní ztráty jsou hrazeny podle výsledků kontroly krevního obrazu. Zohledněny jsou ztráty peroperační a pooperační.
Časná mobilizace pacienta má být zahájena do 24 hodin, pokud to umožňuje celkový stav pacienta a stav operované končetiny. Chůze s oporou a s odlehčením operované končetiny je zahájena za doprovodu rehabilitačního instruktora. Po osteosyntéze je obvykle doporučováno nejméně šestitýdenní odlehčování operované končetiny, hojení zlomeniny je obvykle úplné za 3 měsíce od operace, v mnoha případech však pacienti nejsou schopni odlehčení končetiny, i v těchto případech musí být osteosyntéza stabilní. Po hemiartroplastice je rovněž doporučeno odlehčení na 6 týdnů, i v těchto případech je častá plná zátěž hned po výkonu. Po totální náhradě je doporučeno odlehčení operované končetiny podle tolerance bolesti obvykle 6–12 týdnů.
Součástí časné pooperační péče je prevence obstipace. Permanentní katetrizace moči v pooperačním období má být aplikována pouze v indikovaných případech.
Rehabilitace a propuštění
Duševní schopnosti pacienta před úrazem, mobilita a funkce jsou nejdůležitějšími faktory, které určují úspěch rehabilitace a napomáhají ke stanovení úrovně rehabilitace s ohledem na očekávané schopnosti pacienta. Kognitivní stav pacienta má vliv na funkční schopnosti, délku pobytu v nemocnici a výsledky rehabilitace. Rehabilitace směřuje k obnovení nezávislého pohybu a funkce. Zpočátku je kladen důraz na běžné denní činnosti jako oblékání, osobní hygienu, přemisťování. Úroveň chůze a rovnováha predikují funkční nezávislost.
Snahou je většinu pacientů původně z vlastního domova propouštět dle možností opět do domácí péče. Nesoběstační pacienti jsou překládáni do zařízení následné péče. Institucionalizovaní pacienti často se špatnou prognózou mohou být většinou po ošetření a krátkodobé hospitalizaci překládáni zpět do zařízení, odkud byli přijati.
Osteoporóza a hojení zlomenin
Při hojení zlomenin je obnova strukturní geometrie a mechanických vlastností kosti zajištěna diferenciací a proliferací buněk, tvorbou organické kostní matrix a remodelací vytvořené kostní hmoty. Při nedostatku estradiolu se při hojení zlomenin u žen po menopauze svalek pomaleji mineralizuje a má nižší mechanickou odolnost. Ve vyšším věku je hojení zlomenin horší než u mladých osob a hlavní příčinou toho je pokles osteoblastogeneze a přežívání osteoblastů s věkem (79–80). Při osteoporóze je v experimentálních modelech hojení zlomenin zpomaleno, svalek má menší objem a mechanickou odolnost (81–84).
Pro hojení zlomenin má význam jednak dostatečný příjem bílkovin v potravě a jednak zásobení vitaminem D (85). Během prvních 3 dnů po zlomenině koncentrace kalcitriolu v séru rychle klesá a hormon se akumuluje v místě zlomenin (86). Receptory pro kalcitriol jsou v jádrech osteoblastů a chondrocytů a obsahuje je i callus (87). Experimentálně bylo prokázáno významně lepší hojení zlomenin při podávání kalcitriolu. V prvních 6 týdnech po fraktuře proximálního humeru bylo hojení lepší při podávání vitaminu D (88).
Lepší hojení zlomenin bylo prokázáno také při léčbě kalcitoninem, jehož analgetický efekt umožňuje rychlejší mobilizaci nemocného (89–90). Naopak podávání stroncium ranelátu hojení zlomenin neovlivnilo (91). Vliv některých dalších léků na hojení zlomenin je zatím studován (statiny, litium, destičkový růstový faktor).
Pokud je osteoporóza léčena aminobisfosfonáty, tvoří se při zpomalené remodelaci větší callus, jehož mechanická odolnost je normální (92), nicméně v prvních 6 týdnech může být hojení fraktury zpomaleno (93). Opakované podávání menších dávek aminobisfosfonátu zpomaluje remodelaci hojící se kosti, protože funkce osteoklastů není dostatečná (94). Vliv aminobisfosfonátů na hojení zlomenin při osteoporóze indukované glukokortikoidy nebyl zatím důkladněji studován.
Osteoanabolická léčba teriparatidem (95) zlepšuje fixaci implantátu v kosti (96). Byl také prokázán synergický účinek podávání parathormonu a zatěžování kosti (97). Přesto se při podávání teriparatidu prokazuje v prvních 6 týdnech zrychlené hojení zlomeniny nezatěžované kosti (Collesovy fraktury). Synergický účinek podávání parathormonu a zatěžování kosti znovu potvrdil mnohokrát zdůrazňovanou nutnost a přínos včasné rehabilitace nemocných se zlomeninou (98).
Sekundární prevence zlomenin
Prevence nové zlomeniny horního konce stehenní kosti má být komplexní. Zahrnuje zlepšení kvalitykostní tkáně, udržení či zlepšení pohybové aktivity, opatření v prevenci pádů a řešení vhodného sociálního zázemí. Ortoped a traumatolog se často jako první setkává se zlomeninou jako projevem osteoporózy. Jeho úkolem je nejenom ošetření zlomeniny proximálního femuru, ale také u pacienta doplnit zásobení proteiny, kalciem a vitaminem D a doporučit vhodnou rehabilitaci a následnou farmakologickou léčbu. U nemocných s nízkotraumatickou zlomeninou proximálního femuru a tedy s vysokým absolutním rizikem další zlomeniny by ortopéd měl doporučit vyšetření a léčbu ve specializovaném osteologickém pracovišti.
Algoritmus ortopedické péče u pacientů se zlomeninou horního konce stehenní kosti
Pacienti se zlomeninou proximálního femuru mají být hospitalizováni, preoperačně zajištěni (interní vyšetření, extenze, prevence infekce a tromboembolické nemoci)
- a) Chirurgické řešení by mělo být zajištěno do 24 hodin osteosyntézou DHS nebo nitrodřeňovým implantátem, případně implantací cervikokapitální endoprotézy nebo totální endoprotézy kyčelního kloubu. Osteosyntéza zlomeniny krčku femuru by měla být provedena do 6 hodin.
- b) V pooperačním období má být zajištěno monitorování EKG, TK, bolesti, má být zajištěna saturace kyslíkem, úprava nerovnováhy minerálů, dieta s vysokým obsahem bílkovin a jednorázově podání 60 000 IU vitaminu D3 (85).
- c) Pacient má být mobilizován do 24 hodin, pokud to umožňuje jeho celkový stav a stav operované končetiny. Mobilita, funkce a duševní schopnosti před úrazem určují po chirurgickém ošetření úspěch rehabilitace, délku hospitalizace a stupeň závislosti na dopomoci.
- d) Propuštění do domácího ošetření, zařízení následné péče nebo zpět do institucí má být provázeno zhodnocením rizika další zlomeniny a doporučením léčby osteoporózy nebo dalších vhodných vyšetření. Pacienti mají být po propuštění z ortopedického oddělení předáni do dlouhodobé odborné péče spádového osteologického pracoviště. Jeho úkolem je zajistit vyšetření nutná pro diferenciální diagnostiku a vhodný způsob léčby pacienta. Pacienti mají být rovněž předáni do péče rehabilitačního pracoviště, kde po zhodnocení stavu pacienta jsou zajištěna indikovaná cvičení a prevence pádů.
Práce vznikla v rámci Výzkumného záměru MZd ČR 0002384101 a MZd ČR 000237280
MUDr. Jan Vaculík
Ortopedická klinika IPVZ FN Na Bulovce
Budínova 2
180 81 Praha 8
e-mail: jan-vaculik@volny.cz
Sources
1. Vaculík J, Malkus T, Majerníček M, Podškubka A, Dungl P. Incidence zlomenin proximálního femuru. Ortopedie 2007; 1(2): 62–8.
2. Štěpán JJ, Havelka S, Kamberská Z, Bernátová M. Epidemiologie der Osteoporose in der Tschechischen Republik. J Mineralstoffwechsel 2002; 9(3): 7–13.
3. Boonen S, Autier P, Barette M, Vanderschueren D, Lips P, Haentjens P. Functional outcome and quality of life following hip fracture in elderly women: a prospective controlled study. Osteoporos Int 2004; Feb; 15(2): 87–94.
4. Giversen IM. Time trends of mortality after first hip fractures. Osteoporos Int 2007; Jun; 18(6): 721–32.
5. Koot VC, Peeters PH, de Jong JR, Clevers GJ, van der Werken C. Functional results after treatment of hip fracture: a multicentre, prospective study in 215 patients. Eur J Surg 2000; Jun; 166(6): 480–5.
6. Burge R, Dawson-Hughes B, Solomon DH, Wong JB, King A, Tosteson A. Incidence and economic burden of osteoporosis-related fractures in the United States. 2005-2025. J Bone Miner Res 2007; Mar; 22(3): 465–75.
7. Davis FM, Woolner DF, Frampton C, Wilkinson A, Grant A, Harrison RT, et al. Prospective, multi-centre trial of mortality following general or spinal anaesthesia for hip fracture surgery in the elderly. Br J Anaesth 1987 Sep; 59(9): 1080–8.
8. Villar RN, Allen SM, Barnes SJ. Hip fractures in healthy patients: operative delay versus prognosis. British medical journal (Clinical research ed. 1986; Nov 8; 293(6556): 1203–4.
9. Hefley FG, Jr, Nelson CL, Puskarich-May CL. Effect of delayed admission to the hospital on the preoperative prevalence of deep-vein thrombosis associated with fractures about the hip. J Bone Joint Surg Am 1996 Apr; 78(4): 581–3.
1 0. Perez JV, Warwick DJ, Case CP, Bannister GC. Death after proximal femoral fracture an autopsy study. Injury 1995; May; 26(4): 237–40.
11. Bredahl C, Nyholm B, Hindsholm KB, Mortensen JS, Olesen AS. Mortality after hip fracture: results of operation within 12 h of admission. Injury 1992; 23(2): 83–6.
12. Hamlet WP, Lieberman JR, Freedman EL, Dorey FJ, Fletcher A, Johnson EE. Influence of health status and the timing of surgery on mortality in hip fracture patients. Am J Orthop 1997; Sep; 26(9): 621–7.
13. Holt EM, Evans RA, Hindley CJ, Metcalfe JW. 1000 femoral neck fractures: the effect of pre-injury mobility and surgical experience on outcome. Injury 1994 Mar; 25(2): 91–5.
14. Parker MJ, Handoll HH. Pre-operative traction for fractures of the proximal femur in adults. Cochrane Database Syst Rev 2006; 3: CD000168.
15. Levi N. Urinary tract infection and cervical hip fracture. Int J Risk Safety Med 1998; 11 : 41–4.
16. Gillespie WJ, Walenkamp G. Antibiotic prophylaxis for surgery for proximal femoral and other closed long bone fractures. Cochrane Database Syst Rev 2001; (1): CD000244.
17. Nelson CL, Green TG, Porter RA, Warren RD. One day versus seven days of preventive antibiotic therapy in orthopedic surgery. Clin Orthop Relat Res 1983; Jun(176): 258–63.
18. Gillespie W, Murray D, Gregg PJ, Warwick D. Risks and benefits of prophylaxis against venous thromboembolism in orthopaedic surgery. J Bone Joint Surg Br 2000 May; 82(4): 475–9.
19. Salvati EA, Pellegrini VD, Jr., Sharrock NE, Lotke PA, Murray DW, Potter H, et al. Recent advances in venous thromboembolic prophylaxis during and after total hip replacement. J Bone Joint Surg Am 2000; Feb; 82(2): 252–70.
20. Handoll HH, Farrar MJ, McBirnie J, Tytherleigh-Strong G, Awal KA, Milne AA, et al. Heparin, low molecular weight heparin and physical methods for preventing deep vein thrombosis and pulmonary embolism following surgery for hip fractures. Cochrane Database Syst Rev 2000(2): CD000305.
21. Prevention of pulmonary embolism and deep vein thrombosis with low dose aspirin: Pulmonary Embolism Prevention (PEP) trial. Lancet 2000; Apr 15; 355(9212): 1295–302.
22. Amaragiri SV, Lees TA. Elastic compression stockings for prevention of deep vein thrombosis. Cochrane Database Syst Rev 2001(1).
23. Powers PJ, Gent M, Jay RM, Julian DH, Turpie AG, Levine M, et al. A randomized trial of less intense postoperative warfarin or aspirin therapy in the prevention of venous thromboembolism after surgery for fractured hip. Arch Intern Med 1989; Apr; 149(4): 771–4.
24. Hamilton HW, Crawford JS, Gardiner JH, Wiley AM. Venous thrombosis in patients with fracture of the upper end of the femur. A phlebographic study of the effect of prophylactic anticoagulation. J Bone Joint Surg Br 1970; May; 52(2): 268–89.
25. Borgstroem S, Greitz T, Van Der Linden W, Molin J, Rudics I. Anticoagulant Prophylaxis of Venous Thrombosis in Patients with Fractured Neck of the Femur; a Controlled Clinical Trial Using Venous Phlebography. Acta Chir Scand 1965; May;129 : 500–8.
26. Eriksson BI, Lassen MR. Duration of prophylaxis against venous thromboembolism with fondaparinux after hip fracture surgery: a multicenter, randomized, placebo-controlled, double-blind study. Arch Intern Med 2003; Jun 9; 163(11): 1337–42.
27. Geerts WH, Pineo GF, Heit JA, Bergqvist D, Lassen MR, Colwell CW, et al. Prevention of venous thromboembolism: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy Chest 2004 Sep; 126(3 Suppl): 338S–400S.
28. Sorenson RM, Pace NL. Anesthetic techniques during surgical repair of femoral neck fractures. A meta-analysis. Anesthesiology 1992; Dec; 77(6): 1095–104.
29. Parker MJ, Handoll HH, Griffiths R. Anaesthesia for hip fracture surgery in adults. Cochrane Database Syst Rev 2004(4): CD000521.
30. Raaymakers EL, Marti RK. Non-operative treatment of impacted femoral neck fractures. A prospective study of 170 cases. J Bone Joint Surg Br 1991 Nov;73(6): 950–4.
31. Parker MJ, Myles JW, Anand JK, Drewett R. Cost-benefit analysis of hip fracture treatment. J Bone Joint Surg Br 1992 Mar; 74(2): 261–4.
32. Parker MJ, Blundell C. Choice of implant for internal fixation of femoral neck fractures. Meta-analysis of 25 randomised trials including 4,925 patients. Acta Orthop Scand 1998 Apr; 69(2): 138–43.
33. Hui AC, Anderson GH, Choudhry R, Boyle J, Gregg PJ. Internal fixation or hemiarthroplasty for undisplaced fractures of the femoral neck in octogenarians. J Bone Joint Surg Br 1994 Nov; 76(6): 891–4.
34. Davison JN, Calder SJ, Anderson GH, Ward G, Jagger C, Harper WM, et al. Treatment for displaced intracapsular fracture of the proximal femur. A prospective, randomised trial in patients aged 65 to 79 years. J Bone Joint Surg Br 2001; Mar; 83(2): 206–12.
35. Blomfeldt R, Tornkvist H, Ponzer S, Soderqvist A, Tidermark J. Comparison of internal fixation with total hip replacement for displaced femoral neck fractures. Randomized, controlled trial performed at four years. J Bone Joint Surg Am 2005; Aug; 87(8): 1680–8.
36. Frihagen F, Nordsletten L, Madsen E. Hemiarthroplasty of internal fixation for intracapsular displaced femoral neck fractures: randomised controlled trial. BMJ 2007.
37. Keating JF, Grant A, Masson JM, Scott NW, Forbes JF. Randomized comparison of reduction and fixation, bipolar hemiarthroplasty, and total hip arthroplasty: Treatment of displaced intracapsular hip fractures in healthy older patients. J Bone Joint Surg Am 2006; 88 : 249–60.
38. Tidermark J, Ponzer S, Svensson O, Soderqvist A, Tornkvist H. Internal fixation compared with total hip replacement for displaced femoral neck fractures in the elderly. A randomised, controlled trial. J Bone Joint Surg Br 2003; Apr; 85(3): 380–8.
39. van Vugt AB, Oosterwijk WM, Goris RJ. Osteosynthesis versus endoprosthesis in the treatment of unstable intracapsular hip fractures in the elderly. A randomised clinical trial. Arch Orthop Trauma Surg 1993; 113(1): 39–45.
40. Rogmark C, Carlsson A, Johnell O, Sernbo I. A prospective randomised trial of internal fixation versus arthroplasty for displaced fractures of the neck of the femur: Functional outcomes for 450 patients at 2 years. J Bone Joint Surg Br 2002; 84 : 183–8.
41. Squires B, Bannister G. Displaced intracapsular neck of femur fractures in mobile independent patients: total hip replacement or hemiarthroplasty? Injury 1999; Jun; 30(5): 345–8.
42. Kuokkanen HO, Suominen PK, Korkala OL. The late outcome of femoral neck fractures. Int Orthop 1990; 14(4): 377–80.
43. Jalovaara P, Virkkunen H. Quality of life after primary hemiarthroplasty for femoral neck fracture. 6-year follow-up of 185 patients. Acta Orthop Scand 1991 Jun; 62(3): 208–17.
44. Gebhard JS, Amstutz HC, Zinar DM, Dorey FJ. A comparison of total hip arthroplasty and hemiarthroplasty for treatment of acute fracture of the femoral neck. Clin Orthop Relat Res 1992; Sep(282): 123–31.
45. Nilsson LT, Jalovaara P, Franzen H, Niinimaki T, Stromqvist B. Function after primary hemiarthroplasty and secondary total hip arthroplasty in femoral neck fracture. J Arthroplasty 1994; Aug; 9(4): 369–74.
46. Garden RS. Malreduction and avascular necrosis in subcapital fractures of the femur. J Bone Joint Surg Br 1971; May; 53(2): 183–97.
47. Swiontkowski MF, Hansen ST, Jr., Kellam J. Ipsilateral fractures of the femoral neck and shaft. A treatment protocol. J Bone Joint Surg Am 1984; Feb; 66(2): 260–8.
48. Garden RS. Reduction and fixation of subcapital fractures of the femur. Orthop Clin North Am 1974; Oct; 5(4): 683–712.
49. Banks HH. Nonunion in fractures of the femoral neck. Orthop Clin North Am 1974; Oct;5(4): 865–85.
50. Skinner P, Riley D, Ellery J, Beaumont A, Coumine R, Shafighian B. Displaced subcapital fractures of the femur: a prospective randomized comparison of internal fixation, hemiarthroplasty and total hip replacement. Injury 1989; Sep; 20(5): 291–3.
51. Parker MJ, Tripuraneni G, McGreggor-Riley J. Osteotomy, compression and reaming techniques for internal fixation of extracapsular hip fractures. Cochrane Database Syst Rev 2001; (3): CD000522.
52. Christie J, Robinson CM, Singer B, Ray DC. Medullary lavage reduces embolic phenomena and cardiopulmonary changes during cemented hemiarthroplasty. J Bone Joint Surg Br 1995; May; 77(3): 456–9.
53. Wheelwright EF, Byrick RJ, Wigglesworth DF, Kay JC, Wong PY, Mullen JB, et al. Hypotension during cemented arthroplasty. Relationship to cardiac output and fat embolism. J Bone Joint Surg Br 1993; Sep; 75(5): 715–23.
54. Yamagata M, Chao EY, Ilstrup DM, Melton LJ, 3rd, Coventry MB, Stauffer RN. Fixed-head and bipolar hip endoprostheses. A retrospective clinical and roentgenographic study. J Arthroplasty 1987; 2(4): 327–41.
55. Emery RJ, Broughton NS, Desai K, Bulstrode CJ, Thomas TL. Bipolar hemiarthroplasty for subcapital fracture of the femoral neck. A prospective randomised trial of cemented Thompson and uncemented Moore stems. J Bone Joint Surg Br 1991; Mar; 73(2): 322–4.
56. Dorr LD, Glousman R, Hoy AL, Vanis R, Chandler R. Treatment of femoral neck fractures with total hip replacement versus cemented and noncemented hemiarthroplasty. J Arthroplasty 1986; 1(1): 21–8.
57. Eiskjaer S, Gelineck J, Soballe K. Fractures of the femoral neck treated with cemented bipolar hemiarthroplasty. Orthopedics 1989; Dec; 12(12): 1545–50.
58. Wetherell RG, Hinves BL. The Hastings bipolar hemiarthroplasty for subcapital fractures of the femoral neck. A 10-year prospective study. J Bone Joint Surg Br 1990; Sep; 72(5): 788–93.
59. Calder SJ, Anderson GH, Jagger C, Harper WM, Gregg PJ. Unipolar or bipolar prosthesis for displaced intracapsular hip fracture in octogenarians: a randomised prospective study. J Bone Joint Surg Br 1996; May; 78(3): 391–4.
60. Marcus RE, Heintz JJ, Pattee GA. Don’t throw away the Austin Moore. J Arthroplasty 1992; Mar; 7(1): 31–6.
61. Bartoníček J, Džupa V, Skála-Rosenbaum J, Pazdírek P. Zlomeniny krčku u dospělých – Souhrnný referát. Úraz chir 2003; 11(3). 10–23.
62. Chan RN, Hoskinson J. Thompson prosthesis for fractured neck of femur. A comparison of surgical approaches. J Bone Joint Surg Br 1975; Nov; 57(4): 437–43.
63. Unwin AJ, Thomas M. Dislocation after hemiarthroplasty of the hip: a comparison of the dislocation rate after posterior and lateral approaches to the hip. Ann R Coll Surg Engl 1994; Sep; 76(5): 327–9.
64. Keene GS, Parker MJ, Pryor GA. Mortality and morbidity after hip fractures. BMJ 1993; Nov 13; 307(6914): 1248–50.
65. Sikorski JM, Barrington R. Internal fixation versus hemiarthroplasty for the displaced subcapital fracture of the femur. A prospective randomised study. J Bone Joint Surg Br 1981; 63–B(3): 357–61.
66. Ravikumar KJ, Marsh GD. Internal fixation versus heimarthroplasty versus total hip arthroplasty for displaced subcapital fractures of femur – 13 year results of a prospective randomized study. Injury 2000; 31 : 793–7.
67. Parker MJ, Handoll HH. Gamma and other cephalocondylic intramedullary nails versus extramedullary implants for extracapsular hip fractures in adults. Cochrane Database Syst Rev 2008; (3): CD000093.
68. Palm H, Jacobsen S, Sonne-Holm S, Gebuhr P. Integrity of the lateral femoral wall in intertrochanteric hip fractures: an important predictor of a reoperation. J Bone Joint Surg Am 2007; Mar; 89(3): 470–5.
69. Gotfried Y. The lateral trochanteric wall: a key element in the reconstruction of unstable pertrochanteric hip fractures. Clin Orthop Relat Res 2004; Aug(425): 82–6.
70. Anglen JO, Weinstein JN. Nail or plate fixation of intertrochanteric hip fractures: changing pattern of practice. A review of the American Board of Orthopaedic Surgery Database. J Bone Joint Surg Am 2008; Apr; 90(4): 700–7.
71. Forte ML, Virnig BA, Kane RL, Durham S, Bhandari M, Feldman R, et al. Geographic variation in device use for intertrochanteric hip fractures. J Bone Joint Surg Am 2008; Apr; 90(4): 691–9.
72. Douša P, Bartoníček J, Jehlička D, Skála-Rosenbaum J. Osteosyntéza trochanterických zlomenin proximálním femorálním hřebem (PFN Synthes). Acta Chirurgiae Orthopaedicae et Traumatologiae Čechosl 2002; 69 : 22–30.
73. Pavelka T, Kortus J, Linhart M. Osteosyntéza zlomenin proximálního femuru krátkým proximálním femorálním hřebem. Acta Chirurgiae Orthopaedicae et Traumatologiae Čechosl 2003; 70(31–38).
74. Pavelka T, Matějka J, Červenková H. Komplikace osteosyntézy krátkým proximálním femorálním hřebem. Acta Chirurgiae Orthopaedicae et Traumatologiae Čechosl 2005; 72 : 344–54.
75. Čech O, Košťál R, Váchal J. Nestabilní pertorchanterické zlomeniny – jejich biomechanika, klasifikace a terapie. Acta Chirurgiae Orthopaedicae et Traumatologiae Čechosl 2000; 67 : 17–27.
76. Koval KJ, Zuckermann JD. Hip fractures: II. Evaluation and treatment of intertrochanteric fractures. J Am Acad Orthop Surg 1994; 2 : 150–6.
77. Janzing HM, Houben BJ, Brandt SE. The Gotfried Percutaneous Compression Plate versus the Dynamic Hip Screw in the treatment of pertrochanteric hip fractures: minimal invasive treatment reduces operative time and postoperative pain. J Trauma 2002; 52(293–298).
78. Krasheninnikoff M, Gramkow J, Trholm C, Gotfried PC. CP: a new method for osteosynthesis of intertrochanteric fractures of the femur. Acta Orthop Scand 1998; 280(Suppl): 30–1.
79. Giannoudis P, Tzioupis C, Almalki T, Buckley R. Fracture healing in osteoporotic fractures: is it really different? A basic science perspective. Injury 2007 Mar; 38 Suppl 1: S90–9.
80. D’Ippolito G, Schiller PC, Ricordi C, Roos BA, Howard GA. Age-related osteogenic potential of mesenchymal stromal stem cells from human vertebral bone marrow. J Bone Miner Res 1999; Jul; 14(7): 1115–22.
81. Yingjie H, Ge Z, Yisheng W, Ling Q, Hung WY, Kwoksui L, et al. Changes of microstructure and mineralized tissue in the middle and late phase of osteoporotic fracture healing in rats. Bone 2007 Oct; 41(4): 631–8.
82. McCann RM, Colleary G, Geddis C, Clarke SA, Jordan GR, Dickson GR, et al. Effect of osteoporosis on bone mineral density and fracture repair in a rat femoral fracture model. J Orthop Res 2008; Mar; 26(3): 384–93.
83. van der Poest Clement E, Patka P, Vandormael K, Haarman H, Lips P. The effect of alendronate on bone mass after distal forearm fracture. J Bone Miner Res 2000; Mar; 15(3): 586–93.
84. Goldhahn J, Suhm N, Goldhahn S, Blauth M, Hanson B. Influence of osteoporosis on fracture fixation–a systematic literature review. Osteoporos Int 2008 Jun; 19(6): 761–72.
85. Schurch MA, Rizzoli R, Slosman D, Vadas L, Vergnaud P, Bonjour JP. Protein supplements increase serum insulin-like growth factor-I levels and attenuate proximal femur bone loss in patients with recent hip fracture. A randomized, double-blind, placebo-controlled trial. Ann Intern Med 1998; May 15; 128(10): 801–9.
86. Jingushi S, Iwaki A, Higuchi O, Azuma Y, Ohta T, Shida JI, et al. Serum 1alpha,25-dihydroxyvitamin D3 accumulates into the fracture callus during rat femoral fracture healing. Endocrinology 1998; Apr; 139(4): 1467–73.
87. Kato A, Bishop JE, Norman AW. Evidence for a 1 alpha,25-dihydroxyvitamin D3 receptor/binding protein in a membrane fraction isolated from a chick tibial fracture-healing callus. Biochem Biophys Res Commun 1998; Mar 27; 244(3): 724–7.
88. Doetsch AM, Faber J, Lynnerup N, Watjen I, Bliddal H, Danneskiold-Samsoe B. The effect of calcium and vitamin D3 supplementation on the healing of the proximal humerus fracture: a randomized placebo-controlled study. Calcif Tissue Int 2004; Sep; 75(3): 183–8.
89. Pun KK, Chan LW. Analgesic effect of intranasal salmon calcitonin in the treatment of osteoporotic vertebral fractures. Clin Ther 1989; Mar-Apr; 11(2): 205–9.
90. Huusko TM, Karppi P, Kautiainen H, Suominen H, Avikainen V, Sulkava R. Randomized, double-blind, clinically controlled trial of intranasal calcitonin treatment in patients with hip fracture. Calcif Tissue Int 2002; Dec; 71(6): 478–84.
91. Cebesoy O, Tutar E, Kose KC, Baltaci Y, Bagci C. Effect of strontium ranelate on fracture healing in rat tibia. Joint Bone Spine 2007 Dec; 74(6): 590–3.
92. Peter CP, Cook WO, Nunamaker DM, Provost MT, Seedor JG, Rodan GA. Effect of alendronate on fracture healing and bone remodeling in dogs. J Orthop Res 1996 Jan; 14(1): 74–9.
93. Li C, Mori S, Li J, Kaji Y, Akiyama T, Kawanishi J, et al. Long-term effect of incadronate disodium (YM-175) on fracture healing of femoral shaft in growing rats. J Bone Miner Res 2001; Mar; 16(3): 429–36.
94. McDonald MM, Dulai S, Godfrey C, Amanat N, Sztynda T, Little DG. Bolus or weekly zoledronic acid administration does not delay endochondral fracture repair but weekly dosing enhances delays in hard callus remodeling. Bone 2008; Jun 3.
95. Kakar S, Einhorn TA, Vora S, Miara LJ, Hon G, Wigner NA, et al. Enhanced Chondrogenesis and Wnt Signaling in PTH-Treated Fractures. J Bone Miner Res 2007; Dec; 22(12): 1903–12.
96. Andreassen TT, Fledelius C, Ejersted C, Oxlund H. Increases in callus formation and mechanical strength of healing fractures in old rats treated with parathyroid hormone. Acta Orthop Scand 2001; Jun; 72(3): 304–7.
97. Gardner MJ, van der Meulen MC, Carson J, Zelken J, Ricciardi BF, Wright TM, et al. Role of parathyroid hormone in the mechanosensitivity of fracture healing. J Orthop Res. 2007; Nov; 25(11): 1474–80.
98. Pfeifer M, Sinaki M, Geusens P, Boonen S, Preisinger E, Minne HW. Musculoskeletal rehabilitation in osteoporosis: a review. J Bone Miner Res 2004; Aug; 19(8):1208–14.
Labels
Dermatology & STDs Paediatric rheumatology Rheumatology
Article was published inCzech Rheumatology

2009 Issue 3-
All articles in this issue
- Konkomitující fibromyalgie u pacientů s revmatoidní artritidou
- Rituximab v rukou nefrologa – první zkušenosti
- Péče o pacienty se zlomeninou horního konce stehenní kosti. I. Ortopedická péče. Doporučené postupy České revmatologické společnosti a Společnosti pro metabolická onemocnění skeletu
- Bezpečnost biologické léčby – doporučení České revmatologické společnosti
- Současný pohled na etiopatogenezi fibromyalgie
- Vaskulární endotelový růstový faktor u zánětlivých revmatických nemocí
- Akcelerovaná ateroskleróza u systémového lupus erythematodes
- Czech Rheumatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Péče o pacienty se zlomeninou horního konce stehenní kosti. I. Ortopedická péče. Doporučené postupy České revmatologické společnosti a Společnosti pro metabolická onemocnění skeletu
- Vaskulární endotelový růstový faktor u zánětlivých revmatických nemocí
- Konkomitující fibromyalgie u pacientů s revmatoidní artritidou
- Bezpečnost biologické léčby – doporučení České revmatologické společnosti
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career