-
Medical journals
- Career
Bezpečnost podání anti-TNF alfa léčby u revmatických pacientů s chronickou hepatitidou B nebo C
Authors: O. Šléglová; Z. Mareček 1; P. Urbánek 1; K. Pavelka
Authors‘ workplace: Revmatologický ústav Praha ; Interní klinika ILF UK a ÚVN Praha 1
Published in: Čes. Revmatol., 15, 2007, No. 2, p. 105-111.
Category: Overview Reports
Overview
Použití inhibitorů tumor nekrotizujícího faktoru alfa (anti-TNF alfa) představuje velký pokrok v léčbě zánětlivých revmatických onemocnění, ale zároveň je tato terapie spojená i se zvýšeným rizikem infekcí. V článku je upozorněno na možnost reaktivace hepatitidy B při anti-TNF alfa léčbě, která měla v několika případech závažný průběh. Proto je nezbytné provádět screening hepatitidy B před nasazením léčby. Anti-TNF léčba může být bezpečná i u pacientů s chronickou hepatitidou B, pokud je před zahájením této léčby preventivně nasazen lamivudin nebo adefovir a během této léčby probíhá důsledná monitorace jaterních testů a virémie. Odlišná je situace u hepatitidy C. Anti-TNF alfa léčba se zdá být bezpečná u pacientů s chronickou hepatitidou C, ale screening hepatitid a důsledná monitorace jaterních testů a virémie během léčby je rovněž nezbytná. Jedna z prezentovaným studií ukazuje, že kombinace standardní antivirové léčby hepatitidy C s anti-TNF alfa léčbou může zlepšit naději na časné zastavení replikace viru. Problematice anti-TNF alfa léčby u pacientů s chronickou hepatitidou B nebo C je třeba věnovat více pozornosti a zvážit provedení dalších studií u pacientů s koincidencí těchto onemocnění.
Klíčová slova:
anti-TNF alfa léčba, hepatitida B, hepatitida C, zánětlivá revmatická onemocněníÚvod
Léčba inhibitory tumor nekrotizujícího faktoru alfa (anti-TNF alfa) se ukázala být vysoce efektivní terapií revmatoidní artritidy, juvenilní idiopatické artritidy, psoriatické artritidy i ankylozující spondylitidy. Předpokládá se, že počet takto léčených pacientů ve světě přesahuje 400 000 (1). Narůstající počet pacientů s sebou přináší řadu dalších otázek, které nebyly dosud jednoznačně zodpovězeny. Jednou z nich je otázka anti-TNF alfa léčby u pacientů s virovou hepatitidou B (HBV) nebo virovou hepatitidou C (HCV).
Možnost reaktivace chronické HBV či HBC infekce u pacientů podstupujících imunosupresivní léčbu je dobře známá a není jistě překvapivé, že většina těchto případů byla u transplantovaných nebo onkologických pacientů (2). V poslední době je však nárůst těchto případů i mezi revmatologickými pacienty podstupujícími anti-TNF alfa či anti-B buněčnou léčbu.
Hepatitida C
Infekce virem hepatitidy C je celosvětově se vyskytující infekce postihující okolo 170 milionů lidí. Celosvětová prevalence HCV infekce se pohybuje kolem 3 % populace. Odhaduje se, že ve Spojených státech je infikováno virem hepatitidy C kolem 3,9 milionu obyvatel. Prevalence v České republice byla v roce 2001 0,2 % (3).
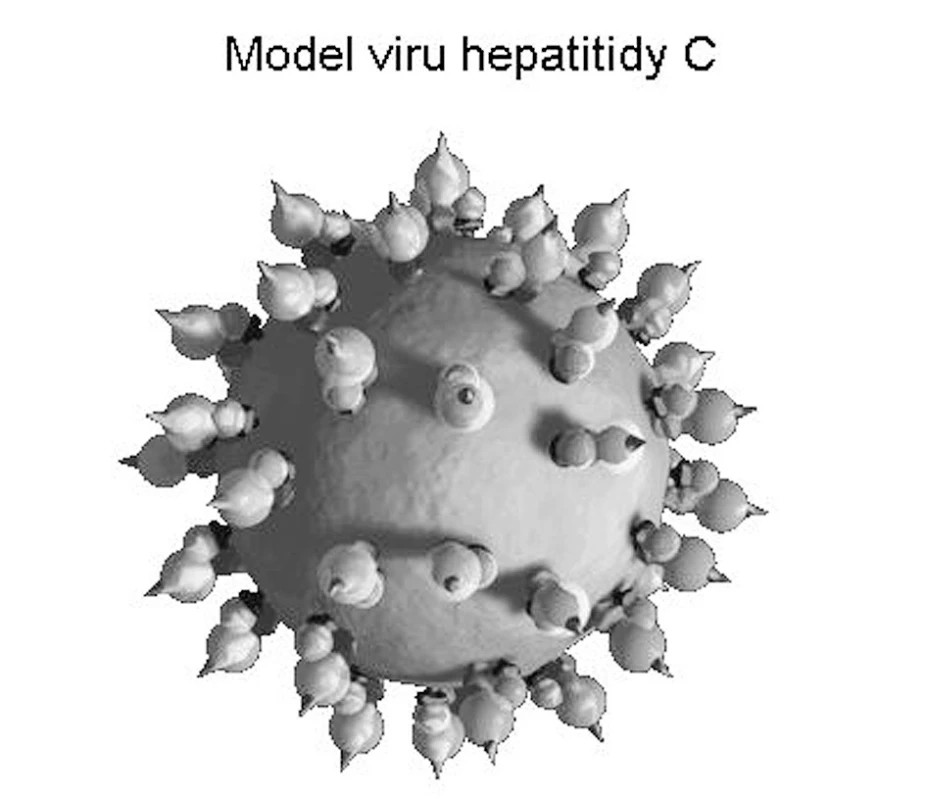
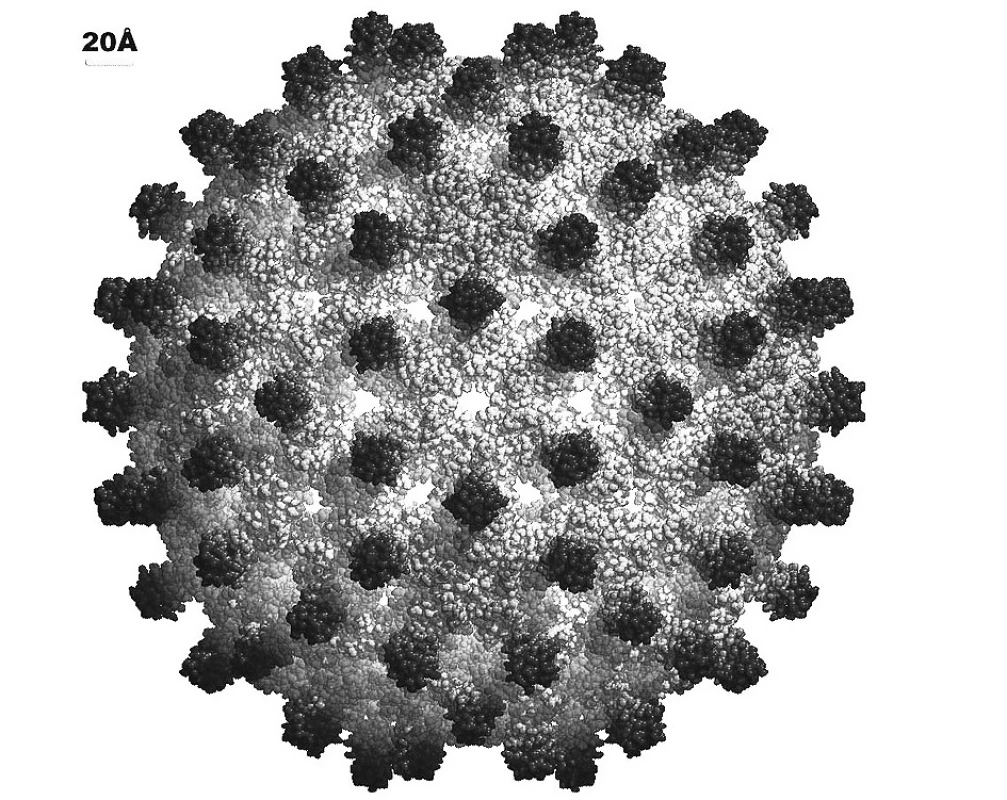
Virus hepatitidy C je RNA virus zařazený do čeledi Flaviridae (obr. 1). Virus zjišťujeme v krvi nepřímo, stanovením specifických protilátek anti-HCV. Skutečným průkazem virémie a infekčnosti je průkaz HCV RNA v séru metodou PCR. Existuje 6 antigenních subtypů viru.
Klinický obraz je velmi pestrý. Nejčastější je průběh asymptomatický v několika vlnách s výrazným kolísáním aktivity sérových trans-amináz. U řady pacientů je infekce provázená symptomatickými obtížemi podobnými revmatickým onemocněním – artralgiemi, myalgiemi, Sjögrenovým syndromem, kryoglobulinemií a vaskulitidou.V 60–85 % případů dochází k přechodu akutní infekce do chronické. Za chronickou HCV infekci je považována infekce s prokazatelnou přítomností viru v organismu delší než 6 měsíců. Chronická HCV infekce je v příčinném vztahu k rozvoji jaterní cirhózy i ke vzniku hepatocelulárního karcinomu (4).
Efekt neutralizace TNF alfa na hepatitidu C
Úloha TNF alfa u hepatitidy C není dosud jednoznačně objasněna. Jeho zvýšené hladiny se zjišťují jak u pacientů s akutní, tak chronickou HCV infekcí. Předpokládá se, že destrukce hepatocytů u chronické HCV infekce může být zprostředkována nadbytkem zánětlivých cytokinů včetně TNF alfa. Výzkumy naznačují, že zvýšená hladina TNF alfa koreluje se zvýšenými hodnotami ALT. Pacienti s výrazněji zvýšenými hladinami TNF alfa obyčejně špatně odpovídají na léčbu interferonem alfa (IFN alfa). Mechanismus TNF alfa indukované snížené odpovědi na léčbu IFN alfa není objasněný, ale obviňuje se inhibiční efekt TNF alfa na T-buňkovou proliferaci. Navíc TNF alfa může přispět k vývoji fibrózy jater, protože aktivuje Kupferovy buňky a makrofágy v játrech, které v důsledku aktivace secernují klíčový profibrogenní mediátor – tumor nekrotizující faktor beta (1, 3, 5, 6).
Klinické zkušenosti s anti TNF alfa léčbou u pacientů s hepatitidou C
Camphell a Host (7) v roce 2001 publikovali případ pacienta s Crohnovou chorobou a současně přítomnou HCV infekcí léčeného infliximabem bez jakéhokoliv zhoršení jaterních funkcí nebo nárůstu replikace viru, měřeného stanovením HCV RNA pomocí kvantitní PCR.
Peterson (8) prezentoval v roce 2003 studii, ve které sledoval 24 pacientů s revmatoidní artritidou a HCV infekcí léčených infliximabem nebo etanerceptem. 21 z nich dostalo etanercept, 3 infliximab. Nebyly zjištěny signifikantní rozdíly mezi úrovní virémie (hodnoceno stanovením HCV RNA pomocí PCR) před podáním léčby a po 3, 6, 9 a 12 měsících. 16 pacientů z 22 sledovaných mělo pokles virémie. Jaterní testy u žádného z 24 pacientů nevykázaly signifikantní změny. Data ukazují, že léčba neměla žádný negativní vliv na průběh chronické HCV infekce.
Parke a Reveille (9) ve svém článku popisují případ jiných 5 pacientů s revmatoidní artritidou, kde dokonce u jednoho z pacientů došlo k signifikantnímu poklesu úrovně virémie po terapii infliximabem.
Magliocco a Gottlieb (10) v poslední době prezentovali data 3 pacientů s psoriatickou artritidou (PsA) a současně přítomnou HCV infekcí léčených etanerceptem bez zhoršení jejich chronické hepatitidy. U těchto pacientů došlo během léčby chronické hepatitidy (interferonem alfa a ribavirinem) k výraznému zhoršení nebo k objevení se PsA. Po zahájení léčby etanerceptem nedošlo k elevaci jaterních testů ani k nárůstu replikace viru sledované pomocí HCV RNA PCR, ale aktivita PsA poklesla u všech sledovaných pacientů.
Nejnovější je studie Rouxe a kolektivu (11) z letošního roku, ve které bylo retrospektivně prověřeno 480 pacientů s revmatoidní artritidou (RA) nebo ankylozující spondylitidou (AS) léčených anti-TNF alfa léčbou. V souboru byli 3 pacienti s chronickou hepatitidou C. U žádného z pacientů nedošlo k vzestupu jaterních testů nebo virémie.
Autoři článků shodně konstatují (7–11), že anti-TNF léčba se zdá být bezpečná u pacientů s chronickou hepatitidou C, ale screening hepatitid a důsledná monitorace jaterních testů a virémie během léčby je nezbytná.
Nicméně v žádné z těchto studií nebyla provedena jaterní biopsie před a po dlouhodobé anti-TNF léčbě, která by dokumentovala, že nedošlo k progresi histologických změn v játrech.
Důkaz, že anti-TNF alfa léčba může mít příznivý efekt na vlastní HCV infekci, přináší studie nedávno publikovaná Zeinem (12). V této studii etanercept byl použit jako adjuvantní léčba k běžně používané léčbě hepatitidy C interferonem a ribavirinem u pacientů s chronickou HCV infekcí. 55 pacientů s chronickou HCV bylo randomizováno do dvou skupin. První skupina byla léčena interferonem alfa + ribavirinem, ke kterým byl přidán etanercept, druhá byla léčena interferon + ribavirin + placebo. Hlavním cílem bylo dosažení nepřítomnosti HCV RNA v séru pacientů ve 24. týdnu. U 12/19 (63 %) pacientů ve skupině s přidaným etanerceptem oproti 8/25 (32 %) ve skupině s placebem bylo dosaženo nepřítomnosti replikace viru. Výsledek ukazuje, že kombinace léčby s etanerceptem může zlepšit naději na časné zastavení replikace viru a snížit výskyt vedlejších účinků. Tato data rovněž naznačují, že anti-TNF alfa léčba může být prospěšná u pacientů s HCV infekcí, ačkoliv další kontrolované studie s větším počtem pacientů jsou nezbytné.
Hepatitida B
Virová hepatitida typu B je nejčastější virovou infekcí na světě postihující játra. Počet pacientů s chronickou hepatitidou B ve světě se odhaduje na více než 400 milionů a patří mezi hlavní příčiny vzniku cirhózy a hepatocelulárního karcinomu. Výskyt v rozvinutých zemích klesá díky hygienickým opatřením a postupně zaváděnému plošnému očkování. Podle posledních sérologických přehledů z roku 2001 je v ČR infikováno 0,56 % našich občanů (13).
Virus hepatitidy B je DNA virus z čeledi Hepadnaviridae. HBV virion se skládá z obalu a z jádra. Obal obsahuje HbsAg. V jádře je přítomen HbcAg, HbeAg, HBV DNA a enzym polymeráza HBV DNA (obr. 2, 3).
Image 3. Struktura HBV (Daneova částice). 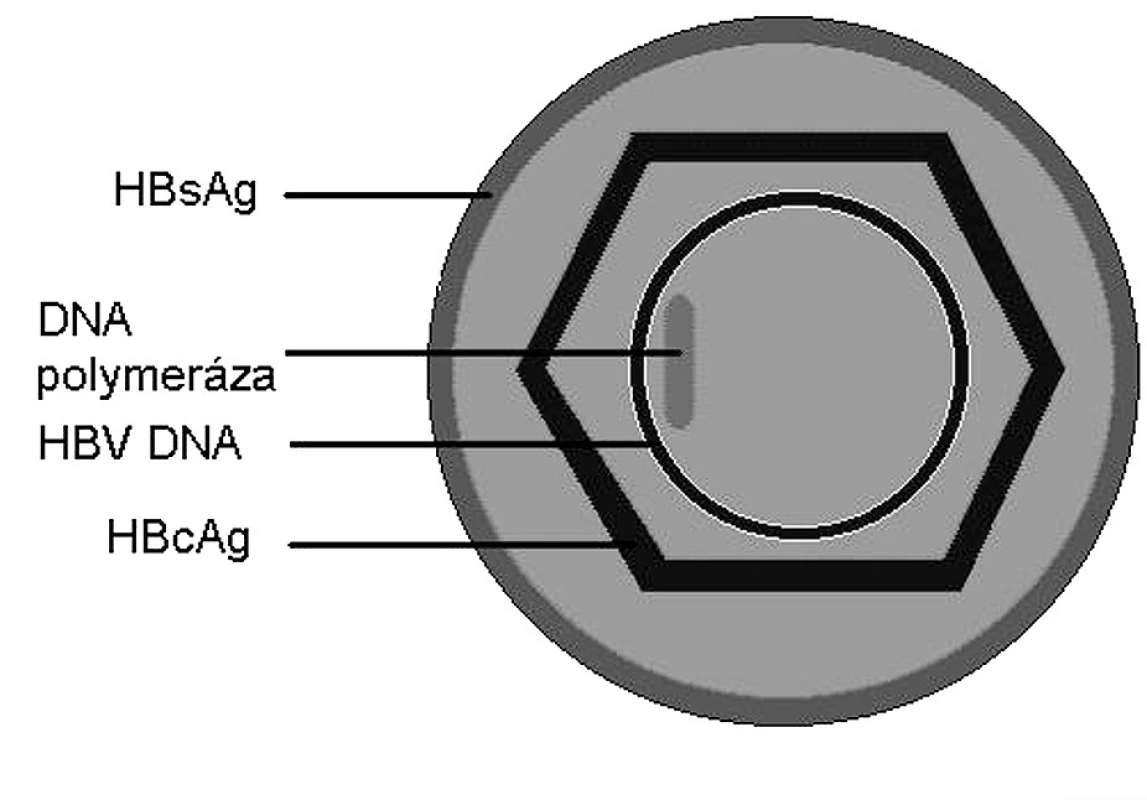
HbsAg je první pozitivní marker, který se objevuje v krvi ještě před manifestací klinických příznaků. U většiny nemocných pak vymizí do 4 měsíců. Při přítomnosti delší něž 6 měsíců se jedná o chronický průběh (graf 1). HbeAg je v séru u pacientů s příznivým průběhem přítomen jen krátce a signalizuje replikaci viru a vysokou infekčnost. HbcAg lze určit jen v játrech. Objevení se anti-Hbe je důležitým bodem, neboť signalizuje sérokonverzi a značí pokles infekčnosti a zastavení replikace viru. Protilátky anti-HBs se objeví po vymizení HbsAg. Nejcitlivější metodou v průkazu přítomnosti replikace viru je určení HBV DNA pomocí polymerázové reakce (PCR).
Graph 1. Průběh nálezu v séru při přechodu akutní hepatitidy B do chronicity. 
Při akutní hepatitidě B nacházíme elevaci ALT a AST spolu s pozitivitou HbsAg, HbeAg a vysokým titrem IgM anti-HBc protilátek. Klinický průběh však kolísá od asymptomatických, anikterických forem až po fulminantní rychle progredující onemocnění. Z mimojaterních manifestací se vyskytují exantémy, artralgie, polyarthritis nodosa či glomerulonefritida.
Chronická hepatitida B je infekce trvající déle než 6 měsíců. Do chronického stadia přechází kolem 5 % akutních hepatitid B prodělaných v dospělosti. V dětství či perinatálně získané infekce mají riziko přechodu do chronicity mnohem vyšší (30–90 %). Z těchto pacientů kolem 20 % progreduje do jaterní cirhózy. Prokázaný je příčinný vztah mezi HBV infekcí a hepatocelulárním karcinomem (tab. 1).
Table 1. Typické sérologické a molekulárně genetické nálezy jednotlivých stadií přirozeného vývoje infekce HBV. 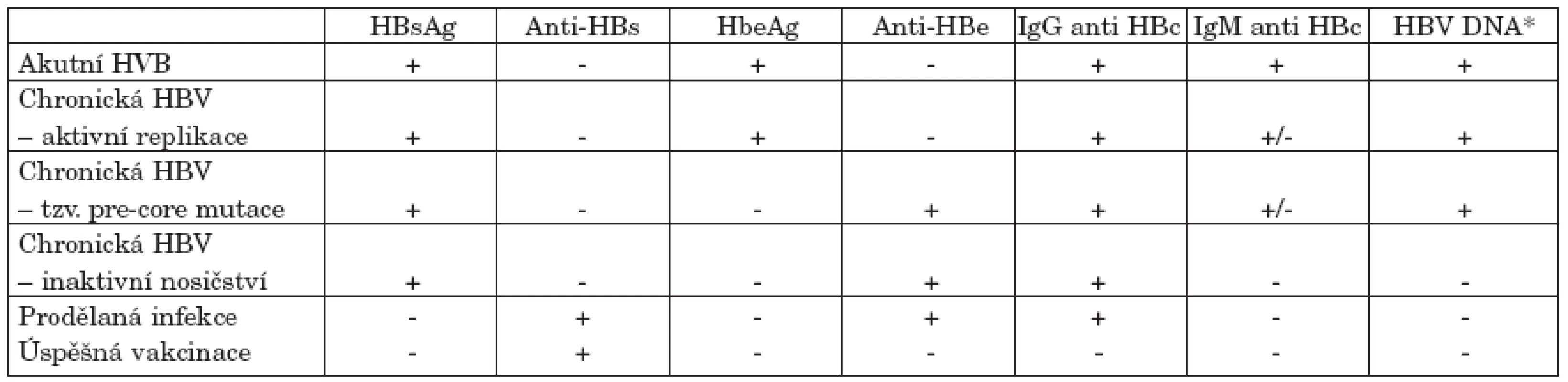
*Jako klinicky významná úroveň replikace HBV se uvádí hladina virémie > 105 kopií v ml. Virémii lze vyjádřit i v mezinárodních jednotkách IU/ml nebo v pg/ml.
Perzistence HBV v organismu i po dosažení HBsAg negativity je trvalá, u většiny HBsAg negativních jedinců s izolovanou pozitivitou anti-HBc lze prokázat nízkou úroveň virémie (HBV DNA v rozmezí 101–102 kopií/ml).
Je vhodné upozornit i na HBeAg negativní formu chronické hepatitidy B (tzv. pre-core mutace viru). Tato forma chronické hepatitidy B je častá ve Středomoří a v Asii. V důsledku mutace v precore oblasti genomu HBV se netvoří HBeAg, přestože virus se aktivně replikuje (HBV DNA v séru >105 kopií/ml).
Antivirová terapie (interferon alfa, lamivudin, adefovir) chronické HBV jednoznačně zvyšuje kvalitu života a při dodržení standardních postupů je levnější než léčba pokročilé jaterní cirhózy a snižuje výskyt hepatocelulárního karcinomu.
Efekt neutralizace TNF alfa na hepatitidu B
U pacientů s chronickou hepatitidou B jsou v séru i v játrech přítomny zvýšené hladiny TNF alfa. Rovněž je zvýšená exprese receptoru p75 pro TNF alfa jak v séru, tak v hepatocytech. TNF alfa je produkovaný pro HBV specifickými cytotoxickými T lymfocyty a snižuje replikaci viru hepatitidy B v hepatocytech non-cytolytickými mechanismy. Současně se předpokládá, že TNF alfa indukuje apoptózu hepatocytů infikovaných virem hepatitidy. Vše nasvědčuje tomu, že TNF alfa se podílí na specifické odpovědi hostitele na HBV infekci, míra důležitosti jeho úlohy není jasná (2, 5).
Studie in vitro i in vivo ukazují, že imunosupresiva zvyšují replikaci HBV (14). Toto zvýšení je pravděpodobně přisuzováno dvěma mechanismům. Jednak stimulačnímu efektu těchto léků na HBV replikaci a jednak přímému imunosupresivnímu efektu na pacientovu imunitu. Stimulační efekt je připisován zejména kortikoidům, protože se předpokládá, že HBV DNA obsahuje na glukokortikoidy citlivý element a ten je odpovědný za nárůst HBV DNA transkripční aktivity a virémie u pacientů dostávající kortikoidy (15). Imunosupresivní mechanismus je připisován nejen onkologické, ale i anti-TNF léčbě.
Klinické zkušenosti
V jednom z prvních zveřejněných případů referoval Ostuni (16) v roce 2003 případ 49letého pacienta s pozitivním HbsAg, u kterého došlo k reaktivaci hepatitidy B po 20 měsících léčby infliximabem pro těžkou revmatoidní artritidu. Byl podán lamivudin (při ponechání inflimabu) a hodnoty ALT a AST se pomalu normalizovaly.
Závažným případem je Duvoxem a Herodem (17) popsaná kazuistika. U mladé 28leté ženy s pozitivním HBsAg vznikla fulminantní hepatitida 2 týdny po podání druhé infuze infliximabu pro refrakterní formu Stillovy nemoci. Fulminantní průběh se nepodařilo odvrátit i přes okamžitou intenzivní péči a vysazení infliximabu. Pacientka musela podstoupit transplantaci jater.
Další případy referuje Estave (18) a kolektiv v roce 2004. V této studii byly testovány markery virové hepatitidy B a C u 80 pacientů s Crohnovou nemocí. Chronická hepatitida B byla zjištěna u 3 pacientů. Dva z těchto tří pacientů vyvinuli reaktivaci chronické hepatitidy B po vysazení léčby infliximabem. Třetí pacient, který byl léčen lamivudinem současně s léčbou infliximabem, neměl žádné známky zhoršení jaterních funkcí ani známky reaktivace HBV infekce.
V roce 2005 je v článku Wendlinga a Auga (19) popsán případ 35letého pacienta s prodělanou chronickou hepatitidou B. Pro progresi ankylozující spondylitidy (AS) byla nasazena léčba infliximabem. Léčba měla výborný efekt na AS, ale došlo k elevaci jaterních testů a nárůstu replikace viru měřen pomocí HBV DNA. Byla zahájena léčba lamivudinem v dávce 100 mg/den a pokračováno v léčbě infliximabem. Došlo k normalizaci jaterních testů a vymizení replikace viru.
Obdobný je případ pacienta publikovaný Millonigem a Kernem (20) v roce 2006. U pacienta léčeného inflimabem pro Crohnovu nemoc se po 3. infuzi infliximabu objevila subfulminantní hepatitida s vysokými hodnotami ALT a AST, bilirubinu a poklesem protrombinu. Sérologicky byl zjištěn pozitivní HbsAg antigen, anti Hbe, anti HBc a replikace viru více než 220 000 000 kopií/ml. Zpětně bylo zjištěno (rozborem staršího zamrazeného vzorku krve), že došlo k reaktivaci dříve inaparentně prodělané hepatitidy B. Vysazení a léčba lamivudinem vedla k postupnému zlepšování stavu.
Nejnovější je studie Rouxe a kolektivu (11) z letošního roku, ve kterém bylo retrospektivně prověřeno 480 pacientů s revmatoidní artritidou nebo ankylozující spondylitidou léčených etanercept nebo infliximab. V souboru byli 3 pacienti s chronickou hepatitidou B, kteří během anti-TNF alfa léčby dostali preventivně lamivudin. U žádného z pacientů nedošlo k vzestupu jaterních testů nebo virémie.
Autoři článků upozorňují na možnost reaktivace hepatitidy B při anti-TNF alfa léčbě, která měla v některých případech závažný průběh (16–20). Zároveň konstatují, že anti-TNF léčba může být bezpečná i u pacientů s chronickou hepatitidou B, ale screening hepatitid a důsledná monitorace jaterních testů a virémie během léčby je nezbytná (11, 16–20). Pacienti s HBV infekcí by měli během léčby preventivně užívat lamivudin nebo adefovir (11, 16, 18, 19, 20).
Diskuse
Revmatologové dosud nemají jednotný postoj ke screeningu a léčebným strategiím k prevenci reaktivace chronické HBV a HCV infekce u pacientů s revmatickými chorobami léčenými anti-TNF alfa léčbou.
Je známo, že imunosupresivní léky všech typů mohou způsobit reaktivaci chronické virové hepatitidy B nebo C. V případě revmatologických pacientů, kteří jsou léčení anti-TNF léčbou, jsou často podávány i další imunosupresivní léky, jako metotrexát, azathioprin či kortikoidy. Je těžké posoudit, kdy je příčinou reaktivace samotná anti-TNF léčba.
Donedávna se brala negativita HbsAg a současná pozitivita protilátek anti-HBs za známku úplné imunologické úzdravy. Podle posledních poznatků je i v tomto případě u řady pacientů prokazatelná virová replikace na velmi nízké úrovni, tudíž může v případě výrazné imunosu-prese dojít k reaktivaci hepatitidy B (13). Uvedené případy ukazují, že je nutné odlišně přistupovat k pacientům s chronickou HCV infekcí než k pacientům s chronickou HBV infekcí.
Kteří revmatologičtí pacienti by měli být vyšetřeni?
Jako efektivnější se jeví strategie vyšetřovat jednak rizikové pacienty a jednak pacienty podstupující imunosupresivní léčbu. Mezi rizikové pacienty patří lidé narození v endemických oblastech, homosexuálové, dialyzovaní pacienti, narkomani, pacienti opakovaně podstupující transfuzní léčbu a lidé žijící s osobami infikovanými hepatitidou. Screening by měl doporučen u všech pacientů podstupujících imunosupresivní léčbu (2).
Vzhledem k existenci případů závažných reaktivací hepatitidy po anti-TNF alfa léčbě (16–20), by měli být vyšetřeni všichni pacienti podstupující anti-TNF alfa léčbu. Rovněž by mělo být zváženo vyšetření u pacientů dostávajících vysoké dávky kortikoidů (více než 7,5 mg prednisonu nebo ekvivalentní dávka jiného kortikoidu denně). Obtížné je rozhodnutí o screeningu všech pacientů léčených methotrexátem nebo leflunomidem, ale data dokládají závažné ač řídké reaktivace hepatitid při užívání, snížení či vysazení těchto léků (16, 21, 22). Testováni nemusejí být pacienti užívající antimalarika, sulfasalazin, zlato nebo malé dávky kortikoidů.
Jaké testy mají být používány?
HBsAg, anti-HBs, anti-HBc pro screening hepatitidy B a anti-HCV pro screening hepatitidy C (1, 2).
U pacientů, kteří budou mít pozitivní HBsAg nebo pozitivní antiHBs + anti HBc nebo pozitivní anti-HBc, by bylo nutno kompletní sérologické vyšetření (HbeAg, anti HBe) včetně kvantitativního stanovení HBV DNA. Kvantitativní stanovení HBV je nezbytné i k odlišení tzv. pre-core mutace viru, kde nelze užít HBeAg jako ukazatel infekčnosti.
U pacientů s pozitivním anti-HCV je nezbytné doplnit kvantitativní vyšetření HCV RNA.
Kdo by měl dostat profylaktickou léčbu?
U všech pacientů chronicky infikovaných HBV či HCV virem podstupujících anti-TNF alfa léčbu je nutné provádět pravidelně monitoraci HBV DNA (u hepatitidy B) či HCV RNA (u hepatitidy C) a ALT k časnému zachycení eventuální reaktivace infekce. Profylaktická léčba by měla být zahájena u všech HBsAg pozitivních pacientů podstupujících imunosupresivní léčbu.
Ačkoliv žádné kontrolované studie nebyly provedeny, ve většině případů byl pozitivně hodnocen přínos preventivního podání lamivudinu (100 mg denně) u pacientů podstupujících imunosupresivní léčbu (23, 24). Je doporučováno podat lamivudin (Zeffix) před a během podání imunosuprese a pokračovat několik měsíců po ukončení, protože reaktivace hepatitidy někdy vzniká i po několika dnech či týdnech po ukončení imunosupresivní léčby. Krátké podání lamivudinu je bezpečné, bez nežádoucích vedlejších reakcí. Dlouhodobé podávání může vést ke vzniku lamivudin rezistentních mutant viru. Alternativní možností antivirové profylaxe je adefovir dipivoxil (Hespera). Doporučená dávka je 10 mg denně.
Pacienti se současně pozitivním HBeAg a/nebo vysokou virémií (měřeno pomocí HBV DNA) jsou pacienti s aktivní chronickou hepatitidou, indikovaní k zahájení protivirové terapie hepatitidy B. Teprve po stabilizaci stavu je možné uvažovat o anti-TNF alfa léčbě.
U pacientů HbsAg negativních, anti-Hbc pozitivních nemusí být rutinně nasazena profylaxe, ale měla by být zvážena individuálně. I v této skupině je nutné provádět pravidelnou monitoraci (1x za 3 měsíce) HBV DNA a ALT k časnému zachycení eventuální reaktivace (graf 2).
Graph 2. Algoritmus pro vyšetřování hepatitidy B (2). 
Vakcinace rizikových pacientů
K očkování proti hepatitidě B se v České republice používá vakcína vyrobená rekombinantní technikou genetického inženýrství. Běžně je k dispozici Engerix B. Povinně jsou očkováni zdravotníci, začala se provádět vakcinace dětí. Ke zvážení je profylaktická vakcinace u pacientů, kteří nebyli infikováni virem hepatitidy B a měla by u nich být zahájena imunosupresivní terapie.
Vakcína proti hepatitidě C zatím nebyla vyrobena.
Závěr
U pacientů zahajujících anti-TNF alfa léčbu je nezbytný screening virových hepatitid.
Je nutno odlišně přistupovat k pacientům s chronickou HBV infekcí než k pacientům s chronickou HCV infekcí.
V případě průkazu prodělané virové hepatitidy B je možné tuto léčbu zvážit u pacientů se stabilizovanou formou onemocnění a nízkou virémií. Pokud je léčba nasazena, je nutná důsledná monitorace pacientů včetně pravidelného sledování virémie pomocí HBV DNA PCR. U HbsAg pozitivních pacientů je vhodné nasadit preventivní léčbu lamivudinem nebo adefovirem. U složitějších případů je nutné postupovat individuálně po konzultaci s hepatologem.
Anti-TNF léčba se zdá být bezpečná u pacientů s chronickou hepatitidou C, ale screening hepatitidy C a důsledná monitorace jaterních testů a virémie pomocí HCV RNA PCR během léčby je nezbytná. Profylaktická léčba není známa.
Vzhledem k poměrně malým zkušenostem s anti TNF alfa léčbou u pacientů s HBV i HCV je nutné provedení dalších kontrolovaných studií s větším počtem takto léčených pacientů. Teprve pak bude možné, aby vznikla závazná doporučení ohledně anti-TNF alfa léčby u pacientů s chronickou HCV či HBV infekcí. Vzhledem k tomu, že se jedná o poměrně specifickou a malou skupinu pacientů budou přínosné i další zkušenosti s léčbou jednotlivých pacientů či z registrů TNF alfa léčby v jednotlivých zemích.
MUDr. Olga Šléglová
Revmatologický ústav
Na Slupi 4
128 50 Praha 2
e-mail: sleg@revma.cz
Sources
1. Desai SB, Furst SE. Problems encountered during anti-tumour necrosis factor therapy. Best Pract. Rese. Clin Rheumatol 2006; 20 : 757–790.
2. Calabrese LH, Zein NN, Vassilopoulos D. Hepatitis B virus reactivation with immunosuppressive therapy in rheumatic diseases: assessment and preventive strategies. Ann Rheum Dis 2006; 65 : 983–989.
3. Frank AP, Reveille JD. Anti-tumor necrosis factor agents for rheumatoid arthritis in the setting of chronic hepatitis C infection. Arthritis Rheum 2004; 51 : 800–804.
4. Urbánek P, Husa P, Kumpel P, Šperl J. Doporučení české hepatologické společnosti pro diagnostiku a léčbu chronické hepatitidy C. Vnitřní lékařství 2005; 51 : 1131–1137.
5. Calabrese LH, Zein NN, Vassilopoulos D. Safety of anti tumor necrosis factor therapy in patients with chronic viral infections: hepatic C, hepatitis B, and HIV infection. Ann Rheum Dis 2004; 63 : 18–24.
6. Tilg H, Kaser A, Moschen AR. How to modulate inflammatory cytokines in liver diseases. Liver International 2006; 26 : 1029–1039.
7. Campbell S, Ghosh S. Infliximab therapy for Crohn’s disease in the presence of chronic hepatitis C infection. Eur J Gastroenterol Hepatol 2001; 13 : 191–2.
8. Peterson JR, Hsu FC, Simkin PA, Wener MH. Effect of tumor necrosis necrosis factor alpha antagonists on serum transaminases and viraemia in patients with rheumatoid arthritis and chronic hepatitis C infection. Ann Rheum Dis 2003; 62 : 1078–82.
9. Parke FA, Reveille JD. Anti-tumor necrosis factor agents for rheumatoid arthritis in the setting of chronic hepatitis C infection. Arthritis Rheum 2004; 51 : 800–4.
10. Magliocco MA, Gottlieb AB. Etanercept therapy for patients with psoriatic arthritis and concurrent hepatitis C virus infection: report of 3 cases. J Am Acad Dermatol 2004; 51 : 580–4.
11. Roux CH, Brocq O, Breuil V, Albert C, Euller-Ziegler L. Safety of anti-TNF-α therapy in rheumatoid arthritis and spondylarthropathies with concurrent B or C chronic hepatitis. Rheumatology 2006; doi: 10.1093/rheumatology/kel123.
12. Zein NN. Etanercept as an adjuvant to interferon and ribavirin in treatment-naive patients with chronic hepatitis C virus infection: a phase 2 randomized, double blind, placebo-controlled study. J Hepatol 2005; 42 : 315–22.
13. Husa P, Plíšek S, Šperl J, Urbánek P, Galský J, Hůlek P, Kumpel P, Němeček V, Volfová M. Diagnostika a léčba chronické hepatitidy B. Doporučený postup ČHS a SIL ČSL JEP. Klin mikrobiol inf lék 2005; 11 : 138–143.
14. Pernillo RP. Acute flares in chronic hepatitis B: the natural and unnatural history of an immunologically mediated liver disease. Gastroenterology 2001; 120 : 1009–22.
15. Cheng AL, Hsiung CA, SU U, Chen PJ, Chang MC, Tsao CJ, et al. Steroid-free chemotherapy decreases risk of hepatitis B virus reactivation in HBV-carriers with lymphoma. Hepatology 2003; 37 : 1320–8.
16. Ostuni P, Botsios C, Punzi L, Sfriso P, Todesco S. Hepatitis B reactivation in a chronic hepatitis B surface antigen carrier with rheumatoid arthritis treated with infliximab and low dose methotrexat. Ann Rheum Dis 2003; 62 : 686–7.
17. Michel M, Duvoux C, Hezode C, Cherqui D. Fulminant hepatitis after infliximab in a patient with hepatitis B virus treated for an adult onset still’s disease. J Rheumatol 2003; 30 : 1624–5.
18. Esteve M, Saro C, Gonzalez-Huix F, Suarez F, Forne M, Viver JM. Chronic hepatitis B reactivation following infliximab therapy in Crohn’s disease patients: need for primary prophylaxis. Gut 2004; 53 : 1363–5.
19. Wendling D, Auge B, Bettinger D, et al. Reactivation of a latent precore mutant hepatitis B virus related chronic hepatitis during infliximab treatment for severe spondylartropathy. Ann Rheum Dis 2005; 64 : 788–9.
20. Millonig G, Kern M, Ludwiczek O, Nachbaur K, Vogel W. Subfulminant hepatitis B after infliximab in Crohn’s disease: Need for HBV-screening? World J Gastroenterol 2006; 12 : 974–6.
21. Flowers MA, Heathcote J, Wanless IR, Sherman M, Reynolds WJ, Cameron RG, et al. Fulminant hepatitis as a consequence of reactivation of hepatitis B virus infection after discontinuation of low-dose methotrexate therapy. Ann Intern Med 1990; 112 : 381–2.
22. Hagiyama H, Kubota T, Komano Y, Kurosaki M, Watanabe M, Miyasaka N. Fulminant hepatitis in an asymptomatic chronic carrier of hepatitis B virus mutant after withdrawal of low-dose methotrexate therapy for rheumatoid arthritis. Clin Exp Rheumatol 2004; 22 : 375–6.
23. Silvestri F, Ermacora A, Sperotto A, Patriarca F, Zaja F, Damiani D, et al. Lamivudine allows completion of chemoterapy in lymphoma patients with hepatis B reactivation. Br J Haematol 2000; 108 : 394–6.
24. Rossi G. Prophylaxis with lamivudine of hepatitis B virus reactivation in chronic HBsAg carriers with hemato-oncological neoplasis treated with chemotherapy. Leuk Lymphoma 2003; 44 : 759–66.
Labels
Dermatology & STDs Paediatric rheumatology Rheumatology
Article was published inCzech Rheumatology

2007 Issue 2-
All articles in this issue
- Stanovení pentosidinu v moči a tkáních kloubního kompartmentu pacientů s pokročilou osteoartrózou
- Výskyt echokardiograficky detekovatelných kardiovaskulárních manifestací systémového lupus erythematodes
- Doporučení České revmatologické společnosti pro léčbu revmatoidní artritidy. Účinnost a strategie léčby
- Monitorování léčby osteoporózy
- Zobrazovací metody v hodnocení strukturální progrese u ankylozující spondylitidy
- Bezpečnost podání anti-TNF alfa léčby u revmatických pacientů s chronickou hepatitidou B nebo C
- Osteonekróza asociovaná se systémovou kortikoterapií
- Trombotická trombocytopenická purpura u nemocných se systémovým lupus erythematodes
- Czech Rheumatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Osteonekróza asociovaná se systémovou kortikoterapií
- Trombotická trombocytopenická purpura u nemocných se systémovým lupus erythematodes
- Doporučení České revmatologické společnosti pro léčbu revmatoidní artritidy. Účinnost a strategie léčby
- Zobrazovací metody v hodnocení strukturální progrese u ankylozující spondylitidy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career