-
Medical journals
- Career
Retroperitoneálna lymfangioleiomyomatóza – kazuistiky
Authors: E. Lajtman 1; Miloš Mlynček 1; M. Matejka 1; A. Sládeček 2; I. Langová 2
Authors‘ workplace: Gynekologicko-pôrodnícka klinika FN a Univerzita Konštantína Filozofa, Nitra, prednosta prof. MUDr. M. Mlynček, CSc. 1; Ústav patológie FN, Nitra, primár MUDr. A. Sládeček 2
Published in: Ceska Gynekol 2013; 78(2): 206-210
Overview
Lymfangioleiomyomatóza (LAM) je zriedkavé ochorenie vyskytujúce sa u žien v reprodukčnom veku. LAM je charakterizovaná abnormálnou proliferáciou nezrelých buniek hladkého svalu. Progresívne ochorenie postihuje najmä pľúcny parenchým a môže mať až fatálny koniec. Mimopľúcna forma LAM sa najčastejšie prejavuje bolesťou brucha, nádormi v retroperitoneu a chylóznym ascitom. V kazuistikách opisujeme výskyt dvoch prípadov mimopľúcnej formy LAM. V obidvoch prípadoch išlo o pelvickú lokalizáciu nádorov v oblasti fossa obturatoria a vasa iliaca externa. Pacientky boli po operácii primárne liečené gestagénmi. Sirolimus bol liekom druhej línie.
Klíčová slova:
lymfangioleiomyomatóza – chylózny ascites – sirolimusÚVOD
Lymfangioleiomyomatóza (LAM) postihuje ženy najčastejšie v reprodukčnom veku. Ochorenie je typické proliferáciou nezrelých a atypických buniek hladkého svalu najmä v pľúcach [14]. Ide o nádory z perivaskulárnych epiteloidných buniek, tzv. PECómy (perivascular epitheloid cell), ktoré sa vyznačujú zároveň hladkosvalovou i melanocytárnou diferenciáciou [3]. Do tejto skupiny patrí angiomyolipóm (AML), svetlobunkový tumor pľúc („sugar“ tumor), svetlobunkový myomelanocytový nádor ligamentum falciforme a teres hepatis a lymfangioleiomyomatóza [8]. LAM prvýkrát opísali Cornog a Enterline v roku 1966 [4]. Väčšina pacientok má pľúcne príznaky (dyspnoe, hemoptýza, pneumotorax), ale u niektorých sa ochorenie prejavuje spočiatku mimopľúcnymi príznakmi (bolesť brucha, nádory v dutine brušnej a chylózny ascites) [10]. Incidencia LAM je 1–2,6 prípadov na 1 milión žien [18]. Priemerný vek žien v čase stanovenia diagnózy je 41 rokov a celosvetová incidencia je 100 nových prípadov ročne [8]. LAM sa vyskytuje ako samostatné ochorenie alebo v spojení s tuberóznou sklerózou (TSC). V tomto prípade ide o autozomálne dominantne dedičné ochorenie charakterizované epileptickými záchvatmi, mentálnou retardáciou a tumormi mozgu, srdca, kože, kostí, pľúc a obličiek [7]. Ani transplantácia pľúc ako posledná možnosť liečby pre pacientov s respiračnou insuficienciou nerieši pretrvávajúci problém s tvorbou chylózneho ascitu alebo pleurálnej efúzie [19]. Chylózna efúzia sa vyskytuje v 10 až 25 % prípadov LAM [19].
KAZUISTIKA 1
Na Gynekologicko-pôrodnícku kliniku FN Nitra bola 18. 8. 2009 prijatá 43-ročná pacientka s tumorom v malej panve. Počas gynekologického vyšetrenia pomocou sonografie sme zistili solídne nádory v mieste vaječníkov veľkosti 5, resp. 6 cm a ascites s vertikálnym stĺpcom tekutiny 8 cm. Gynekologická anamnéza bola bez pozoruhodností, v anamnéze 2 spontánne pôrody. Hladina CA125 bola 647 IU/ml, ostatné laboratórne parametre v norme. Pri laparotómii sa verifikoval chylózny ascites (peroperačne odsaté 1,5 l tekutiny), parailiakálne a paraaortálne vľavo boli zväčšené lymfatické uzliny (dve uzliny veľkosti 5 a 6 cm). Maternica bola zväčšená a deformovaná myomatóznymi uzlami. Na obidvoch vaječníkoch boli prítomné cysty veľkosti 3, resp. 4 cm. Vykonali sme odstránenie zväčšených lymfatických uzlín v okolí vasa iliaca externa vľavo, intrafasciálnu hysterektómiu spolu s obojstrannou adnexektómiou. Lymfatické uzliny neboli peroperačne vyšetrované. Indikáciou k hysterektómii s adnexektómiou bol uterus myomatosus a cysty na obidvoch vaječníkoch. Peroperačným histopatologickým vyšetrením vaječníkov neboli zistené malígne zmeny. Vo všetkých histopatologických rezoch lymfatických uzlín boli zistené fascikulárne usporiadané bunkové elementy s nízkym stupňom proliferácie (obr. 1). Bunková populácia imunohistochemicky exprimovala melanocytárny marker HMB-45 (human melanoma black-45), SMA (alpha-smooth muscle actin), vimentín, dezmín a S 100 proteín. Potvrdená pozitivita na HMB-45 je v prípade LAM kľúčová (obr. 2). Zároveň sa zistila 85% až 90% pozitivita na estrogénové a progesterónové receptory. Uvedený mikroskopický a imunohistochemický obraz je typický pre LAM. Histologické vyšetrenie maternice a vaječníkov dokázalo 4 leiomyómy v stene maternice a folikulárne cysty na obidvoch vaječníkoch. Pacientka následne 2 roky užívala megestrol acetát (Megace) v dávke 3×160 mg denne. Priebežne sa podrobovala paracentéze ascitu v 5 až 6 mesačných intervaloch. V roku 2011 bola hospitalizovaná pre kardiálnu dekompenzáciu a výraznú tvorbu chylózneho ascitu. Vzhľadom k jeho excesívnej produkcii bola zavedená trvalá drenáž dutiny brušnej. V súčasnosti je produkcia chylóznej tekutiny asi 4 litre za 24 hodín. Pacientka 5. mesiac užíva kombináciu sirolimus (Rapamun) 1 mg denne a hydrochlorochínsulfát (Plaquenil) 400 mg denne. Ide o izolovanú abdominálnu formu LAM, bez postihnutia iných orgánov, čo bolo preukázané ďalšími vyšetreniami (USG a CT vyšetrenie hrudníka a dutiny brušnej).
Image 1. Mikroskopické vyšetrenie lymfatickej uzliny s charakteristickou abnormálnou proliferáciou nezrelých buniek hladkého svalu (hematoxilín-eozín, zväčšené 200×). 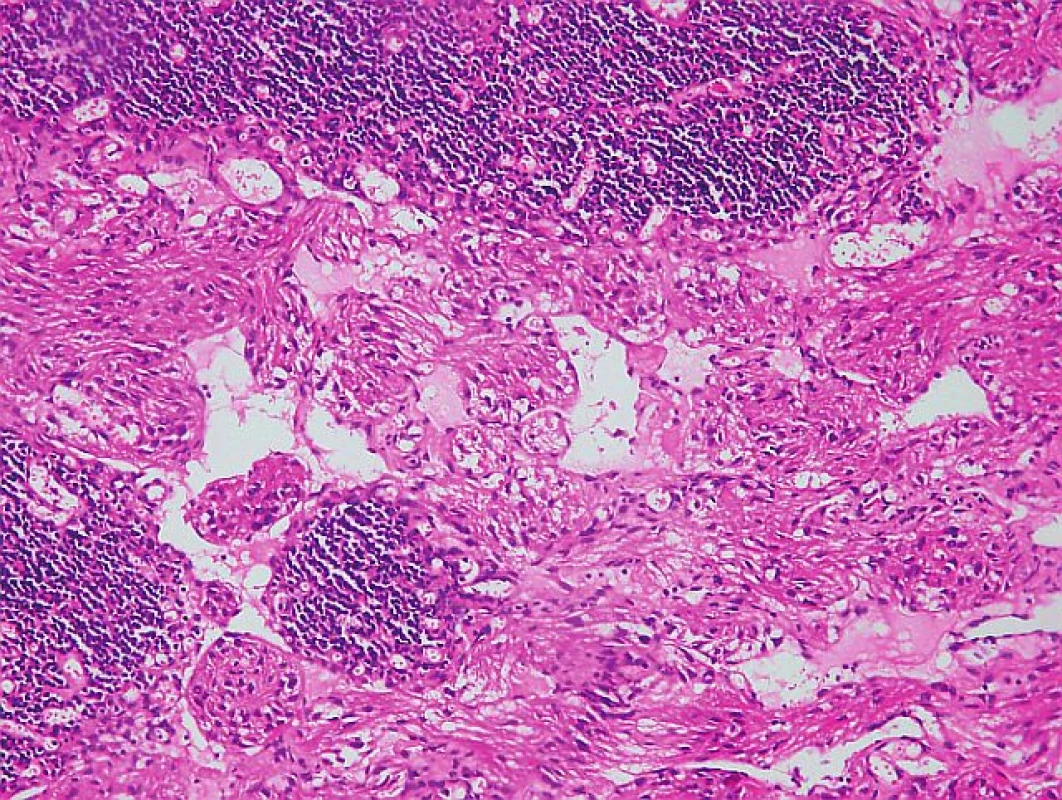
Image 2. Mikroskopické vyšetrenie nádorových buniek s pozitivitou na HMB-45 (human melanoma black-45, zväčšené 200×). 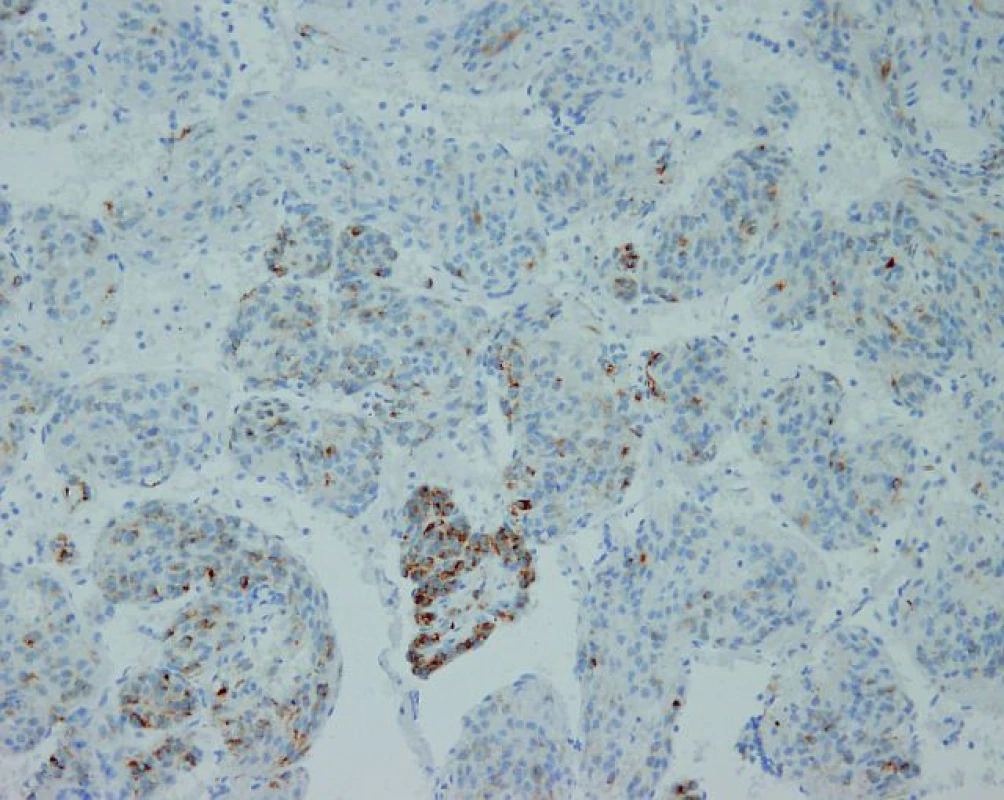
KAZUISTIKA 2
Pacientka vo veku 41 rokov bola prijatá 1. 1. 2012 na Gynekologicko-pôrodnícku kliniku FN Nitra na plánovanú operačnú liečbu pre početné tumory v malej panve nejasnej etiológie. Predoperačne bolo vykonané ultrazvukové vyšetrenie malej panvy s nálezom solídneho nádoru v oblasti pravých adnex veľkosti 6×8 cm. Nález na maternici a ľavých adnexách bol normálny. Pri laparotómii sme odstránili 3 uzliny veľkosti 4 až 5 cm z fossa obturatoria vpravo. Nález na vnútornom genitáli bol normálny. Zväčšené lymfatické uzliny imitovali adnexálny nádor. Spracovaná vzorka lymfatickej uzliny, histologická skladba ako aj imunohistochemické vyšetrenia zodpovedali morfologickej entite LAM. Z osobnej anamnézy je pozoruhodné, že ide o pacientku dlhodobo sledovanú na dermatologickej ambulancii pre Bournevilleho-Pringleho syndróm (tuberózna skleróza). Pacientka v minulosti opakovane podstúpila operácie kožných tumorov v kapilíciu ako aj dermabráziu tváre. Rovnaké ochorenie bolo zistené aj u dcéry. V pooperačnom období bolo vykonané CT vyšetrenie hrudníka s negatívnym nálezom. Iniciálne bol pacientke nasadený megestrol acetát (Megace) v dávke 3×160 mg denne. Napriek tomu došlo k zhoršeniu zdravotného stavu, objavili sa bolesti brucha s akcelerovanou tvorbou chylózneho ascitu. S odstupom 4 mesiacov od operačného výkonu CT vyšetrenie dutiny brušnej ukázalo v retroperitoneu dobre ohraničený nádor veľkosti 10×6 cm nasadajúci na ľavú obličku (obr. 3). Rádiologicky bol obraz lézie konzistentný s diagnózou LAM. Nakoľko tumor ultáčal ľavý ureter, bola zavedená prechodná endodrenáž ureteru. Následná spontánna dislokácia drénu po 2 týždňoch bola bez klinickej odozvy. Šesť mesiacov po operácii bol CT vyšetrením zistený fluidothorax a biopsia potvrdila pľúcnu formu LAM. Vzhľadom na rýchlo progredujúci stav ochorenia bola u pacientky indikovaná liečba sirolimom.
Image 3. CT zobrazenie nádoru v retroperitoneu 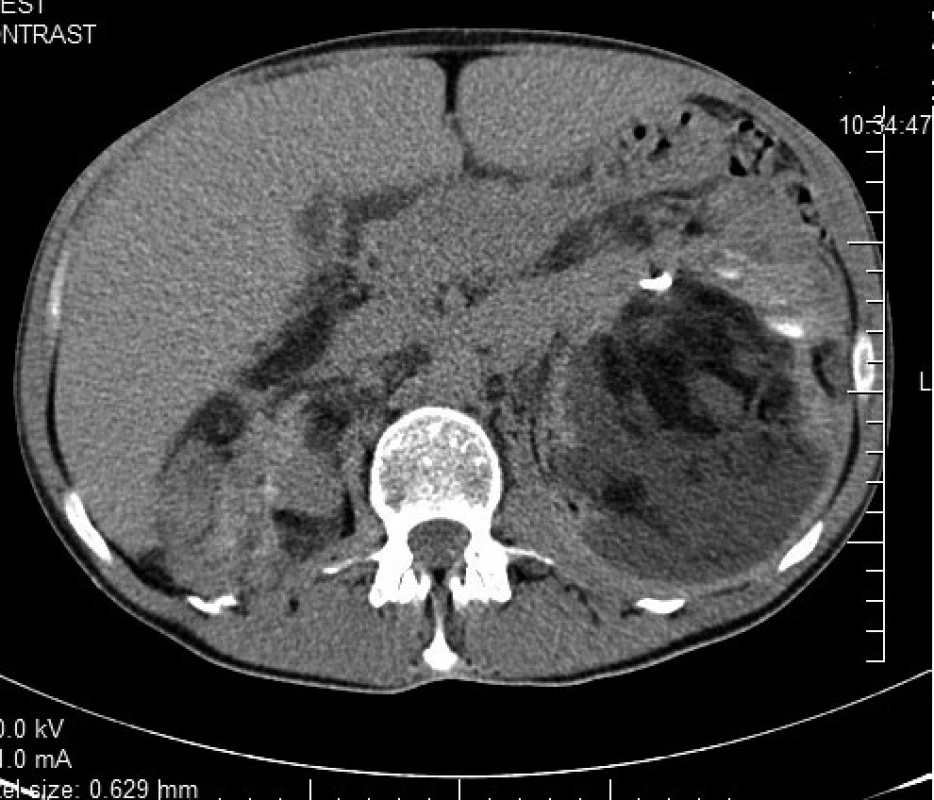
DISKUSIA
LAM je raritné ochorenie a izolovaná mimopľúcna forma je extrémne zriedkavá. Matsui a spol. uvádzajú, že v súbore 188 pacientok len 3 (2 %) mali izolovanú extrapulmonálnu formu [10]. LAM spravidla vzniká v reprodukčnom veku, hoci sú známe prípady aj u postmenopauzálnych žien užívajúcich hormonálnu substitučnú liečbu. Úloha estrogénových a progesterónových receptorov v patogenéze ochorenia nie je jasná. Ich pozitivita dáva predpoklad, že hormonálna liečba môže byť úspešná [8].
Patogenéza ochorenia nie je jasná. V prípade, ak LAM prebieha v spojení s tuberóznou sklerózou, ide o genetickú mutáciu lokalizovanú na choromozómoch 9q34 (TSC1 gén) a 16p13 (TSC2 gén). Tieto supresorové gény sú zodpovedné za kódovanie hamartínu (TSC1) a tuberínu (TSC2). Nedostatok týchto dvoch proteínov spôsobuje aktiváciu mTOR (mammalian target of rapamycín). Následkom procesu je zvýšenie proliferácie cieľových buniek hladkého svalu, ktoré pritom zároveň získavajú aj rysy melanocytu [17].
Úloha enviromentálnych faktorov v patogenéze LAM doteraz nebola objasnená, hoci ide o diskutovaný problém [10, 14].
Diagnostika LAM nie je jednoduchá. Ochorenie najčastejšie imituje karcinóm ovária, endometria alebo lymfóm, prípadne sarkóm, resp. leiomyosarkóm. Stanovenie diagnózy v prípade izolovanej mimopľúcnej formy je náročné. Matsui a spol. uvádzajú 12% výskyt chylózneho ascitu [10]. V prípadoch manifestujúcej sa kožnej formy TSC je vhodné myslieť aj na možný výskyt LAM. Definitívne potvrdenie je založené na histologickom a imunohistochemickom dôkaze hladkosvalového fenotypu s expresiou melanocytárnych markerov [3, 8]. Všetky ostatné laboratórne vyšetrenia (krvný obraz, biochemické vyšetrenie séra, analýza moču) vykazujú normálne hodnoty [2]. Pre pľúcnu formu je typický CT obraz [12].
Liečba LAM prešla v ostatných dekádach vývojom. Postupne boli v terapii využívané metódy rádioterapie, kortikosteroidy a chemoterapia. Všetky spomenuté modality priniesli len malý benefit [9]. Hormonálna liečba progesterónom, ooforektómiou, tamoxifénom alebo GnRH analógmi má diskutabilný efekt [9]. Eliasson a spol. referujú o 50% úspešnosti (stabilizácii) s použitím gestagénov [5].
Sirolimus (Rapamun) je imunosupresívum s potenciálom významne zlepšiť prognózu pacientok s LAM. Aj napriek tejto skutočnosti, ide o „off-label“ liečbu, pretože jedinou indikáciou jeho použitia je stav po transplantácii obličky [13]. Ide o inhibítor mTOR, ktorého efekt bol overený v štúdii MILES [11]. Sirolimus stabilizuje pľúcne funkcie, zlepšuje symptómy a kvalitu života. V jednej zo štúdií vplyvom sirolimu došlo k výraznej redukcii chylózneho ascitu a/alebo k redukcii nádorov [16]. Použitie lieku je rezervované pre pacientky, u ktorých nemala progesterónová liečba benefit a ktoré spĺňajú nasledujúce podmienky: rýchla progresia pľúcneho postihnutia, vrátane chylóznej efúzie, potreba drenáže chylotoraxu alebo pleurodézy a v prípadoch významnej symptomatológie abdominálnej alebo pľúcnej formy [17]. Sirolimus sa iniciálne podáva v dávke 2 mg/deň, pričom je potrebné sledovať jeho hladinu v sére, ktorá má byť v rozmedzí 5–15 ng/ml [17]. Neskôr je možná redukcia na 1 mg/deň. Výskyt vedľajších účinkov môže byť limitujúcim, najmä ak sa vyskytuje hypertenzia, hyperlipidémia, ulcerácie v dutine ústnej, recidivujúce infekcie, elevácia hladiny kreatinínu alebo intersticiálna pneumónia. Antimalarikum a antireumatikum hydrochlorochínsulfát (Plaquenil) má podobné účinky ako sirolimus, a to najmä vtedy, keď sú užívané súčasne. Opäť sa jedná o liek v indikácii „off-label“. Aktuálne sa začína prvá fáza intervenčnej štúdie, ktorá má overiť bezpečnosť užívania kombinácie sirolimu a hydrochlorochínu u žien s LAM [6].
Vzhľadom k tomu, že LAM je raritné ochorenie imitujúce gynekologickú malignitu, môže dôjsť k oddialeniu stanovenia diagnózy, zbytočne rozsiahlej operačnej intervencii či k nevhodnej liečbe. U prvej pacientky sme indikovali laparotómiu pre podozrenie na tumor ovária. V druhom prípade sme suponovali na LAM už pred operačným výkonom (tuberózna skleróza a lymfadenopatia v panve). Je namieste otázka väčšieho benefitu laparoskopického prístupu namiesto laparotomického. Pacientky s mimopľúcnou formou LAM zvyčajne podstúpia operačnú liečbu pre nádor v dutine brušnej. Peroperačné histologické vyšetrenie a definitívne overenie erudovaným patológom určí správnu diagnózu. Hysterektómia spolu s adnexektómiou nemá liečebný účinok. Úlohou operačného výkonu je histologické vyšetrenie cystických útvarov a potvrdenie diagnózy. Významným problémom je pretrvávajúca tvorba chylózneho ascitu a následná potreba drenáže dutiny brušnej. Obštrukcia lymfatických ciev môže viesť k úniku lymfy do brušnej alebo hrudnej dutiny. Následkom toho vzniká hypoproteinémia, lymfopénia, hypokalcémia, hyponatriémia, metabolická acidóza, hypovitaminóza A, D, E, K a imunodeficientný stav (hypoimunoglubilinémia a deficit T-lymfocytov). Liečba spočíva v diétnych opatreniach, pričom je indikovaná beztuková alebo nízkotuková diéta a triglyceridy so stredne dlhým reťazcom (MCT). Totálna parenterálna výživa niekedy zastaví tvorbu chylózneho ascitu [1]. Pokiaľ nie sú tieto opatrenia adekvátne, efektívna môže byť medikamentózna alebo chirurgická liečba. Používa sa aj oktreotid, etiliefrin, faktor XIII, prípadne skleroterapia alebo rádioterapia [1].
Progredujúci charakter ochorenia a nevyhnutnosť trvalej drenáže významne zhoršuje kvalitu života pacientok. Prognóza pacientok nie je priaznivá, dĺžka prežitia bola v minulosti maximálne 10 rokov od stanovenia diagnózy [15]. V súčasnosti s využitím všetkých dostupných liečebných modalít, vrátane transplantácie pľúc, 78 % pacientok prežíva 8,5 roka [14]. Pokiaľ sa extrapulmonálna forma manifestuje ako prvá, predchádza pľúcnemu postihnutiu zvyčajne 1–2 roky [10]. Toto sme pozorovali u nášho druhého prípadu, keď sa u pacientky zistila pľúcna forma 6 mesiacov po diagnóze extrapulmonálnej LAM. V tejto súvislosti treba zdôrazniť potrebu „follow-up“ u pacientok s LAM.
Žurková a spol. navrhujú u pacientok s LAM vždy vylúčiť prítomnosť tuberóznej sklerózy (oftalmologické, kožné a neurologické vyšetrenie). Pacientky s LAM a bilaterálnymi angiolipómami, rovnako ako aj pacientky s podozrením na TSC je potrebné odoslať na genetické vyšetrenie. Rutinné genetické vyšetrenie u pacientok so sporadickou formou LAM nie je indikované [20].
V liečebnej schéme sa v prvom rade využíva efekt gestagénov, ktorú považujeme za liečbu prvej línie. V obidvoch prípadoch sme liečbu gestagénmi aplikovali ako primárnu. Podanie sirolimu je v našich podmienkach limitované osobitným schválením a obyčajne je v kompetencii onkologického pracoviska. Sirolimus nemá byť rutinne predpisovaný mimo klinických štúdií. Liečba je indikovaná v prípadoch rýchlej progresie ochorenia u pacientok liečených gestagénmi alebo po vyčerpaní dostupných liečebných možností [12]. Vytvorenie centrálneho registra na európskej a celosvetovej úrovni môže priniesť benefit v diagnostike, liečbe a hlavne v prognóze pacientok s LAM.
MUDr. Erik Lajtman, PhD.
Gynekologicko-pôrodnícka klinika
FN a UKF Nitra
Špitálska 6
949 01 Nitra
Slovenská republika
e-mail: lajtmanerik@gmail.com
Sources
1. Blei, F. Medical Management. In Lee, B.-B., Bergan, J., Rockson, SG. Lymphedema. London: Springer-Verlag, 2011, p. 449–453.
2. Bonetti, F., Chiodera, P., Pea, M., et al. Transbronchial biopsy in lymphangioleiomyomatosis of the lung: HMB 45 for diagnosis. Am J Surg Pathol, 1993, 17, p. 1092–1102.
3. Bonetti, F., Pea, M., Martignoni, G., et al. Clear cell (Sugar) tumor of the lung is a lesion strictly related to angiomyolipoma: the concept of a family of lesion characterized by the presence of the perivascular epithelioid cells (PEC). Pathology, 1994, 26, p. 230–236.
4. Cornog, JL., Enterline, HT. Lymphangiomyoma, a benign lesion of chyliferous lymphatic synonymous with lymphangiopericytoma. Cancer, 1966, 19, p. 1909–1930.
5. Eliasson, AH., Phillips, YY., Tenholder, MF. Treatment of lymhangioleiomyomatosis. A meta-analysis. Chest, 1989, 96, p. 1352–1355.
6. Henske, E. Safety study of sirolimus and hydrochloroquine in women with lymphangioleiomyomatosis [on line]. [cit. 2012-10-01].Dostupný na WWW: http://clinicaltrialsfeeds.org/clinical-trials/show/NCT01687179>
7. Hohman, DW., Noghrehkar, D., Ratnayake, S. Lymphagio-leiomyomatosis: a review. Eur J Intern Med, 2008, 19, p. 319–324.
8. Kebria, M., Black, D., Bonelli, C., et al. Primary retroperitoneal lymphangioleiomyomatosis in a postmenopausal woman: a case report and review of the literature. Int J Gynecol Cancer, 2007, 2007, 17, p. 528–532.
9. Kelly, J., Moss, J. Lymphangioleiomyomatosis. Am J Med Sci, 2001, 321, p. 17–25.
10. Matsui, K., Tatsuguchi, A., Valencia, J., et al. Expora-pulmonary lymphangioleiomyomatosis (LAM): clinicopathologic features in 22 cases. Hum Pathol, 2000, 31, p. 1242–1248.
11. McCormack, FX., Yoshikazu, Y., Moss, J., et al. Multicenter international lymphangioleiomyomatosis efficaccy and safety of sirolimus (MILES) trial. N Engl J Med, 2011, 364, p. 1595–1606.
12. Nebeský, T., Pokojová, E., Dvořák, K. Lymfangioleio-myomatóza. Čes Radiol, 2004, 58, 1, s. 27–29.
13. Rapamune. SPC [on line]. [cit. 2012-10-01]. Dostupný na WWW:http://sukl.sk/buxus/generate_page.php?page_id=368&lie_id=34341
14. Sullivan, EJ. Lymphangioleiomyomatosis: a review. Chest, 2006, 114, 6, p 1689–1703.
15. Svendsen, TL., Viskum, K., Hansborg, N., et al. Pulmonary lymphagioleiomyomatosis: a case of progesterone receptor positive lymphangioleiomyomatosis treated with medroxyprogesterone, oophorectomy and tamoxifen. Br J Dis Chest, 1984, 78, p. 264–271.
16. Taviera-DaSilva, AM., Hathaway, O., Stylianou, M.,Moss, J. Changer in lung funkction and chylous effusion in patients with lymphangioleiomyomatosis treated with sirolimus. Ann Intern Med, 2011, 154, p. 797–805.
17. Taviera-DaSilva, AM., Moss, J. Progress in the treatment of lymfangioleiomyomatosis: From bench to bedside. Rev Port Pneumol, 2012, 18, p. 142–144.
18. Taviera-DaSilva, AM., Steagall, W., Moss, J. Lymphangio-leiomyomatosis. Cancer, Control, 2006, 13, 4, p 276–285.
19. Toshiaki, O., Takhiro, O., Kentaro, M., et al. Sirolimus ameliorated post lung transplant chylothorax in lymphangioleiomyomatosis. Ann Thorac Surg, 2008, 86, p. e7–e8.
20. Žurková, M., Kolek, V., Vašáková, M., Loštáková, V. Lymfangioleiomyomatóza – standard diagnózy, léčby a sledování [on line]. [cit. 2012-09-28]. Dostupný na WWW: http://pneumologie.cz/odborne/doporučenie-postupy.php
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inCzech Gynaecology

2013 Issue 2-
All articles in this issue
- Selektivní modulátory progesteronového receptoru a jejich terapeutické využití
- L-arginin v prevenci a léčbě preeklampsie
- Systémová enzymoterapie v léčbě recidivující vulvovaginální kandidózy
- Význam stanovení proteinu p16 v managementu prekanceróz děložního hrdla
- Opakované potrácení – přehledový článek
- Doporučení k provádění prevence RhD aloimunizace u RhD negativních žen
- Těhotenství a roztroušená skleróza – analýza výsledků z let 2003–2011
- Hyperlipidémie v těhotenství
-
Psychosociální klima porodnice očima rodiček I.
Výsledky celorepublikového průzkumu spokojenosti s perinatální péčí v ČR u reprezentativního souboru 1195 rodiček -
Kmenové buňky a karcinom ovaria
Charakteristika, význam a potenciální aplikacev klinické praxi - Retroperitoneálna lymfangioleiomyomatóza – kazuistiky
- Transfusion-related acute lung injury (TRALI) – přehledový článek
- Blokáda vápníkových kanálů – perspektiva mužské antikoncepce?
- Atlas gamét a embryí niektorých živočichov a človeka
- Czech Gynaecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Transfusion-related acute lung injury (TRALI) – přehledový článek
- Opakované potrácení – přehledový článek
- Význam stanovení proteinu p16 v managementu prekanceróz děložního hrdla
- Hyperlipidémie v těhotenství
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

