-
Medical journals
- Career
SROVNÁNÍ ANTIMIKROBIÁLNÍCH VLASTNOSTÍ NOVÝCH PRYSKYŘICÍ MODIFIKOVANÝCH MATERIÁLŮ POUŽÍVANÝCH PŘI VÝKONECH SE ZACHOVÁNÍM VITALITY ZUBNÍ DŘENĚ: IN VITRO STUDIE
Authors: B. Novotná 1,2,*; P. Holík 1,2; Y. Morozova 1,2; L. Somolová 1,2; M. Rosa 1,2; L. Svobodová 3,4
Authors‘ workplace: Korespondující autorka *; Klinika zubního lékařství, Lékařská fakulta Univerzity Palackého v Olomouci 1; Klinika zubního lékařství, Fakultní nemocnice Olomouc 2; Ústav mikrobiologie, Lékařská fakulta Univerzity Palackého v Olomouci 3; Ústav mikrobiologie, Fakultní nemocnice Olomouc 4
Published in: Česká stomatologie / Praktické zubní lékařství, ročník 126, 2026, 1, s. 5-15
Category: Original articles
doi: https://doi.org/10.51479/cspzl.2025.009Overview
Úvod a cíl: V případě sanace hlubokých kariézních lézí je stále více preferována metoda selektivní exkavace, u které však lze předpokládat perzistenci malého množství mikroorganismů v oblasti změklého dentinu v blízkosti zubní dřeně. Z tohoto důvodu je žádoucí, aby výplňový materiál měl mimo jiné také antimikrobiální schopnosti. Předmětem této in vitro studie je zhodnocení antimikrobiálního efektu zvolených pryskyřicí modifikovaných kalciumsilikátových (TheraCal LC, TheraCal PT) a kalciumfosfátových cementů (ApaCal ART) a jejich srovnání s referenčním materiálem (Biodentine).
Metodika: Pro tuto in vitro studii byly zvoleny čtyři zkoumané skupiny mikroorganismů: 1. viridující streptokoky, 2. rod Lactobacillus, 3. Enterococcus faecalis a 4. Candida albicans. Pomocí difuzního agarového testu byly změřením šíře inhibiční zóny růstu zhodnoceny antimikrobiální účinky zkoumaných materiálů. Následně bylo provedeno statistické zpracování získaných dat, všechny testy byly provedeny na hladině významnosti 0,05.
Výsledky: Bylo ověřeno, že Biodentine má antimikrobiální účinek vůči všem zvoleným mikroorganismům. ApaCal ART vykazoval pouze nízkou aktivitu vůči skupině viridujících streptokoků, TheraCal PT měl obdobný účinek, nicméně inhiboval růst i v případě skupiny Lactobacillus. TheraCal LC měl antimikrobiální schopnost vůči všem zkoumaným mikroorganismům, v případě skupin Enterococcus, Candida a Lactobacillus se výsledky statisticky významně nelišily od referenčního materiálu.
Závěr: Pryskyřicí modifikované kalciumsilikátové nebo kalciumfosfátové materiály mají všeobecně menší antimikrobiální potenciál než klasické kalciumsilikátové cementy. Nicméně je důležité si uvědomit, že jejich aktivita se u různých výrobků liší. Ze zvolených materiálů v této in vitro studii dosahoval TheraCal LC nejlepších výsledků, podobných jako referenční cement.
Klíčová slova:
kaz blízký dřeni – nepřímé překrytí zubní dřeně – kalciumsilikátový cement – kalciumfosfátový cement
ÚVOD A CÍLE
V soudobém zubním lékařství je při ošetření stálých zubů kladen důraz především na zachování vitality zubní dřeně, a proto pro ošetření hlubokých kariézních lézí rozlišujeme několik různých způsobů exkavace, které tento výsledek mohou ovlivnit. Typy exkavace můžeme rozdělit na dvě hlavní skupiny: neselektivní exkavaci a selektivní exkavaci. Neselektivní exkavace (dříve kompletní nebo totální exkavace [1]) znamená odstranění veškerého měkkého kariézního dentinu z periferní i centrální části kavity až do dosažení tvrdého zdravého dentinu. Tvrdý dentin (angl. hard dentine) je typický odolností a skřípáním při použití ostrého exkavátoru nebo sondy [2] a nebarví se detekčním barvivem [3]. V posledních letech jsou tendence od tohoto typu exkavace v případě hlubokých kariézních lézí spíše ustupovat z důvodu vysokého rizika otevření dřeňové dutiny a expozice zubní dřeně [1, 2, 4]. Selektivní exkavace (dříve částečná, nekompletní exkavace [1]) znamená odstranění kariézního dentinu na periferii kavity až po tvrdý zdravý dentin, v centrální části kavity je ponechána tenká vrstva měkkého nebo pevného dentinu. Měkký infikovaný dentin (angl. soft dentine) je možné velmi snadno odstranit použitím rotačních nebo ručních nástrojů bez vynaložení většího úsilí. Pevný neboli kožovitý dentin (angl. firm, leathery dentine) je demineralizovaná, již však minimálně infikovaná tkáň, kterou lze odstranit s větší silou ostrým exkavátorem [2]. Obě tyto tkáně (měkký i pevný dentin) se barví detekčním barvivem [3]. V současnosti je rostoucím trendem tento typ exkavace u hlubokých kariézních lézí stále více doporučovat, ať už jako definitivní jednodobé ošetření, nebo v rámci dvoudobého ošetření (sekvenční exkavace, angl, stepwise excavation, intermittent excavation). Akcentace na tento typ exkavace v odborné literatuře roste, především z důvodu menšího rizika expozice a dráždění zubní dřeně při preparaci [2], a také proto, že je v tomto případě zachováno větší množství tvrdých zubních tkání [4]. Jedním z úskalí selektivní exkavace je nemožnost standardizace stupně exkavace. Plocha změklého dentinu by sice měla být co nejmenší, záleží však na zkušenostech a preferencích daného lékaře, navíc samotný ošetřující může v různých případech při stejném typu exkavace odstranit více, nebo méně kariézních tkání. Proto je velmi obtížné určit ideální množství změklého dentinu, které je možné v kavitě ponechat [3, 4]. Dalším úskalím je nemožnost zjištění dg. chronické ireverzibilní pulpitidy a z toho plynoucí nesprávná indikace zhotovení výplně/provedení nepřímého překrytí zubní dřeně v situaci, která vyžaduje radikálnější způsob ošetření [3]. V případě hlubokých kazů totiž studie prokázaly přítomnost bakterií v dentinových tubulech cirkumpulpálně jak před ošetřením, tak v mnohých případech i po provedení selektivní exkavace [5, 6]. Za předpokladu, že malé množství mikroorganismů v tkáních zůstává, je pro zastavení kariézního procesu nezbytné zamezit jim přístup k živinám, omezit prostor pro jejich množení a tvorbu toxinů. Toho je možné docílit hermetickým uzavřením kavity pomocí vhodného prostředku, který je využitý jako fyzikální bariéra mezi zubní dření a ústní dutinou. Tento materiál by měl mít adhezi k dentinu a případným jiným výplňový materiálům [7]. Kompozitní materiály jsou ideální volbou pro dokonalý hermetický uzávěr kavity [3]. Avšak vzhledem k blízkosti zubní dřeně je také vhodné zvážit použití materiálu, který by byl pro buňky zubní dřeně biokompatibilní a co nejméně cytotoxický, stimuloval by tvorbu terciárního dentinu, měl by remineralizační potenciál (uvolňování fluoridových nebo vápenatých iontů) a dostatečnou mechanickou a chemickou odolnost. V neposlední řadě, vzhledem k přítomnosti a přežívání bakterií v dentinových tubulech, jsou velmi žádoucí antimikrobiální vlastnosti [8, 9]. Pro dlouhodobou kontrolu je vhodná také rentgenkontrastnost vyšší než u dentinu pro možnost hodnocení tvorby dentinového můstku.
Většinu z těchto požadovaných vlastností splňuje skupina kalciumsilikátových cementů, které jsou v této indikaci také v dnešní době doporučovány [1, 2]. Tyto materiály jsou na dentálním trhu od 90. let 20. století [10] a jejich vlastnosti již byly důkladně prozkoumány [11]. Ačkoliv se jedná o prostředky s velmi dobrými vlastnostmi, jejich použití někdy skýtá i určité nevýhody, mezi které je možné řadit obtížnou manipulaci, délku tuhnutí nebo tendenci k dyskoloracím. Snahou výrobců bylo tato negativa odstranit nebo alespoň zmírnit, a proto v průběhu času vzniklo mnoho různých variant kalciumsilikátů, které mají obdobné složení a vlastnosti, ale snaží se především kompenzovat výše zmíněné slabé stránky. Pro lepší přehlednost je kalciumsilikátové cementy možné rozdělit na čtyři skupiny:
1. Materiály ve formě prášku a tekutiny:
Do této skupiny patří všechny cementy dodávané ve formě prášku a tekutiny, např.
ProRoot® MTA (Dentsply, USA), MTA+ (Cerkamed, Polsko), PD™ MTA White (PD dental, Švýcarsko) a mnoho dalších, které je nutné míchat ručně do konzistence „tekutého písku“ [12]. Tuhnutí je zajištěno hydratační reakcí (většinou trikalciumsilikát s vodou) a doba tuhnutí je v rámci několika hodin. Z důvodu obtížné manipulace a dlouhé doby tuhnutí [13] byly tyto materiály v rámci výkonů se zachováním vitality již překonány materiály novějšími, které jsou v této indikaci preferovány.2. Materiály ve formě prášku a tekutiny dodávané v kapslích: Jedná se o produkty, které jsou připraveny v kapslích a míchány strojově těsně před použitím. Výhodou je přesnější míchací poměr a lepší smíchání materiálu (a tím rovnoměrná hydratace) [14, 15]. Do této skupiny je možné zařadit například Biodentine® (Septodont, Francie), Harvard®
MTA-Cap (Harvard, Germany), MTA Biorep (Itena, Francie) a další. Jednodušší způsob aplikace je ve většině případů zajištěn právě využitím speciálních aplikačních kapslí. Biodentine je možné použít v rozsahu kavity jako „náhradu dentinu“ [16] a jeho předností ve srovnání s předchozí skupinou je příměs chloridu vápenatého, který zajišťuje tuhnutí v rámci 12–15 minut [17].3. Předmíchané materiály: Tyto produkty jsou dostupné v předmíchané formě, jejíž tuhnutí je iniciováno přítomností vlhka. Obsahují příměs kalciumfosfátu, a proto jsou často označované také jako biokeramika. Podle různých konzistencí (sealer, pasta, putty) je možné je použít v mnoha indikacích. Pro výkony se zachováním vitality (především pro přímý kontakt se zubní dření) je ideální použít variantu pasta nebo putty, které mají dobré manipulační vlastnosti a je možné je okamžitě překrýt definitivním výplňovým materiálem [18]. Také z této skupiny je na dentálním trhu velké množství různých produktů, např. NeoPutty™ (Avalon Biomed, USA), Wellroot™ PT (Vericom, Korea), Totalfill® BC RRM Putty (FKG, Švýcarsko) a další.
4. Hybridní materiály – modifikované pryskyřicí: I když byly u předchozích dvou skupin manipulační vlastnosti vylepšeny a doba tuhnutí výrazně zkrácena, stále dochází k tuhnutí v řádu desítek minut, což prodlužuje celkovou délku ošetření. Cílem výrobců tedy bylo inovovat materiál tak, aby tuhnul ideálně okamžitě po aplikaci. Z tohoto důvodu byly vytvořeny hybridy, které jsou modifikovány pryskyřicí a jejich tuhnutí je zajištěno buď světelnou polymerací, nebo duálně, tedy tuhnou chemicky a světlem. V poslední době se na trhu objevuje velké množství těchto produktů a jsou výrobci uváděny jako vhodné pro přímý i nepřímý kontakt se zubní dření. Obsahují různé poměry pryskyřice, kalciumsilikátové nebo kalciumfosfátové složky i rentgenkontrastního činidla
[19–21]. Na trhu jsou dostupné např. Theracal LC® (Bisco, USA), Harvard BioCal®-Cap
(Harvard, Německo), ApaCal ART® (Prevest DenPro, Indie) a další.Je zřejmé, že pro praktického zubního lékaře může být obtížné zorientovat se v tomto velkém množství různých produktů a použít je v optimální indikaci. Z výše popsaných charakteristik je možné odvodit, že pro výkony se zachováním vitality je ideální používat materiály z druhé, třetí, případně i čtvrté skupiny. V případě pryskyřicí modifikovaných hybridů, které jsou na dentálním trhu výrazně kratší dobu, je otázkou, jakým způsobem ovlivní přítomnost monomerů celkové vlastnosti materiálu (např. cytotoxický efekt v přímém kontaktu s buněčnou kulturou je výrazně vyšší než u klasických kalciumsilikátů [20]).
Vzhledem k výše popsané problematice bylo cílem této in vitro studie u vybraných pryskyřicí modifikovaných materiálů zhodnotit jejich antibakteriální vlastnosti, které předpokládáme, že budou podobné nebo lepší než u referenčního vzorku.
Hypotézy
Nulová hypotéza A0: Vybrané kalciumsilikátové nebo kalciumfosfátové materiály modifikované pryskyřicí mají stejný nebo vyšší antimikrobiální efekt vůči vybraným mikroorganismům než klasické kalciumsilikátové cementy.
Alternativní hypotéza Aa: Vybrané kalciumsilikátové nebo kalciumfosfátové materiály modifikované pryskyřicí mají menší antimikro-
biální efekt vůči vybraným mikroorganismům než klasické kalciumsilikátové cementy.MATERIÁL A METODIKA
Materiály
Jako referenční vzorek pro tuto studii byl zvolen BiodentineTM (Septodont, Francie)
jakožto zlatý standard používaný u výkonů
se zachováním vitality [16, 17].Z obsáhlé skupiny pryskyřicí modifikovaných hybridních materiálů byly na základě typu tuhnutí a použitých částic vybrány:
TheraCal LC® (Bisco, USA), jako zástupce světlem tuhnoucích materiálů s kalciumsilikátovou složkou; TheraCal PT® (Bisco, USA), jako zástupce duálně tuhnoucích materiálů s kalciumsilikátovou složkou; ApaCal ART® (Prevest DenPro, Indie), jako zástupce světlem tuhnoucích materiálů s kalciumfosfátovou složkou (tab. 1).Table 1. Přehled vybraných materiálů. Tab. 1 Overview of selected materials. 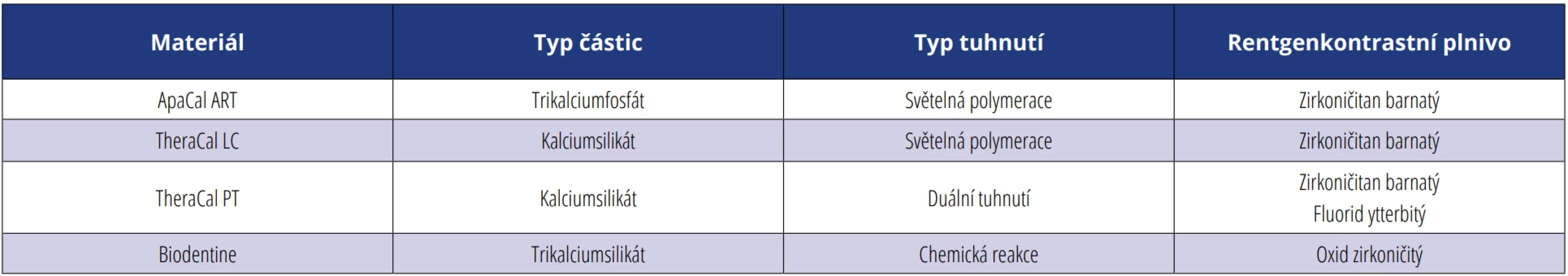
Metodika
Pro in vitro studii byly zvoleny čtyři skupiny mikroorganismů: 1. viridující streptokoky (čtyři kmeny Streptococcus mitis, tři kmeny Streptococcus parasanguinis a tři kmeny Streptococcus vestibularis), 2. rod Lactobacillus (tři kmeny Lactobacillus gasseri, čtyři kmeny Lactobacillus jensenii, tři kmeny Lactobacillus crispatus), 3. Enterococcus faecalis,
4. Candida albicans. Experiment zahrnoval pro každou ze čtyř skupin mikroorganismů deset biologických replikací (tj. 4 × 10 různých kmenů), které pocházely ze sbírky mikroorganismů Ústavu mikrobiologie Lékařské fakulty Univerzity Palackého a Fakultní nemocnice v Olomouci. Pro zhodnocení antimikrobiálních účinků jednotlivých materiálů byl u těchto skupin proveden agarový difuzní test, experiment proběhl paralelně pro všechny vzorky.K identifikaci mikroorganismů byl použit hmotnostní spektrometr. Malé množství vyšetřované kultury bylo pomocí dřevěného párátka přeneseno na terčík MALDI destičky. V případě kvasinek byl testovaný vzorek nejprve překryt 1 μl 70% roztoku kyseliny mravenčí (Bruker Daltonics, Německo). V dalším kroku byly všechny vzorky převrstveny 1 µl matrice (Bruker Daltonics, Německo). Po zaschnutí reagencií byla destička vložena do přístroje Microflex LT (Bruker Daltonics, Německo) a byl spuštěn proces stanovení hmotnostního spektra proteinů. K analýze výsledků byl využit program MALDI Biotyper (Bruker Daltonics, Německo).
Před testováním byl izolát každého kmene inokulován na Columbia krevní agar v separátní nádobě (plastová Petriho miska o průměru 90 mm, Trios, Česká republika) a inkubován 18–24 h ve velkoobjemovém inkubátoru (35 ± 1 °C, 5 % CO2, PHCBi, Japonsko). Následující den bylo přeneseno několik kolonií daného izolátu do zkumavky se sterilním fyziologickým roztokem a konečná denzita suspenze byla pomocí turbidimetru DENSILAMETER-II (EMO, Česká republika) upravena tak, aby odpovídala hodnotě 0,5
McFarlandovy zákalové stupnice. To odpo-
vídá množství 1–5 × 106 CFU (colony forming units – jednotek tvořících kolonie) v 1 ml. Poté byla mikrobiální suspenze daného kmene inokulována pomocí vatového tamponu na celou plochu Mueller Hintonova agaru s koňskou krví v separátní nádobě (plastová Petriho miska o průměru 90 mm, Trios, Česká republika). Následně byly do každé ze 40 kultivačních nádob s inokulovaným agarem vytvořeny čtyři jamky o průměru 5 mm a výšce 4 mm (hloubka celé vrstvy agaru), které byly za podmínek určených výrobcem vyplněny vzorky ApaCal ART, TheraCal LC, TheraCal PT a Biodentine (obr. 1).Image 1. Schéma lokalizace vzorků na ploše agaru. Fig. 1 Diagram showing the localization of samples on the agar surface. 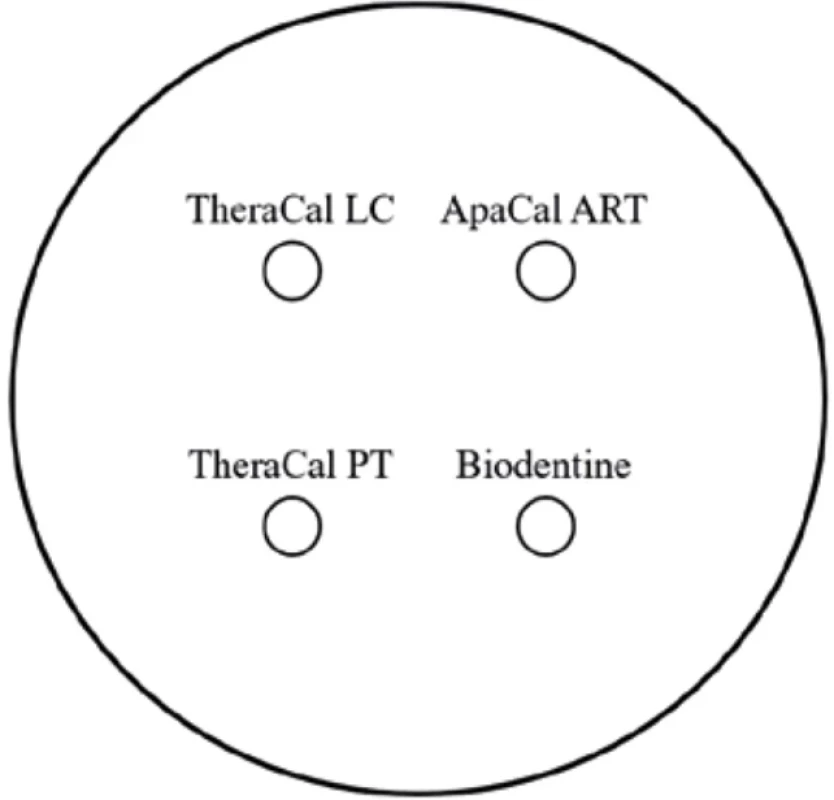
ApaCal ART, Theracal LC a TheraCal PT, materiály v již předmíchané formě ve stříkačce s kanylou, byly injikovány do jamky a následně ze vzdálenosti 2 mm fotopolymerovány po dobu stanovenou výrobcem pomocí polymerační lampy ValoTM (Ultradent
Products, USA) za standardního výkonu
1000 mW/cm2. Biodentine byl připraven podle instrukcí výrobce a aplikován do jamky, kde během 15 minut došlo k jeho chemickému tuhnutí. Následovala inkubace naočkovaných půd 24–48 h ve velkoobjemovém inkubátoru (35 ± 1 °C, 5 % CO2, PHCBi, Japonsko). Průměry vzniklých zón inhibice růstu byly měřeny pomocí digitálního posuvného měřidla po 24 a 48 h inkubace (obr. 2 a 3), z naměřených hodnot bylo odečteno
5 mm (průměr jamky s materiálem). V případě kmenů Lactobacillus byly inhibiční zóny měřeny pouze po 48 h z důvodu typicky pomalejšího růstu tohoto mikroorganismu.Image 2. Kultivace viridujících streptokoků, zřetelné inhibiční zóny u materiálů TheraCal LC, TheraCal PT a Biodentine. Fig. 2 Viridans streptococci culture showing inhibition zones around TheraCal LC, TheraCal PT, and Biodentine. 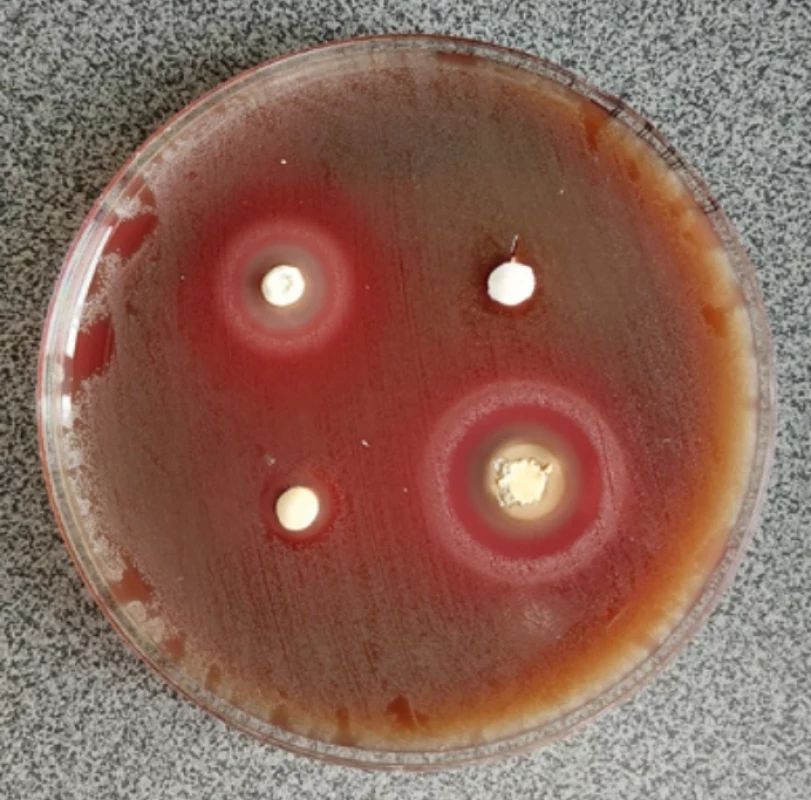
Image 3. Kultivace Candida albicans, zřetelné inhibiční zóny u materiálů TheraCal LC a Biodentine. Fig. 3 Candida albicans culture, inhibition zones around TheraCal LC, and Biodentine. 
Statistická analýza dat
Získaná data byla statisticky zpracována. Shapirovými-Wilkovými testy normality bylo ověřeno, že většina veličin neměla normální distribuci.
Porovnání čtyř skupin materiálů bylo provedeno pomocí Kruskalova-Wallisova testu, následnými post hoc testy s Bonferroniho korekcí byly porovnány zkoumané materiály s referenčním materiálem.
Pro každý materiál byly pomocí Kruskalova-Wallisova testu porovnány velikosti inhibičních zón u všech skupin mikroorganismů, aby bylo možné zhodnotit jeho antimikrobiální účinky vůči konkrétním bakteriím nebo kvasinkám. Pokud se výsledky statistiky významně lišily, následovaly post hoc testy s Bonferroniho korekcí pro porovnání po dvojicích.
U každého materiálu byly pro každý mikroogranismus porovnány velikosti inhibiční zóny při měření po 24 a 48 h pomocí Wilcoxonových testů.
Všechny testy byly provedeny na hladině významnosti 0,05. Pokud byla p-hodnota nižší než 0,05, byly považovány rozdíly za statisticky významné a jsou označeny tučně. Ke statistickému zpracování byl použit statistický software IBM SPSS Statistics for Windows, Version 23.0. Armonk, NY: IBM Corp.
VÝSLEDKY
Kvantitativní proměnné (průměry inhibičních zón) jsou prezentovány pomocí mediánů, minimálních a maximálních hodnot, případně průměrů a směrodatných odchylek (SD).
Velikosti inhibičních zón znázorňuje krabicový graf na obrázku 4. Vodorovná čára v krabici znázorňuje hodnotu mediánu, dolní hrana krabice hodnotu 1. kvartilu, horní hrana hodnotu 3. kvartilu. Svorky ukazují maximální a minimální naměřené hodnoty.
Odlehlé (hodnoty, které jsou od kvartilů vzdáleny více než 1,5násobek mezikvartilového
rozpětí), jsou zakresleny kroužky.Image 4. Rozložení naměřených hodnot velikostí inhibičních zón (uvedených v mm) u všech mikroorganismů po 24 a 48 h pro všechny zkoumané materiály: vodorovná čára v krabici – hodnota mediánu; dolní hrana krabice – hodnota 1. kvartilu (25. percentilu); horní hrana – hodnota 3. kvartilu (75. percentilu); svorky – maximální a minimální naměřené hodnoty; 0 – odlehlé hodnoty (od kvartilů vzdáleny více než 1,5násobek mezikvartilového rozpětí); * – extrémní hodnoty (jsou od kvartilů vzdáleny více než trojnásobek mezikvartilového rozpětí). Fig. 4 Distribution of measured values of inhibition zone sizes (in mm) for all microorganisms after 24 and 48 hours for all tested materials: horizontal line in the box – median value; lower edge of the box – 1st quartile value (25th percentile); upper edge – 3rd quartile value (75th percentile); whiskers – maximum and minimum measured values; 0 – outliers (more than 1.5 times the interquartile range from the quartiles); * – extreme values (more than three times the interquartile range from the quartiles). 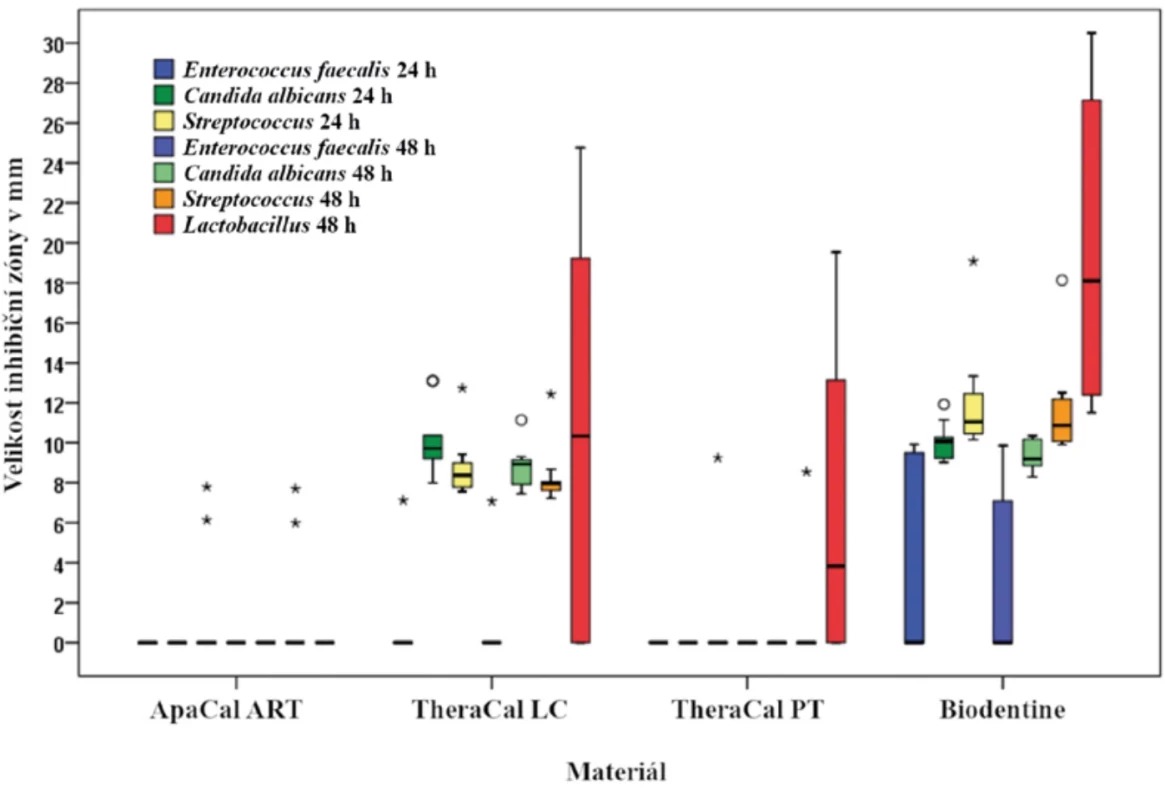
Extrémní (hodnoty, které jsou od kvartilů vzdáleny více než trojnásobek mezikvartilového rozpětí), jsou zakresleny hvězdičkami.
Vzájemné porovnání čtyř materiálů je prezentováno v tabulce 2. U všech mikrobiálních kmenů v obou měřených časech se velikosti inhibičních zón v rámci skupiny všech mate-
riálů statisticky významně lišily (p < 0,05).Table 2. Kruskalův-Wallisův test pro porovnání čtyř skupin zkoumaných materiálů, hodnoty uvedeny v mm, v případě p < 0,05 označeno tučně. Tab. 2 Kruskal-Wallis test for comparing the four groups of examined materials. Values are given in mm, with p < 0.05 indicated in bold. 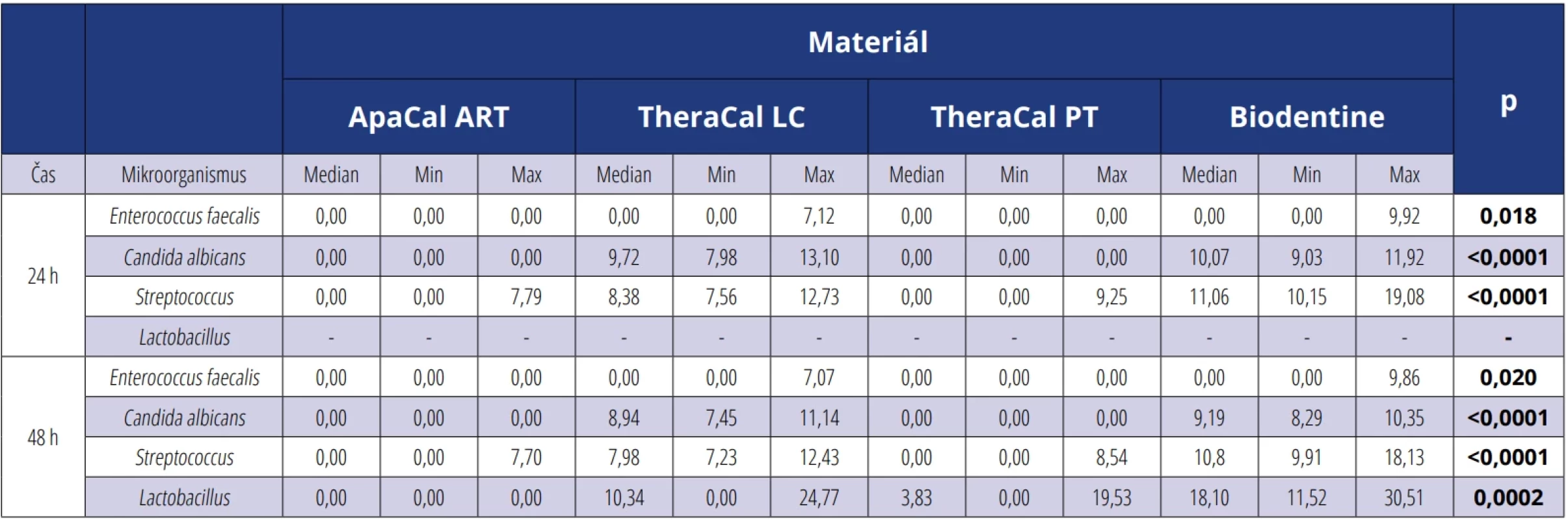
Tabulka 3 ukazuje porovnání jednotlivých vzorků s referenčním materiálem. V několika případech byly zaznamenány statisticky významné rozdíly mezi zkoumanými materiály a referenčním materiálem.
Table 3. Post hoc test s Bonferroniho korekcí pro srovnání zkoumaných materiálů s referenčním materiálem u všech skupin mikroorganismů v měřených časech po 24 a 48 h, v případě p < 0,05 označeno tučně. Tab. 3 Post hoc test with Bonferroni correction comparing the investigated materials with the reference material for all groups of microorganisms at 24 and 48 h. Results with p < 0.05 are indicated in bold. 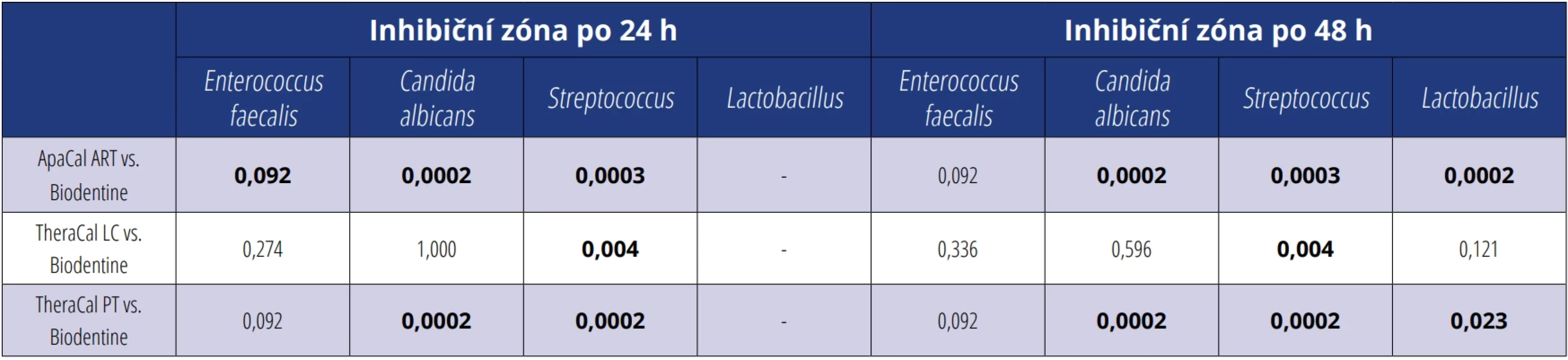
Porovnání antimikrobiálních účinků materiálů vůči jednotlivým mikroorganismům jsou shrnuta v tabulkách 4 a 5. Inhibiční zóny tvořené ApaCal ART se u jednotlivých mikroorganismů v čase měření po 24 ani 48 h statisticky významně nelišily. U TheraCal LC se statisticky významně lišily při měření po 24 i 48 h; inhibiční zóny u Enterococcus faecalis byly signifikantně menší než u Candida albicans a Streptococcus, jiné rozdíly statisticky významné nebyly. Pro TheraCal PT se velikost inhibičních zón statisticky významně lišila pouze při měření po 48 h, avšak post hoc testy statisticky významné rozdíly neprokázaly; na hranici signifikance byly pouze rozdíly mezi Lactobacillus, Enterococcus faecalis a Candida albicans, kde antibakteriální efekt vůči skupině Lactobacillus byl vyšší. Velikost inhibičních zón u Biodentine se statisticky významně lišila při měření po 24 i 48 h; statisticky významné byly rozdíly mezi všemi mikroorganismy, nejvyšší účinek byl u Lactobacillus, následoval Streptococcus, Candida albicans, nejnižší účinek byl u Enterococcus faecalis.
Table 4. Srovnání velikosti inhibičních zón u všech mikroorganismů pro každý materiál pomocí Kruskalova-Wallisova testu, v případě p < 0,05 označeno tučně. Tab. 4 Comparison of inhibition zone sizes for all microorganisms for each material using the Kruskal-Wallis test. Values with p < 0.05 are indicated in bold. 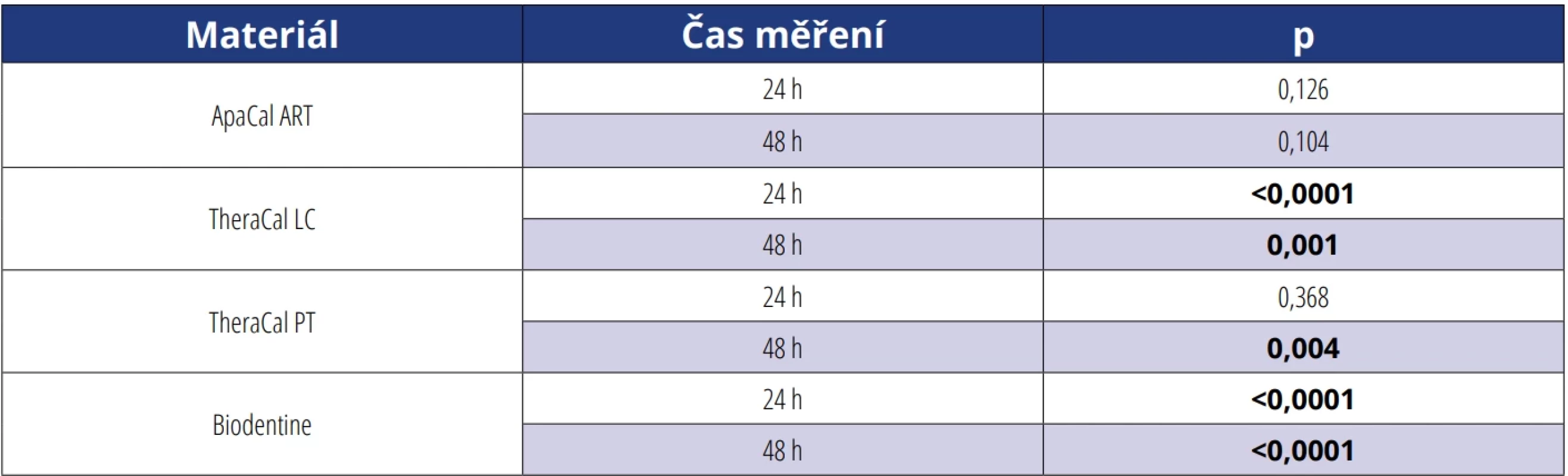
Table 5. Post hoc testy s Bonferroniho korekcí pro porovnání po dvojicích (E.F. – Enterococcus faecalis, C.A. – Candida albicans, S. – Streptococcus, L. – Lactobacillus), v případě p < 0,05 označeno tučně. Tab. 5 Post hoc tests with Bonferroni correction for pairwise comparisons (E.F. – Enterococcus faecalis, C.A. – Candida albicans, S. – Streptococcus, L. – Lactobacillus). Results with p < 0.05 are indicated in bold. 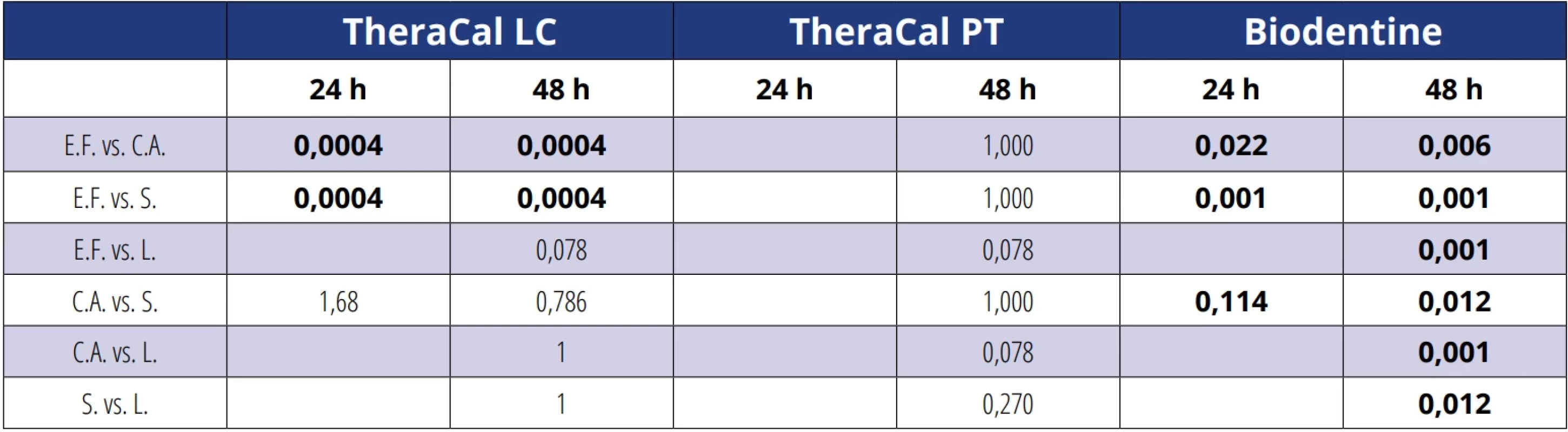
Porovnání velikosti inhibičních zón v čase ukazuje tabulka 6. Rozdíl velikosti inhibičních zón po 24 a 48 h u vzorků ApaCal ART a TheraCal PT nebyl u žádného mikroorganismu statisticky významný. U materiálů TheraCal LC a Biodentine byly zjištěny po 48 h signifikantně nižší hodnoty ve srovnání s měřením po 24 h u skupin Candida albicans a Streptococcus.
Table 6. Srovnání velikosti inhibičních zón v závislosti na čase měření (po 24 a 48 h), v případě p < 0,05 označeno tučně. Tab. 6 Comparison of the inhibition zone sizes depending on the measurement time (after 24 and 48 h). Values with p < 0.05 are indicated in bold. Materiál 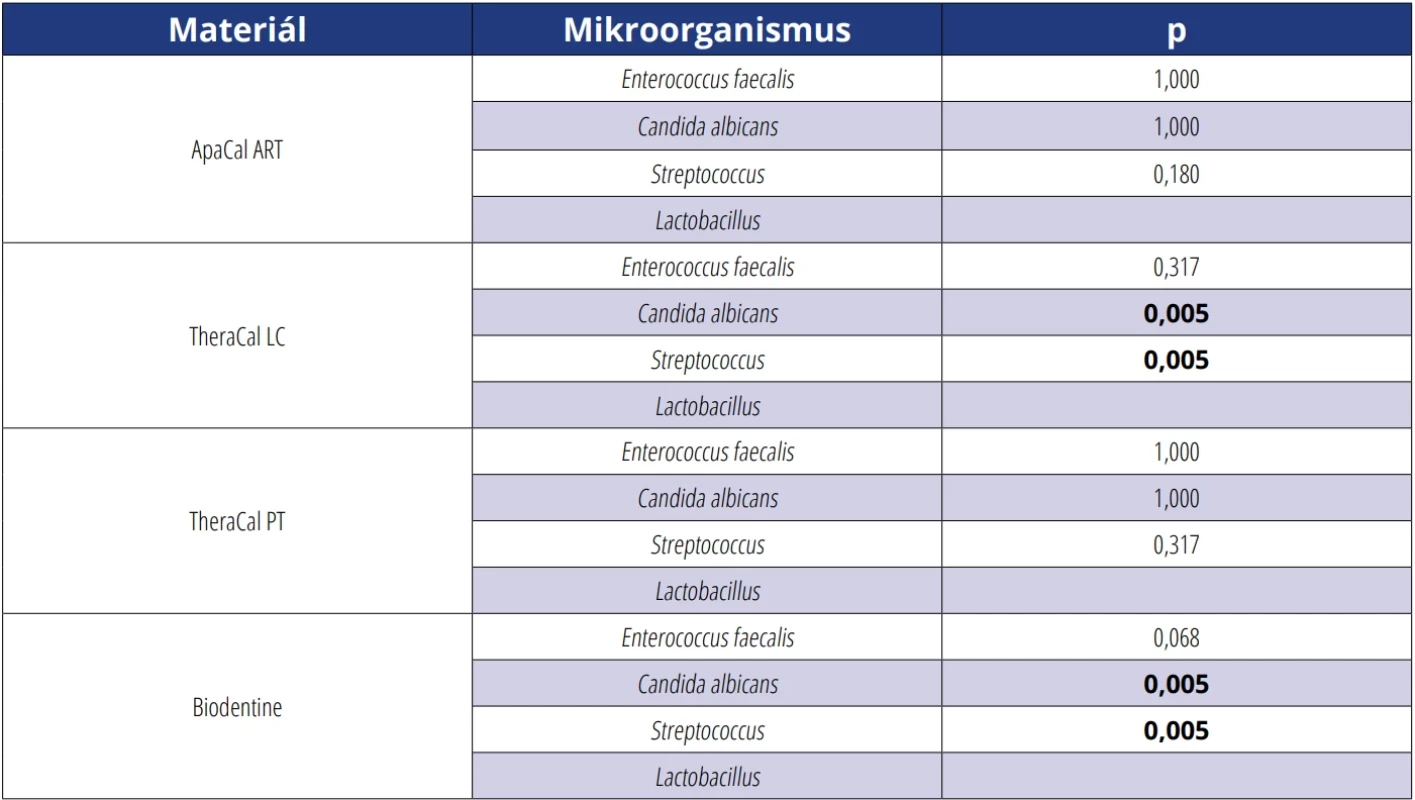
DISKUSE
Vzhledem k tomu, že při selektivní exkavaci ponecháváme v kavitě změklý dentin, který může obsahovat malé množství bakterií, je žádoucí, aby měl výplňový materiál antibakteriální, případně i antifungální vlastnosti [8]. Cílem této studie bylo pomocí difuzního agarového testu zhodnotit antimikrobiální účinek vybraných kalciumsilikátových a kalciumfosfátových cementů modifikovaných pryskyřicí vůči 1. viridujícím streptokokům, 2. rodu Lactobacillus, 3. Enterococcus faecalis, 4. Candida albicans.
Viridující streptokoky jsou označovány jako hlavní kariogenní patogeny [22], zejména pak Streptococcus mutans, vůči kterému již byla antibakteriální aktivita zkoumána [23–25]. U hlubokých kariézních lézí se však do popředí dostávají jiné rody bakterií, rod Streptococcus je zde přítomen již v menší míře a je zde větší variabilita druhů, které může být mnohdy obtížné specifikovat [26–28]. Cílem naší in vitro studie bylo zhodnotit antimikrobiální působení vůči dalším vybraným druhům orálních streptokoků (mimo S. mutans), které se v hlubokých kazech vyskytují, konkrétně se jednalo o dostupné kmeny druhů Streptococcus mitis (čtyři kmeny), Streptococcus parasanguinis (tři kmeny) a Streptococcus vestibularis (tři kmeny). V této práci jsou výše popsané druhy zahrnuty do jedné skupiny viridujících streptokoků, jelikož cílem bylo zhodnocení antibakteriálních vlastností materiálů vůči těmto streptokokům obecně. Rod Lactobacillus patří mezi dominantní skupinu u hlubokých kariézních lézí, hlavním druhem je Lactobacillus acidophilus [29], nicméně podle dostupné literatury je zřejmé, že je zde velká variabilita mnoha dalších druhů [22, 26–28]. Z toho důvodu byly pro naši in vitro studii vybrány dostupné kmeny druhů Lactobacillus gasseri (tři kmeny), Lactobacillus jensenii (čtyři kmeny) a Lactobacillus crispatus (tři kmeny). V textu jsou tyto kmeny pro zjednodušení a lepší přehlednost zařazeny do jedné zkoumané skupiny Lactobacillus, neboť cílem bylo zhodnotit, zda mají materiály antibakteriální efekt obecně vůči rodu Lactobacillus. Enterococcus faecalis byl zvolen, protože tento patogen bývá často vůči stomatologickým prostředkům rezistentní a v případě přítomnosti v kariézní lézi zde často perzistuje i po ošetření [30]. Candida albicans je v dnešní době také označována jako jeden z mnoha potenciálních kariogenních patogenů, a proto byla do této studie také zahrnuta [31].
Vzhledem k tomu, že dostupná literatura se většinou orientuje na antibakteriální schopnosti vůči jednomu až dvěma typům bakterií, záměrem této in vitro studie bylo spojit do jednoho výzkumu jak hlavní kariogenní patogeny [22], tak také kvasinky a bakterie, které jsou velmi odolné a bývá problematické je odstranit [30, 31]. Dalším cílem bylo srovnat působení zkoumaných vzorků s referenčním materiálem, který je v klinické praxi již delší dobu a jeho vlastnosti jsou již důkladně prozkoumány [32, 33].
Při hodnocení získaných výsledků byla pro možnost srovnání s dalšími publikacemi hlavním problémem nedostatečná standardizace metodik. Mnohé studie využívaly zcela jiný typ testování [29, 34], odlišné inkubační prostředí [25], v případě difuzního agarového testu byla použita jiná kultivační média [24] nebo byl nastaven odlišný čas měření inhibičních zón [35]. Dalším úskalím může být různá virulence dostupných bakteriálních kmenů, které byly získány z odlišných zdrojů, proto byly rozdílné velikosti inhibičních zón při využití obdobné metodiky [35].
Bylo ověřeno, že Biodentine vykazuje antimikrobiální schopnosti vůči všem zkoumaným skupinám. Toto zjištění je v souladu s dalšími studiemi [23, 35–37]. Největší inhibiční zóny v rozmezí 11,52–30,51 mm byly vytvořeny u skupiny Lactobacillus, dále u Streptococcus bylo rozmezí hodnot 9,91–19,8 mm, u Candida albicans 8,29–11,92 mm, nejnižší hodnoty byly zjištěny u Enterococcus faecalis 0–9,92 mm. Při srovnání v čase došlo po 24 hodinách od prvního měření ke zmenšení zón u skupin Streptococcus a Candida albicans.
Velikosti inhibičních oblastí u všech skupin mikroorganismů srovnaných mezi sebou a také v čase po 24 a 48 h v případě ApaCal ART nebyly statisticky významně rozdílné, je tedy možné předpokládat, že tento materiál má podobné antimikrobiální schopnosti vůči všem zkoumaným mikroorganismům. Nicméně se většinou jednalo o nulové hodnoty, pouze u Streptococcus byly naměřeny zóny 0–7,79 mm. Při srovnání s ostatními zkoumanými vzorky, a především s referenčním materiálem je tedy zřejmé, že antimikrobiální potenciál materiálu ApaCal ART je ze všech nejnižší, přesněji je omezen pouze na skupinu Streptococcus. Vzhledem k tomu, že se jedná o poměrně nový produkt, o kterém bylo v posledních pěti letech publikováno pouze omezené množství studií převážně hodnotících fyzikální vlastnosti [38, 39], sílu vazby k adhezivním systémům [40, 41], radioopacitu [21], případně cytotoxicitu [20], ne však antimikrobiální vlastnosti, nebylo možné srovnat výsledek této in vitro studie s jinou publikací zaměřující se na stejné téma.
TheraCal PT vykazoval tvorbu inhibiční zóny v rozmezí 0–19,53 mm u skupiny Lactobacillus, dále u Streptococcus 0–9,25 mm, v případě
Candida albicans a Enterococcus faecalis nebyly vytvořeny inhibiční zóny. U žádné skupiny se neprokázaly statisticky významné rozdíly v čase. Ve srovnání s referenčním materiálem se ovšem také jedná o statisticky významně rozdílné (nižší) hodnoty u většiny inhibičních zón. Nesignifikantní rozdíly byly pouze u Enterococcus faecalis, kde však u TheraCal PT nedošlo k tvorbě inhibičních zón a u ostatních materiálů bylo omezení růstu také nevýrazné. Nejedná se sice o nový výrobek, publikace zkoumající tento materiál se však ve většině případů zaměřují na bioaktivitu nebo cytokompatibilitu [19, 42, 43]. Pouze jedna publikace se zaměřila také na inhibici růstu Enterococcus faecalis, kde však TheraCal PT vykazoval výrazně vyšší antimikrobiální aktivitu než Biodentine, což se neshoduje s výsledkem této in vitro studie [34]. Důvodem rozdílných výsledků může být volba odlišné metodiky a způsob použití vzorku, jelikož ve zmíněné publikaci byl materiál použit k tvorbě extraktu v neztuhlé formě. Antimikrobiální schopnosti vůči ostatním zkoumaným mikroorganismům nebylo možné srovnat s odbornou literaturou. Podle této studie však lze TheraCal PT popsat jako materiál s lepšími antimikrobiálními schopnostmi než ApaCal ART, nicméně stále zcela nedosahujícími potenciálu referenčního materiálu.TheraCal LC je dostupný na dentálním trhu již přes deset let, a proto byly jeho vlastnosti mnohem důkladněji prozkoumány a popsány [44]. Antimikrobiální efekt byl v některých publikacích srovnáván s klasickými podložkovými materiály, především s kalciumsalycilátovými nebo skloionomerními cementy za použití různých metodik. Například Moradi a kol. uvádí podobnou aktivitu vůči Lactobacillus acidophilus, Lactobacillus casei a Streptococcus mutans u TheraCal LC stejně jako u světlem tuhnoucích kalciumsalycilátových nebo skloionomerních cementů, ale nižší než u chemicky tuhnoucích kalciumsalycilátových materiálů [29]. Vzhedem k tomu, že publikací zaměřených na antimikrobiální účinek TheraCal LC je v posledních letech větší množství, pro srovnání této in vitro studie byly vybrány především publikace zaměřující se na odpovídající spektrum mikroorganismů a srovnávající TheraCal LC s čistě kalciumsilikátovými cementy. V naší in vitro studii bylo prokázáno, že TheraCal LC vykazuje antimikrobiální aktivitu vůči všem zkoumaným skupinám, což je v souladu s dalšími studiemi, ve kterých byla prokázána aktivita vůči skupinám Lactobacillus [29], Streptococcus [24, 25, 45] a Enterococcus faecalis [24, 25]. Pouze v případě aktivity vůči Candida albicans zatím nejsou dostupné jiné publikace. Při srovnání TheraCal LC s referenčním materiálem jsou rozdíly hodnot statisticky významně odlišné pouze u skupiny Streptococcus, v ostatních skupinách jsou výsledky podobné, inhibiční zóny u TheraCal LC byly nepatrně menší. Toto zjištění u aktivity vůči Lactobacillus, Enterococcus faecalis a Streptococcus koreluje s dalšími studiemi [24, 35, 45]. V případě výzkumu od Niranjana a kol. byly velikosti inhibičních zón u skupin Enterococcus a Streptococcus podobně velké, zatímco v naší studii byly u skupiny Enterococcus výrazně menší. Důvodem je pravděpodobně rozdíl v metodice agarového testu, neboť v naší studii byl použit krevní agar pro všechny zkoumané skupiny, zatímco ve zmíněné práci byl pro inkubaci skupiny Enterococcus použit agar Mueller Hinton [24]. Ačkoliv v naší studii byly velikosti inhibičních zón jednotlivých mikroorganismů statisticky významně rozdílné, hodnoty byly vyšší než u ostatních zkoumaných materiálů a podobné s referenčním vzorkem. Je tedy zřejmé, že TheraCal LC má ze zkoumaných výrobků největší antimikrobiální potenciál.
Po zhodnocení všech výsledků je nulová hypotéza A0 zamítnuta, jelikož zkoumané materiály nemají stejný nebo vyšší antimikrobiální efekt vůči vybraným mikroorganismům než klasické kalciumsilikátové cementy. Vzhledem k tomu, že jej mají v různé míře nižší než referenční materiál, je přijata alternativní
hypotéza Aa.ZÁVĚR
Kalciumsilikátové a kalciumfosfátové pryskyřicí modifikované hybridní materiály vykazují nižší antimikrobiální efekt vůči vybraným mikroorganismům než klasické kalciumsilikátové cementy. Z tohoto důvodu je v klinické praxi stále vhodnější preferovat použití nemodifikovaných kalciumsilikátových materiálů. Vzhledem k výrazné odlišnosti výsledků mezi jednotlivými zkoumanými vzorky však nelze prohlášení o nízkých antimikrobiálních schopnostech zobecnit pro všechny pryskyřicí modifikované hybridní materiály. ApaCal ART nevykazuje téměř žádnou antimikrobiální aktivitu vůči vybraným mikroorganismům, TheraCal PT má výsledky lepší, naproti tomu nejvýraznějšího antimikrobiálního efektu dosahuje TheraCal LC. Na základě této in vitro studie je tedy možné TheraCal LC volit jako alternativu klasických kalciumsilikátových cementů, nicméně je třeba ještě dalších in vitro a in vivo studií k důkladnějšímu prozkoumání dalších vlastností těchto materiálů.
Poděkování
Autoři děkují Mgr. Kateřině Langové, Ph.D. (Ústav lékařské biofyziky, Lékařská fakulta Univerzity Palackého v Olomouci) za statistické zpracování získaných dat.
Prohlášení o střetu zájmů
Autoři deklarují, že nemají žádný konflikt zájmů týkající se problematiky zkoumané v této původní práci.
Podíl autorů na publikaci
B. N., P. H. a Y. M. se podíleli na designu experimentu. B. N. a L. Sm. se podílely na přípravě vzorků. B. N. a L. Sv. provedly vlastní testování a následné měření. L. Sm. a M. R. vyhodnotili získaná data. Všichni autoři přispěli k sepsání rukopisu.
Dostupnost dat
Data jsou v případě odůvodněného požadavku dostupná u korespondující autorky.
Korespondující autorka
MDDr. Barbora Novotná
Klinika zubního lékařství
Lékařská fakulta Univerzity Palackého v Olomouci
Fakultní nemocnice Olomouc
Palackého 12
779 00 Olomouc
e-mail: barbora.novotna@upol.cz
Sources
1. Innes NPT, Frencken JE, Bjørndal L, Maltz M, Manton DJ, Ricketts D, et al. Managing carious lesions: consensus recommendations on terminology. Adv Dent Res. 2016; 28(2): 49–57. doi: 10.1177/0022034516639276
2. Duncan HF, Galler KM, Tomson PL, Simon S, El-Karim I, Kundzina R, et al. European Society of Endodontology position statement: Management of deep caries and the exposed pulp. Int Endod J. 2019; 52(7): 923–934. doi: 10.1111/iej.13080
3. Alleman DS, Magne P. A systematic approach to deep caries removal end points: the peripheral seal concept in adhesive dentistry. Quintessence Int. 2012; 43(3): 197–208.
4. Barros MMAF, De Queiroz Rodrigues MI, Muniz FWMG, Rodrigues LKA. Selective, stepwise, or nonselective removal of carious tissue: which technique offers lower risk for the treatment of dental caries in permanent teeth? A systematic review and meta-analysis. Clin Oral Investig. 2020; 24(2): 521–532. doi: 10.1007/s00784-019-03114-5
5. Ricucci D, Siqueira JF, Li Y, Tay FR. Vital pulp therapy: histopathology and histobacteriology-based guidelines to treat teeth with deep caries and pulp exposure. J Dent. 2019; 86 : 41–52. doi: 10.1016/j.jdent.2019.05.022
6. Iwami Y, Hayashi N, Takeshige F, Ebisu S. Relationship between the color of carious dentin with varying lesion activity, and bacterial detection. J Dent. 2008; 36(2): 143–151. doi: 10.1016/j.jdent.2007.11.012
7. Wells C, Dulong C. Vital pulp therapy for endodontic treatment of mature teeth: a review of clinical effectiveness, cost-effectiveness, and guidelines. Canadian Agency for Drugs and Technologies in Health; 2019 : 1–31.
8. Hanna SN, Alfayate RP, Prichard J. Vital pulp therapy an insight over the available literature and future expectations. Eur Endod J. 2020; 5(3): 46–53. doi: 10.14744/eej.2019.44154
9. Novotná B, Harvan Ľ, Somolová L, Morozova Y, Voborná I. Ošetření kazu blízkého zubní dřeni a metoda odložené exkavace. Čes. stomatol. Prakt. zub. lék. (Czech Dental Journal) 2021; 121(3): 83–89. doi: 10.51479/cspzl.2021.011
10. Lee SJ, Monsef M, Torabinejad M. Sealing ability of a mineral trioxide aggregate for repair of lateral root perforations. J Endod. 1993; 19(11): 541–544. doi: 10.1016/S0099-2399(06)81282-3
11. Cervino G, Laino L, D’Amico C, Russo D, Nucci L, Amoroso G, et al. Mineral trioxide aggregate applications in endodontics: A review. Eur J Dent. 2020; 14(4): 683–691. doi: 10.1055/s-0040-1713073
12. Žižka R, Šedý J, Voborná I. Příprava kalciumsilikátových cementů. LKS. 2020; 30(1): 8–11. 13. Kadali N, Krishna Alla R, Guduri V, Av R, Sajjan Mc S, Venkateswara Raju R, Lecturer R. Mineral trioxide aggregate: an overview of composition, properties and clinical applications. Int J Dent Mater. 2020; 2(1): 11–18. doi: 10.37983/IJDM.2020.2103
14. Žižka R, Šedý J, Škrdlant J, Kučera P, Čtvrtlík R, Tomáštík J. Kalciumsilikátové cementy. 1. část: Vlastnosti a rozdělení. LKS. 2018; 28(2): 37–43. 15. Domingos Pires M, Cordeiro J, Vasconcelos I, Alves M, Quaresma SA, Ginjeira A, et al. Effect of different manipulations on the physical, chemical and microstructural characteristics of iodentine. Dent Mater. 2021; 37(7): e399–406. doi: 10.1016/j.dental.2021.03.021
16. Awawdeh L, Al-Qudah A, Hamouri H, Chakra RJ. Outcomes of vital pulp therapy using mineral trioxide aggregate or biodentine: a prospective randomized clinical trial. J Endod. 2018; 44(11): 1603–1609. doi: 10.1016/j.joen.2018.08.004
17. Kadali NS, Alla RK, Av R, Mc SS, Raju Mantena S, Raju RV. An overview of composition, properties, and applications of Biodentine. Int J Dent Mater. 2021; 03(04): 120–126. doi: 10.37983/ijdm.2021.3404
18. Lozano-Guillén A, López-García S, Rodríguez-Lozano FJ, Sanz JL, Lozano A, et al. Comparative cytocompatibility of the new calcium silicate-based cement NeoPutty versus NeoMTA Plus and MTA on human dental pulp cells: an in vitro study. Clin Oral Investig. 2022; 26 : 7219–7228. doi: 10.1007/s00784-022-04682-9
19. Rodríguez-Lozano FJ, López-García S, García-Bernal D, Sanz JL, Lozano A, Pecci-Lloret MP, et al. Cytocompatibility and bioactive properties of the new dual-curing resin-modified calcium silicate-based material for vital pulp therapy. Clin Oral Investig. 2021; 25 : 5009–5024. doi: 10.1007/s00784-021-03811-0/Published
20. Novotná B, Holík P, Morozova Y, Rosa M, Galandáková A, Langová K. Evaluation of cytotoxicity of the dental materials TheraCal LC, TheraCal PT, ApaCal ART and Biodentine used in vital pulp therapy: in vitro study. Dent J. 2024; 12(8): 249. doi: 10.3390/dj12080249
21. Karadas M, Köse TE, Atıcı MG. Comparison of radiopacity of dentin replacement materials. 2020; 9(4): 195–202. doi: 10.22038/jdmt.2020.48196.1366
22. Tanzer J. Microbiology of dental caries. J Biol Earth Sci. 1992; 1(1): 377–424.
23. Esteki P, Jahromi M, Tahmourespour A. In vitro antimicrobial activity of mineral trioxide aggregate, Biodentine, and calcium-enriched mixture cement against Enterococcus faecalis, Streptococcus mutans, and Candida albicans using the agar diffusion technique. Dent Res J (Isfahan). 2021; 18(1). doi: 10.4103/1735-3327.310032
24. Niranjana M, Sunil J, Thomas G, Shyam A, Aparna M. Antimicrobial properties of newer calcium silicate-based pulp-capping agents against Enterococcus faecalis and Streptococcus mutans: an in-vitro evaluation. Cureus J Med Sci. 2024; 16(9): e70459. doi: 10.7759/cureus.70459
25. Morita M, Kitagawa H, Nakayama K, Kitagawa R, Yamaguchi S, Imazato S. Antibacterial activities and mineral induction abilities of proprietary MTA cements. Dent Mater J. 2021; 40(2): 297–303. doi: 10.4012/DMJ.2019-351
26. Liu G, Wu C, Abrams WR, Li Y. Structural and functional characteristics of the microbiome in deep-dentin caries. J Dent Res. 2020; 99(6): 713–720. doi: 10.1177/0022034520913248
27. Spatafora G, Li Y, He X, Cowan A, Tanner ACR. The evolving microbiome of dental caries. microorganisms. 2024; 12(1): 121. doi: 10.3390/MICROORGANISMS12010121
28. Rôças IN, Alves FRF, Rachid CTCC, Lima KC, Assunção I V., Gomes PN, et al. Microbiome of deep dentinal caries lesions in teeth with symptomatic irreversible pulpitis. PLoS One. 2016; 11(5): e0154653. doi: 10.1371/JOURNAL.PONE.0154653
29. Moradi Z, Abbasi M, Bahador A, Yekaninejad MS, Khanghah XM, Hoseini AP, et al. Evaluation of cytotoxicity and antibacterial activity of different pulp capping liners. Biomater Investig Dent. 2023; 10(1): 2287019. doi: 10.1080/26415275.2023.2287019
30. Kuzmanović Radman I, Djeri A, Arbutina A, Milašin J. Microbiological findings in deep caries lesions. Stomatol Glas Srb. 2016; 63(1): 7–14. doi: 10.1515/sdj-2016-0001
31. Pereira DFA, Seneviratne CJ, Koga-Ito CY, Samaranayake LP. Is the oral fungal pathogen Candida albicans a cariogen? Oral Dis. 2018; 24(4): 518–526. doi: 10.1111/odi.12691
32. Davaie S, Hooshmand T, Ansarifard S. Different types of bioceramics as dental pulp capping materials: A systematic review. Ceram Int. 2021; 47(15): 20781–20792. doi: 10.1016/j.ceramint.2021.04.193
33. Docimo R, Carrante VF, Costacurta M. The physical-mechanical properties and biocompatibility of Biodentine: A review. J Osseointegration. 2021; 13(1): 47–50. doi: 10.23805/JO.2021.13.01.8
34. Kim M, Lee SH, Shin DH. In vitro study of the biological and physical properties of dual-cure resin-modified calcium silicate-based cement. Dent J. 2023; 11(5): 120. doi: 10.3390/DJ11050120
35. Eissa M, Ibrahim S, Abdelfattah M, Elawady B. Antimicrobial activity of different bioactive therapeutic pulp capping materials with relevance to their biological and clinical consideration: A comparative in vitro study. Egypt Dent J. 2024; 70(2): 2107–2016. doi: 10.21608/edj.2024.267931.2925
36. Bhavana V, Chaitanya KP, Gandi P, Patil J, Dola B, Reddy RB. Evaluation of antibacterial and antifungal activity of new calcium-based cement (Biodentine) compared to MTA and glass ionomer cement. J Conserv Dent. 2015; 18(1): 44. doi: 10.4103/0972-0707.148892
37. Subhi H, Subhi N, Alhaidary S, Azeez MS, Tabnjh AK. Antibacterial activity of biodentine against Enterococcus faecalis: a systematic review. Front Dent Med. 2024; 5(1498353): 1–19. doi: 10.3389/fdmed.2024.1498353
38. Swathi Priyadharshini S, Ragavendran C, Anand Sherwood I, Jeyapalan R. Comparative evaluation of compressive strength and morphological interface of carbonated hydroxyapatite with other pulp capping materials: An in vitro analysis. Endodontology. 2025; 37(1): 90–95. doi: 10.4103/ENDO.ENDO_92_24
39. Anthrayose P, Aggarwal A, Yadav S, Nawal RR, Talwar S. Microscopic and elemental characterization of hydrated dental pulp capping agents. J Conserv Dent Endod. 2021; 24(5): 496–501. doi: 10.4103/jcd.jcd_460_21
40. Bakir Ş, Bakir EP, Akbiyik SY. Evaluation of the bond strength of resin-modified glass ionomer enhanced with bioactive glass to composite resin with different dental adhesive systems. Anal Quant Cytopathol Histopathol. 2021; 43(4): 235–241.
41. Akbiyik SY, Bakir EP, Bakir S. Evaluation of the bond strength of different pulp capping materials to dental adhesive systems: an in vitro study. J Adv Oral Res. 2021; 12(2): 286–295. doi: 10.1177/2320206821997983
42. Park SH, Ye JR, Asiri NM, Chae YK, Choi SC, Nam OH. Biocompatibility and bioactivity of a dual-cured resin-based calcium silicate cement: in vitro and in vivo evaluation. J Endod. 2024; 50(2): 235–242. doi: 10.1016/J.JOEN.2023.11.009
43. Sanz JL, Soler-Doria A, López-García S, García-Bernal D, Rodríguez-Lozano FJ, Lozano A, et al. Comparative biological properties and mineralization potential of 3 endodontic materials for vital pulp therapy: Theracal PT, Theracal LC, and Biodentine on human dental pulp stem cells. J Endod. 2021; 47(12): 1896–906. doi: 10.1016/j.joen.2021.08.001
44. Arandi NZ, Rabi T. TheraCal LC. From biochemical and bioactive properties to clinical applications. Int J Dent. 2018; 2018 : 6 pages. doi: 10.1155/2018/3484653
45. Poggio C, Beltrami R, Colombo M, Ceci M, Dagna A, Chiesa M. In vitro antibacterial activity of different pulp capping materials. J Clin Exp Dent. 2015; 7(5): e584-588. doi: 10.4317/JCED.52401
Labels
Maxillofacial surgery Orthodontics Dental medicine
Article was published inCzech Dental Journal

2026 Issue 1-
All articles in this issue
- Editorial
- Zpráva ze zasedání redakční rady ČSPZL a informace o činnosti časopisu v roce 2025
- Doktor Ladislav Korábek oslavil významné životní jubileum
- Poděkování recenzentům
- EVALUATION OF THE ANTIMICROBIAL PROPERTIES OF SELECTED NEW RESIN-MODIFIED MATERIALS USED IN VITAL PULP THERAPY: AN IN VITRO STUDY
- SUPERNUMERARY TEETH – PREVALENCE, AETIOLOGY, CLASSIFICATION, DIAGNOSIS, THERAPY, AND COMPLICATIONS
- Z konference „Stomatologie ruku v ruce se všeobecnou medicínou
- Czech Dental Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- EVALUATION OF THE ANTIMICROBIAL PROPERTIES OF SELECTED NEW RESIN-MODIFIED MATERIALS USED IN VITAL PULP THERAPY: AN IN VITRO STUDY
- SUPERNUMERARY TEETH – PREVALENCE, AETIOLOGY, CLASSIFICATION, DIAGNOSIS, THERAPY, AND COMPLICATIONS
- Z konference „Stomatologie ruku v ruce se všeobecnou medicínou
- Doktor Ladislav Korábek oslavil významné životní jubileum
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

