-
Medical journals
- Career
Hodnocení vlivu sterilizační metody na stabilitu karboxymethylcelulosového krytí na rány
Authors: Jan Muselík; Lenka Wojnarová; Ruta Masteiková; Tomáš Sopuch
Authors‘ workplace: Veterinární a farmaceutická univerzita Brno, Farmaceutická fakulta, Ústav technologie léků 1; Lékárna Sfinx, Brno 2; Holzbecher spol. s r. o. barevna a bělidlo Zlíč, divize Holzbecher Medical 3
Published in: Čes. slov. Farm., 2013; 62, 95-98
Category: Original Articles
Overview
Karboxymethylcelulosa, hlavně její sodná sůl mají v podobě pomocných látek mnohostranné využití ve farmacii. Z terapeutického hlediska se sodná sůl karboxymethylcelulosy uplatňuje ve výrobě moderních krytí na rány umožňujících vlhké hojení. Krytí na rány musí být sterilní a stabilní po celou dobu použitelnosti při uchovávání za různých teplotních podmínek. V současné době je k dispozici řada sterilizačních metod. V případě polymerních látek je důležité, aby zvolený postup sterilizace nevyvolával změny ve struktuře polymeru, jako štěpení polymerních řetězců, změny zesítění apod. Tato práce hodnotí vliv různých sterilizačních metod (γ-záření, β-záření, ethylenoxid) na stabilitu karboxymethylcelulosy a dále stabilitu v podmínkách zrychlené a dlouhodobé stabilitní studie. Hodnocení vzorků je provedeno s využitím rozměrově vylučovací chromatografie. Z dosažených výsledků vyplývá, že sterilizace ethylenoxidem představuje nejšetrnější variantu z testovaných způsobů sterilizace. V případě použití sterilizace γ-záření docházelo ke změnám velikosti molekuly karboxymethylcelulosy. V průběhu zrychlené a dlouhodobé stabilitní studie, ale nebyly další degradační změny pozorovány a takto sterilizované vzorky jsou vhodné pro dlouhodobé skladování.
Klíčová slova:
karboxymethylcelulosa – sterilizace – stabilitní studie – rozměrově vylučovací chromatografieÚvod
Hodnocené krytí na rány ve formě netkané textilie představuje karboxymethylcelulosu (CMC) v kyselé formě (CMC H) nebo jako její sodnou sůl (CMC Na). Jako každé krytí na rány musí být v první řadě sterilní a samozřejmě stabilní po celou dobu použitelnosti při uchovávání za různých teplotních podmínek.
K zajištění sterility se krytí na rány vyrábí za podmínek vyhovujících požadavkům Správné výrobní praxe a na závěr výrobního procesu se sterilizují. Účelem sterilizačního procesu je inaktivace jakékoliv přítomné mikrobiální kontaminace.
V současné době je k dispozici řada sterilizačních metod, neexistuje však metoda, která by se hodila pro všechny látky či přípravky, každá má své kladné a záporné stránky. V případě polymerních látek, kam CMC patří, je důležité, aby zvolený postup nevyvolával strukturální změny polymeru, jako štěpení polymerních řetězců, změny zesítění apod. případně, aby tyto změny neovlivňovaly významně mechanické a další vlastnosti.
Sterilizační metody použitelné v případě krytí na rány zahrnují sterilizaci teplem (nasycenou párou pod tlakem), sterilizaci ionizujícím zářením a sterilizaci plynem1). Sterilizace nasycenou párou pod tlakem (autokláv) patří mezi nejspolehlivější metody a je široce používána k sterilizaci léčivých přípravků a zdravotnických prostředků. Účinně a rychle ničí mikroorganismy, nezanechává rezidua a je relativně levná. Podmínkou však je termostabilita látek i použitých obalů2). V případě CMC H a CMC Na nemůže být tato metoda uplatněna, jednak proto, že materiál je citlivý na nadměrnou vlhkost (absorbuje a bobtná), a též proto, že sekundární obal krytí tvoří vysokodenzitní netkaný polyethylen (TYVEK®), který se nehodí pro sterilizaci teplem.
Pro termolabilní látky může být alternativou ionizující záření. V současné době patří tato metoda mezi základní pro sterilizaci zdravotnických prostředků (šicí materiál, implantáty aj.). Vystavení materiálu působení γ-záření z vhodného zdroje (např. kobalt-60) nebo svazku elektronů o vysoké energii vycházejících z vhodného urychlovače elektronů (β-záření) v odpovídajících dávkách (nejčastěji 25 kGy) zaručuje sterilitu produktu2). Nicméně se nehodí pro sterilizaci všech typů polymerů, protože i minimální dávky ionizujícího záření mohou způsobit změny v polymerních řetězcích3). Z hlediska citlivosti na ionizující záření se polymery značně liší, a je obtížně předpovědět jejich vlastnosti po ozáření. γ - a β-záření se liší hloubkou a rychlostí penetrace do materiálu, avšak účinky na fyzikální či mechanické vlastnosti jsou podobné (degradace, štěpení řetězců, změna zesítění), např. je známo, že u kolagenu působí γ-záření fragmentaci řetězců, v důsledku čehož vznikají sloučeniny o nižší molekulové hmotnosti s horšími mechanickými vlastnostmi1).
Sterilizace plynem (převážně ethylenoxidem – EtO) představuje další možnost pro polymery citlivé na teplotu a vlhkost. EtO má dostačující účinnost při nižších teplotách, snadno penetruje do materiálu a je kompatibilní s širokou škálou látek. Umožňuje rychlou a spolehlivou inaktivaci bakteriálních zárodků narušením enzymových systémů a DNA. EtO je však hořlavý a výbušný, může reagovat s řadou funkčních skupin; rovněž rezidua plynu v zdravotnických prostředcích může ohrozit jejich biokompatibilitu, proto je nezbytné důkladné odvětrání sterilizovaného materiálu2).
O možném vlivu ionizujícího záření na CMC bylo pojednáváno v řadě výzkumných prací, i když se pokusy většinou týkaly CMC v jiné formě než textilního krytí, např. v podobě roztoku4), či ve formě tuhé nebo polotuhé5, 6). Nepodařilo se však najít zdroje věnované vlivu EtO na vlastnosti CMC.
Cílem této práce bylo posoudit stabilitu vzorků CMC ve formě textilního krytí při použití různého způsobu sterilizace a následně posoudit stabilitu sterilizovaných vzorků po ukončení zrychlené a dlouhodobé stabilitní studie.
Pokusná část
Materiál
Vzorky karboxymethylcelulosy ve formě plošného krytí určeného k hojení ran dodala firma Holzbecher spol. s r.o. barevna a bělidlo Zlíč. U testovaných vzorků (tab. 1) se v rámci stabilitní studie hodnotil vliv různých typů sterilizace (γ-záření, β-záření, EtO) a vliv dlouhodobého skladování (zrychlená a dlouhodobá stabilitní studie).
Table 1. Testované vzorky CMC a jejich stupeň substituce (DS) 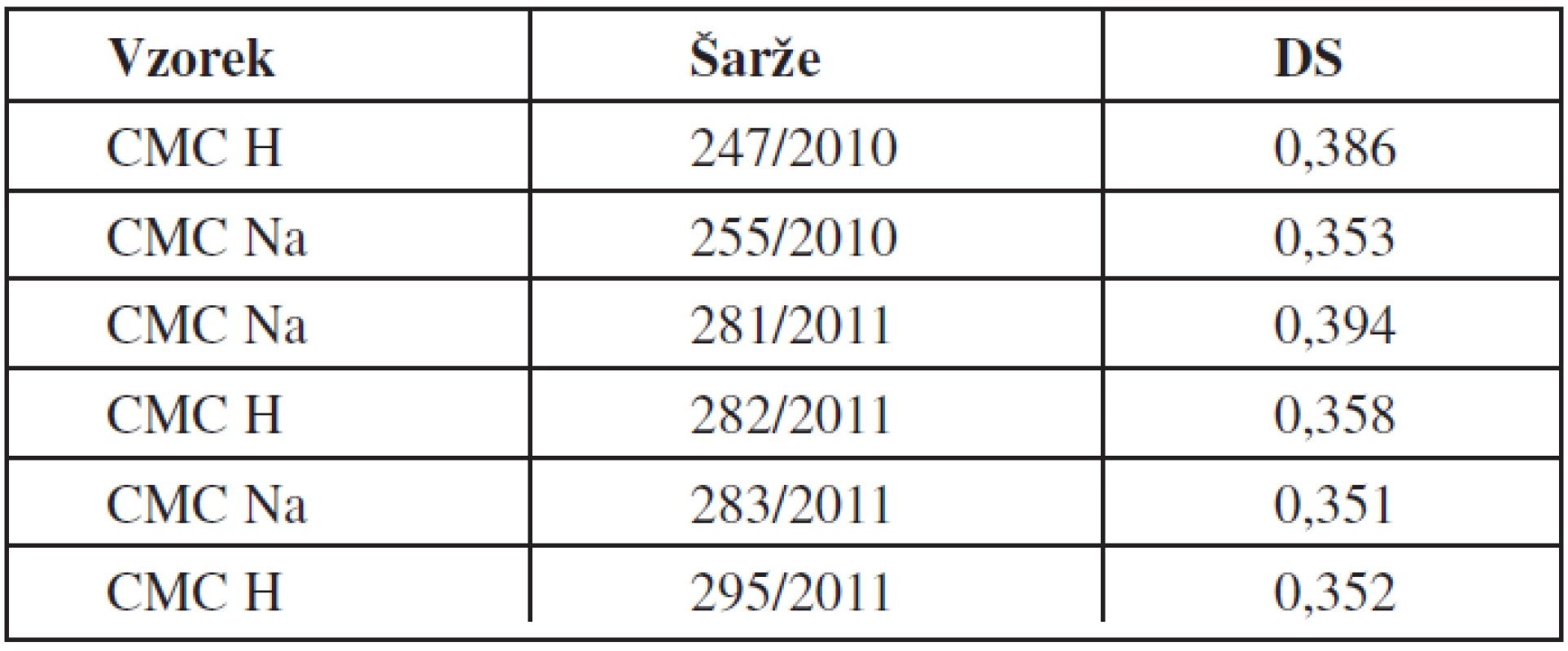
Sterilizace vzorků
Sterilizace γ-zářením byla provedena firmou Bioster, a.s., Česká republika. Jako zdroj záření byl použit radioizotop Co-60, technické zařízení pro sterilizaci dodala firma Atomic Energy of Canada (nyní Nordion International). Celková obdržená dávka po jednom ozáření byla 25 kGy, vzorky, které prošly dvěma cykly sterilizace, obdržely dávku 50 kGy.
Sterilizace β-zářením byla provedena firmou BGS BETA-GAMMA-SERVICE GmbH&Co., Německo. Jako zdroj záření byl použit 10 MeV urychlovač elektronů. Absorbovaná dávka neklesla pod 25 kGy, průměrná absorbovaná dávka byla 26,8 kGy.
Sterilizace ethylenoxidem byla provedena firmou DINA-HITEX, s r.o., Česká republika. Sterilizace probíhala ve vakuovém sterilizačním zařízení výrobce Mallet division de C.A.T.S., Francie, objem sterilizační komory 14,5 m3. Vzorky byly předkondicionovány v předehřívací místnosti po dobu 12 hodin při teplotě 50 °C a vlhkosti 50 %. Samotná sterilizace probíhala při teplotě 50 °C a vlhkosti 50 % v podtlakové sterilizační komoře (hodnota dosaženého vakua 125 mbar). Jako sterilizační médium byl použit N-plyn (100% ethylenoxid) v množství 12 kg, doba působení plynu byla 4 hodiny. Po sterilizačním cyklu následovalo větrání v komoře složené z osmi proplachovacích cyklů (každý cyklus 20 minut) při 50 °C a následně 3 dny v desorpčním prostoru při teplotě 35 °C.
Zrychlená a dlouhodobá stabilitní studie
Při zrychlené stabilitní studii byly vzorky sterilizované γ-zářením dávkou 25 kGy a uchovávány po dobu 6 měsíců při teplotě 40 °C a relativní vzdušné vlhkosti 75 %. Při dlouhodobé stabilitní studii byly vzorky sterilizované γ-zářením dávkou 25 kGy a uchovávány po dobu 12 měsíců při teplotě 25 °C a relativní vzdušné vlhkosti 60 %.
Rozměrově vylučovací chromatografie (Size exclusion chromatography, SEC)
Změny v testovaných vzorcích byly hodnoceny s využitím rozměrově vylučovací chromatografie. Rozpouštění vzorků bylo provedeno následujícím způsobem: Vzorky byly ponechány v malém množství čištěné vody při teplotě –20 °C po dobu 24 hodin. Po rozmrznutí byly vzorky rozpuštěny v roztoku NaOH o koncentraci 4,0 mol . l-1 a doplněny čištěnou vodou na výslednou koncentraci NaOH ve vzorku 2,0 mol . l-1. Takto připravené roztoky byly míchány po dobu 24 hodin za laboratorní teploty. Před provedením chromatografické separace byly vzorky 10krát naředěny čištěnou vodou na výslednou koncentraci karboxymethylcelulosy 0,1 mg . ml-1 a zfiltrovány přes membránový filtr o velikosti pórů 0,45 μm. Vzorky se připravovaly před každým měřením vždy čerstvé.
Pro stanovení se použil vysokoúčinný kapalinový chromatograf HP 1100 (Agilent Technologies, USA) s kvarterní pumpou, automatickým dávkovačem a refraktometrickým detektorem. Chromatografická separace byly provedeny na koloně Shodex OHpak SB-806M HQ (300 × 0,8 cm; velikost částic 13 μm) s předkolonou Shodex OHpak SB-G (50 × 0,6 cm). Jako mobilní fáze byl použit 0,1 mol . l-1 roztok NaCl v čištěné vodě, rychlost průtoku mobilní fáze byla 0,5 ml . min-1, teplota kolony byla 25 °C. Velikost nástřiku vzorku byla 100 μl. Celková délka analýzy byla 40 minut.
Statistické zpracování výsledků
Rozdíly mezi analyzovanými vzorky byly hodnoceny na základě srovnání retenčních časů píku karboxymethylcelulosy. Statistické hodnocení se provedlo metodou ANOVA na hladině významnosti α = 0,01 (počet vzorků n = 3).
Výsledky a diskuze
Hodnocené vzorky CMC (tab. 1) se odlišovaly způsobem sterilizace (γ-záření, β-záření, EtO). Vliv sterilizace γ-zářením se hodnotil u tří šarží, 281/2011, 283/2011 a 295/2011. Všechny tři vzorky obdržely výslednou dávku záření 25 kGy, u šarží 295/2011 a 281/2011 se testoval také vliv opakované sterilizace s celkovou obdrženou dávkou záření 50 kGy. U všech šarží byl zjištěn statisticky významný rozdíl mezi vzorkem nesterilizovaným a vzorkem sterilizovaným γ-zářením. Na obrázku 1 je dobře patrný posun píku k vyšším retenčním časům u sterilizovaného vzorku, což ukazuje na změnu velikosti makromolekuly karboxymethylcelulosy. Také mezi vzorkem sterilizovaným dávkou 25 kGy a vzorkem sterilizovaným dávkou 50 kGy byl zjištěn statisticky významný rozdíl (295/2011), který potvrdil vliv obdržené dávky záření na stabilitu produktu. Toto zjištění bylo ověřeno i analýzou vzorku 281/2011 po aplikaci dávky 25 kGy a 50 kGy (tab. 2). Vzhledem k očekávaným výsledkům byly vzorky šarže 281/2011 měřeny pouze 1krát.
Table 2. Vliv sterilizační metody na stabilitu vzorků CMC 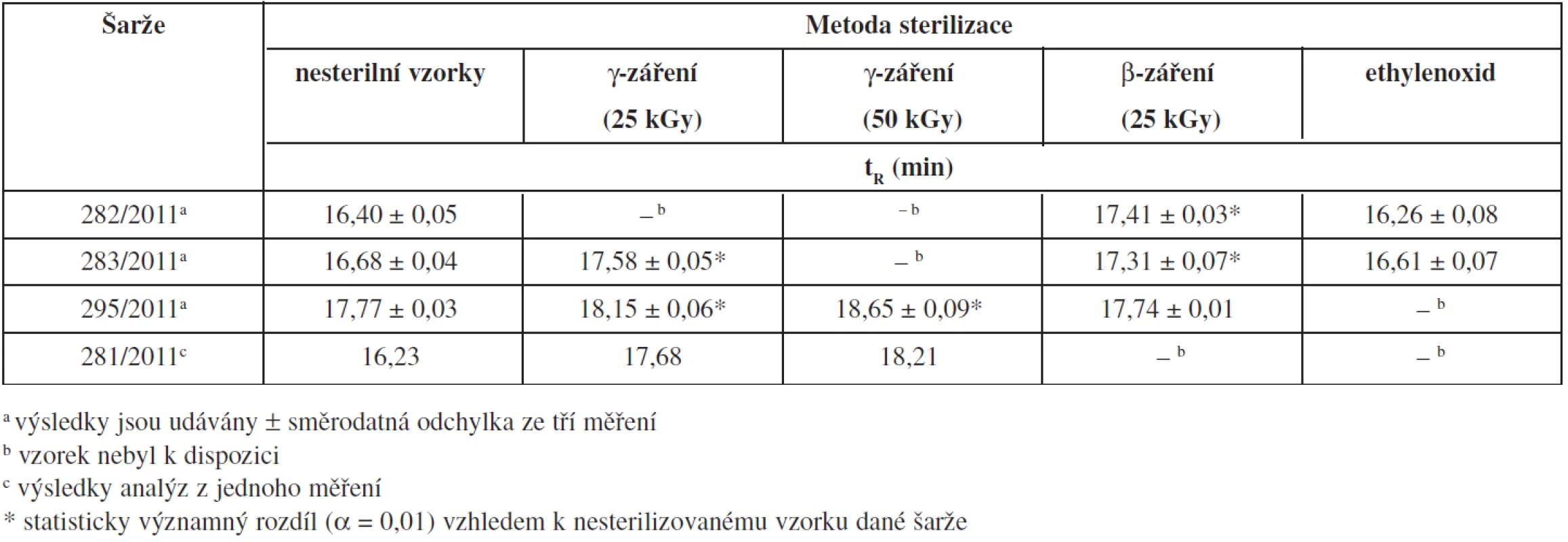
Image 1. Chromatogramy vzorků CMC Na šarže 283/2011 sterilizovaných γ-zářením (− ·−), β-zářením (−··−), ethylenoxidem (---) a nesterilizovaných (—) 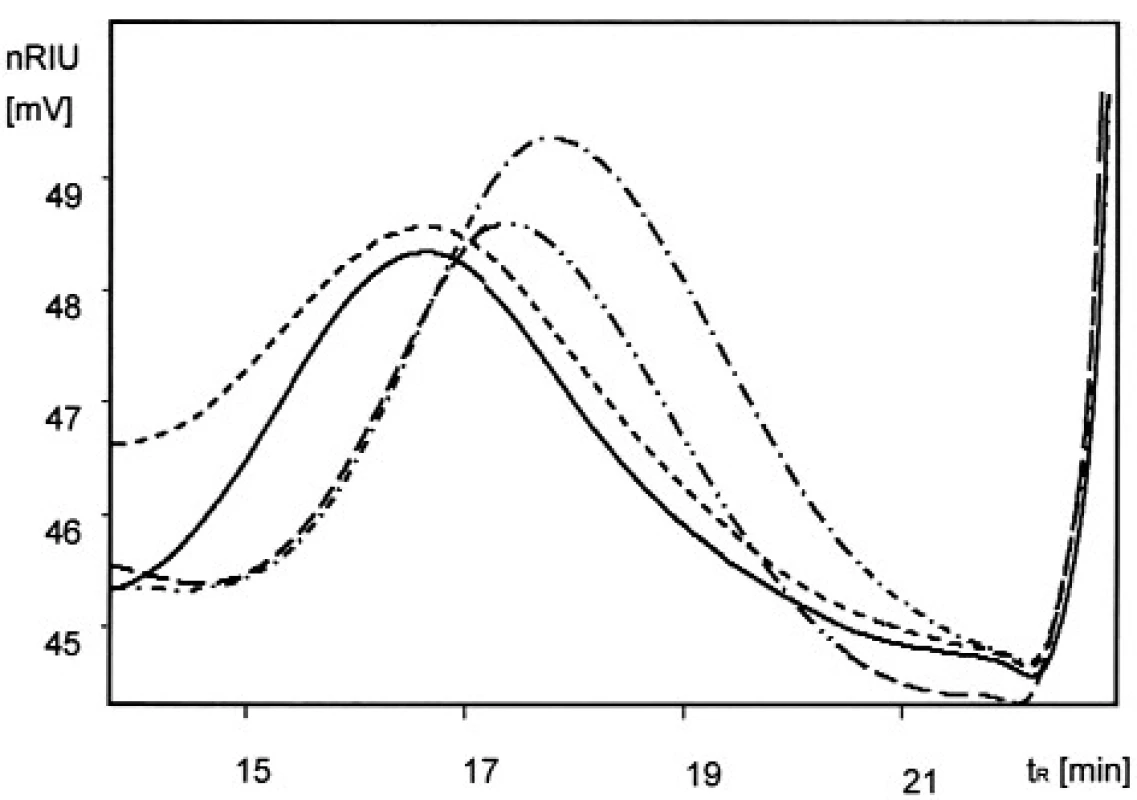
Vliv sterilizace β-zářením se hodnotil u tří šarží, 282/2011, 283/2011 a 295/2011. Všechny tři vzorky obdržely výslednou dávku záření 25 kGy. U šarží 282/2011 a 283/2011 byl zjištěn statisticky významný rozdíl mezi nesterilizovaným vzorkem a vzorkem sterilizovaným β-zářením. I zde je patrný posun píku vzorku na chromatogramu směrem k vyšším retenčním časům (obr. 1), což odpovídá změnám velikosti makromolekuly karboxymethylcelulosy. U šarže 295/2011 nebyl zjištěn statisticky významný rozdíl mezi vzorkem nesterilizovaným a sterilizovaným β-zářením (tab. 2).
Tyto výsledky odpovídají poznatkům publikovaným v dostupné literatuře, kde při sterilizaci roztoků karboxymethylcelulosy stejnou dávkou γ - a β-záření jako v tomto experimentu byl sledován pokles jejich viskozity, která přímo souvisí s velikostí makromolekuly. Dle údajů z literatury byl pokles viskozity u vzorků sterilizovaných γ-zářením více než 90%, u vzorků sterilizovaných β-zářením klesla viskozita přibližně o 70 %4, 7, 8).
Vliv sterilizace ethylenoxidem se sledoval u šarží 282/2011 a 283/2011. Ani u jedné z testovaných šarží nebyl nalezen statisticky významný rozdíl mezi nesterilizovaným a sterilizovaným vzorkem (tab. 2).
Z uvedených výsledků lze vyvodit, že ze všech tří testovaných způsobů představuje sterilizace ethylenoxidem nejšetrnější metodu z pohledu degradace polymerní molekuly CMC. EtO je však schopen reagovat s řadou funkčních skupin za vzniku různých derivátů. Stanovení takovýchto produktů bude součástí dalšího testování studovaných vzorků. Dále bude třeba posoudit, zda pozorované změny v případě sterilizace γ - nebo β-zářením mají významný vliv na ostatní (fyzikální, mechanické) vlastnosti produktu, např. schopnost pojmout dostatečné množství tekutiny, pevnost výsledného krytí nebo schopnost nelepit se k ráně.
V další části práce se sledoval vliv dlouhodobého skladování na stabilitu vzorků CMC (šarže 247/2010 a 255/2010) sterilizovaných γ-zářením. Po sterilizaci se vzorky umístily do stabilitních boxů za podmínek dlouhodobé a zrychlené stabilitní studie. Výsledky těchto hodnocení uvádí tabulka 3. Zrychlený test je část stabilitní studie prováděná za extrémních skladovacích podmínek a slouží k urychlení fyzikálních a chemických změn produktu. Lze ho použít také pro ověření stability přípravku při krátkodobém skladování mimo navržené podmínky (např. při přepravě)9). Ani u jedné z testovaných šarží nebyl nalezen statisticky významný rozdíl mezi původním vzorkem a vzorkem ze zrychlené stabilitní studie. Dlouhodobé stabilitní testy se provádějí za doporučených podmínek skladování pro určení doby použitelnosti9). Ani u jedné z testovaných šarží nebyl nalezen statisticky významný rozdíl mezi původním vzorkem a vzorkem z dlouhodobé stabilitní studie. Ze získaných výsledků vyplývá, že i v případě použití sterilizace γ-zářením nedochází ve vzorcích CMC k dalším degradačním změnám a jsou vhodné pro dlouhodobé skladování.
Table 3. Výsledky hodnocení vzorků CMC ze stabilitních studií 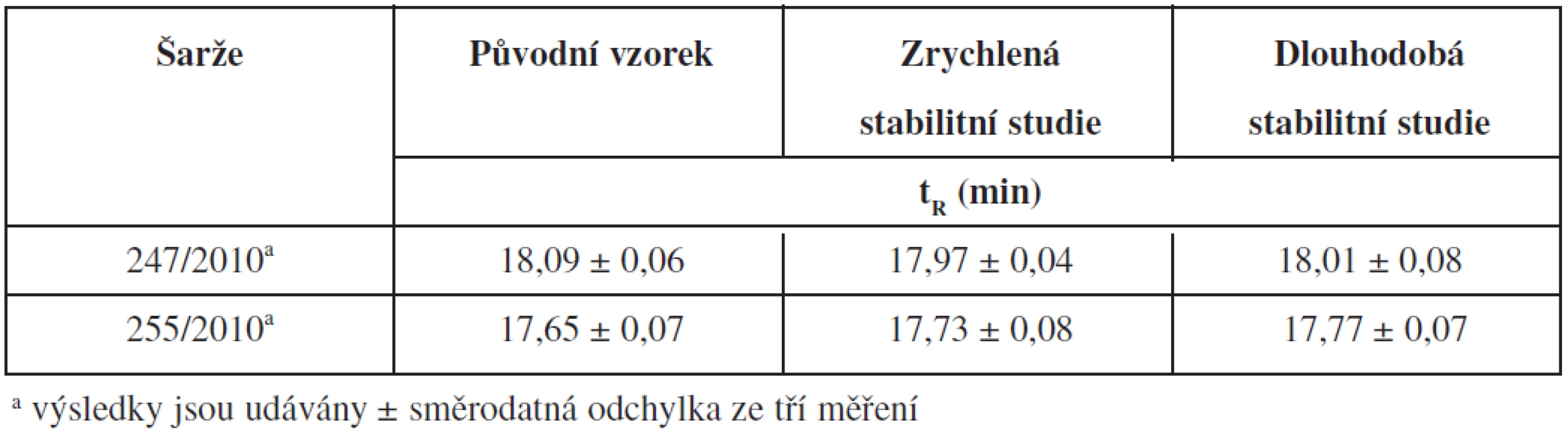
Výsledky práce byly získány za finančního přispění TA ČR v rámci řešení projektu programu ALFA č. TA01010244.
Střet zájmů: Experiment se prováděl ve spolupráci s firmou Holzbecher spol. s r.o. barevna a bělidlo Zlíč v rámci společného řešení uvedeného projektu.
Došlo 20. února 2013 / Přijato 7. března 2013
Mgr. Jan Muselík, Ph.D., R. Masteiková
Veterinární a farmaceutická univerzita Brno, Farmaceutická fakulta, Ústav technologie léků
Palackého 1/3, 612 42 Brno
e-mail: muselikj@vfu.cz
L. Wojnarová
Lékárna Sfinx, Brno
T. Sopuch
Holzbecher spol. s r.o. barevna a bělidlo Zlíč, divize Holzbecher Medical
Sources
1. Wiegand C., Abel M., Ruth P., Wilhelms T., Schulze D., Norgauer J., Hipler U.-C. Effect of the sterilization method on the performance of collagen Type I on chronic wound parameters in vitro. Biomed. Mater. Res. Part B 2009; 90B, 710–719.
2. Labarre D., Ponchel G., Vauthier C. Biomedical and Pharmaceutical Polymers. 1st ed. London: Pharmaceutical Press 2010.
3. Bushell J. A., Claybourn M., Williams H. E., Murphy D. M. An EPR and ENDOR study of γγ - and ββ-radiation sterilization in poly(lactide-co-glycolide) polymers and microspheres. J. Control. Release 2005; 110, 49–57.
4. Choi J. I., Lee H. S., Kim J. H., Lee K. W., Lee J. W. Seo S. J., Kang K. W., Byun M. W. Controlling the radiation degradation of carboxymethylcellulose solution. Polym. Degrad. Stabil. 2008; 93, 310–315.
5. Fei B., Wach R. A., Mitomo H., Yoshi, F., Kume T. Hydrogel of biodegradable cellulose derivatives. I. Radiation-induced crosslinking of CMC. J. Appl. Polym. Sci. 2000; 78, 278–283.
6. Liu P., Zhai M., Li J., Peng J., Wu J. Radiation preparation and swelling behavior of sodium carboxymethyl cellulose hydrogels. Rad. Phys. Chem. 2002; 63, 525–528.
7. Lee H. S., Choi J. I., Kim J. H., Lee K. W., Chung Y. J., Shin M. H., Byun M. W., Shin M. G., Lee J. W. Investigation on radiation degradation of carboxymethylcellulose by ionizing irradiation. Appl. Radiat. Isotopes 2009; 67, 1513–1515.
8. Choi J. I., Lee H. S., Kim J. H., Lee K. W., Chung Y. J., Byun M. W., Lee J. W. Effect of electron beam irradiation on the viscosity of carboxymethylcellulose solution. Nucl. Instrum. Meth. B 2008; 266, 5068–5071.
9. Vetchý D., Frýbortová K., Rabišková M., Häring A. Testování stability léčivých přípravků. Chem. Listy. 2006; 100, 24–29.
Labels
Pharmacy Clinical pharmacology
Article was published inCzech and Slovak Pharmacy

2013 Issue 2-
All articles in this issue
-
Fyziologické aspekty lipoxygenázy v signálnych systémoch rastlín
Časť I. Oktadekánová cesta - Pokroky ve využití instrumentálního měření barevnosti ve vývoji, výrobě a v kontrole jakosti léčiv, léčivých přípravků a farmaceutických pomocných látek I
- Vliv stupně substituce na nasákavost kyselé formy karboxymethylcelulosy v podobě netkané textilie
- Hodnocení vlivu sterilizační metody na stabilitu karboxymethylcelulosového krytí na rány
- Prolegomenon of the Czech pharmacognosy: 21st century
- Optimalizace disolučního profilu diklofenaku sodné soli z halloysitových nanotubulů
- Thiosemikarbazony a jejich antimykobakteriální účinky
- Estery aminopyrazinkarboxylové kyseliny jako potenciální antimykobakteriální léčiva
-
Fyziologické aspekty lipoxygenázy v signálnych systémoch rastlín
- Czech and Slovak Pharmacy
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Hodnocení vlivu sterilizační metody na stabilitu karboxymethylcelulosového krytí na rány
- Prolegomenon of the Czech pharmacognosy: 21st century
-
Fyziologické aspekty lipoxygenázy v signálnych systémoch rastlín
Časť I. Oktadekánová cesta - Vliv stupně substituce na nasákavost kyselé formy karboxymethylcelulosy v podobě netkané textilie
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

