-
Medical journals
- Career
Optimalizácia extrakčnej metódy na stanovenie metadónu a jeho metabolitu EDDP v moči plynovou chromatografiou
: R. Horáková; J. Valentová; I. Pechová; F. Devínsky
: Univerzita Komenského Bratislava, Farmaceutická fakulta, Katedra chemickej teórie liečiv
: Čes. slov. Farm., 2008; 57, 265-268
: Original Articles
Cieľom práce bolo vypracovať extrakčnú metódu na stanovenie metadónu a jeho metabolitu EDDP v moči s použitím plynovej chromatografie (GC) vybavenej špecifickým dusíkovým detektorom (NPD). Extrakčná metóda bola optimalizovaná s cieľom získať čo najlepšiu výťažnosť stanovovaných zlúčenín z moču. Optimálne výsledky boli dosiahnuté alkalickou extrakciou (~ pH 9) s dietyléterom, kde ako vnútorný štandard bol použitý proadifén (PA). Stanovená bola výťažnosť extrakcie pre metadón (MTD) 91 ± 5 % a pre jeho metabolit EDDP 86 ± 5 %. Limit detekcie (LOD) pre MTD je 8 ng/ml moču, pre EDDP 23 ng/ml moču a limit kvantifikácie (LOQ) je pre MTD 27 ng/ml moču a pre metabolit EDDP 77 ng/ml moču. Presnosť metódy v rámci jedného dňa sa pohybovala pre MTD v rozmedzí 1,1–2,32 %, pre EDDP 7,3–9,3 % a presnosť metódy v rámci troch dní pre MTD bola 9,1–13,7 %, pre EDDP 4,7–8,7 %.Vhodnosť metódy pre rutinné monitorovanie metadónu a jeho metabolitu EDDP v moči bola overená na 5 vzorkách pacientov zúčastňujúcich sa metadónového udržiavacieho programu.
Kľúčové slová:
metadón (MTD) – 2-ethylidene-3,3-diphenyl-1,5-dimethylpyrrolidine (EDDP) – moč – GC/NPDÚvod
Metadón (MTD) ako jedna zo substitučných zlúčenín sa používa pri liečbe závislosti na opiátoch, no najmä na heroíne 1). Patrí medzi syntetické opiáty pôsobiace na μ a δ opioidné receptory 2).Stanovenie metadónu (4,4-difenyl-6-(N,N-dimetylamino)heptán-3-ónu) a jeho metabolitu 2 etylidén-1,5-dimetyl-3,3-difenylpyrolidínu (EDDP) v moči a ďalších biologických tekutinách je dôležitou súčasťou odvykacieho programu pri liečbe drogových závislostí. Pomáha pri optimalizácii terapeutickej dávky metadónu a pri kontrole liečby drogovo závislých pacientov. Metadónový udržiavací program bol po prvýkrát zahájený v USA v roku 1964 3). Metadón možno podávať intravenózne, ale aj perorálne v tekutej forme alebo v tabletkách. Má dlhodobý účinok, a preto ho stačí podávať liečeným pacientom 1×denne. Vyznačuje sa pomalým ustálením maximálnej hladiny v krvi (4 hodiny) a dlhým biologickým polčasom (10–18 hodín). Na trhu je známy pod firemnými označeniami Physepton, Polamidon, Macodin. Účinná dávka je determinovaná ako dávka primeraná na prevenciu abstinenčného syndrómu a pohybuje sa v rozmedzí od 60–700 mg/deň 4).
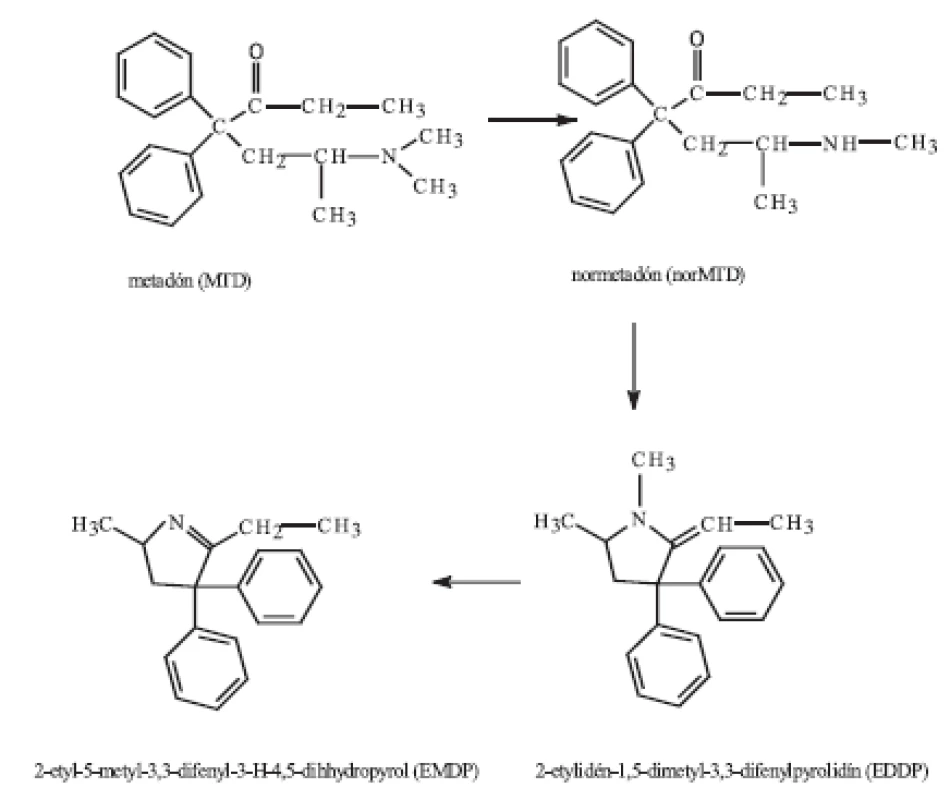
Metadón v organizme podlieha intenzívnej metabolizácii, pri ktorej okrem farmakologicky aktívneho metabolitu normetadónu (nachádza sa v krvi) vznikajú i inaktívne metabolity 2-etylidén-1,5-dimetyl-3,3-difenylpyrolidín (EDDP) a 2-etyl-5-metyl-3,3-difenyl-3-H-4,5-dihydropyrol (EMDP) (obr. 1) 5). Hlavný metabolit EDDP ako i EMDP sú vylučované močom a ich eliminácia spolu s metadónom je závislá od pH moču.
Stanovenie množstva metadónu ako i jeho metabolitov v biologických vzorkách si vyžaduje citlivú a špecifickú analytickú metódu. V súčasnosti publikované metódy zahŕňajú ako analytické metódy tenkovrstvovú chromatografiu (TLC) 6, 7), vysokoúčinnú kvapalinovú chromatografiu (HPLC) 8–10), plynovú chromatografiu (GC) 5, 11–17), v ktorej najčastejšie používanými detektormi sú plameňovo-ionizačný detektor (FID), detektor elektrónového záchytu (ECD), hmotnostný detektor (MSD), alebo termoionizačný dusíkovo-fosforečný detektor (NPD).
POKUSNA ČASŤ
Chemikálie
Metadónium chlorid bol od UNODC (Viedeň, Rakúsko) 2-etylidén-1,5-dimetyl-3,3-difenylpyrolidín (EDDP), proadifénium chlorid (vnútorný štandard 1 – IS 1) ako aj imipramínium chlorid (vnútorný štandard 2 – IS 2) boli od firmy Sigma (Steinheim, Germany), ich príslušné bázy boli pripravené v laboratóriu. Všetky ďalšie použité chemikálie a rozpúšťadlá boli analyticky čisté od firmy Merck (Darmstadt, Germany) a dietyléter od firmy Slavus (Bratislava, Slovensko), bol predestilovaný pred použitím.
Predúprava vzoriek
Na predúpravu vzoriek sa použili tri extrakčné metódy, označené A, B a C.
Metóda A
K 1 ml moču v zábrusových skúmavkách sa pridalo vypočítané množstvo metadónu (5 μg, 15 μg a 30 μg/ml), EDDP (15 μg, 25 μg a 50 μg/ml) a konštantné množstvo vnútorného štandardu (proadifénu, 15 μg/ml – IS 1 a imipramínu, 25 μg/ml – IS 2).
Do každej skúmavky sa pridalo 50 μl (5 mol/dm) vodného roztoku HCl, 0,5 ml (1 mol/dm) vodného roztoku K2CO3 a 5 ml zmesi hexán : izobutylalkohol (99 : 1, v/v). Obsah skúmaviek sa miešal 20 min na mechanickej trepačke a následne sa centrifugoval 10 minút pri 2500 ot/min. Vrchná organická vrstva sa odpipetovala do ďalšej skúmavky a odparila sa pod prúdom dusíka do sucha. Odparok sa kvantitatívne preniesol do vialky v 2× 500 μl metanolu.
Metóda B
K 1 ml moču v zábrusových skúmavkách sa pridalo vypočítané množstvo metadónu (5 μg, 15 μg a 30 μg/ml), EDDP (15 μg, 25 μg a 50 μg/ml), konštantné množstvo vnútorného štandardu (proadifénu, 15 μg ×ml – IS 1 a imipramínu, 25 μg/ml – IS 2), 1 ml 26% amoniaku a 5 ml chloroformu. Obsah skúmaviek sa následne premiešal 20 min na mechanickej trepačke a následne sa centrifugoval 10 minút pri 2500 ot/min. Po odpipetovaní hornej organickej vrstvy sa vodná vrstva opätovne extrahovala 5 ml chloroformu vyššie uvedeným postupom. Organické vrstvy sa spojili a vysušili bezvodým Na2SO4. Po odstránení sušidla sa z organickej vrstvy odparilo rozpúšťadlo pod prúdom dusíka a odparok sa preniesol do vialky v 2× 500 μl metanolu.
Metóda C
K 1 ml moču v zábrusových skúmavkách sa pridalo vypočítané množstvo metadónu (5 μg, 15 μg a 30 μg/ml), EDDP (15 μg, 25 μg a 50 μg/ml) a konštantné množstvo vnútorného štandardu (proadifénu, 15 μg/ml – IS 1 a imipramínu, 25 μg/ml – IS 2). Vzorka moču sa upravila 1 ml boraxového tlmivého roztoku na pH 9 a následne sa extrahovala 5 ml dietyléteru. Obsah skúmaviek sa miešal na mechanickej trepačke 20 min a centrifugoval 10 minút pri 2500 ot/min. Éterická vrstva sa premyla 0,5 ml destilovanej vody, vysušila sa bezvodým Na2SO4 a odparila sa do sucha pod prúdom dusíka. Odparok sa preniesol do vialky v 2× 500 μl metanolu.
Plynová chromatografia
Chromatografické analýzy boli uskutočnené na plynovom chromatografe HP 5890 Series II s NP detektorom v splitless režime.
Nosný plyn: hélium (tlak: 9,8 psi, prietok: 0,3 ml/min a rýchlosť: 30,0 cm/sec).
Zažíhacie plyny pre NPD: vodík, hélium a vzduch (prietoky: 20,0; 150,0 a 3,5 ml/min). Teplota injektora a NP detektora: 220 °C.
Kolóna: ULTRA 2 (12 m/0,2 mm/0,33 μm) so stacionárnou fázou tvorenou s 95 % dimetylsiloxánu a 5 % difenylsiloxánu.
Teplotný program GC: 100 °C – 1 min – 20 °C min – 300 °C – 2 min.
Celkový čas analýzy bol 13 minút. Vzorka sa dávkovala v objeme 1 μl.
VÝSLEDKY A DISKUSIA
Príprava vzoriek na analýzu tvorí často problémovú a kritickú časť analýzy liečiv a ich metabolitov. Najčastejšie používaným postupom na odstránenie nežiadúcich prímesí a látok zo vzorky nachádzajúcej sa v biologickom či inom materiály je extrakcia. Počas práce sa odskúšali tri metódy extrakcie kvapalina-kvapalina, tzv. liquid-liquid extrakcia (LLE) na stanovenie metadónu a jeho metabolitu EDDP v moči, označené ako metóda A, B a C. Na základe nameraných hodnôt štandardov a vzoriek moču boli vypočítané účinnosti extrakcie pre jednotlivé koncentrácie MTD a EDDP pre všetky tri extrakčné metódy. Pre lepšiu detegovateľnosť a citlivosť na GC/NPD sa pri validácii najlepšej extrakčnej metódy (metóda C) použil ako vnútorný štandard proadifén. Výsledky sú v tabuľke 1.
1. Účinnosť extrakcií z kvapaliny do kvapaliny pre metadón a EDDP z moču (n = 5) 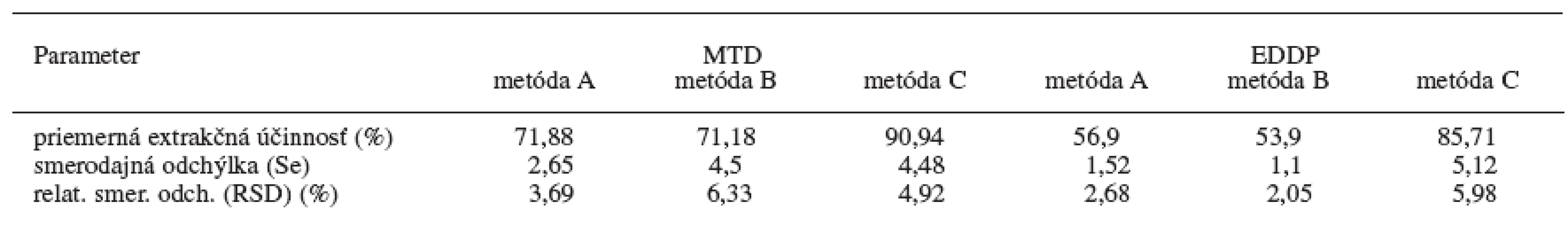
Z uvedených údajov (tab. 1) vyplýva, že najlepšie výsledky extrakčnej účinnosti pri daných koncentráciách MTD a EDDP za použitia proadifénu ako vnútorného štandardu sú pri extrakčnej metóde C, kde ako extrakčné činidlo sa použil dietyléter a na vysolenie analytu z moču chlorid sodný. U tejto metódy sa hodnotila následne presnosť a správnosť metódy pre stanovenie MTD a EDDP v moči pomocou GC/NPD v rámci jedného dňa a troch dní (tab. 2). Limitom detekcie pre MTD je 8 ng/ml moču a limitom kvantifikácie pre MTD je 27 ng/ml moču. Limitom detekcie pre EDDP je 23 ng/ml moču a limitom kvantifikácie pre MTD je 77 ng/ml moču. Relatívna štandardná odchýlka pre jednotlivé koncentrácie MTD je v rozsahu 1,10–2,32 % v rámci jedného dňa a 9,14–13,72 % troch dní. Relatívna štandardná odchýlka pre jednotlivé koncentrácie EDDP je v rozsahu 7,26 až 9,29 % v rámci jedného dňa a 4,72–8,73 % troch dní.
2. Presnosť a správnosť metódy C 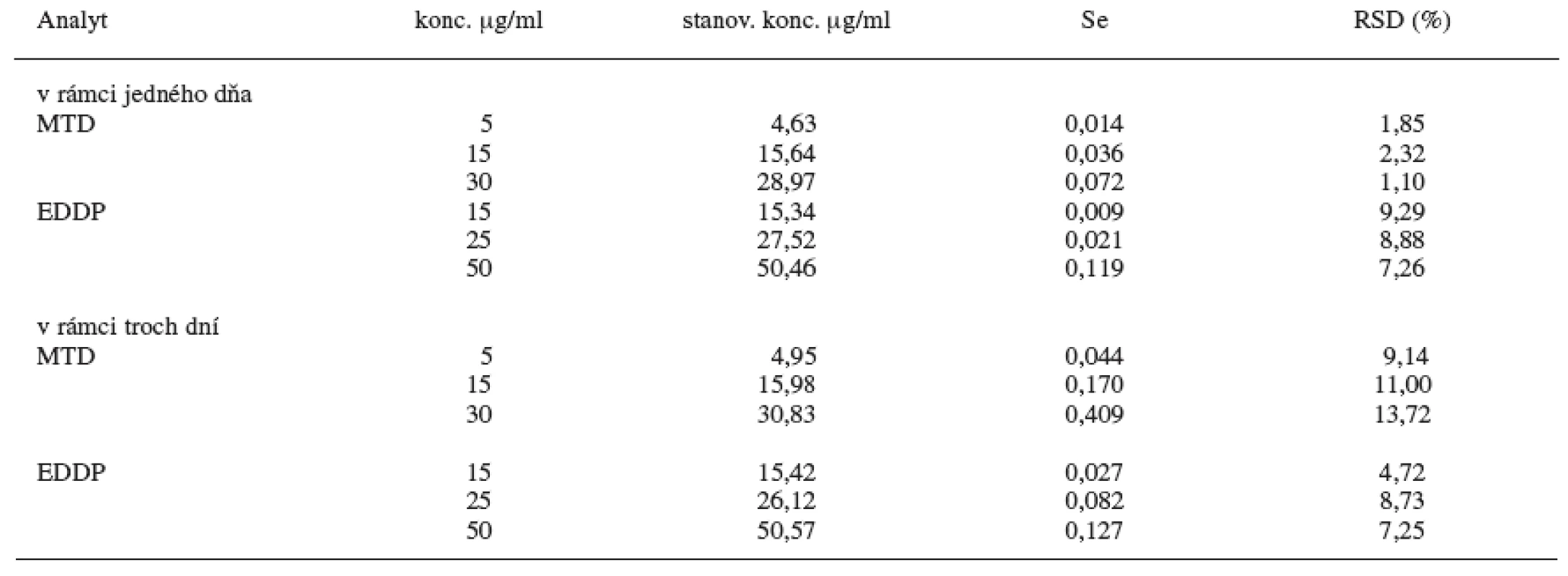
Podľa validačných parametrov vykazuje táto nami zvolená metóda na stanovenie metadónu a jeho metabolitu EDDP v moči pomocou GC/NPD správne a reprodukovateľné výsledky.
Pre stanovenie MTD a EDDP v moči pomocou GC/NPD bola získaná z použitého koncentračného rozsahu pre MTD 0,5–50,0 μg/ml moču a pre EDDP 1,0–50,0 μg/ml moču kalibračná krivka. Korelačné koeficienty získané pre MTD a pre EDDP sú:
MTD : y = 0,0966x + 0,0032 (R2 = 0,9994)
EDDP : y = 0,0331x + 0,0722 (R2 = 0,9925)
Metóda bola následne použitá na 5 náhodne vybraných reálnych vzoriek moču pacientov z Centra pre liečbu drogovej závislosti v Bratislave a na základe kalibračnej krivky boli stanovené koncentrácie MTD a EDDP liečených pacientov pri odvykacej kúre z drogovej závislosti na heroíne. Výsledky hladín MTD a EDDP v reálnych vzorkách moču pacientov sú uvedené v tabuľke 3.
3. Hladiny MTD a EDDP v reálnych vzorkách moču pacientov z Centra pre liečbu drogovej závislosti v Bratislave 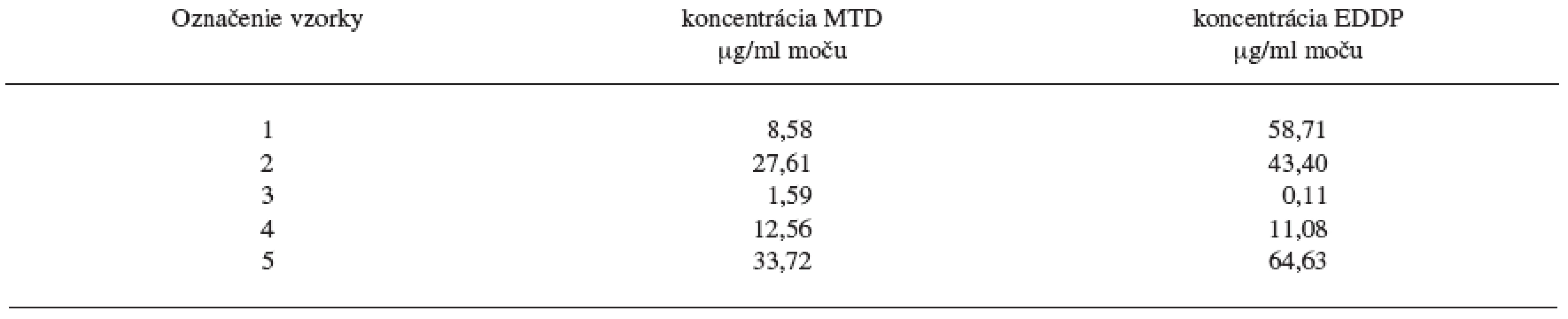
Ako môžeme vidieť z výsledkov reálnych vzoriek moču pacientov liečených z drogovej závislosti v Centre pre liečbu drogovej závislosti v Bratislave, extrakčná metóda C ako i následné stanovenie hladín MTD a EDDP v moči metódou GC/NPD je vhodné pre terapeutické stanovovanie vzoriek moču pacientov liečiacich sa z drogovej závislosti. Napriek veľkému rozptylu stanovených koncentrácii metadónu a jeho metabolitu EDDP v pacientských vzorkách moču je ešte stále stanovený obsah metadónu ako i EDDP v rozsahu stanovenia vytvorenej metódy na GC/NPD. Chromatografický záznam z GC/NPD vzorky moču pacienta 5 liečiaceho sa z drogovej závislosti pomocou substitučnej liečby metadónom je na obrázku 2.
2. Chromatografický záznam vzorky moča pacienta 5 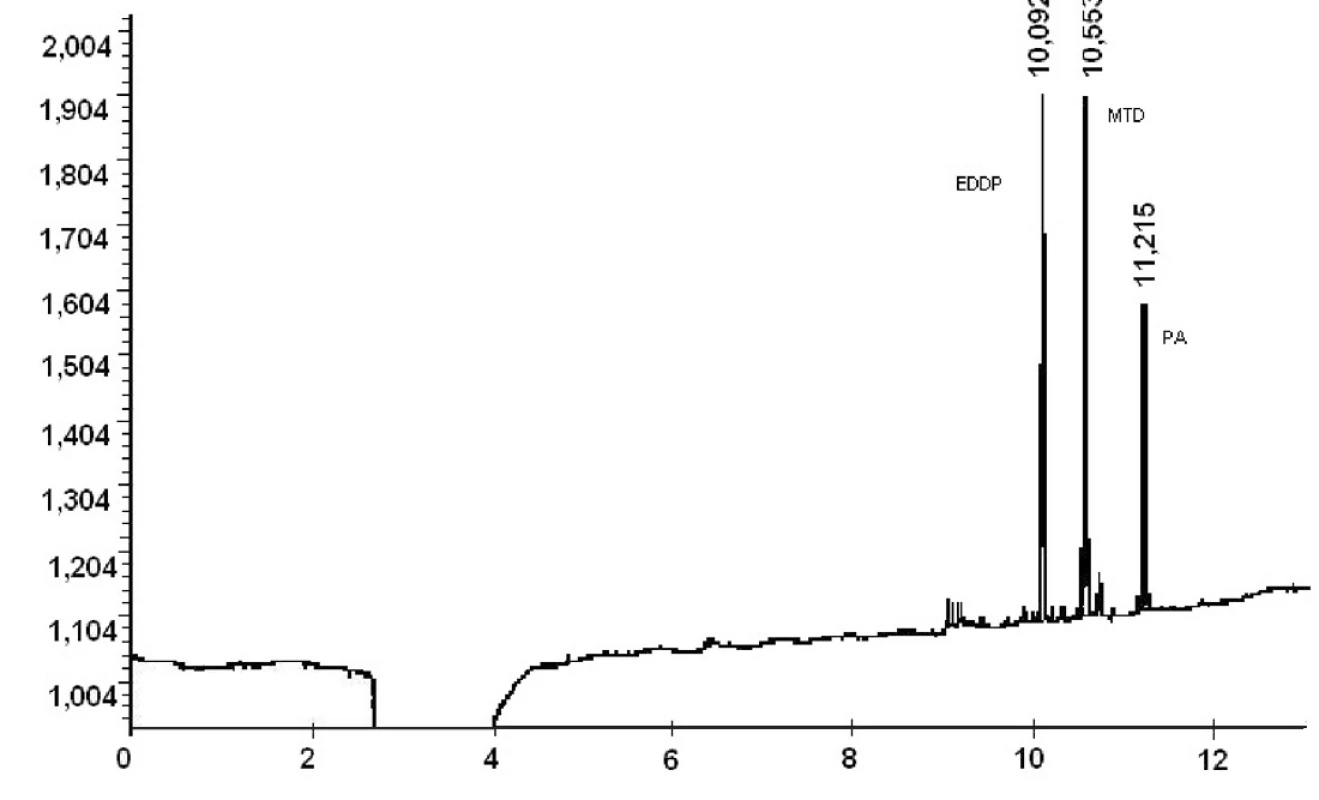
Táto práca bola riešená za podpory grantov VEGA č. 1/3416/06, 1/4300/07 a grantu APVV č. 20-030804.
Došlo 25. září 2008
Přijato 29. října 2008
Adresa pro korespondenci:
ing. Renáta Horáková
Katedra chemickej teórie liečiv FaF UK
Kalinčiakova 8, 832 32 Bratislava, Slovenská republika
e-mail: horakova@fpharm.uniba.sk
Sources
1. Pothier, J., Galand, N.: J. Chromatogr. A, 2005; 1080, 186–191.
2. Whelan, G., Lintzeris, N., McDonough, M. et al.: Methadone guidelines prescribers and pharmacists. 1. vydanie. Melbourne: State of Victoria, 2000; 7–15.
3. Kreek, M. J., Ann, N. Y.: Acad. Sci., 2000; 909, 186.
4. Eap, CH. B., Buclin, T., Bacmann, P.: Clin. Pharmacokinet., 2002; 41, 1153–1193.
5. Habrdová, V., Balíková, M.: Chem. Listy, 2002; 96, 1006–1009.
6. Misztal, G.: Acta Pol. Pharm., 1990; 47(5–6), 5–8.
7. Digiusto, E., Seres, V., Bibb, Z. A., Batey, R.: Addict. Behav., 1996; 21, 319–329.
8. Adams, P. S., Haines-Nutt, R. F.: J. Chromatogr., 1985; 329, 438–440.
9. Pierce, T. L., Murray, A. G. W., Hoff, W.: Science, 1992; 30, 443–447.
10. Choo, R. E., Murphy, C. M., Jones, H. E., Huestis, M. A.: J. Chromatogr. B, 2005; 814, 369–373.
11. Quintela, O., López, P., Bermejo, A.M., López-Rivadulla, M.: J. Chromatogr. B, 2006; 834, 188–194.
12. Müller, K.: Pharmazie, 1983; 38, 596–601.
13. Georgakopoulos, C. G., Kiburis, J. C.: Anal. Chem., 1991; 63, 2021–2004.
14. Schmidt, N., Still, R., Brune, K., Geisslinger, G.: Pharm. Research, 1993; 10 (3), 441–444.
15. Charotti, M., Marsili, R.: J. Microcol., 1994; 6, 577–580.
16. Balíková, M.: Remedia 1995; 5, 211–216.
17. Cooper, G. A. A., Oliver, J. S.: J. Anal. Toxicol., 1998; 22, 389–392.
Labels
Pharmacy Clinical pharmacology
Article was published inCzech and Slovak Pharmacy

2008 Issue 6-
All articles in this issue
- Consumption of hipolipidemics in the Czech Republic in 2000–2007
- Testing the effect of 2’, 3, 4’-trihydroxychalcone in experimental diabetes mellitus: a pilot study
- Determination of metoprolol and its metabolite α-hydroxymetoprolol in serum by HPLC method with fluorescence detection
- Studies of local anesthetics Part 185: Thermodynamic parameters of heptacainium chloride in the solution of NaBr
- Optimization of the extraction method for the determination of methadone and its metabolite EDDP in urine by gas chromatography
- The effect of lipophilic carrier concentration on hydrophilic-lipophilic matrix systems characteristics
- Possible effects on the liberation of alaptid from dermal semisolid preparations
- The effect of Crataegus extract on heart mitochondrial function
- Czech and Slovak Pharmacy
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Possible effects on the liberation of alaptid from dermal semisolid preparations
- Studies of local anesthetics Part 185: Thermodynamic parameters of heptacainium chloride in the solution of NaBr
- Optimization of the extraction method for the determination of methadone and its metabolite EDDP in urine by gas chromatography
- The effect of lipophilic carrier concentration on hydrophilic-lipophilic matrix systems characteristics
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career