-
Medical journals
- Career
Aplikace Dysportu® – možnost doprovodného vedlejšího efektu na postavení víček (klinicko-histologická studie)
Authors: J. Krásný; J. Šach
Authors‘ workplace: Ústav patologie 3. LF UK a FNKV, Praha, přednosta prof. MUDr. Václav Mandys, CSc. ; Oční klinika FNKV, Praha, přednosta prof. MUDr. Pavel Kuchynka, CSc.
Published in: Čes. a slov. Oftal., 68, 2012, No. 5, p. 216-220
Category: Original Article
Předneseno na XVI. Výročním sjezdu ČOS ve Špindlerově Mlýně, září 2008
Overview
Cíl:
Seznámit s možností negativního dopadu opakovaného podání derivátu botulotoxinu A na postavení víček se změnami jejich tkáňové struktury. Současně autoři podávají literární rozbor pozitivního a negativního vlivu tohoto neurotoxinu z medicínského hlediska.Materiál a metodika:
Na Oční klinice FN Královské Vinohrady v Praze byli v letech 2006 až 2008 chirurgicky ošetřeni tři pacienti po opakovaných aplikacích derivátů botulotoxinu A. Jednou se jednalo o oboustrannou ptózu horních víček a dvakrát byla indikací entropia s trichiázou dolních víček. Po anamnesticky udávané 10leté léčbě pro pracovní diagnózu blefarospazmu byla aplikací výše uvedeného léku u 65letého muže vyvolaná oboustranná symetrická ptóza. Vzhledem k následnému postižení m. frontalis i částečnému oslabení funkce levátorů víček byl stav postavení horních víček řešen plastikou aponeurózy s dobrým funkčním výsledkem. U dvou pacientek ve věku 72 a 90 let bylo indikací úspěšné chirurgické intervence trvale přetrvávající entropium dolních víček původně neefektivně řešené opakovanými intradermálními injekcemi přípravky na bázi botulotoxinu A.Výsledky:
Histologická vyšetření odebraných vzorků kůže a podkoží při plastikách entropií ukázala nepříznivé a ireverzibilní změny, mezi které patřilo zejména projizvení víčka a atrofie snopců příčně pruhovaného svalu.Závěr:
Indikace aplikace derivátů botulotoxinu v obličeji je nutno vždy dobře zvážit a volit správnou indikaci. Z očního hlediska je plně vhodnou diagnózou pouze blefarospazmus a relativní indikací je dočasně vyvolaná ptóza horního víčka uzavírající oční štěrbinu z důvodu prevence rohovkových změn u lagoftalmu různé etiologie jako eventualita tarzorafie. Vždy je nutno posoudit četnost aplikací, neboť opakovaně používaný derivát tohoto neurotoxinu zanechává nevratné změny v kožní a podkožní tkáni.Klíčová slova:
botulotoxin A, entropium, histologie, ptóza, vedlejší efekt léčbyÚVOD
Botulotoxin je přirozený bakteriální toxin produkovaný sporující anaerobní tyčkou Clostridium botulinum, která u člověka způsobuje závažná onemocnění charakterizovaná blokádou cholinergního neurosvalového přenosu. Vlastní účinek spočívá v blokádě uvolňování acetylcholinu na presynaptické membráně nervosvalové ploténky. Proces probíhá ve třech fázích: předpokládá se navázání na receptor, internalizace, tzn. přechod přes presynaptickou membránu aktivním transportem a výsledkem je vlastní intracelulární blokáda acetylcholinu. Tento princip se využívá v léčbě lokálních svalových spasmů. Botulotoxin je proto zřejmě nejjedovatější látka používaná jako lék [25]. První definoval a využil botulotoxin německý lékař Kerner již v roce 1820.
Kromě neurologie princip blokády cholinergního neurosvalového přenosu našel uplatnění v oftalmologii, která byla průkopníkem jeho využití. Odborné oftalmologické publikace tvoří cca 3 % medicínských citací na téma problematiky botulotoxinu v posledních 15 letech. Přibližně ve stejné době (80. léta minulého století) se začal využívat v terapii blefarospazmu a strabismu. V posledních dvaceti letech se také využívá jako alternativa dočasné úpravy postavení horního víčka, kdy lagoftalmus ohrožuje rohovku z oschnutí.
Použití derivátu botulotoxinu A v současné době konzumní společnosti moderních industriálních států nachází uplatnění a rozmach především v kosmetické medicíně. Odpovídá tomu i odpověď farmaceutického průmyslu vývojem nových produktů. Po původním Onabotulinumtoxinu A (Botox®) firmy Allergan, z druhé poloviny 80. let minulého století, se objevil v roce 1990 Abobotulinumtoxin A (Dysport®) firmy Porton Down později Speywood. Dalším preparáty jsou Incobotulinumtoxin A (Xeomin®) od firmy Metz Pharma a licenční přípravky na bázi výše uvedených derivátů botulotoxinu A: Azzulure® (Ipsen Ltd.), Reloxin® (Ipsen Pharama) či Meditoxin® (Medy-Tox). Základem všech uvedených preparátů je Clostridium botulinum typ A toxin – haemaglutin komplex, proto není významného rozdílu mezi účinky těchto injekčních léků [21, 23, 33, 37]. V současnosti nejvíce používaný derivátem tohoto neurotoxinu je stále Botox®.
VLASTNÍ SESTAVA
Na Oční klinice FN Královské Vinohrady byla v letech 2006 až 2008 chirurgicky řešena patologická postavení víček. U těchto tří dospělých nemocných odeslaných k ošetření byla v předchozím období do postižené oblasti či nejbližšího okolí opakovaně aplikovány deriváty botulotoxinu A. Vždy se jednalo o Abobotulinumtoxin A (Dysport®).
1. Ptóza
65letý pacient byl deset let léčen aplikací Dysportu podle klasického schématu čtyř aplikačních bodů pro 15 let anamnesticky udávaný oboustranný blefarospazmus, jež byl diagnostikován a léčen na mimopražském neurologickém pracovišti. V jednom sezení bylo vždy aplikováno celkem do víček obou očí 140 j., a to nejméně čtyřikrát každý rok. V posledních třech letech před námi indikovaným chirurgickým výkonem v přímé souvislosti s aplikací Dysportu se začal projevovat pokles obou horních víček. Stav byl sice přechodný, ale postupně se prohluboval. Výsledek byl proto pacienta neuspokojivý, neboť jej výsledná oboustranná ptóza nutila zaklánět hlavu.
Při prvotním ambulantním vyšetření na Oční klinice FNKV v lednu 2007 (tři měsíce po poslední aplikaci Dysportu) bylo zastiženo jen náhlé uzavření oční štěrbiny, neschopnost otevřít oči na pokyn doprovázené zachvíváním víček, ale nikoliv již klasický obraz blefarospazmu s obrazem křečí (obr. 1). Po spontánním zklidnění byla šíře očních štěrbin 2–3 mm (obr. 2), margopupilární diametr vpravo 0, vlevo 1 mm. Funkce levátorů byla omezena na 4–6 mm, palpačně byla oblast frontální svalu v dolní polovině ztuhlá, bez známek schopnosti funkčního zapojení k podpoře zvednutí horních víček. Oboustranná artefakie byla provázená se shodným vizem na obou očích 1,0 nat. Vzhledem k omezené funkci zvedačů obou víček a funkčním postižením m. frontalis stav byl řešen plastikou aponeurózy pomocí dvou „X“ stehů Prolen 6-0. Tři měsíce po operaci byly oční štěrbiny široké 7 mm a margopupilární diametr 3 mm (obr. 3).
Image 1. Stav postavení víček v době záchvatu – uzavření oční štěrbiny 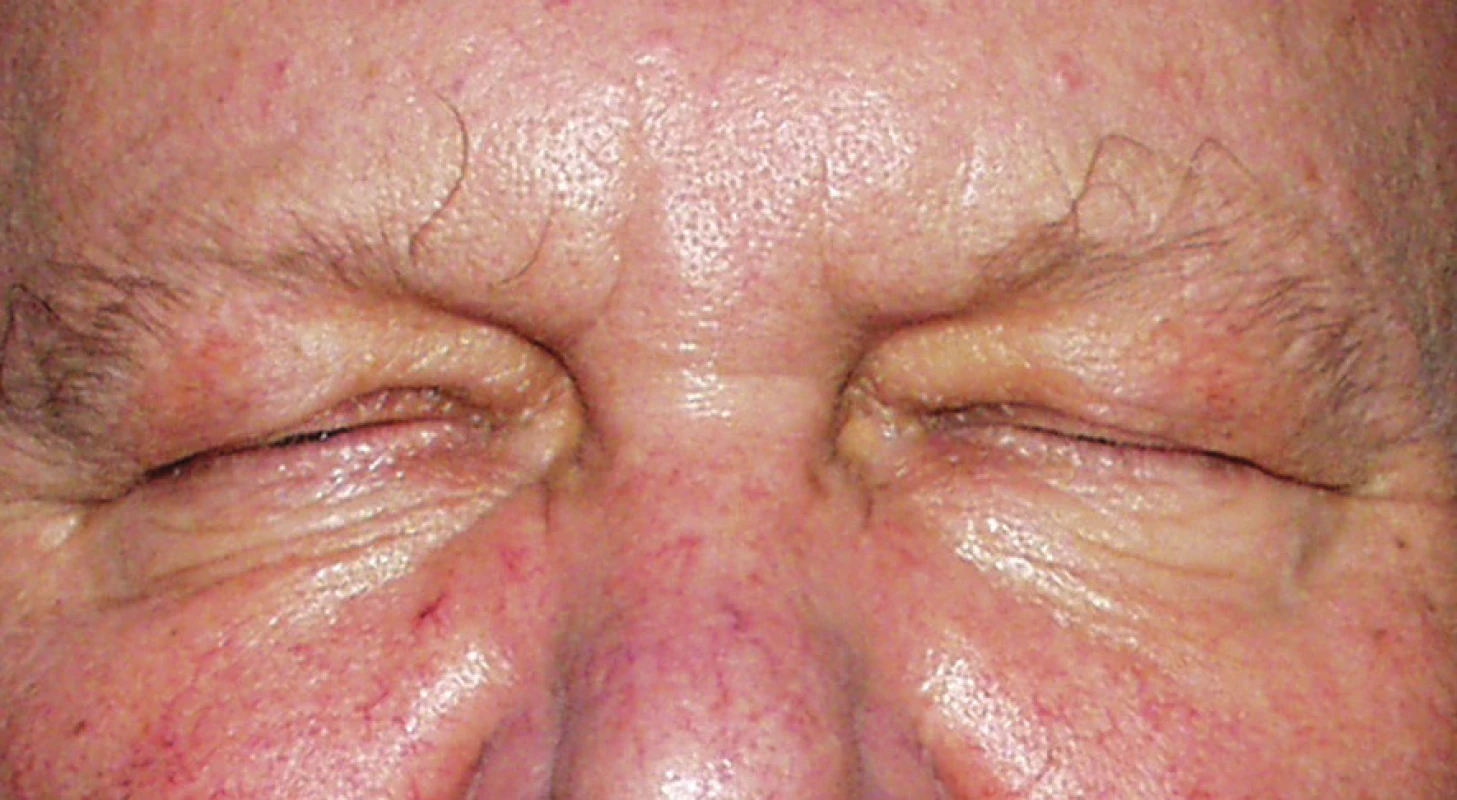
Image 2. Stav postavení víček v době uvolnění – pootevření oční štěrbiny 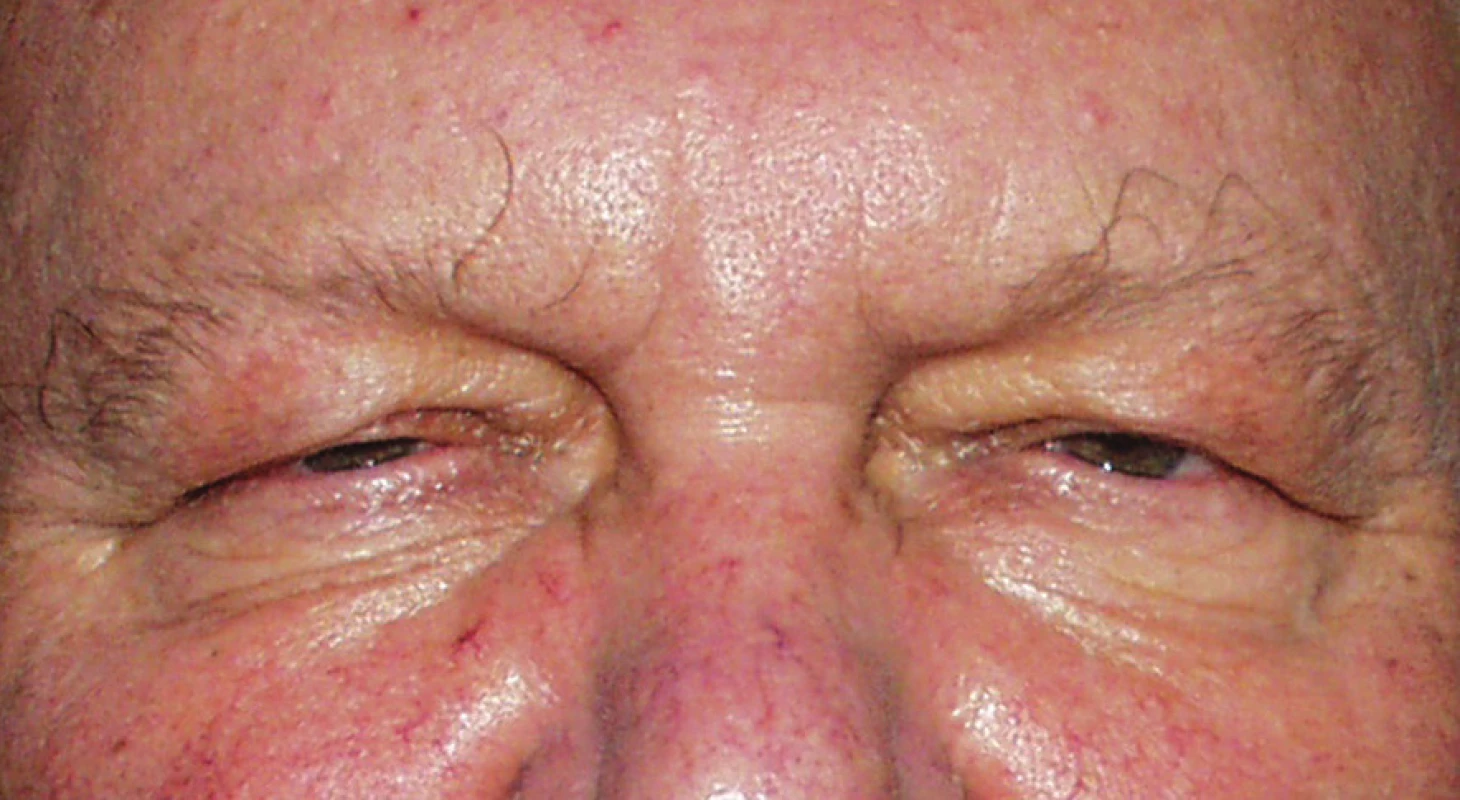
Image 3. Stav postavení víček po oboustranné plastice aponeurózy horních víček 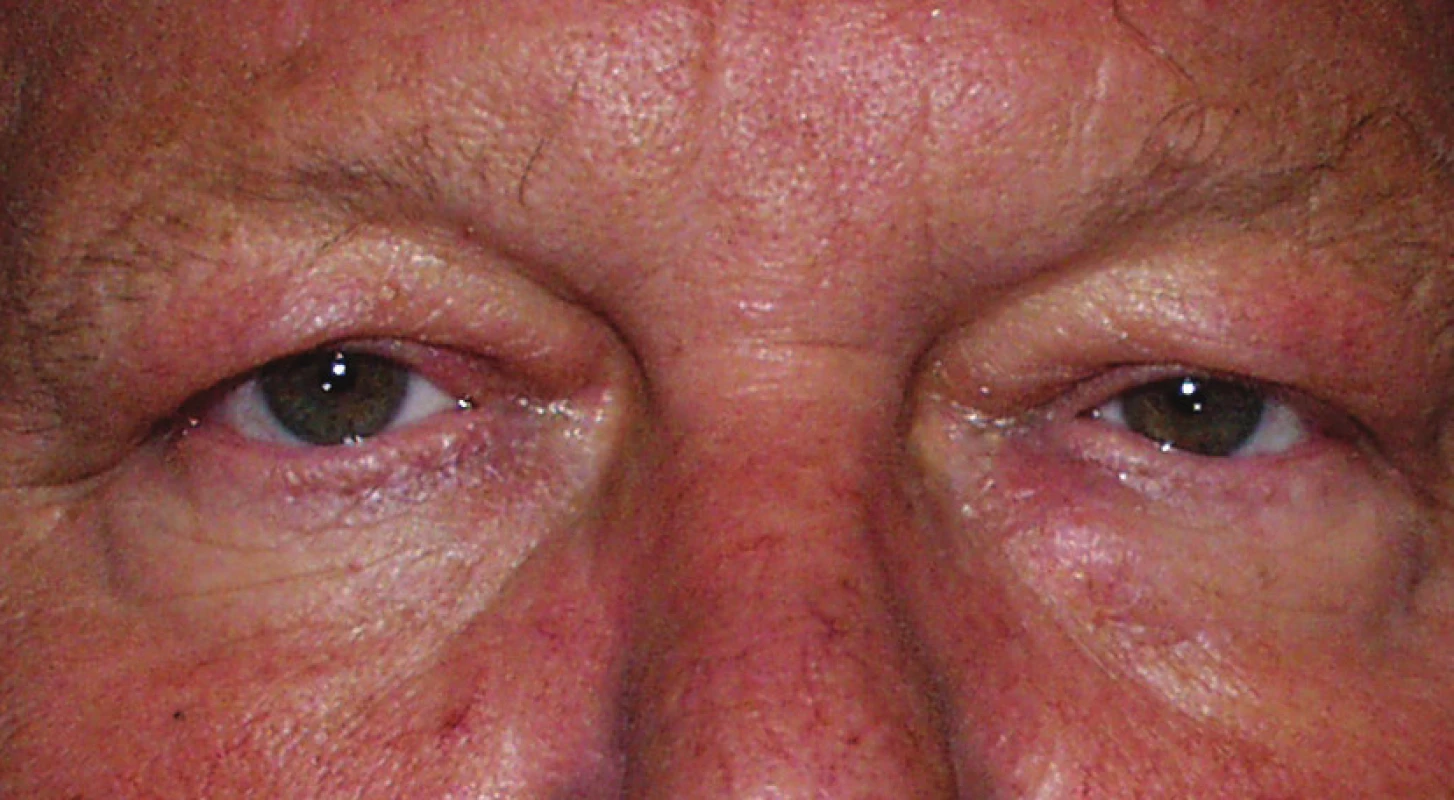
2. Entropium
90letá pacientka byla vyšetřena na ambulanci Oční kliniky FNKV pro přetrvávající entropium levého dolního víčka (obr. 4) v dubnu 2007. Anamnesticky byly uváděné opakované injekce Dysportu v průběhu 3 let, jen s dočasným efektem, jak uváděla nemocná. Tento stav si dobře uvědomovala, neboť postižené oko bylo vedoucím, vizus 0,25 s korekcí +10,0 = +1,5/120 st. pro pooperační afakii. Vpravo bylo vidění pokleslé na pohyb před okem vzhledem k těžké amblyopii provázené divergencí ex anopsia. V průběhu 3 aplikací od června 2003 do listopadu 2005 bylo vždy podáno v pěti bodech do dolního víčka 100 j.
Image 4. Entropium a trichiáza dolního víčka vlevo před operací 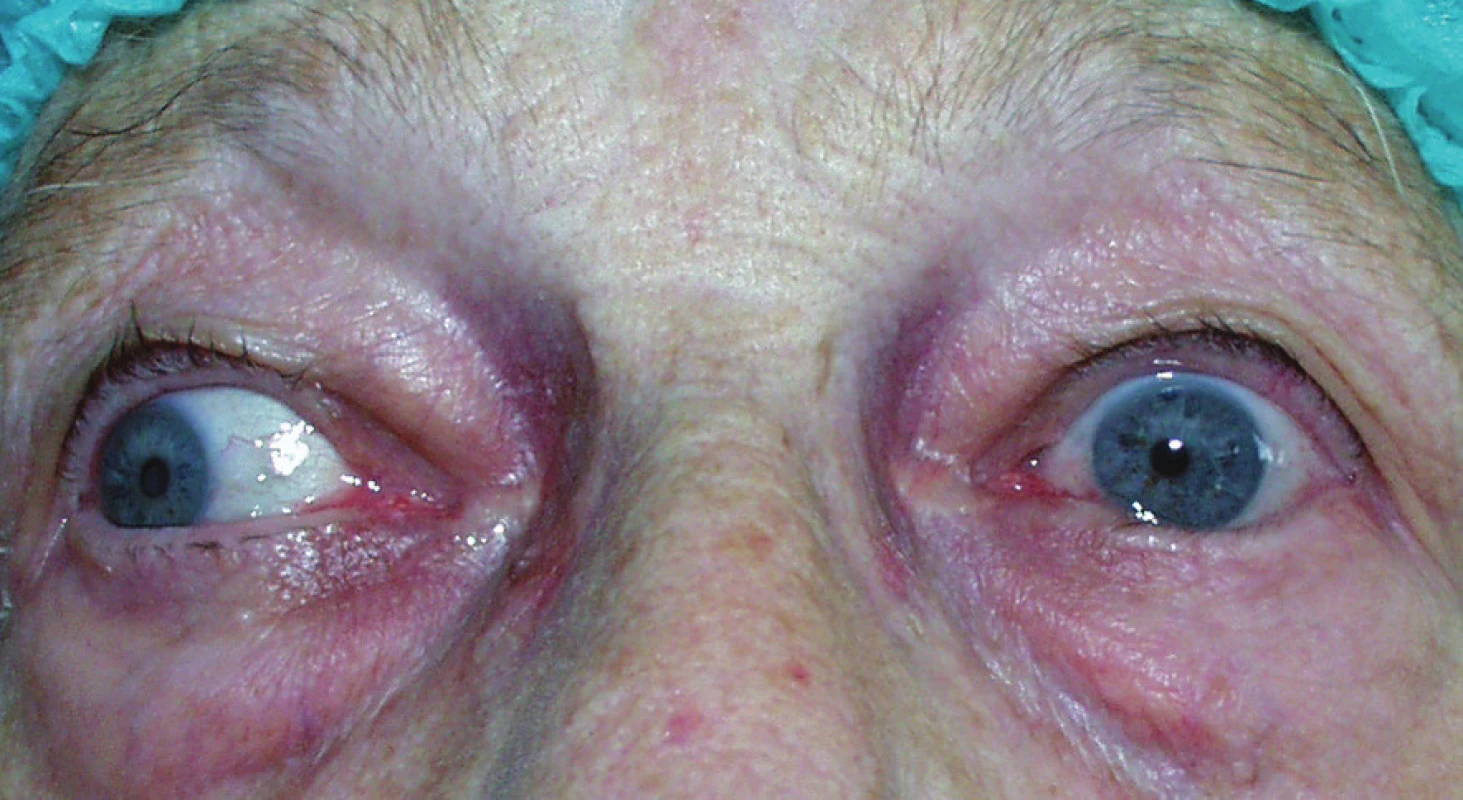
72letá pacientka byla pro oboustranné entropium dolních víček vyšetřena tamtéž v únoru 2007. Vizus oboustranně 0,66 pro myopický astigmatismus -0,5 = -1,5/100 st. vpravo a 20 st. vlevo. Anamnéza podání Dysportu byla delší, a to od října 2003 do června 2006, nemocné bylo v osmi sezeních ve čtyřech bodech do obou dolních víček aplikováno vždy celkově 120 až 160 j. Výsledným efektem bylo přetrvání entropia dolních víček, neboť po injekcích neurotoxinu nemocná nezaznamenala trvalý efekt ani významné přechodné zlepšení.
U obou pacientek byl při našem prvotním vyšetření shledán klasický obraz involučního entropia, charakterizovaný spontánním zarolováním dolních víček oproti bulbu při výzvě o zavření očí, které nebylo doprovázeno spastickou křečí. Úprava polohy víček se znormalizovala masážím tahem kůže dolů. Epifora byla jen v souvislosti s trichiázou. Stav byl vždy řešen plastikou dolního víčka myrtovitým vystřižením kůže a podkoží až na m. orbicularis, který byl v povrchních vrstvách částečně resekován. Po elektrokoagulaci byl operační postup ukončen pouze kožními trakčními stehy s tahem směrem dolů. U první starší pacientky to bylo 6 měsíců po poslední aplikaci Dysportu a u druhé mladší 9 měsíců, respektive 11 měsíců po poslední injekci. Za 3 měsíce po operacích bylo postavení víček znormalizováno, marga dolních víček dobře konturovala okraj oční štěrbiny, stav byl trvalý (obr. 5).
Image 5. Normalizace polohy víčka vlevo po plastické operaci 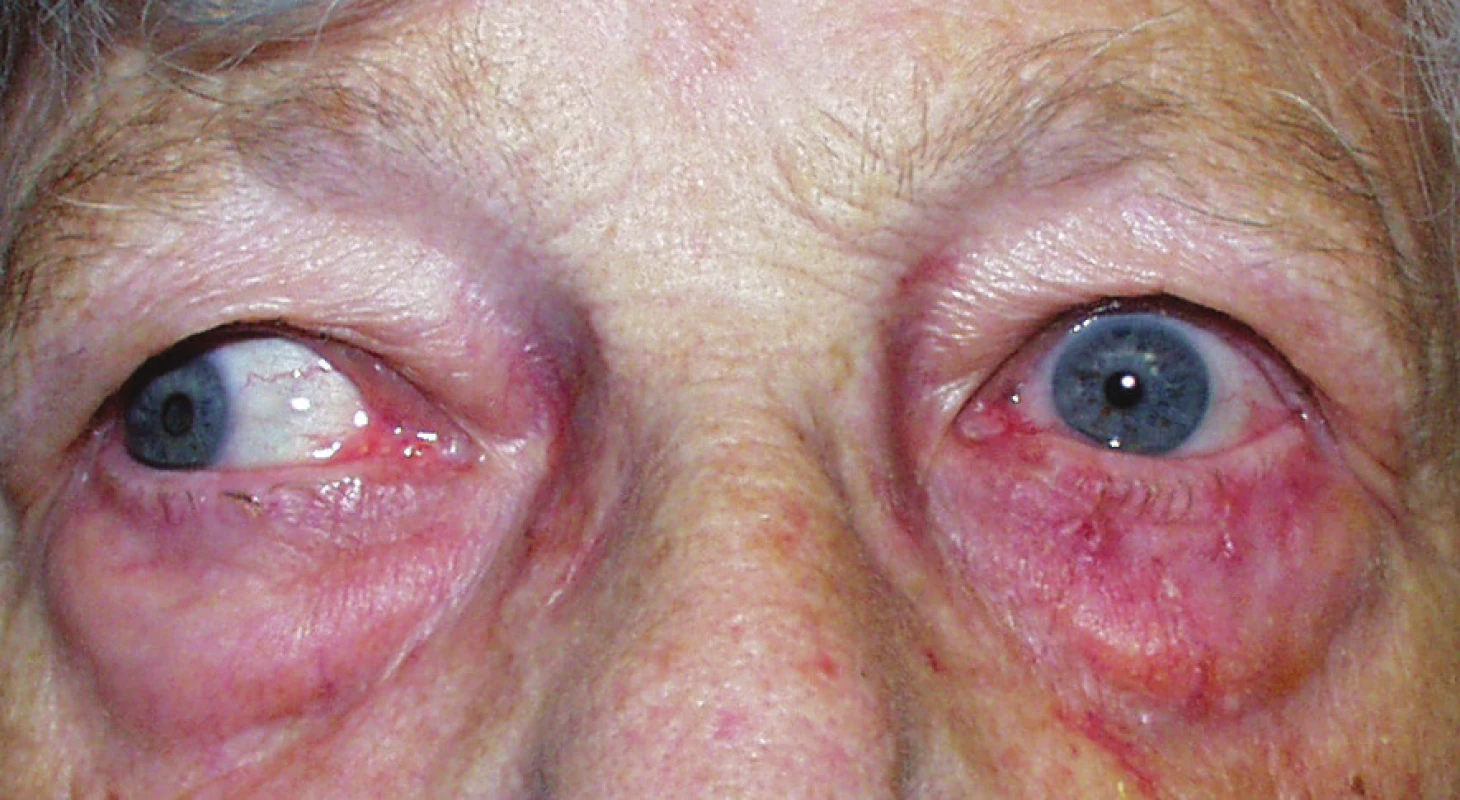
Výsledky histologického vyšetření z resekovaných částí kůže a podkoží ukázaly dva typy patologických změn: Prvním typem změn bylo nestejnoměrné projizvení koria a přilehlého podkoží, místy i s reziduálními mikroskopickými strukturami nespecifické granulační tkáně a mikroskopickými rezidui hematomu, vzniklého patrně v souvislosti s předchozí injekční aplikací (obr. 6). Druhým pozorovaným typem změn byla různě rozsáhlá atrofie snopců příčně pruhovaného svalu se ztenčením jejich jednotlivých vláken a zmnožením vaziva v jejich intersticiu (obr. 7) a s eventuální chronickou zánětlivou infiltrací (obr. 8).
Image 6. Projizvení víčka při povrchu s nespecifickou granulační tkání a v hloubi se zbytky resorbujícího se hematomu (barvení HE, zvětšení 100x) 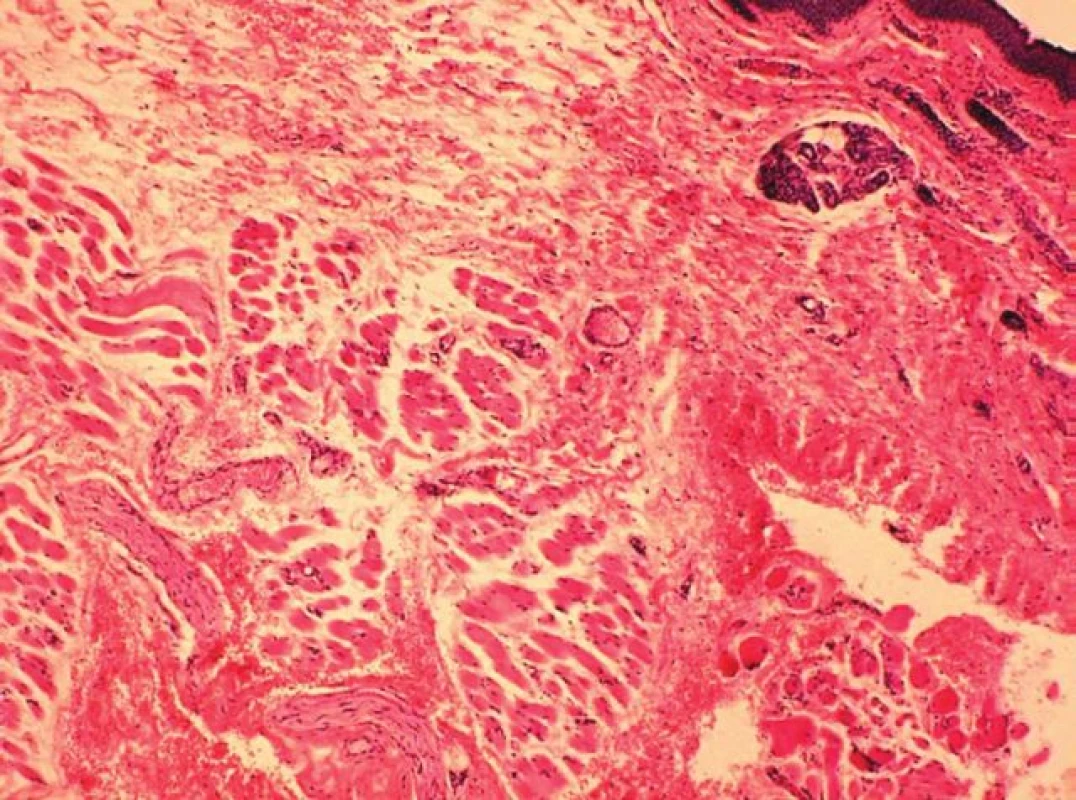
Image 7. Projizvení a atrofie svalu ve víčku a novotvořené vazivo s drobnými cévami nespecifické granulační tkáně (barvení HE, zvětšení 100x) 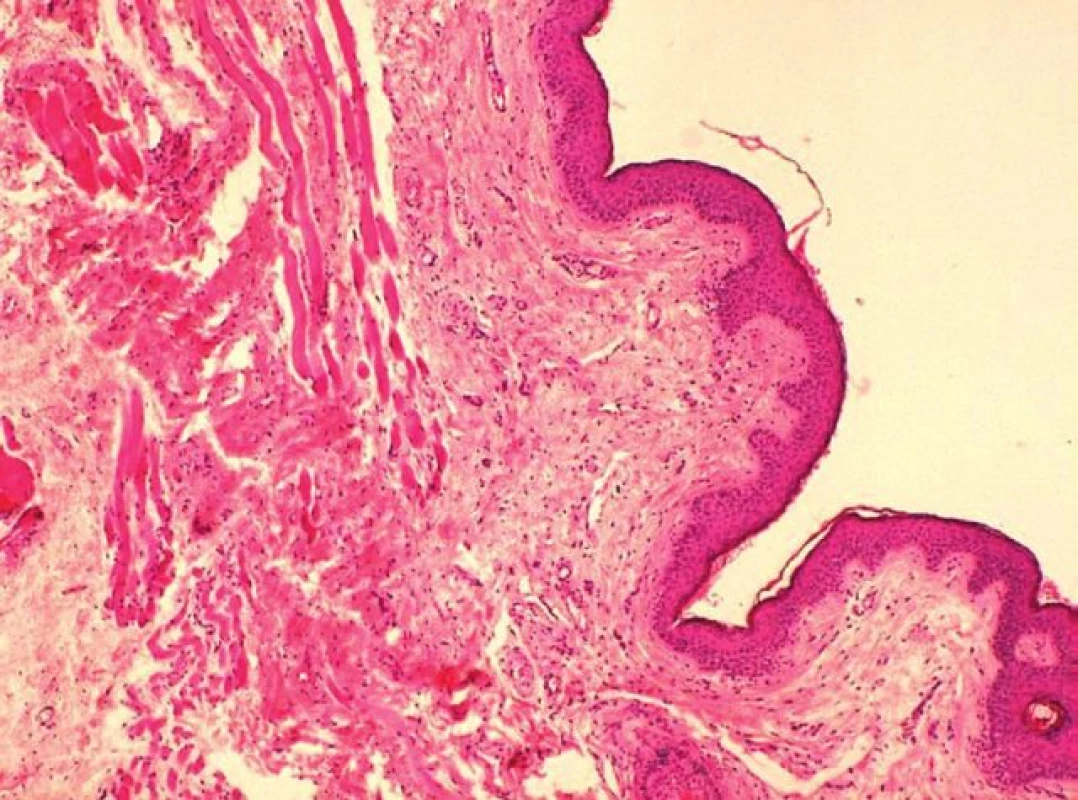
Image 8. Víčko s výrazným projevením, s jizevnatě zahoustlým vazivem a chronickou zánětlivou infiltrací (barvení HE, zvětšení 100x) 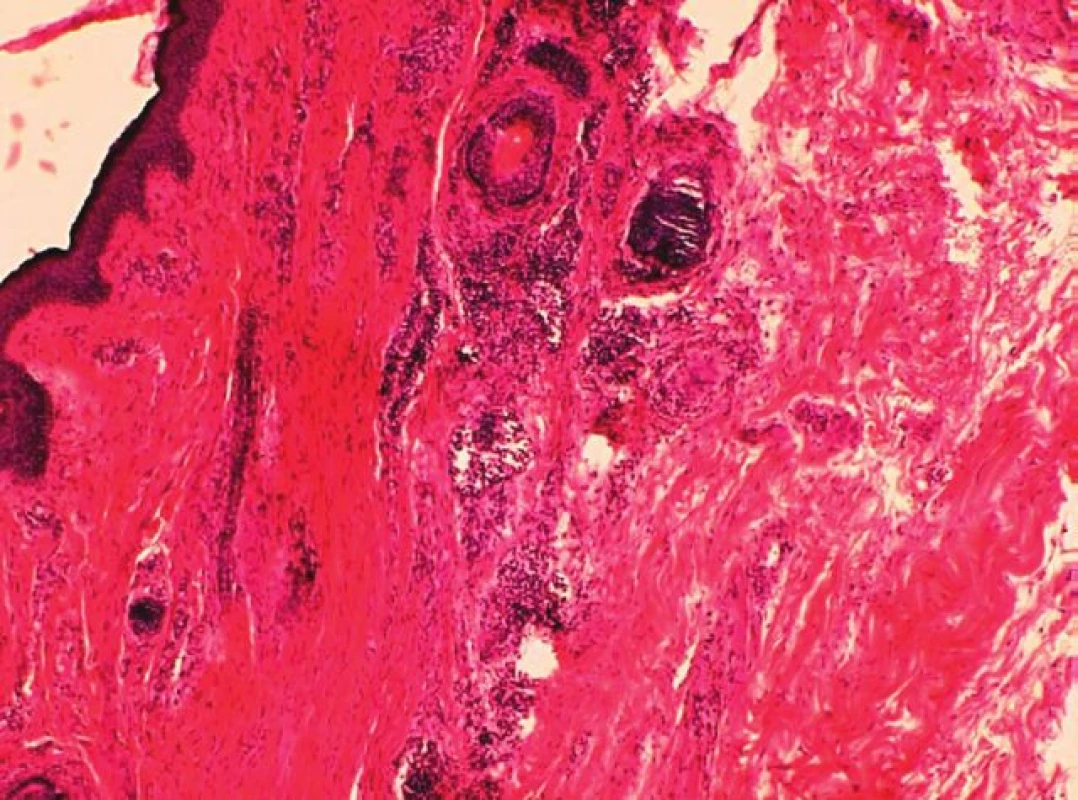
DISKUSE
První vědecky podložené sdělení o aplikaci derivátu botulotoxinu A v oftalmologii je spojeno v roce 1980 se jménem prof. A.B. Scotta [30], jenž jej aplikoval v léčbě strabismu jako alternativu chirurgického postupu, přičemž jej poprvé použil již v roce 1973 [5]. Až později nezávisle na sobě přichází publikace dvou pracovních skupin [7, 31] při využití tohoto neurotoxinu v léčbě blefarospazmu v roce 1985. FDA dala souhlas pro aplikaci Botoxu® již v roce 1989 v indikaci strabismu a blefarospazmu, ale až v roce 2002 pro cervikální dystonii.
Na přelomu minulého a tohoto stolení století se objevují práce o využití BotoxuR v léčbě strabismu i v regionu bývalého Československa [8, 32]. Obě publikace ve své době hodnotí jeho použití za velice úspěšné a zařazují je do moderního terapeutického arzenálu. Úspěšnost podání botulinum toxinu z hlediska dvouletého sledování v současné době u kojenecké esotropie nad 60 pdpt je jen 74 %, tzn. se zbytkovou úchylkou pod 10 pdpt [15]. Vyplývá z toho nyní určitá opatrnost k indikacím jeho aplikace, neboť má variabilnější výsledek než klasické chirurgické řešení [28]. Rozhodující pro negativní postoj jsou sekundární vedlejší efekty jako je především vertikální deviace, ale i ptóza, atd. [14], a to 24 % u Dysportu a 55 % u Botoxu [28]. Do komplikací je sice započítán otok a krvácení, které jsou také následkem i chirurgických výkonů, ale rozhodující pro negativní hodnocení jsou záporné motorické změny.
Rozsáhlá studie o 264 pacientech s blefarospasmem uzavřená již v roce 1988, prokázala zásadní léčebný efekt derivátu botulinum toxin A u tohoto onemocnění na rozdíl od dříve používané avulse faciálního nervu. Příznivý dopad léčby byl u 57 % nemocných, z toho signifikantní zlepšení ve 44 %. V této studii byl poprvé vyzkoušen Abobotulinumtoxin A [10]. Tento preparát byl použit při prvních českých aplikacích [29] na začátku 90. let minulého století. K vedlejším přechodným projevům patří ptóza či diplopie v krátkodobém sledování[10]. Veškeré formy injekčních produktů botulintoxinu A zůstávají základním lékem blefarospazmu i v současné době [21, 34, 37].
V našem prvním případu vzhledem k předchozí anamnestické desetileté aplikaci Dysportu byl pokles horních víček již trvalý. Pro vliv výše uvedeného neurotoxinu na poklesu víček svědčí vymizení motoriky dolní poloviny frontálního svalu, ale i symetrické omezení funkce obou zvedačů víček způsobený jejich spádovou a gravitační infiltrací neurotoxinu z čela. Klinický obraz postavení víček v době operace ptózy se blížil spíše obrazu apraxie než klasickému blefarospazmu [19], ale ověření nálezů v předchozím období nebylo již k dispozici. Úspěšný operační postup navíc potvrdil naší úvalu o příčině ptózy, neboť jsme neprováděli frontotarzální závěs ani resekci levátorů, čímž jsme se vyhnuli postiženým strukturám.
U dvou dalších pacientek byla odesílající diagnóza spastického entropia vzhledem k věku diskutabilní, neboť v tomto věku se uvažuje o involuční formě a navíc klinický obraz našeho nálezu před plastikou dolních víček svědčil pro tuto involuční formu. Aplikace tohoto neurotoxinu v léčbě entropia není neurooftalmology popisována. Prováděná předchozí intradermální aplikace neurotoxinu se ukázaly být neúčinné a navíc entropická postavení víček pro vyvolané trofické změny byla zakonzervována.
Další využítí botulotoxinu se uplatňuje při řešení retrakce horního víčka v rámci Gravesovy choroby [4] na místo tarzorafie jako ochrana postižení rohovky vyvoláním dočasné ptózy [2, 16, 24]. Jeho aplikace k blokádě symptomatické epifory [36] , či při léčbě špatně ovlivnitelné filamentózní keratitidy [11], vyvolává spíše řadu otázek než zavedení do běžné praxe.
Léčebné deriváty botulotoxinu A si našly uplatnění především v neurologii, kam patří neurooftalmologická problematika blefarospazmu. Jeho aplikace do víček příznivě současně ovlivňuje případně přítomnou oromandibulární dystonii [10, 29]. Injekční aplikace těchto léků se uplatňuje při útlumu obtíží při faciálních spazmech [3, 25] či samostatných cervikálních dystoniích [21, 25] nebo při jejich kombinacích s migrénami [35]. Další využití derivátů botulotoxinu je popisováno u spazmu flexorů kotníku [27], eventuálně u tenisového lokte [12].
Kosmetická medicina je velice populární především v USA, z celkové sumy 11 miliard dolarů vynaložených klienty v roce 2007 byly zaplaceny 3 miliardy jen za aplikaci botulotoxinu A, především Botoxu [17]. Vrásky v oblasti čela a perioribální oblasti lze dobře kosmeticky ovlivnit pomocí Botoxu, ale tento postup není schválen FDA a považuje se za off-label [13]. Před deseti lety při posouzení výsledů více než jednoho tisíce pacientů po intradermálním podání botulinum toxinu A v obličejové oblasti nebyla popsána žádná závažná komplikace, ale pouze uspokojení klientů z výsledků aplikace [18]. Po určitém čase si ojediněle kosmetičtí chirurgové začali uvědomovat možnosti komplikací. Po lokálních aplikacích se objevuje místní bolestivost a hematomy, cefalea, pokles horních víček i obočí a řada dalších změn [17, 23]. K popsaným vedlejším projevům v kožní orbitální oblasti po aplikaci tohoto neurotoxinu patří také změna pigmentace kůže [26] nebo raritní herniace orbitálního tuku [20] či pseudoaneuryzma frontální větve povrchní temporální arterie [22]. Větší riziko komplikací mají pacienti s předchozí plastickou operací dané oblasti s anamnézou neuromuskulární nemoci či hluboké vrásky [33]. Podrobná studie v porovnání Botoxu a placeba prokázala signifikantní rozdíl ve vyvolání ptózy a edému víček v neprospěch botulotoxinu, ale bez celkových projevů na CNS [1]. Literární informace hovoří, že i omylem podané jednorázové desetinásobné zvýšení dávky Botoxu oproti běžné aplikaci nevyvolalo závažné celkové neurologické projevy [25, 29]. Naopak opakované aplikace se mohou projevit v celkové imunitní odpovědi u rizikových jedinců tvorbou protilátek proti botulotoxinu A [6].
Patologickohistologické rozbory vedlejších účinků derivátů botulotoxinu A na tkáni kůže pro případně nutné chirurgické úpravy nejsou specialisty styčných oborů hodnoceny. Z cca 2000 citaci v PubMedu do roku 1997 existuje jediná samostatná histologická studie zabývající se zvířecím modelem [8], která hodnotí atrofické změny svalu projevující se změnou obsahu MyHC mRNA ve svalových vláknech. Aplikace Botoxu takto může vést k nekontrolovatelným strukturálním změnám postižených svalů. Autoři zvažují tento klinický dopad, léčba hypertrofických svalů pomocí Botoxu může mít za následek jejich funkční nevyváženost. V naší studii byla ireverzibilní atrofizace příčně pruhovaného svalu víček v přímé souvislosti s aplikací Dysportu nikoliv vlivem involučních změn, neboť výraznější změny byly u mladší pacientky s četnější aplikací Dysportu.
ZÁVĚR
Autoři chtěli poukázat na histologicky verifikované nepříznivé změny ve strukturách kůže i podkoží po opakovaných aplikacích derivátu botulotoxinu A. Seznámit odbornou veřejnost s tímto faktem pro vlastní úvahu u svého osobního použití. Nelze přepokládat, že by to nějakým způsobem ovlivnilo četnost podání v komerčních pracovištích kosmetické dermatologie či v soukromých očních centrech, přestože je to považováno za off-label aplikaci.
Do redakce doručeno dne 5. 9. 2012
Do tisku přijato dne 16. 11. 2012
MUDr. Jan Krásný
Oční klinika FN Královské Vinohrady
Šrobárova 50
100 34 Praha 10
e-mail: jan.krasny@fnkv.cz
Sources
1. Brin, M.F., Boodhoo, TI, et. al.: Safety and tolerability of onabotulinumtoxin A in the treatment of facial lines: a meta-analysis of individual patient data from global clinical registration studies in 1678 participants. J Am Acad Dermatol, 61; 2009 : 961–970.
2. Choi, J.C., Lucarelli, M.J., Shore, J.V.V.: Use of botulinum toxin A in pacients at risk of wound complications following eyelid reconstruction. Ophthal Plast Reconstr Surg, 13; 1997 : 259–264.
3. Clark, G.T.: The management of oromandibular motor disorders and facial spasm with injections of botulinum toxin. Phys Med Rehabil Clin N Am, 14; 2003 : 727–748.
4. Costa, P.G., Saraiva, F.P., et al.: Comparative study of Botox injection treatment for upper eyelid retraction with 6-moth follow-up in patients with thyroid eye disease in the congestive or fibrotic stage. Eye, 223; 2009 : 767–773.
5. Crouch, E.R.: Use of botulinum toxin in strabismus., Curr Opin Ophthalmol, 17; 2006 : 435–440.
6. Dressler, D., Wohlfahrt, K., et al.: Antibody-induced failure of botulinum toxin a therapy in cosmetic indication. Dermatol Surg, 36; 2010, Suppl. 4 : 2182–2187.
7. Eston, J.S., Russel, B.W.: Effect of treatment with botulinum toxin on neurogenic blepharospasm. Brit Med J, 290; 1985 : 1857–1859.
8. Gedrange, T., Gredes, T., et al.: Histological changes and changes in the myosin mRNA content of the porcine masticatory muscles after masseter treatment botulinum toxin A. Clin Oral Investig, 2012, Springer, (v předstihu publikováno na PubMed).
9. Gerinec, A., Slyško, P., Fišerová, O.: Prinos botulotoxínu v liečbě strabizmu. Čes a Slov Oftal, 54; 1998 : 174–178.
10. Grandas, F., Elston, J., et al.: Blepharospasm: a review of 264 patients. J Nerol Neurosurg Psychiat, 51; 1988 : 767–772.
11. Gumus, K., Lee, S., et al.: Botulinum toxin injection for the management of refractory filamentary keratitis. Arch Ophthalmol, 130; 2012 : 446–450.
12. Hayton, MJ., Dantini, A.J., et al.: Botulinum toxin injection in the treatment of tennis elbow. A double-blind, randomized, controlled, pilot study. J Bone Joint Surg Am, 87; 2005 : 503–507.
13. Klein, A.V.V.: Botox for the eyes and eyebrows. Dermatol Slin, 22; 2004 : 145–149.
14. Kowal, L., Wong, E., Yahalon, C.: Botulinum toxin in the treatment of strabismus. A review of its use and effects. Disdabil Rehabil, 23; 2007 : 1823–1831.
15. Lueder, G.T., Galli, M., et al.: Long-term reset of botulinum toxin-augmended medial rectus recessions for large-angle infantile esotropia. Am J Ophthalmol, 153; 2012 : 560–563.
16. Naik, M.N., Gangopadhyay, N., et al.: Anterior chemodenervation of levator palpebrae superioris with botulinum toxin type-A (Botox) to induce temporary ptosis for corneal protection. Eye, 22; 2008 : 1132–1136.
17. Niautu, J. 3rd: Complications in Fillers and Botox. Oral. Maxillofac. Surg Clin North A, 21; 2009 : 13–21.
18. Niautu, J. 3rd.: Botulin toxin A: a review of 1.085 oral and maxillofacial patient treatments. J Oral Maxillofac Surg, 61; 2003 : 317–324.
19. Otradovec, J.: Klinická neurooftalmologie, Grada, Praha, 2003, s. 339.
20. Paloma, V., Samper, A.: A complication with the aesthetic use a Botox: Herniation of the orbital fat. Plast Reconstr Surg, 107; 2001 : 1315.
21. Pagen, F.L., Harrison, A.: A guide to dosing in the treatment of cervical dystonia and blepharospasm with XeominR: new botulin neurotoxin A. Parkinsonism Relat. Disord., 18, 2012 : 441–445.
22. Prado, A., Fuentes, P., et al.: Pseudoaneurysm of the frontal branch of the superfacial temporal artery: an unusual complication after the injection of Botox. Plast. Reconstr. Surg., 119, 2007 : 2334–2335.
23. Prager, W., Huber-Vorländer, J., Taufig, A,Z.. et al.: Botulinum toxin type A treatment to the upper face: retrospective analysis of daily practice. Clin Cosmet Investig Dermatol, 5; 2012 : 53–56.
24. Reddy, U.P., Woodward, J.A.: Abobotulinum toxin A (Dysport) and botulinum toxin type A (Botox) for purposeful induction of eyelid ptosis. Ophthal Plast Reconstr Surg, 26; 2010 : 489–491.
25. Remeš, F., Roth, J., Růžička, E.: Léčebné použití Botulotoxinu v neurologii. Prakt Lék, 74; 1994 : 174–177.
26. Roehm, P.C., Perry, J.D. et al.: Prevalence of periocular depigmentation after repeated botulin toxin A injections in African American patients. J Neroophthalmol, 19; 1999 : 7–9.
27. Rousseaux, M., Buisset, N., et al.: Comparison of botulinum toxin injection and nerotomy in patiens with distal lower limb spasticity. Eu J Neurol, 15, 2008 : 506–511.
28. Rowe, F.J., Noonan, C.P.: Botulin toxin for the treatment of strabismus. Cochrane Database Syst. Rev., 2012, Ef. 15 : 2: CD006499.
29. Růžička, E., Roth, J., Diblík, P.: Botulotoxin v léčbě blefarospazmu. Čas Lék čes, 131; 1992 : 213–216.
30. Scott, AB.: Botulinum toxin injections into extra-ocular muscles as an alternative to strabismus surgery. Ophthalmology, 87; 1980 : 1044–1049.
31. Scott, A.B., Kennedy, R.A., Stubbs, H.A.: Botulinum toxin injection as treatment for blefarospasm., Arch. Ophthalmol., 103; 1985 : 347–350.
32. Vácha, J., Bodnár, M., et al.: Botulotoxín A – jedna z možností léčby strabismu. Folia Strabol Neuroophtalmol, 6; 2003, Suppl. 1.: 50–51.
33. Vartanian, A.J., Davan, S., H.: Complications of botulinum toxin A use in facial rejuvenation., Facial. Plast. Surg. Clin North Am, 11; 2003 : 483–492.
34. Wabbels, B., Reichel, G., Fulford-Smith, A. et al.: Double-blind, randomized, parallel group pilot study comparing two botulinum toxin type A products for treatment of blepharospasm. J Neural Trans, 118; 2011 : 233–239.
35. Winner, P.K., Sadowsky, C.H. et al.: Concurrent Onabotulinum toxin A treatment of cervical dystonia and concomitant migrace. Haedache, 18; 2012 : 15 - 26.
36. Wojno, T.H.: Results of lacrimal gland botulinum toxin injection for epifora in lacrimal obstruction and gustatory tearing. Ophthal Plast Reconstr Surg, 27; 2011 : 119–121.
37. Yoon, J.S., Kim, J.C., Lee, S.Y.: Double-blind, randomized, comparative study of Medoxin versus Botox in the treatment of essential blepharospasm. Korean J Ophthalmol, 23; 2009 : 137–141.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2012 Issue 5-
All articles in this issue
- Ranibizumab v léčbě vlhké formy VPMD – dvouleté výsledky léčby z registru AMADEuS
- Pars plana vitrektómia a kombinovaná liečba pars plana vitrektómia, triamcinolon acetonid intravitreálne a laserkoagulácia makuly pri diabetickom edéme makuly – ročné výsledky
- Klinická rozmanitosť Bestovej choroby
- Súčasný stav evidencie zhubných nádorov oka a očných adnexov (dg. C69) v SR a ČR
- Srovnání metody nastavitelných versus fixních stehů při operaci strabismu u pacientů s endokrinní orbitopatií
- Aplikace Dysportu® – možnost doprovodného vedlejšího efektu na postavení víček (klinicko-histologická studie)
- Transnazální endoskopická chirurgie nádorů očnice
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Klinická rozmanitosť Bestovej choroby
- Aplikace Dysportu® – možnost doprovodného vedlejšího efektu na postavení víček (klinicko-histologická studie)
- Pars plana vitrektómia a kombinovaná liečba pars plana vitrektómia, triamcinolon acetonid intravitreálne a laserkoagulácia makuly pri diabetickom edéme makuly – ročné výsledky
- Srovnání metody nastavitelných versus fixních stehů při operaci strabismu u pacientů s endokrinní orbitopatií
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

