-
Medical journals
- Career
Změny hemostázy a další poruchy způsobené monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci
Authors: Adam Z. 1; Řehák Z. 2; Krejčí M. 1; Boichuk I. 1; Pour L. 1
Authors‘ workplace: Interní hematologická a onkologická klinika LF MU a FN Brno 1; Oddělení nukleární medicíny, MOÚ Brno 2
Published in: Klin Onkol 2026; 39(1): 31-39
Category: Review
doi: https://doi.org/10.48095/ccko202631Overview
Východiska: Monoklonální imunoglobulin a/nebo volné lehké řetězce způsobují pestré komplikace, které mohou postihnout snad všechny tkáně či orgány. Cíl: Monoklonální imunoglobulin může zasáhnout do hemostázy a způsobit jak hyperkoagulaci, tak hemoragickou diatézu. U pacientů s nemaligní gamapatií a zatím neléčeným mnohočetným myelomem jsou častější komplikace trombotické než hemoragické. Monoklonální imunoglobulin může výjimečně mít i vlastnost autoprotilátky, a způsobovat tak různorodé poškození orgánů. Z těch častějších forem je to nemoc chladových aglutininů, neuropatie, různé formy poškození oka. V textu jsou pak zmiňovány i méně časté poruchy. Závěr: Všechny komplikace popsané v textu mohou být způsobeny monoklonálním imunoglobulinem, ale mohou mít i jiné příčiny. Pokud se podaří prokázat etiopatogenetickou souvislost těchto problémů s monoklonálním imunoglobulinem, tak může cílená léčba potlačující jeho tvorbu vést k vymizení problému.
Klíčová slova:
volné lehké řetězce – monoklonální imunoglobulin – monoklonální gamapatie klinického významu – MGCS
Úvod
Tento text je pokračováním série článků, které popisují jednotlivé formy poškození organizmu monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci. Multisystémovým chorobám způsobeným monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci, které (mimo jiné) poškozují ledviny, byl věnován samostatný článek. Druhý článek se zaměřil na multisystémové poruchy při monoklonálních gamapatiích, které (mimo jiné) poškozují kůži.
Do tohoto třetího zařazujeme patologické stavy, které vznikají interferencí monoklonálního imunoglobulinu s hemostázou, a dále různé imunologicky mediované poruchy, s nimiž může ale i nemusí souviset monoklonální imunoglobulin. Zmiňujeme také možné poškození oka. U každé jednotky uvádíme, zda je její etiologie jednoznačně způsobena gamapatií, nebo zda má popisovaná jednotka více možných vyvolávajících příčin. V těchto třech článcích chceme stručnou formou upozornit na všechny vzácné nemoci řazené do skupiny monoklonální gamapatie klinického významu (monoclonal gammopathy of clinical significance – MGCS).
Vliv monoklonálního imunoglobulinu a/nebo volných lehkých řetězců na hemostázu
Monoklonální gamapatie může zasahovat do procesu hemostázy a vychylovat rovnováhu jak trombotickým, tak hemoragickým směrem. U pacientů s nemaligní gamapatií či zatím neléčeným mnohočetným myelomem je koagulace častěji vychylována směrem k trombotické diatéze než k hemoragické.
Tromboembolické komplikace u monoklonálních gamapatií
V roce 2023 Dimopoulos et al. vydali publikaci Monoclonal Gammopathy of Thrombotic Significance, která shrnuje již dříve publikované epidemiologické studie, které prokázaly signifikantně vyšší riziko vzniku tromboembolických komplikací u pacientů nejen s mnohočetným myelomem, ale také s monoklonální gamapatií nejistého významu (monoclonal gammopathy of undetermined significance – MGUS). Autoři stručně shrnuli i v té době známé mechanizmy hyperkoagulačních stavů u monoklonálních gamapatií [1,2].
Zde uvedeme jen výsledky studie zveřejněné v roce 2025. Sledováno bylo 3 668 pacientů s MGUS. Při mediánu sledování 3,7 roku zjistili 10,3 případů žilních trombóz a 21 případů arteriálních trombóz v přepočtu na 1 000 osob. Ve skupině osob bez MGUS to bylo 6,0 žilních a 13,8 arteriálních trombóz v přepočtu na 1 000 osob. Statisticky byl významně vyšší jen počet žilních trombóz ve skupině v MGUS ve srovnání s kontrolní skupinou [3].
Monoklonální imunoglobulin ovlivňuje koagulační kaskádu na více místech, často interferencí na úrovni systému aktivovaného proteinu C, což pak vyústí v trombotickou, případně i embolickou komplikaci [4–7].
Teprve nedávno rozpoznanou etiopatogenezí trombofilních stavů u gamapatií je aktivita monoklonálního imunoglobulinu namířená proti destičkovému faktoru 4 (platelet factor 4 –PF4). Protilátky proti tomuto faktoru hrají centrální roli v patofyziologii trombóz a trombocytopenií u heparinem indukované trombocytopenie a vakcínou indukované trombocytopenie. Popsány byly ovšem případy, kdy rekurentní trombózy při současné trombocytopenii byly způsobeny aktivitou monoklonálního imunoglobulinu proti PF4. Typické znaky této poruchy jsou opakované trombózy, perzistující trombocytopenie a pozitivita klasického testu na heparin indukovanou trombocytopenii. Na tuto spojitost autoři upozornili i v názvu článku – Monoclonal gammopathy of thrombotic/thrombocytopenic significance – v němž poukazují na možnou vazbu mezi trombózou, trombocytopenií a monoklonální gamapatií [8–10].
Tromboembolické komplikace se mohou manifestovat jako akutní plicní embolie anebo jako sukcesivní plicní embolizace způsobující pomalu narůstající dušnost a vedoucí k plicní hypertenzi. Obě tyto poruchy někdy bývají prvním příznakem mnohočetného myelomu. A proto specialisté hemokoagulačních ambulancí při vyšetřování příčiny trombotické diatézy vždy provádějí analýzu přítomnosti monoklonálního imunoglobulinu a volných lehkých řetězců. A někdy tak odhalí dříve nepoznaný MGUS anebo mnohočetný myelom [3–7].
Krvácivé poruchy provázející monoklonální gamapatie
Krvácivé poruchy jsou u osob s nemaligní gamapatií či zatím neléčeným mnohočetným myelomem méně časté než poruchy trombotické. Vyjma krvácivých komplikací při získaném von Willebrandově syndromu může monoklonální imunoglobulin zasahovat do systému hemostázy na četných dalších místech a způsobovat hemoragickou diatézu. Je obtížné přesně pojmenovat a určit místo v koagulační kaskádě, kde nastala porucha. A tak se mnohdy konstatuje, že je to hemoragická diatéza související s monoklonální gamapatií bez další specifikace. Analýzy příčin krvácivých stavů vedly k rozpoznání následujících příčin:
- deficit faktoru X, který je vychytáván amyloidovými hmotami;
- deficit faktoru V;
- dysfibrinogenemie;
- získaná hemofilie;
- získaná trombocytopatie [4,5,11–14].
Proto je u pacientů s monoklonálními gamapatiemi vhodné anamnesticky zjišťovat případné předcházející známky hemoragické diatézy. V případě, že náš pacient s mnohočetným myelomem či jinou gamapatií jde na operaci, má koagulační část předoperačního vyšetření na starosti koagulační specialista, který obvykle volí rozsáhlejší spektrum vyšetření než u pacientů bez monoklonální gamapatie. Naopak při diferenciální diagnostice hemoragické diatézy nejasné etiologie je vhodné vždy vyšetřit monoklonální imunoglobulin a volné lehké řetězce [8–14].
Získaný von Willebrandův syndrom
Von Willebrandův syndrom je hemoragická porucha způsobovaná deficitem aktivity von Willebrandova faktoru (vWF). Podobně jako jiné koagulační poruchy se dělí na vrozenou a získanou. Vrozený deficit je genetickou abnormalitou. Získaný von Willebrandův syndrom může souviset s různými dalšími chorobami, jejichž výčet je poměrně pestrý [15,16].
Analýza 211 případů získané formy von Willebrandova syndromu ukázala, že nejčastějším podkladem této poruchy byly lymfoproliferace (48 %), zatímco jiné myeloidní neoplazie byly zodpovědné za 15 % a solidní tumory za 5 % případů. Patofyziologie vzniku deficitu aktivity vWF je u jednotlivých onemocnění odlišná.
Protilátky zaměřené na domény vWF byly detekovány v případech získané von Willebrandovy choroby přidružené k plazmocelulárním dyskraziím anebo k autoimunitní chorobě. Tyto protilátky vytváří s vWF imunitní komplexy, které jsou pak odstraňovány retikuloendoteliálním systémem. Je zde jistě i možnost neutralizačních protilátek, ale ty byly popsány jen vzácně. Dalším možným patofyziologickým mechanizmem vzniku von Willebrandova syndromu je snížení plazmatických koncentrací vWF díky selektivní adsorpci multimerů vWF na maligních buňkách. Tento mechanizmus byl také pozorován u lymfoproliferací typu mnohočetného myelomu, Waldenströmovy makroglobulinemie, nehodgkinských lymfomů, vlasatobuněčné leukemie i u solidních tumorů. V některých případech MGUS byla popsána aberantní plazmatická exprese glykoproteinu Ib (hlavní destičkový receptor vWF) na klonálních plazmocytech, což vedlo k vazbě vWF na tyto buňky a k akcelerované plazmatické clearence. Stejný mechanizmus snížení plazmatické aktivity vWF byl popsán u myeloproliferativních chorob [15–19].
Recentní klinická studie analyzovala 137 pacientů. Byl hodnocen účinek 1-deamino-8-D-arginin vasopresinu, dále pak factor replacement therapy a nitrožilní imunoglobuliny (IVIG). První skupina měla klinicky dobrou léčebnou odpověď ve 43,8 %, druhá ve 33,3 % a třetí v 85,4 %. Autoři této studie došli k závěru, že IVIG mají nejlepší účinnost u získaného von Willebrandova syndromu, který provází MGUS [20]. V textech přinášejících přehled léčby získaného von Willebrandova syndromu je léčba vysokými dávkami IVIG uváděna vedle substituční léčby koncentrátem von Willebrandova faktoru [21,22]. V databázi PubMed jsme do léta 2025 našli jen dva případy popisující přínos clone oriented therapy [23,24], zatímco prací popisujících přínos léčby pomocí IVIG je hodně. Je to pochopitelné, protože krvácení je komplikace, která se musí řešit okamžitě, zatímco nástup efektu clone oriented therapy je pozvolný.
Image 1. Znaky anemie s chladovými aglutininy 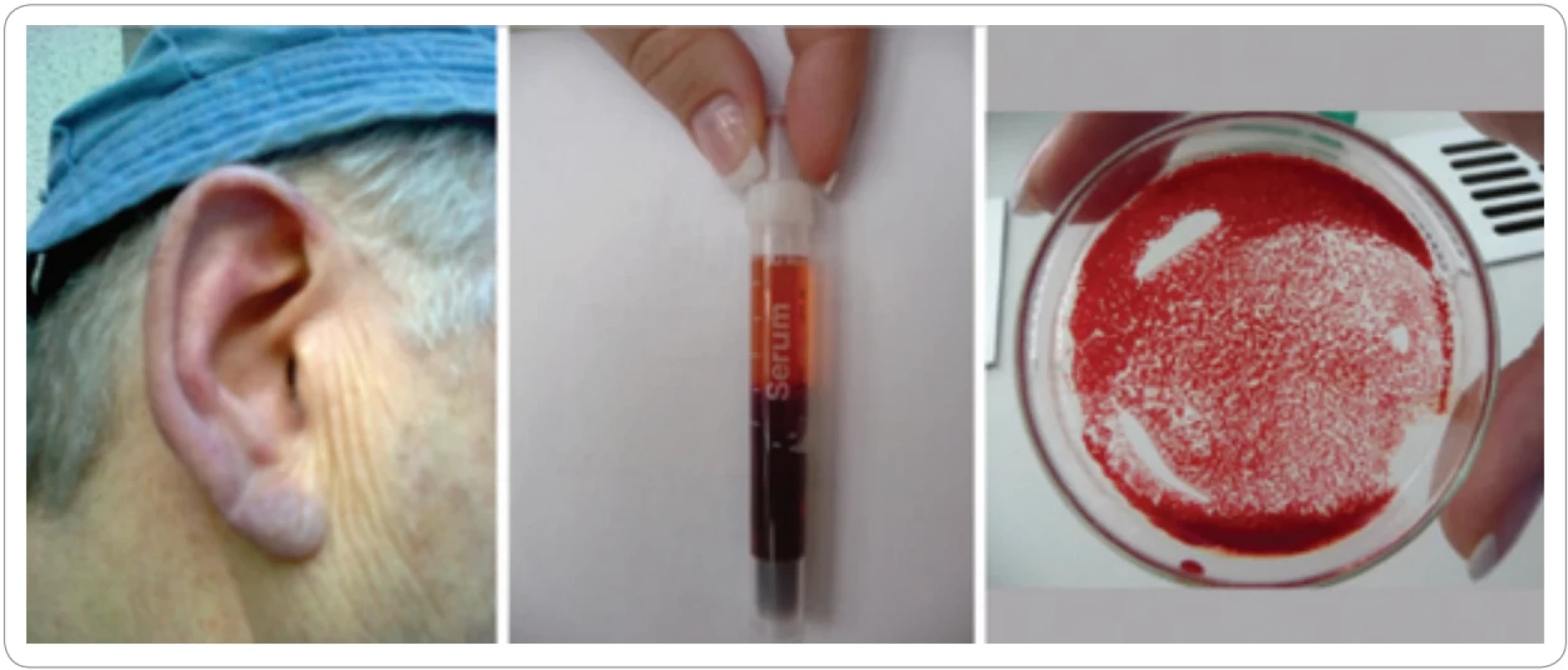
Charakteristické znaky chladových aglutininů: akrocyanóza na prochlazených místech těla. Po oddělení krve od séra vidíme červené zbarvení séra místo obvyklého žlutého (intravaskulární hemolýza). Po vystříknutí čerstvě odebrané krve na Petriho misku při pokojové teplotě ihned došlo k aglutinaci. Paradoxním problémem pacientů s chladovými aglutininy je, že infekce (horečka) zvýší koncentraci komplementu a výrazně zvýší intenzitu hemolýzy! Nemoc chladových aglutininů
Autoimunitní hemolytické anemie je skupinové označení pro hemolýzu způsobenou vazbou imunoglobulinů na erytrocyty. Rozlišují se dva zásadní typy, relativně častá autoimunitní hemolytická anemie s tepelnými protilátkami (autoimmune hemolytic anemia – AIHA) a relativně vzácnější hemolytická anemie s chladovými protilátkami (cold aglutinin disease – CAD) [25–27].
Epidemiologická data z ČR nemáme, k dispozici je analýza pacientů s autoimunitními hemolytickými anemiemi z USA, která proběhla v letech 2016–2023.
Incidence AIHA se pohybovala 1,4–6,6 / 100 000 obyvatel v jednotlivých databázích. Incidence CAD byla 0,6–1,2 / 100 000 obyvatel. Prevalence AIHA činila 4,2–20,6 / 100 000 obyvatel a prevalence CAD byla 1,4–3,0 / 100 000 obyvatel [28].
Chladové protilátky mají v 90 % případů charakter IgM imunoglobulinu a pouze v 10 % byl prokázán jiný typ imunoglobulinu. Obvykle se podaří prokázat CD20 pozitivní lymfoproliferaci v kostní dřeni. V případě CAD vyvolává expozice chladu ischemické problémy prochlazených akrálních částí těla a indukuje extravaskulární, ale i intravaskulární hemolýzu vazbou monoklonálního IgM na autoantigeny erytrocytů. Vazba chladových aglutininů na erytrocyty vzniká v chladu. Tato vazba nastartuje komplementem mediovanou hemolýzu. Proto také vzestup koncentrace komplementu při infekcích zvýší intenzitu hemolýzy a prohloubí anemii. V teple se zruší vazba chladové protilátky na erytrocyt, ale komplement dokončí svůj úkol – hemolýzu [29]. Typické projevy, akrocyanózu, okamžitou aglutinaci při vystříknutí krve na misku a známky intravaskulární hemolýzy ve zkumavce ilustruje obr. 1.
Dle mezinárodního doporučení pro získané hemolytické anemie z roku 2020 Diagnosis and treatment of autoimmune hemolytic anemia in adults: recommendations from the First International Consensus Meeting [29] se musí odlišit primární nemoc chladových aglutininů, u níž se v kostní dřeni nalézá jen menší klon B-lymfocytů, pro který bylo zvoleno označení primary CAD-associated lymphoproliferative disorder (LPD). Tento klon se může nepatrně odlišovat od lymfoplazmocytárního lymfomu nebo od lymfomu marginální zóny, které taktéž mohou produkovat chladové protilátky. Pokud histologické vyšetření prokáže v kostní dřeni lymfoplazmocytární lymfom nebo lymfom marginální zóny, tak mluvíme o nemoci chladových aglutininů provázející zjištěné maligní onemocnění [29].
Mutace MYD88 L265P je přítomna u všech případů lymfoplazmocytárního lymfomu, ale chybí u klonu CAD-associated LPD [29].
Hemolýzu lze zastavit podáním léčebné protilátky proti C5 složce komplementu neboli anti-C5 protilátky zvané ekulizumab. Tato protilátka má potenciál rychle zastavit hemolýzu způsobenou chladovými aglutininy. Pokud nejde o kritický stav, tak se obvykle podává kombinace rituximabu, dexametazonu a bendamustinu s cílem potlačit tvorbu monoklonálního IgM, který má vlastnost chladového aglutininu, jak popsal ve velké studii Berentsen [30].
V publikacích z roku 2024 a 2025 uvádí Berentsen také přínos kombinací zahrnujících bortezomib [31,32], obvykle v kombinaci s anti-CD20 monoklonální protilátkou (rituximab, obinutuzumab) [33]. Výjimečně lze použít i plazmaferézu [34].
Asociace monoklonálního imunoglobulinu s autoimunitními chorobami
Monoklonální imunoglobulin je častěji detekován u autoimunitních chorob než v průměrné populaci. Zde je pak problém rozpoznat, co je způsobeno monoklonálním imunoglobulinem a co samostatnou autoimunitní chorobou [35].
A někdy se popisuje souběh monoklonální gamapatie a autoimunitní nemoci, např. poškození oka při souběhu nemoci asociované s imunoglobulinem IgG4 (IgG4-related disease) a mnohočetným myelomem nebo autoimunitní encefalitis u pacienta s myelomem [36–40]. Zatím výjimečně popisovaná komplikace asociovaná s monoklonálním imunoglobulinem je inzulinový autoimunitní syndrom, který spontánními epizodami hyperinzulinové hypoglykemie způsobené autoprotilátkami proti inzulinu, které mohou mít také charakter monoklonálního imunoglobulinu. Příznaky tedy podobné jako způsobuje inzulinom [41,42]. Na našem pracovišti jsme se setkali s pacientkou se symptomatickou Waldenströmovou makroglobulinemií, která měla bolesti svalů a zvýšenou hladinu myoglobulinu a kreatinkinázy, což vypovídalo o poškození svalů. Po léčbě rituximabem a bendamustinem se dostala do kompletní remise a tyto potíže vymizely [43]. Usuzujeme tedy, že její potíže byly způsobeny monoklonálním IgM. V domácí literatuře byl popsán podobný případ [44].
Monoklonální imunoglobulin může tedy ojediněle způsobovat velmi pestré poškození vazbou na antigeny vlastních tkání a orgánů, ale prokázat to je problém. Nepřímo lze na souvislost usuzovat zpětně, pokud potlačení tvorby monoklonálního imunoglobulinu utlumí jím vyvolané problémy.
Neuropatie
Neuropatie a monoklonální gamapatie mohou mít souvislost. Monoklonální gamapatie je popisována u 10 % osob s periferní neuropatií. V případech, kdy je monoklonální gamapatie příčinou neuropatie, popisují jak domácí, tak i zahraniční autoři ústup neuropatie při léčbě potlačující tvorbu monoklonálního imunoglobulinu [45,46].
Monoklonální imunoglobulin může nervová vlákna poškozovat více mechanizmy, nejen svojí protilátkovou aktivitou, ale také depozicí amyloidu z lehkých řetězců, anebo k poškození nervů může docházet vlivem zvýšené hladiny vaskulárního endoteliálního růstového faktoru (VEGF), která provází POEMS syndrom.
U pacientů s abnormální hladinou VEGF a patologickým poměrem volných lehkých řetězců při senzorické a autonomní neuropatii bychom měli myslet na možnost AL-amyloidózy.
V případně monoklonální gamapatie typu lambda a klinickým fenotypem chronické inflamatorní demyelinizační neuropatie (chronic inflammatory demyelinating polyneuropathy – CIDP) by se měla zvážit možnost diagnózy POEMS syndromu.
Monoklonální imunoglobuliny typu IgM mají vyšší asociaci s neuropatiemi než ostatní typy gamapatií. Pacienti s monoklonálním imunoglobulinem typu IgM mohou mít distální demyelinizační senzomotorické onemocnění (distal acquired demyelinating symmetric polyneuropathy – DADS).
Monoklonální imunoglobulin typu IgM může mít vlastnosti autoprotilátky proti glykoproteinu asociovanému s myelinem (antibodies against myelin-associated glycoprotein – anti-MAG). Pokud tomu tak je, může být monoklonální imunoglobulin příčinou poškozování nervových vláken. S autoprotilátkami může být také asociováno neurologické onemocnění zvané CANOMAD syndrom, což je akronym vytvořený z počátečních písmen popisného názvu chronic ataxic neuropathy, ophthalmoplegia, monoclonal immunoglobulin IgM, cold agglutinins, and disialosyl antibodies. Pacienti s touto nemocí také mají prospěch z cílené léčby [45–50].
Autoři z Padovy zveřejnili vlastní algoritmus vyšetření pacientů s neuropatií, u nichž se prokáže monoklonální imunoglobulin. Jejich postup ilustruje schéma 1 a 2 [48,51,52]. Zodpovězení otázky, zda při koexistenci monoklonální gamapatie a neuropatie je mezi těmito fenomény příčinná souvislost, je velmi obtížné. Elektrofyziologické neurologické vyšetření je základem, ale je k němu třeba i dalších laboratorních metod. V případech, kdy neurologové prokáží souvislost mezi monoklonálním imunoglobulinem a neuropatií, je indikována léčba, která v současnosti má nejvyšší potenciál dosáhnout dlouhodobé kompletní hematologické remise neboli dosáhnout vymizení monoklonálního imunoglobulinu potvrzené negativním výsledkem imunofixační elektroforézy.
Schéma 1. Vyšetření prováděná u pacientů s monoklonální gamapatií typu IgM a neuropatií, potvrzenou neurofyziologickými testy [51]. ![Schéma 1. Vyšetření prováděná u pacientů s monoklonální gamapatií typu IgM a neuropatií, potvrzenou neurofyziologickými testy [51].](https://pl-master.mdcdn.cz/media/image/e6a002bfd1902e781ad5c79506cbf78b.png?version=1772166851)
anti-MAG – autoprotilátka proti glykoproteinu asociovanému s myelinem, CIDP – chronická infl amatorní demyelinizační polyneuropatie Schéma 2. Vyšetření prováděná u pacientů s monoklonální gamapatií typu IgG nebo IgA, potvrzenou neurofyziologickými testy [51]. ![Schéma 2. Vyšetření prováděná u pacientů s monoklonální gamapatií typu IgG nebo IgA, potvrzenou neurofyziologickými testy [51].](https://pl-master.mdcdn.cz/media/image/23485d491284024c7e6a42524fb43d4f.png?version=1772166899)
CIDP – chronická infl amatorní demyelinizační polyneuropatie, POEMS – polyneuropatie, organomegalie, endokrinopatie, monoklonální gamapatie, kožní změny, VEGF – vaskulární endoteliální faktor Poškození oka monoklonálním imunoglobulinem
Z očních manifestací monoklonální gamapatie je v lékařské veřejnosti znám nejvíce fundus paraproteinemicus. Ten jen však vázán spíše na maligní monoklonální gamapatii. Ostatní projevy jsou méně známé a snad právě proto byla v roce 2025 zveřejněna doposud největší analýza sumarizující téma gamapatie a oko [53]. Nejčastější je paraproteinemická keratopatie, na kterou by si měl oční lékař vzpomenout při nálezu oboustranných korneálních opacit, které může jinak chybně vyhodnotit jako korneální dystrofie či jizvy [53].
Frekvence očního poškození monoklonální gamapatií byla nedávno analyzována německými lékaři. Celkem 51 pacientů s monoklonální gamapatií (MGUS 19, mnohočetný myelom 32) podstoupilo podrobné oční vyšetření. U 19 pacientů byly nalezeny oboustranné korneální opacity [54].
I z dalších recentních publikací v oftalmologické literatuře vyplývá, že oční poškození monoklonálním imunoglobulinem nebude až tak raritní [55–60]. V domácí literatuře tuto problematiku popisují Skalická et al. [61].
Výjimečně mohou v oku vznikat depozita monoklonálního imunoglobulinu vázajícího měď [62]. A raritní je autoimunitní retinopatie asociovaná s monoklonální gamapatií [63,64].
Proto je nutné v případě, že posíláme pacienta s monoklonální gamapatií na oční vyšetření, upozornit na tuto možnost očního specialistu, protože monoklonální imunoglobulin může způsobit více typů poškození oka. Z tohoto důvodu se v americkém oftalmologickém časopise objevil termín monoclonal gammopathy of ocular significance [60].
Choroby s nejasnou rolí monoklonálního imunoglobulinu
U dvou chorob, jejichž diagnostika spadá do kompetence imunologických laboratoří, je často přítomný monoklonální imunoglobulin, ale příčinná souvislost zde není jasná, protože existují i další možné příčiny. Tyto choroby se projevují formou jednotlivých atak, takže zde budou ještě další faktory, které se podílejí na jejich manifestaci, nejen monoklonální imunoglobulin.
Capillary leak syndrome
Capillary leak syndrome neboli Clarkson syndrome (pojmenováno po autorovi prvního popisu syndromu z roku 1960) je choroba charakterizovaná epizodami zvýšené vaskulární permeability, zvýšené propustnosti pro ionty, vodu a bílkoviny, ne však po krvinky. To způsobuje závažnou hemokoncentraci a současně hypotenzi, hypovolemii a šok [65].
Capillary leak syndrome se manifestuje v jednotlivých atakách, mezi nimiž jsou období klidu.
Ke komplikacím tohoto syndromu patří plicní edém, akutní selhání ledvin, výpotky v perikardiální či pohrudniční dutině a také kompartmentové syndromy.
Nedávno byla popsána i chronická forma, které se projevuje refrakterním edémem, výpotky v serózních dutinách a závažnou hypoalbuminemií. Capillary leak syndrome lze charakterizovat třemi kritérii:
- hypotenzí se systolickým tlakem < 90 mm Hg;
- hemokoncentrací (hematokrit > 49–50 % u mužů a > 43–45 % u žen);
- hypoalbuminemií (albumin < 30 g/l).
Lékaři by si měli tuto diagnózu vždy vybavit u pacientů s nejasnými edémy, zvýšeným hematokritem, hypoalbuminemií a hypotenzí, případně s šokovým stavem nejasného původu [66].
Zvýšená hodnota hematokritu může vést k mylné diagnóze polyglobulie či polycytemie, jak popsali Doubek et al. [67]. Systémový capillary leak syndrome je třeba odlišit od podobné diagnózy, kterou je získaný angioedém, u něhož sice vznikají lokalizované edémy, ale nedochází k vzestupu hematokritu.
U osob splňujících kritéria capillary leak syndrome byl v 68–85 % případů prokázán monoklonální imunoglobulin, obvykle IgG nebo IgA kappa. Vysoká četnost monoklonální gamapatie u této jednotky znamená, že monoklonální imunoglobulin se nějakým způsobem podílí na etiopatogenezi. Jde ale o atakovité onemocnění, takže u něj jistě bude ještě další vyvolávající moment při monoklonální gamapatii, který celý patologický proces spustí. Existují také četné popisy případů, kdy je capillary leak syndrome dáván do souvislosti s očkováním, některými novými léky používanými pro léčbu maligních chorob nebo s virovými infekcemi.
Léčba akutního stavu je symptomatická – náhrada tekutin, stresová dávka kortikoidů, noradrenalin a literatura občas také zmiňuje terbutalin. Pro profylaxi recidiv je považováno za nejúčinnější podávání IVIG. Při potvrzení diagnózy se v jejich podávání pokračuje i mezi atakami jako prevence recidiv [68].
Francouzská skupina EurêClark hodnotila 59 pacientů. Léčebné podávání IVIG mělo alespoň jeden výpadek u 31 % pacientů a pravidelně dostávalo IVIG 69 % pacientů. Pravděpodobnost 10letého přežití byla ve skupině s pravidelným podáváním 83 %, zatímco ve skupině, v níž alespoň jednou došlo k přerušení podávání IVIG, jen 50 %. Nedodržování pravidelné aplikace IVIG bylo spojeno s vyšší rekurencí tohoto syndromu a vyšší mortalitou. Autoři uvádějí, že přerušení pravidelné aplikace IVIG je možné jen u dlouhodobě stabilních pacientů [69]. Zásadní přínos imunoglobulinů zde potvrdila i starší studie této skupiny, která hodnotila celkem 69 pacientů [70].
V literární databázi PubMed jsme k datu srpen 2025 našli jen dvě zprávy o přínosu léčby potlačující buněčný klon clone-oriented therapy, který produkuje monoklonální imunoglobulin [71,72]. Takže k získání jasného názoru, zda cílená léčba bude přínosem i pro tuto jednotku, bude zapotřebí více zkušeností.
Získaný angioedém
Angioedém neboli též angioneurotický edém je lokalizovaný otok vznikající na různých místech těla, nejčastěji však v oblasti kůže (hlavně obličej nebo končetiny), na sliznici dýchacího a trávicího ústrojí. Potíže, na které si nemocný stěžuje a které jej případně ohrožují, se liší podle postiženého místa. Angioedém může vyvolat život ohrožující komplikaci, pokud postihne hrtan, může dojít k udušení.
Případné postižení střeva s možnou edematózní střevní obstrukcí se může projevit atakami bolestí břicha závažnosti až náhlé příhody břišní. Tento typ ataky angioedému může být provázen případnou hypotenzí [73].
Typickou, a tedy diagnostickou vlastností angioedému je dobrá ohraničenost a postižení nejen kůže, ale i hlubších vrstev podkoží. Na rozdíl od kopřivky kůže nečervená a nesvědí. Ataky angioedému jsou náhlé a trvají několik dní. Lokální angioedém při nepřítomnosti kopřivky je vždy spojen s podezřením na proces vázaný na bradykinin.
Klíčovou patofyziologickou roli v rozvoji angioedému má deficit C1 inhibitoru (C1 INH). Následkem je zvýšená produkce především bradykininu. Ve valné většině případů je deficit vrozený, existuje ale i získaná forma. Získaný deficit C1 INH může souviset s autoimunitním onemocněním nebo lymfoproliferativní nemocí či monoklonální gamapatií [74–76].
Všechny osoby s podezřením na angioedém je nutno odeslat do specializovaných center, laboratorně se diagnóza stanoví na podkladě sníženého množství a poruchy funkce C1 INH. Výborným a široce dostupným screeningovým testem je velmi nízká hladina sérové C4 složky komplementu. U získaného angiodému lze často nalézt snížení hladiny C1q složky komplementu.
Pokud se získaný angioedém prokáže, je lékem volby u atak blokátor bradykininového receptoru icatibant. V profylaxi, případně i léčbě atak je možné použít C1 INH, nejčastěji získaný z plazmy dárců, případně i rekombinantně připravený [74–76]. V současné době probíhá intenzivní výzkum dalších léků použitelných pro vrozenou a zřejmě i získanou formu angioedému.
V roce 2021 vyšla práce analyzující pacienty se získaným angioedémem v ČR. Imunologická pracoviště v ČR v té době léčila 14 pacientů, kteří splňovali kritéria získaného angioedému. Medián věku těchto pacientů byl 59 let. Medián intervalu mezi prvními příznaky angioedému a stanovením diagnózy získaného angioedému byl 1 rok. Faciální edém měli všichni sledovaní pacienti. Otoky horních cest dýchacích trpělo 85,7 % pacientů. Všichni pacienti měli léčebnou odpověď na icatibant nebo na C1 inhibitor, ať již připravený z plazmy, nebo rekombinantní technologií. Lymfoidní malignity byly potvrzeny u devíti pacientů (64 %), bez upřesnění, zda byl, či nebyl přítomen monoklonální imunoglobulin. Monoklonální gamapatie byla známa u tří pacientů (21 %). Pouze jeden pacient měl autoimunitní chorobu, která byla provázena angioedémem. Pouze u jednoho pacienta ze 14 nebyla nalezena žádná nemoc, s níž by získaná forma angioedému souvisela [77,78].
Francouzští autoři zveřejnili svou analýzu 41 pacientů s MGUS a získaným angioedémem. U 68 % prokázali protilátky proti C1 inhibitoru. Monoklonální imunoglobulin typu IgM prokázali u 24 pacientů, IgG u 11 a IgA u 6 pacientů [79]. Klinický průběh pacientů s přítomnou gamapatií se podobal průběhu skupiny bez gamapatie [80]. Přínos léčby potlačující tvorbu monoklonálního imunoglobulinu u této jednotky není zatím jasně prokázán [81]. Pokud jsou prokázány protilátky proti C1 inhibitoru, tak se jako u jiných autoimunitních chorob může použít rituximab, i když nebyla prokázána žádná B-buněčná lymfoproliferace [82].
Závěr
Cílem našeho textu je upozornit na novou jednotku MGCS, která zatím nemá přidělen kód v 10. verzi Mezinárodních klasifikací nemocí [83]. Proto tyto jednotky unikají zatím evidenci. Uvedením přehledu všech nemocí, které jsou v současnosti řazeny do skupiny MGCS, chceme přispět k lepší diagnostice, a tedy i léčbě těchto vzácných chorob, a podpořit začlenění této diagnózy do nové Mezinárodní klasifikace nemocí.
Protože těchto jednotek je velmi mnoho, tak závěrem uvedeme pravidlo, jehož dodržování by mohlo zvýšit frekvenci záchytu těchto chorob:
- U pacienta, jehož příznaky nejsou jednoduše vysvětlitelné a zdůvodnitelné, proveďte vyšetření přítomnosti monoklonálního imunoglobulinu, polyklonálních imunoglobulinů a volných lehkých řetězců [84].
- Pokud jsou výsledky těchto vyšetření patologické, tak lze hledat souvislost v odborné literatuře a v databázi PubMed zadáním anglického termínu pro patologické nálezy a hesla „monoclonal gammopathy“. Např. do vyhledávače PubMed napsat „pemphigus and monoclonal gammmopathy“ a objeví se články s tímto tématem a je možné, že v nich naleznete problém vašeho pacienta, a podaří se vám tak pojmenovat onemocnění a vybrat vhodnou léčbu.
- Alternativou je poslat pacienta za hematologem, o němž víte, že hledání těchto souvislostí a diagnóz je pro něj zábavnější a přitažlivější než čtení detektivky.
Dedikace
Publikace byla vytvořena na podporu těchto aktivit: MZ ČR – RVO (FNBr, 65269705) a Institucionální aktivity MOÚ: MZ ČR – RVO (MOÚ, 00209805).
Sources
1. Gkalea V, Fotiou D, Dimopoulos MA et al. Monoclonal gammopathy of thrombotic significance. Cancers (Basel) 2023; 15 (2): 480. doi: 10.3390/cancers15020480.
2. Gkalea V, Fotiou D, Kastritis E. More on monoclonal gammopathy of thrombotic significance. N Engl J Med 2024; 391 (15): 1463–1464. doi: 10.1056/NEJMc2411324.
3. Rögnvaldsson S, Gasparini A, Thorsteinsdottir S et al. Monoclonal gammopathy of undetermined significance and the risk of thrombotic events: results from iStopMM, a prospective population-based screening study. Br J Haematol 2025; 206 (3): 899–906. doi: 10.1111/bjh.19957.
4. Radocha J, Maisnar V. Tromboprofylaxe u monoklonálních gamapatií. Cesk Geriatr Revue 2007; 5 (3): 129–133.
5. Dulíček P, Maisnar V. Možné klinické projevy přítomnosti M-Ig. Změny hemostázy vlivem přítomnosti monoklonálního imunoglobulinu. Monoklonální imunoglobuliny – výskyt, význam a možnosti jejich průkazu. Praha: Nucleus HK 2012 : 90–92.
6. Špička I, Cieslar P, Hrkal Z et al. Vliv paraproteinu na antitrombotické mechanismy – další typ interference paraproteinu s hemostázou. Cas Lek Cesk 1996; 135 (4): 126–127.
7. Chen H, Zhang Y, Wang Z et al. Thrombotic events in patiens with multiple myeloma and their impact on overall survival. Hematology 2025; 30 (1): 2464316. doi: 10.1080/16078454.2025.2464316.
8. Kanack AJ, Schaefer JK, Sridharan M et al. Monoclonal gammopathy of thrombotic/thrombocytopenic significance. Blood 2023; 141 (14): 1772–1776. doi: 10.1182/blood.2022018797.
9. Kanack AJ, Leung N, Padmanabhan A. Diagnostic complexity in monoclonal gammopathy of thrombotic significance. N Engl J Med 2024; 391 (20): 1961–1963. doi: 10.1056/NEJMc2409428.
10. Mainville L, Coitoru D. Monoclonal gammopathy of thrombotic significance. Br J Dermatol 2025; 193 (4): 807. doi: 10.1093/bjd/ljaf144.
11. Siddiq N, Bergstrom C, Anderson LD et al. Bleeding due to acquired dysfibrinogenemia as the initial presentation of multiple myeloma. BMJ Case Rep 2019; 12 (7): e229312. doi: 10.1136/bcr-2019-229312.
12. Zhang S, Chen Z, Huang M et al. Monoclonal gammopathy of undetermined significance (MGUS) characterized by refractory lower gastrointestinal postoperative bleeding with coagulopathy. Intractable Rare Dis Res 2022; 11 (4): 206–210. doi: 10.5582/irdr.2022.01120.
13. Ohara F, Suzuki A, Suzuki N et al. Newly diagnosed multiple myeloma with bleeding and coagulation abnormalities caused by a thrombin-inhibiting substance. Int J Hematol 2024; 120 (6): 743–749. doi: 10.1007/s12185-024-03849-2.
14. Trabelsi B, Baccouche H, Eddhib J et al. Acquired factor XIII deficiency and its unprecedented association with multiple myeloma: case report and literature review. Blood Coagul Fibrinolysis 2024; 35 (5): 293–295. doi: 10.1097/MBC.0000000000001311.
15. Vengenechten I, Smejkal P, Zapletal O et al. Analysis of von Willebrand disease in the South Moravian population (Czech Republic): results from the BRNO-VWD study. Thromb Haemost 2019; 119 (4): 594–605. doi: 10.1055/s-0039-1678528.
16. Penka M, Smejkal P, Matýšková M et al. K diagnostice von Willebrandovy choroby. Laboratorní hematologie. Hradec Králové: HK Credit 2006 : 46–48.
17. Drenko P, Přenosilová P, Lavičková A et al. Acquired von Willebrand syndrome (AvWS).Vnitr Lek 2022; 68 (4): E16–E19.
18. Nicol C, Pan-Petesch B, Ianotto JC. Acquired von Willebrand syndrome and lymphoid neoplasms: a review of malignancy management, and propositions of practical recommendations. Haemophilia 2022; 28 (6): 938–949. doi: 10.1111/hae.14648.
19. Galletta E, Galvanin F, Bertomoro A et al. Acquired von Willebrand syndrome in patiens with monoclonal gammopathy of undetermined significance investigated using a mechanistic approach. Blood Transfus 2023; 21 (1): 74–82. doi: 10.2450/2021.0121-21.
20. Abou-Ismail MY, Rodgers GM, Bray PF et al. Acquired von Willebrand syndrome in monoclonal gammopathy – a scoping review on hemostatic management. Res Pract Thromb Haemost 2021; 5 (2): 356–365. doi: 10.1002/rth2.12481.
21. Ghariani I, Braham N, Veyradier A et al. Acquired von Willebrand syndrome: five cases report and literature review. Thromb Res 2022; 218 : 145–150. doi: 10.1016/j.thromres.2022.08.025.
22. Langer AL, Connell NT. Acquired von Willebrand syndrome. Hematol Oncol Clin North Am 2021; 35 (6): 1103–1116. doi: 10.1016/j.hoc.2021.07.005.
23. Mathew Thomas V, Gilreath JA, Newton S et al. Daratumumab as a novel treatment for refractory acquired von Willebrand syndrome associated with monoclonal gammopathy. Haemophilia 2021; 27 (4): e563–e566. doi: 10.1111/hae.14323.
24. Shah CP, Delaune J, Mandernach MW. Acquired von Willebrand syndrome in association with multiple myeloma: remission after stem cell transplant. BMJ Case Rep 2021; 14 (1): e239053. doi: 10.1136/bcr-2020 - 239053.
25. Čermák J, Písačka M. Autoimmune hemolytic anemia. Vnitr Lek 2018; 64 (5): 514–519.
26. Gumulec J, Brát R, Kolek M et al. Pre-operative care for cardiac surgery patients with cold antibody disorder, cryoglobulinaemia and cryofibrinogenemia. Vnitr Lek 2009; 55 (3): 236–241.
27. Adam Z, Pejchvalová A, Chlupová G et al. Cold agglutinin disease – no response to glucocorticoids and rituximab, what treatment is best for the 3rd line of therapy? Case report and review of the literature. Vnitr Lek 2013; 59 (9): 828–840.
28. Bozzi S, Umarje S, Hawaldar K et al. Prevalence and incidence of primary autoimmune hemolytic anemia and cold agglutinin disease in the United States, 2016–2023. PLoS One 2025; 20 (6): e0323843. doi: 10.1371/journal.pone.0323843.
29. Jäger U, Barcellini W, Broome CM et al. Diagnosis and treatment of autoimmune hemolytic anemia in adults: recommendations from the First International Consensus Meeting. Blood Rev 2020; 41 : 100648. doi: 10.1016/j.blre.2019.100648.
30. Berentsen S, Barcellini W, D‘Sa S et al. Cold aglutinin disease revisited: a multinational observational study od 232 patiens. Blood 2020; 136 (4): 480–488. doi: 10.1182/blood.2020005674.
31. Berentsen S. Cold-antibody autoimmune hemolytic anemia: its association with neoplastic disease and impact on therapy. Curr Oncol Rep 2024; 26 (9): 1085–1096. doi: 10.1007/s11912-024-01569-8.
32. Berentsen S. Treatment of autoimmune hemolytic anemia: novel and investigational approaches. Minerva Med 2025; 116 (3): 249–264. doi: 10.23736/S0026 - 4806.25.09617-X.
33. Piatek C, Murakhovskaya I, Karaouni A et al. Real - -world use of rituximab in the treatment of cold agglutinin disease in the United States: a retrospective study. EJHaem 2025; 6 (4): e70082. doi: 10.1002/jha2.70082.
34. Shima T, Iwasaki H, Henzan T et al. Successful management of total plasma exchange for hemolytic cold agglutinin disease. Intern Med 2025; 64 (1): 119–122. doi: 10.2169/internalmedicine.3606-24.
35. Quartuccio L, Manfrè V, Treppo E et al. Monoclonal Gammopathy of Rheumatologic Significance (MGRhS): a systemic vision of clonal disorders with multiple organ involvement. Autoimmun Rev 2025; 24 (11): 103895. doi: 10.1016/j.autrev.2025.103895.
36. Liang S, Xu W, Zhong P et al. Case report: IgG4-RD-related ophthalmopathy combined with monoclonal gammopathy of undetermined significance. Front Immunol 2025; 16 : 1565388. doi: 10.3389/fimmu.2025.1565388.
37. Cheng Z, Song Y, Zhao S et al. Anti-GluK2 antibody-positive autoimmune encephalitis concurrent with multiple myeloma: a case report. BMC Neurol 2025; 25 (1): 27. doi: 10.1186/s12883-025-04037-3.
38. Musilová L, Kryštůfková O. Monoklonální gamapatie u systémových onemocnění pojiva. Rheumatologia (Bratislava) 2002; 16 (1): 31–36.
39. Jonsson V, Kierkegaard A, Salling S et al. Autoimunity in Waldenström‘s macroglobulinemia. Leukemia Lymphoma 1999; 34 (3–4): 373–379. doi: 10.3109/10428199909050962.
40. Sigurbergsdóttir AÝ, Love TJ, Kristinsson SY. Autoimmunity, infections, and the risk of monoclonal gammopathy of undetermined significance. Front Immunol 2022; 13 : 876271. doi: 10.3389/fimmu.2022.876271.
41. Askeland FB, Frøen HM, Bolstad N et al. Monoclonal insulin autoimmune syndrome successfully treated with plasma cell directed therapy. Clin Lymphoma Myeloma Leuk 2025; 25 (3): e127–e130. doi: 10.1016/j.clml.2024.10.005.
42. Clifford L, Joseph F, Joshi T. A clinical case of insulin autoimmune syndrome with monoclonal gammopathy of uncertain significance; complexity in management. Oxf Med Case Reports 2024; 2024 (6): omae054. doi: 10.1093/omcr/omae054.
43. Adam Z, Kissová J, Pour L et al. Myopathy in patients with Waldenströms macroglobulinemia. A case study and an overview of autoimmune expressions of type IgM monoclonal immunoglobulins. Vnitr Lek 2015; 61 (9): 821–828.
44. Forgáč M, Uher T, Zámečník J. Nemalinová myopatie asociovaná s monoklonální gamapatií – kazuistika. Cesk Slov Neurol N 2014; 77/110 (2): 247–250.
45. Pika T, Folprechtová P, Roubalová L et al. Úspěšná léčba anti MAG neuropatie asociované s monoklonální gamapatií nejistého významu kombinací rituximabu s dexametazonem – kazuistika. Cesk Slov Neurol N 2015; 78/111 (4): 474–476. doi: 10.14735/amcsnn2015474.
46. Le Cann M, Bouhour F, Viala K et al. CANOMAD: a neurological monoclonal gammopathy of clinical significance that benefits from B-cell-targeted therapies. Blood 2020; 136 (21): 2428–2436. doi: 10.1182/blood.2020007092.
47. Traub R, Qarni T, Cohen AD et al. Paraproteinemic neuropathies. Muscle Nerve 2024; 70 (2): 173–179. doi: 10.1002/mus.28164.
48. Min YG, Visentin A, Briani C et al. Neuropathy with anti-myelin-associated glycoprotein antibodies: update on diagnosis, pathophysiology and management. J Neurol Neurosurg Psychiatry 2025; 96 (4): 340–349. doi: 10.1136/jnnp-2024-334678.
49. Klein CJ, Triplett JD, Murray DL et al. Optimizing anti-myelin-associated glycoprotein and IgM-gammopathy testing for neuropathy treatment evaluation. Neurology 2024; 103 (11): e210000. doi: 10.1212/WNL.0000000000210000.
50. Perrain V, Molinier-Frenkel V, Dupuis J et al. Prevalence and spectrum of neuropathies in a cohort of 585 patients with immunoglobulin a monoclonal gammopathy. Eur J Neurol 2025; 32 (2): e70087. doi: 10.1111/ene.70087.
51. Visentin A, Pravato S, Castellani F et al. From biology to treatment of monoclonal gammopathies of neurological significance. Cancers (Basel) 2022; 14 (6): 1562. doi: 10.3390/cancers14061562.
52. Briani C, Visentin A, Cerri F et a. From pathogenesis to personalized treatments of neuropathies in hematological malignancies. J Peripher Nerv Syst 2020; 25 (3): 212–221. doi: 10.1111/jns.12405.
53. Ripa M, Schipa C, Aceto P et al. Exploring the ocular involvement in multiple myeloma: a comprehensive review of 70-year clinical studies. Int Ophthalmol 2025; 45 (1): 89. doi: 10.1007/s10792-025-03467-9.
54. Al Hariri M, Munder M, Lisch W et al. Prevalence of corneal findings and their interrelation with hematological findings in monoclonal gammopathy. PLoS One 2022; 17 (10): e0276048. doi: 10.1371/journal.pone.0276048.
55. Nouira C, Ghazal W, Panthier C et al. Monoclonal gammopathy presenting with paraproteinemic keratopathy documented with anterior segment OCT: a case report. BMC Ophthalmol 2025; 25 (1): 356. doi: 10.1186/s12886-025-04161-1.
56. Garderet L, Al Hariri M, Wasielica-Poslednik J et al. Monoclonal gammopathy of ocular significance (MGOS) – a short survey of corneal manifestations and treatment outcomes. Leuk Lymphoma 2022; 63 (4): 984–990. doi: 10.1080/10428194.2021.2008385.
57. Kormányos K, Kovács K, Németh O et al. Ocular signs and ocular comorbidities in monoclonal gammopathy: analysis of 80 subjects. J Ophthalmol 2021; 2021 : 9982875. doi: 10.1155/2021/9982875.
58. Singh RB, Singhal S, Sinha S et al. Ocular complications of plasma cell dyscrasias. Eur J Ophthalmol 2023; 33 (5): 1786–1800. doi: 10.1177/11206721231155974.
59. Lindemann C, Enders P, Brinkkoetter PT et al. Crystalline deposits in the cornea and various areas of the kidney as symptoms of an underlying monoclonal gammopathy: a case report. BMC Nephrol 2021; 22 (1): 117. doi: 10.1186/s12882-021-02309-x.
60. Karakus S, Gottsch JD, Caturegli P et al. Monoclonal gammopathy of „ocular“ significance. Am J Ophthalmol Case Rep 2019; 15 : 100471. doi: 10.1016/j.ajoc.2019.100471.
61. Skalicka P, Dudakova L, Palos M et al. Paraproteinemic keratopathy associated withmonoclonal gammopathy of undetermined significance (MGUS): clinical findings in twelve patiens including recurrence after keratoplasty. Acta Ophthalmol 2019; 97 (7): e987–e992. doi: 10.1111/aos.14123.
62. Del-Pozo-Lérida S, Llopart AS, Widmer-Pintos J et al. Bilateral corneal copper deposition in monoclonal gammopathy of undetermined significance: diagnostic insights and treatment with descemet membrane endothelial keratoplasty and descemet stripping only. Cornea 2025; 44 (9): 1192–1196. doi: 10.1097/ICO.0000000000003880.
63. Thomson AC, Raviskanthan S, Mortensen PW et al. Paraneoplastic autoimmune retinopathy associated with non-IgM lymphoplasmacytic lymphoma. J Neuroophthalmol 2023; 43 (4): e184–e187. doi: 10.1097/WNO.0000000000001450.
64. Bergman Z, Mohammed T, Schocket L et al. Autoimmune retinopathy in a patient with smoldering multiple myeloma: a case report. Doc Ophthalmol 2024; 148 (3): 167–171. doi: 10.1007/s10633-024-09965-y.
65. Clarkson B, Thompson D, Horwith M et al. Cyclical edema and shock due to increased capillary permeability. Am J Med 1960; 29 : 193–216. doi: 10.1016/0002-9343 (60) 90018-8.
66. Ounci-Essad, Bouchlarhem A, Lamzouri O et al. Consider systemic capillary leak syndrome in monoclonal gammopathy with shock. Ann Med Surg (Lond) 2021; 72 : 103013. doi: 10.1016/j.amsu.2021.103013.
67. Doubek M, Brychtové Y, Tomíška M et al. Idiopathic systemic capillary leak syndrome misdiagnosed and treated as polycythemia vera. Acta Haematol 2005; 113 (2): 150–151. doi: 10.1159/000083455.
68. Pecker MS, Hammudi M, Melchio R et al. Management of acute episodes of Clarkson disease (monoclonal gammopathy-associated systemic capillary leak syndrome) with intravenous immunoglobulins. Ann Intern Med Clin Cases 2022; 1 (6). doi: 10.7326/aimcc.2022.0496.
69. Moyon Q, Pineton de Chambrun M, Gousseff M et al. Intravenous immunoglobulins tapering and withdrawal in systemic capillary leak syndrome (Clarkson disease). J Allergy Clin Immunol Pract 2022; 10 (11): 2889–2895. doi: 10.1016/j.jaip.2022.07.006.
70. Pineton de Chambrun M, Gousseff M, Mauhin W et al. Intravenous immunoglobulins improve survival in monoclonal gammopathy-associated systemic capillary-leak syndrome. Am J Med 2017; 130 (10): 1219.e19–1219.e27. doi: 10.1016/j.amjmed.2017.05.023.
71. Hermida G, Alvarez-Nuño R, San Miguel-Izquierdo J et al. Long term remission of capillary leak syndrome associated with monoclonal gammopathy with progression to multiple myeloma after autologous stem cell transplantation: a case report and review of the literature. Oncol Ther 2024; 12 (1): 183–188. doi: 10.1007/s40487-024-00263-w.
72. Bu Q, Zhou H, Gao W et al. Systemic capillary leak syndrome associated with smouldering multiple myeloma treated by bortezomib plus dexamethasone: a case report. Br J Haematol 2025. doi: 10.1111/bjh.20193.
73. Pinto AR, Carolino F. Acute abdominal pain as the initial presentation of an acquired C1 inhibitor deficiency. GE Port J Gastroenterol 2023; 31 (4): 273–277. doi: 10.1159/000533179.
74. Šantavý O, Žák J. Angioedém na podkladě deficitu C1 inhibitoru. Vnitr Lek 2025; 71 (1): 47–49.
75. Sobotková M. Současná doporučení v léčbě hereditárního angioedému. [online]. Dostupné z: https: //farmakoterapeutickarevue.cz/cs/soucasna-doporuceni-v-lecbe-hereditarniho-angioedemu.
76. Sobotková M, Segethová J. Získaný angioedém s deficitem C1 inhibitoru u pacientky s B-lymfomem nízké malignity a efekt léčby základního onemocnění na projevy angioedému. Trans Hematol Dnes 2017; 23 (3): 145–150.
77. Sobotkova M, Zachova R, Hakl R et al. Acquired angioedema with C1 inhibitor deficiency: occurrence, clinical features, and management: a Nationwide retrospective study in the Czech Republic patients. Int Arch Allergy Immunol 2021; 182 (7): 642–649. doi: 10.1159/000512933.
78. Sobotková M, Zachová R, Hakl R et al. Získaný angioedém s deficitem C1 inhibitoru – výsledky retrospektivní studie z České republiky. 2020 [online]. Dostupné z: https: //uia.fnplzen.cz/sites//users/uia2/Ziskany%20angioedem%20s%20deficitem%20C1%20inhibitoru-vysledky%20retrospektivni%20studie%20z%20%C4% 8CR.pdf.
79. Lahuna C, Defendi F, Bouillet L et al Angioedema due to acquired C1-inhibitor deficiency associated with monoclonal gammopathies of undetermined significance characteristics of a French national cohort. J Allergy Clin Immunol Pract 2024; 12 (12): 3283–3291. doi: 10.1016/j.jaip.2024.09.016.
80. Stammler R, Defendi F, Aubineau M et al. Angioedema due to acquired C1-inhibitor deficiency without hematological condition: a multicenter French cohort study of 34 patients. J Allergy Clin Immunol Pract 2025; 13 (3): 542–550.e2. doi: 10.1016/j.jaip.2024.12.027.
81. Petersen RS, Fijen LM, Franssen LE et al. Daratumumab-based treatment of monoclonal gammopathy-associated angioedema due to acquired C1-inhibitor deficiency. J Allergy Clin Immunol Glob 2024; 3 (4): 100322. doi: 10.1016/j.jacig.2024.100322.
82. Kalmi G, Nguyen Y, Amarger S et al. Efficacy and safety of rituximab-based treatments in angioedema with acquired C1-inhibitor deficiency. J Allergy Clin Immunol Pract 2024; 12 (1): 212–222. doi: 10.1016/j.jaip.2023.10.017.
83. Dispenzieri A. Monoclonal gammopathies of clinical significance. Hematology Am Soc Hematol Educ Program 2020; 2020 (1): 380–388. doi: 10.1182/hematology.2020000122.
84. Kušnierová P. Laboratorní diagnostika monoklonálních gamapatií. Ostravská univerzita 2022.
Labels
Paediatric clinical oncology Surgery Clinical oncology
Article was published inClinical Oncology

2026 Issue 1-
All articles in this issue
- Dimenze onkochirurgie II
- O tvrdosti dat
- Kožní nemoci způsobené monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci (monoklonální gamapatie kožního významu)
- Změny hemostázy a další poruchy způsobené monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci
- Fenomén nádeje, ako neoddeliteľná súčasť starostlivosti o onkologického pacienta v terminálnom štádiu
- Výsledky léčby Hodgkinova lymfomu v České republice
- Rozsah reportování při vyšetření predispozice k nejčastějším solidním nádorům dospělého věku pomocí sekvenování nové generace
- Logopedická intervence u pacientky s mnohočetným myelomem a dysfagií – případová studie z klinické praxe
- Strategie snižování rizik „harm reduction“ jako součást primární prevence
- AKTUALITY Z NÁRODNÍHO ÚSTAVU PRO VÝZKUM RAKOVINY
- Clinical Oncology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Rozsah reportování při vyšetření predispozice k nejčastějším solidním nádorům dospělého věku pomocí sekvenování nové generace
- Výsledky léčby Hodgkinova lymfomu v České republice
- Kožní nemoci způsobené monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci (monoklonální gamapatie kožního významu)
- Změny hemostázy a další poruchy způsobené monoklonálním imunoglobulinem a/nebo volnými lehkými řetězci
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

