-
Medical journals
- Career
Výsledky léčby Hodgkinova lymfomu v České republice
Authors: H. Móciková; J. Michalka; A. Sýkorová; M. Lukášová; K. Hradská; N. Černá; J. Baranová; J. Marková; Ľ. Gahérová; M. Maco; E. Maule; A. Janíková; P. Štěpánková; A. Kredátusová; J. Ďuraš; V. Procházka; Z. Král; T. Kozák
Authors‘ workplace: Hematologická klinika 3. LF UK a FN Královské Vinohrady, Praha 1; Interní hematologická a onkologická klinika LF MU a FN Brno 2; IV. interní hematologická klinika LF v Hradci Králové UK a FN Hradec Králové 3; Hematoonkologická klinika LF UP a FN Olomouc 4; Klinika hematoonkologie LF OU a FN Ostrava 5; Institut biostatistiky a analýz, s. r. o, Brno 6
Published in: Klin Onkol 2026; 39(1): 45-55
Category: Original Articles
doi: https://doi.org/10.48095/ccko202645Overview
Východiska: Cílem analýzy bylo vyhodnocení účinnosti léčby a jejího vlivu na prognózu pacientů s Hodgkinovým lymfomem (HL) zařazených do českého registru HL. Soubor pacientů a metody: Do analýzy bylo zařazeno 2 241 hodnotitelných pacientů s klasickým HL (cHL) a 130 pacientů s HL s nodulární lymfocytární predominancí (nodular lymphocyte-predominant Hodgkin lymphoma – NLPHL), kteří byli léčeni v letech 2000–2024. Medián věku při diagnóze cHL byl 37 let a u NLPHL 42 let. Výsledky: Nejčastějším režimem u pacientů v časných a intermediárních stadiích byl režim ABVD (doxorubicin, bleomycin, vinblastin, dakarbazin) s radioterapií (RT), navíc u pacientů ve věku < 60 let v intermediárních stadiích byly použity dva cykly eskalovaného režimu BEACOPP (bleomycin, etoposid, doxorubicin, cyklofosfamid, vinkristin, prokarbazin, prednison) v kombinaci s dvěma cykly ABVD a RT. V pokročilém stadiu byl u pacientů ve věku < 60 let nejčastěji použit eskalovaný režim BEACOPP (4–8 cyklů) a u pacientů ve věku ≥ 60 let režim ABVD (6–8 cyklů). U pacientů s NLPHL byla použita dle klinického stadia samostatná RT nebo kombinace rituximabu s chemoterapií +/−RT. U pacientů s cHL ve věku < 60 let bylo 10leté přežití bez progrese (progression free survival – PFS) a celkové přežití (overall survival – OS) v iniciálních stadiích 91,5 % a 94,2 %, v intermediárních stadiích 91,0 % a 96,6 % a v pokročilých stadiích 83,9 % a 92,6 %. U cHL ve věku ≥ 60 let bylo 10leté PFS a OS v iniciálních stadiích 67,0 % a 74,2 %, v intermediárních stadiích 36,4 % a 45,7 %, v pokročilých stadiích 41,6 % a 52,0 %. U NLPHL bylo 10leté PFS a OS 77,5 % a 95,8 %. Závěr: Podle dat z registru je prognóza HL výborná u pacientů ve věku < 60 let – 10letého OS dosahuje více než 90 % pacientů. Ve věku ≥ 60 let je medián přežití kolem 10 let. Zavedení checkpoint inhibitorů a brentuximab vedotinu do 1. linie léčby dále zlepší účinnost a sníží toxicitu léčby.
Klíčová slova:
Hodgkinův lymfom – ABVD – BEACOPP
Úvod
Registr Hodgkinova lymfomu prospektivně sbírá a vyhodnocuje prognostické faktory a léčbu pacientů s Hodgkinovým lymfomem (HL) v České republice (ČR). Do registru jsou zahrnuta data z pěti center v ČR (Hematologická klinika FN Královské Vinohrady Praha, Interní hematologická a onkologická klinika FN Brno, Interní hematologická klinika FN Hradec Králové, Hematoonkologická klinika FN Olomouc a Klinika hematoonkologie FN Ostrava), která jsou vedena v databázi Institutu biostatistiky a analýz, s. r. o. Cílem této analýzy bylo vyhodnocení účinnosti léčby a její vliv na dlouhodobé přežití pacientů s HL. V současnosti se zkoumá význam cirkulující nádorové DNA pro biologii cHL a NLPHL při diagnóze a v relapsu, dále pro sledování minimální reziduální nemoci v průběhu léčby a po léčbě. K úspěšné léčbě HL v ČR významně přispěla spolupráce s Německou studijní skupinou Hodgkinova lymfomu (German Hodgkin Study Group – GHSG), která umožnila aktivní zapojení hematologických klinik z Prahy a z Brna do mezinárodních randomizovaných studií GHSG fáze III. Proto i léčba všech klinických stadií byla vedena převážně podle výsledků klinických studií GHSG.
Pacienti a metody
Všichni pacienti podepsali informovaný souhlas s účastí v registru Hodgkinova lymfomu včetně sběru dat a statistických analýz, který byl schválen multicentrickou etickou komisí ve Fakultní nemocnici Královské Vinohrady v Praze. Tato analýza byla provedena v souladu s Helsinskou deklarací. Histologické nálezy byly potvrzeny čtením v referenčních ústavech patologie ČR. Z celkového počtu 2 800 pacientů bylo do analýzy zařazeno 2 241 pacientů s cHL (80,0 %) a 130 pacientů s NLPHL (4,6 %) s vyplněnými formuláři, kteří byli léčeni v letech 2000–2024. Medián věku při diagnóze byl 37 let (rozmezí 18–91) u cHL a 42 let (rozmezí 18–76) u NLPHL.
Standardní diagnostický postup zahrnoval fyzikální a laboratorní vyšetření, pozitronovou emisní tomografii v kombinaci s počítačovou tomografií (PET/CT) nebo samostatné CT krku, hrudníku, břicha a malé pánve. V rámci určení klinického stadia po zavedení PET/CT se od roku 2014 upustilo od rutinního vyšetření kostní dřeně [1]. Charakteristiky pacientů cHL a NLPHL jsou uvedeny v tab. 1 a 2.
Table 1. Charakteristika pacientů s klasickým Hodgkinovým lymfomem. 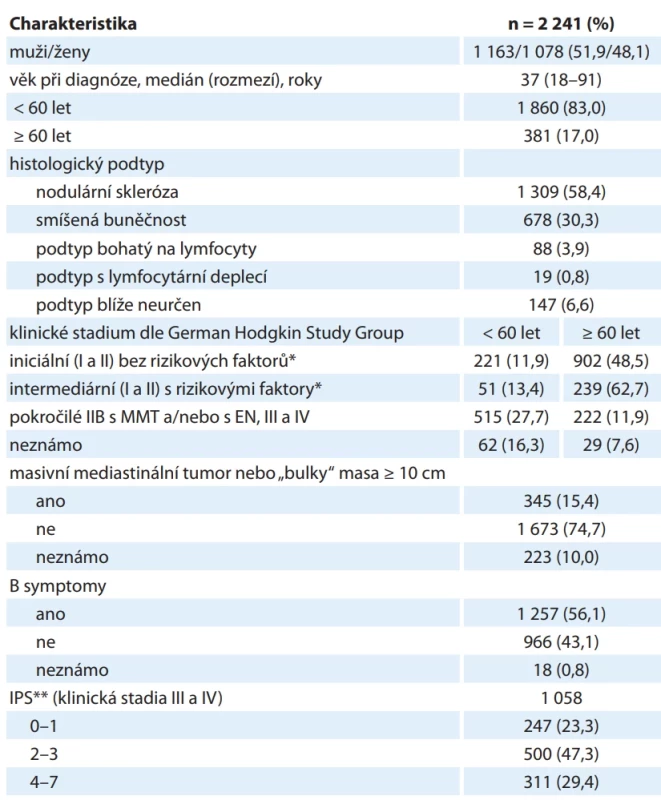
*rizikové faktory: masivní mediastinální tumor (MMT) > 1/3 průměru hrudníku nebo mediastinální masa > 10 cm, extranodální postižení (EN), FW > 50 mm/h (bez B symptomů) nebo FW > 30 mm/h (s B symptomy); **Mezinárodní prognostické skóre
(IPS): albumin v séru < 40 g/l, Hb < 105 g/l, mužské pohlaví, klinické stadium IV, věk > 45 let, leukocyty > 15×109 /l, lymfocyty < 0,6×109 /l nebo < 8 % z leukocytůTable 2. Charakteristika pacientů s Hodgkinovým lymfomem s nodulární lymfocytární predominancí. 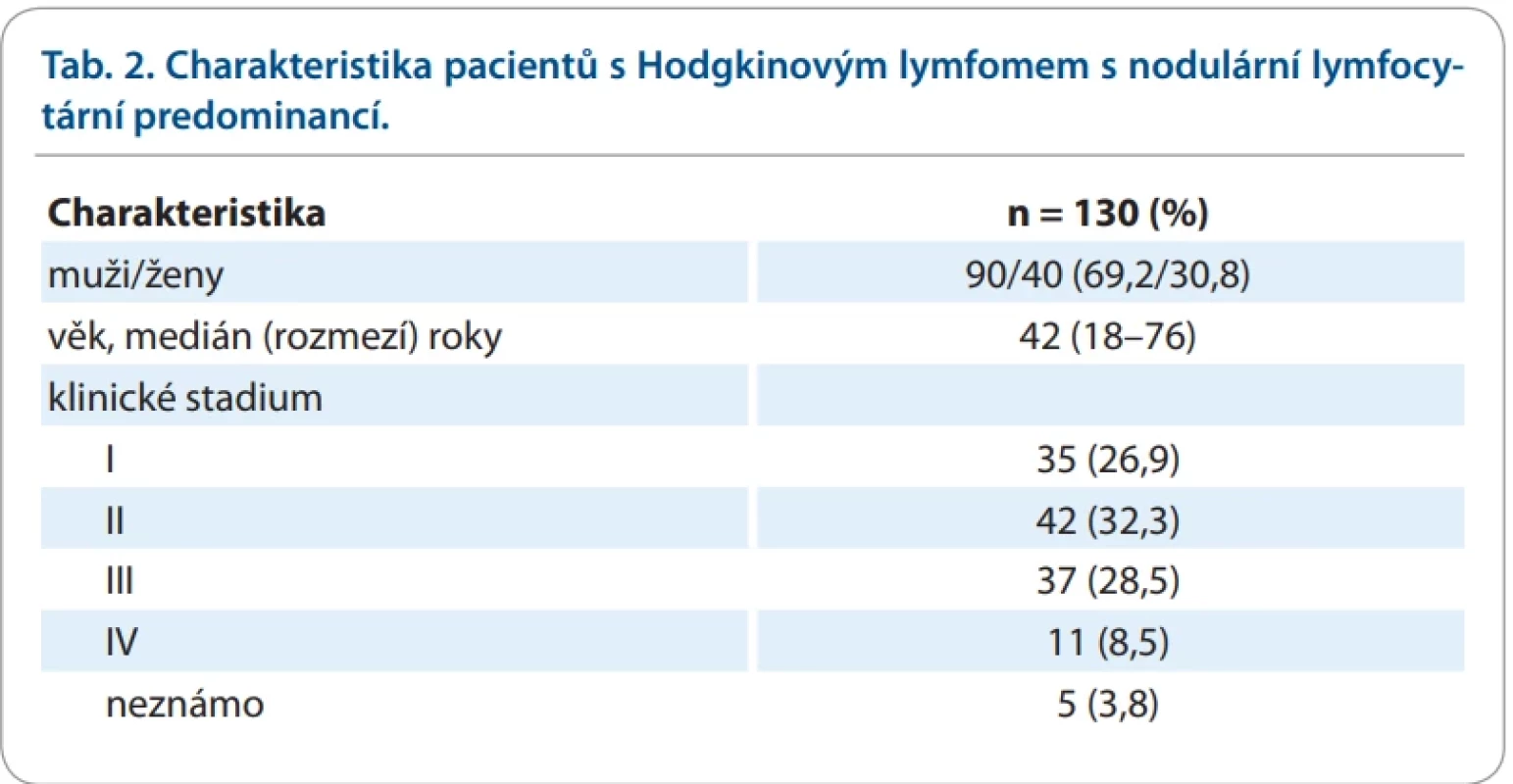
Do iniciálních stadií byli zařazeni pacienti v klinickém stadiu I nebo II bez rizikových faktorů. Do intermediárních stadií byli zařazeni pacienti v klinickém stadiu I nebo II s rizikovými faktory: masivní mediastinální tumor (> třetina průměru hrudníku) nebo extranodální postižení, postižení ≥ tří oblastí lymfatických uzlin, vysoká sedimentace (> 30 mm/h s B symptomy, > 50 mm/h bez B symptomů). Výjimku tvořili pacienti v klinickém stadiu IIB s masivním mediastinálním tumorem a/nebo s extranodálním postižením, dále pacienti s nádorovou masou o velikosti ≥ 10 cm, kteří byli zařazeni do pokročilých stadií. Pacienti v klinickém stadiu III nebo IV byli zařazeni do pokročilých stadií. Mezinárodní prognostické skóre (IPS) pro pacienty v pokročilém stadiu III a IV je uvedeno v tab. 1.
Odpověď na léčbu (kompletní remise, parciální remise, stabilní nemoc, progrese) byla hodnocena po ukončení léčby podle Chesonových kritérií z let 1999, 2007 a od roku 2014 podle Luganské klasifikace [1–3].
Přežití bez progrese (progression-free survival – PFS) bylo definováno jako časový interval od data zahájení 1. linie léčby do data relapsu/progrese nebo data úmrtí z jakékoliv příčiny. Celkové přežití (overall survival – OS) bylo hodnoceno od data diagnózy do data posledního sledování nebo do úmrtí z jakékoliv příčiny. Křivky přežití byly odhadnuty Kaplan-Meierovou metodou a porovnání mezi podskupinami bylo provedeno pomocí log-rank testu.
Výsledky
První linie léčby
Medián sledování pacientů s cHL byl 146 měsíců. Podle registru HL v ČR v letech 2000–2024 bylo celkem 272 pacientů léčeno pro iniciální stadia cHL, z toho 221 pacientů ve věku < 60 let a 51 pacientů ve věku ≥ 60 let. Podaná chemoterapie, RT a odpovědi na léčbu jsou uvedeny v grafech 1a,b. Desetileté PFS u pacientů v věku < 60 let bylo 91,5 % (95% interval spolehlivosti (IS) 87,1–96,0) a ve věku ≥ 60 let 67,0 % (95% IS 52,5–85,6) (graf 2a). Desetileté OS u pacientů ve věku < 60 let bylo 94,2 % (95% IS 90,2–98,4) a ve věku ≥ 60 let 74,2 % (95% IS 60,4–91,3) (graf 3a).
Graf 1a. Iniciální stadia – léčba pacientů ve věku < 60 let (n = 221). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese,
PR – parciální remise, SD – stabilní nemocGraf 1b. Iniciální stadia – léčba pacientů ve věku ≥ 60 let (n = 51). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese,
PR – parciální remise, SD – stabilní nemocGraf 1c. Intermediární stadia – léčba pacientů ve věku < 60 let (n = 515). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese,
PR – parciální remise, SD – stabilní nemocGraf 1d. Intermediární stadia – léčba pacientů ve věku ≥ 60 let (n = 62). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese,
PR – parciální remise, SD – stabilní nemocGraf 1e. Pokročilá stadia – BEACOPPesk.+ modifi kace a kombinace a jiné (n = 809 pacientů ve věku < 60 let). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese, PR
– parciální remise, SD – stabilní nemocGraf 1f. Pokročilá stadia – ABVD + modifi kace a kombinace (n = 93 pacientů ve věku ≥ 60 let). 
CHT – chemoterapie, RT – radioterapie Graf 1g. Pokročilá stadia – léčba pacientů ve věku ≥ 60 let. 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese, PR – parciální remise,
RT – radioterapie, SD – stabilní nemocGraf 2a. Klasický Hodgkinův lymfom – PFS dle věku a klinického stadia. 
Analýza z let 2000–2024 (n = 2 241).
GHSG – German Hodgkin Study Group, KS – klinické stadiumGraf 2b. Pokročilé stadium klasického Hodgkinova lymfomu u pacientů ve věku < 60 let – přežití bez progrese dle chemoterapie v 1. linii. 
Analýza z let 2000–2024.
CHT – chemoterapiePro intermediární stadia cHL s výjimkou stadia IIB s masivním mediastinálním tumorem a/nebo s extranodálním postižením bylo ve výše uvedeném období léčeno 515 pacientů ve věku < 60 let a 62 pacientů ve věku ≥ 60 let. Podaná chemoterapie, RT a odpovědi na léčbu jsou uvedeny v grafech 1c,d. Desetileté PFS u pacientů ve věku < 60 let bylo 91,0 % (95% IS 88,2–93,9) a ve věku ≥ 60 let 36,4 % (95% IS 22,1–60,0) (graf 2a). Desetileté OS u pacientů ve věku < 60 let bylo 96,6 % (95% IS 94,7–98,6) a ve věku ≥ 60 let 45,7 % (95% IS 29,5–70,6) (graf 3a).
Pro pokročilá stadia cHL (stadia IIB s masivním mediastinálním tumorem a/nebo s extranodálním postižením, stadia III a IV) bylo ve výše uvedeném období léčeno 902 pacientů ve věku < 60 let a 239 pacientů ve věku ≥ 60 let. Podaná chemoterapie, RT a odpovědi na léčbu jsou uvedeny v grafech 1e – g. Desetileté PFS u pacientů ve věku < 60 let bylo 83,9 % (95% IS 81,1–86,8) a ve věku ≥ 60 let 41,6 % (95% IS 33,0–52,4) (graf 2a). Desetileté OS u pacientů ve věku < 60 let bylo 92,6 % (95% IS 90,5–94,8) a ve věku ≥ 60 let 52,0 % (95% IS 43,0–63,0) (graf 3a). PFS u pacientů ve věku < 60 let bylo signifikantně delší po léčbě eskalovaným BEACOPP oproti režimu ABVD či kombinaci (p = 0,011) (graf 2b). Rovněž bylo signifikantně delší OS u pacientů ve věku < 60 let po léčbě eskalovaným BEACOPP oproti režimu ABVD (p < 0,001) (graf 3b).
Medián sledování u pacientů s NLPHL byl 7,9 roku. Ze 130 pacientů s NLPHL bylo léčeno 118 pacientů RT nebo kombinací chemoterapie s rituximabem +/ − RT, u dalších 12 pacientů nebyla léčba zadána do registru HL. Způsob léčby a odpověď na léčbu u NLPHL jsou uvedeny v grafu 4. Z hlediska prognózy bylo vyhodnoceno celkem 110 pacientů. Pětileté a 10leté PFS bylo 84,2 % (95% IS 76,9–92,2) a 77,5 % (95% IS 68,4–87,7). Pětileté a 10leté OS bylo 98,2 % (95% IS 95,7–100,0) a 95,8 % (95% IS 91,8–100,0).
Graf 3a. Klasický Hodgkinův lymfom – celkové přežití dle věku a klinického stadia. 
Analýza z let 2000–2024 (n = 2 241).
GHSG – German Hodgkin Study Group, KS – klinické stadiumGraf 3b. Pokročilé stadium klasického Hodgkinova lymfomu u pacientů ve věku < 60 let – celkové přežití dle chemoterapie v 1. linii. 
Analýza z let 2000–2024.
CHT – chemoterapieGraf 4. Léčba pacientů s Hodgkinovým lymfomem s nodulární lymfocytární predominancí (n = 118). 
CR – kompletní remise, nehod – nehodnoceno, PD – progrese, PR – parciální remise, SD – stabilní nemoc Léčba relapsu
Medián sledování u relabovaných pacientů od data relapsu byl 7,6 roku. Podle dat v registru HL bylo v období od 2000 do 2023 vyhodnoceno 268 pacientů s relapsem HL, z nich 233 bylo ve věku≤ 65 let a 35 pacientů ve věku > 65 let. Medián OS u pacientů ve věku ≤ 65 let nebyl dosažen, 5leté OS bylo 75,2 % (95 % IS 69,4–81,6), naproti tomu signifikantně kratší bylo přežití u pacientů ve věku > 65 let: medián OS byl 1,3 roku (95 % IS 0,9–nedosaženo; p < 0,001) a 5leté OS bylo 24,6 % (95 % IS 11,5–52,5). Z 233 pacientů ve věku ≤ 65 let bylo léčeno vysokodávkovanou chemoterapií s následnou autologní transplantací kmenových buněk (autologous stem cell transplant – ASCT) 131 (56 %) pacientů. Pětileté OS od data relapsu je významně lepší u pacientů ve věku ≤ 65 let, kteří dostali ASCT, oproti těm, kteří ASCT nepodstoupili: 82,7 % (95% IS 75,7–90,4) vs. 65,8 % (95% IS 56,6–76,5), p = 0,008; hazard ratio (HR) 1,96 (95% IS 1,18–3,28).
Nivolumab byl podán v relapsu cHL u 44 pacientů, charakteristiky pacientů a odpovědi na léčbu uvádí tab. 3. Medián sledování od zahájení nivolumabu byl 38,6 měsíce. Medián, 2leté a 5leté PFS byly 13,5 měsíce, 30,5 % a 5,7 % (graf 5). Medián, 2leté a 5leté OS byly 58,8 měsíce, 77,4 % a 37,5 % (graf 5).
Table 3. Charakteristika pacientů léčených nivolumabem a léčebná odpověď na nivolumab. 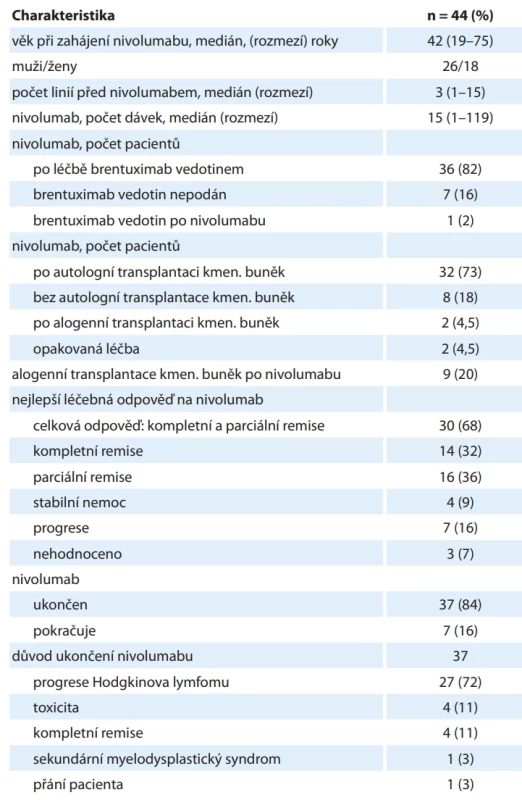
Graf 5. Přežití bez progrese a celkové přežití při léčbě nivolumabem u pacientů s relapsem klasického Hodgkinova lymfomu. 
OS – celkové přežití, PFS – přežití bez progrese Pembrolizumab byl podán v relapsu cHL u 48 pacientů, charakteristiky pacientů a odpovědi na léčbu uvádí tab. 4. Medián sledování od zahájení léčby pembrolizumabem byl 11,5 měsíce. Medián, 2leté a 5leté PFS byly 16,5 měsíce, 33,5 % a 26,8 % (graf 6). Dvouleté a 5leté OS byly 83,3 % a 77,3 %, mediánu nebylo dosaženo (graf 6).
Table 4. Charakteristika pacientů léčených pembrolizumabem a léčebná odpověď na pembrolizumab. 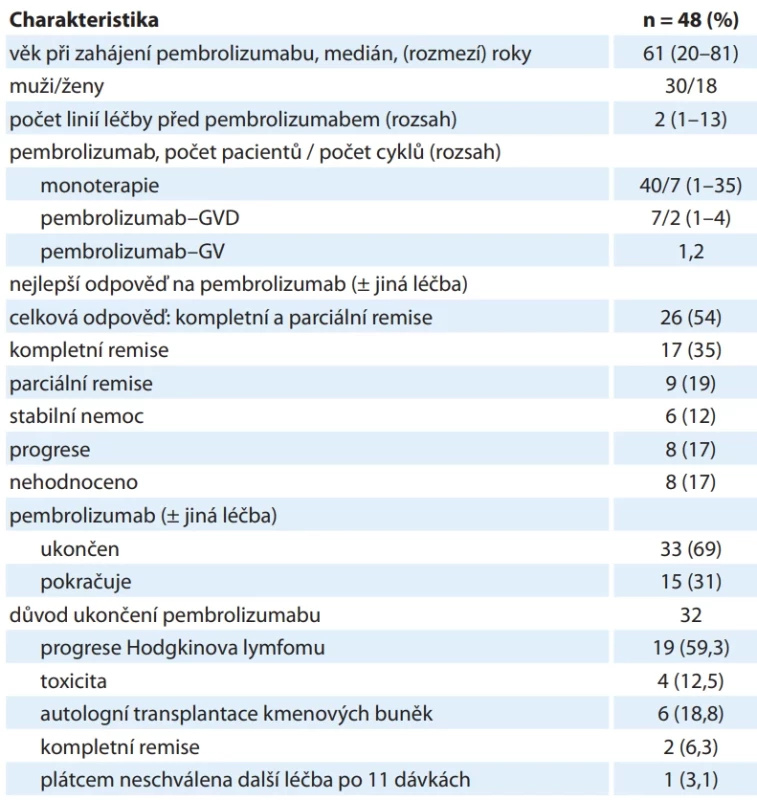
GVD – gemcitabin, vinorelbin, lipozomální doxorubicin Graf 6. Celkové přežití a přežití bez progrese při léčbě pembrolizumabem u pacientů s relapsem klasického Hodgkinova lymfomu. 
OS – celkové přežití, PFS – přežití bez progrese Diskuze
Desetileté výsledky PFS a OS v našem souboru pacientů v iniciálním stadiu ve věku < 60 let jsou srovnatelné s výsledky studie pro iniciální stadia GHSG HD10 : 87,2 % a 94,1 % [4,5]. Desetileté PFS a OS u našich pacientů z registru HL ve věku ≥ 60 let byly horší, což odpovídá obecně horší prognóze starších pacientů s nutností redukce chemoterapie vzhledem ke komorbiditám. Z analýzy studií GHSG HD10 a HD13 pro iniciální stadia vyplynulo, že u starších pacientů je nutné vysadit bleomycin po dvou cyklech ABVD, aby se zabránilo vzniku plicní toxicity a zvýšenému riziku úmrtí na ni [6,7]. Snahy o vynechání RT po dvou cyklech ABVD u PET-2 negativních pacientů ve studii GHSG HD16 pro iniciální stadia [8,9] vedly k významné ztrátě účinnosti, proto aktuálním standardem léčby v ČR pro tuto skupinu pacientů v iniciálním stadiu zůstávají dva cykly ABVD a „involved site“ RT (ISRT) 20 Gy [10].
V GHSG studii HD11 pro intermediární stadia byly nejlepší výsledky dosaženy čtyřmi cykly ABVD + 30 Gy „involved field“ RT (IFRT). Tato kombinace měla 10leté PFS a OS 83,3 % a 90,9 % [5,11]. Ve studii GHSG HD14 pro intermediární stadia byly nejlepší výsledky dosaženy u pacientů ve věku < 60 let kombinací dvou cyklů eskalovaného BEACOPP + dvou cyklů ABVD + 30 Gy IFRT [12]: 10leté PFS bylo 91,2 % a OS 94,1 % [13]. Výše uvedené režimy byly nejčastěji podány i v kohortě našich pacientů v intermediárním stadiu, proto 10leté výsledky PFS a OS u pacientů ve věku < 60 let byly srovnatelné s uvedenými podskupinami pacientů ve studiích HD11 a HD14. Obdobně jako u časných stadií i u intermediárních stadií ve věkové skupině ≥ 60 let, která byla léčena převážně režimem ABVD a jeho modifikacemi, bylo 10leté PFS a OS horší oproti populaci ve věku < 60 let. Současným standardem léčby v ČR u pacientů v intermediárním stadiu ve věku < 60 let je podání dvou cyklů eskalovaného BEACOPP a dvou cyklů ABVD, po kterých je možné vynechat RT u těch pacientů, kteří podle studie GHSG HD17 dosáhli PET-4 negativní kompletní remise [14]. U pacientů ve věkové skupině ≥ 60 let je v ČR indikováno podání dvou cyklů ABVD + dvou cyklů AVD a 30 Gy ISRT [10].
Studie GHSG HD9 s úspěchem zavedla do léčby cHL v pokročilém stadiu ve věku < 60 let eskalovaný BEACOPP [15]. Další studie GHSG HD12, HD15, HD18 postupně snížily počet cyklů z osmi na čtyři u pacientů s negativním PET po dvou cyklech chemoterapie a umožnily vynechání RT u pacientů, kteří dosáhli PET negativní kompletní remise po ukončení chemoterapie [16–19]. Intenzifikace léčby u PET-2 pozitivních pacientů přidáním rituximabu k eskalovanému BEACOPP nezlepšila 3leté PFS [18,19]. Pětileté výsledky PFS a OS všech pacientů v registru HL v pokročilých stadiích ve věku < 60 let a zejména těch, kteří byli léčeni eskalovaným BEACOPP (90,7 % a 96,9 %), jsou srovnatelné se studiemi GHSG HD15 a HD18. Podle českého registru HL PFS u pacientů v pokročilém stadiu ve věku < 60 let bylo signifikantně delší po léčbě eskalovaným BEACOPP (4–8 cyklů) oproti 6–8 cyklům ABVD (p = 0,011). Rovněž bylo signifikantně delší OS u našich pacientů ve věku < 60 let po léčbě eskalovaným BEACOPP oproti režimu ABVD (p < 0,001). Čtyřleté výsledky studie GHSG HD21 prokázaly, že režim BRECADD (brentuximab vedotin, etoposid, cyklofosfamid, doxorubicin, dakarbazin, dexametazon) je ještě účinnější a má méně nežádoucích účinků oproti režimu eskalovaný BEACOPP (4leté PFS 94,3 % vs. 90,9 %, hazard ratio 0,66 a 4leté OS 98,6 % vs. 98,2 %), proto je 4/6 cyklů BRECADD jedním ze současných standardů léčby v 1. linii u pokročilých stadií v ČR a jeho použití v běžné praxi bylo již zahájeno [10,20]. Podle dat z registru HL jsou 10leté výsledky PFS a OS u pacientů v pokročilém stadiu ve věku ≥ 60 let na léčbě ABVD a jeho modifikacích neuspokojivé. Studie SWOG S1826 prokázala u pacientů ve věku ≥ 12 let včetně populace ≥ 60 let v pokročilých stadiích III a IV, že šest cyklů léčby nivolumabu v kombinaci s AVD (N-AVD) je účinnější než šest cyklů brentuximab vedotinu v kombinaci s AVD (BV-AVD) [21]: 2leté PFS bylo 92 % po N-AVD ve srovnání s 83 % po BV-AVD (HR 0,45). Režim N-AVD je rovněž jedním ze současných standardů léčby v ČR u pacientů v klinickém stadiu III nebo IV, který se aktuálně již používá u pacientů zejména ve věku ≥ 60 let [10].
Na základě RNA sekvenování a cirkulující nádorové DNA byly definovány tři lymfocytárně predominantní ekotypy NLPHL (LPE): LPE1 a LPE2 byly charakterizovány imunosupresivním mikroprostředím s vysokou expresí B2M na nádorových buňkách, vyčerpáním CD8 T lymfocytů a lepším PFS ve srovnání s LPE3 [22]. K základní kohortě (n = 109, 65 % LPE1/2) byla ve validační kohortě (n = 62, 61 % LPE1/2) použita data a vzorky od 62 pacientů s NLPHL z českého registru HL. Ve srovnání s literaturou, kde je medián věku u pacientů s NLPHL uveden v rozmezí 35–40 let [23], je medián věku pacientů v registru HL vyšší – 42 let. V naší hodnocené kohortě 130 pacientů převažují muži, ale podíl klinických stadií I a II je nižší (59,2 %) oproti literatuře (75 %) [23]. Pouze 7 pacientů absolvovalo chirurgickou exstirpaci bez další léčby a 23 pacientů v časném stadiu IA mělo samostatnou RT 30 Gy [24]. Nejčastější použitou chemoterapií v pokročilých stadiích byl R-C (H) OP (rituximab, cyklofosfamid, doxorubicin, vinkristin, prednison) s RT, nebo bez ní (41 pacientů) [25,26]. Podle sledování v registru HL mají pacienti s NLPHL v souladu s literaturou velmi dobrou prognózu, což dokládají 5leté a 10leté výsledky PFS a OS.
Standardem léčby relapsu klasického HL ve věku ≤ 65 let zůstává záchranná chemoterapie s následnou vysokodávkovanou chemoterapií a ASCT. Data z registru HL potvrzují lepší OS u pacientů ve věku ≤ 65 let, pokud měli provedenou ASCT, ve srovnání s pacienty bez ASCT. Podle registru European Bone Marrow Transplantation (EBMT) byla v ČR v letech 2020–2024 provedena ASCT u 122 pacientů s HL (v průměru 24 ASCT ročně). U pacientů s vysokým rizikem dalšího relapsu se podává konsolidace brentuximab vedotinem à 3 týdny do maximálního počtu 16 cyklů [27]. Retrospektivní analýzy léčby brentuximab vedotinem u relabovaných nebo refrakterních pacientů s cHL včetně konsolidace po ASCT s využitím dat z českého registru HL byly již publikovány [28–30], proto nejsou předmětem tohoto sdělení. Ve druhém relapsu po ASCT se i podle českých standardních doporučení podává checkpoint inhibitor nivolumab do relapsu [10,31]. V relapsu bylo v naší kohortě odléčeno nivolumabem 44 pacientů, z nich 32 % dosáhlo kompletní remise a celkové odpovědi 68 %. Podíl remisí byl u našich pacientů vyšší oproti studii CheckMate-205 (21 % a 71 %), ale 5leté PFS (5,7 %) a OS (37,5 %) byly v naší neselektované kohortě pacientů horší oproti studii CheckMate-205 (17,9 % a 66,6 %). U pacientů nevhodných k ASCT je podle aktuálních standardních doporučení ve druhém relapsu indikován checkpoint inhibitor pembrolizumab [10,32,33], který se podává do celkového počtu 35 cyklů. Pembrolizumab byl použit v relapsu u 48 pacientů, z nich 35 % dosáhlo kompletní remise a celkové odpovědi 54 % (ve studii Keynote 087 kompletní remise 27,6 % a celková odpověď 71 %). Pětileté PFS (26,8 %) a OS (77,3 %) u naší kohorty pacientů jsou srovnatelné se studií Keynote 087 (14,2 % a 70,7 %).
Závěr
Data z registru HL potvrzují dlouhodobě velmi dobrou prognózu: 10leté přežití dosahuje až 90 % pacientů ve věku < 60 let a pacienti věkové skupiny ≥ 60 let mají medián přežití kolem 10 let. Se zavedením nových léčebných možnosti jako je BRECADD a N-AVD se očekává snížení toxicity a zvýšení účinnosti léčby zejména u pacientů ve věku ≥ 60 let. V relapsu zůstává standardem léčby u mladších pacientů ASCT. V relapsu jsou účinné léky jako nivolumab, pembrolizumab nebo brentuximab vedotin.
Poděkování
Tato práce byla realizována za podpory Agentury pro zdravotnický výzkum MZ ČR NU22-03-00182, za podpory programu Cooperatio – výzkumná oblast onkologie a hematologie a za podpory MH CZ – DRO (FNOL, 00098892).
Sources
1. Cheson BD, Fisher RI, Barrington SF et al. Recommendations for initial evaluation, staging, and response assessment of Hodgkin and non-Hodgkin lymphoma: the Lugano classification. J Clin Oncol 2014; 32 (27): 3059–3068. doi: 10.1200/JCO.2013.54.8800.
2. Cheson BD, Horning SJ, Coiffier B et al. Report of an international workshop to standardize response criteria for non-Hodgkin’s lymphomas. NCI Sponsored International Working Group. J Clin Oncol 1999; 17 (4): 1244. doi: 10.1200/JCO.1999.17.4.1244.
3. Cheson BD, Pfistner B, Juweid ME et al. Revised response criteria for malignant lymphoma. J Clin Oncol 2007; 25 (5): 579–586. doi: 10.1200/JCO.2006.09.2403.
4. Engert A, Plütschow A, Eich HT et al. Reduced treatment intensity in patients with early-stage Hodgkin‘s lymphoma. N Engl J Med 2010; 363 (7): 640–652. doi: 10.1056/NEJMoa1000067.
5. Sasse S, Bröckelmann PJ, Goergen H et al. Long-term follow-up of contemporary treatment in early-stage Hodgkin lymphoma: updated analyses of the German Hodgkin study group HD7, HD8, HD10, and HD11 trials. J Clin Oncol 2017; 35 (18): 1999–2007. doi: 10.1200/JCO.2016.70.9410.
6. Behringer K, Goergen H, Hitz F et al. Omission of dacarbazine or bleomycin, or both, from the ABVD regimen in treatment of early-stage favourable Hodgkin‘s lymphoma (GHSG HD13): an open-label, randomised, non--inferiority trial. Lancet 2015; 385 (9976): 1418–1427. doi: 10.1016/S0140-6736 (14) 61469-0.
7. Böll B, Goergen H, Behringer K et al. Bleomycin in older early-stage favorable Hodgkin lymphoma patients: analysis of the German Hodgkin Study Group (GHSG) HD10 and HD13 trials. Blood 2016; 127 (18): 2189–2192. doi: 10.1182/blood-2015-11-681064.
8. Fuchs M, Goergen H, Kobe C et al. Positron emission tomography-guided treatment in early-stage favorable Hodgkin lymphoma: final results of the International, randomized phase III HD16 trial by the German Hodgkin Study Group. J Clin Oncol 2019; 37 (31): 2835–2845. doi: 10.1200/JCO.19.00964.
9. Fuchs M, Jacob AS, Kaul H et al. Follow-up of the GHSG HD16 trial of PET-guided treatment in early-stage favorable Hodgkin lymphoma. Leukemia 2024; 38 (1): 160–167. doi: 10.1038/s41375-023-02064-y.
10. Belada D, Trněný M. Diagnostické a léčebné postupy u nemocných s maligními lymfomy. XV. Vydání. 2025 [online]. Dostupné z: https: //www.lymphoma.cz/_uploads/attachments/KLS_guidelines_2025_31579.pdf.
11. Eich HT, Diehl V, Görgen H et al. Intensified chemotherapy and dose-reduced involved-field radiotherapy in patients with early unfavorable Hodgkin‘s lymphoma: final analysis of the German Hodgkin Study Group HD11 trial. J Clin Oncol 2010; 28 (27): 4199–4206. doi: 10.1200/JCO.2010.29.8018.
12. von Tresckow B, Plütschow A, Fuchs M et al. Dose--intensification in early unfavorable Hodgkin‘s lymphoma: final analysis of the German Hodgkin Study Group HD14 trial. J Clin Oncol 2012; 30 (9): 907–913. doi: 10.1200/JCO.2011.38.5807.
13. Gillessen S, Plütschow A, Fuchs M et al. Intensified treatment of patients with early stage, unfavourable Hodgkin lymphoma: long-term follow-up of a randomised, international phase 3 trial of the German Hodgkin Study Group (GHSG HD14). Lancet Haematol 2021; 8 (4): e278–e288. doi: 10.1016/S2352-3026 (21) 00029-6.
14. Borchmann P, Plütschow A, Kobe C et al. PET-guided omission of radiotherapy in early-stage unfavourable Hodgkin lymphoma (GHSG HD17): a multicentre, open-label, randomised, phase 3 trial. Lancet Oncol 2021; 22 (2): 223–234. doi: 10.1016/S1470-2045 (20) 30601-X.
15. Diehl V, Franklin J, Pfreundschuh M et al. Standard and increased-dose BEACOPP chemotherapy compared with COPP-ABVD for advanced Hodgkin‘s disease. N Engl J Med 2003; 348 (24): 2386–2395. doi: 10.1056/ NEJMoa022473.
16. Borchmann P, Haverkamp H, Diehl V et al. Eight cycles of escalated-dose BEACOPP compared with four cycles of escalated-dose BEACOPP followed by four cycles of baseline-dose BEACOPP with or without radiotherapy in patients with advanced-stage Hodgkin‘s lymphoma: final analysis of the HD12 trial of the German Hodgkin Study Group. J Clin Oncol 2011; 29 (32): 4234–4242. doi: 10.1200/JCO.2010.33.9549.
17. Engert A, Haverkamp H, Kobe C et al. Reduced-intensity chemotherapy and PET-guided radiotherapy in patients with advanced stage Hodgkin‘s lymphoma (HD15 trial): a randomised, open-label, phase 3 non-inferiority trial. Lancet 2012; 379 (9828): 1791–1799. doi: 10.1016/S0140-6736 (11) 61940-5.
18. Borchmann P, Goergen H, Kobe C et al. PET-guided treatment in patients with advanced-stage Hodgkin‘s lymphoma (HD18): final results of an open-label, international, randomised phase 3 trial by the German Hodgkin Study Group. Lancet 2017; 390 (10114): 2790–2802. doi: 10.1016/S0140-6736 (17) 32134-7.
19. Kreissl S, Goergen H, Buehnen I et al. PET-guided eBEACOPP treatment of advanced-stage Hodgkin lymphoma (HD18): follow-up analysis of an international, open-label, randomised, phase 3 trial. Lancet Haematol 2021; 8 (6): e398–e409. doi: 10.1016/S2352-3026 (21) 00101-0.
20. Borchmann P, Ferdinandus J, Schneider G et al. Assessing the efficacy and tolerability of PET-guided BrECADD versus eBEACOPP in advanced-stage, classical Hodgkin lymphoma (HD21): a randomised, multicentre, parallel, open-label, phase 3 trial. Lancet 2024; 404 (10450): 341–352. doi: 10.1016/S0140-6736 (24) 01315-1.
21. Herrera AF, Leblanc ML, Castellino SM et al. Nivolumab-AVD in advanced stage classic Hodgkin lymphoma. N Engl J Med 2024; 391 (15): 1379–1389. doi: 10.1056/ NEJMoa2405888.
22. Subramanian A, Shengqin S, Flerlage J et al. Distinct cell state ecosystems for nodular lymphocyte-predominant Hodgkin lymphoma. Nat Commun 2025; 16 (1): 8473. doi: 10.1038/s41467-025-63339-9.
23. Salvaris RT, Allanson BM, Collins G et al. Nodular lymphocyte-predominant Hodgkin lymphoma: advances in disease biology, risk stratification, and treatment. Haematologica 2024; 109 (11): 3476–3487. doi: 10.3324/haematol.2024.285903.
24. Nogova L, Reineke T, Eich HT et al. Extended field radiotherapy, combined modality treatment or involved field radiotherapy for patients with stage IA lymphocyte-predominant Hodgkin’s lymphoma: a retrospective analysis from the German Hodgkin Study Group (GHSG). Ann Oncol 2005; 16 (10): 1683–1687. doi: 10.1093/annonc/mdi323.
25. Fanale MA, Cheah CY, Rich A et al. Encouraging activity for R-CHOP in advanced stage nodular lymphocyte-predominant Hodgkin lymphoma. Blood 2017; 130 (4): 472–477. doi: 10.1182/blood-2017-02-766121.
26. Wilson MR, Bagguley T, Smith A et al. Frontline management of nodular lymphocyte predominant Hodgkin lymphoma-a retrospective UK multicentre study. Br J Haematol 2019; 186 (6): e214–e217. doi: 10.1111/bjh.16109.
27. Moskowitz CH, Nademanee A, Masszi T et al. Brentuximab vedotin as consolidation therapy after autologous stem-cell transplantation in patients with Hodgkin‘s lymphoma at risk of relapse or progression (AETHERA): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2015; 385 (9980): 1853–1862. doi: 10.1016/S0140-6736 (15) 60165-9.
28. Desai SH, Spinner MA, Evens AM et al. Overall survival of patients with cHL who progress after autologous stem cell transplant: results in the novel agent era. Blood Adv 2023; 7 (23): 7295–7303. doi: 10.1182/bloodadvances.2023011205.
29. Michalka J, Král Z, Marková J et al. Konsolidační léčba brentuximab vedotinem u pacientů s relabujícím/refrakterním klasickým Hodgkinovým lymfomem po provedení autologní transplantace hematopoetických kmenových buněk v České republice. Onkologie 2023; 17 (4): 267–272. doi: 10.36290/xon.2023.051.
30. Král Z, Michalka J, Móciková H et al. Treatment of relapsed/refractory Hodgkin lymphoma: real-world data from the Czech Republic and Slovakia. J Cancer 2019; 10 (21): 5041–5048. doi: 10.7150/jca.29308.
31. Ansell SM, Bröckelmann PJ, von Keudell G et al. Nivolumab for relapsed/refractory classical Hodgkin lymphoma: 5-year survival from the pivotal phase 2 Check - -Mate 205 study. Blood Adv 2023; 7 (20): 6266–6274. doi: 10.1182/bloodadvances.2023010334.
32. Kuruvilla J, Ramchandren R, Santoro A et al. Pembrolizumab versus brentuximab vedotin in relapsed or refractory classical Hodgkin lymphoma (KEYNOTE-204): an interim analysis of a multicentre, randomised, open-label, phase 3. Lancet Oncol 2021; 22 (4): 512–524. doi: 10.1016/S1470-2045 (21) 00005-X.
33. Armand P, Zinzani PL, Lee HJ et al. Five-year follow-up of KEYNOTE-087: pembrolizumab monotherapy for relapsed/refractory classical Hodgkin lymphoma. Blood 2023; 142 (10): 878–886. doi: 10.1182/blood.2022019386.
Labels
Paediatric clinical oncology Surgery Clinical oncology
Article was published inClinical Oncology

2026 Issue 1-
All articles in this issue
- Dimenze onkochirurgie II
- O tvrdosti dat
- Cutaneous diseases caused by monoclonal immunoglobulin and/or free light chains (monoclonal gammopathy of cutaneous significance)
- Changes in hemostasis and other disorders caused by monoclonal immunoglobulin and/or free light chains
- The phenomenon of hope as an inseparable part of oncology patient care in the terminal disease stage
- Treatment outcomes of Hodgkin lymphoma in the Czech Republic
- Reporting framework in the testing of predisposition to common adult solid tumors using next-generation sequencing
- Speech therapy intervention in a patient with multiple myeloma and dysphagia – a case study from clinical practice
- Strategie snižování rizik „harm reduction“ jako součást primární prevence
- AKTUALITY Z NÁRODNÍHO ÚSTAVU PRO VÝZKUM RAKOVINY
- Clinical Oncology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Reporting framework in the testing of predisposition to common adult solid tumors using next-generation sequencing
- Treatment outcomes of Hodgkin lymphoma in the Czech Republic
- Cutaneous diseases caused by monoclonal immunoglobulin and/or free light chains (monoclonal gammopathy of cutaneous significance)
- Speech therapy intervention in a patient with multiple myeloma and dysphagia – a case study from clinical practice
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

