-
Medical journals
- Career
Laparoskopická resekce sigmatu pro divertikulární chorobu
: L. Vrbenský; J. Šimša
: Chirurgická klinika 1. LF UK a Thomayerovy nemocnice, Praha přednosta: Doc. MUDr. J. Šimša, Ph. D.
: Rozhl. Chir., 2013, roč. 92, č. 7, s. 414-419.
: Various Specialization
Práce je určena k postgraduálnímu vzdělávání lékařů.
Úvod:
Laparoskopická resekce sigmatu pro divertikulární postižení je dnes plně akceptovanou alternativou klasické otevřené operace.Cíl:
Cílem práce je shrnout indikace, výhody i rizika laparoskopické resekce sigmatu pro divertikulární chorobu.Metodika:
Přehled literatury a aktuálních názorů na význam laparoskopické resekce sigmatu pro divertikulární onemocnění.Závěr:
Práce popisuje indikace, rizika, techniku a perioperační péči u nemocných po laparoskopické resekci sigmatu pro divertikulární chorobu.Klíčová slova:
divertikulární choroba – sigma – laparoskopická resekceÚvod
Laparoskopická resekce sigmatu je v současné době považována za akceptabilní alternativu otevřené resekce sigmatu pro divertikulární nemoc. V období nad 45 let věku trpí divertikulární nemocí v západní společnosti kolem 33 % populace, kolem 80. roku věku je to až 60 %. Asi u 25 % osob se divertikulární nemoc v nějaké formě v průběhu jejich života projeví. Iniciální stavy onemocnění jsou obvykle léčeny konzervativně, kolem 30 % nemocných však již v době prvních projevů vyžaduje operační řešení. Třetina pacientů s konzervativně léčenou první atakou onemocnění prodělá v dalším průběhu života recidivu, další třetina bude mít recidivy opakované. Statisticky je v literatuře udávána mortalita a morbidita při první atace divertikulární nemoci mezi 5 až 25 %, při recidivách se toto číslo pohybuje mezi 10 až 60 % [1]. Až do roku 1991 byly všechny resekční výkony na sigmatu prováděny otevřenou operační technikou, která dodnes zůstává zlatým standardem. V roce 1991 byla poprvé popsána laparoskopická resekce sigmatu [2]. S rozvojem technického vybavení a zkušeností chirurgů podíl laparoskopických výkonů při léčbě divertikulární nemoci narůstá. Zpočátku byli operováni pouze nemocní s nekomplikovanou symptomatickou divertikulární nemocí, v současnosti jsou laparoskopické výkony prováděny i u recidivující a komplikované divertikulární nemoci včetně fistulujících forem nebo perforací. Z rozsáhlé analýzy databází z let 1992–2001 bylo zjištěno, že laparoskopická technika byla použita celkově jen u 3,6 % nemocných [3]. Toto číslo v poslední době nepochybně narůstá, nicméně i v současnosti je laparoskopická resekce sigmatu uplatňována jen menšinou chirurgů u malého počtu pacientů, a to i přesto, že bylo prokázáno, že jde o bezpečnou a efektivní metodu, která přináší nemocným řadu výhod. Jako základní výhody laparoskopického přístupu jsou uváděny menší pooperační bolest, časnější obnova střevních funkcí, kratší doba hospitalizace a nižší výskyt závažných komplikací proti otevřeným výkonům. Nezanedbatelný je i lepší kosmetický efekt. Stran závažných pooperačních komplikací je ve skupině časných komplikací prokázán nižší výskyt ranných infekcí, plicních a kardiovaskulárních komplikací i pooperačních střevních neprůchodností. Z pozdních komplikací jde především o výskyt kýl a srůstů [4–10]. Nevýhodou laparoskopických výkonů je delší operační čas oproti otevřeným operacím a vyšší bezprostřední finanční náklady [11,12]. Názory na celkové ekonomické náklady miniinvazivních výkonů se však zejména v poslední době vyvíjejí a někteří autoři dokumentují úsporu zkrácením doby hospitalizace a rychlejší rekonvalescencí [11–14]. Významný je i průkaz bezpečnosti laparoskopických resekcí sigmatu pro vyšší věkové skupiny pacientů, a to i nad 75 let věku. I u těchto nemocných bylo prokázáno snížení morbidity, kratší doba hospitalizace a nižší potřeba dodatečné rehabilitace. Výhody laparoskopie byly dokumentovány i pro obézní nemocné s BMI nad 30, v této skupině však je vyšší riziko konverze [15,16]. V současné době jsou operováni laparoskopickou technikou bezpečně nemocní až do ASA IV, vždy však s podmínkou důsledné hemodynamické monitorace a snížením tlaku pneumoperitonea pod 12 mmHg.
Metodika
Indikace laparoskopické resekce sigmatu
Základní všeobecně akceptované indikační schéma u nekomplikované divertikulitidy je elektivní operační výkon u pacientů starších 50 let po dvou atakách divertikulitidy. U nemocných mladších 50 let stačí k indikaci výkonu jedna proběhlá ataka onemocnění. Jako další indikační kritérium pro elektivní výkon je považováno krvácení z divertiklů nebo stenóza. Operační výkon je také indikován po první atace u imunosuprimovaných pacientů nebo v případech, kdy není možné vyloučit konkomitantní karcinom. U komplikované divertikulitidy je pro indikace v současnosti využívána klasifikace podle Hincheyho – viz. předchozí text. Klasifikace byla poprvé zveřejněna v roce 1978 jako určité vodítko pro to, který z pacientů je při otevřeném resekčním výkonu vhodný pro primární anastomózu. Klasifikace byla postupně modifikována zvláště v souvislosti s rozvojem perkutánních intervencí při léčbě komplikované divertikulární nemoci [17–18]. Pro laparoskopickou resekci sigmatu jsou běžně indikováni pacienti ve stadiu onemocnění Hinchey I-II, nelze-li je v první době řešit pomocí perkutánní drenáže, a to včetně pacientů s kolovezikálními nebo kolovaginálními píštělemi. Řada provedených studií prokazuje srovnatelné výsledky mezi jednotlivými skupinami co do operačního času nebo včasnosti obnovení střevních funkcí. U pacientů s kolovezikálními nebo kolovaginálními píštělemi byly prokázány srovnatelné výsledky s otevřenými operačními výkony [19–21]. Riziko konverzí je uváděno mezi 7,7 a 26 %, některé práce však uvádějí i hodnoty vyšší [1]. Stejně jako u otevřených operací komplikované divertikulární nemoci není jednotná shoda, kdy konstruovat primární anastomózu a kdy zvolit laparoskopicky provedenou Hartmannovu operaci. Volba závisí na řadě faktorů, uvádějí se především body mass index (BMI), Hincheyho klasifikace, urgentnost operace, erudice chirurga, celkový stav pacienta a komorbidity [22]. Stran srovnání nutnosti konverze při laparoskopické resekci sigmatu pro nekomplikovanou a komplikovanou divertikulární nemoc je uváděna až pětinásobně vyšší četnost konverzí v neprospěch laparoskopické operace komplikované divertikulitidy. Literární údaje v tomto směru nepřesahují 26 % [1]. Rozhodující je především pokročilost zánětlivých změn, rozsah adhezí a přítomnost píštělí. Indikace k laparoskopické operaci pro stadia Hinchey III a IV jsou v současné době limitované, podmínkou je možnost srovnatelné toalety peritoneální dutiny jako u otevřené operace. Také v těchto případech zůstává otevřená otázka volby primární anastomózy nebo laparoskopicky provedené Hartmannovy operace. V současné době European Association for Endoscopic Surgery doporučuje laparoskopické řešení pro stadia Hinchey III a IV jen ve vybraných centrech a u selektovaných pacientů – nejde tedy zatím o všeobecné doporučení [23]. Obdobný přístup je i v případě American Society of Colon and Rectal Surgeons, kde není přijat guideline laparoskopického řešení divertikulární nemoci ve stadiu Hinchey III a IV [24]. Podobný přístup zaujímají i další odborné společnosti. Nicméně počet prací a četnost souborů zabývajících se laparoskopickými operacemi těchto stadií narůstá a nové výsledky jsou napjatě očekávány.
Příprava nemocného
Předoperační příprava se odvíjí od předpokládaného rozsahu chirurgického výkonu a celkového klinického stavu nemocného. V následujícím textu jsou uvedena pouze specifika přípravy před laparoskopickou resekcí sigmatu pro divertikulární nemoc a údaje související s multimodální fast-track rehabilitací (ERAS – Enhanced Recovery After Surgery – zrychlená pooperační rehabilitace). U pacientů, kteří přicházejí k plánovanému laparoskopickému operačnímu výkonu pro nekomplikovanou divertikulární nemoc, stejně jako u pacientů s komplikovanou divertikulární nemocí (stadium Hinchey I-II včetně fistulací) je řadou autorů preferována příprava střeva, je-li možná. Způsob přípravy není standardizovaný, osciluje od pouhých dietních opatření před výkonem (bezezbytková, popřípadě chemicky definovaná strava) přes ortográdní přípravu hypertonickými roztoky až po čistě mechanickou přípravu kolon očistnými klyzmaty. Ta sama o sobě však nemusí být technicky dokonalá. Je také možné jednotlivé způsoby přípravy kombinovat. Na základě řady prací z poslední doby je samozřejmě možné provádět operační výkony i na nepřipraveném střevě. Z hlediska techniky laparoskopických operací je však manipulace s připraveným střevem výrazně snazší a příprava střeva umožňuje provedení peroperační koloskopie, ukáže-li se během výkonu jako potřebná. Standardně je před výkonem podávána profylaktická dávka antibiotik, obvykle jde o kombinaci širokospektrého penicilinu nebo cefalosporinu s metronidazolem. Při prodloužení operačního výkonu nad 3 hodiny má být dávka opakována. Stejně tak mají být antibiotika podána při větší peroperační krevní ztrátě, uvádí se více než 1500 ml. Eventuální terapeutické podání antibiotik po plánované operaci komplikované divertikulární nemoci se řídí podle lokálního operačního nálezu. Pacienti jsou standardně zajištěni proti vzniku tromboembolické nemoci, dnes nejčastěji aplikací nízkomolekulárního heparinu (LMWH). U komplikované divertikulární nemoci ve stadiu Hinchey III-IV se většinou jedná o akutní nebo urgentní operaci, tedy bez přípravy střeva. Antibiotika jsou zde podávána v terapeutické dávce. Prevence vzniku tromboembolické nemoci je opět standardem.
Systém multimodální fast-track rehabilitace (ERAS) je popsán a uplatňován u pacientů, kteří jsou plánovaně operováni pro kolorektální karcinom. U pacientů operovaných laparoskopickou technikou pro divertikulární nemoc zatím obdobné práce publikovány nebyly. Pro divertikulární nemoc existuje vzhledem k podobnosti chirurgických výkonů předpoklad obdobných výhod jako u pacientů operovaných pro kolorektální karcinom. Jde zejména o redukci předoperačního a pooperačního hladovění, snížení lokální bolesti, možnost rychlého zatížení stravou a včasnou rehabilitaci umožňující rychlý přechod do ambulantní péče a návrat do běžného života. V předoperační přípravě jsou pacienti v systému fast-track v den přijetí k hospitalizaci vyprázdněni klyzmaty. Je-li to nutné, je redukován příjem pevné stravy 6 hodin před výkonem a doporučuje se pití tekutin bohatých na sacharidy. V den operačního výkonu mohou pacienti přijímat tekutiny bohaté na sacharidy ještě 2 hodiny před výkonem [25–27].
Taktika a technika výkonu
V průběhu doby se vyvinulo několik technik laparoskopické resekce sigmatu. Původně byla resekce popsána jako plně nitrobřišní výkon s extrakcí resekátu přes rektum a transrektálně provedenou staplerovou anastomózou [2,28]. Tento postup byl již víceméně opuštěn. Dnes jsou preferovány víceportové laparoskopicky asistované resekce (Laparoscopic-Assited Colectomy – LAC), kdy je resekát extrahován z minilaparotomie. Druhou variantou jsou rukou asistované výkony (Hand-Assisted Laparoscopic Surgery – HALS), kde je používán speciální port k zavedení ruky do peritoneální dutiny a preparát je extrahován ranou po tomto portu [1]. S rozvojem technického vybavení jsou dnes prováděny i laparoskopicky asistované robotické resekce, vlastní princip operace v peritoneální dutině je však shodný s víceportovou asistovanou laparoskopií [29]. Snaha o další zlepšování kosmetického efektu laparoskopických výkonů a snížení rizika některých komplikací (poruchy hojení ran, vznik hernií) a další redukce pooperační bolesti vedla k vývoji metody jednoincizní, respektive jednoportové laparoskopie (Single-Incision Laparoscopic Surgery – SILS, Minimally Invasive Single-Site Surgery – MISS, Single-Port Surgery – SPS, Single-Access Endoscopic Surgery – SAES, LaparoEndoscopic Single-Site Surgery – LESS, v literatuře existují další synonyma), kdy je pro vstup do peritoneální dutiny využívána jediná incize v oblasti pupku, přes kterou je zavedeno více běžných portů. Využívají se buď běžné laparoskopické nástroje, nebo jediný multiport a pro tento účel specificky vyvinuté instrumentárium. Vlastní operační výkon probíhá však identicky jako u víceportové asistované laparoskopie [30]. Pro úplnost je nutné zmínit zcela nový směr v miniinvazivní chirurgii pohybující se na hranici s digestivní endoskopií označovaný jako NOTES (Natural Orifice Transluminal Endoscopic Surgery), kdy jsou operační výkony v peritoneální dutině včetně resekce sigmatu prováděny zcela novými instrumentárii transgastricky, transvaginálně a v poslední době i transkolonicky nebo transrektálně. Publikované soubory jsou zatím malé, v řadě případů se doposud jedná o experimentální práce na laboratorním zvířeti [31].
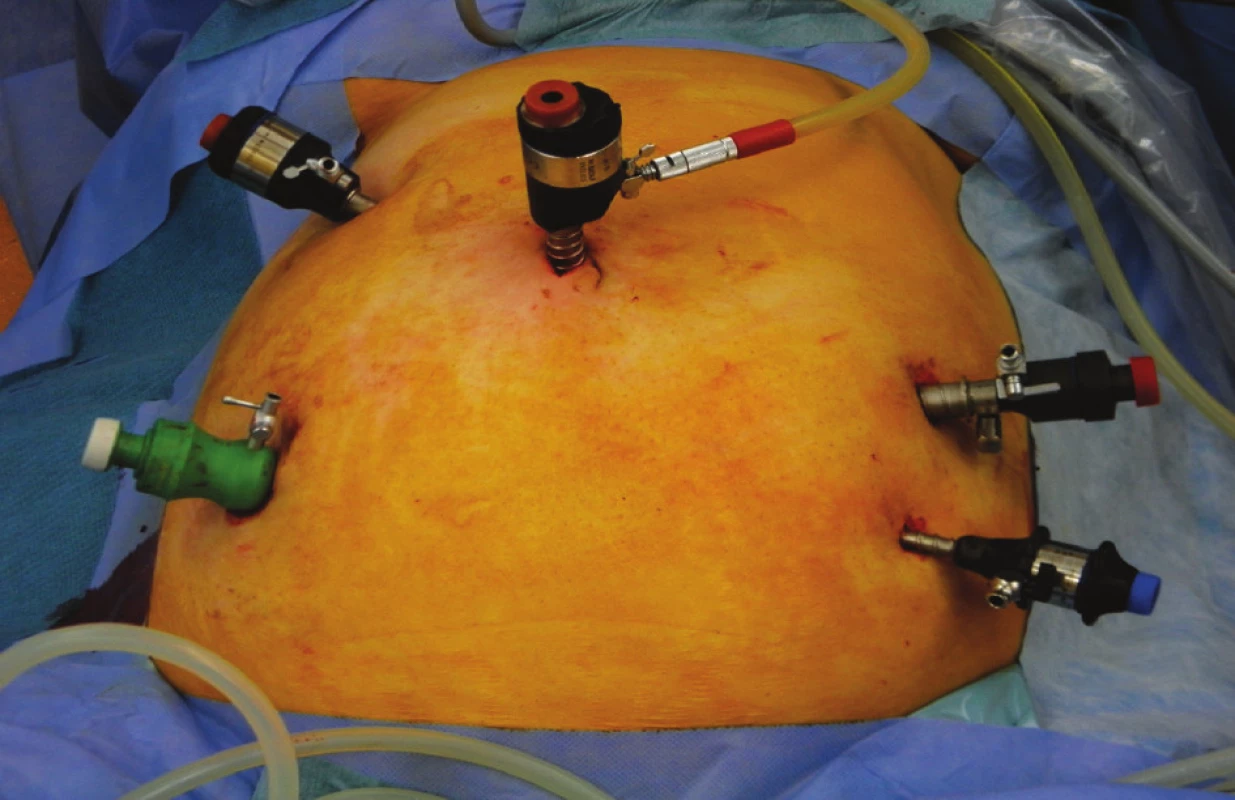
Další část textu se blíže zabývá v současnosti nejpoužívanější technikou laparoskopické resekce sigmatu, a to laparoskopicky asistovanou resekcí (LAC) s několika poznámkami uvádějícími odlišnosti při rukou asistovaných výkonech (HALS). Operační výkon probíhá v celkové anestezii. Epidurální analgezie, není-li pacient zařazen do systému multimodální fast-track rehabilitace, není obvykle vyžadována. Pacient je standardně v poloze na zádech v modifikované litotomické pozici s abdukovanými a v kolenou mírně flektovanými končetinami. Pravá i levá paže jsou u těla, levá paže může být upažena v úhlu 90 stupňů. V průběhu výkonu je pacient v Trendelenburgově pozici minimálně o 15 stupňů, výhodné je také mírné natočení na pravý bok. V případě nezbytnosti mobilizace slezinného ohbí je pacient převeden do anti-Trendelenburgovy pozice. Operatér a druhý asistent stojí na pravé straně pacienta, první asistent vlevo. Postavení instrumentářky není jednotné, může být jak na pravé straně pacienta, tak při jeho levé dolní končetině a odvíjí se od místních zvyklostí, polohy laparoskopické věže a počtu monitorů. Počet, umístění a průměr trokarů pro laparoskopickou resekci sigmatu jsou variabilní a opět závisí na zvyklostech, instrumentáriu a zkušenostech operačního týmu. Zhruba 70 % autorů používá 5 trokarů, 30 % 4 trokary – Obr. 1. Asi 30 % autorů provádí rukou asistované výkony [32]. Pneumoperitoneum se zakládá nejčastěji v oblasti pupku s použitím Veressovy jehly, někteří autoři preferují použití 10mm Hassanova trokaru [1]. Při předpokladu srůstů v dutině břišní je pro zavedení prvního portu bezpečnější otevřený přístup. Tlak v dutině břišní během výkonu se doporučuje v rozmezí 12–15 mmHg. Po stránce umístění portů panuje všeobecná shoda na zavedení 12mm trokaru v pravém podbřišku pro lineární stapler. Další porty se zavádějí v oblasti pupku a pravého horního kvadrantu, podle zvyklosti mohou být oba využity jako kamerové. V levém dolním kvadrantu je zaváděn jeden nebo 2 porty (Obr. 1). Při rukou asistovaných výkonech je hand-port zaváděn v oblasti pupku. Minilaparotomie pro extrakci resekátu z peritoneální dutiny a zavedení klobouku cirkulárního stapleru jsou prováděny v levém dolním kvadrantu, lze využít i suprapubického řezu nebo dolní střední minilaparotomie. Při rukou asistovaných výkonech je k extrakci resekátu používána incize po zavedení hand-portu [1]. Vlastní operační výkon zahajujeme revizí peritoneální dutiny otevřením retroperitoneální fascie podél pravé ilické tepny. Pokračujeme kraniálně s identifikací dolní mezenterické tepny při jejím odstupu a dále dolní mezenterické žíly. Za dolní mezenterickou tepnou je vypreparován levý ureter, identifikují a šetří se hypogastrické nervy, gonadální cévy a vypreparuje se levá ilická tepna. K preparaci lze použít mono nebo bipolární elektrokauter, nůžky, ultrazvukový nůž nebo jiný nástroj. Dolní mezenterická tepna je přerušena lineárním staplerem, ultrazvukovým nožem, s využitím extrakorporální nebo intrakorporální ligace nebo vůbec nejčastěji po naložení klipů – Obr. 2. Dolní mezenterická žíla se přeruší, pokud je to nezbytné. Po zvednutí pediklu dolní mezenterické tepny je dokončena mediolaterální preparace v řídké vazivové tkáni podél Toldtovy fascie. Kolon je následně přesunuto mediálně s dokončením laterální disekce. Je možný i lateromediální postup. Pro beznapěťovou anastomózu je někdy nezbytné mobilizovat levé kolon a slezinné ohbí. Pacient je přesunut do anti-Trendelenburgovy polohy, je otevřeno gastrokolické ligamentum, přerušeno frenokolické a splenokolické ligamentum a dokončena mobilizace levého tračníku. V případě kolovezikální nebo kolovaginální píštěle je s výhodou jejich přerušení ultrazvukovým nožem, sutura defektu není vždy nezbytná. Po dokončení mobilizace a skeletizace mezokolon se tračník přeruší lineárním staplerem pod úrovní sigmoideorektálního přechodu – Obr. 3. Je prokázán vyšší výskyt recidiv divertikulární nemoci, je-li distální resekční linie posunuta orálněji na sigma [33]. Resekát je vytažen před břišní stěnu z minilaparotomie, vhodná je ochrana rány plastikovým rukávem. Proximální resekční linie je volena orálně od hranice zánětlivých změn, hypertrofie svaloviny nebo jiné patologie související se základním onemocněním. Po přerušení střeva je do orálního pahýlu zaveden klobouk cirkulárního stapleru. Střevo je poté reponováno zpět do peritoneální dutiny, je uzavřena minilaparotomie a obnoveno pneumoperitoneum. Transanálně zavedeným cirkulárním staplerem je konstruována anastomóza – Obr. 4. Následně je provedena tlaková zkouška. Při eventuálním anastomotickém leaku je ve většině případů nutné založit pojistnou ileostomii. Výhody užití ruky pro preparaci při hand-asistovaných výkonech není potřeba blíže rozvádět. Při urgentních nebo akutních resekcích sigmatu pro divertikulární nemoc ve stadiu Hinchey III nebo IV může být provedena laparoskopická resekce sigmatu podle Hartmanna s konstrukcí terminální kolostomie v místě orální resekční linie, ponecháním slepě uzavřeného pahýlu rekta, důslednou laváží a drenáží peritoneální dutiny a konstrukcí definitivní anastomózy ve druhé době. Při konstrukci primární staplerové anastomózy může být v těchto stadiích doplněna pojistná ileostomie [24, 34,35].
2. Přerušená dolní mezenterická tepna po jejím zaklipování 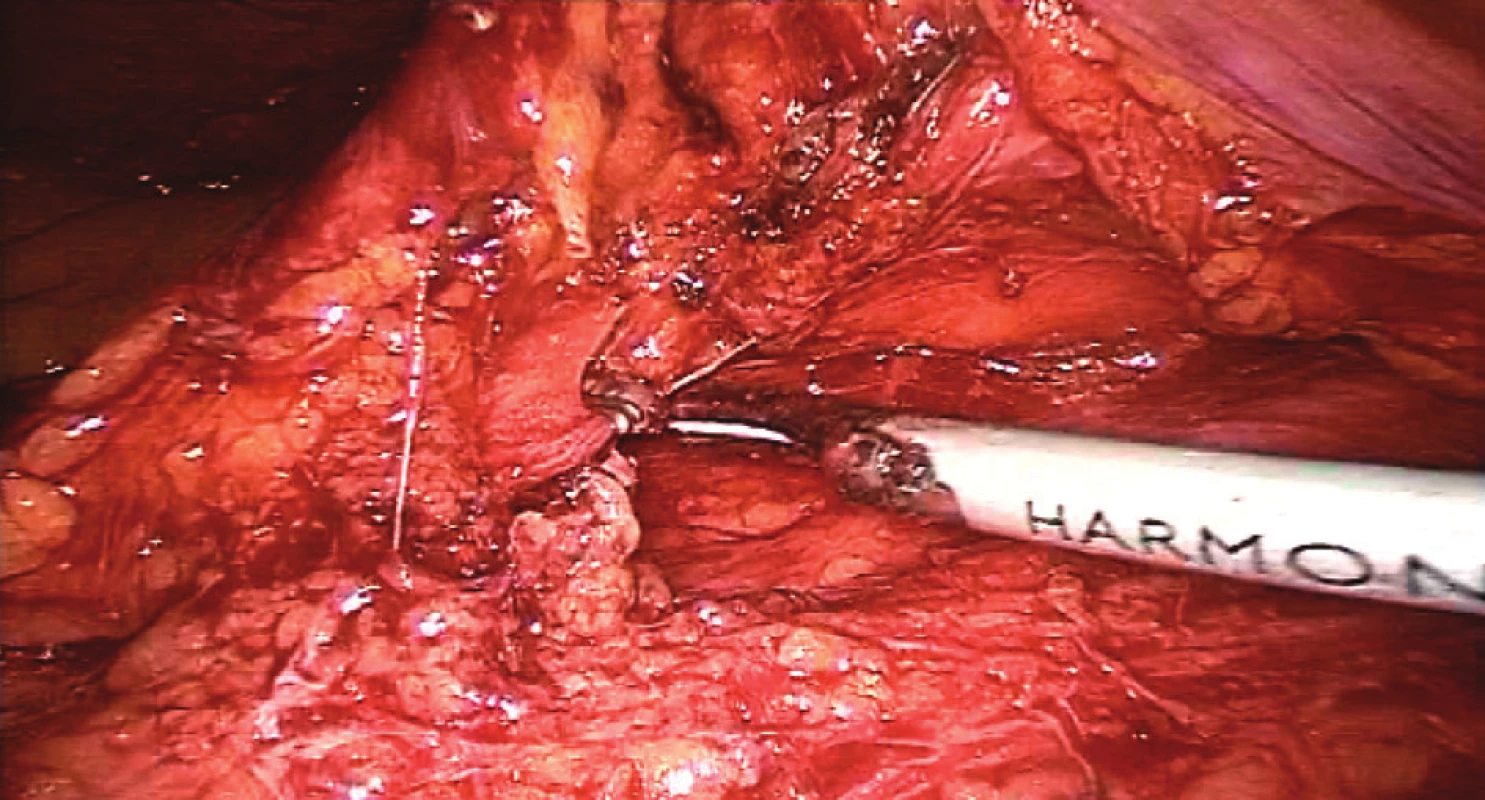
3. Naložení lineárního stapleru na střevo 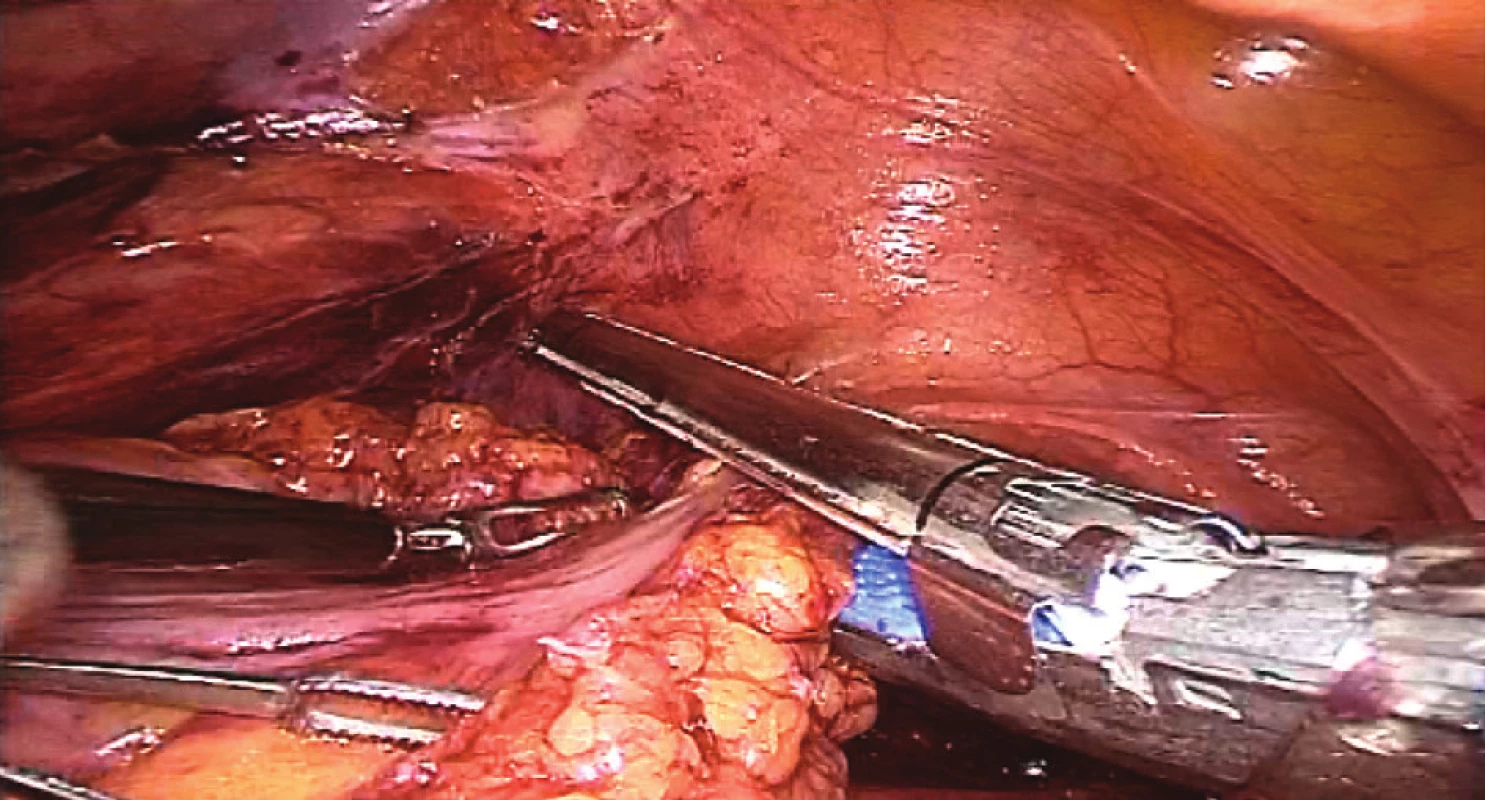
4. Konstrukce staplerové anastomózy 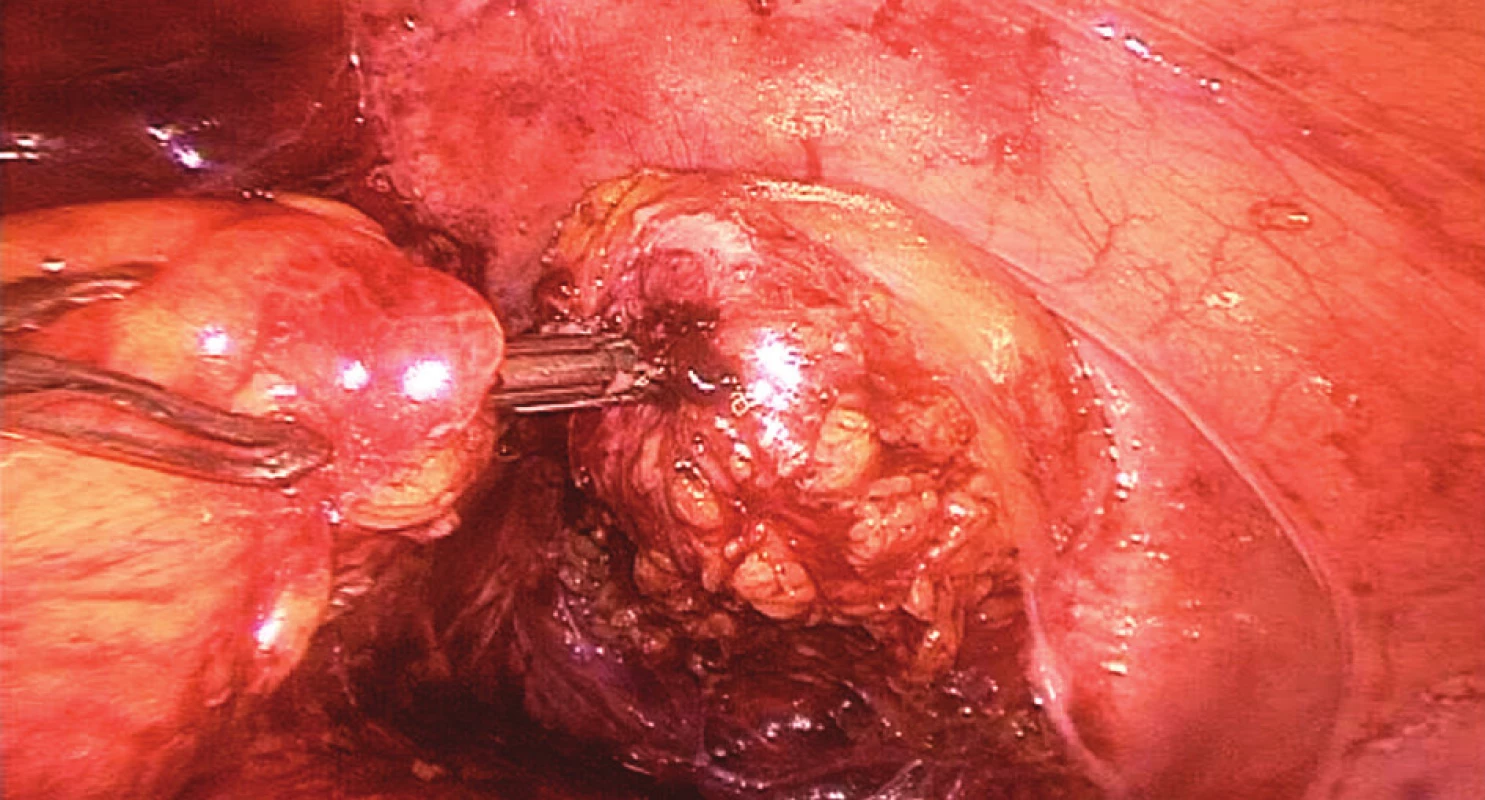
Při provedení výkonu v celkové anestezii systémem multimodální fast-track rehabilitace se doporučuje několik zásad:
- restrikce intravenózního příjmu tekutin na 500 ml krystaloidů a 500 ml koloidů peroperačně,
- použití vazopresorů při korekci peroperační hypotenze
- infiltrace ran lokálním anestetikem,
- v případě zavedení nazogastrické sondy její extrakce před extubací,
- zavedení permanentního močového katetru jen na nezbytně nutnou dobu,
- po stránce drenáže peritoneální dutiny nejsou doporučení zatím jednoznačná [25,26,27].
Pooperační péče
V současné době nejsou publikována žádná závazná doporučení, týkající se pooperační péče po laparoskopické resekci sigmatu pro divertikulární nemoc, která by se lišila od standardních postupů po laparoskopických resekčních výkonech na tračníku pro kolorektální karcinom, respektive obecně po resekčních výkonech na tračníku. Laparoskopický výkon umožňuje vzhledem k nižší pooperační bolesti kratší dobu podávání analgetik s časným přechodem na perorální formy, užití opiátových analgetik není v řadě případů vůbec nutné. Časná realimentace vzhledem k dřívější obnově pasáže proti otevřeným výkonům i možnost časné mobilizace bývají pravidlem.
V systému multimodální fast-track rehabilitace se v časném pooperačním období doporučuje kombinovat epidurální analgezii s podáváním paracetamolu. Vhodnou alternativou jsou také gabapentanoidy nebo nesteroidní antirevmatika. První tekutiny přijímá pacient dvě hodiny po operaci, s výhodou je podání roztoků bohatých na sacharidy. Intravenózní příjem tekutin by neměl překročit 1,5 litru. Drén, je-li zaveden, je odstraněn do 24 hodin po výkonu. Je zahájena časná rehabilitace s pobytem dvě hodiny mimo lůžko. Večer po operaci pacient přijímá polotuhou stravu. První pooperační den se doporučuje perorální příjem tekutin okolo 2 litrů, vhodné jsou opět roztoky se sacharidy. Možné je začít s běžnou dietou, zastavuje se i.v. příjem roztoků a podle potřeby mohou být podána laxativa. Permanentní močový katétr je odstraněn, jestliže je mikční reziduum nižší než 50 ml. Požadavek na rehabilitaci mimo lůžko je v rozsahu více než 6 hodin. Druhý pooperační den je odstraněn epidurální katétr, pacient by již měl užívat jen perorální analgetika. Je odstraněna i.v. kanyla. Pokračuje se v podávání laxativ, je-li to nutné. Pacient dostává běžnou dietu. Rehabilitace by měla přesáhnout 8 hodin mimo lůžko. Další pooperační dny se již režimově neliší. Pacient je dimitován v okamžiku, kdy je pooperační bolest řešitelná pouze perorálními analgetiky, má obnovenou pasáž a je plně realimentován. Podmínkou časné dimise je také absence vážnějších ranných komplikací [25–27].
Závěr
Laparoskopická resekce sigmatu pro divertikulární chorobu je dnes plně akceptovanou alternativou klasického operačního řešení. S rozvojem zkušeností chirurgických týmů a technického vybavení umožňuje operační řešení u pacientů s komplikovanou divertikulární nemocí včetně ošetření náhlých břišních příhod. Přínosem je především redukce morbidity, nižší pooperační bolest a kratší doba hospitalizace. Ze závažných komplikací je v případě laparoskopií prokázán nižší výskyt raných infekcí, plicních a kardiovaskulárních komplikací a pooperačních ileózních stavů. Z pozdních komplikací se u laparoskopií uvádí nižší výskyt kýl a srůstů. Určitou nevýhodou jsou vyšší ekonomické náklady dané cenou technického a materiálního vybavení. Provádění plánovaných laparoskopických resekcí sigmatu pro divertikulární nemoc v systému multimodální fast-track rehabilitace je příslibem dalšího zlepšení a zefektivnění péče o pacienty s divertikulární nemocí.
MUDr. Lukáš Vrbenský
Chirurgická klinika 1. LF UK a TN
Vídeňská 800
140 59 Praha 4 – Krč
e-mail: lukas.vrbensky@ftn.cz
Sources
1. Lipman JM, Reynolds HL. Laparoscopic Management of Diverticular Disease. Clin Colon Rectal Surg 2009;223 : 173–180.
2. Jacobs M, Verdeia JC, Goldstein HS. Minimally invasive colon resection (laparoscopic colectomy). Surg Laparosc Endosc 1991;1,3 : 144–150.
3. Weber WP, Guller U, Jain NB, Pietrobon R, Oertli D. Impact of surgeon and hospital caseload on the likelihood of performing laparoscopic vs open sigmoid resection for diverticular disease: a study based on 55,949 patients. Arch Surg 2007;142,3 : 253–259, discussion 259.
4. Klarenbeek BR, Veenhof AA, Bergamashi R, et al. Laparoscopic sigmoid resection for divertikulitis decreases major morbidity rates: a randomized kontrol trial: short-term results of the sigma Trial. Ann surf 2009;249,1 : 39–44.
5. Milsom JW, Böhm B, Hammerhofer KA, Fazio V, Steiger E, Elson P. A prospective, randomized trial comparing laparoscopic versus conventional techniques in colorectal cancer surgery: a preliminary report. J Am Coll Surg 1998;187,1 : 46–54, discussion 54–55.
6. Schwenk W, Böhm B, Müller JM. Postoperative pain and fatigue after laparoscopic or conventional colorectal resections. A prospective randomized trial. Surg Endosc 1998;12,9 : 1131–1136.
7. Purkayastha S, Constantinides VA, Tekkis PP, et al. Laparoscopic vs. open colectomiy for diverticular disease: a meta-analysis of nonrandomized studies. Dis Colon Rectum 2006;49,4 : 446–463.
8. Dwivedi A, Chahin F, Agrawal S, et al. Laparoscopic colectomy vs. open colectomy for sigmoid diverticular disease. Dis Colon Rectum 2002;45,10 : 1309-1314, discussion 1314–1315.
9. Chen HH, Wexner SD, Iroatulam AJ, et al. Laparoscopic colectomy compares favorably with colectomy by laparotomy for reduction of postoperative ileus. Dis Colon Rectum 2000;43,1 : 61–65.
10. Senagore AJ. Laparoscopic sigmoid colectomy for diverticular disease. Surg Clin North Am 2005;85,1 : 19–24, vii.
11. Guller U, Jain J, Hervey S, Purves H, Pietrobon R. Laparoscopic vs. open colectomy: outcomes comparison based on large nationwide databases. Arch Surg 2003;138,11 : 1179–1186.
12. Lawrence DM, Pasquale MD, Wasser TE. Laparoscopic versus open sigmoid colectomy for divertikulitis. Am Surg 2003;69, 6 : 499–503.
13. Senagore AJ, Duepree HJ, Delaney CP, Dissanaike S, Brady KM, Fazio VW. Cost structure of laparoscopic and open sigmoid colectomy for diverticular disease: similarities and differences. Dis Colon Rectum 2002;45,4 : 485–490.
14. Liberman MA, Phillips EH, Carroll BJ, Fallas M, Rosenthal R. Laparoscopic colectomy vs traditional colectomy for divertikulitis. Outcome and costs. Surg Endosc 1996;10,1 : 15–18.
15. Stocchi L, Nelson H, Young-Fadok TM, Larson DR, Ilstrup DM. Safety and edvantages of laparoscopic vs. open colectomy in elderly: matched-control study. Dis Colon Rectum 2000;43, 3 : 326–332.
16. Tuech JJ, Pessaux P, Rouge C, Regenet N, Bergamaschi R, Arnaud JP. Laparoscopic vs open colectomy for sigmoid diverticulitis: a prospective comparative study in the elderly. Surg Endosc 2000;14,11 : 1031–1033.
17. Hinchey EJ, Schaal PG, Richards GK. Treatment of perforated diverticular disease of colon. Adv Surg 1978;12 : 85–109.
18. Wexner SD, Moscovitz ID. Laparoscopic colectomy in diverticular and Crohn‘s disease. Surg Clin North Am 2000;80,4 : 1299–1319.
19. Poulin EC, Schlachta CM, Mamazza J, Seshadri PA. Should enteric fistulas from Crohn‘s disease or diverticulitis be treated laparoscopically or by open Surgery? A matched kohort study. Dis Colon Rectum 2000;43,5 : 621-626, discussion 626–627.
20. Laurent SR, Detroz B, Detry O, Dagaugue C, Honoré P, Meurisse M. Laparoscopic sigmoidectomy for fistulized diverticulitis. Dis Colon Rectum 2005;48,1 : 148–152.
21. Bartus CM, Lipof T, Sarwar CM, et al. Colovesical fistula: not a contraindication to elective laparoscopic colectomy. Dis colon Rectum 2005;48,2 : 233–236.
22. Aydin HN, Tekkis PP, Remzi FH, Constantinides V, Fazio VW. Evaluation of the risk of a nonrestorative resection for the treatment of diverticular disease: Cleveland Clinic diverticular disease propensity score. Dis Colon Rectum 2006;49,5 : 629–639.
23. Kreis ME, Jauch KW. Diverticular Disease – Update 2006. In: Neugebauer EAM, Sauerland S, Fingerhut A, Millat B, Buess G. EAES Guidelines for Endoscopic Surgery. Berlin Heidelberg New York, Springer, 2006 : 157–160.
24. Sauerland S, Agresta F, Bergamaschi R, et al. Laparoscopy for abdominal emenrgencies: evidence-based guidelines of the European Association for Endoscopic Surgery. Surg Endosc 2006;20,1 : 14–29.
25. Kehlet H, Wilmore DW. Fast-track surgery. Br J Surg 2005; 92 : 3–4.
26. Schwenk W, Neudecker J, Raue W, Haase O, Müller JM. ‚‘Fast-track‘‘ rehabilitation after rectal cancer resection. Int J Colorectal Dis 2005;9 : 1–7.
27. Basse L, Jakobsen DH, Bardram L, Billesbolle P, Lund C, Mogensen T, Rosenberg J, Kehlet H. Functional recovery after open versus laparoscopic colonic resection: a randomized, blinded study. Ann Surg 2005;241 : 416–423.
28. Redwine DB, Sharpe DR. Laparoscopic segmental resection of sigmoid colon for endometriosis. J Laparoendoscop Surg 1991;1, 4 : 217–220.
29. Baik HS. Robotic colorectal surgery. Yonsei Med J 2008;49, 6 : 891–896.
30. Diana M, Dhumane P, Cahill RA, Mortensen N, Leroy J, Marescaux J. Minimal invasive single-site surgery in colorectal procedures: Current state of the art. J Minim Access Surg 2011;7, 1 : 52–60.
31. Zorron R. Natural orifice surgery applied for colorectal diseases.World J Gastrointest Surg 2010;2,2 : 35–38.
32. Veldkamp R, et al. The EAES Clinical Practice Guidelines on Laparoscopic Resection of Colonic Cancer (2004). In: Neugebauer EAM, Sauerland S, Fingerhut A, Millat B, Buess G. EAES Guidelines for Endoscopic Surgery. Berlin Heidelberg New York, Springer 2006 : 161–207.
33. Thaler K, Baig MK, Berho M, et al. Determinants of recurrence after sigmoid resection for uncomplicated diverticulitis. Dis Colon Rectum 2003;46,3 : 385–388.
34. Mutter D, Bouras G, Forgione A, Vix M, Leroy J, Marescaux J. Two-stage totally minimally invasive approach for acute complicated diverticulitis. Colorectal Dis 2006;8,6 : 501–505.
35. Franklin ME, Jr, Dorman JP, Jacobs M, Plasencia G. Is laparoscopic surgery applicable to complicated colonic diverticular disease? Surg Endosc 1997;1110 : 1021–1025.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2013 Issue 7-
All articles in this issue
- When a surgical patient needs parenteral nutrition
- The staple line in sleeve gastrectomy
- Intraoperative CT navigation in spinal and pelvic surgery: initial experience
- CT diagnostics of scapular fractures
- Repetitive reoperation of the DHS failure: clinical and biomechanical analysis – a case report
- Ileocaecal actinomycosis – a case report
- Diverticular disease of the large bowel – imaging methods
- Diverticular disease of the large bowel – surgical treatment
- Laparoscopic resection of the sigmoid colon for the diverticular disease
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Laparoscopic resection of the sigmoid colon for the diverticular disease
- Diverticular disease of the large bowel – surgical treatment
- Diverticular disease of the large bowel – imaging methods
- The staple line in sleeve gastrectomy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career