-
Medical journals
- Career
Podtlaková terapie (vacuum-assisted closure) v léčbě ranných infekčních komplikací po kardiochirurgických výkonech
Authors: M. Šimek 1; P. Němec 1; B. Zálešák 2; R. Hájek 1; M. Kaláb 1; I. Fluger 1; M. Kolář 3; L. Ječmínková 1; P. Gráfová 1
Authors‘ workplace: Kardiochirurgická klinika, přednosta: doc. MUDr. P. Němec, CSc. 1; Oddělení plastické a estetické chirurgie, přednosta: MUDr. B. Zálešák, Ph. D. 2; Ústav mikrobiologie, antibiotické centrum, přednostka: doc. MUDr. D. Koukalová, CSc. FN a LF Univerzity Palackého v Olomouci 3
Published in: Rozhl. Chir., 2007, roč. 86, č. 8, s. 404-409.
Category: Monothematic special - Original
Overview
Úvod:
Podtlaková terapie (vaccum-assisted closure) představuje moderní strategii léčby rozsáhlých ranných infekčních komplikací po kardiochirurgických výkonech, zvláště v léčbě hluboké sternální infekce.Metody:
Prospektivní sledování souboru 40 nemocných, u kterých byla aplikována podtlaková terapie (VAC system™, KCI, Austria, Hartmann-Rico, a.s., ČR) v období XI/2005–I/2007. U 36 nemocných (90 %) byla terapie použita v léčbě sternální infekce, z toho u 10 nemocných (25 %) pro povrchovou a 26 nemocných (65 %) pro hlubokou sternální infekci. Dále byli 4 nemocní (10 %) léčeni pro rozsáhlé infekční komplikace po odběru žilního štěpu či kanylaci femorální tepny. Střední věk souboru byl 69,9 ± 9,7 let, ženy lehce dominovaly (57 %), diabetes mellitus byl přítomen u 22 nemocných (55 %) a 4 nemocní (10 %) předoperačně užívali imunosupresiva. U 7 nemocných (18 %) byla podtlaková terapie použita po předchozím selhání konvenční terapie.Výsledky:
U 38 nemocných (95 %) došlo ke zhojení rány, 2 nemocní (5 %) léčení pro hlubokou sternální infekci v souboru zemřeli. Průměrná hospitalizační doba dosáhla 36,4 ± 22,6 dnů, průměrná doba aplikace VAC systému 9,7 ± 3,9 dnů a průměrně bylo provedeno 4,6 ± 1,8 převazů (výměn systému) v rámci jedné léčby. U všech nemocných byl VAC systém použit jako příprava k sekundárnímu uzávěru rány. Čtyři nemocní (10 %) v souboru byli s různým měsíčním časovým odstupem od uzávěru rehospitalizováni pro píštěle vázané na drátěné kličky po uzávěru sternotomie.Závěr:
Podtlaková terapie představuje účinnou a efektivní léčbu rozsáhlých raných komplikací v kardiochirurgii. Nízké riziko selhání léčby, ale především významné snížení mortality a morbidity nemocných léčených pro hlubokou sternální infekci, upřednostňuje primární aplikaci této terapie, zvláště u nemocných s přítomností rizikových faktorů poruch hojení.Klíčová slova:
podtlaková terapie – vacuum-assited closure – chirurgické komplikace – sternální infekce – kardiochirurgieÚVOD
V posledních letech jsou ke kardiochirurgickým výkonům indikováni nemocní, jejichž pokročilý věk či přítomnost významných přidružených komorbidit by jistě ještě před 10 lety znamenaly kontraindikaci těchto výkonů. Pokrok v chirurgických technikách, snaha o menší invazivitu během výkonů společně s úzkostnou pooperační péčí umožňují dosahovat velmi dobrých výsledků z pohledu mortality u této skupiny nemocných [1]. Na druhou stranu je zřejmé, že právě tato skupina nemocných je zatížena vyšším výskytem pooperačních komplikací [2, 3]. Rané infekční komplikace po kardiochirurgických výkonech přestavují vážný medicínský problém, který je spojen s významným nárůstem morbidity a mortality nemocných [3, 4]. Dále tyto komplikace způsobují neméně významný ekonomický problém spojený s nárůstem nákladů na léčbu, prodlouženou délku hospitalizace či potřebu následné péče [4, 5]. I když se incidence těchto komplikací liší mezi jednotlivými institucemi, obecně je udávána mezi 3 až 11 % [4, 6, 7].
Podtlaková terapie (Vacuum-assisted closure, VAC) byla zavedena do klinické praxe v roce 1997, původně jako léčebná metoda terapeuticky špatně ovlivnitelných ran jako jsou proleženiny či syndrom diabetické nohy [8, 9]. Posléze byla prokázána účinnost VAC terapie u rozsáhlých infekčních komplikací po břišních chirurgických výkonech a následně se terapie ukázala i vysoce efektivní v léčbě raných infekčních komplikací v kardiochirurgii [10, 11].
SOUBOR NEMOCNÝCH A METODA
V období XI/2005–I/2007 byla podtlaková terapie (VAC system™, KCI Austria, Hartmann-Rico, a.s., ČR) použita u 40 nemocných, kteří podstoupili kardiochirurgický výkon na našem pracovišti. U 36 nemocných (90 %) byl systém použit v léčbě infekce sternotomie, z toho u 10 nemocných (25 %) pro povrchovou a 26 nemocných (65 %) pro hlubokou sternální infekci. Čtyři pacienti (10 %) byli léčeni pro rozsáhlé infekční komplikace po odběru žilního štěpu či kanylaci femorální tepny. Tabulka 1 shrnuje demografické ukazatele (věk, BMI, pohlaví, přítomnost rizikových faktorů), tabulka 2 udává typy jednotlivých kardiochirurgických výkonů a v tabulce 3 jsou popsány jednotlivé charakteristiky podtlakové terapie (počet převazů, délka VAC terapie a celková délka hospitalizace). Do léčebného protokolu použití VAC systému byli nejdříve zahrnuti pacienti s povrchovou sternální infekcí a nemocní s rozsáhlými infekčními komplikacemi ve stehenní oblasti po odběrech vena safena magna či po kanylaci arteria femoralis. Následně byla VAC terapie použita u 7 nemocných s hlubokou sternální infekcí po selhání do té doby standardní léčby zavřenou laváží. Na základě pozitivní a vzrůstající zkušenosti s terapií byla VAC terapie použita u následných 19 nemocných s hlubokou sternální infekcí jako léčebná strategie první volby. V souboru je zahrnuto i 18 nemocných (48 %), kteří byli rehospitalizovaní z důvodu hluboké infekce sternotomie, a to i přes klinické známky primárního hojení sternotomie v době jejich propuštění. S tímto faktem koresponduje i průměrná doba klinické manifestace raného infektu od výkonu, která dosáhla 18,5 ± 11,8 dnů.
Table 1. Předoperační charakteristika souboru Tab. 1. The study group preoperative characteristics 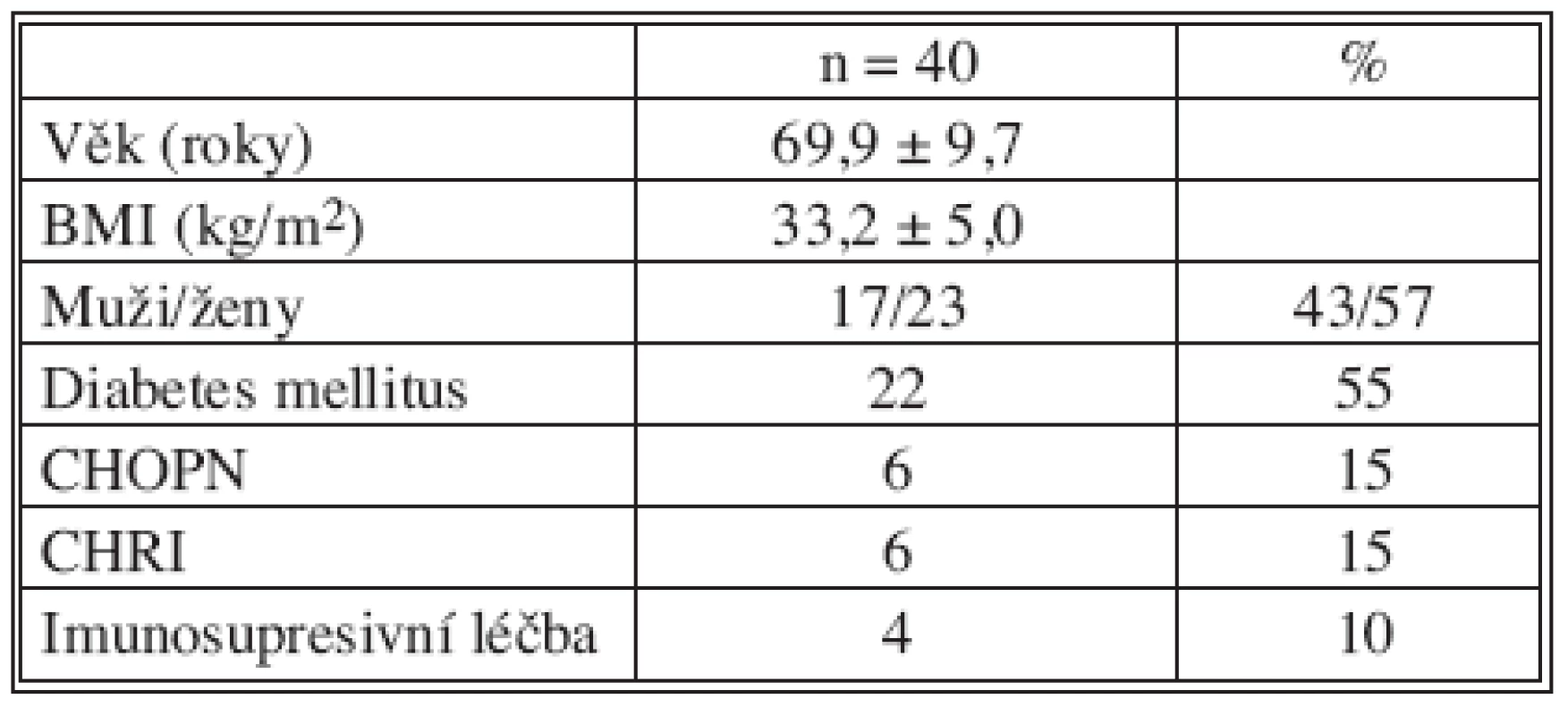
BMI – body mass index CHRI – chronická renální insuficience CHOPN – chronická obstrukční plicní nemoc Table 2. Chirurgické výkony Tab. 2. Surgical procedures 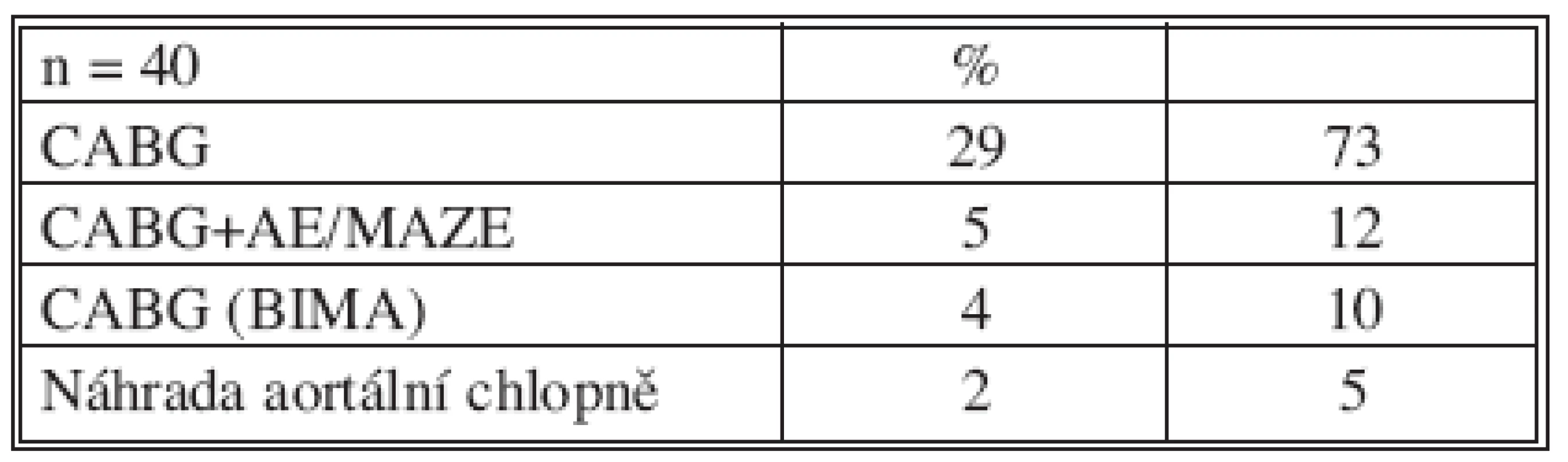
CABG – aortokronární bypass AE – aneurysmectomie levé komory MAZE – chirurgická léčba fibrilace síní BIMA – použití obou a. thoracica interna Table 3. Charakteristika podtlakové terapie Tab. 3. Vacuum therapy characteristics 
KLASIFIKACE STERNÁLNÍHO INFEKTU A RIZIKOVÉ FAKTORY JEHO ROZVOJE
Sternální infekce byla definován na základě doporučení Centra pro kontrolu a prevenci chorob (Center for Disease Control and Prevention, Atlanta, USA) [12]. Postižení měkkých tkání sternotomie nad pektorální fascií bylo klasifikováno jako povrchová, postižení hrudní kosti či struktur mediastina jako hluboká sternální infekce. Rovněž diagnóza rané infekce byla stanovena na základě těchto doporučení, tedy na podkladě kultivačního průkazu agens či klinických a laboratorních známek infektu [12, 13]. Za rizikové faktory rozvoje sternální infekce byly pokládany: obezita (BMI > 30), pediklovaný odběr obou a. thoracica interna, diabetes mellitus, chronická obstrukční choroba plicní, revize pro krvácení a podání více než 5 krevní transfuzí v pooperačním období [4, 12, 13].
PROTOKOL APLIKACE PODTLAKOVÉ TERAPIE
Pro léčbu všech infekčních komplikací byl zaveden jednotný protokol. Za aseptických kautel byly nejdříve provedeny stěry z rány pro kultivační vyšetření. Následoval šetrný chirurgický debridement, kdy byla odstraněna veškerá nekrotická tkáň a v případě hlubokého sternálního infektu i všechen cizorodý materiál (drátěné kličky) (Obr. 1). Důraz byl kladen na pečlivou hemostázu a poté byla rána opakovaně vypláchnuta fyziologickým roztokem. Do rány byla vložena polyuretanová pěna s definovanou strukturou (Granufoam™, KCI Austria, Hartmann-Rico, a.s., ČR), jejíž tvar byl upraven podle tvaru a velikosti rány. V případě hluboké infekce sternotomie byla aplikována pěna ve 2 vrstvách a to tak, že nejdříve byla vložena do předního mediastina a pod sternální okraje, a následně druhá vrstva byla použita k vyplnění prostoru mezi a nad hrudní kostí. Rána vyplněná pěnou společně s okolní kůží byla přelepena adhezivní fólií s přesahem minimálně 3–5 cm od okrajů rány. Drenážní systém (TRACpad™, KCI Austria, Hartmann-Rico a.s., ČR) byl fixován v centrální části pěny a následně spojen s generátorem podtlaku (VAC ATS™ pump unit; KCI Austria, Hartmann-Rico a.s., ČR) (Obr. 2), jehož součástí je i 500 ml sběrný kanystr. Iniciálně byl podtlak nastaven na 50 mm Hg a byla provedena modelace pěny. Následovala terapeutická aplikace nepřerušovaného podtlaku s cílovou hodnotou 100–125 mm Hg (Obr. 3). Převazy byly prováděny za 24–72 hodin v závislosti na charakteru rány, charakteru exsudátu a průběhu terapie. Při následném převazu byl aplikován identický protokol. Nemocní s defekty na dolních končetinách a povrchových sternálním infektem byli převazováni v analgosedaci či trankanalgezii. Převazy u nemocných s hlubokou sternálním infekcí byly provedeny v celkové anestezii s myorelaxací na operačním sále. Krátce po převazu a dosažení terapeutického podlaku byli tito nemocní extubováni, pokud to dovolil jejich celkový stav (Obr. 4). Součastí protokolu byla nutriční podpora s důrazem na enterální výživu a striktní protokol kontroly glykemií pomocí inzulinoterapie. Bezprostředně po vyjádření podezření pro ranou infekci byla zahájena empirická antibiotická léčba a následně upravena dle kultivačního nálezu a stanovené citlivosti. Kultivační nálezy shrnuje tabulka 4. K uzávěru rány bylo přikročeno na základě příznivého lokálního nálezu, opakované negativity kultivačních vyšetření a poklesu zánětlivých markerů (hodnota CRP < 30 mmol/l) (Obr. 5). Antibiotické terapie byla vysazena po uzávěru rány, v případě hluboké infekce sternotomie bylo v perorální terapii pokračováno po dobu dalších 4 týdnů. Následný uzávěr rány, respektive rekonstrukce defektu, byla provedena na podkladě jeho rozsahu tak, aby bylo docíleno beztahové sutury (Obr. 6). V případě hluboké sternální infekce byla vždy snaha kompletně či částečně osteosyntezovat sternální okraje k dosažení stability hrudního koše.
Image 1. Hluboká sternální infekce. Debridement před aplikací VAC systému Fig. 1. Deep sternal infection. Surgical debridement prior to application of the VAC system 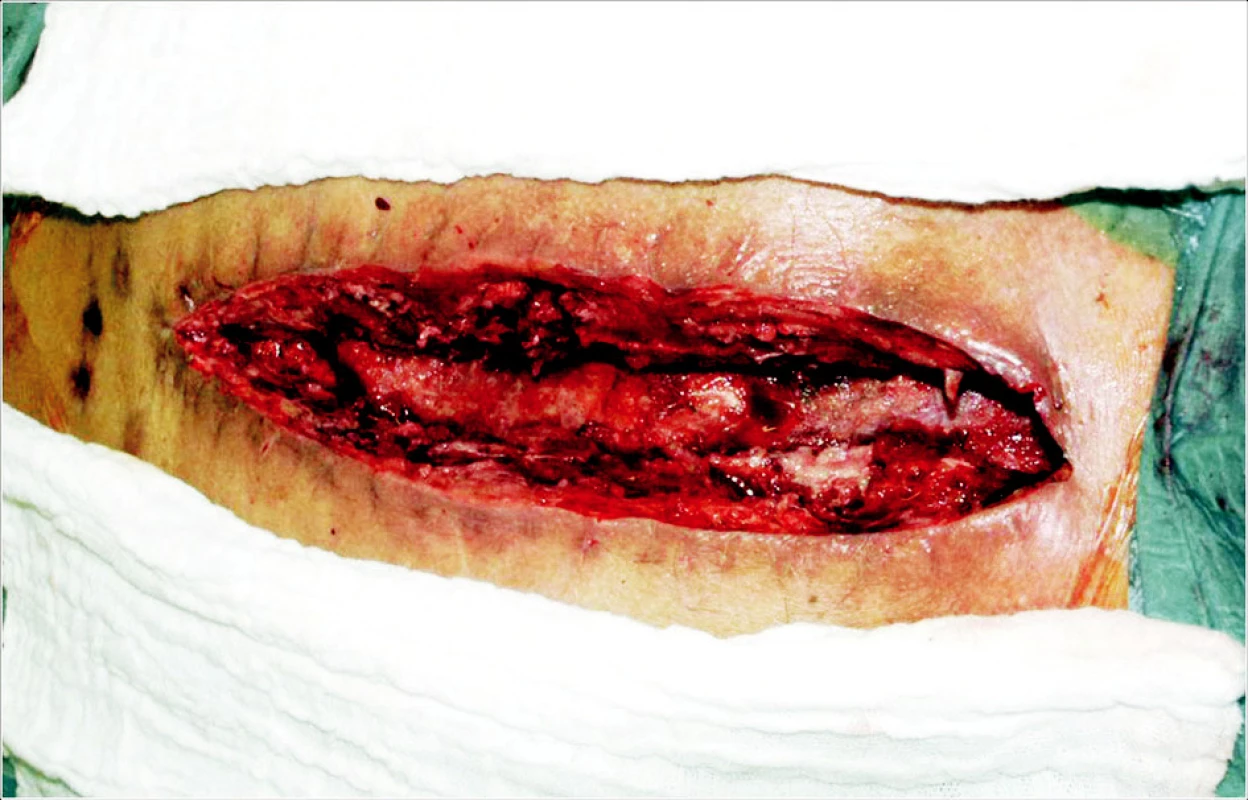
Image 2. Generátor podtlaku VAC ATS™ Fig. 2. VAC ATS™ pump unit 
Image 3. Hluboká sternální infekce. Aktivní podtlaková terapie Fig. 3. Deep sternal infection. Working VAC therapy 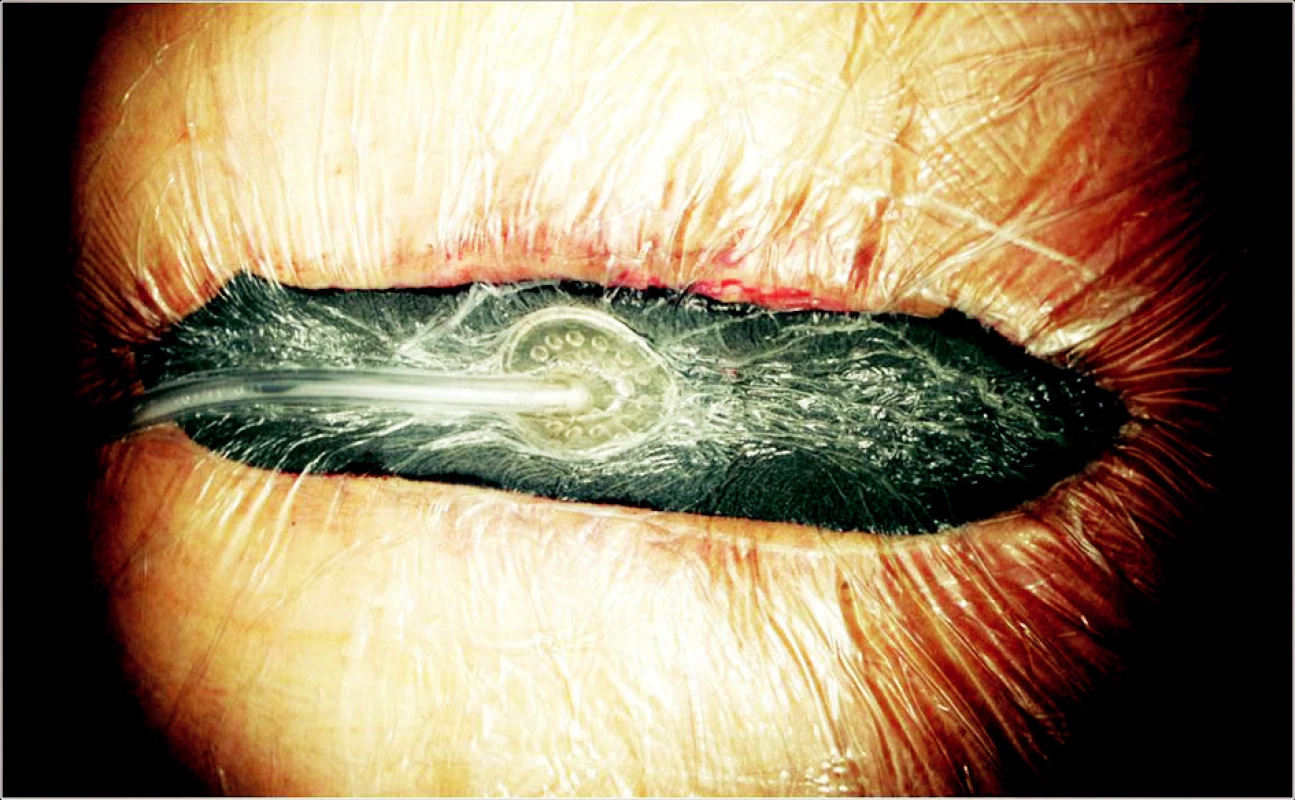
Image 4. Nemocný s hlubokou sternální infekcí během VAC terapie Fig. 4. The patient with deep sternal infection on the VAC therapy 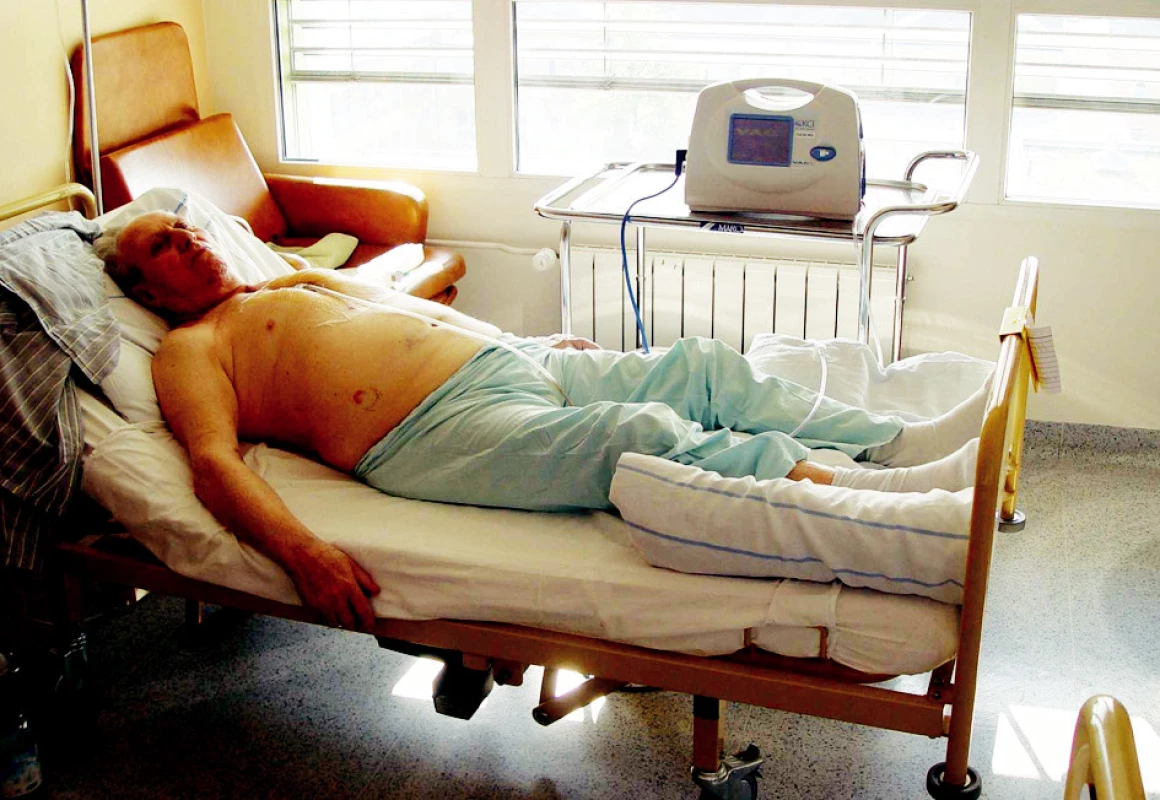
Image 5. Výsledný stav podtlakové terapie Fig. 5. Deep sternal infection. The result of the VAC therapy 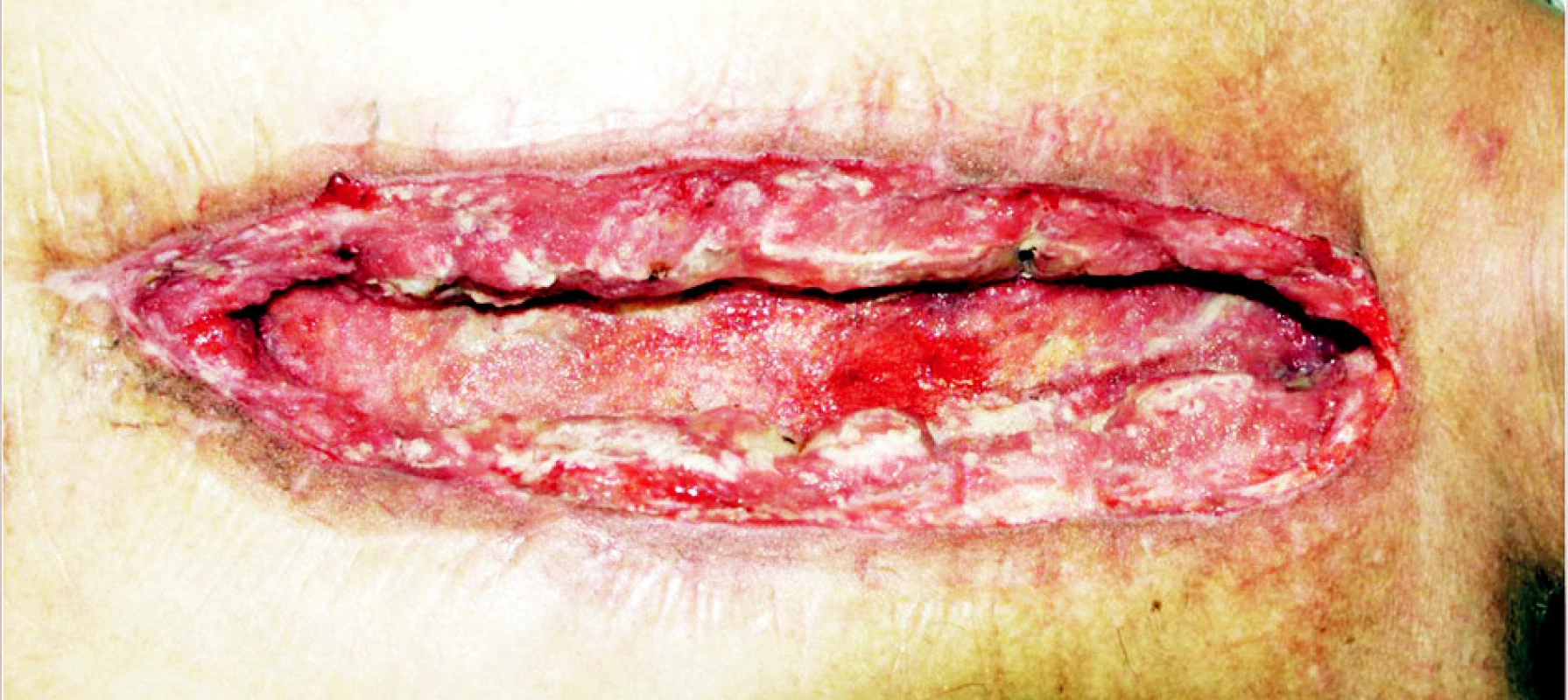
Image 6. Stav po rekonstrukci hrudní stěny oboustranným posunem pektorálních svalů Fig. 6. The result after the chest reconstruction by bilateral advancement pectoral flap 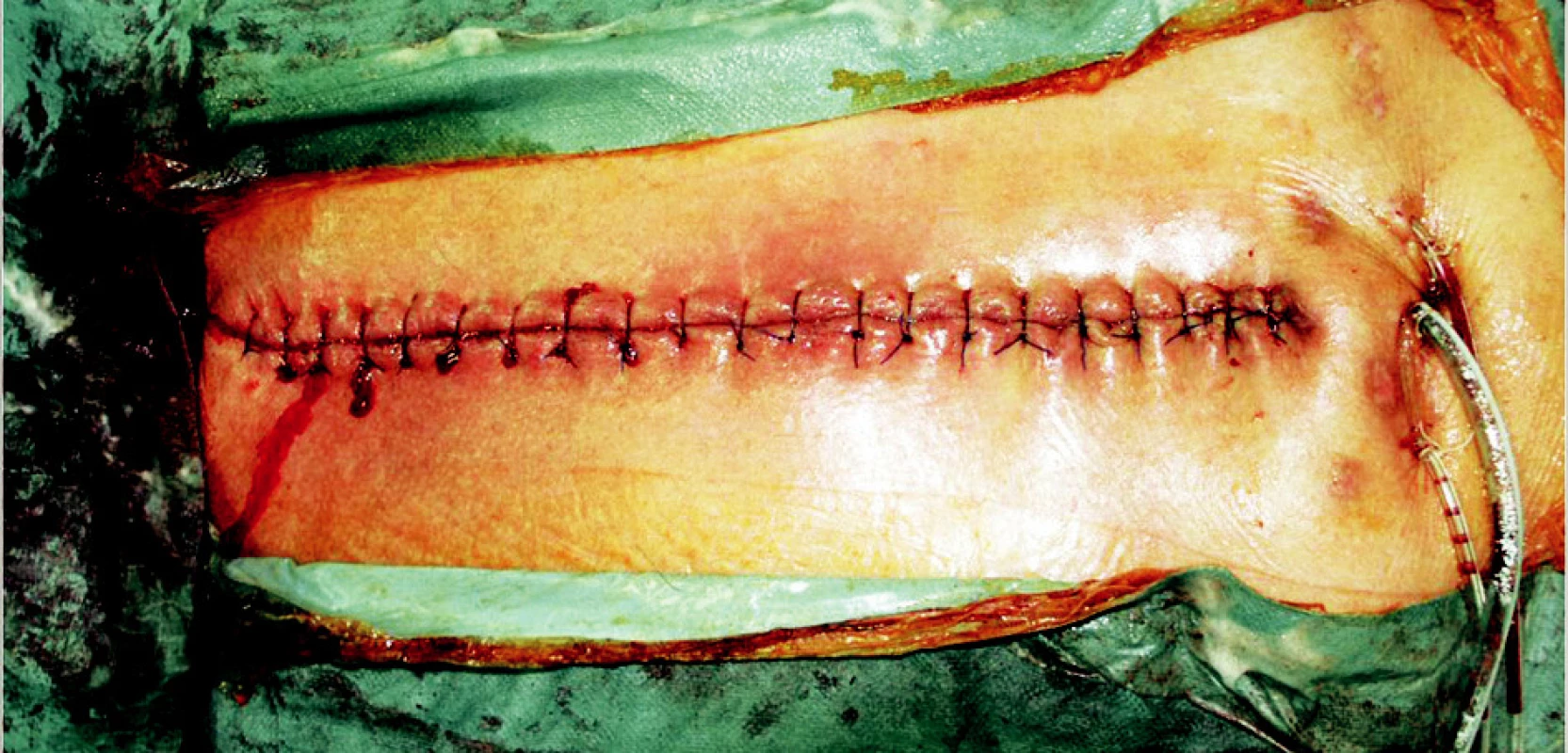
VÝSLEDKY
U 38 nemocných (95 %) došlo ke zhojení rány, 2 nemocní v souboru (5 %) léčení pro hlubokou sternální infekci zemřeli. Jedna nemocná zemřela 24. pooperační den na podkladě rozvinutého multiorgánového selhání. Druhá nemocná zemřela na krvácení z pravé srdeční komory po primární revizi pro hluboký sternální infekt. Průměrná hospitalizační doba v souboru nemocných dosáhla 36,4 ± 22,6 dnů, průměrná doba aplikace VAC systému byla 9,7 ± 3,9 dnů a průměrně bylo provedeno 4,6 ± 1,8 převazů (výměn systému) v rámci jedné léčby. U všech nemocných byl VAC systém použit jako příprava k sekundárnímu uzávěru rány.
U nemocných léčených pro rozsáhlé ranné infekční komplikace na dolních končetinách byla provedena sekundární sutura reziduálního defektu. Následné hojení nebylo komplikováno. Ve skupině 10 nemocných s povrchovou sternální infekcí byla u poloviny nemocných provedena sekundární sutura, u druhé poloviny byl defektu uzavřen cestou fasciokutánního či myokutanního posunu. U 1 nemocného došlo následně k dehiscenci v dolním pólu sternotomie, která byla řešena sekundární suturou. U 25 nemocných (96 %) léčených pro hlubokou sternální infekci byla provedena kompletní či částečná osteosyntéza sternálních okrajů v závislosti na ztrátě kostní hmoty, u 1 nemocné (4 %) nebylo možno osteosyntézu provést pro ztrátu hrudní kosti v celém rozsahu. Reziduální defekt měkkých tkání byl u všech těchto nemocných kryt oboustranným myokutánním posunem velkých pektorálních svalů. Podobně jako u předchozí skupiny nemocných došlo u 1 nemocné k dehiscenci v dolním pólu sternotomie, dále u 1 nemocného bylo nutno opakovaně punktovat serom z prostoru po mobilizaci pektorálních svalů. Celkem 4 nemocní, 1 ze skupiny povrchové sternální infekce a 3 ze skupiny hluboké sternální infekce, byli rehospitalizováni s odstupem 1 až 12 měsíců pro píštěle vázané na kovový materiál v hrudní kosti (drátěné kličky). Nemocní byli léčeni extrakcí kovového materiálu. Z kultivačních nálezů dominovaly stafylokokové infekce, u jedné nemocné byl prokázán metycilin-rezistentní kmen stafylokoka (MRSA). Terapeutický tlak 100–125 mm Hg byl nemocnými dobře tolerován a efektivně stabilizoval hrudní stěnu i u nemocných s hlubokým sternálním infektem. Během léčby nebyly zaznamenány žádné technické problémy s generátorem podtlaku.
DISKUSE
Podtlaková terapie si našla poměrně rychle svoje místo v léčbě akutních i chronických ran v celém spektru chirurgických oborů. Její hlavní doménou se dnes staly rozsáhlé ranné komplikace a defekty po výkonech v břišní dutině, komplikace po traumatologických a ortopedických výkonech. Dále si VAC terapie našla i široké využití v popáleninové medicíně [8, 9, 10]. Systém umožňuje kombinovat výhody otevřené léčby, kdy je možno opakovaně provádět ranný debridement, a výhody léčby zavřené, doplněné o neomezeně vysokou drenážní schopnost systému. Prostá lokální aplikace podtlaku přímo v ráně vede ke snížení tkáňového otoku a bakteriálního osídlení, navíc dochází i k arteriolární vazodilaci v bezprostředním okolí rány. Výsledkem je aktivní podpora tvorby granulační tkáně a akcelerace celého procesu hojení [8, 9, 10]. Navíc polyuretanová pěna komprimovaná podtlakem mechanicky stabilizuje ránu a postupně redukuje její velikost [10, 11, 15].
V kardiochirurgii představuje VAC terapie především velmi slibnou léčebnou strategii léčby hluboké sternální infekce. Časný chirurgický debridement následovaný aplikací VAC systému přináší významně lepší výsledky ve srovnání s konvenční terapii založené na zavřené kontinuální laváži či otevřeném hojení [11, 14, 15, 16, 17]. Ve skupině nemocných léčených VAC systémem bylo dosaženo efektivnější bakteriální sanace rány, bylo docíleno rychlejšího poklesu zánětlivých markérů a byla rovněž významně zkrácena celková délka hospitalizace [18, 19]. Aplikace VAC systému vedla navíc k významné redukci nejen krátkodobé, ale i dlouhodobé mortality nemocných a nutnost reintervence pro reziduální infekt [20]. VAC terapie je nejčastěji používána jako nástroj sanace rány či její přípravy k následnému uzávěru [21, 22]. Rozsah následné rekonstrukce se odvíjí od velikosti reziduálního defektu, zkušenosti a preference pracoviště ve volbě lalokového posunu. Nejčastěji jsou požívány m. pectoralis major, m. latissmus dorsi a m. rectus abdominis [14, 16, 21, 22]. Načasování rekonstrukce reziduálního defektu, nejen tradičně na podkladě negativity kultivačních vyšetření a příznivému lokálnímu nálezu, ale i na podkladě poklesu hodnoty CRP (< 30–50 mmol/l), jsou spojena s nižší morbiditou nemocných a zkrácením doby léčby [8, 23]. Na druhou stranu lze použít VAC terapii jako definitivní terapii. Tento přístup se jeví být výhodný především pro vysoce rizikové nemocné, protože nevyžaduje následnou rekonstrukci reziduálního defektu [14]. Nicméně tento přístup je spojen s významným prodloužení délky aplikace systému a tím i nárůstem ceny léčby [8, 14].
ZÁVĚR
Autoři prezentují svoji zkušenost s aplikací podtlakové terapie v léčbě raných infekčních komplikací po kardiochirurgických výkonech. Předkládaná kohorta nemocných není homogenní a spíše prezentuje průřez zkušeností s podtlakovou terapií, která byla nejdříve použita u ranných komplikací po odběru vena safena magna a pro léčbu povrchové sternální infekce. Později se doménou VAC terapie stala léčba hluboké sternální infekce, nejdříve jako záchranná terapie po selhání léčby zavřenou laváži a posléze jako léčebná strategie první volby. Společně s VAC terapií byl zaveden i agresivnější přístup u všech nemocných s hlubokou infekcí sternotomie, zahrnující velmi časný chirurgický debridement, spojený s kompletním odstraněním kovového materiálu. Navazující VAC terapie byla vždy použita jako nástroj sanace a přípravy rány k jejímu uzávěru. Při rekonstrukci byla provedena stabilizace sternálních okrajů drátěnými kličkami či minidlahami a myokutánní posun pektorálních svalů k docílení stabilizace hrudního koše a uzávěru defektu bez tahu. Tento přístup, doplněný o zavedení protokolu striktní korekce hyperglykemie, vedl k významnému snížení mortality hluboké sternální infekce na našem pracovišti. V období od II/2002 do X/2004 byla hospitalizační mortalita 22 %, po zavedení tohoto protokolu od XI/2004 poklesla hospitalizační mortalita hluboké sternální infekce na 7 % [24]. U všech našich nemocných byl navíc přítomen minimálně jeden rizikový faktor rozvoje sternálního infektu. Nicméně tento přístup je zatížen určitým rizikem pozdních komplikací (píštěle vázané na kovový materiál) zvyšujících morbiditu nemocných. Tímto problémem bude nutno se dále zabývat.
MUDr. M. Šimek
Kardiochirurgická klinika FN a UP
I. P. Pavlova 6
775 20 Olomouc
e-mail: martin.simek@c-mail.cz
Sources
1. Kolh, P., Kerzmann, A., Lahaye, L., Gerard, P., Limet, R. Cardiac surgery in octogenarians; peri-operative outcome and long-term results. Eur. Heart. J., roč. 2001, č. 14, s. 1235–1243.
2. Pritisanac, A., Gulbins, H., Rosendahl, U., Ennker, J. Outcome of heart surgery procedures in octogenarians: is age really not an issue? Expert. Rev. Cardiovasc. Ther., roč. 2007, č. 5, s. 243–250.
3. Engoren, M., Arslanian-Engoren, C., Steckel, D., et al. Cost, outcome, and functional status in octogenarians and septuagenarians after cardiac surgery. Chest, roč. 2002, č. 4, s. 1309–1315.
4. Ridderstolpe, L., Gill, H., Granfeldt, H., et al. Superficial and deep sternal wound complications: incidence, risk factor and mortality. Eur. J. Cardiothorac. Surg., roč. 2001, č. 20, s. 1168–1175.
5. Francel, T. J., Kouchoukos, N. T. A rational approach to wound difficulties after sternotomy: The problem. Ann. Thorac. Surg., roč 2001, č. 72, s. 1411–1418.
6. Finkelstein, R., Rabino, G., Mashiah, T., et al. Surgical site infection rates following cardiac surgery: The impact of a 6-year infection control program. Am. J. Infect. Control., roč. 2005, č. 33, s. 450–454.
7. Lepelletier, D., Perron, S., Bizouarn, P., et al. Surgical-site infection after cardiac surgery: incidence, microbiology, and risk factors. Infect. Control. Hosp. Epidemiol., roč. 2005, č. 26, s. 466–472.
8. Argenta, L. C., Morykwas, M. J. Vacuum-assisted closure. A new method for wound control and treatment: Clinical experience. Ann. Plast. Surg., roč. 1997, č. 38, s. 563–577.
9. Mendez-Eastman, S. Negative pressure wound therapy. Plast. Surg. Nurs., roč. 1998, č. 18, s. 27–29.
10. Sjoegren, J., Malmsjoe, M., Gustafsson, R., Ingemansson, R. Poststernotomy mediastinitis: a review of conventional surgical treatments, vacuum-assisted closure therapy and presentation of the Lund University Hospital mediastinitis algorithm. Eur. J. Cardiothoracic. Surg., roč. 2006, č. 30, s. 898–905.
11. Mangram, A. J., Horan, T. C., Pearson, M. L, et al. The hospital infection control practise advisory comittee. Guidelines for prevention of surgical site infection. Infect. Control. Hosp. Epidemiol., roč. 2005, č. 20, s. 247–278.
12. El Oakley, R., Wright, J. Postoperative mediastinitis: Classification and management. Ann. Thorac. Surg., roč 1996, č. 61 s. 1030–1036.
13. Cowan, K. N., Teague, L., Sue, S. C.,et al. Vaccum-assisted wound closure of deep sternal infection in high-risk patients after cardiac surgery. Ann. Thorac. Surg., roč 2005, č. 80, č. 2205–2212.
14. Fleck, T. M., Fleck, M., Moidl, R., et al. The vaccum-assisted closure system for the treatment of deep sternal wound infection after cardiac surgery. Ann. Thorac. Surg., roč. 2002, č. 74, s. 1596–1600.
15. Kirsch, M., Mekontso-Dessap, A., Houel, R., et al. Closed drainage using redon catheters for poststernotomy mediastinitis: Results and risk factors for adverse outcome Ann. Thorac. Surg., roč. 2001, č. 71, s. 1580–1586.
16. Fuchs, U., Zittermann, A., Stuetten, B., et al. Clinical outcome of patients with deep sternal infection managed by vaccum-assisted closure compared to conventional therapy with open packing: A retrospective analysis. Ann. Thorac. Surg., roč. 2005, č. 79, s. 526–531.
17. Sjoegren, J., Gustafsson, R., Nilsson, J., et al. Clinical outcome after poststernotomy mediastinitis: Vaccum-assisted closure versus conventional treatment. Ann. Thorac. Surg., roč 2005, č. 79, s. 2049–2055.
18. Doss, M., Martens, S., Wood, J. P., et al. Vaccum-asisted suction drainage versus conventional treatment in the management of poststernotomy osteomyelitis. Eur. J Cardiothorac. Surg., roč. 2002, č. 22, s. 934–938.
19. Sjoegren, J., Gustafsson, R., Nilsson, J., et al. The impact of Vacuum-assisted closure on long term survival after post-sternotomy mediastinitis. Ann. Thorac. Surg., roč. 2005, č. 80, s. 1270–1275.
20. Scholl, L,. Chang, E., Reitz, B., et al. Sternal osteomyelitis: use of vaccum-assisted closure device as an adjunct to definitive closure with sternectomy and muscle flap reconstruction. J. Card. Surg., roč. 2004, č. 19, s. 453–461.
21. Ascherman, J. A., Patel, S. M, Malhotra, S. M, Smith, C. R. Management of sternal wounds with bilateral pectoralis major myocutaneous advancement flaps in 114 consecutively treated patients: Refinements in technique and outcomes analysis. Plast. Reconstr. Surg., roč. 2004, č. 114, s. 676–683.
22. Kletenský, J., Paděra, J. Defect of sternal area. Acta chirurgiae plasticae, roč. 2006, č.1, s. 5–9.
23. Gustafsson, R. I., Johnsson, P., Algotsson, L., et al. Vaccum-assisted closure therapy quided by C-reactive protein level in patients with deep sternal wound infection. J. Thorac. Cardiovasc. Surg., roč. 2002, č. 123, s. 895–900.
24. Gustafsson, R. I., Sjoegren, J., Ingemansson, R. Deep sternal wound infection: a sternal-sparing technique with vacuum-asisted closure therapy. Ann. Thorac. Surg., roč. 2003, č. 76, s. 2048–2053.
25. Šimek, M., Němec, P., Zálešák, B., Hájek, R. Vacuum-assisted closure v léčbě hlubokého sternálního infektu. II. sjezd České společnosti kardiovaskulární chirurgie, Brno 2006. Sborník přednášek, s. 72.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2007 Issue 8-
All articles in this issue
- Diagnostické a léčebné postupy u torakoabdominálních poranění – současný stav
- Podtlaková terapie (vacuum-assisted closure) v léčbě ranných infekčních komplikací po kardiochirurgických výkonech
- Naše první zkušenost s rigidní fixací sterna
- Aproximační střevní anastomóza při multifokální nekrotizující enterokolitidě u novorozence
- Komplikace laparoskopické operace tříselné kýly diagnostikované kolonoskopicky
- Demografická a epidemiologická studie pacientů s poraněním pánve
- 10 let zkušeností s Barronovou ligaturou na chirurgické klinice Ostrava
- Radikální resekce u nemocných s karcinomem hlavy pankreatu. Retrospektivní analýza přežívání u souboru 307 nemocných
- Videotorakoskopie, standardní a méně časté indikace
- Laparoskopická cholecystektómia v ambulantnej chirurgii
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Komplikace laparoskopické operace tříselné kýly diagnostikované kolonoskopicky
- 10 let zkušeností s Barronovou ligaturou na chirurgické klinice Ostrava
- Videotorakoskopie, standardní a méně časté indikace
- Podtlaková terapie (vacuum-assisted closure) v léčbě ranných infekčních komplikací po kardiochirurgických výkonech
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

