-
Medical journals
- Career
Vyšetření sympatické inervace myokardu v diferenciální diagnostice parkinsonismu
Authors: O. Lang 1,2,3; D. Šuhajová Do 2; M. Bejtic 2; V. Kamírová 2; M. Lang 2
Authors‘ workplace: Kardiologická klinika, 3. LF UK Praha 1; Institut nukleární medicíny, PMCD s. r. o., Praha 2; Oddělení nukleární medicíny, ON Příbram, ČR 3
Published in: NuklMed 2026;15:5-9
Category: Review Article
Overview
Vyšetření sympatické inervace myokardu se provádí u pacientů se srdečním selháním, s ICHS a u kardiomyopatií. Jako indikátor se používá 123I-MIBG (meta-jodo-benzyl-guanidin). Je to analog adrenergního blokátoru guanetidinu, má stejnou chemickou strukturu jako noradrenalin. Představuje ideální prostředek pro hodnocení funkce postganglionického presynaptického sympatického nervového systému v myokardu.
Existuje řada neurodegenerativních poruch, které jsou způsobené akumulací bílkovin v neuronech, hovoříme proto o proteinopatiích. Obvykle se rozlišují dva typy, tauopatie a alfa-synukleinopatie. Oba typy vedou k neurodegeneraci a k poruše neuronového přenosu. Postižení nigrostriatálního systému v mozku se klinicky projeví jako parkinsonismus, postižení srdečního sympatiku se může projevit zvýšeným sklonem k arytmiím a náhlé smrti. Parkinsonský syndrom zahrnuje řadu klinických potíží, jako je třes, bradykineze, potíže s rovnováhou a chůzí, rigiditu a kognitivní poruchy. Tyto příznaky se mohou vyskytovat jak u Parkinsonovy nemoci, tak u řady parkinsonských syndromů a u různých typů demence. Některé však mají jinou příčinu, než je neurodegenerace. Jejich odlišení, které je důležité z hlediska racionální léčby, je obtížné klinicky a neodliší je ani použití MRI.
Metody nukleární medicíny mají prostředky jak pro detekci neurodegenerace striata, tak myokardu. Pro detekci striatální poruchy se používá 123I-joflupan (DaTSCAN), pro myokard výše zmíněný 123I-MIBG. Má-li pacient s parkinsonským syndromem poruchu inervace striata, ale normální inervaci myokardu, nejedná se o Parkinsonovu chorobu, ale o jiný typ parkinsonismu. Má-li ale současně poruchu inervace striata i myokardu, jedná se o Parkinsonovu chorobu.
Scintigrafické metody je možné použít v diagnostice různých neurodegenerativních poruch nejen myokardu, ale také mozku. Přitom kombinace obou metod umožňuje poměrně přesně určit správnou diagnózu ve více než 90 % případů klinického parkinsonismu.
Klíčová slova:
diferenciální diagnóza – neurodegenerace – MIBG – DaTSCAN – parkinsonismus
Úvod
123I-MIBG (metajodobenzylguanidin) je důležité radiofarmakum používané pro diagnostické účely v kardiologii, onkologii a neurologii. 1 V kardiologii se 123I-MIBG používá pro hodnocení sympatické inervace myokardu zejména u pacientů se srdečním selháním, kde poskytuje prognostické informace. V onkologii slouží zejména pro detekci neuroendokrinních nádorů vycházejících z adrenergní tkáně, jako je neuroblastom a feochromocytom. V neurologii pak je schopen přispět k diferenciální diagnostice parkinsonismů a demencí díky své schopnosti detekovat postganglionickou presynaptickou sympatickou dysfunkci.
Od svého zavedení do klinické praxe se scintigrafie s 123I-MIBG ukázala jako vysoce reprodukovatelná a spolehlivá metoda pro hodnocení globální i regionální sympatické inervace myokardu. 2 Sympatická inervace myokardu při zvýšené aktivitě zvyšuje srdeční frekvenci (pozitivně chronotropní efekt) a zvyšuje kontraktilitu myokardu (pozitivně inotropní efekt). Přenašečem signálu je noradrenalin, je skladován ve vezikulách presynaptických nervových zakončení. Exocytózou je uvolňován do synaptické štěrbiny, většina (70–90 %) je ho pak zpětně vychytána, takže jen malé množství je použito pro stimulaci postsynaptických beta receptorů myocytů.
U chronického srdečního selhání je aktivita sympatiku zvýšená jednak zvýšeným uvolňováním noradrenalinu do synaptické štěrbiny, jednak snížením jeho zpětného vychytávání. Díky tomu je zpočátku kontraktilní porucha funkce myokardu kompenzovaná, při dlouhém trvání však dochází ke snížení citlivosti postsynaptických beta receptorů. To má za následek remodelaci levé komory srdeční s dalším poklesem ejekční frakce a se zvýšením morbidity i mortality. 3
V posledních letech se scintigrafie s 123I-MIBG uplatňuje také u neurologických poruch. Důvodem je schopnost této metody detekovat dysfunkci autonomního nervového systému, zejména sympatiku. To se uplatňuje v diagnostice a zejména diferenciální diagnostice poruch hybnosti, ale také demencí. 1
Parkinsonismus
Parkinsonismus nebo parkinsonský syndrom zahrnuje množství různých klinických jednotek, které mají společnou symptomatologii způsobenou postižením bazálních ganglií, především nigrostriatálního systému. 4–6 Jedná se spíše o klinickou, nikoli etiologickou jednotku. K základním klinickým příznakům patří zejména klidový třes, rigidita, bradykineze a postižení posturálních reflexů. Klasifikace je různá, obvykle se parkinsonismy dělí na 3 skupiny:
- primární degenerativní parkinsonismy [Parkinsonova choroba (PD – někdy se vyděluje jako 4. skupina), progresivní supranukleární obrna (PSP), multisystémová atrofie (MSA), kortikobasální degenerace (CBD), parkinsonská demence (PDD) a demence s Lewyho tělísky (LBD)],
- sekundární nedegenerativní parkinsonismy [polékové, infekční, toxické, metabolické (např. hyperthyreóza), při tumoru, hydrocefalu apod.],
- dědičné neurodegenerativní choroby (Huntington, Wilson a další).
Z hlediska etiopatogeneze můžeme parkinsonismy rozdělit na degenerativní a nedegenerativní.
Společným patogenetickým mechanismem degenerativních poruch je abnormální intracelulární hromadění normálních, ale nedegradovaných bílkovin ve specifických populacích neuronů a gliových buněk, hovoříme o proteinopatiích. 7,8 Patologické změny u proteinopatií závisejí na typu hromaděných bílkovin a na anatomické lokalizaci jejich hromaděni. 6,7
Tauopatie se vyznačují hromaděním fosforylovaných agregovaných tau bílkovin s vazbou na mikrotubuly vytvářejících neurofibrilární propletenec. Hromadí se jak v neuronech, tak v gliových buňkách. Klinicky sem patří Alzheimerova demence (AD), frontotemporální demence (FTD), Pickova choroba, PSP a CBD.
Alfa-synukleinopatie se vyznačují neuronální přítomností Lewyho tělísek, která jsou tvořena agregáty fosforylovaných alfa-synukleinových presynaptických bílkovin. Jedná se o multifokální proces, který postihuje selektivně některé neurony centrálního a periferního autonomního nervového systému. Klinicky sem patří PD (hromadění v neuronech), PDD, LBD a MSA (hromadění v gliových buňkách).
Oba typy postižení se však mohou kombinovat. V důsledku toho je klinická diferenciální diagnostika neřešitelný problém zejména v časných stadiích onemocnění. Rozhodování o vhodné léčbě je tedy obtížné.
K nedegenerativním parkinsonismům patří např. vaskulární parkinsonismus, otrava manganem, parkinsonismus při antipsychotické léčbě a parkinsonismus jako následek prodělané encefalitidy.
Mezi nejčastější degenerativní parkinsonismy patří PD, MSA a PSP.
Nejčastější nedegenerativní parkinsonismus je vaskulární parkinsonismus, jehož příčinou jsou cévní mozkové příhody ischemické i krvácivé. 7
Scintigrafické metody pro hodnocení neurotransmise
Metody nukleární medicíny umožňují detekci různých biomarkerů in vivo u různých postižení mozku. Jedná se zejména o možnost hodnocení neurotransmise (zejména nigrostriatální dopaminergní systém), metabolické aktivity a přítomnosti abnormálních bílkovin. Představují tak užitečný nástroj pro diagnostiku těchto poruch v časných stadiích včetně rozlišení různých parkinsonských syndromů. Vzhledem k zaměření této práce se budeme věnovat pouze hodnocení neurotransmise.
Degenerace dopaminergních neuronů v substancia nigra s následnou redukcí produkce dopaminu je patofyziologickým podkladem mnohých parkinsonských příznaků. Řada samoregulačních mechanismů produkce dopaminu (inhibice tyrosin hydroxylázy, uvolňování dopaminu do synaptické štěrbiny a hustota postsynaptických receptorů) vede k tomu, že klinické příznaky se projeví až při výrazné ztrátě dopaminergních neuronů (60–70 %). 9 Radiofarmaka, která máme k dispozici pro hodnocení funkční integrity dopaminergního systému, můžeme rozdělit na dvě skupiny:
- presynaptické dopaminové transportéry (DaT),
- dopaminové D2 receptory.
DaT regulují zpětné vychytávání dopaminu ze synaptické štěrbiny a jsou hodnoceny pomocí indikátorů odvozených od kokainu (např. ioflupan). D2 receptory mohou být hodnoceny indikátory odvozenými od benzamidu (např. IBZM).
Nejdostupnější a nejvíce v praxi používané radiofarmakum pro hodnocení DaT je 123I-ioflupan. Jedná se o kokainový analog a má řadu vlastností, které ho činí ideálním. Jedná se zejména o vysokou afinitu k presynaptickým transportérům, vysokou specificitu pro dopaminové transportéry ve srovnání se serotoninovými transportéry, poměrně rychlé dosažení ekvilibria po i. v. podání (3 až 6 hodin) a absenci závažných nežádoucích účinků. 10
Klinické použití
Klinické použití kombinace scintigrafických metod s radiofarmaky MIBG a ioflupan v diagnostice parkinsonismů a demencí vychází z patofyziologických změn těchto chorob a z vlastností obou radiofarmak. Vzhledem k zaměření této práce se budeme věnovat pouze použití u parkinsonismů.
Nejčastější klinicky významné choroby způsobené neurodegenerací nigrostriatálního systému jsou Parkinsonova choroba, progresivní supranukleární obrna a multisystémová atrofie. 7 PSP a MSA jsou také někdy označovány jako parkinson plus poruchy, protože se projevují dalšími příznaky, které nejsou jasně spojené s parkinsonismem. U PSP je to např. porucha hybnosti očí a demence, u MSA nystagmus a ataxie. Je to známkou toho, že degenerativní změny postihují nejen dopaminergní neurony, ale také jiné části mozku včetně mozečku.
U všech těchto postižení detekujeme poruchu nigrostriatálního systému (neurodegeneraci), a tedy patologický nález na scintigrafii pomocí 123I-ioflupanu. (Obr. 1) Pokud je ale scintigrafický nález normální (Obr. 2), můžeme přítomnost neurodegenerace s vysokou přesností vyloučit. Pro odlišení degenerativních a nedegenerativních parkinsonismů se udává senzitivita v rozmezí 87–98 % a specificita 80–100 %. 6,11,12 V klinické praxi můžeme tedy díky samotné scintigrafii s 123I-ioflupanem odlišit s vysokou přesností nedegenerativní parkinsonismy, jako je esenciální třes a vaskulární a lékový parkinsonismus.
Image 1. Patologicky snížená akumulace 123I-ioflupanu ve striatu svědčí pro neurodegeneraci. 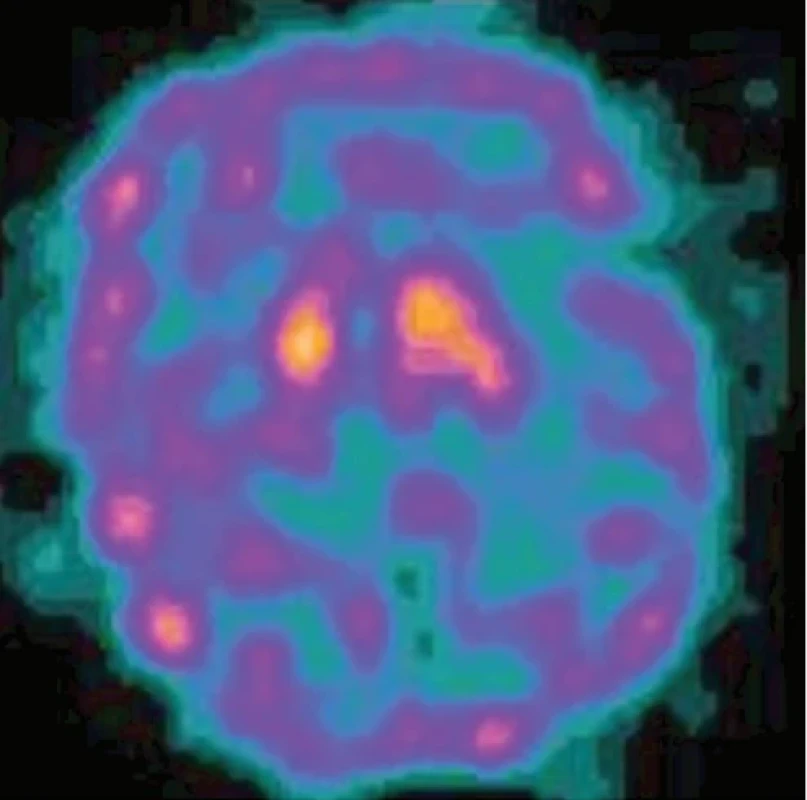
Image 2. Fyziologická akumulace 123I-ioflupanu ve striatu prakticky vylučuje neurodegenerativní změny. 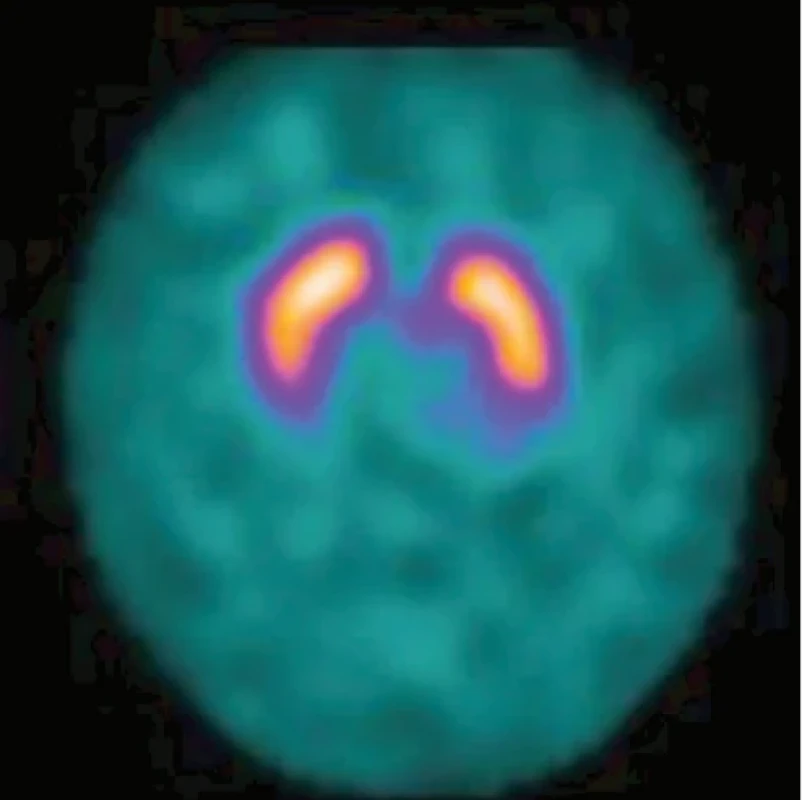
Pozitivní scintigrafický nález však vzhledem k výše zmíněnému neumožňuje odlišit PD od MSA a PSP. V tomto ohledu je nutné vycházet z faktu, že PD je spojena také s poruchou autonomního nervového systému. 1,12 Postižení sympatiku myokardu se klinicky může projevit jako posturální hypotenze nebo ztráta variability srdečního rytmu, scintigraficky ho můžeme prokázat pomocí 123I-MIBG. U PD, na rozdíl od PSP a MSA, je akumulace 123I-MIBG v myokardu výrazně redukovaná, což ukazuje na ztrátu nervových zakončení sympatiku.
Aby však situace nebyla tak jednoduchá, pozitivní nález na scintigrafii s 123I-ioflupanem může být také v některých případech vaskulárního, tedy nedegenerativního parkinsonismu, pokud je cévní léze lokalizovaná do oblasti basálních ganglií. 6 Příčinou je pravděpodobně nemožnost dosažení vazebných míst radiofarmakem v důsledku poruchy cévního zásobení. Ve správné diagnóze může pomoci klinická symptomatologie (příznaky cévního onemocnění mozku, jako je tranzitorní ischemická ataka nebo cévní mozková příhoda v anamnéze) nebo MRI mozku (nález ischemických lézí), nejsou však specifické.
Scintigrafické charakteristiky
Scintigrafické obrazy mohou být hodnoceny vizuálně kvalitativně nebo semikvantitativně pomocí různých softwarů (SW). Některé z těchto SW umožňují porovnat dosažený výsledek vyšetření s normálovou databází. Základní výhodou SW analýzy je nižší variabilita mezi hodnotiteli i při opakovaném hodnocení jedním hodnotitelem a také lepší reprodukovatelnost výsledků. To vede k redukci falešně pozitivních nálezů. Semikvantitativní softwarová analýza by se měla užívat především tam, kde není vizuální hodnocení jednoznačné. K velkému rozvoji užívání SW analýzy vedla především dostupnost komerčních programů. Jsou dodávané všemi výrobci a dodavateli SW vybavení.
Programy pro hodnocení dopaminergního systému využívají automatické označení oblastí zájmu (ROI) s výpočtem specifického vazebného poměru (SBR) ioflupanu v nucleus caudatus a v putamen vůči pozadí. 6,13 Také je možné získat další parametry, jako je symetrie mezi levým a pravým striatem a poměr akumulace mezi nucleus caudatus a putamen. Těmito metodami byla zjištěna závislost vazebné kapacity na věku a pohlaví, nikoli však na body mass indexu, pravo-levorukosti či cirkadiánním a sezónním rytmu. Literární data v tomto směru jsou však kontroverzní.
Dalším problémem je stanovení hranice akumulace 123I-ioflupanu ve striatu, aby bylo možné rozlišit mezi normální a patologickou vazbou, obvykle se uvádí hranice 3,3. 14 V tomto směru se využívají také některé metody umělé inteligence (AI), např. konvoluční neuronové sítě (CNN). 15 Pomocí těchto metod je možné odlišit úbytek dopaminergní inervace s vysokou senzitivitou i specificitou kolem 90 %. Přitom se zdá, že nejlepším diskriminátorem pro detekci PD je akumulace 123I-ioflupanu v oblasti putamen. 16
Pro správnou interpretaci nálezů při vyšetření 123I-MIBG je důležitá standardizace vyšetřovacích protokolů, příprava pacienta a zpracování obrazů. 1,14,17 Pacienti by před vyšetřením měli vysadit léky ovlivňující vychytávání 123I-MIBG, jako jsou tricyklická antidepresiva, antipsychotika, blokátory kalciových kanálů a sympatomimetika. Snímání planárních obrazů je třeba načasovat za 15–30 minut a za 3–4 hodiny po podání radiofarmaka. Jako normální nález hodnotíme homogenní akumulaci v myokardu, jako patologický nález akumulaci nehomogenní nebo žádnou. Pro semikvantitativní hodnocení se používá výpočet poměru akumulované radioaktivity v myokardu vůči mediastinu (heart-to-mediastinum ratio, H/M ratio) na časných i pozdních obrazech. Za hraniční hodnotu je považován poměr 1,56; tento poměr má stejnou hodnotu bez ohledu na to, zda je počítán z časných nebo pozdních obrazů 14, i když to někteří zpochybňují. Podle jejich výsledků má lepší diferenciálně diagnostické parametry H/M ratio počítané za 4 hodiny po aplikaci radiofarmaka, udávají však jiné hraniční hodnoty (1,72 pro časné a 1,63 pro pozdní obrazy). 18
Závěr
Kombinace obou scintigrafických metod posouzení inervace striata i myokardu umožňuje poměrně přesně určit správnou diagnózu ve více než 90 % případů klinického parkinsonismu.
Normální nález na scintigrafii s 123Iioflupanem u pacientů s klinickým parkinsonským syndromem znamená, že se jedná o nedegenerativní onemocnění, tedy nejčastěji esenciální tremor nebo lékový parkinsonismus.
Mohou však také nastat případy, kdy scintigrafie s 123I-ioflupanem je normální, ale je přítomná porucha inervace myokardu. Tito pacienti by měli být pečlivě sledováni, protože porucha inervace myokardu může předcházet poruchu inervace nigrostriatálního systému v časných stadiích PD. 6
Pro PD je typický pozitivní nález jak na scintigrafii s 123I-ioflupanem, tak na scintigrafii s 123I-MIBG (Obr. 3), zatímco u PSP a MSA je pozitivní nález pouze na scintigrafi i s 123I-ioflupanem, ale nález na scintigrafii s 123I-MIBG je normální. (Obr. 4)
Image 3. Patologicky snížená akumulace 123I-MIBG v myokardu. 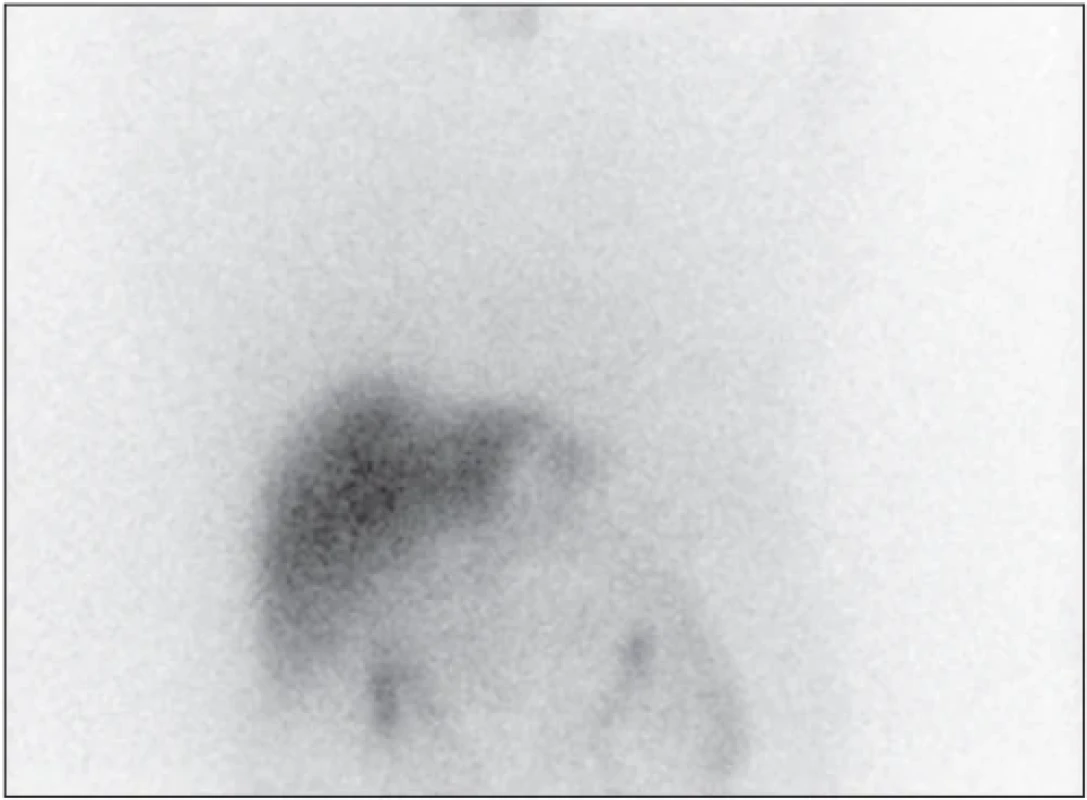
Image 4. Fyziologická akumulace 123I-MIBG v myokardu. 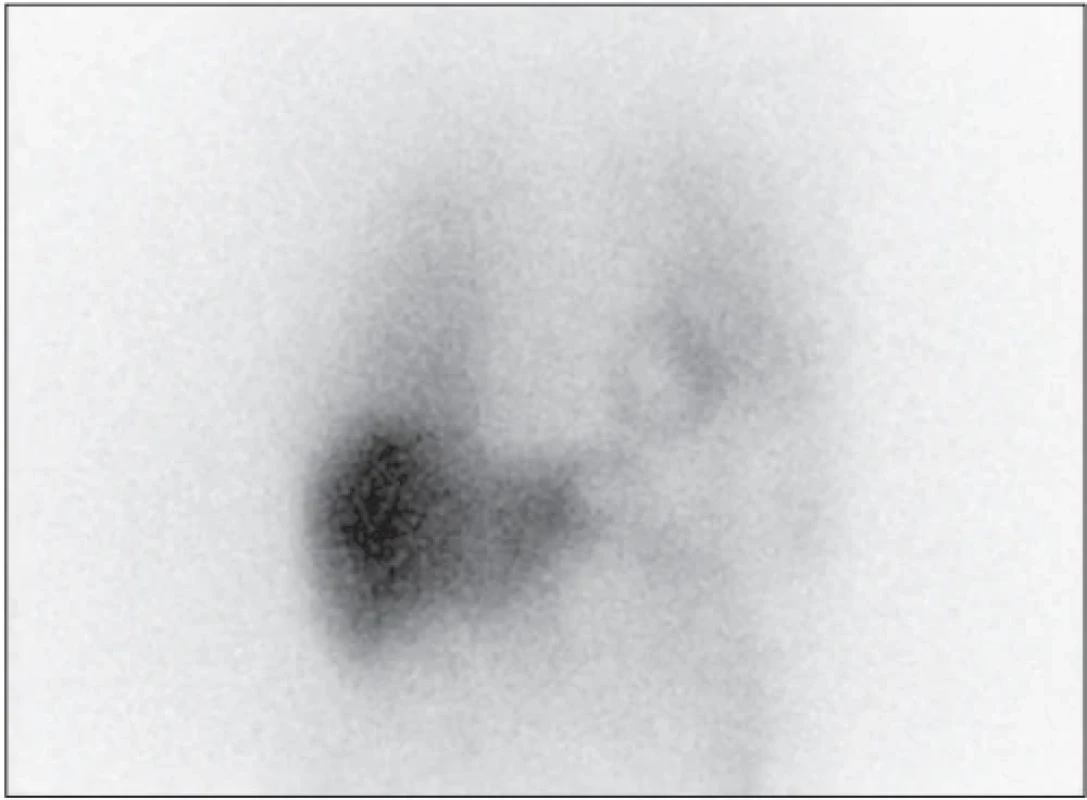
Zvláštním případem mohou být některé vaskulární, tedy nedegenerativní parkinsonismy. Ty také mohou mít patologický nález na scintigrafii s 123I-ioflupanem a normální nález na scintigrafii s 123I-MIBG, mívají však symptomatologii cévního onemocnění mozku. Rovněž mohou mít detekovány ischemické změny na MR mozku, ty jsou však velmi nespecifické (mohou být přítomné i u PD a u klinicky zdravých seniorů s kardiovaskulárním postižením nebo hypertenzí).
Obrazová dokumentace – archiv autorů.
Sources
1. Chang MC, Peng CL, Chen CT, et al. Iodine-123 Metaiodobenzylguanidine (I-123 MIBG) in Clinical Applications: A Comprehensive Review. Pharmaceuticals (Basel).2024;17 : 1563. doi: 10.3390/ph17121563
2. Verschure DO, Nakajima K, Verberne HJ. Cardiac 123I-mIBG Imaging in Heart Failure. Pharmaceuticals (Basel). 2022 May 25;15(6):656. doi: 10.3390/ph15060656. PMID: 35745574; PMCID: PMC9230638
3. Bristow MR, Ginsburg R, Minobe W, et al. Decreased Catecholamine Sensitivity and β-Adrenergic-Receptor Density in Failing Human Hearts. N Engl J Med.1982; 307 : 205–211
4. Kaňovský P. Parkinsonské syndromy. Neurol. pro Praxi,2000; 1 : 23-27
5. Bareš M. Diagnostika a klinické příznaky Parkinsonovy nemoci. Neurol. pro Praxi,2001;1 : 22-24
6. Nuvoli S, Palumbo B, Malaspia S, et al. 123I-ioflupane SPET and 123I-MIBG in the diagnosis of Parkinson's disease and parkinsonian disorders and in the differential diagnosis between Alzheimer's and Lewy's bodies dementias. Hell J Nucl Med 2018; 21(1):60-68
7. Dickson DW. Parkinson's disease and parkinsonism: neuropathology. Cold Spring Harb Perspect Med. 2012 Aug 1;2(8):a009258. doi: 10.1101/cshperspect.a009258
8. Moussaud S, Jones DR, Moussaud-Lamodière EL, et al. Alpha-synuclein and tau: teammates in neurodegeneration? Mol Neurodegener. 2014 Oct 29;9 : 43. doi: 10.1186/1750-1326-9-43. PMID: 25352339; PMCID: PMC4230508
9. Kalia LV, Lang AE. Parkinson's disease. Lancet 2015;386 : 896–912. doi: 10.1016/S0140-6736(14)61393-3. Epub 2015 Apr 19. PMID: 25904081
10. Grosset DG, Tatsch K, Oertel WH, et al. Safety analysis of 10 clinical trials and for 13 years after first approval of ioflupane 123I injection (DaTscan). J Nucl Med 2014; 55 : 1281–1287. doi: 10.2967/jnumed.114.138032. Epub 2014 Jun 19. PMID: 24947061.
11. Suwijn SR, van Boheemen CJ, de Haan RJ, et al. The diagnostic accuracy of dopamine transporter SPECT imaging to detect nigrostriatal cell loss in patients with Parkinson's disease or clinically uncertain parkinsonism: a systematic review. EJNMMI Res. 2015;5 : 12. doi: 10.1186/s13550-015-0087-1. PMID: 25853018; PMCID: PMC4385258.
12. Pagano G, Niccolini F, Politis M. Imaging in Parkinson's disease. Clin Med (Lond). 2016;16 : 371-375. doi: 10.7861/clinmedicine.16-4-371. PMID: 27481384; PMCID: PMC6280219.
13. Morbelli, S., Esposito, G., Arbizu, J. et al. EANM practice guideline/SNMMI procedure standard for dopaminergic imaging in Parkinsonian syndromes 1.0. Eur J Nucl Med Mol Imaging 2020;47 : 1885–1912. https://doi.org/10.1007/s00259-020-04817-8.
14. Nuvoli S, Spanu A, Piras MR, et al. 123I-ioflupane brain SPECT and 123I-MIBG cardiac planar scintigraphy combined use in uncertain parkinsonian disorders. Medicine 2017;96 : 21(e6967).
15. Bejtic M, Kamírová V, Lang O, et al. Umělá inteligence v nukleární medicíně: historické milníky a principy. NuklMed 2025;14 : 60–64.
16. Palumbo B, Fravolini ML, Buresta T, et al. Diagnostic accuracy of Parkinson disease by support vector machine (SVM) analysis of 123I-FP-CIT brain SPECT data: implications of putaminal findings and age. Medicine (Baltimore) 2014;93:e228. doi: 10.1097/MD.0000000000000228. PMID: 25501084; PMCID: PMC4602813.
17. Flotats A, Carrió I, Agostini D, et al. Proposal for standardization of 123I-metaiodobenzylguanidine (MIBG) cardiac sympathetic imaging by the EANM Cardiovascular Committee and the European Council of Nuclear Cardiology. Eur J Nucl Med Mol Imaging 2010;37 : 1802–1812.
18. Xue T, Cui Y, Kan Y, et al. Value of multi parameter 123I MIBG scintigraphy in the differential diagnosis of Parkinson’s disease. EJNMMI Res. 2025;15 : 7. doi: 10.1186/s13550-025-01197-8. PMID: 39875667; PMCID: PMC11775374.
Labels
Nuclear medicine Radiodiagnostics Radiotherapy
Article was published inNuclear Medicine

2026 Issue 1-
All articles in this issue
- Dopis redakci
- Vyšetření sympatické inervace myokardu v diferenciální diagnostice parkinsonismu
- Význam anamnézy pro interpretaci PET/CT: osteitis fibrosa cystica
- Ze společnosti NM
- Vyhlášení voleb do orgánů organizační složky ČSNM ČLS JEP, z. s. (číslo OS 28) PRO ELEKTRONICKOU VOLBU
- Vyhlášení voleb do rady sekcí ČSNM ČLS JEP, z. s. (číslo OS 28) PRO ELEKTRONICKOU VOLBU
- Nuclear Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Dopis redakci
- Vyšetření sympatické inervace myokardu v diferenciální diagnostice parkinsonismu
- Význam anamnézy pro interpretaci PET/CT: osteitis fibrosa cystica
- Ze společnosti NM
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

