-
Medical journals
- Career
Přínos nukleární medicíny v diagnostice a terapii pacientky s peritoneální strumózou – kazuistika
Authors: D. Chroustová 1; K. Žabková 2; V. Ptáčník 1; L. Planičková 3; K. Táborská 4; P. Vlček 4
Authors‘ workplace: Ústav nukleární medicíny 1; 3. interní klinika 2; Ústav patologie 1. LF UK a VFN Praha 3; Klinika nukleární medicíny a endokrinologie, 2. LF UK a FN Motol Praha, ČR 4
Published in: NuklMed 2025;14:34-38
Category: Casuistry
Overview
Struma ovarii je vzácný nádor definovaný jako ovariální teratom. Většina metastatických struma ovarii se skládá z papilárního nebo folikulárního karcinomu. V našem sdělení prezentujeme ojedinělý případ pacientky se strumou ovarií a s peritoneální strumózou. 58letá žena sledovaná na endokrinologii se symptomatickou hypertyreózou nejasné etiologie, která přetrvávala i po totální tyreoidektomii. Po řadě zobrazovacích vyšetření a biopsii lymfatické uzliny byl prokázán dobře diferencovaný folikulární karcinom vzniklý v anamnesticky dodatečně zjištěné struma ovarií. Při celotělové scintigrafii pomocí 99mTc-techecistanu sodného byla detekována vícečetná ložiska v dutině břišní akumulující radiofarmakum, odpovídající tkáni štítné žlázy při podezření na strumózu ovarii. Pacientka podstoupila debulking s hysterektomií a bilaterální adnexektomií a s další exstirpací tumorózních ložisek v dutině břišní. Histologicky se jednalo o diseminaci dobře diferencované folikulární neoplasie s okrsky folikulární varianty papilárního karcinomu štítné žlázy. Byla provedena terapie 131I a následně diagnostická a poterapeutická scintigrafie pomocí 131I.
Klíčová slova:
peritoneální strumóza – 99mTc-TO4 SPECT/low dose CT – terapie a sledování pomocí 131I
Úvod
Struma ovarii s maligní transformací je vzácný ovariální tumor s výskytem přibližně okolo 5 % všech ovariálních strum, což představuje méně než 1/10 000 všech nádorů vaječníků. Struma ovarii byla poprvé popsaná Boettlinem v roce 1888 a následně charakterizovaná na počátku 20. století Ludwigem Pickem jako forma zralého teratomu. 1 Bývá jako součást zralých teratomů cca ve 3 %. 2 V nádoru převažuje tyreoidální tkáň více než v 50 %. 2 Výskyt strumy ovarii je nejčastější ve 4.–6. dekádě věku. Většina metastatických struma ovarii se skládá z papilárního nebo folikulárního karcinomu. 3 V našem sdělení prezentujeme ojedinělý případ pacientky se strumou ovarii a s peritoneální strumózou léčenou tyreoidektomií a radiojódovou ablací.
Kazuistika
Naší pacientkou je žena (1958) sledována na endokrinologii pro hypertyreózu s anamnézou stavu po pravostranné adnexektomii z roku 2004 a nálezem zralého teratomu s obsahem tyreoidní tkáně. Dále stav nebyl řešen.
Nynější onemocnění: Pacientka ambulantně sledována na endokrinologii s klinickými příznaky: palpitace s neklidem, cefalea, prekolapsové stavy a únava.
Laboratorně vykazovala známky hypertyreózy: TSH: 0,064 mIU/l [0,350…4,940], TRAK 1,01 IU/l [0,00...1,22] fT4.: 14,4 pmol/l [9,0…19,0], anti Tg 14 kU/l [0…115], fT3.: 4,4 pmol/l [3,1…6], antiTPO < 28 kIU/l [< 60].
Na provedené sonografii štítné žlázy byl nález neostře ohraničené žlázy, která byla zhrubělá, difuzně mírně hypoechogenní. Oba laloky obvyklé velikosti, v levém laloku nalezen hypoechogenní uzel o velikosti 3 x 4 x 5,8 mm, jiné ložiskové změny nebyly patrny. Závěr endokrinologického vyšetření: Symptomatická hypertyreóza zatím nejasné etiologie. Pacientka nejdříve léčena Thyrozolem, ale s následkem těžké kožní alergické reakce. Po změně terapie nasazen Propycil, po kterém zjištěna hepatopatie. Po vysazení tyreostatik přetrvávala symptomatická hypertyreóza. Pacientka preferovala totální tyreoidektomii, která byla v krátké době provedena (březen 2023) s hojením per primam. Poté nasazen Euthyrox s dávkou 100 mg denně. Mikroskopicky byl zjištěn obraz mikromakrofolikulární koloidní strumy. Přesto u pacientky i po totální tyroidektomii se sonografickým nálezem bez rezidua štítné žlázy, bez farmakologické substituce, stále laboratorně přetrvávala hypertyreóza.
Začala se zvažovat extratyroidální produkce hormonů štítné žlázy, diferenciálně diagnosticky přicházela v úvahu zejména struma ovarií nebo funkční metastázy dobře diferencovaného karcinomu štítné žlázy.
V lednu 2024 byla provedena sonografie a MRI pánve. V nálezech byla upřesněna multicystická expanze v oblasti levého ovaria velikosti 35 x 31 x 25 mm, dále vícečetná měkkotkáňová ložiska na peritoneu do velikosti 35 mm a zvětšené uzliny v levém třísle (největší velikosti 29 x 25 x 24 mm) a v retroperitoneu (velikost 20 x 13 mm). Diagnostická rozvaha směřovala k tomu, že nález může odpovídat teratomu, s vícečetnými implantačními lézemi na peritoneu a infiltrací uzlin. Jedna suspektní uzlina byla nalezena rovněž v retroperitoneu velikosti 20 x 13 mm. (Obr. 1)
V laboratorních nálezech (Tab. 1) dominoval zvýšený alfa fetoprotein – marker tumoru vaječníků a zvýšený tyreoglobulin – marker nádorů štítné žlázy. Zvýšený tyroxin a suprimovaný TSH dávaly informaci, že někde v těle stále funguje tyreoidální tkáň.
Další vyšetření pomocí transvaginálního ultrazvuku prokázalo multilokulární solidní tumor atypického vzhledu s nádorovými ložisky na peritoneu vpravo a při pánevní stěně. Dále byla zjištěna patologická lymfadenopatie vlevo při externích ilických cévách, při v. epigastrica inferior, v podkoží a intraaortokaválně. Na omentu byly patrné nodularity fixované k přední stěně břišní, vše vedoucí k podezření na maligní transformaci ovariální strumy a lymfatickou diseminaci v dutině břišní. Provedená biopsie z ložiska v levém třísle prokázala dobře diferencovanou tkáň štítné žlázy. (Obr. 2) Nález měl charakter extraovariálního šíření strumy ovarii, resp. představoval diseminaci velmi dobře diferencovaného folikulárního karcinomu.
V únoru 2024 následovalo celotělové scintigrafické vyšetření pomocí 99mTc-technecistanu sodného s doplněním SPECT/low dose CT břicha. (Obr. 3 a 4) Vyšetření prokázalo mnohočetné patologické okrsky zvýšené akumulace radiofarmaka v oblasti dutiny břišní a na peritoneu, v mesenteriu, jedno ložisko v retroperitoneu před obratlovým tělem L3 a další ložiska byla v malé pánvi.
Pacientka byla indikována k chirurgickému debulkingu, který byl proveden v březnu 2024. Z chirurgického hlediska došlo ke kompletnímu odstranění tumoru s provedením totální hysterektomie s adnexektomií, infrakolickou omentektomií, exstirpací tumoru z levé inguiny a z Retziova prostoru, z paraaortální oblasti, z mezenteria a peritonea a parakolických prostor. (Obr. 5) Histologicky byla ve velkém procentu na řadě míst tkáň dobře diferencovaná, ale ojediněle s nepravidelnými okrsky mikrofolikulů a téměř až solidních okrsků s jadernými znaky papilárního karcinomu. (Obr. 6) Definitivní závěr potvrzoval diseminaci dobře diferencované folikulární neoplazie s okrsky folikulární varianty papilárního karcinomu štítné žlázy. Laboratorní výsledky potvrdily normalizaci hodnot TT4 a TSH.
Pacientka byla následně indikována k terapii 131I, která se uskutečnila v květnu 2024. V přípravě na podání terapeutické aktivity byly intramuskulárně aplikovány v odstupu 24 hodin 2 injekce 0,9 mg rekombinantní formy TSH (Thyrogen). Poté byla podána aktivita 5,5 GBq 131I p.o. Poterapeutická scintigrafie proběhla v odstupu čtyř dnů. Hodnoty tyreoglobulinu (Tg) bazálně činily 61,68 mg/l, po stimulaci 2342 mg/l. S ohledem na výši hladiny Tg a přítomná mnohočetná ložiska v oblasti břicha a pánve byla další terapie naplánována v odstupu šesti měsíců taktéž po přípravě Thyrogenem s podáním 11 GBq 131I. Při další hospitalizaci v listopadu 2024 byl zaznamenán výrazný pokles hladiny Tg jak na supresi (0,065 mg/l při TSH 0,112 mIU/l)), tak po stimulaci Thyrogenem (Tg 8,2 mg/l). Na poterapeutické scintigrafii byla přítomná výrazná regrese patologické akumulace radiojódu, přetrvávala akumulace v inguinálních uzlinách a v jednom ložisku na peritoneu. Kontrolní diagnostická scintigrafie s podáním 185 MBq 131I po přípravě Thyrogenem proběhla v půlročním odstupu v dubnu 2025. Na snímcích včetně hybridního tomografického zobrazení byl již nález bez průkazu patologické akumulace radiojódu, stimulovaná hladina Tg byla 0,46 mg/l a odpovídala remisi onemocnění. Na Obr. 7 je patrný vývoj nálezu akumulace radiojódu v průběhu léčby.
Tab. 1: Laboratorní výsledky.
Třídy a metody
Výsledek
Normy
TT3
1,89
0,9–3 (nmol/l)
fT3
5,7
3,4–6,3 (pmol/l)
TT4
183,3
60–150 (nmol/l)
fT4
22,3
11,5–22,7 (pmol/l)
TSH
0,015
0,5–4,9 (mIU/l
TBG
25,8
10,9–34,9 (mg/l)
antiTg
< 1,3
< 4,5 (kU/l)
antiTPO
< 28
< 60 (kIU/l)
TRAK
0,81
0–1,75 (IU/l)
HCG
4
0–10 (IU/l)
Kalcitonin
< 1
0–4,8 (ng/l)
Chromogranin
65,3
0–85 (ng/l)
Thyreoglobulin
120,7
0,1–50 (mg/l)
AFP
11,6
0–8,1 (mg/l)
Ca 19-9
15,6
0–37 (kIU/l)
Ca 125
25,6
0–35 (kIU/l)
Ca15-3
28
0–33 (kIU/l)
Image 1. MRI pánve 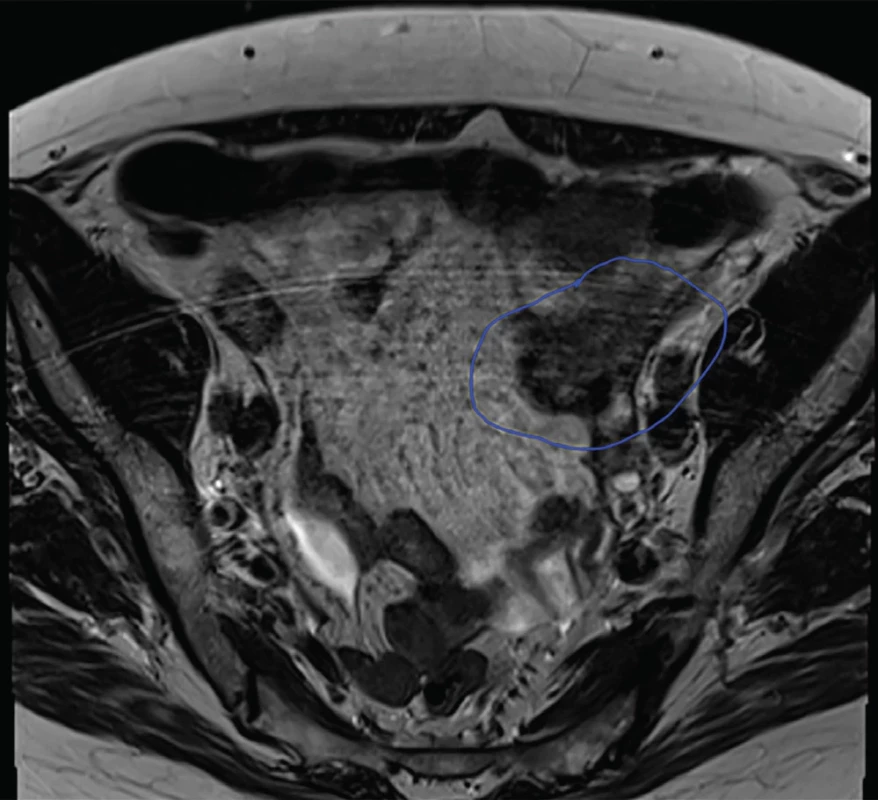
Na obraze je patrná multicystická expanze v oblasti levého ovaria 35 x 31 x 25 mm – nález může odpovídat teratomu. K tomu byly nalezeny vícečetné implantační léze na peritoneu do 35 mm, lymfadenopatie třísla vlevo velikosti 29 x 25 x 24 mm a jedna suspektní uzlina v retroperitoneu velikosti 20 x 13 mm. Image 2. Histologický nález z odebrané lymfatické uzliny 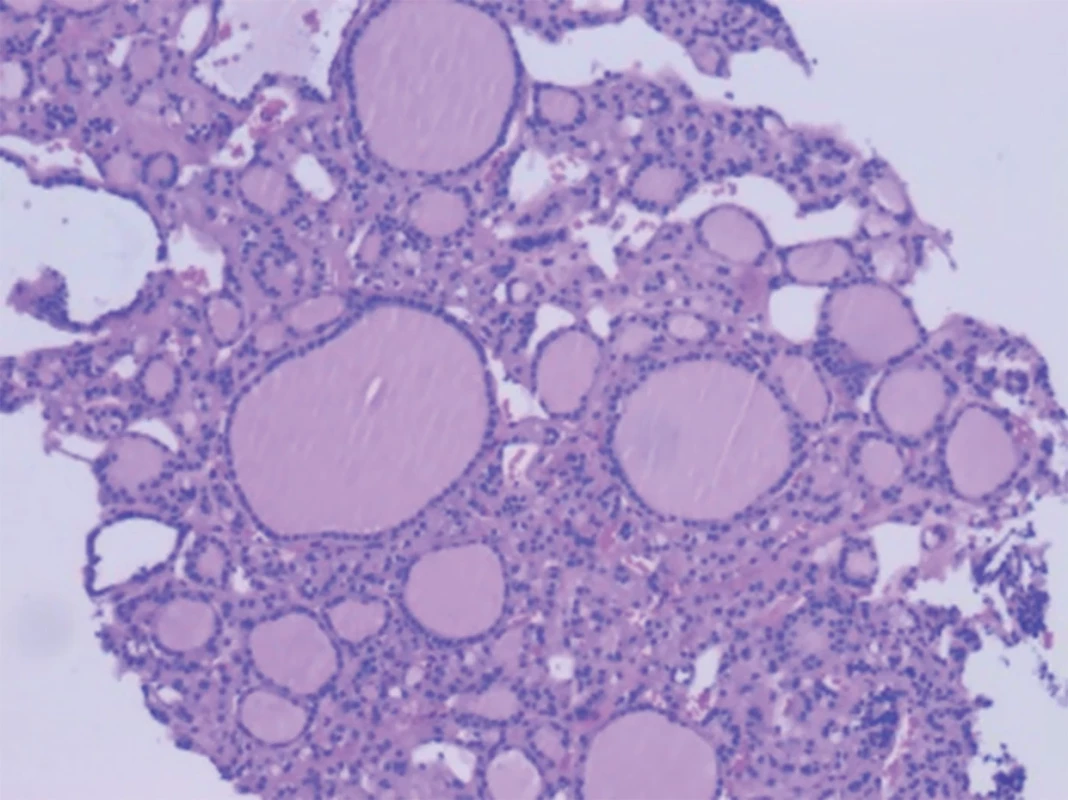
Folikuly jsou vystlány pravidelnými tyreocyty, v lumen je patrna stagnace koloidu a ojediněle mikrokalcifikace. Noduly jsou na periferii obklopeny malým množstvím vaziva. Image 3. Celotělové vyšetření po aplikaci 99mTc-TO4 
Vícečetná ložiska se zvýšenou akumulací radiofarmaka v. s. odpovídají tkáni štítné žlázy. Při hodnocení obrazu je nutné počítat s fyziologickou akumulací 99mTc-TO4 v oblasti žaludku, částečně v ledvinách a močovém měchýři. Image 4. Obrazy SPECT/CT po aplikaci 99mTc-TO4 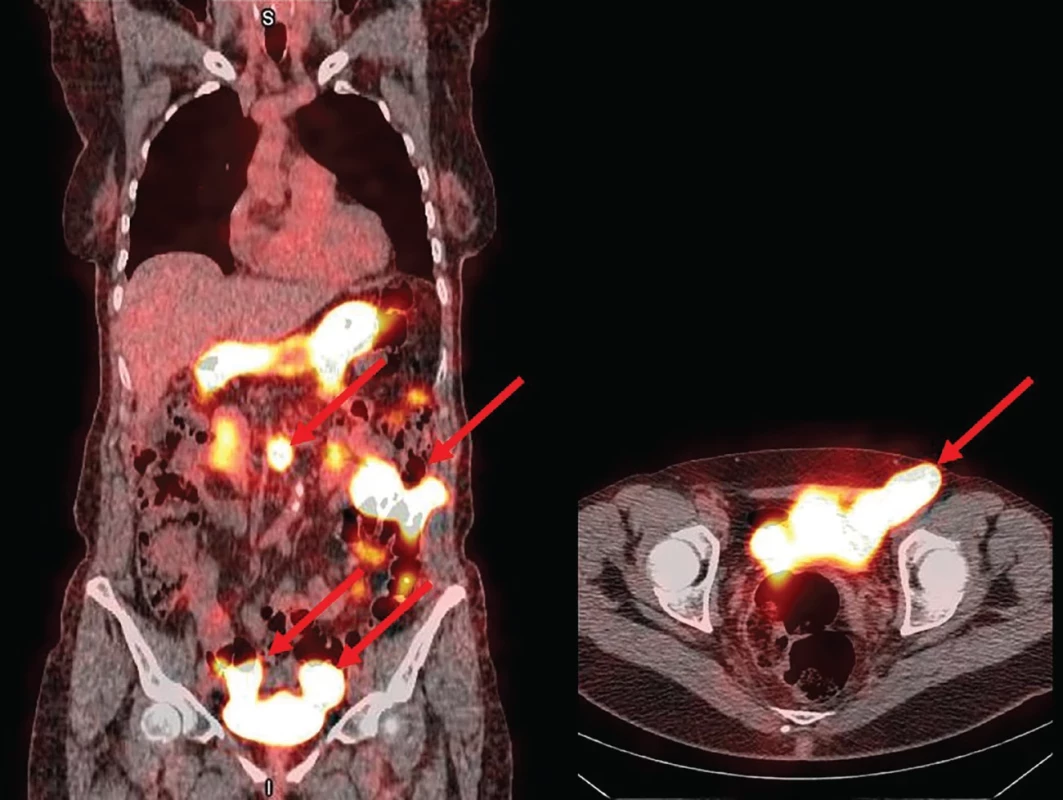
Vícečetná ložiska se zvýšenou akumulací radiofarmaka v dutině břišní označená šipkami, odpovídají tkáni štítné žlázy s upřesněním lokalizace podle low dose CT v koronálním a axiálním řezu. Image 5. Komplexní odstranění tumoru 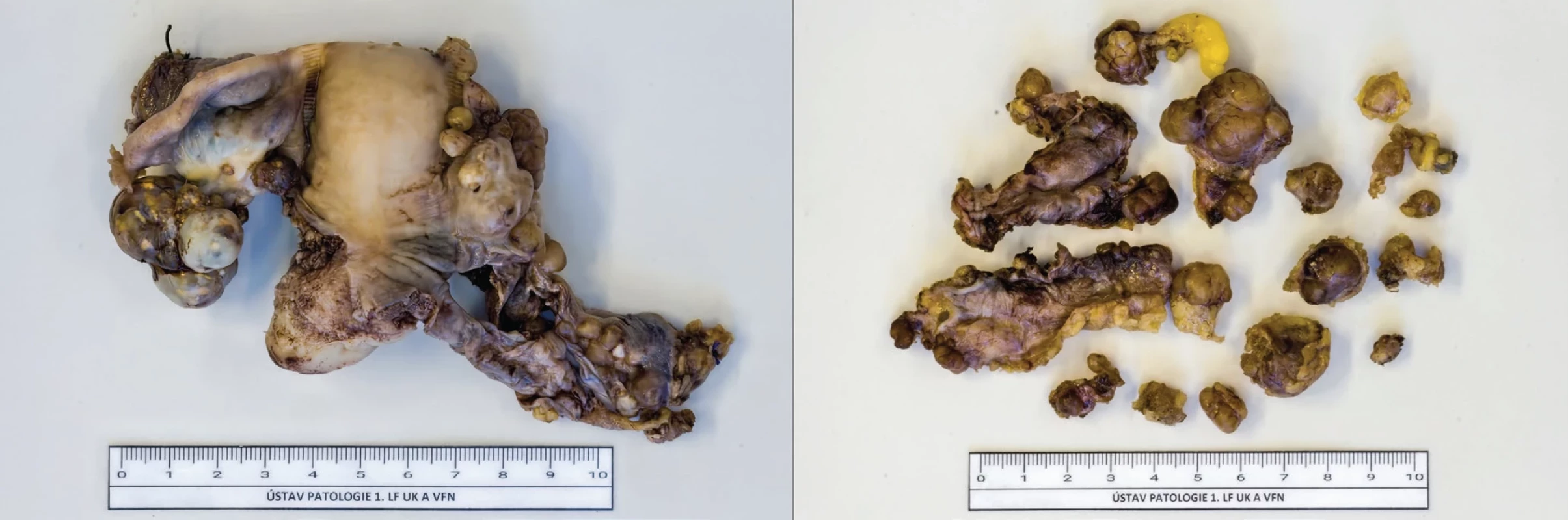
Operační rozsah: totální hysterektomie s adnexektomií, dále infrakolická omentektomie, exstirpace tumoru z levé inguiny a z Retziova prostoru,
z paraaortální oblasti, z mezenteria, peritonea a parakolických prostor.
Vlevo: děloha a ložiska levé děložní tuby a ovaria.
Vpravo: implantační metastázy potvrzeny na serózních površích peritonea i subperitoneálně.Image 6. Histologické nálezy z odstraněných ložisek 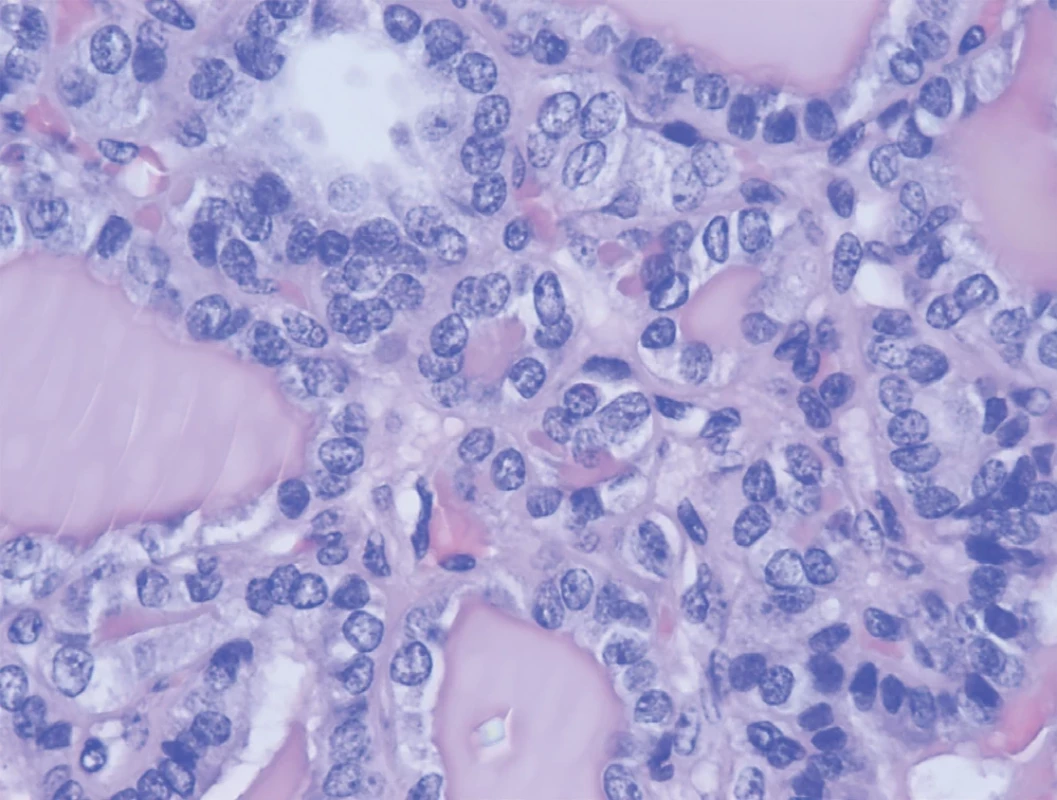
Histologicky byla ve velkém procentu na řadě míst tkáň dobře diferencovaná, ale ojediněle s nepravidelnými okrsky mikrofolikulů a téměř až solidních okrsků s jadernými znaky papilárního karcinomu. Image 7. Vývoj akumulace radiojodu v průběhu léčby, snímky v přední projekci 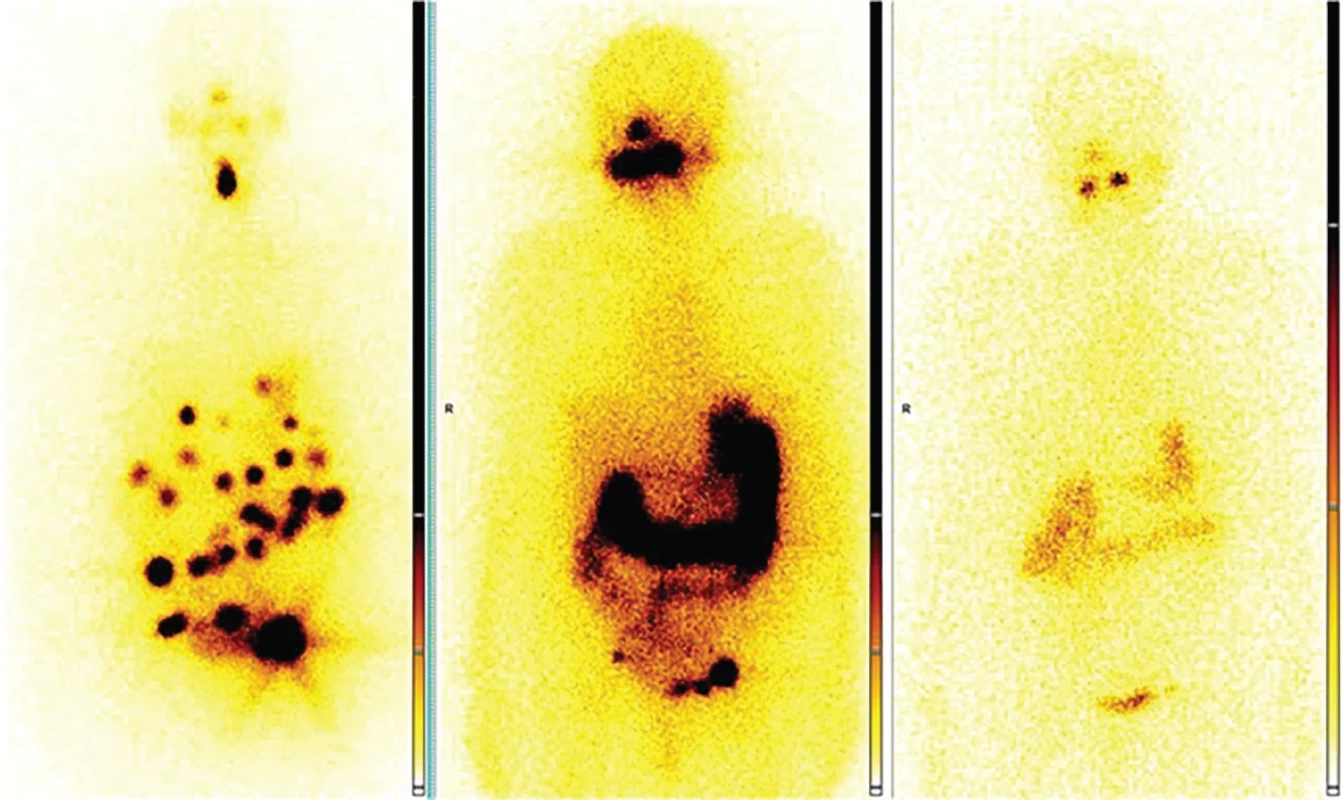
Na I. snímku přítomná akumulace v reziduu tyreoidey a mnohočetná ložiska v oblasti břicha a pánve na mesenteriu a peritoneu a v inguinálních uzlinách.
Na snímku II. došlo k eliminaci reziduí tyreoidey a vymizela četná ložiska, patologický nález přetrvává především v inguinálních uzlinách, je přítomné vyloučené radiofarmakum v průběhu kliček střevních a sytě se zobrazuje akumulace v alveolech maxilly.
Na snímku III. již ložiska s patologickou akumulací nejsou přítomná.DISKUZE
U naší pacientky bylo klíčové diferenciálně diagnosticky uvažovat o extratyroidální produkci hormonů štítné žlázy, která nastává u strumy ovarii nebo při funkčních metastázách dobře diferencovaného karcinomu štítné žlázy. U pacientky byla prokázána zvýšená hladina thyreoglobulinu. Pacientka sice uvedla, že u ní byla provedena adnexetomie v roce 2004, ale uváděla, že se jednalo o benigní nález. Teprve až v roce 2024 se začalo uvažovat, že se jednalo o strumu ovarii.
Přibližně u 5 % všech strum ovarii se vyvinou rysy maligní transformace. 4 Co se týče intratyreoidálních malignit, nejčastěji se vyskytuje papilární karcinom štítné žlázy, který vykazuje typické histologické charakteristiky, jako jsou překrývající se zábrusová jádra, vaskulární invaze nebo přítomnost psamomových tělísek. 5
Folikulární karcinom štítné žlázy je druhým nejčastějším typem, který představuje diagnostické problémy, protože při absenci pouzdra štítné žlázy je jeho jedinou definující charakteristikou u struma ovarii vaskulární invaze.
V diagnostice strumy ovarii je využití scintigrafických metod velmi přínosné. V našem případě i vyšetření pomocí 99mTc-pertechnetátu při celotělovém vyšetření a doplnění SPECT/CT vyšetření dopomohlo k cílené biopsii a upřesnění diagnózy a rozsahu postižení před chirurgickým debulkingem. V literatuře se lze setkat s dobře hodnoceným vyšetřením pomocí 123I se SPECT/CT, kdy scany jsou přínosné k odlišení benigního extraovariálního šíření od případů, kdy diagnostikované postižení lymfatických uzlin nebo vzdálených metastáz zvyšuje pravděpodobnost maligního průběhu onemocnění. 6
Tyreoidektomie je nejbezpečnější cestou k vyloučení primárního nebo koexistujícího karcinomu štítné žlázy ve štítné žláze a je předpokladem pozdější léčby radiojódem. 7 Naše pacientka dospěla k chirurgickému debulkingu a přestože se jednalo o rozsáhlou operaci s odstraněním mnoha patologických ložisek různé velikosti, následně na diagnostickém celotělovém obraze pomocí 131I jich řada v dutině břišní přetrvávala.
Po tyreoidektomii a ablativní léčbě radiojódem může tyreoglobulin sloužit jako spolehlivý marker pro sledování a časnou detekci biochemické recidivy. V případech s hojným extraovariálním šířením může exogenní stimulace TSH představovat vhodnou volbu po tyreoidektomii kvůli produkci ektopických hormonů. U těchto pacientů bývá úspěšně použit rekombinantní lidský TSH (rhTSH). 8
Léčba strumy ovarii s maligními rysy postrádá randomizované důkazy pro klinické rozhodování. V přítomnosti vysoce rizikových rysů, včetně velké velikosti nádoru, extraovariálního rozšíření nebo vzdálených metastáz, je tyreoidektomie následovaná léčbou radiojodem bezpečnou a účinnou léčebnou strategií. 9
ZÁVĚR
Peritoneální strumóza je vzácný projev extraovariální struma ovarii s benigní histologií štítné žlázy. Léčebný přístup je podobný se zavedeným doporučením pro malignitu štítné žlázy, která zahrnuje totální tyreoidektomii a radioaktivní ablaci pomocí 131I. Vyžaduje se další dlouhodobé sledování pacientky např pomocí skenů 123I a hladin tyreoglobulinu.
Obrazová dokumentace: Obr. 1 MUDr. Wagnerová, Radiologická klinika VFN a 1. LF UK Praha; Obr 2, 5 a 6 MUDr. Planičková, Ústav patologie 1. LF UK a VFN Praha; Obr. 3 a 4 MUDr. Chroustová a MUDr. Ptáčník, ÚNM 1. LF UK a VFN Praha, Obr. 7 MUDr. Táborská, KNME 2. LF UK a FN Motol Praha
Sources
- Gruhn J. A selective historical survey of ovarian pathology emphasizing neoplasms in Roth I.M. Czernobilsky B, editors. Tumors and tumor like conditions of the ovary vol 6, New York: Churchill Livingstone 1985, p.269-285
- Roth IM, Telerman A. Recent edvances the pathology and classification of ovarian germ cell tumors. Int J Gynecol Pathol 2006; 25 : 305-320
- Kaleem T, Peterson J, Krishna M. Peritoneal strumosis: Presentation and management with multiple radioactive indine treatments. Journal of Clinical and Translational Endocrinology: Case reports; 2018; 8 : 1-4. doi.org/10.1016/j.jecr.2018.01.002
- Roth IM, Telerman A. The enigma of struma ovarii. Pathology 2007; 39 : 139-146
- Garg K, Soslow RA, Rivera M et al: Histologically bland extremely welldifferenciated thyroid carcinoma sarising in struma ovarii canrecur and metastazice. Int J Gynecol Pathol 2009; 28 : 222-230
- Koo PJ, Klingensmith WC 3rd, Bagrosky BM, Haugen BR. SPECT/CT of metastatic struma ovarii. Clin Nucl Med 2014; 39 : 186-187
- Young RH, Jackson A, Wells M. Ovaria nmetastasis from thyroid carcinoma 12 years after partial thyroidectomy mimicking struma ovarii: report of a case. Int J Gynecol Pathol 1994; 13 : 181-185
- Checrallah A, Medlej R, Saade C et al. Malignant struma ovarii: an unusual presentation. Thyroid 2001; 11 : 889-892
- Groener D, Baumgarten J, Happel Ch et al. Thyroid papillary cancer elements arising from struma ovarii with bening peritoneal strumosis: Utility of iodine -123-imaging in diagnostics and treatment planning. Clin Case Rep 2023; 11: e07311
Labels
Nuclear medicine Radiodiagnostics Radiotherapy
Article was published inNuclear Medicine

2025 Issue 3-
All articles in this issue
- Editorial
- Přínos nukleární medicíny v diagnostice a terapii pacientky s peritoneální strumózou – kazuistika
- Neúmyslná intraarteriální aplikace 99mTc-HDP při scintigrafii skeletu u 64leté pacientky – kazuistika
- Význam hybridního zobrazení plicní perfuze pro detekci možné příčiny dušnosti
- Okénko do literatury
- Noví členové společnosti
- XLVI. Pracovní dny radiofarmaceutické sekce ČSNM, Olomouc 28. – 30. 5. 2025
- Z historie NM
- S1 Abstrakta – 61. DNM, Liberec 24. – 26. září 2025
- S2 Abstrakta – XLVI. Pracovní dny radiofarmaceutické sekce ČSNM, Olomouc 28. – 30. května 2025
- Nuclear Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- S1 Abstrakta – 61. DNM, Liberec 24. – 26. září 2025
- Neúmyslná intraarteriální aplikace 99mTc-HDP při scintigrafii skeletu u 64leté pacientky – kazuistika
- XLVI. Pracovní dny radiofarmaceutické sekce ČSNM, Olomouc 28. – 30. 5. 2025
- Přínos nukleární medicíny v diagnostice a terapii pacientky s peritoneální strumózou – kazuistika
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

