-
Medical journals
- Career
Oboustranné vícečetné pneumatokély jako vzácná pozdní komplikace pneumonie covid-19
Authors: Samuel Genzor 1; Jan Mizera 1; Milan Sova 1,2; Shayan Nadjarpour 3; Petr Jakubec 1
Authors‘ workplace: Klinika plicních nemocí a tuberkulózy FN a LF UP Olomouc 1; Klinika nemocí plicních a tuberkulózy FN a LF MU Brno 2; Lékařská fakulta Univerzity Palackého Olomouc 3
Published in: Vnitř Lék 2021; 67(8): 485-488
Category: Case reports
Overview
Pneumatokéla je dutinová plicní léze, která může vzniknout jako vzácná komplikace pneumonie. Častěji se vyskytuje u pacientů po mechanické ventilaci. Po pneumonii covid-19 jsou popisovány zatím pouze jednotlivé kazuistiky. Prezentujeme případ muže bez zásadních komorbidit, u kterého v post‑akutní fázi středně těžkého průběhu covidu-19 vznikly oboustranné vícečetné pneumatokély. Komplexním vyšetřením byly vyloučeny jiné potenciálně závažné příčiny tohoto stavu. Během sledování bez jakékoliv terapie dochází k postupné spontánní resorpci nálezu oboustranně. Klinicky je pacient nadále ve velmi dobrém stavu.
Klíčová slova:
komplikace – COVID-19 – pneumonie – pneumatokéle
Úvod
Pneumatokéla je dutinová, vzduchem vyplněná plicní léze (1). Její výskyt je vzácný s neznámou prevalencí. Etiopatogenetické příčiny lze rozdělit na infekční a neinfekční. Pneumatokély (post)infekčního původu jsou většinou komplikace pneumonií. Byly popsány při infekcích Mycobacterium tuberculosis, Streptococcus pneumoniae, Proteus mirabilis, Staphylococcus aureus a jiných (1).
Častěji jsou popisovány u novorozenců, kde je nejčastějším etiologickým agens zlatý stafylokok (2). Mezi neinfekční příčiny vzniku pneumatokél patří trauma (včetně iatrogenního), následek mechanické ventilace (invazivní/neinvazivní), či inhalace toxických výparů a horkých plynů (1).
V případě nekomplikované pneumatokély dochází často ke spontánní regresi a není nutná žádná specifická terapie (1).
Prezentace případu
Náš pacient byl muž ve věku 59 let, dosud léčen pouze s arteriální hypertenzí, nekuřák, normostenik. Od poloviny října 2020 udával nechutenství, horečky a anosmii. Negoval jakékoliv respirační potíže. Z tohoto důvodu byl praktickým lékařem dne 21. 10. 2020 odeslán k ambulantnímu vyšetření PCR SARS‑CoV - 2, které prokázalo pozitivitu. Jeho stav zatím umožňoval domácí léčbu. Postupně však docházelo k dalšímu zhoršování stavu a dne 29. 10. 2020 se dostavil na infekční ambulanci oddělení urgentního příjmu. V laboratorních odběrech byla výrazná elevace C‑reaktivního proteinu (CRP) – 228,3 mg/l, na skiagramu hrudníku (Obr. 1) byla popsána bilaterální plicní infiltrace s periferní predominancí, další nálezy byly bez pozoruhodností. Byl přijat k hospitalizaci k i. v. antibiotické terapii (cefuroxim/axetine + klarythromycin). Podávány byly i glukokortikoidy (dexamethason 8 mg pro die). Během hospitalizace nebyla nutná oxygenoterapie, postupně docházelo ke zlepšování klinického stavu, poklesu CRP (51,4…20,3…13,7 mg/l) i mírné parciální regresi plicních infiltrátů (Obr. 2). Na základě komplexních mikrobiologických odběrů nebyla prokázána spoluúčast jiného bakteriálního či virového agens (vylučovány Mycoplasma, Chlamydia, Bortedella, RS virus, influenza A i B; negativní byly rovněž kultivace ze sputa). Dne 6. 11. 2020 byl dimitován v kardiopulmonálně kompenzovaném stavu do domácí péče.
Image 1. Skiagram hrudníku při příjmu, 29. 10. 2020 – bilaterální infiltráty s periferní predominancí 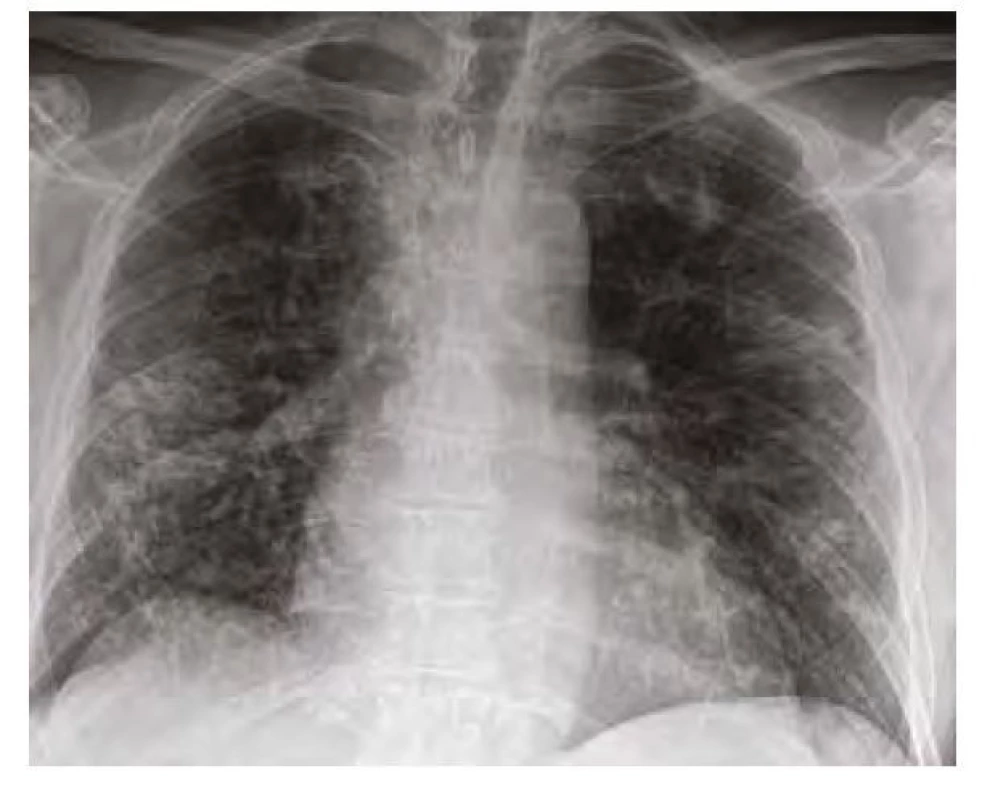
Image 2. Skiagram hrudníku před propuštěním 6. 11. 2020 – mírná parciální regrese infiltrátů, patrná zejména vlevo bazálně 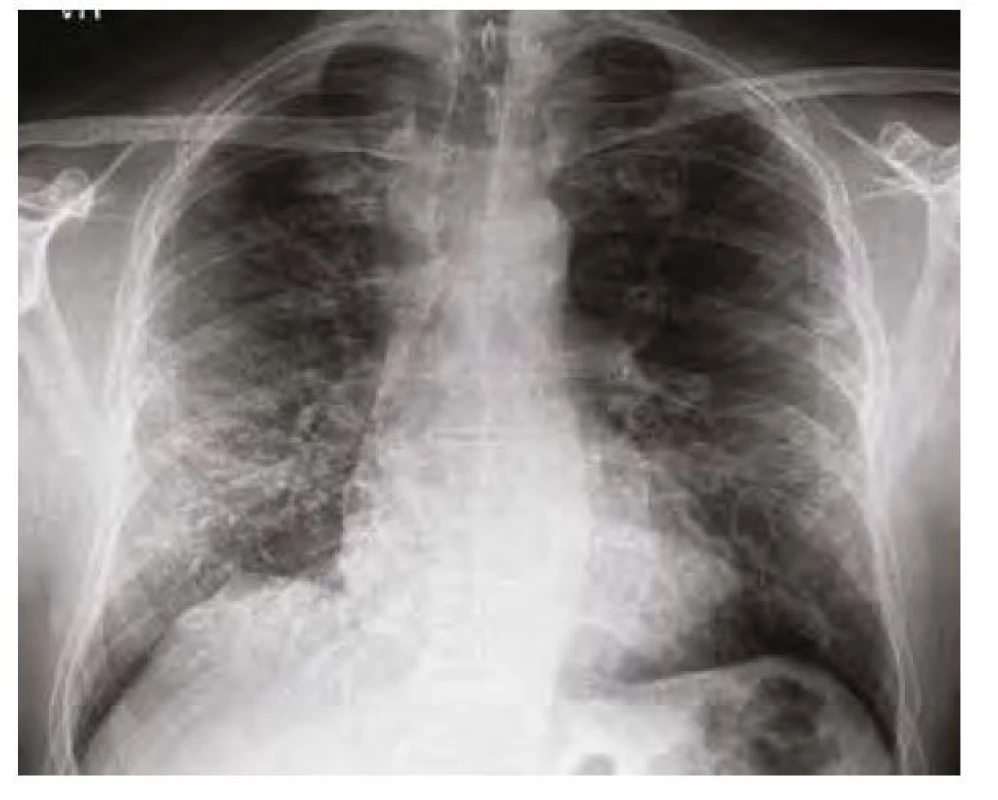
Dne 23. 11. 2020 se dostavil na kontrolu do post‑covidové ambulance Kliniky plicních nemocí a tuberkulózy Fakultní nemocnice Olomouc. Nereferoval jakékoliv subjektivní potíže. Na skiagramu hrudníku byly ale překvapivě nově přítomny heterogenní stíny vpravo ve středním a dolním poli. Na levé plíci byla dále zřetelná progrese heterogenních stínů ve středním poli, které byly až ložiskového charakteru (Obr. 3). Laboratorní nález byl bez pozoruhodností, CRP 8,2 mg/l. K objasnění nálezu jsme doplnili počítačovou tomografii s vysokým rozlišením (high‑resolution computed tomography – HRCT). Ta prokázala přítomnost vícečetných solidních i dutinových ložisek s maximem v obou dolních lalocích plic. Část lézí měla širší stěnu, některá i tekutinový obsah (Obr. 4 a, b, c). V diferenciální diagnostice v tuto chvíli připadal v úvahu mykotický či specifický proces, septické emboly, eventuálně granulomatóza s polyangiitidou. Vyšetření na panel autoprotilátek neprokázalo podezření na vaskulitidu či jiné systémové autoimunitní onemocnění (negativní ANA, ANCA, RD, anti‑ss‑DNA, anti‑ds‑DNA). Normální bylo taktéž vyšetření hladin základních tříd imunoglobulinů a parametrů buněčné imunity. Doplnili jsme ORL vyšetření (normální nález), doplněna byla i biopsie nosní sliznice, kde byl popsán histologicky pouze papilom s lehkou dysplazií. Dne 4. 12. 2020 bylo doplněno bronchoskopické vyšetření v lokální anestezii: endoskopicky bez patologie v dosahu bronchoskopu. Bronchoaleveolární laváž prokázala pouze hraničně zvýšené zastoupení lymfocytů (10 %) a neutrofilů (6 %); imunoregulační index (CD4/CD8) byl snížen – 0,54. Komplexní mikrobiologické vyšetření (včetně průkazu pneumocysty, cytomegaloviru, Epstein‑Barrové viru, Herpes simplex viru, kultivace na Kochův bacil a mykologické kultivace) bylo kompletně negativní.
Image 3. Skiagram hrudníku 23. 11. 2020 – nově heterogenní stíny vpravo ve středním a dolním poli, vlevo navíc progrese heterogenních stínů ve středním poli, některé s naznačeným fenoménem hladiny 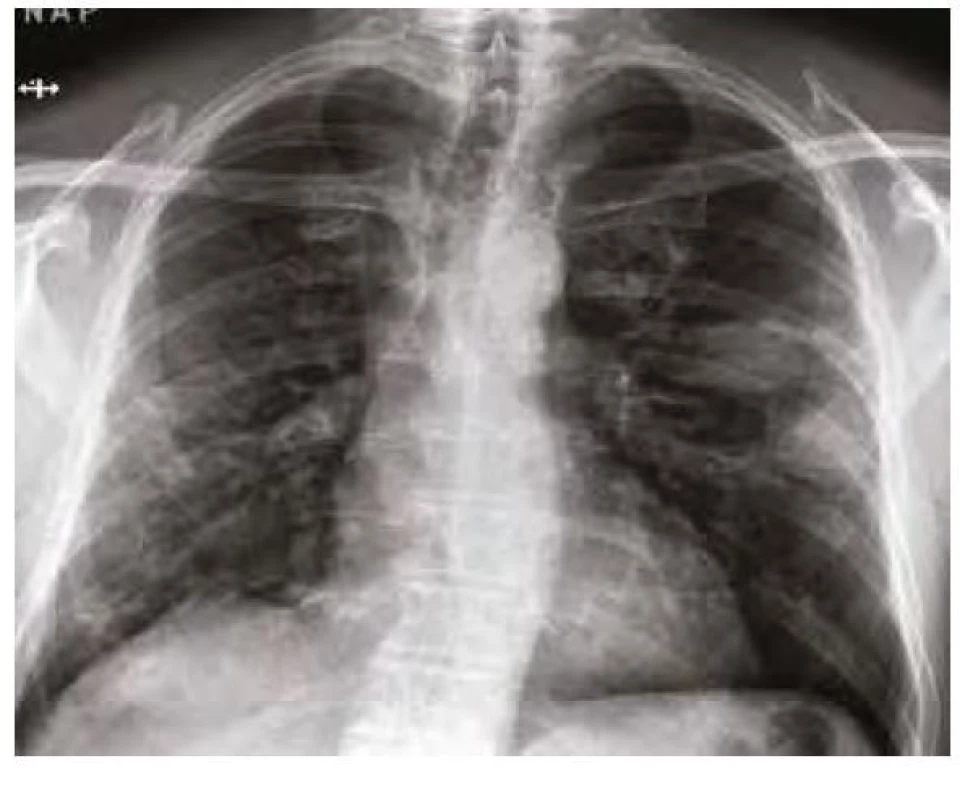
Image 4. A, B, C. HRCT plic 26. 11. 2020 – oboustranně patrné dutinové částečně vyplněné léze 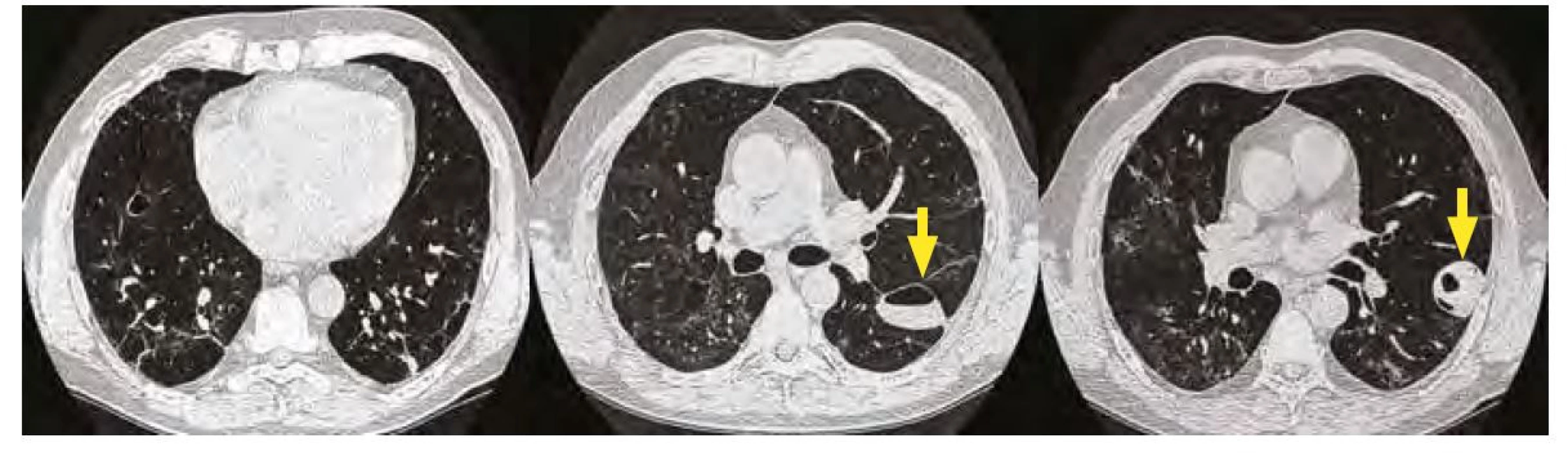
Vzhledem k chybění klinických potíží byla domluvena strategie observace. Dne 27. 1. 2021 jsme doplnili kontrolní HRCT plic, kde byla patrna spontánní parciální regrese solidních i dutinových ložisek v obou plicích – ložisek ubylo a přítomná ložiska byla již bez kavitací (Obr. 5A, B, C).
Image 5. A, B, C. HRCT plic 27. 1. 2021 – parciální regrese dutinových lézí oboustranně, dutinová léze v pravém dolním laloku již není přítomna 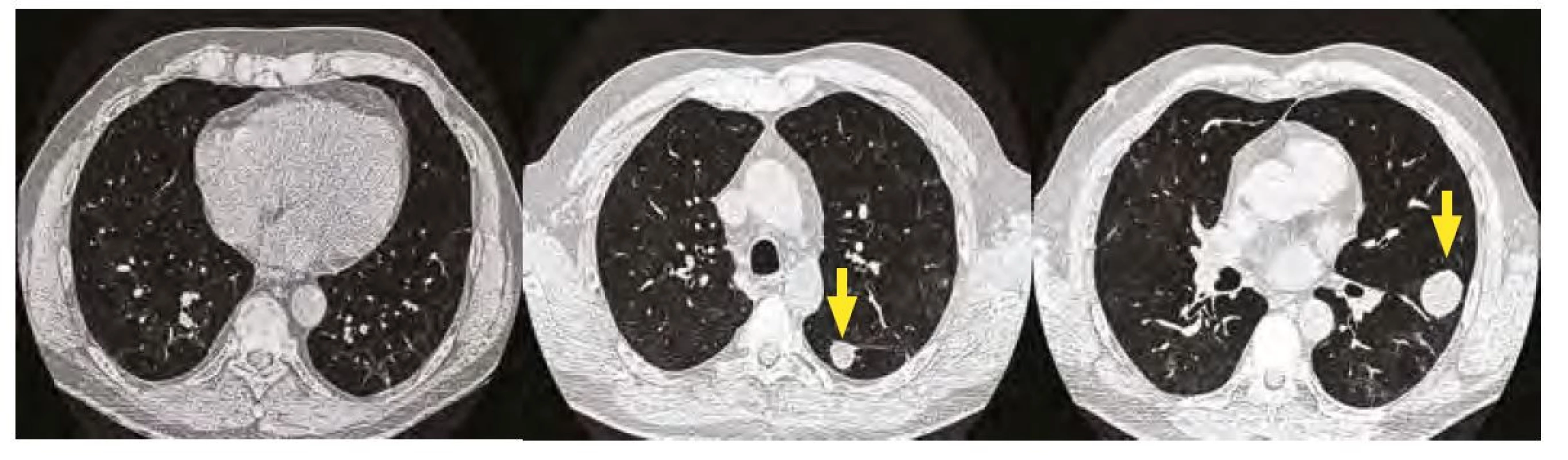
Sledování pacienta dále pokračovalo v režimu kontrolních skiagramů hrudníku a preventivních laboratorních odběrů k vyloučení demaskování jiného onemocnění. V dalším sledování byla nadále patrna postupná spontánní regrese nálezu oboustranně (obrázek 6A, B, C). Klinický stav pacienta je nadále příznivý a zůstává v našem sledování.
Image 6. A, B, C. Další postupná regrese dutinových lézí, měření nejlépe viditelné léze v levém dolním laloku 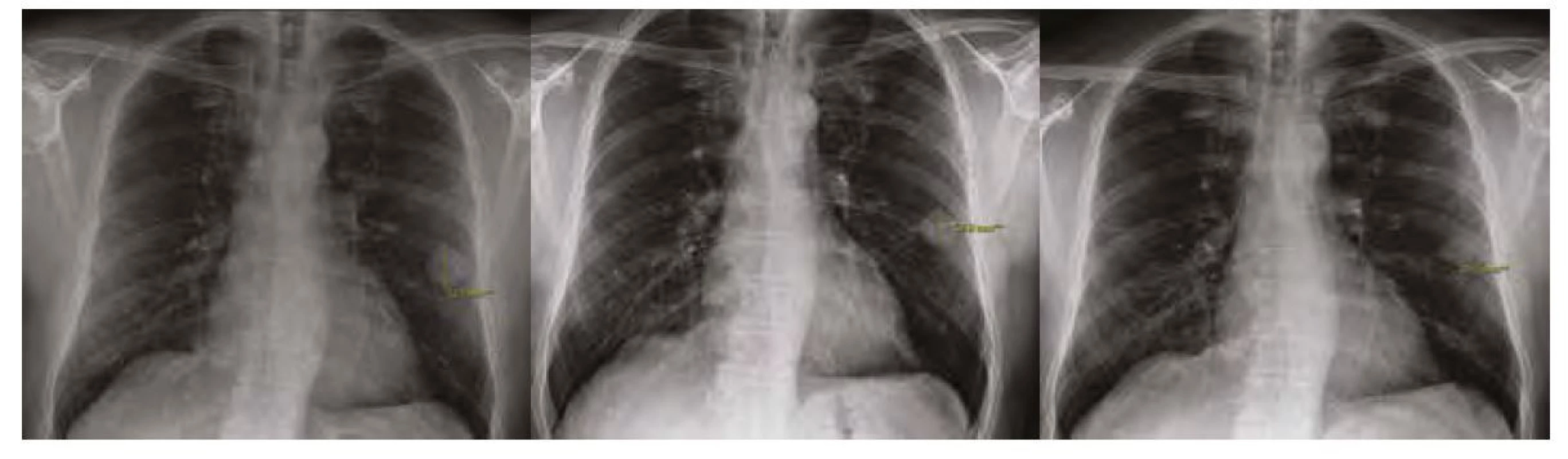
Diskuze
Přesná příčina vzniku (post)infekčních pneumatokél není dosud známa. Většina autorů uvádí teorii o endobronchiálním chlopenním mechanismu spojeném s hromaděním vzduchu v plicích (tzv. air trapping). U některých pacientů dochází ke vzniku distálně lokalizovaných vzduchových cyst (3). Další teorie pracuje s myšlenkou, že zánět a nekrotické změny v dýchacích cestách vedou k fokálnímu nahromadění vzduchu v plicním interstíciu, z kterého se vzduch dostává až do subpleurálního prostoru. Právě zde se pneumatokély vyskytují nejčastěji (4). Tyto léze mohou vznikat časně v akutním stádiu onemocnění, ale i s odstupem několika týdnů (5), což byl také případ našeho pacienta. V případě použití umělé plicní ventilace jsou tyto změny častější, ale i tak poměrně raritní (1). U pacientů s pneumonií covid-19 je jejich výskyt také poměrně vzácný, největší publikovaný soubor obsahuje pouze 12 osob, přičemž u všech byla použita invazivní mechanická ventilace (6). Postižení plic vyvolané nadměrným dechového úsilím je označováno jako patient self‑inflicted lung injury, zkracováno jako P‑SILI (7). Náš případ je zajímavý také tím, že náš pacient byl po celou dobu ventilačně suficientní, bez subjektivní dušnosti, kašle či nutnosti oxygenoterapie. O postižení typu P‑SILI se tedy u něj určitě nejednalo.
V literatuře jsou většinou popsány jednostranné léze, oboustranné pneumatokély jsou méně časté a častěji bývají spojeny s komplikacemi (8). Možné komplikace představují zejména superinfekce (9, 10) či rozvoj pneumothoraxu (11). V méně jasných případech je pak nutné diferenciální diagnózu rozšířit o mycetomy, tuberkulomy a autoimunitní onemocnění (zejména granulomatóza s polyangiitidou). Pokud není dostupná předchozí obrazová dokumentace, tak i vyloučení nádorového onemocnění. Pokud jsou možné závažnější příčiny vyloučeny, a nedochází ke vzniku komplikací, lze pacienta pouze observovat. U většiny pacientů je předpoklad spontánní resorpce (1). Tento případ ilustrovala i naše kazuistika.
Závěr
Pneumonie covid-19 může být vzácně komplikována vznikem pneumatokély. Její diagnóza by měla být vždy až po vyloučení jiných potenciálně závažných příčin dutinových lézí. U většiny pacientů dochází ke spontánní úpravě nálezu bez nutnosti jakékoliv terapie.
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Samuel Genzor, Ph.D.
Klinika plicních nemocí a tuberkulózy, Fakultní nemocnice Olomouc I. P. Pavlova 6, 779 00 Olomouc
Cit. zkr: Vnitř Lék 2021; 67(8): 485–488
Článek přijat redakcí: 12. 10. 2021
Článek přijat po recenzích: 18. 11. 2021
Sources
1. Jamil A, Kasi A. Pneumatocele. In: StatPearls. StatPearls Publishing, Treasure Island (FL); 2020. PMID: 32310606.
2. Rocha G. Pulmonary pneumatoceles in neonates. Pediatric Pulmonology. 2020; 55 : 2532–2541. https://doi.org/10.1002/ppul.24969
3. Hamad AM, El‑Saka HA. Post COVID-19 large pneumatocele: clinical and pathological perspectives. Interact Cardiovasc Thorac Surg. 2021;33(2):322–324. doi:10.1093/icvts/ivab072
4. Hamad AM, Elmahrouk AF, Abdulatty OA. Alveolar air leakage in COVID-19 patients: pneumomediastinum and/or pneumopericardium. Heart Lung 2020; 49 : 881–2.
5. Al‑Saleh S, Grasemann H, Cox P. Necrotizing pneumonia complicated by early and late pneumatoceles. Can Respir J. 2008 Apr;15(3): 129-32. doi: 10.1155/2008/136708. PMID: 18437254; PMCID: PMC2677935.
6. Zoumot Z, Bonilla MF, Wahla AS, Shafiq I, Uzbeck M, et al. Pulmonary cavitation: an under‑recognized late complication of severe COVID-19 lung disease. BMC Pulmonary Medicine. 2021; 21(1): 24. doi: 10.1186/s12890-020-01379-1.
7. Battaglini D, Robba C, Ball L et al. Noninvasive respiratory support and patient self‑inflicted lung injury in COVID-19: a narrative review. Br J Anaesth. 2021 Sep; 127(3): 353 – 364. doi: 10.1016/j.bja.2021. 05. 024.
8. Alhakeem A, Khan MM, Al Soub H et al. Case Report: COVID-19-Associated Bilateral Spontaneous Pneumothorax‑A Literature Review. Am J Trop Med Hyg. 2020 Sep; 103(3): 1162–1165.
9. Kim SH, Chung YT, Lee KD, Seon KY, Lee JH, Lee SH et al. Infected pneumatocele following anaerobic pneumonia in adult. Korean J Intern Med 2005; 20 : 343–345.
10. Kunyoshi V, Cataneo DC, Cataneo AJ. Complicated pneumonias with empyema and/or pneumatocele in children. Pediatr Surg Int. 2006 Feb; 22(2): 186–190. doi: 10.1007/s00383 - 005-1620-5. Epub 2005 Dec 16. PMID: 16362309.
11. González‑Pacheco H, Gopar‑Nieto R, Jiménez‑Rodríguez GM et al. Bilateral spontaneous pneumothorax in SARS‑CoV - 2 infection: A very rare, life‑threatening complication. Am J Emerg Med. 2021 Jan; 39 : 258.e1-258.e3. doi: 10.1016/j.ajem.2020. 07. 018.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2021 Issue 8-
All articles in this issue
- Problematika antibiotické léčby u pacientů s covidem-19
- Aktivní vyhledávání a časná diagnostika HCV infikovaných osob
- Optimální hladina kalia u pacientů se srdečním selháním
- Lokalizovaná (unicentrická) forma Castlemanovy nemoci. Klinické projevy, diagnostika a léčba
- Glifloziny – nové léky pro pacienty se srdečním selháním?
- Renoparenchymatózní hypertenze – aktuality v diagnostice a léčbě
- Oboustranné vícečetné pneumatokély jako vzácná pozdní komplikace pneumonie covid-19
- Jaká jsou specifika syndromu diabetické nohy a proč potřebujeme mezioborová doporučení pro jeho diagnostiku a léčbu?
- Expertní konsenzus k významu deficitu železa a možnosti jeho korekce u pacientů se srdečním selháním
- Memorandum z jednání zástupců ČIS a ČPFS dne 6. 5. 2021 v Lékařském domě ČLS JEP v Praze
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Renoparenchymatózní hypertenze – aktuality v diagnostice a léčbě
- Glifloziny – nové léky pro pacienty se srdečním selháním?
- Optimální hladina kalia u pacientů se srdečním selháním
- Problematika antibiotické léčby u pacientů s covidem-19
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

