-
Medical journals
- Career
Biosurfaktanty a ich úloha v inhibícii biofilm tvoriacich patogénnych baktérií
Authors: Karolína Englerová; Radomíra Nemcová; Eva Styková
Published in: Čes. slov. Farm., 2018; 67, 107-112
Category: Original Article
Overview
Rezistencia patogénnych baktérií je v dnešnej dobe jedným z hlavných medicínskych problémov. Väčšina mikrobiálnych infekcií má základ v tvorbe biofilmov, ktoré sú významným rezervoárom patogénov. Táto práca sa zaoberá antibiofilmovou a antimikrobiálnou aktivitou biosurfaktantov z črevných laktobacilov a baktérií izolovaných zo vzoriek mora. Biosurfaktanty (BS) izolované z kmeňov L. fermentum 2I3, L. fermentum B2/6, L. reuteri SL16, L. reuteri B6/1, S. luteola 3/22, Brevibacillus sp. 4/9, Brevibacillus sp. 2/30 a B. amyloliquefaciens 1/6K signifikantne (p < 0,001) inhibovali tvorbu biofilmu u S. aureus CCM 3953 a P. mirabilis CCM 7188, pričom výraznejšia inhibícia bola detegovaná v prípade BS morských baktérií oproti laktobacilovým BS. Výsledky naznačujú, že mechanizmus antibiofilmového efektu laktobacilových BS voči obidvom referenčným kmeňom je rovnaký a nie je výsledkom ich antimikrobiálneho pôsobenia. Naproti tomu, mechanizmus antibiofilmového efektu BS získaných z morských baktérií je pravdepodobne závislý od vlastností použitého referenčného kmeňa.
Kľúčové slová:
biosurfaktanty • biofilm • patogény • inhibícia
Úvod
Antibiotická rezistencia a nozokomiálne infekcie sa stávajú čoraz rozsiahlejším problémom súčasnej medicíny. Podiel na tejto situácii majú, okrem iného, aj biofilmy. Biofilmy umožňujú mikroorganizmom kolonizovať nielen tkanivá a orgány, ale aj rôzne medicínske nástroje a zariadenia, čím významne prispievajú k vzniku a šíreniu nozokomiálnych infekcií. Biofilm tvoriace mikroorganizmy sú charakteristické zvýšenou odolnosťou voči antimikrobiálnym a dezinfekčným látkam a schopnosťou odolávať imunitnému systému hostiteľa. ATB terapia biofilmových infekcií je veľmi náročná a mnohokrát nedostatočná, preto tieto infekcie mávajú dlhodobý, často návratný charakter1–4). V celosvetovom meradle prevláda snaha o hľadanie nových prístupov, resp. cielených a racionálnych stratégií riešenia tejto problematiky bez rizika navodenia rezistencie. Stále aktuálnejšími a vyhľadávanejšími sú metódy využívajúce prírodné a bakteriálne bioaktívne látky, u ktorých možno pozorovať lepší profil aj z hľadiska toxicity, biodegradovateľnosti a ekologického dopadu5).
Biosurfaktanty (BS) sú povrchovo aktívne zlúčeniny produkované rôznymi druhmi mikroorganizmov. Ich molekuly sú amfifilné, tvorené hydrofilnými a hydrofóbnymi oblasťami, ktoré spôsobujú agregáciu na rozhraní medzi kvapalinami rôznej polarity, ako je napríklad voda a uhľovodíky6). BS majú schopnosť modifikovať povrchové vlastnosti a tým ovplyvniť priľnavosť mikroorganizmov. Tieto vlastnosti BS je možné využiť v oblasti antimikrobiálnej a antibiofilmovej aplikácie4). V rámci terapeutickej praxe sa BS môžu použiť ako fungicídne, baktericídne, insekticídne, antivírusové a antiadhézne činidlá a inhibítory enzýmov7).
Cieľom práce bola izolácia BS z črevných laktobacilov a baktérií získaných zo vzoriek mora a testovanie ich antibiofilmových a antimikrobiálnych vlastností voči biofilm tvoriacim referenčným kmeňom Staphylococcus aureus CCM 3953 a Proteus mirabilis CCM 7188 v podmienkach in vitro.
Experimentálna časť
Materiál a metodika
Bakteriálne kmene
V práci boli použité kmene Lactobacillus fermentum 2I3, Lactobacillus fermentum B2/6, Lactobacillus reuteri SL16, Lactobacillus reuteri B6/1 izolované z trusu sliepky, bažanta a ošípanej a kmene Sporosarcina luteola 3/22, Bacillus amyloliquefaciens 1/6K, Brevibacillus sp. 2/30, Brevibacillus sp. 4/9 izolované z morskej vody a morského piesku. Ako referenčné biofilm tvoriace kmene boli použité kmene Staphylococcus aureus CCM 3953 a Proteus mirabilis CCM 7188 (Česká zbierka mikroorganizmov, Masarykova univerzita, Brno, ČR).
Izolácia BS viazaných na bunky
Na izoláciu BS bola použitá modifikovaná metóda podľa Gudiña a kol.8). Laktobacily rástli na de Man-Rogosa-Sharpe agare (MRS; pH 6.5; Carl Roth GmbH, Germany) v anaeróbnych podmienkach (Gas Pak Plus, BBL, Microbiology Systems, Cockeysville, USA) 48 hodín pri 37 °C. Morské baktérie boli inkubované na Brain Heart Infusion agare (BHI; pH 7; HIMEDIA) v aeróbnom prostredí pri teplote 27 ºC 48 hodín. Na prípravu štandardizovanej suspenzie testovaných kmeňov boli použité 3–4 solitárne kolónie, ktoré boli resuspendované v 5 ml fyziologického roztoku tak, aby vzniknutý zákal odpovedal 1. stupňu McFarland zákalovej stupnici. MRS bujón (50 ml) bol inokulovaný 0,5 ml štandardizovanej suspenzie kmeňov laktobacilov. Kmene boli inkubované aeróbne 24 hodín pri 37 °C. Štandardizované suspenzie morských baktérií (0,5 ml) boli inokulované do 50 ml McKeen média (20 g/l glukóza; 5 g/l kyselina glutámová; 1 g/l K2HPO4; 1,02 g/l MgSO4; 0,5 g/l KCl; 1 g/l minerálny roztok: 0,5 g/l MnSO4. 7 H2O; 0,16 g/l CuSO4. 5 H2O; 0,015 g/l FeSO4. 7 H2O; pH 7) a inkubované aeróbne 24 hodín pri 27 °C v trepacom vodnom kúpeli (Julabo SW 2C, Labor Technik, Seelbach, Germany). Pomnožené kultúry boli centrifugované 45 minút, pri 4 °C a 4500 otáčkach/min. Supernatanty boli odstránené a premyté bunky boli resuspendované v 20 ml PBS (8 g/l NaCl; 0,2 g/l KCl; 1,42 g/l Na2HPO4; 0,24 g/l KH2HPO4; pH 7,4). Bunky boli dve hodiny jemne pretrepávané na orbitálnej trepačke (150 otáčok/min.) a následne centrifugované. Získané supernatanty boli sterilizované filtráciou cez mikrobiologické filtre s veľkosťou pórov 0,25 µm (Frisenette ApS, Denmark). Potom boli supernatanty dialyzované voči destilovanej vode (6–8 kDa, 4 °C, 72 h; D-TubeTM Dialyzer, Merck) za účelom odstránenia solí a iných komponentov a zlyofilizované.
Oil spreading test
Na meranie povrchovej aktivity BS bol použitý oil spreading test (test šírenia oleja) (obr. 1) podľa Morikawa a kol.9) s následnou modifikáciou: na povrch 10 ml destilovanej vody v Petriho miske (priemer 60 mm) bola pridaná kvapka ropy tak, aby sa na povrchu vody vytvorila tenká membrána. Na vytvorenú vrstvu ropy bolo opatrne napipetovaných 100 µl supernatantu získaného po pretrepaní bakteriálnych buniek v PBS. V pozitívnom prípade došlo vo vrstve ropy k vytvoreniu prečistenej zóny, ktorej priemer bol následne zmeraný. Ako pozitívna kontrola bol použitý detergent Tween 80 a ako negatívna kontrola PBS. Testovanie každého BS bolo uskutočnené v troch opakovaniach.
Image 1. Oil spreading test (tvorba prečistenej zóny) PK – pozitívna kontrola, NK – negatívna kontrola 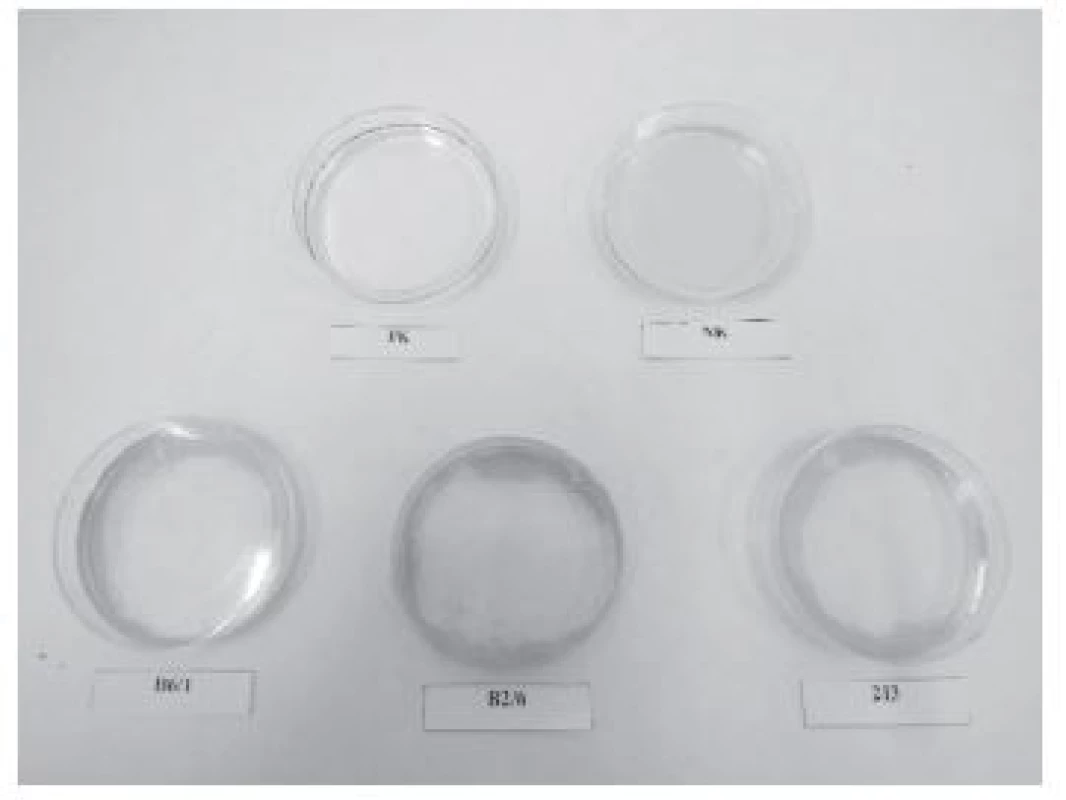
Antimikrobiálna a antibiofilmová aktivita BS
Efekt BS na rast a tvorbu biofilmu u referenčných kmeňov S. aureus CCM 3953 a P. mirabilis CCM 7188 bol sledovaný modifikovanou metódou podľa O’Toole a kol.10) nasledovne: získané množstvo BS (180 mg) bolo rozpustené v Tryptónovom sójovom bujóne (TSB; pH 7; Carl Roth GmbH, Germany) na výslednú koncentráciu 8,57 mg/ml. Štandardizovaná nočná kultúra referenčného kmeňa (Mc Farland 1) bola pridaná do takto pripraveného bujónu v pomere 100 : 1. Ako kontroly boli použité TSB s referenčným kmeňom bez BS a TSB s BS bez referenčného kmeňa. Do jamiek stripov (Greiner ELISA 8 Well Strips, Flat Bottom, Medium Binding; Cruinn Diagnostics Ltd., Dublin, Ireland) bolo pridaných 200 µl jednotlivých roztokov. Uzavreté stripy fixované v rámčekoch boli inkubované aeróbne v termostate 24 hodín pri teplote 37 ºC. Po inkubácii bola zmeraná optická denzita (Synergy TM 4 Multi-Mode Microplate Reader, BioTek, USA) pri vlnovej dĺžke 570 nm za účelom hodnotenia rastu referenčných kmeňov v prítomnosti BS. Následne bol supernatant odsatý a jamky 3-krát premyté deionizovanou vodou a vysušené pri izbovej teplote. Po vysušení boli jamky ofarbené 0,1% roztokom kryštálovej violete (200 µl) a ďalej inkubované pri izbovej teplote 30 minút. Po odstránení prebytočného farbiva boli jamky 3-krát premyté deionizovanou vodou a vysušené pri izbovej teplote 30 minút. Kryštálová violeť naviazaná na adherované bunky (biofilm) bola extrahovaná 200 µl 95% etanolu. Optická denzita roztoku bola meraná spektrofotometricky pri vlnovej dĺžke 570 nm. Na základe získaných hodnôt absorbancie bola za tvorbu biofilmu považovaná absorbancia vyššia ako 0,1. Kmene boli testované najmenej v troch nezávislých experimentoch, každý s 8 opakovaniami.
Štatistické vyhodnotenie
Pre vyhodnotenie výsledkov bola použitá jednorozmerná analýza rozptylu (ANOVA) s doplnkovým Tukeyho testom v štatistickom programe GraphPad Prism verzia 3.00.
Výsledky a diskusia
BS patria v súčasnosti k významným mikrobiálnym produktom, ktorých potenciálne využitie sa skúma v mnohých priemyselných a medicínskych odvetviach. Z toxikologického aj ekologického hľadiska predstavujú vhodnejšiu náhradu k aktuálne používaným syntetickým surfaktantom11). Vzhľadom na pomerne malé percento preskúmanej časti morských ekosystémov a tiež na extrémnejšie podmienky prostredia, ktorým sú baktérie v nich vystavené, sa predpokladá, že by morské baktérie mohli byť veľmi bohatým zdrojom nových BS. Navyše takto získané BS by mohli byť odolnejšie voči určitým vonkajším faktorom, akými sú napríklad teplota, salinita, hodnota pH alebo tlaku, ako BS získané z iných prírodných zdrojov. Predpokladá sa úzky vzťah medzi produkciou bioaktívnych metabolitov a procesmi adaptácie baktérií12).
Laktobacily produkujú rôzne metabolické produkty, ktoré majú antimikrobiálnu aktivitu, ako je napríklad kyselina mliečna, peroxid vodíka, bakteriocíny, bakteriocínové látky a tiež biosurfaktanty. Široká škála kmeňov Lactobacillus spp. produkuje rôzne typy BS13). Glykolipidy, lipopeptidy, látky podobné proteínu, fosfolipidy, mastné kyseliny a lipopolysacharidy produkované Lactobacillus spp. boli charakterizované viacerými výskumníkmi14–16). Jedným zo špecifických lipidových BS produkovaných len kmeňmi Lactobacillus je surlaktín. Ten je svojím mechanizmom pôsobenia podobný rhamnolipidom produkovaným Pseudomonas spp. a surfaktínom produkovaným Bacillus spp.17).
Na testovanie a skríning mikroorganizmov tvoriacich BS boli vyvinuté a úspešne aplikované rôzne metódy. Niektorými sa testuje prítomnosť povrchovej a medzipovrchovej aktivity, iné sa využívajú na meranie týchto aktivít. Ďalšou skupinou testov sú testy založené na hydrofóbnosti bunkového povrchu. Sú to nepriame metódy a je nimi možná rýchla identifikácia BS. Avšak hydrofóbnosť baktérií závisí od fyziologických aspektov (rastové podmienky, vek buniek). Medzi špecifické testy zaraďujeme CTAB agar plate test a test na hemolýzu, pretože nepatria medzi testy všeobecného skríningu baktérií tvoriacich BS18).
Oil spreading test sa môže využiť ako kvalitatívna metóda19). Princíp tejto metódy je založený na schopnosti BS meniť kontaktný uhol na rozhraní voda – olej. Priemer vzniknutej vyčírenej zóny na povrchu oleja koreluje s aktivitou povrchovo aktívnej látky. Táto metóda je rýchla a ľahko realizovateľná, nevyžaduje špecializované zariadenia a je potrebný len malý objem vzorky. Môže sa použiť, ak je aktivita a množstvo BS nízke. BS sú produkované buď na povrchu buniek, alebo extracelulárne do prostredia20). V našej práci boli izolované a testované BS viazané na povrchu buniek, ktoré boli extrahované jemným pretrepávaním do PBS. BS získané z testovaných kmeňov laktobacilov a morských baktérií vykazovali povrchovú aktivitu (tab. 1). U BS kmeňov S. luteola 3/22, Brevibacillus spp. 4/9, B. amyloliquefaciens 1/6K, L. reuteri B6/1 a L. fermentum 2I3 boli zaznamenané zóny vyčírenia v rozmedzí od 49 do 58 mm. Tieto hodnoty boli porovnateľné s hodnotou zistenou pri pozitívnej kontrole Tween 80 (60 mm), čo poukazuje na vysoké povrchovo aktívne vlastnosti testovaných BS. Nižšiu povrchovú aktivitu (veľkosť zón 22–35 mm) preukazovali BS z kmeňov Brevibacillus spp. 2/30, L. fermentum B2/6 a L. reuteri SL16. Namerané hodnoty boli vyššie ako tie, ktoré zistil Fracchia a kol.21) pri testovaní 12 vzoriek Lactobacillus sp. izolovaných z rôznych druhov čerstvého ovocia a zeleniny. Všetky vzorky preukazovali povrchovú aktivitu s veľkosťami zón vyčírenia od 5 do 15 mm. Na koncentrácii závislá povrchová aktivita bola popísaná u BS izolovaného z L. plantarum CFR 2194 s veľkosťou zón od 1,9 ± 0,28 do 3,4 ± 0,12 mm14), u BS z L. rhamnosus s veľkosťou zón od 6,8 ± 0,5 do 4,1 ± 0,1 mm a u BS z L. jensenii s veľkosťou zón od 7,6 ± 0,5 do 3,8 ± 0,2 mm20). Supernatanty z pomnožených kultúr Bacillus sp. a Pseudomonas sp. vykazovali povrchovú aktivitu s veľkosťou zón 4,0 mm22).
Table 1. Povrchová aktivita BS. Výsledky sú prezentované ako aritmetický priemer troch nameraných hodnôt ± smerodajná odchýlka 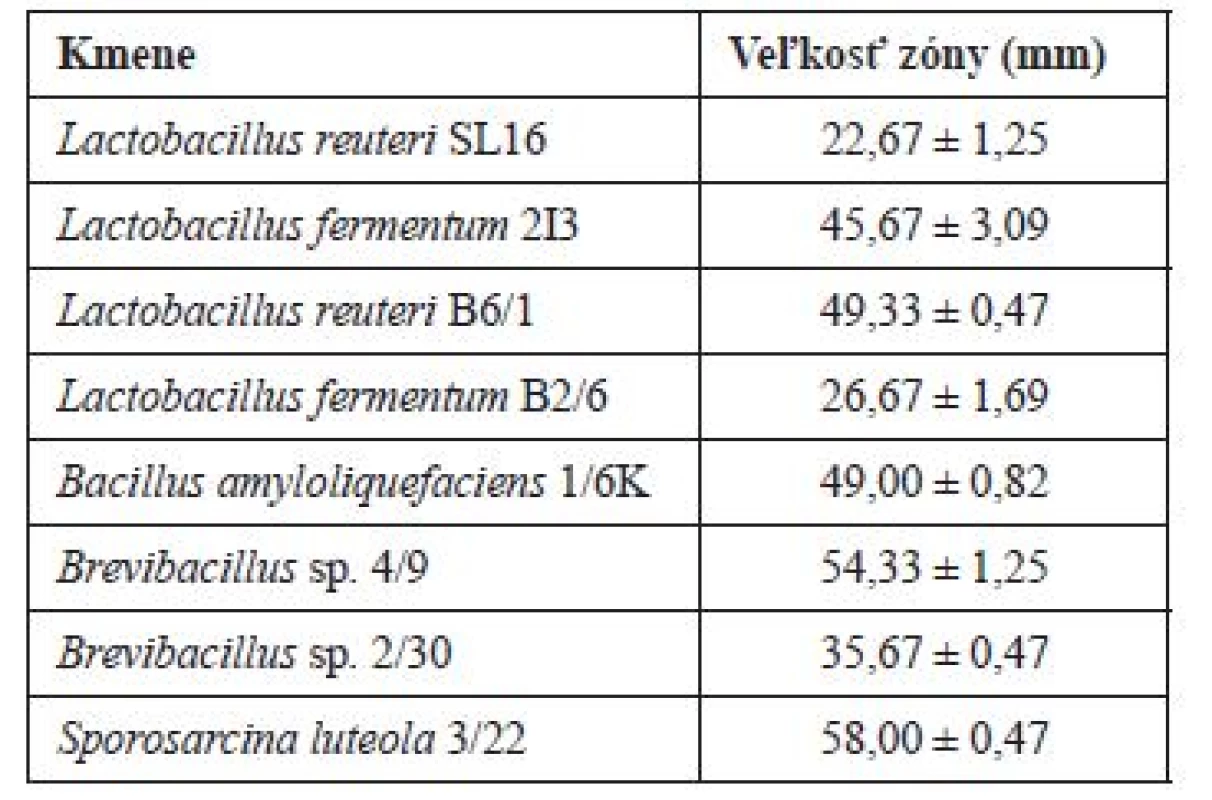
Po zistení existencie BS ako aktívnych produktov sa vedci zameriavali hlavne na ich antiadhezívnu a neskôr antimikrobiálnu aktivitu23). Až Sambanthamoorthy a kol.20) ako prví popísali u BS získaných z bunkového povrchu kmeňov L. jensenii a L. rhamnosus výraznú antimikrobiálnu, antiadhezívnu a antibiofilmovú aktivitu voči A. baumanii, E. coli a S. aureus pri koncentrácii BS 50 mg/ml. Nami izolované BS inhibovali tvorbu biofilmu u testovaných referenčných kmeňov (obr. 2 a 3). Zaznamenali sme signifikantne nižšiu tvorbu biofilmu u kmeňa S. aureus CCM 3953 a P. mirabilis CCM 7188 oproti kontrole (p < 0,001) v prítomnosti laktobacilových BS, ako aj BS získaných z morských baktérií. Pri porovnaní účinku jednotlivých BS, výraznejšia antibiofilmová aktivita (p < 0,001) bola zaznamenaná u BS z morských kmeňov (s výnimkou účinku BS získaného z kmeňa Brevibacillus sp. 2/30 voči P. mirabilis CCM 7188) oproti laktobacilovým BS. Antibiofilmová aktivita môže súvisieť s chemickou štruktúrou BS. Zatiaľ, čo laktobacily produkujú hlavne glykoproteíny, zástupcovia rodov Bacillus a Brevibacillus produkujú lipoproteíny s výraznou povrchovou aktivitou a antibiotickým potenciálom24). Ciandrini a kol.25) pozorovali antibiofilmovú aktivitu BS izolovaných z L. acidophilus, L. reuteri, L. rhamnosus a L. paracasei voči S. mutans a S. oralis. Zistili, že pri koncentrácii 10 mg/ml bola inhibícia tvorby biofilmu takmer 100 %. V našej práci použitá koncentrácia 8,57 mg/ml v prípade laktobacilových BS inhibovala tvorbu biofilmu 70–80 % a v prípade väčšiny BS z morských baktérií takmer 100 %. Avšak existujú aj také práce, kde bola použitá nižšia koncentrácia BS s porovnateľnou antibiofilmovou aktivitou. BS surfaktín izolovaný z B. subtilis s koncentráciou 100 µg/ml inhiboval tvorbu biofilmu E. coli a S. marscescens26) a s koncentráciou 66 µg/ml rozrušil 6-dňový biofilm L. pneumophila27). BS izolované z B. pumilus a ďalších morských baktérií inhibovali biofilm P. aeruginosa ATCC 10145 pri koncentrácii 100 µg/ml28). Glykolipidový BS produkovaný baktériou Brevibacterium casei MSA19 pri koncentrácii 30 μg/ml odstránil vytvorené biofilmy patogénnych mikroorganizmov C. albicans, E. coli, P. mirabilis, P. aeruginosa, K. pneumoniae, V. parahaemolyticus, V. hareyi, V. alginolyticus, V. alcaligenes, V. vulnificus, Thalassomonas sp., Alteromonas sp., Pseudoalteromonas sp., Pseudoalteromonas sp. a Ruegeria sp.29). Hassan a Mohammad30) v rámci svojej štúdie dokázali antibiofilmovú aktivitu lipopeptidových BS produkovaných Bacillus cereus. Na koncentrácii závislá inhibícia tvorby biofilmu bola pozorovaná pri gramnegatívnych baktériách (P. aeruginosa a Klebsiella pneumoniae). Pri grampozitívnej baktérii S. aureus bola zistená najvyššia aktivita pri nižších koncentráciách a s ich zvyšovaním sa zaznamenal, naopak, pokles inhibície.
Image 2. Antibiofilmová aktivita BS (c = 8,57 mg/ml) izolovaných z laktobacilov a morských baktérií voči S. aureus CCM 3953 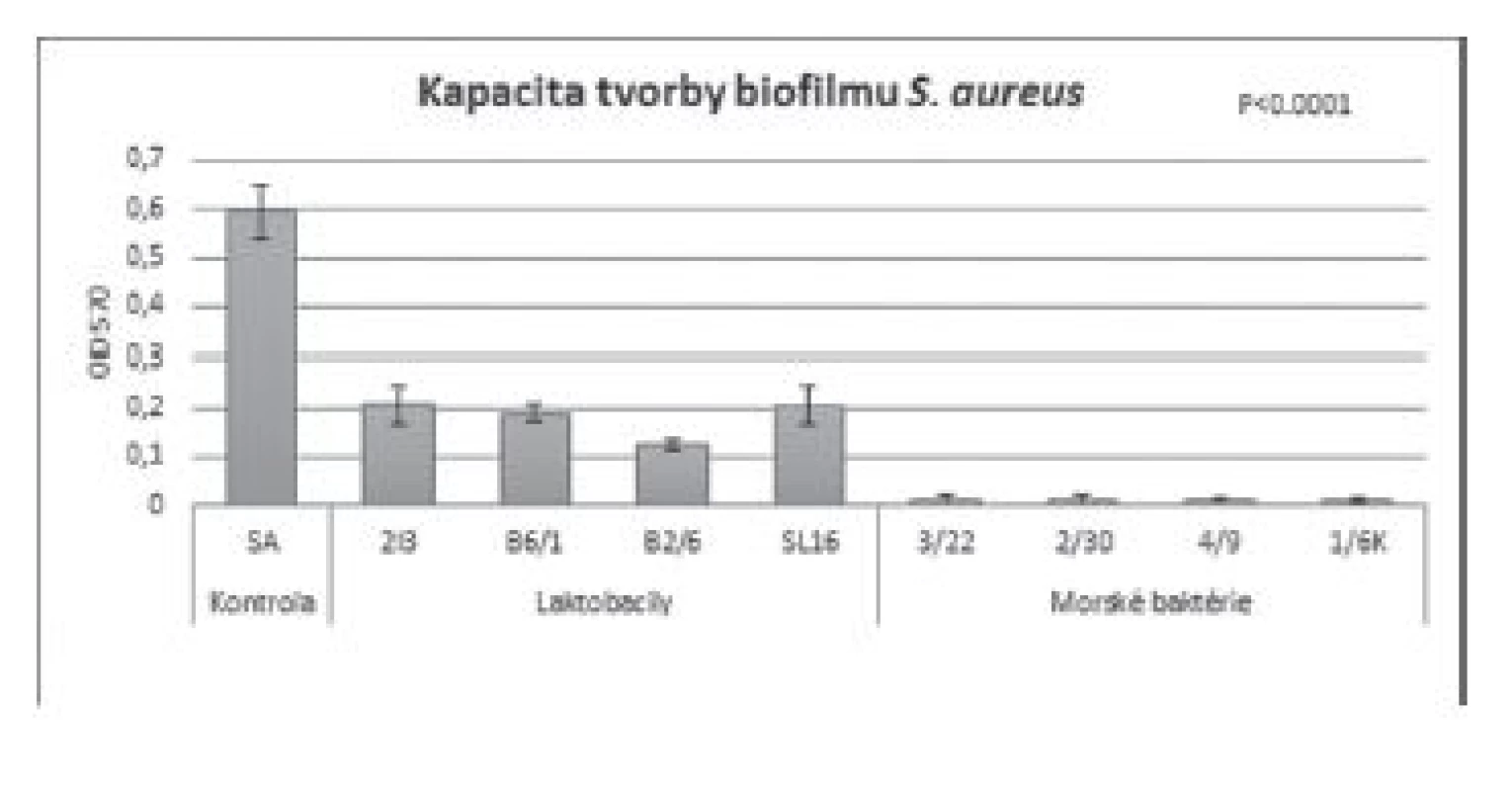
Image 3. Antibiofilmová aktivita BS (c = 8,57 mg/ml) izolovaných z laktobacilov a morských baktérií voči P. mirabilis CCM 7188 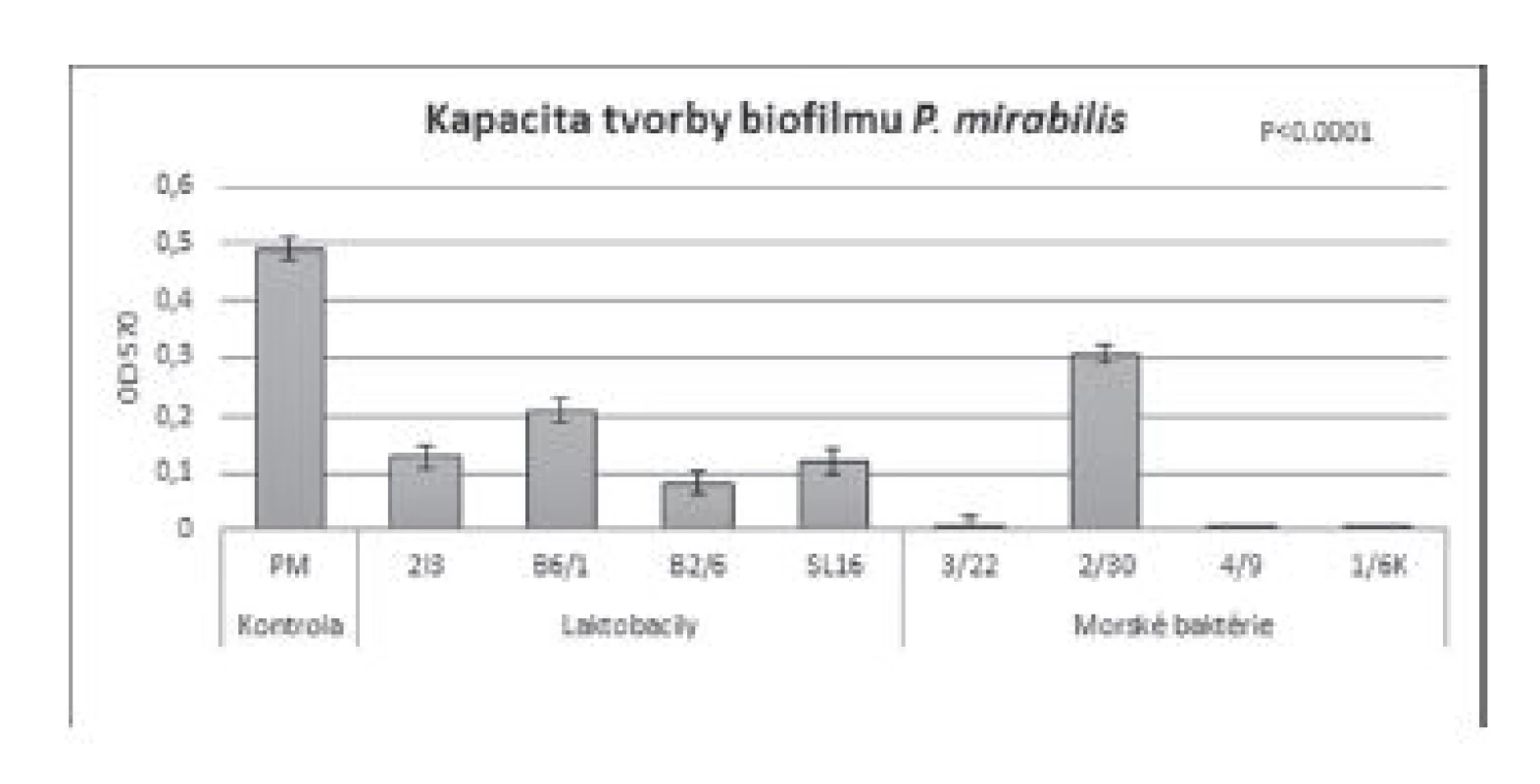
Exaktný mechanizmus antibiofilmového efektu nie je úplne objasnený. Najjednoduchší spôsob, ako vysvetliť antibiofilmovú aktivitu BS, by mohlo byť ich priame antimikrobiálne pôsobenie. Pravdepodobný mechanizmus antimikrobiálneho účinku je schopnosť BS interagovať s bunkovými membránami, vytvárať v nich póry, a tým viesť ku destabilizácii bunkového povrchu, narušeniu metabolických a transportných procesov a v konečnom dôsledku môžu spôsobiť až lýzu, čiže smrť bunky31). Avšak, inhibícia rastu nebola pozorovaná vo všetkých prípadoch32, 33). Podobne bolo v našich experimentoch zistené, že BS negatívne neovplyvnili rast S. aureus CCM 3953 (obr. 4). Naopak, pozitívne (p < 0,001) bol podporený jeho rast oproti kontrole, s výnimkou BS získaného z kmeňa Brevibacillus sp. 2/30. Tieto výsledky naznačujú, že nami zistený antibiofilmový efekt BS voči S. aureus CCM 3953 nie je pravdepodobne výsledkom antimikrobiálneho pôsobenia, ale môže súvisieť s antiadhezívnou aktivitou testovaných BS. Spôsob, akým BS ovplyvňujú interakcie medzi baktériou a povrchom (alebo interakcie bunka–bunka), je pravdepodobne úzko spätý so zmenami v povrchovom napätí a náboji bunkovej steny baktérie. BS môžu interagovať s fázovým rozhraním a ovplyvňovať adhéziu a odlúpnutie baktérií z povrchu. Interakcie BS s povrchom bunky a pevným substrátom závisí od chemických vlastností BS a povrchovej energii buniek a substrátu34). Viacerí autori uvádzajú pozitívny účinok BS produkovaných laktobacilmi na inhibíciu adhézie patogénov na biomateriáloch a bunkových povrchoch12, 15, 35). BS produkovaný B. circulans vykazoval antiadhezívnu aktivitu v koncentráciách medzi 0,1–10 mg/ml voči patogénom E. coli, M. flavus, P. vulgaris, S. marcescens, C. freundii, K. aerogenes, A. faecalis a S. Typhimurium. Pri najvyššej testovanej koncentrácii (10 mg/ml) bola mikrobiálna adhézia inhibovaná v rozmedzí od 84–89 % a biofilm všetkých testovaných patogénnych mikroorganizmov bol odstránený36). Obrázok 5 poukazuje na rozdielnosť vplyvu BS izolovaných z laktobacilov a morských baktérií na rast P. mirabilis. Zatiaľ, čo v prípade laktobacilových BS nebol inhibovaný jeho rast, BS morských baktérií, s výnimkou kmeňa Brevibacillus sp. 2/30, signifikantne (p < 0,001) inhibovali rast P. mirabilis oproti kontrole. Tieto výsledky korelujú s výsledkami Bernat a kol.37), ktorí taktiež zistili antimikrobiálnu aktivitu BS izolovaných z B. subtilis voči gramnegatívnym uropatogénnym kmeňom E. coli, E. cloacae, P. mirabilis, C. freundii. Naproti tomu, Das a kol.38) zistili, že BS izolovaný z B. circulans neselektívne inhiboval rast grampozitívnych aj gramnegatívnych bakteriálnych kmeňov. To je do značnej miery protichodné aj s predchádzajúcimi štúdiami o antimikrobiálnych účinkoch BS, pri ktorých sa uvádza, že lipopeptidové BS sú aktívne väčšinou proti grampozitívnym baktériám39, 40).
Image 4. Vplyv BS (c = 8,57 mg/ml) izolovaných z laktobacilov a morských baktérií na rast S. aureus CCM 3953 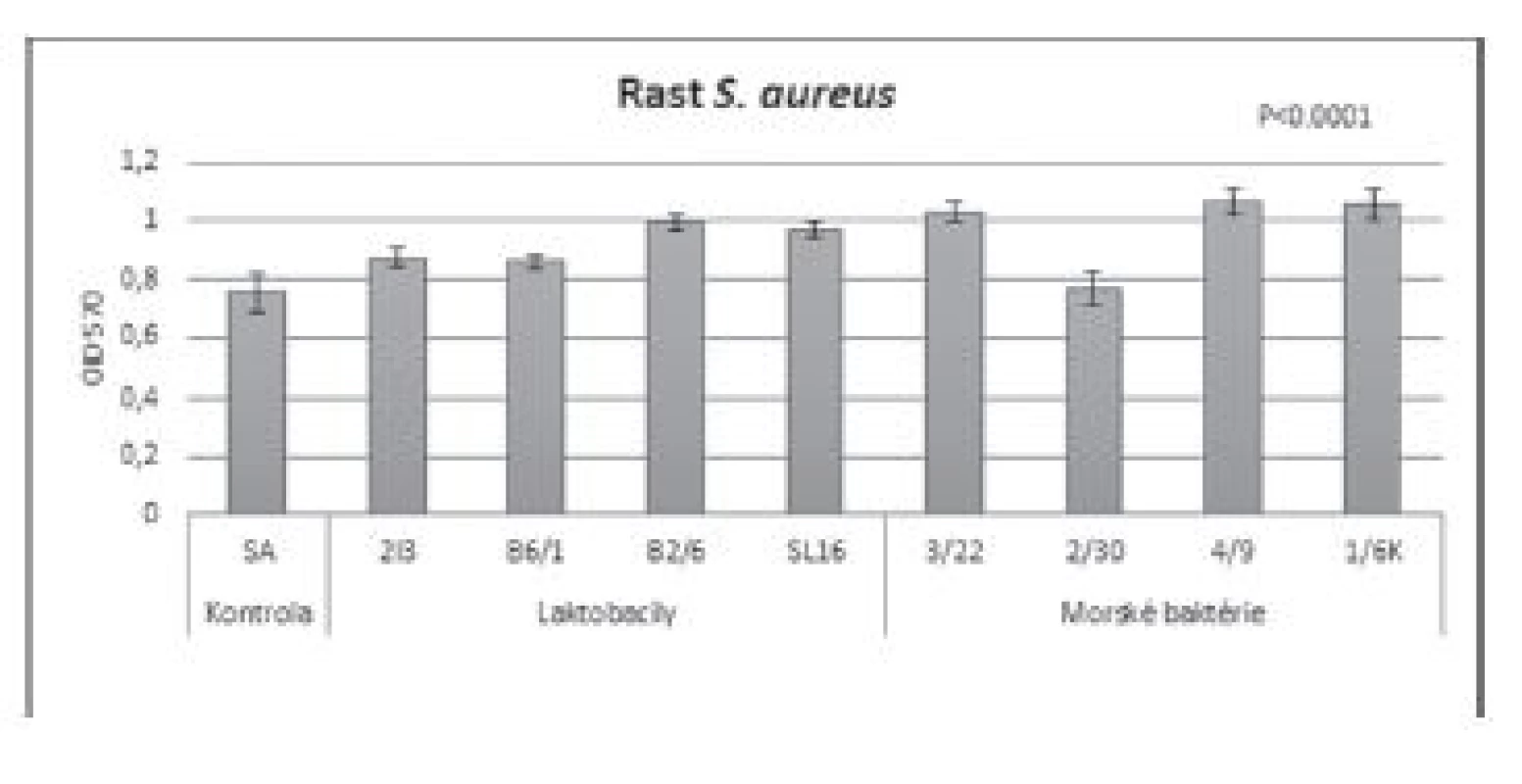
Image 5. Vplyv BS (c = 8,57 mg/ml) izolovaných z laktobacilov a morských baktérií na rast P. mirabilis CCM 7188 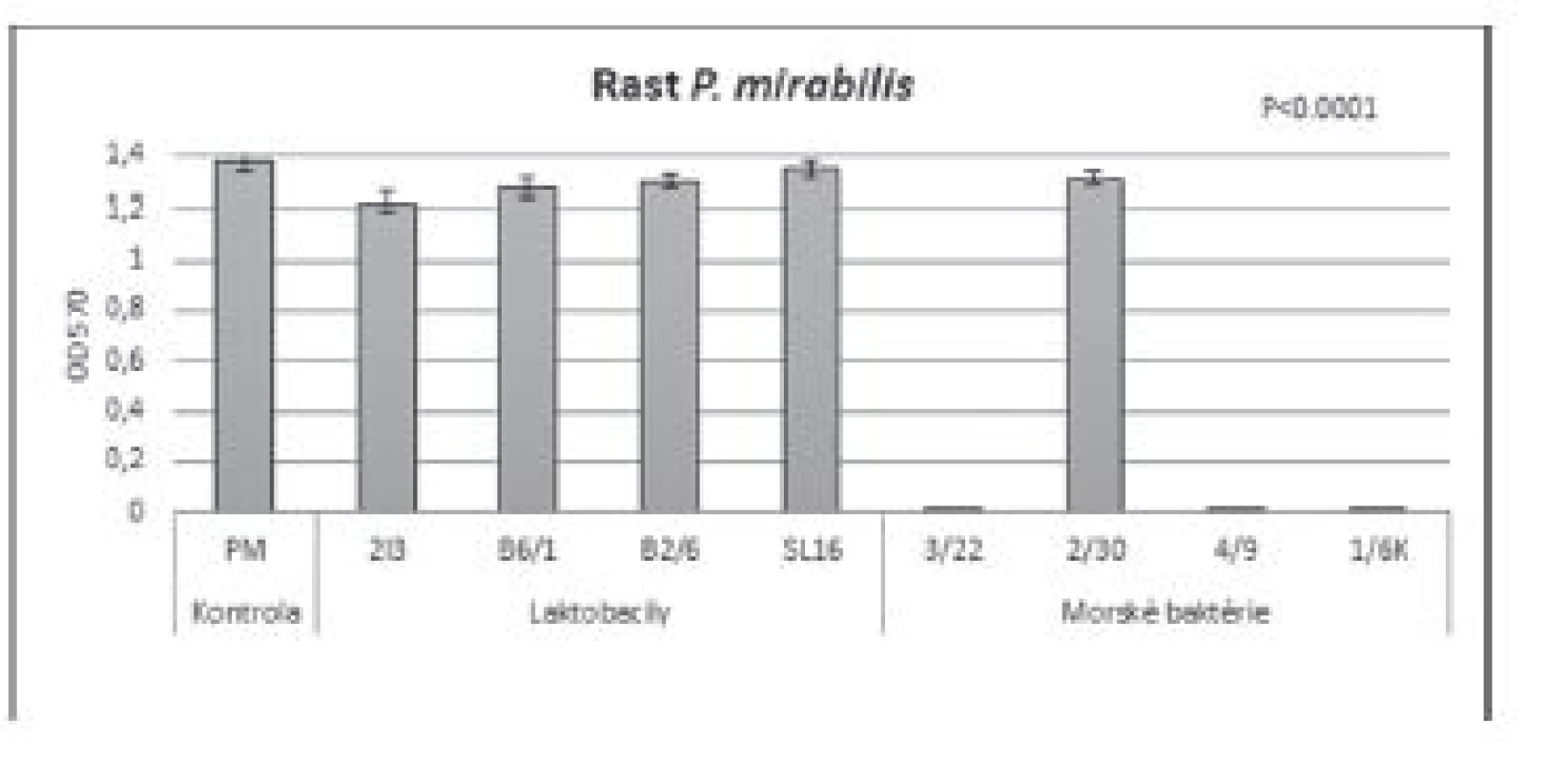
Záver
Dosiahnuté výsledky poukazujú na možný antibiofilmový potenciál BS získaných z črevných laktobacilov a baktérií izolovaných zo vzoriek mora. Bola potvrdená ich povrchová aktivita a schopnosť inhibovať tvorbu biofilmov patogénnych baktérií. Za biofilm-inhibičný efekt BS je pravdepodobne zodpovedný tak antimikrobiálny, ako aj antiadhezívny účinok testovaných BS, ktorý sa zdá byť závislý od typu BS a vlastností cieľovej mikrobiálnej bunky. Ďalšie štúdie si budú vyžadovať objasnenie mechanizmu antibiofilmového efektu aj na molekulárnej úrovni so zameraním na posúdenie zmien v expresii génov zodpovedných za syntézu bakteriálnych faktorov zapojených do procesu tvorby biofilmov.
Práca vznikla za podpory Agentúry na podporu výskumu a vývoja na základe zmluvy č. APVV-15-0377, č. APVV-16-0203 a projektu VEGA 1/0081/17.
Stret záujmov: žiadny.
Došlo 28. mája 2018 / Prijaté 10. júla 2018
PharmDr. Karolína Englerová (∗) • R. Nemcová
Univerzita veterinárskeho lekárstva a farmácie
Komenského 73, 041 81 Košice, SR
e-mail: karolina.englerova@student.uvlf.sk
E. Styková
Klinika koní, Univerzita veterinárskeho lekárstva a farmácie, Košice, SR
Sources
1. Donlan R. M., Costerton J. W. Biofilms, survival mechanisms of clinically relevant microorganisms. Clin. Microbiol. Rev. 2002; 15, 167–193.
2. Kurtz S., et al. Projections of primary and revision hip and knee arthroplasty in the United States from 2005 to 2030. J. Bone Joint Surg. Am. 2007; 89, 780–785.
3. Hamilton H., Jamieson J. Deep infection in total hip arthroplasty. Can. J. Surg. 2008; 51, 111–117.
4. Fracchia L., et al. Potential therapeutic applications of microbial surface-activecompounds. AIMS Bioeng. 2015; 2, 144–162.
5. Chung P. Y., Toh Y. S. Anti-biofilm agents: recent breakthrough against multi-drug resistant Staphylococcus aureus. Pathog. Dis. 2014; 70, 231–239.
6. Jennings E. M., Tanner R. S. Biosurfactant-producing bacteria found in contaminated and uncontaminated soils. Proceedings of the 2000 Conference on Hazardous Waste Research. 2000; 306, 299–306.
7. Rangarajan V., Ramkrishna S. An inexpensive strategy for facilitated recovery of metals and fermentation products by foam fractionation process. Colloids Surf. B. 2013; 104, 99–106.
8. Gudiña E. J., et al. Antimicrobial and antiadhesive properties of a biosurfactant isolated from Lactobacillus paracasei ssp. paracasei A20. Lett. Appl. Microbiol. 2010; 50(4), 419–424.
9. Morikawa M., Hirata Y., Imanaka T. A study on the structure–function relationship of the lipopeptide biosurfactants. Biochim. Biophys. Acta 2000; 1488, 211–218.
10. O’Toole G. A. et al. Genetic approaches to study of biofilms. Methods Enzymol. 1999; 310, 91–109.
11. Santos D. K. F. et al. Biosurfactants: multifunctional biomolecules of the 21st century. Int. J. Mol. Sci. 2016; 17, 401.
12. Gudiña E. J., Teixeira J. A., Rodrigues L. R. Biosurfactants produced by marine microorganisms with therapeutic applications. Mar. Drugs. 2016; 14, E38.
13. Satpute S. K., et al. Multiple roles of biosurfactants in biofilms. Curr. Pharm. Des. 2016; 22, 429–448.
14. Madhu A. N., Prapulla S. G. Evaluation and functional characterization of a biosurfactant produced by Lactobacillus plantarum CFR 2194. Appl. Biochem. Biotechnol. 2014; 172, 1777–1789.
15. Sharma D., et al. Production and structural characterization of Lactobacillus helveticus derived biosurfactant. The Scientific World J. 2014; 1–9.
16. Moldes A. B., et al. Partial characterization of biosurfactant from Lactobacillus pentosus and comparison with sodium dodecyl sulphate for the bioremediation of hydrocarbon contaminated soil. BioMed. Res. Int. 2013; 1–9.
17. Satpute S. K., et al. Biosurfactants from Lactobacilli species: properties, challenges and potential biomedical applications. J. Basic Microbiol. 2016; 56, 1–19.
18. Walter V., Syldatk C., Hausmann R. Screening concepts for the isolation of biosurfactant producing microorganisms. Adv. Exp. Med. Biol. 2010; 672, 1–13.
19. Płaza G. A., Zjawiony I., Banat I. M. Use of different methods for detection of thermophilic biosurfactant-producing bacteria from hydrocarbon-contaminated and bioremediated soils. J. Petrol. Sci. Eng. 2006; 50, 71–77.
20. Sambanthamoorthy K. et al. Antimicrobial and antibiofilm potential of biosurfactants isolated from lactobacilli against multi-drug-resistant pathogens. BMC Microbiol. 2014; 14(1), 197.
21. Fracchia L., et al. Lactobacillus-derived biosurfactant inhibits biofilm formation of human pathogenic Candida albicans biofilm producers. In: Mendez Vilas A (ed.) Current Research, Technology and Education Topics in Applied Microbiology and Microbial Biotechnology; Spain, 2010; 827–837.
22. Femi-Ola T. O., et al. Isolation and screening of biosurfactant bacteria from soil contaminated with domestic waste water. Brit. J. Environ. Sci. 2015; 3(1), 58–63.
23. Lin S. Biosurfactants: Recent advances. J. Chem. Tech. Biotech. 1996; 66(2), 109–120.
24. Rodrigues L., et al. Biosurfactants: potential applications in medicine. J. Antimicrob. Chemother. 2006; 57(4), 609–618.
25. Ciandrini E., et al. Characterization of biosurfactants produced by Lactobacillus. Appl. Microbiol. Biotechnol. 2016; 100(15), 6767–6777.
26. Moryl M., et al. Antimicrobial, antiadhesive and antibiofilm potential of lipopeptides synthesised by Bacillus subtilis, on uropathogenic bacteria. Acta Biochim. Pol. 2015; 62(4), 725–732.
27. Loiseau C., et al. Surfactin from Bacillus subtilis displays an unexpected anti-Legionella activity. Appl. Microbiol. Biotechnol. 2015; 99(12), 5083–5093.
28. Padmavathi A. R., Pandian S. K. Antibiofilm activity of biosurfactant producing coral associated bacteria isolated from Gulf of Mannar. Indian J. Microbiol. 2014; 54(4), 376–382.
29. Kiran G. S., Sabarathnam B., Selvin J. Biofilm disruption potential of a glycolipid biosurfactant from marine Brevibacterium casei. FEMS Immunol. Med. Microbiol. 2010; 59, 432–438.
30. Hassan S. S., Mohammad F. R. Effect of biosurfactant extracted from Bacillus sp. on biofilm formation by some pathogenic bacteria. World J. Exp. Biosci. 2015; 3, 139–145.
31. Carrillo C., et al. Molecular mechanism of membrane permeabilization by the peptide antibiotic surfactin. Biochim. Biophys. Acta 2003; 1611(1), 91–97.
32. Vesterlund S., et al. Staphylococus aureus adheres to human intestinal mucus but can be displaced by certain lactic acid bacteria. Microbiology 2006; 152, 1819–1826.
33. Walencka E., et al. The Influence of Lactobacillus acidophilus-derived surfactants on staphylococcal adhesion and biofilm formation. Folia Microbiol. 2008; 53, 61–66.
34. Banat I. M., De Rienzo M. A. D., Quinn G. A. Microbial biofilms: Biosurfactants as antibiofilm agents. Appl. Microbiol. Biotechnol. 2014; 98, 9915–9929.
35. Saravanakumari P., Mani K. Structural characterization of a novel xylolipid biosurfactant from Lactococcus lactis and analysis of antibacterial activity against multi-drug resistant pathogens. Bioresour. Technol. 2010; 101(22), 8851–8854.
36. Das P., Mukherjee S., Sen R. Antiadhesive action of a marine microbial surfactant. Colloids Surf. B. 2009; 71(2), 183–186.
37. Bernat P. et al. Lipid composition in a strain of Bacillus subtilis, a producer of iturin A lipopeptides that are active against uropathogenic bacteria. World J. Microbiol. Biotechnol. 2016; 32(10), 157.
38. Das P., Mukherjee S., Sen R. Antimicrobial potential of a lipopeptide biosurfactant derived from a marine Bacillus circulans. J. Appl. Microbiol. 2008; 104, 1675–1684.
39. Kitamoto D., et al. Surface-active propertiesand antimicrobial activities of mannosylerythritol lipids asbiosurfactants produced by Candida antarctica. J. Biotechnol. 1993; 29, 91–96.
40. Singh P., Cameotra S. S. Potential applications ofmicrobial surfactants in biomedical sciences. Trends Biotechnol. 2004; 22, 142–146.
Labels
Pharmacy Clinical pharmacology
Article was published inCzech and Slovak Pharmacy

2018 Issue 3-
All articles in this issue
- Nešpecifické zápalové ochorenia čreva: faktory podieľajúce sa na patogenéze
- Biosurfaktanty a ich úloha v inhibícii biofilm tvoriacich patogénnych baktérií
- Lékárna, lékárníci a léky v ghettu Terezín
- Imunomodulační aktivita etanolových extraktů z Galium verum L. herb.
- Výzkum chemického složení kůry Sorbus aucuparia
- Czech and Slovak Pharmacy
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nešpecifické zápalové ochorenia čreva: faktory podieľajúce sa na patogenéze
- Lékárna, lékárníci a léky v ghettu Terezín
- Biosurfaktanty a ich úloha v inhibícii biofilm tvoriacich patogénnych baktérií
- Imunomodulační aktivita etanolových extraktů z Galium verum L. herb.
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

