-
Medical journals
- Career
Lékový registr – trabectedin
Authors: K. Kubáčková 1; J. Fínek 2; R. Vyzula 3; M. Zvaríková 3; M. Vočka 4; S. Batko 1; J. Dreslerová 2; P. P. Lazarov 5; M. Lysý 6; Z. Ptáčková 7; V. Benešová 8; Z. Bortlíček 9; V. Kandrnal 9
Authors‘ workplace: Fakultní nemocnice v Motole, Praha 1; Fakultní nemocnice Plzeň 2; Masarykův onkologický ústav, Brno 3; Všeobecná fakultní nemocnice, Praha 4; Krajská nemocnice Liberec 5; Masarykova nemocnice Ústí nad Labem 6; Fakultní nemocnice Hradec Králové 7; Nemocnice Jihlava 8; Institut biostatistiky a analýz, MU Brno 9
Published in: Klin Onkol 2011; 24(6): 470-474
Category: Reports from Clinical Registries
Overview
Východiska:
Projekt Yondelis® (trabectedin) byl zahájen v lednu 2011 s cílem získat základní epidemiologické informace o pacientech se sarkomy měkkých tkání, o standardních postupech léčby a výsledcích léčby přípravkem trabectedin v běžné klinické praxi. Odbornou garanci nad projektem převzala Česká onkologická společnost ČSL JEP. Projekt reprezentativně pokrývá síť komplexních onkologických center, která se systematicky zabývají léčbou sarkomů měkkých tkání.Soubor pacientů a metody:
Do databáze bylo retrospektivně zařazeno 45 nemocných s diagnózou sarkomu měkkých tkání. Medián věku při zahájení terapie trabectedinem byl 51 let (23–72 let). V databázi se nejčastěji vyskytovali nemocní s leiomyosarkomem (35,6 %), synoviální sarkom se vyskytl u 13,3 % pacientů, liposarkom, maligní tumor periferních nervových pochev a blíže nespecifikované sarkomy byly zastoupeny každý u 6,7 % nemocných. Velikost větší než 5 cm dosáhlo 62,2 % sarkomů. Trabectedin byl podáván v dávce 1,5 mg/m2 1krát za 3 týdny. U 40 % nemocných byl podáván v II. linii léčby, u 35,6 % ve III. linii a u 24,4 % v linii IV. Výsledky: Medián podaných cyklů byl 4 (1–10 cyklů). Nejčastěji se vyskytujícím nežádoucím účinkem byla neutropenie u 28,9 % nemocných a elevace jaterních enzymů u 26,7 %. Celkem 73,8 % nemocných ukončilo léčbu pro progresi onemocnění. Léčebné odpovědi bylo dosaženo u 6,6 % nemocných (kompletní remise a parciální remise), u 26,7 % pacientů došlo ke stabilizaci onemocnění a u 53,3 % k progresi choroby. Medián celkového přežití (95% IS) je 11,7 měsíce (9,6; 13,8), medián přežití bez známek progrese (95% IS) 3 měsíce.Závěr:
Trabectedin je v současnosti doporučován onkologickými odbornými společnostmi jako druhá linie paliativní léčby u sarkomů měkkých tkání s prokázanou efektivitou především u liposarkomů a leiomyosarkomů s dobrým toxickým profilem.Klíčová slova:
sarkomy měkkých tkání – chemoterapie – trabectedin – léčbaVýchodiska
Cílem retrospektivního přehledu bylo získat základní epidemiologická data o pacientech se sarkomy měkkých tkání léčených trabectedinem v komplexních onkologických centrech v období 2008–2010 v podmínkách běžné klinické praxe. Trabectedin je látka původně izolovaná z mořského živočicha Ecteinascidia turbinata. Patří mezi alkylační činidla; mechanizmus jeho antiproliferačního účinku spočívá ve vazbě na DNA a interferenci s jejími reparačními procesy [1–4].
Soubor pacientů a metody
Údaje byly získány z databáze, do které byla anonymně konsekutivně ukládána data. Léčba i frekvence sledování byly v kompetenci zadávajícího lékaře, který do databáze zaznamenával informace o výsledcích a nežádoucích účincích léčby. Do databáze bylo zařazeno 45 nemocných léčených v období 2008–2010, z toho bylo 55,6 % žen a 44,4 % mužů. Medián věku při stanovení diagnózy byl 47 let (21–70 let) a 51 let (23–72 let) při zahájení terapie trabectedinem. Věkové rozložení při stanovení diagnózy a při zahájení léčby udává obr. 1. Dva nemocní před stanovením diagnózy sarkomu podstoupili radioterapii, u ostatních pacientů nebyl zaznamenán žádný rizikový faktor pro vznik sarkomů měkkých tkání, jako jsou známé genetické mutace, expozice k chemickým karcinogenům, chronický lymfedém či jiný známý rizikový faktor. Funkční stav pacienta byl hodnocen dle Karnofského indexu (KI). U 62,2 % nemocných byl KI 90–100 % a 26,7 % pacientů mělo KI 70–80 %. U 5 nemocných nebyl funkční stav uveden. Nejčastějším histologickým typem sarkomů v souboru byl leiomyosarkom u 35,6 % pacientů a synoviální sarkom u 13,3 %; liposarkom, maligní tumor periferních nervových pochev a blíže nespecifikované sarkomy byly zastoupeny u stejného počtu pacientů – 6,7 %. Výskyt dalších typů tumoru ukazuje tab. 1. U všech typů sarkomů byla diagnóza potvrzena histopatologicky, u 77,8 % byla doplněna imunohistochemickým vyšetřením a u 3,6 % sarkomů bylo provedeno molekulárně-genetické vyšetření.
Image 1. Věková struktura pacientů. 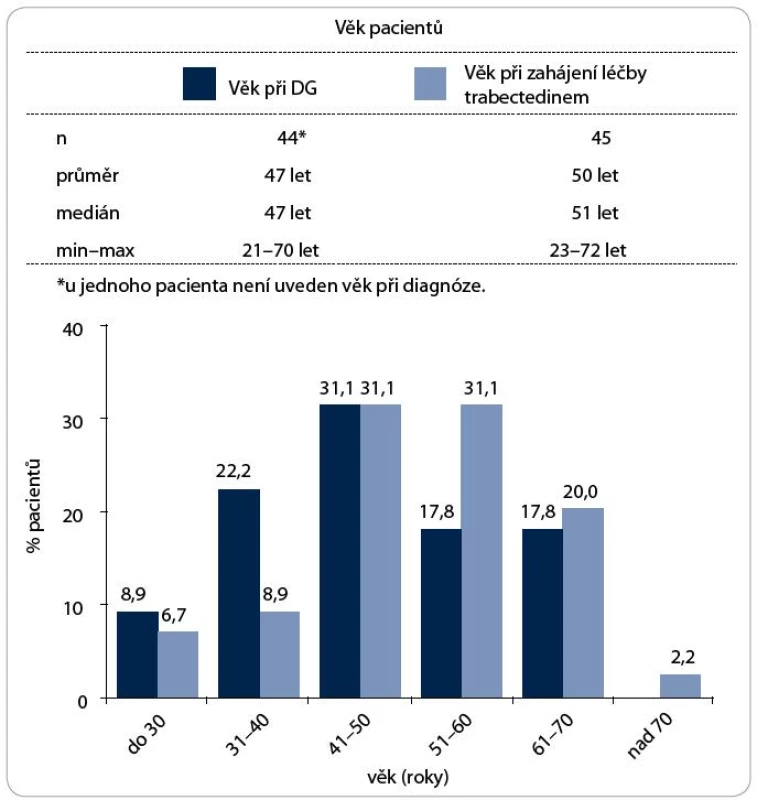
Table 1. Histologický typ nádoru. 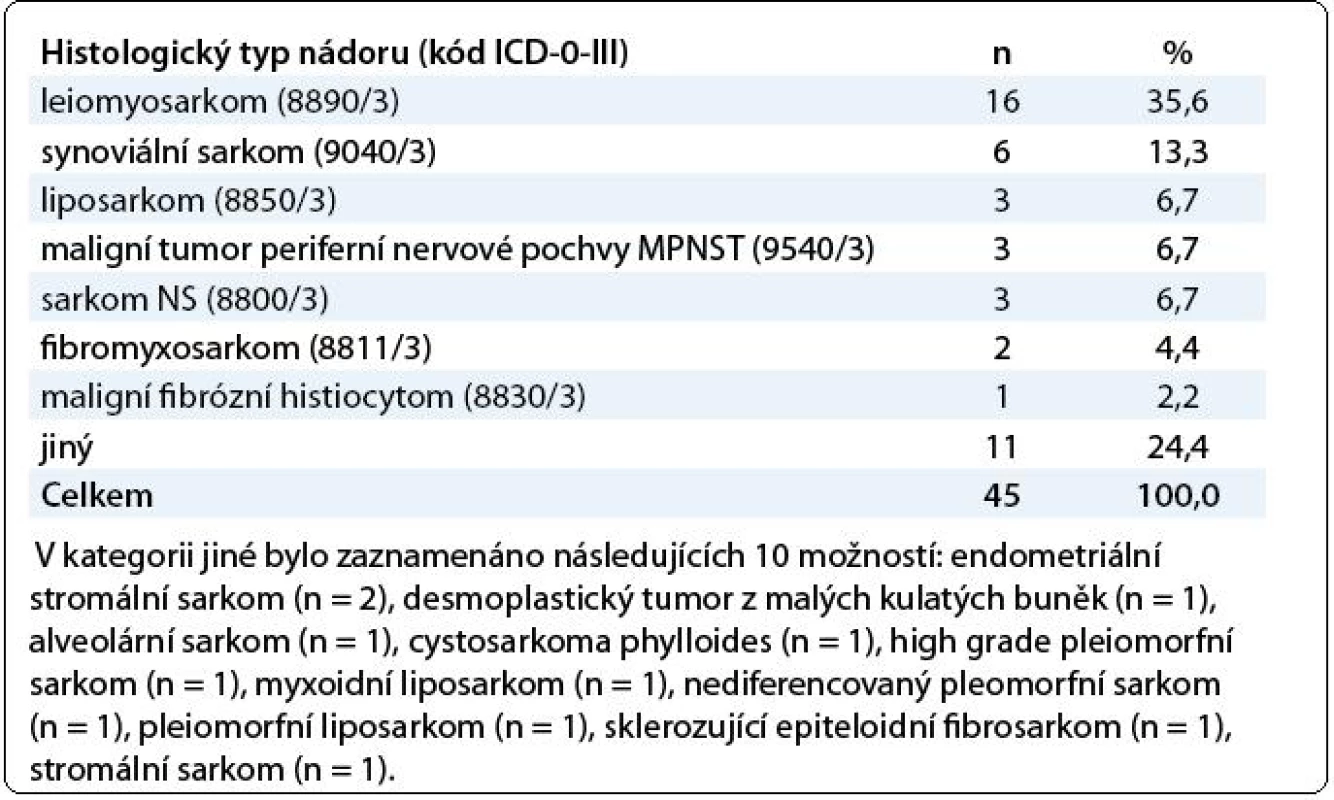
Téměř polovina sarkomů (48,9 %) byla diagnostikována s nádorovým grade 3, u 20 % byl stanoven nádorový grade 2, u 6,7 % grade 4 a u 4,4 % tumorů grade 1. U 26,7 % nemocných byl sarkom lokalizován na dolních končetinách, v 15,6 % se jednalo o sarkom dělohy, u 11,5 % byl tumor lokalizován v dutině břišní, u 6,7 % se nádor nacházel v retroperitoneu a u stejného počtu v oblasti hlavy a krku. V době primární diagnózy bylo 17,8 % nádorů uloženo povrchově nad superficiální facií, v hloubce bylo lokalizováno 48,9 % tumorů a u 33,3 % nemocných nebyla informace o uložení relevantní. U 13,3 % nemocných byl primárně diagnostikován tumor o velikosti 2–5 cm, u 37,8 % nemocných byl tumor velikosti 6–10 cm, 24,4 % nemocných bylo diagnostikováno s tumorózní rezistencí přesahující 10 cm a u stejného procenta nemocných nebyla velikost primárního tumoru určena. S klinickými projevy onemocnění zahájilo léčbu 80 % nemocných, 20 % nemocných bylo asymptomatických. 63,9 % nemocných bylo prezentováno s klinicky manifestní progredující tumorózní rezistencí, u 33,3 % nemocných se tumorózní proces projevoval tlakem na lokální struktury, u 3 nemocných bylo jediným příznakem gynekologické krvácení, u dvou dušnost a ulcerace.
U 53,7 % pacientů byla provedena kompletní resekce tumoru v době diagnózy, u 46,4 % nebyl radikální chirurgický výkon možný. V databázi sledovaných pacientů byla léčba trabectedinem zahájena u 40 % nemocných ve II. linii paliativní chemoterapie, u 35,6 % ve III. linii a u 24,4 % v linii IV. Trabectedin byl podáván v dávce 1,5 mg/m2 ve 24hodinové kontinuální infuzi do centrálního žilního řečiště v 3týdenním intervalu. Medián podaných cyklů byl 4 (rozmezí 1–10) a medián délky léčby byl 10 týdnů (rozmezí 1–38 týdnů) – viz obr. 2. Léčba trabectedinem byla zahájena u 37,8 % pacientů s KI 90–100 %, 48,9 % nemocných mělo KI 70–80 %, 13,3 % nemocných mělo KI 50–60 %. V době zahájení léčby trabectedinem bylo 95,6 % nemocných ve IV. stadiu onemocnění, pouze 4,4 % mělo stadium III. Přežití pacientů bylo hodnoceno metodikou podle Kaplana a Meiera.
Image 2. Počet cyklů léčby a celková délka léčby. 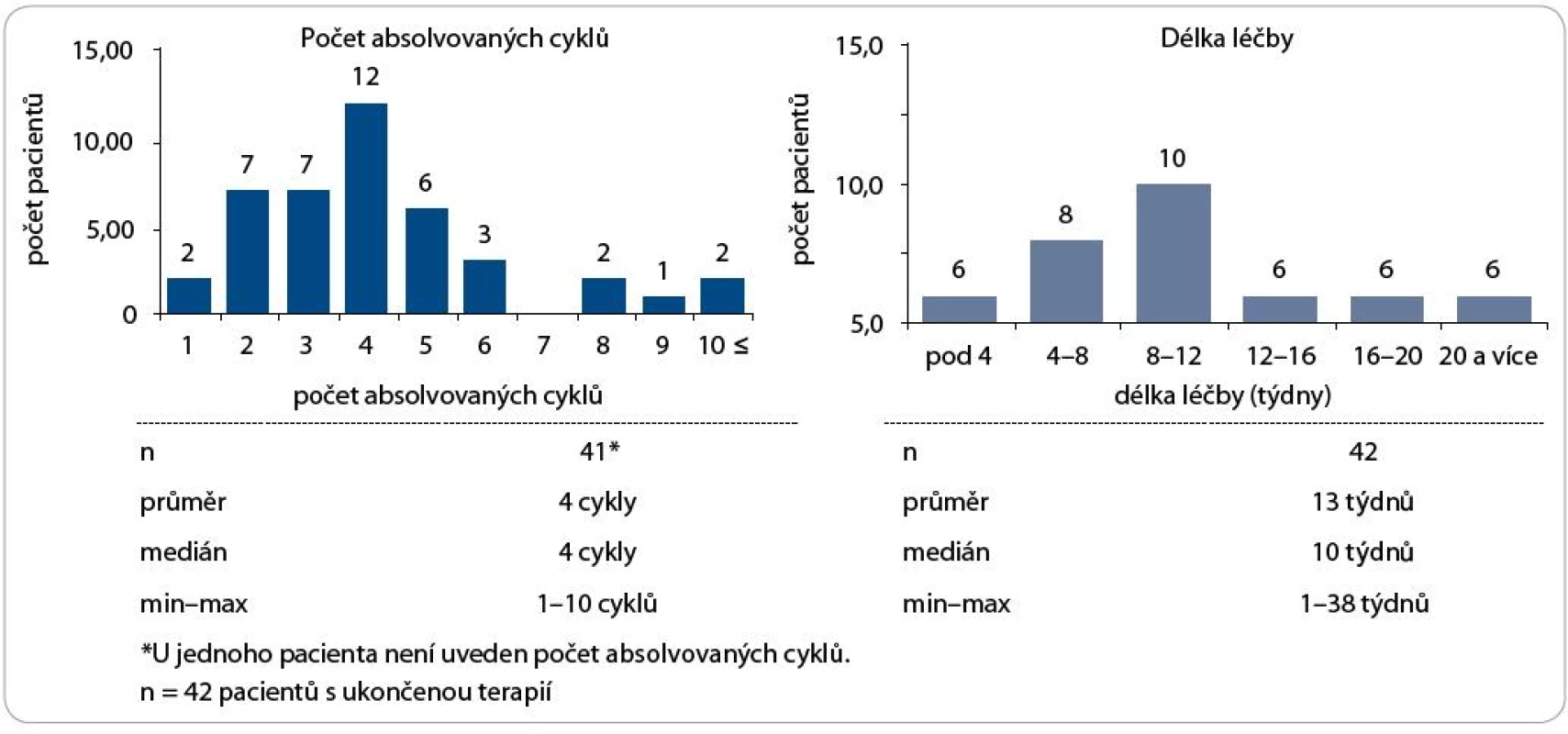
Výsledky léčby trabectedinem
Léčebné odpovědi bylo dosaženo u 6,6 % nemocných (kompletní remise a parciální remise), u 26,7 % nemocných byla zaznamenána stabilizace onemocnění (tab. 2). Medián celkového přežití (95% IS) byl 11,7 měsíce (9,6; 13,8) a medián doby do progrese (95% IS) 3 měsíce (2,4; 3,6). Celkové přežití v jednom roce (95% IS) bylo 49,4 % (31,7; 67,1), v 18 měsících (95% IS) přežívalo 32,3 % (14,1; 50,4). Ve 3 měsících bylo bez progrese onemocnění 48,4 % (32,9; 63,9) nemocných, v 6 měsících bez progrese onemocnění přežívalo 19,2 % (6,1; 32,3) nemocných (obr. 3). V době analýzy dat byla u 73,8 % nemocných léčba ukončena pro progresi onemocnění, u 6,7 % léčba pokračovala, 48,9 % nemocných zemřelo a 40 % žilo, u 5 nemocných nebyl stav znám.
Table 2. Nejlepší dosažená léčebná odpověď na léčbu trabectedinem. 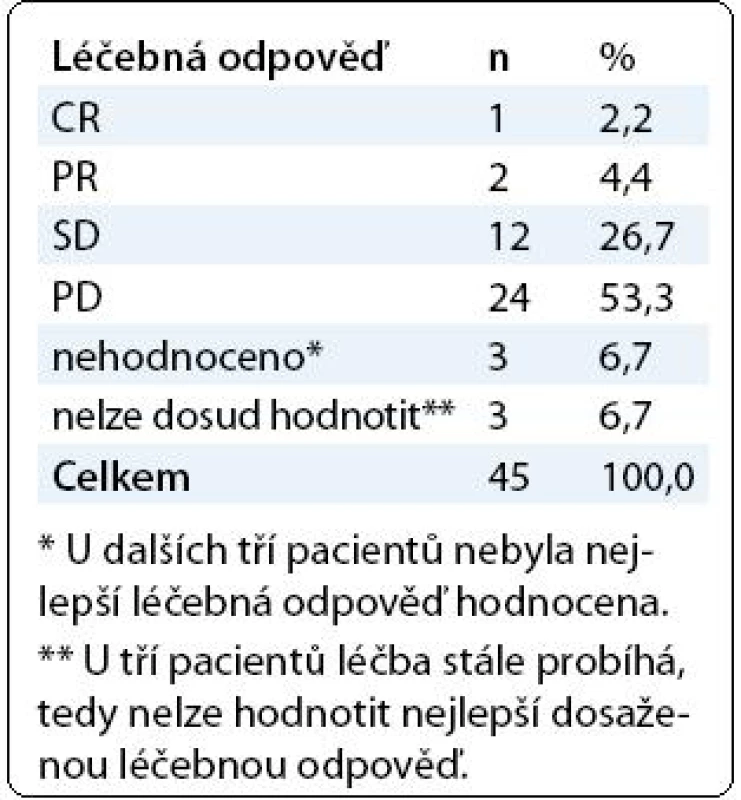
Image 3. Celkové přežití a přežití bez známek progrese. 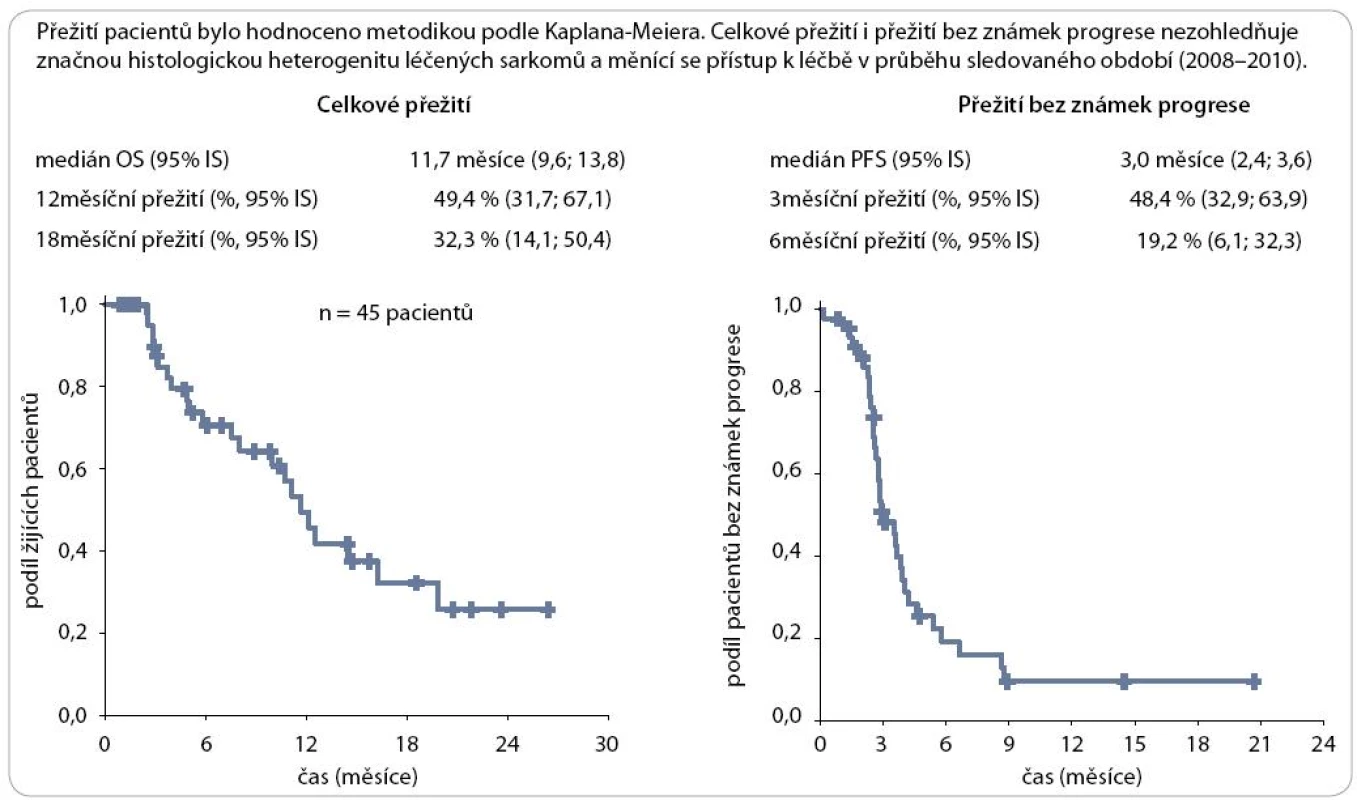
Nejčastěji se vyskytujícím nežádoucím účinkem byla neutropenie u 28,9 % nemocných, elevace jaterních enzymů u 26,7 %, snížení renálních testů u 4,4 % a anémie a trombocytopenie u 2,2 % nemocných.
Diskuze
Sarkomy měkkých tkání představují značně heterogenní skupinu vzácných maligních onemocnění. Určení histologického typu nádoru je jednou z klíčových podmínek pro správnou volbu léčebného algoritmu. Řada autorů doporučuje doplnění histologického a imunohistochemického vyšetření ke zpřesnění diagnostiky dalšími metodikami, jako jsou například molekulárně-genetická vyšetření [5–8]. Doporučováno je též druhé čtení na specializovaných pracovištích, která se systematicky věnují diagnostice sarkomů. Dle údajů Národního onkologického registru se incidence sarkomů měkkých tkání v České republice pohybovala v letech 2000–2008 v rozmezí 3,26–3,59 případu na 100 000 obyvatel za rok [9]. Z hlediska incidence není rozdíl v populaci mužů a žen. V databázi trabectedinu mírně převažovaly ženy (55,6 %) nad muži (44,4 %). V České republice se sarkomy měkkých tkání vyskytují nejčastěji mezi 50. a 70. rokem věku. Medián věku pacientů při stanovení diagnózy v našem souboru byl 47 let, v době zahájení terapie trabectedinem byl 51 let, tedy odpovídající věkovému rozmezí výskytu sarkomů. Léčba generalizovaných sarkomů měkkých tkání je paliativní, jejím základním cílem je zpomalení růstu nádoru, zmírnění symptomů onemocnění a zlepšení kvality života. Medián přežívání v době diagnózy metastatického onemocnění je 12 měsíců, pouze 20–25 % nemocných přežívá 2 roky. Zlatým standardem první linie paliativní chemoterapie je doxorubicin. U vybrané skupiny nemocných v dobrém klinickém stavu, kde chceme dosáhnout rychlého efektu léčby, je možná kombinovaná terapie doxorubicinu s ifosfamidem. Trabectedin byl v roce 2007 schválen agenturou EMA pro léčbu pokročilých sarkomů měkkých tkání u nemocných, u nichž selhala léčba antracykliny či ifosfamidem, nebo pro pacienty, kteří nejsou vhodní pro tuto terapii [10]. Data o jeho účinnosti byla doložena pro leiomyosarkomy a liposarkomy na základě randomizované studie fáze II srovnávající účinnost a bezpečnost dvou různých léčebných schémat u pacientů po selhání předchozí terapie antracykliny a ifosfamidem [11]. Leiomyosarkom byl v našem souboru nemocných léčených trabectedinem nejčastějším typem sarkomu. Výsledky léčby trabectedinem u všech typů sarkomů v databázi jsou srovnatelné s výsledky v registrační studii – přežití bez známek progrese onemocnění 3 měsíce, v registrační studii 3,7 měsíce, medián celkového přežití 11,7 měsíce ve srovnání s 13,9 měsíce v randomizované registrační studii. Výskyt nežádoucích účinků byl zaznamenán u 46,7 % nemocných a pouze u dvou nemocných se jednalo o závažné nežádoucí účinky. Nežádoucí účinky nebyly důvodem k ukončení terapie trabectedinem. Ve shodě se známým toxickým profilem trabectedinu byla nejčastěji zaznamenaným nežádoucím účinkem neutropenie a elevace jaterních enzymů. Žádný pacient neukončil léčbu pro toxicitu. Dle doporučení České onkologické společnosti je trabectedin indikován k léčbě liposarkomů, leiomyosarkomů a synovialosarkomů po selhání terapie doxorubicinem v kombinaci či bez předléčení ifosfamidem [12]. Dle doporučení ESMO (European Society of Medical Oncology) je trabectedin možnou volbou pro II. linii léčby u leiomyosarkomů a liposarkomů, s pozorovanou léčebnou odpovědí u myxoidních liposarkomů a synoviálních sarkomů [13]. Během našeho tříletého sledování je patrný měnící se trend zahájení léčby trabectedinem. Zatímco v roce 2008, kdy získal registraci a jeho dostupnost byla omezená, byl trabectedin nasazován převážně ve třetí či další linii; v roce 2010 již byla léčba trabectedinem zahájena u 55,6 % pacientů v rámci druhé linie léčby. Tato skutečnost značně komplikuje provedenou analýzu přežití a determinuje dosažitelnost výsledků. Při indikaci léčby trabectedinem bychom měli zvažovat histologický typ sarkomu a celkový stav nemocného s jeho komorbiditami tak, aby mohlo být dosaženo maximálního efektu [14–16].
Závěr
Trabectedin je registrován pro léčbu sarkomů měkkých tkání po selhání doxorubicinu a ifosfamidu či pro nemocné, kteří nejsou indikováni k této léčbě. Lékový registr trabectedinu zahrnuje 45 nemocných. Výsledky léčby i toxický profil trabectedinu jsou srovnatelné s výsledky registrační studie. Snahou ČOS je koncentrovat léčbu pacientů se sarkomy měkkých tkání do komplexních onkologických center, která mají s léčbou tohoto onemocnění zkušenosti a jsou schopna zajistit multidisciplinární přístup, který léčba těchto vzácných nádorů vyžaduje. Jenom tak může být zaručena správná indikace léčby.
MUDr. Vít Kandrnal
Institut biostatistiky a analýz
MU Brnoa
Kotlářská 2
611 37 Brno
e-mail: kandrnal@iba.muni.cz
Obdrženo: 18. 7. 2011
Přijato: 8. 11. 2011
Sources
1. Carter NJ, Keam SJ. Trabectidin: a review of its use in soft tissue sarcoma and ovarian cancer. Drugs 2010; 70(3): 355–376.
2. Chuk MK, Balis FM, Fox E. Trabectedin. Oncologist 2009; 14(8): 794–799.
3. Schöffski P, Dumez H, Wolter P et al. Clinical impact of trabectedin (ecteinascidin-743) in advanced/metastatic soft tissue sarcoma. Expert Opin Pharmacother 2008; 9(9): 1609–1618.
4. Blay JY, von Mehren M, Samuels BK et al. Phase I combination study of trabectidin and doxorubicin in patients with soft-tissue sarcoma. Clin Cancer Res 2008; 14(20): 6656–6662.
5. Clark MA, Fisher C, Judson I et al. Soft-tissue sarcomas in adults. N Engl J Med 2005; 353(7): 701–711.
6. Hogendoorn PC, Collin F, Daugaard S et al. Changing concepts in the pathological basis of soft tissue and bone sarcoma treatment. Eur J Cancer 2004; 40(11): 1644–1654.
7. Veselý K. Histopatologická diagnostika nádorů měkkých tkání. Onkologie 2010; 4(5): 293–296.
8. Cormier JN, Pollock RE. Soft tissue sarcomas. CA Cancer J Clin 2004; 54(2): 94–109.
9. Dušek L, Mužík J, Kubásek M et al. Epidemiologie zhoubných nádorů v České republice [online]. Masarykova univerzita 2005 [cit. 2011-4-27]. Dostupný z http://www.svod.cz.
10. Yondelis Summary of Product Characteristics SPC. EMA 2010. Available from: http://www.ema.europa.eu/docs/cs_CZ/document_library/EPAR_Product_Information/human/000773/WC500045832.pdf.
11. Demetri GD, Chawla SP, von Mehren M et al. Efficacy and safety of trabectedin in patients with advanced or metastatic liposarcoma or leiomyosarcoma after failure of prior anthracyclines and ifosfamide: results of a randomized phase II study of two different schedules. J Clin Oncol 2009; 27(25): 4188–4196.
12. Vyzula R et al. Zásady cytostatické léčby maligních onkologických onemocnění. 13. vydání. Brno: Masarykův onkologický ústav 2011.
13. Casali PG, Blay JY. ESMO/CONTICANET/EUROBONET Consensus Panel of Experts. Soft tissue sarcomas: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2010; 21 (Suppl 5): v198–v203.
14. Schöffski P, Taron M, Jimeno J et al. Predictive impact of DNA repair functionality on clinical outcome of advanced sarcoma patients treated with trabectedin: a retrospective multicentric study. Eur J Cancer 2011; 47(7): 1006–1012.
15. Ray-Coquard I. An increasing role for trabectidin in gynecological cancers: efficacy in uterine sarcomas. Int J Gynecol Cancer 2011; 21 (10 Suppl 1): S3–S5.
16. Scurr M. Histology-driven chemotherapy in soft tissue sarcomas. Curr Treat Options Oncol 2011; 12(1): 32–45.
Labels
Paediatric clinical oncology Surgery Clinical oncology
Article was published inClinical Oncology

2011 Issue 6-
All articles in this issue
- Plazminogen aktivátor systém a jeho klinický význam u pacientů s nádorovým onemocněním
- Castlemanova choroba
- Naše päťročné výsledky in vitro testovania chemorezistencie u onkologických pacientov
- Neskoré následky u pacientov liečených alogénnou transplantáciou kmeňových krvotvorných buniek
- Použití chemoterapie v kombinaci s cílenou biologickou léčbou u diseminovaného kolorektálního karcinomu: kazuistika dlouhodobé a výrazné klinické odpovědi
- Lékový registr – trabectedin
- Pozitronová emisní tomografie v diagnostice a sledování pacientů s neseminomovými germinálními nádory
- Prediktivní hodnota ultrazvukových parametrů, CA-125 a indexu rizika malignity u pacientek s karcinomem ovarií
- Aktuálne charakteristiky deskriptívnej epidemiológie nádorov žalúdka v Slovenskej republike v kontexte medzinárodného porovnania
- Dlouhodobé sledování pacienta s eozinofilním granulomem žebra
- HER2 pozitivní T1N0M0 tumor: Čas pro změnu?
- Clinical Oncology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Castlemanova choroba
- Dlouhodobé sledování pacienta s eozinofilním granulomem žebra
- Lékový registr – trabectedin
- Prediktivní hodnota ultrazvukových parametrů, CA-125 a indexu rizika malignity u pacientek s karcinomem ovarií
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

