-
Medical journals
- Career
Moderní trendy v léčbě dlouhodobé perzistující fibrilace síní
Authors: A. Bulava 1,2; A. Mokráček 3
Authors‘ workplace: Kardiologické oddělení, Kardiocentrum, Nemocnice České Budějovice 1; ZSF JU v Českých Budějovicích 2; Kardiochirurgické oddělení, Kardiocentrum, Nemocnice České Budějovice 3
Published in: Kardiol Rev Int Med 2014, 16(3): 185-190
Category: Cardiology Review
Overview
Fibrilace síní představuje v moderní populaci stále větší medicínský i socioekonomický problém. Poslední desetiletí zaznamenalo výrazný rozmach nefarmakologické léčby fibrilace síní. Radiofrekvenční katetrová ablace získala v léčbě této arytmie významnou pozici obzvláště tam, kde selhala léčba antiarytmiky, a v určitých případech i jako léčba první volby dle preference pacienta. Neuspokojivá úspěšnost prvního ablačního výkonu, zejména u dlouhodobě perzistující formy fibrilace síní, vedla k rozvoji chirurgických miniinvazivních a především hybridních přístupů v léčbě této arytmie. Autoři v článku shrnují dosavadní literární data o těchto kombinovaných přístupech a uvádějí i vlastní zkušenosti.
Klíčová slova:
radiofrekvenční katetrová ablace – perzistující fibrilace síní – hybridní výkonyFibrilace síní (FS) představuje ve stárnoucí populaci západního světa stále větší medicínský i socioekonomický problém. Zatímco starší odhady hovořily o prevalenci kolem 1 % obecné populace [1], novější výzkumy potvrdily, že vzhledem k poměrně častému asymptomatickému průběhu této arytmie může jít jen o „špičku ledovce“ a výskyt v populaci se blíží spíše 4 – 5 % [2]. Původní studie výskyt FS zkoumaly na podkladě jednorázového EKG záznamu nebo krátkých holterovských EKG. S rozvojem poznání FS bylo zjištěno, že v obecné populaci je patrně většina paroxyzmů FS asymptomatická nebo oligosymptomatická. Např. ve studii ASSERT byl výskyt FS monitorován u více než 2 500 pacientů ve věku nad 65 let s hypertenzí za použití recentně implantovaného kardiostimulátoru nebo kardioverteru ‑ defibrilátoru. Během tříměsíčního sledování byla u 10 % jedinců zaznamenána asymptomatická epizoda síňové frekvence > 190/ min trvající po dobu alespoň 6 min [3]. Klinicky vnímaná FS byla v témže období zachycena pouze u 0,28 % pacientů. Obecně se výskyt arytmie zvyšuje s věkem (graf 1). Zatímco v populaci mladší 40 let se arytmie vyskytuje jen v řádu menším než desetiny promile, v populaci osmdesátníků je to již více než 10 %.
Graph 1. Prevalence FS podle jednotlivých věkových skupin. V každé věkové skupině je výskyt arytmie nižší u žen než u mužů (adaptováno podle studie ATRIA [1]). ![Prevalence FS podle jednotlivých věkových skupin. V každé věkové skupině je výskyt arytmie nižší u žen než u mužů (adaptováno podle studie ATRIA [1]).](https://pl-master.mdcdn.cz/media/image/a27740df659c189f05131e1344c828e4.jpg?version=1537795670)
S rozvojem moderní nefarmakologické léčby FS došlo i k významnému posunu v indikačních kritériích [4]. Základem léčby je sice stále farmakoterapie, ale vzhledem k neuspokojivým výsledkům léčby farmaky se do popředí dostává radiofrekvenční katetrová ablace (RFA) (schéma 1). Výsledky srovnávacích studií jednoznačně ukázaly [5], že úspěšnost farmakologické léčby je významně nižší než u léčby katetrovou ablací (graf 2). Na druhé straně je třeba připustit, že výsledky katetrové léčby FS nejsou optimální a jsou také striktně závislé na zkušenosti centra, manuální dexteritě operatéra, použité technologii a nakonec na intenzitě sledování pacientů [6]. Nejpřesnější hodnocení úspěšnosti léčby je za pomocí kontinuálních implantabilních záznamníků (např. Biomonitor, záznamové zařízení firmy Biotronik s možností telemedicínského sledování EKG). Pro svou invazivitu a finanční náročnost však implantabilní záznamníky nejsou mimo kontrolovaných studií v běžné klinické praxi používány.
Schéma 1. Postavení radiofrekvenční katetrové ablace v léčbě FS v závislosti na přítomnosti strukturálního srdečního onemocnění, typu arytmie a preferenci pacienta. Pro paroxyzmální typ FS je doporučení v třídě I (úroveň důkazů A), pro perzistující FS v třídě IIa (úroveň důkazů B), pro dlouhodobou perzistující FS je pak doporučení v třídě IIb (úroveň důkazů B). 
Graph 2. Srovnání úspěšnosti léčby FS antiarytmiky (tmavé sloupce) a radiofrekvenční katetrové ablace (světlé sloupce). Zatímco úspěšnost farmakoterapie osciluje v těchto devíti randomizovaných studiích mezi 10–40 %, úspěšnost katetrové léčby dosahuje 60–90 % (upraveno podle [5]). ![Srovnání úspěšnosti léčby FS antiarytmiky (tmavé sloupce) a radiofrekvenční katetrové ablace (světlé sloupce). Zatímco úspěšnost farmakoterapie osciluje v těchto devíti randomizovaných studiích mezi 10–40 %, úspěšnost katetrové léčby dosahuje 60–90 % (upraveno podle [5]).](https://pl-master.mdcdn.cz/media/image/7d70a0997a0134ea774b750ca895a919.jpg?version=1537794815)
Úspěšnost ablační léčby FS se liší podle typu arytmie, a to i v publikovaných registrech i jednotlivých observačních studiích [7,8]. Zatímco úspěšnost první RFA pro paroxyzmální FS hodnocená jako absence recidivy arytmie po dobu 12 měsíců od výkonu bez antiarytmické farmakologické léčby (s výjimkou tzv. blanking periody, tj. 2 – 3 měsíce po vlastním zákroku, kdy je recidiva arytmie připuštěna vzhledem k hojícímu se substrátu) se v současné době pohybuje kolem 70 – 80 %, pro perzistující FS nedosahuje úspěšnost jedné katetrové ablace ani 30 % [9]. Léčbě dlouhodobé perzistující FS při větší dilataci levé síně se většina center z tohoto důvodu více či méně vyhýbá a více než dvě třetiny ablací pro FS v ČR je provedeno pro paroxyzmální formu této arytmie (graf 3).
Graph 3. Procentuální zastoupení invazivní léčby FS radiofrekvenční katetrovou ablací pro jednotlivé typy arytmie. V roce 2013 bylo v ČR provedeno celkem 2 082 výkonů, více než 2/3 pro paroxyzmální formu arytmie (data z registru ablací). 
Chirurgické a hybridní operační přístupy v léčbě perzistující FS
Chirurgické metody v léčbě FS se rozvíjely od 80. let 20. století. Katetrová léčba tehdy neexistovala a hlavním motorem rozvoje byla absence účinných antiarytmik. Přelomem ve vývoji chirurgických metod byla operace „MAZE“ (z angl. bludiště), která byla po letech animálních studií a experimentálního vývoje představena kardiochirurgem Jamesem L. Coxem v roce1987 společně s kardiologem Johnem Boineauem a fyziologem Richardem Schuesslerem a následně doznala různých modifikací až do podoby Cox ‑ MAZE III souborů lézí v pravé a levé síni, které byly designovány s cílem zabránit vzniku a udržení arytmie [10]. Soubor těchto lézí měl působivou účinnost. Sami autoři uvádějí 97% úspěšnost v udržení SR po pěti letech od operace. Bohužel tyto vynikající výsledky nebyly nikým jiným na světě reprodukovány. Širšího rozšíření se MAZE procedura dočkala až s rozvojem alternativních energií (kryoablace, radiofrekvence), které při vytváření lézí nahradily původní metodu „cut ‑ and ‑ sew“. Použití těchto způsobů chirurgické ablace je často nazýváno operací Cox ‑ MAZE IV (obr. 1). Ačkoli původní autoři uvádějí podobnou úspěšnost jako u procedury typu III [11], jiným pracovištím se vysoká úspěšnost této techniky nepotvrdila a v souladu s našimi zkušenostmi uvádějí úspěšnost mezi 60 a 82 %, v závislosti na typu FS a použitých metodách monitorování [12,13].
Image 1. Schéma procedury Cox-MAZE IV. 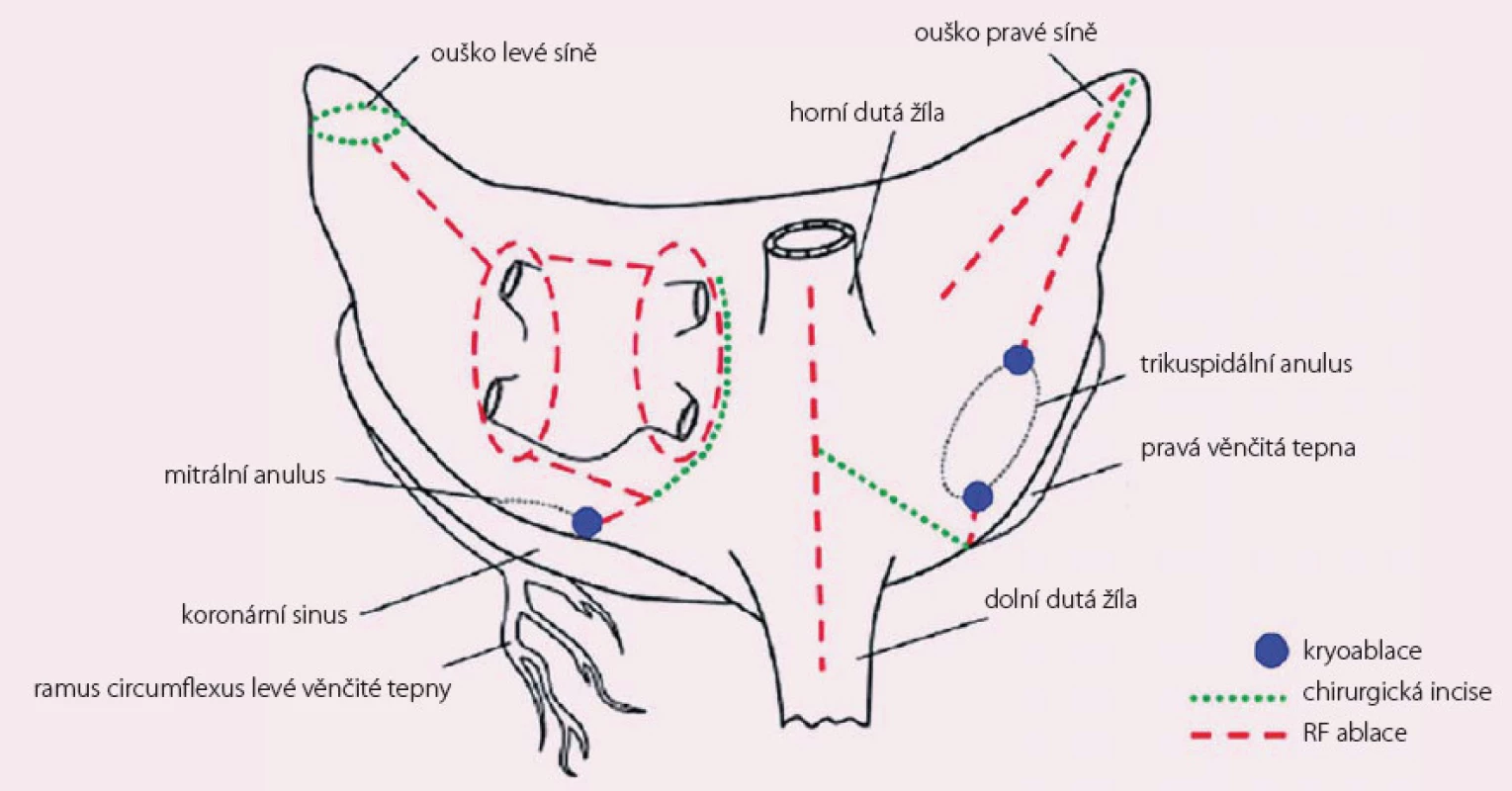
Doposud existuje jediná studie srovnávající léčbu RFA a chirurgickou [14]. Studie FAST poněkud nehomogenně zahrnula pacienty s paroxyzmální nebo perzistující FS s rozměrem levé síně (LS) přesahujícím 40 mm a arteriální hypertenzí nebo rozměrem LS přesahujícím 45 mm a předchozí selhanou RFA. Vyloučeni byli pacienti s významnou chlopenní vadou, pacienti s EF levé komory srdeční ≤ 45 %, pacienti s LS ≥ 65 mm a pacienti s dlouhodobou perzistující FS (FS o délce trvání > 1 rok). Celkem 124 pacientů bylo randomizováno na skupinu podstupující chirurgickou epikardiální a katetrovou endokardiální ablaci. Přežití bez arytmie po 12 měsících od výkonu bylo významně vyšší ve skupině chirurgické než ve skupině katetrizační (65,6 % vs 36,5 %; p = 0,002), ovšem za cenu významně vyšších komplikací (23 % vs 3,2 %; p = 0,001). Zarážející extrémně nízkou úspěšnost katetrové ablace lze do jisté míry vysvětlit nehomogenní skupinou studovaných pacientů (u 2/ 3 z nich již jedenkrát katetrová ablace selhala) a také nejednotným protokolem dvou zúčastněných center: zatímco nizozemské centrum používalo k léčbě fibrilace síní systém NavX a provádělo jen cirkumferenční ablaci okolo plicních žil nezávisle na typu arytmie, barcelonské centrum používalo k 3D navigaci systém CARTO a u perzistujících typů FS provádělo v LS i lineární léze.
V současných doporučených postupech je pozice samotné chirurgické metody v léčbě FS poněkud slabší než pozice léčby katetrovou ablací. Chirurgický přístup může být zvážen u pacientů s paroxyzmální, perzistující nebo dlouhodobě perzistující FS, kteří dosud neprodělali katetrovou ablaci (ale preferují chirurgickou léčbu) nebo u nichž jedna nebo více ablací selhala s tím, že přínos operace je větší nebo roven hrozícím rizikům (třída IIb, úroveň důkazů C) [7].
Ideální invazivní léčba FS by měla splňovat minimální základní atributy (tab. 1). Bohužel v současné době s dostupným stupněm poznání a ablačními technikami čelíme dvěma zásadním výzvám: 1. poznání patofyziologie FS u konkrétního léčeného pacienta (spouštěče a perpetuátory FS, lokalizované reentry, rotory aj.), 2. docílení permanentních transmurálních ablačních lézí. Zatímco na první otázku se snaží odpovědět již více než tři desetiletí intenzivní bazální výzkum a v poslední době publikované klinické zkušenosti ukazují, že je možné lokalizované zdroje (rotory) FS najít (mapovat) a ablací eliminovat [15], k řešení druhé oblasti technologicky přispívají nové systémy a katetry s možností odhadu hloubky vytvářené léze, kdy je konec katetru vybaven tzv. contact ‑ force senzorem umožňujícím snímat tlak (v g), který je vyvíjen katetrem proti endokardu, a jeho směr [16,17]. Z dosud publikovaných dat o nízké dlouhodobé úspěšnosti jak samotné chirurgické, tak i samotné katetrové léčby je možné nepřímo dovodit, že zásadní problém v současných technologiích spočívá především v nemožnosti vytvořit v síních kontinuální a trvalé léze, ať již jedním nebo druhým přístupem. Ani epikardiální ablace pod kontrolou zraku z rukou chirurga totiž není zárukou vytvoření permanentní léze. Výsledky akutního endokardiálního mapování při provádění RF epikardiálních ablací ukazují, že až v 80 % případů není možné vytvořit transmurální lézi pouhým jedním epikardiálním pálením [18] a že 20 – 30 % pacientů vyžaduje k zajištění kompletnosti lézí po epikardiální i opakované aplikaci RF energie endokardiálně provedená pálení [19].
Table 1. Charakteristika optimální invazivní léčby fibrilace síní (ideální stav). 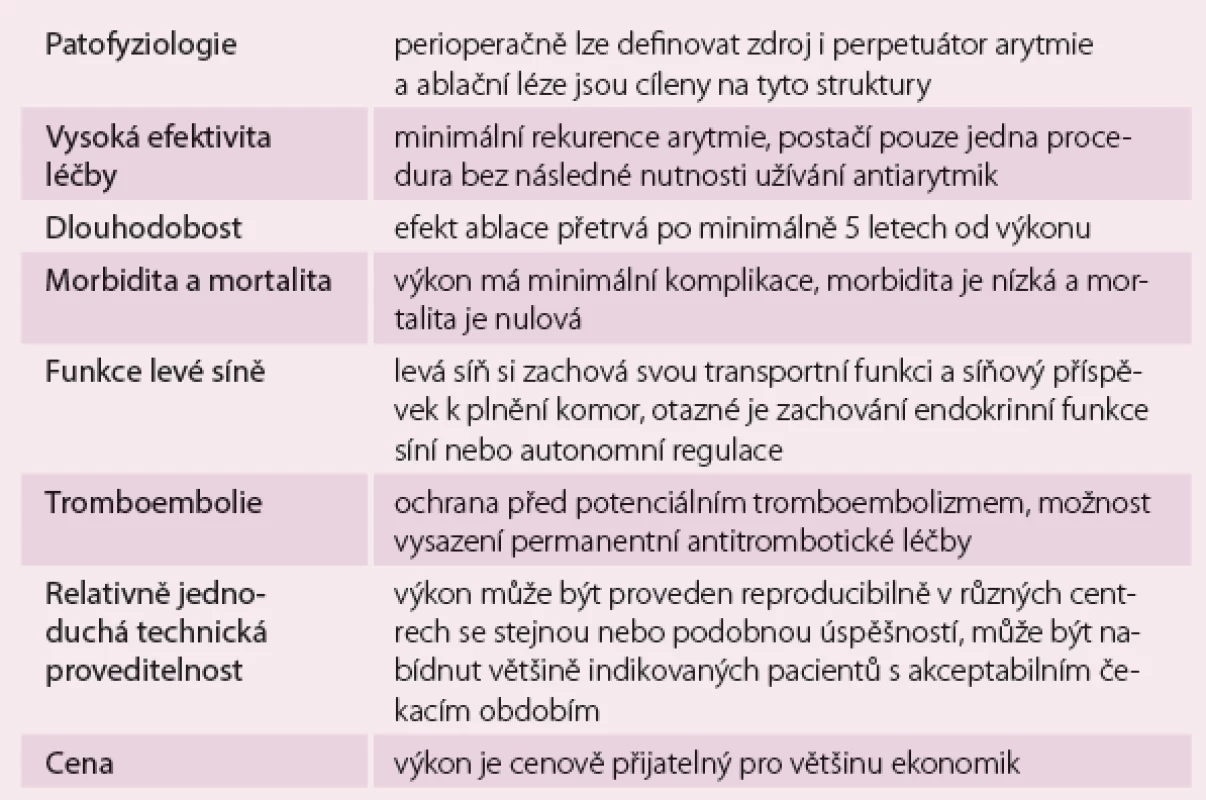
Nízká úspěšnost katetrové léčby u dlouhodobé perzistující FS, relativně variabilní úspěšnost izolované chirurgické léčby společně s pokrokem v technologii miniinvazivních chirurgických přístupů podpořené poznáním, že ani jedna metoda není v současné době schopna v LS vytvořit 100% kompletní trvalé a transmurální léze, vedly k rozvoji hybridních metod. Pojem hybridní operace znamená, že se na ablaci podílí jak kardiochirurg, který ablační léze vytváří instrumentáriem z epikardu, tak i kardiolog (arytmolog), který léze vytváří za pomocí zavedeného katetru endokardiálně. Výkon lze provádět jak simultánně (tedy na tzv. hybridním operačním sále), tak tzv. sekvenčně, kdy nejprve pacient podstupuje v celkové anestezii epikardiální ablaci a v druhé době (např. s odstupem 8 – 12 týdnů, jak je tomu v našem centru) podstoupí selektivní endokardiální RF ablaci. Doporučené postupy vnímají tento postup jako hybridní poněkud extenzivně: výkon lze označit za hybridní, pokud mezi epikardiální a endokardiální fází neuběhlo více než šest měsíců [4]. Doporučené postupy tedy indikační kritéria pro použití hybridních přístupů specificky nezmiňují, indikaci je možno vnímat v rovině indikace chirurgických metod.
Dosavadní publikovaná data o výsledcích hybridních výkonů u perzistující nebo dlouhodobě perzistující FS sumarizuje tab. 2. Z historického pohledu je možné konstatovat, že jako zdroj energie byla zcela opuštěna mikrovlnná technologie, ultrazvuk o vysoké intenzitě nebo monopolární RF energie [20]. Všechny tyto zdroje byly buď nebezpečné, nebo velice málo efektivní. Většina publikovaných studií zahrnuje zkušenosti jednoho centra, mají řádově maximálně desítky pacientů a rozdílnou metodiku. Sedm studií z let 2011 – 2014 [21 – 27] uvádělo výsledky léčby (absence FS bez nutnosti užívání antiarytmik) po 12 měsících. Úspěšnost byla mezi 85 a 92 % v pracích, kde byla použita bipolární RF energie, a mezi 36,8 a 88,9 % tam, kde byla použita monopolární RF energie.
Table 2. Přehled studií hybridní léčby fibrilace síní užívající výlučně bipolární RF energii. 
AA+ – možnost užívání antiarytmických léků, AA- – bez užívání antiarytmik, D – dny, ablace GP – ablace gangliových plexů, HDŽ – horní dutá žíla, IPŽ – izolace plicních žil, M – měsíce, n – počet pacientů zařazených do studie (Pa/P/DP – poměry paroxyzmální, perzistující a dlouhodobě perzistující fibrilace síní), OLS – ouško levé síně, t – čas od chirurgického ke katetrovému výkonu (0 znamená současný hybridní výkon), SR – sinusový rytmus (bez dokumentované fibrilace síní) Pracoviště autorů se začalo systematicky věnovat sekvenční hybridní léčbě pacientů s dlouhodobou perzistující FS a dilatovanými síněmi prakticky jako první v ČR v roce 2012 a tuto metodu nadále rozvíjí. Pacienti jsou poměrně rigorózně sledováni za pomocí 7D Holterovských systémů každé tři měsíce. Prvotní výsledky léčby již byly publikovány jinde [23]. V současné době máme k dispozici kompletní data prvních 40 pacientů, kteří jsou sledováni více než jeden rok. Relaps paroxyzmální FS nastal během doby sledování u dvou pacientů (5 %), přičemž u obou se jednalo o asymptomatický izolovaný paroxyzmus trvající minuty (u prvního) a 2 hod (u druhého pacienta). Tito pacienti byli nadále léčeni konzervativně. U dalších dvou pacientů (5 %) se objevily setrvalé síňové tachykardie, které nebylo možné úspěšně odstranit ani po druhé RF katetrové ablaci. U první pacientky se jednalo o extrémní dilataci a fibrózní postižení pravé síně, u dalšího pacienta pak o síňovou tachykardii vycházející z ouška LS, kde by případná RF katetrová reablace znamenala kompletní elektrickou izolaci ouška (které nebylo ošetřeno klipem), a byla obava z iatrogenního, vysoce protrombogenního stavu. U jediného pacienta jsme nebyli schopni docílit stabilního sinusového rytmu ani po kompletizaci protokolu a všech cirkumferenčních a lineárních lézí. Šlo o pacienta s extrémní dilatací (objem LS měřený systémem CARTO činil 210 ml!) a pokročilou fibrotickou přestavbou obou síní. Všichni pacienti byli po kompletizaci hybridního zákroku bez antiarytmické léčby. Celková úspěšnost po minimálně 12měsíčním sledování (v průměru 445 ± 92 dnů) tak v našem souboru pacientů s dlouhodobou perzistující fibrilací síní po jednom sekvenčním hybridním zákroku činila 87,5 %.
Závěr
Fibrilace síní představuje nejčastější supraventrikulární arytmii s narůstající incidencí i prevalencí. Zatímco paroxyzmální forma arytmie by vzhledem k současným dostupným technologiím contact ‑ force ablačních katetrů a poměrně vysoké úspěšnosti prvního ablačního výkonu při minimálních komplikacích měla zůstat doménou arytmologů provádějících RF katetrové ablace, řešení perzistujících a zejména dlouhodobě perzistujících FS s dilatovanými síněmi je katetrovou cestou obtížné. Hybridní výkony kombinací epi ‑ i endokardiálního přístupu mají velkou naději na vytvoření permanentní sestavy lézí v levé i pravé síni a potenciál být jednou z možných cest zvýšení úspěšnosti léčby této arytmie. Pro další rozšíření této nadějné léčby budou zapotřebí data z randomizovaných multicentrických studií prokazující vyšší úspěšnost jednoho hybridního zákroku ve srovnání s jedním nebo dvěma katetrovými ablacemi při zachování srovnatelné bezpečnosti a nízkého počtu případných komplikací.
Poděkování
Tato práce vznikla za finanční podpory Zdravotně sociální fakulty Jihočeské univerzity v Českých Budějovicích (č. výzkumného projektu BOV 2012_001).
Doručeno do redakce: 12. 5. 2014
Přijato po recenzi: 28. 5. 2014
doc. MUDr. Mgr. Alan Bulava, Ph.D.
www.nemcb.cz
alanbulava@seznam.cz
Sources
1. Go AS, Hylek EM, Phillips KA et al. Prevalence of diagnosed atrial fibrillation in adults: national implications for rhythm management and stroke prevention: the AnTicoagulation and Risk Factors in Atrial Fibrillation (ATRIA) Study. JAMA 2001; 285 : 2370 – 2375.
2. Heeringa J, van der Kuip DA, Hofman A et al. Prevalence, incidence and lifetime risk of atrial fibrillation: the Rotterdam study. Eur Heart J 2006; 27 : 949 – 953.
3. Healey JS, Connolly SJ, Gold MR et al. Subclinical atrial fibrillation and the risk of stroke. N Engl J Med 2012; 366 : 120 – 129. doi: 10.1056/ NEJMoa1105575.
4. Calkins H, Kuck KH, Cappato R et al. 2012 HRS/ EHRA/ ECAS Expert Consensus Statement on Catheter and Surgical Ablation of Atrial Fibrillation: recommendations for patient selection, procedural techniques, patient management and follow‑up, definitions, endpoints, and research trial design. Europace 2012; 14 : 528 – 606. doi: 10.1093/ europace/ eus027.
5. Bulava A. Nefarmakologická léčba z pohledu nových doporučení pro léčbu nemocných s fibrilací síní. Kardiol Rev 2011; 13 : 143 – 152.
6. Bulava A, Hanis J. The influence of the technology on the success of the treatment of paroxysmal atrial fibrillation: single center experience. Cor Vasa 2012; 54: e393 – e400.
7. Camm AJ, Lip GY, De Caterina R et al. 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: An update of the 2010 ESC Guidelines for the management of atrial fibrillation – developed with the special contribution of the European Heart Rhythm Association. Europace 2012; 14 : 1385 – 1413.
8. Cappato R, Calkins H, Chen SA et al. Updated worldwide survey on the methods, efficacy, and safety of catheter ablation for human atrial fibrillation. Circ Arrhythm Electrophysiol 2010; 3 : 32 – 38. doi: 10.1161/ CIRCEP.109.859116.
9. Fiala M, Wichterle D, Bulkova V et al. A prospective evaluation of haemodynamics, functional status, and quality of life after radiofrequency catheter ablation of long‑standing persistent atrial fibrillation. Europace 2014; 16 : 15 – 25. doi: 10.1093/ europace/ eut161.
10. Cox JL, Schuessler RB, D'Agostino HJ Jr et al. The surgical treatment of atrial fibrillation. III. Development of a definitive surgical procedure. J Thorac Cardiovasc Surg 1991; 101 : 569 – 583.
11. Damiano RJ Jr, Bailey M. The Cox ‑ Maze IV procedure for lone atrial fibrillation. Multimed Man Cardiothorac Surg 2007: doi: 10.1510/ mmcts.2007.002758.
12. Budera P, Straka Z, Osmancik P et al. Comparison of cardiac surgery with left atrial surgical ablation vs. cardiac surgery without atrial ablation in patients with coronary and/ or valvular heart disease plus atrial fibrillation: final results of the PRAGUE ‑ 12 randomized multicentre study. Eur Heart J 2012; 33 : 2644 – 2652. doi: 10.1093/ eurheartj/ ehs290.
13. Camm CF, Nagendran M, Xiu PY et al. How effective is cryoablation for atrial fibrillation during concomitant cardiac surgery? Interact Cardiovasc Thorac Surg 2011; 13 : 410 – 414. doi: 10.1510/ icvts.2011.271676.
14. Boersma LV, Castella M, van Boven W et al. Atrial fibrillation catheter ablation versus surgical ablation treatment (FAST): a 2 - center randomized clinical trial. Circulation 2012; 125 : 23 – 30. doi: 10.1161/ CIRCULATIONAHA.111.074047.
15. Narayan SM, Krummen DE, Clopton P et al. Direct or coincidental elimination of stable rotors or focal sources may explain successful atrial fibrillation ablation: on ‑ treatment analysis of the CONFIRM trial (Conventional ablation for AF with or without focal impulse and rotor modulation). J Am Coll Cardiol 2013; 62 : 138 – 147. doi: 10.1016/ j.jacc.2013.03.021.
16. Squara F, Latcu DG, Massaad Y et al. Contact force and force ‑ time integral in atrial radiofrequency ablation predict transmurality of lesions. Europace 2014; 16 : 660 – 667. doi: 10.1093/ europace/ euu068.
17. Kimura M, Sasaki S, Owada S et al. Comparison of lesion formation between contact force ‑ guided and non‑guided circumferential pulmonary vein isolation: a prospective, randomized study. Heart Rhythm 2014; 11 : 984–991. doi: 10.1016/ j.hrthm.2014.03.019.
18. Lockwood D, Nakagawa H, Peyton MD et al. Linear left atrial lesions in minimally invasive surgical ablation of persistent atrial fibrillation: techniques for assessing conduction block across surgical lesions. Heart Rhythm 2009; 6: S50 – S63. doi: 10.1016/ j.hrthm.2009.09.010.
19. Pison L, La MairM, van Opstal J et al. Hybrid thoracoscopic surgical and transvenous catheter ablation of atrial fibrillation. J Am Coll Cardiol 2012; 60 : 54 – 61. doi: 10.1016/ j.jacc.2011.12.055.
20. La Meir M. Surgical options for treatment of atrial fibrillation. Ann Cardiothorac Surg 2014; 3 : 30 – 37. doi: 10.3978/ j.issn.2225 ‑ 319X.2014.01.07.
21. Muneretto C, Bisleri G, Bontempi L et al. Durable staged hybrid ablation with thoracoscopic and percutaneous approach for treatment of long‑standing atrial fibrillation: a 30-month assessment with continuous monitoring. J Thorac Cardiovasc Surg 2012; 144 : 1460 – 1465. doi: 10.1016/ j.jtcvs.2012.08.069.
22. Pison L, Gelsomino S, Luca F et al. Effectiveness and safety of simultaneous hybrid thoracoscopic and endocardial catheter ablation of lone atrial fibrillation. Ann Cardiothorac Surg 2014; 3 : 38 – 44. doi: 10.3978/ j.issn.2225 ‑ 319X.2013.12.10.
23. Kurfirst V, Mokracek A, Bulava A et al. Two‑staged hybrid treatment of persistent atrial fibrillation: short‑term single‑centre results. Interact Cardiovasc Thorac Surg 2014; 18 : 451 – 456. doi: 10.1093/ icvts/ ivt538.
24. La Meir M, Gelsomino S, Lorusso R et al. The hybrid approach for the surgical treatment of lone atrial fibrillation: one‑year results employing a monopolar radiofrequency source. J Cardiothorac Surg 2012; 7 : 71. doi: 10.1186/ 1749 ‑ 8090 ‑ 7 ‑ 71.
25. La Meir M, Gelsomino S, Luca F et al. Minimally invasive surgical treatment of lone atrial fibrillation: early results of hybrid versus standard minimally invasive approach employing radiofrequency sources. Int J Cardiol 2013; 167 : 1469 – 1475. doi: 10.1016/ j.ijcard.2012.04.044.
26. Krul SP, Driessen AH, van Boven WJ et al. Thoracoscopic video ‑ assisted pulmonary vein antrum isolation, ganglionated plexus ablation, and periprocedural confirmation of ablation lesions: first results of a hybrid surgical ‑ electrophysiological approach for atrial fibrillation. Circ Arrhythm Electrophysiol 2011; 4 : 262 – 270. doi: 10.1161/ CIRCEP.111.961862.
27. Bisleri G, Rosati F, Bontempi L et al. Hybrid approach for the treatment of long‑standing persistent atrial fibrillation: electrophysiological findings and clinical results. Eur J Cardiothorac Surg 2013; 44 : 919 – 923. doi: 10.1093/ ejcts/ ezt115.
28. Mahapatra S, LaPar DJ, Kamath S et al. Initial experience of sequential surgical epicardial ‑ catheter endocardial ablation for persistent and long‑standing persistent atrial fibrillation with long‑term follow‑up. Ann Thorac Surg 2011; 91 : 1890 – 1898. doi: 10.1016/ j.athoracsur.2011.02.045.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2014 Issue 3-
All articles in this issue
- Dráždivý tračník – diagnostika a léčba
- Divertikulární choroba tlustého střeva – nové trendy v léčbě
- Screening kolorektálního karcinomu
- Idiopatické střevní záněty
- Chronická pankreatitida
- Léčba akutního srdečního selhání
- Pravidelné supraventrikulární tachykardie – diagnóza, léčba a zkušenosti vysokoobjemového kardiocentra
- Moderní trendy v léčbě dlouhodobé perzistující fibrilace síní
- Standardizace ošetřovatelské péče k dekanylaci sheathu na intervenčních pracovištích v České republice
- Perorální endoskopická myotomie (POEM) – nová endoskopická možnost léčby achalázie jícnu
- Refluxní nemoc jícnu
- Léčba inhibitory protonové pumpy
- Celiakie – současný pohled na etiopatogenezi, diagnostiku a terapii
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Divertikulární choroba tlustého střeva – nové trendy v léčbě
- Dráždivý tračník – diagnostika a léčba
- Chronická pankreatitida
- Léčba inhibitory protonové pumpy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

