-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Jak vybrat preparát mezi biologickými léky?
How to choose a biological agent?
An increasing number of available biological drugs for the treatment of rheumatic diseases raise a question how to choose the right agent. To date, biological drugs have not been directly compared. In addition to the diagnosis, mechanism of action and the risk of adverse events need to be taken into account when choosing a biological drug for a particular patient. The following article, which is based on the recommendations of the Czech Society for Rheumatology, uses specific examples to show the benefits of particular drugs and all issues which have to be taken into account when deciding upon therapy.
Key words:
biological therapy, case reports, rheumatoid arthritis, psoriatic arthritis, ankylosing spondylitis.
Autoři: L. Šedová
Působiště autorů: Revmatologický ústav, Praha
Vyšlo v časopise: Čes. Revmatol., 19, 2011, No. 2, p. 73-75.
Kategorie: Příspěvky z kongresu
Souhrn
Rostoucí počet dostupných biologických preparátů pro léčbu revmatických onemocnění staví revmatology často před otázkou, podle čeho vybírat. Zatím nebyla provedena přímá srovnání biologických léků mezi sebou. Při výběru biologického léčiva pro konkrétního nemocného je třeba zohledňovat kromě diagnózy i mechanismus účinku a riziko nežádoucích účinků daného preparátu. Následující článek, který se opírá o doporučení České revmatologické společnosti, na konkrétních příkladech ukazuje jaké benefity nabízí konkrétní léky a co vše je nutné brát v potaz při rozhodování o terapii.
Klíčová slova:
biologická léčba, kazuistiky, revmatoidní artritida, psoriatická artritida, ankylozující spondylitidaDostupnost stále většího počtu moderních preparátů pro léčbu revmatických onemocnění (tab. 1) otevírá mnoho terapeutických možností a vybrat mezi nimi pro pacienta ten nejvhodnější je složité. Avšak na otázku jestli existuje jeden ideální preparát pro konkrétního pacienta lze mnohdy najít částečnou odpověď. U řady nemocných může být určitá okolnost (komorbidita, sociální prostředí, funkční fyzická nebo duševní schopnost), která si žádá právě jeden preparát ze skupiny biologik. Pokud připustíme poněkud schematický přístup, lze toto demonstrovat na příkladech.
Tab. 1. Základní charakteristika hlavních preparátů. 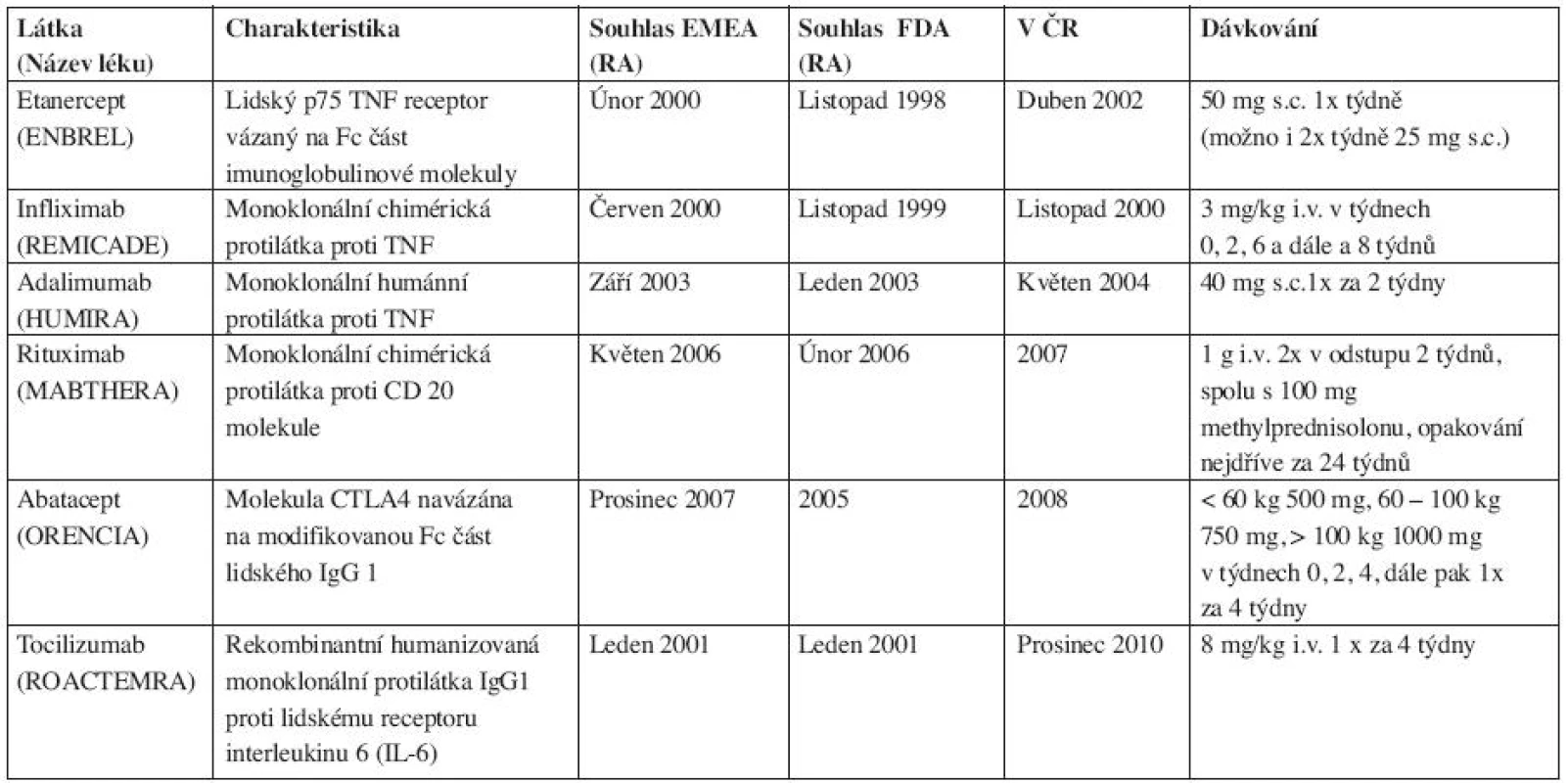
Případ 1.: Pan XA je 50letý muž, který trpí ankylozující spondylitidou, je HLA B27 pozitivní a zároveň má diagnostikovaný idiopatický střevní zánět. Pacient se bojí samostatné aplikace injekcí.
U tohoto pacienta je prvním biologikem, na které budeme myslet nejspíše, infliximab.
Infliximab je rekombinantní chimérická IgG1 lidská-myší monoklonální protilátka proti TNFα. Má schopnost fixovat komplement, což vede k lýze buněk a tím ovlivňuje apoptózu imunitních efektorových buněk. Při podávání v intravenózním bolusu dosahuje vysokých sérových koncentrací nutných pro průnik buněčnou membránou. Tyto vlastnosti mezi jinými zakládají na významné účinnosti tohoto preparátu nejen u revmatických nemocí jako je ankylozující spondylitida, ale i u idiopatických střevních zánětů (1, 2).
Případ 2.: Pan XB je 30letý muž, který také trpí ankylozující spondylitidou, je HLA B27 pozitivní a má rovněž diagnostikovaný idiopatický střevní zánět. Důležitým rozdílem oproti předchozímu případu je jeho pracovní náplň, pro kterou je nucen trávit pravidelně v zahraničí krátké pobyty cca 10 až 12 týdnů dlouhé.
Za těchto okolností je lékem volby adalimumab. Tato rekombinantní humanní IgG1 monoklonální protilátka proti TNFα má taktéž schopnost fixovat komplement, vede tedy rovněž k lýze buněk a ovlivňuje apoptózu imunitních buněk, ale umožňuje pacientovi samostatnost při dlouhých cestách díky aplikaci s prokázanou dostatečnou sérovou koncentrací preparátu po subkutánním podání (2, 3).
Případ 3.: Paní XC je 30letá žena s psoriatickou artritidou. Důležitým faktorem při výběru biologického preparátu bude v tomto případě její zaměstnání. Je totiž zdravotní sestrou v tuberkulózní léčebně, což významně zvyšuje risk akvizice specifické infekce. Proto bude zde nejvhodnějším lékem etanercept.
Preparáty blokující TNFα mají tzv. class effect zvyšující riziko specifické infekce, z tohoto důvodů existují přísná pravidla sledování nemocných na terapii s pravidelnými preventivními kontrolami.
Solubilní IgG TNFα váže převážně a reverzibilně solubilní TNFα, neaktivuje komplement, nevede k lýze buněk. Riziko tuberkulózní infekce je dle literárních údajů u tohoto preparátu nižší a proto by za stejně přísných kontrol mohl být vhodnějším lékem (4; 5).
Případ 4.: Paní XD je 45letá žena s vysoce aktivní séropozitivní a anti-CCP pozitivní revmatoidní artritidou. V její osobní anamnéze je ovšem i lymfom. Nejedná se ovšem o vzácnou výjimku. V populaci nemocných s revmatoidní artritidou významně stoupá riziko lymfomů dle aktivity revmatického onemocnění a u vysoce aktivních je to riziko až pětadvacetinásobní (tab. 2) (6).
Tab. 2. Riziko lymfomů u pacientů s revmatoidní artritidou dle aktivity onemocnění. 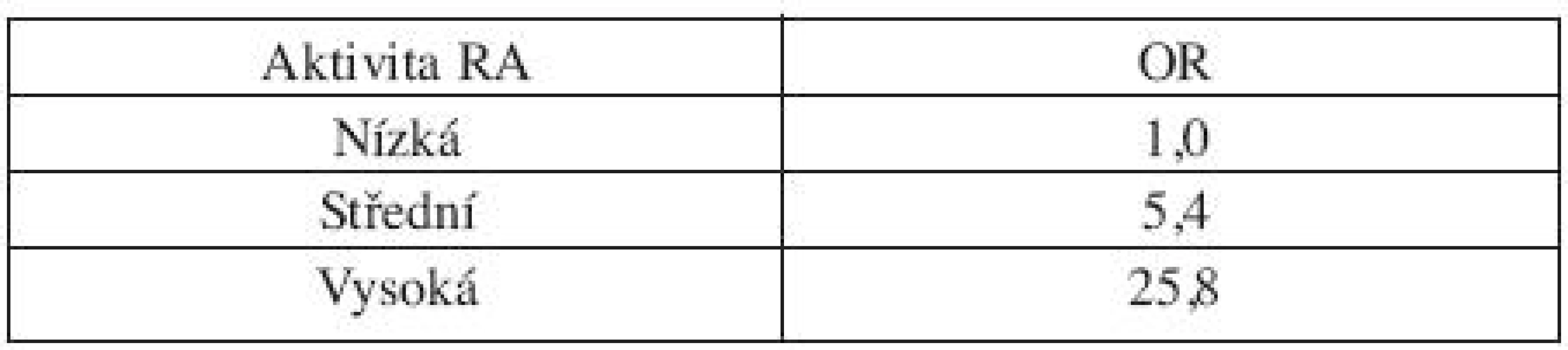
Rituximab je protilátka proti B buňkám-anti CD20 pozitivním. Je indikován u pacientů s aktivní revmatoidní artritidou po selhání TNFα léčby avšak má prokázanou účinnost i jako lék 1. linie. U pacientů s revmatoidní artritidou s přítomnou protilátkovou aktivitou (revmatoidní faktory, anticitrulinové protilátky) jsou výsledky jeho účinnosti ještě výraznější (7).
Vzhledem k anamnéze malignity u této pacientky jsou blokátory TNFα kontraindikovány (minimální odstup je 5 let) (8). Rituximab byl však původně použití u „non-Hodginských“ lymfomů (9, 10) z čehož vyplývá pro nemocnou jednoznačný benefit a proto je v tomto případě indikován právě tento preparát.
Případ 5.: Paní XE, 36letá pacientka se séronegativní, anti-CCP negativní revmatoidní artritidou má za sebou léčbu řadou chorobu modifikujícími léky a také blokátorem TNFα bez dostatečné účinnosti.
Abatacept je biologický preparát s jiným mechanismem účinku než je blokáda TNFα. Zabraňuje kostimulačnímu signalu pro T-lymfocyty zprostředkovanému molekulami CD28 na T buňkách a CD80/86 na povrchu antigen prezentující buňky. Má prokázanou bezpečnost a účinnost (nejen) u pacientů s neadekvátní odpovědí na TNFα inhibitory bez závislosti na přítomnost či nepřítomnost protilátkové aktivity (11; 12).
Případ 6.: Paní XF, 56 let stará nemocná byla pro velmi aktivní revmatoidní artritidu léčena různými chorobu modifikujícími léky (sulfasalazin, metotrexát, leflunomid), po kterých měla vždy těžkou leukopenii. Je indikována k biologické léčbě avšak může ji pro tuto komplikaci užívat jen v monoterapii.
Jediný preparát, který má prokázanou lepší účinnost v monoterapii než metotrexát je tocilizumab, humanizovaná IgG1 monoklonální protilátka proti receptoru interleukinu 6 (13; 14) a proto by měl být v tomto případě zvažován právě on.
Případů, kdy je volba preparátu jednoznačná je však menšina. U ostatních pacientů je možnosti více a v tomto smyslu vyzní též doporučení České revmatologické společnosti, kde je přímo uvedeno, že „Nebylo zatím prokázáno, že by některý z biologik byl účinnější než jiný a neexistuje tedy důvod k doporučení látky, která by měla být používána prioritně“ (8). V procesu volby je nutné dát také prostor preferencím pacienta, což zdůrazňuje jak doporučení České revmatologické společnosti (8), tak i Evropské ligy proti revmatismu (15). Pacient může dát přednost určitému způsobu nebo časovému schématu aplikace. Je třeba proto probrat charakteristiku každého indikovaného léku a brát v potaz i názor nemocného.
Neméně důležitou při výběru nebo změně léčby je otázka účinnosti. Cílem terapie by měla být remise, nebo alespoň velmi nízká aktivita choroby hodnocena pomocí indexu DAS 28 (disease aktivity score). Nepodaří-li se při prvním výběru tohoto cíle dosáhnout, nebo dojde-li ke ztrátě účinnosti, měla by následovat změna (tzv. switch) na jiný preparát.
Vzhledem k tomu, že byly popsány individuální rozdíly mezi pacienty v reaktivitě na různé TNFα inhibitory není vyloučeno, že pacient nereagujícím nebo reagující nedostatečně na jeden lék blokující TNFα bude mít dobrou odpověď na léčbu jiným preparátem z této skupiny. Při relapsu po ukončení jednoho preparátu, který vedl k remisi, by nejdříve měli být nasazen opět tento lék.
Rituximab a abatacept jsou indikovány u nemocných, u kterých selhala anti-TNFα terapie a dle posledních literárních zdrojů není mezi není mezi nimi v účinnosti v této indikaci rozdíl (16). Abatacept je již též registrován pro použití v 1. linii.
Rozhodnutí o tom, zda dalším biologickým preparátem bude jiný anti-TNFα lék nebo preparát s jiným mechanismem účinku je individuální a závisí na několika okolnostech, mezi které patří např. charakteristika nemoci pacienta, komorbidita, opět preference nemocného, předcházející nežádoucí účinky a případně i ekonomické aspekty terapie.
Pro srovnání biologických preparátů mezi sebou by byly za potřeby tzv. head to head studie, které nejsou k dispozici. Poslouží proto zatím metaanalýzy, jejichž výpověďní hodnota je ovšem omezena. Vždy bude proto při rozhodování nejdůležitější podrobný rozbor konkrétního případu, včetně názoru nemocného.
Poděkování tato publikace vznikla za podpory výzkumných záměrů MZ ČR NO: 000 000 23728
MUDr. Liliana Šedová
Revmatologický ústav
Na Slupi 4,
128 50 Praha 2
sedo@revma.cz
Zdroje
1. Mpofu S, Fatima F, Moots RJ. Anti-TNF-alpha therapies: they are all the same (aren’t they?). Rheumatology (Oxford). 2005;44 : 271-3.
2. Sieper J, Van Den Brande J. Diverse effects of infliximab and etanercept on T lymphocytes. Semin Arthritis Rheum. 2005;34(5 Suppl1):23-7.
3. Schwartzman S, Morgan GJ Jr. Does route of administration affect the outcome of TNF antagonist therapy? Arthritis Res Ther 2004;6 Suppl 2:S19-23.
4. Keane J. TNF-blocking agents and tuberculosis: new drugs illuminate an old topic. Rheumatology (Oxford). 2005;44 : 714-20.
5. Tubach F, Salmon D, Ravaud P et al. Research Axed on Tolerance of Biotherapies Group. Risk of tuberculosis is higher with anti-tumor necrosis factor monoclonal antibody therapy than with soluble tumor necrosis factor receptor therapy: The three-year prospective French Research Axed on Tolerance of Biotherapies registry. Arthritis Rheum 2009;60 : 1884-94.
6. Franklin J, Lunt M, Bunn D, Symmons D, Silman A: Incidence of lymphoma in a large primary care derived cohort of cases of inflammatory polyarthritis. Ann Rheum Dis 2006;65 : 617-622.
7. Emery P, Fleischmann R, Filipowicz-Sosnowska A et al. DANCER Study Group. The efficacy and safety of rituximab in patients with active rheumatoid arthritis despite methotrexate treatment: results of a phase IIB randomized, double-blind, placebo-controlled, dose-ranging trial. Arthritis Rheum 2006;54 : 1390-400.
8. Bečvář R, Vencovský J, Němec P1, Suchý D2, Procházková L1, Pavelka K. Doporučení České revmatologické společnosti pro léčbu revmatoidní artritidy. Účinnost a strategie léčby. Čes Revmatol 2007; 2 : 73-90.
9. Baecklund E, Ekbom A, Sparén P, Feltelius N, Klareskog L. Disease activity and risk of lymphoma in patients with rheumatoid arthritis: nested case-control study. BMJ. 1998;317(7152):180-1.
10. Grillo-López AJ, White CA, Varns C, et al. Overview of the clinical development of rituximab: first monoclonal antibody approved for the treatment of lymphoma. Semin Oncol. 1999;26(5 Suppl 14):66-73.
11. Genovese MC, Schiff M, Luggen M, et al. Efficacy and safety of the selective co-stimulation modulator abatacept following 2 years of treatment in patients with rheumatoid arthritis and an inadequate response to anti-tumour necrosis factor therapy. Ann Rheum Dis 2008;67 : 547-54.
12. Lutt JR, Deodhar A. Rheumatoid arthritis: strategies in the management of patients showing an inadequate response to TNFalpha antagonists. Drugs 2008;68 : 591-606.
13. Jones G, Sebba A, Gu J, et al. Comparison of tocilizumab monotherapy versus methotrexate monotherapy in patients with moderate to severe rheumatoid arthritis: the AMBITION study. Ann Rheum Dis 2010;69 : 88-96.
14. Nishimoto N, Miyasaka N, Yamamoto K, Kawai S, Takeuchi T, Azuma J. Long-term safety and efficacy of tocilizumab, an anti-IL-6 receptor monoclonal antibody, in monotherapy, in patients with rheumatoid arthritis (the STREAM study): evidence of safety and efficacy in a 5-year extension study. Ann Rheum Dis 2009;68 : 1580-4.
15. Smolen JS, Landewé R, Breedveld FC, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs. Ann Rheum Dis 2010;69 : 964-75.
16. Salliot C, Finckh A, Katchamart W, Lu Y, Sun Y, Bombardier C, Keystone E. Indirect comparisons of the efficacy of biological antirheumatic agents in rheumatoid arthritis in patients with an inadequate response to conventional disease-modifying antirheumatic drugs or to an anti-tumour necrosis factor agent: a meta-analysis. Ann Rheum Dis 2010 Dec 22. [Epub ahead of print]
Štítky
Dermatologie Dětská revmatologie Revmatologie
Článek vyšel v časopiseČeská revmatologie
Nejčtenější tento týden
2011 Číslo 2- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
- Kterým pacientům se SLE nasadit biologickou léčbu?
- Stillova choroba: vzácné a závažné systémové onemocnění
- Jak souvisí časné zahájení biologické léčby SLE/LN s prevencí nevratného poškození?
-
Všechny články tohoto čísla
- Malé molekuly RNA a jejich význam v imunitní odpovědi organismu
- Příspěvky z kongresu Biologická léčba
- Existují prediktivní ukazatele úspěšnosti biologické léčby?
- Jak vybrat preparát mezi biologickými léky?
- Jak se dívat na strukturální progresi u biologické léčby?
- Mimokloubní projevy revmatických onemocnění a možnosti jejich ovlivnění biologickou léčbou
- Výskyt infekcí při léčbě antagonisty TNF alfa v registru ATTRA
- Biologická léčba revmatoidní artritidy a riziko nádorových onemocnění
- Biologická léčba a speciální situace (těhotenství, kojení, vakcinace a perioperační období)
- Česká revmatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Biologická léčba a speciální situace (těhotenství, kojení, vakcinace a perioperační období)
- Mimokloubní projevy revmatických onemocnění a možnosti jejich ovlivnění biologickou léčbou
- Biologická léčba revmatoidní artritidy a riziko nádorových onemocnění
- Výskyt infekcí při léčbě antagonisty TNF alfa v registru ATTRA
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



