-
Medical journals
- Career
LÉČBA CHRONICKÉ OSTEOMYELITIDY TIBIE S POUŽITÍM DOČASNÉHO ANTIBIOTICKÉHO SPACERU, ROTAČNÍHO SVALOVÉHO LALOKU, TERAPIE LARVAMI A SPONGIOPLASTIKY S PEROSSALEM – KAZUISTIKA
Authors: Eva Čurlejová 1; Miroslav Homza 1; Igor Čižmář 1; Pavel Dráč 1; Milan Kamínek 2
Authors‘ workplace: Traumatologické oddělení FN Olomouc Department of Trauma surgery, Faculty Hospital Olomouc 1; Klinika nukleární medicíny FN Olomouc Department of Nuclear medicine, Faculty Hospital Olomouc 2
Published in: Úraz chir. 22., 2014, č.1
Category: Case report
Overview
CÍL PRÁCE:
Cílem práce bylo představit diagnostický a chirurgický postup při léčbě chronické osteomyelitidy tibie.MATERIÁL a METODY:
Autoři popisují diagnostickou a chirurgickou intervenci u 55letého pacienta s chronickou osteomyelitidou tibie po dlahové osteosyntéze. K diagnostice použili 18F-FDG (18F-fluorodeoxyglucose) PET/CT a vyšetření značenými leukocyty Le 99mTc-HMPAO (hexametylpropylen amin oxim) SPECT/CT. Při léčbě vykonali radikální chirurgický debridement, laváž, aplikaci antibiotické výplně do celé dřeňové dutiny postižené kosti a následně spongioplastiku spolu s hydroxiapatitovou kostní náhradou PerOssalem. Defekty měkkých tkání byly primárně dočasně uzavřeny pomocí Vacuum Assisted Closure (V.A.C.) a následně kryty rotačním svalovým lalokem. K nekrektomii byla použita terapie larvami bzučivky zelené.VÝSLEDKY:
Pacient je po léčbě více než 19 měsíců bez obtíží, bez známek rekurence infektu. Postiženou končetinu plně zatěžuje a rozsahy pohybu v kolenním kloubu jsou bez výraznějšího omezení.ZÁVĚR:
Popsaný chirurgický postup představuje jednu z možností léčby chronické osteomyelitidy.KLÍČOVÁ SLOVA:
Antibiotický spacer, chronická osteomyelitida, larvální terapie, svalový lalok, tibie.ÚVOD
Navzdory zavedení nových chirurgických metod do klinické praxe a pokroku v antibiotické léčbě zůstává současná terapie osteomyelitidy u části pacientů neúspěšná. Při léčbě tohoto onemocnění je stále klíčový radikální debridement, který však sám o sobě na eradikaci infekce nestačí a navíc často způsobuje významnou ztrátu kosti i okolních měkkých tkání. Optimální management léčby osteomyelitidy zahrnuje sekvestrektomii, nekrektomii, obliteraci mrtvého prostoru, zabezpečení mechanické stability kosti a adekvátní krytí měkkými tkáněmi [11]. Níže popsaný terapeutický postup představuje jednu z možností léčby chronické osteomyelitidy.
KAZUISTIKA
55letý muž byl poraněn (přibližně 20 let před příchodem na naše pracoviště) na pravém bérci padajícím motocyklem. Došlo ke vzniku otevřené zlomeniny distální třetiny pravého bérce II. stupně podle klasifikace Gustila a Andersona [7]. Primárně byl ošetřený ve spádovém chirurgickém pracovišti, kde byla provedena dlahová osteosyntéza. Po šesti měsících bylo na základě rentgenologického vyšetření konstatováno zpomalené hojení a zlomenina po extrakci dlahy byla dále léčena zevní fixací po dobu dalších šesti měsíců. Ačkoliv se při následujícím rentgenologickém vyšetření jevila zlomenina zhojena, objevila se na mediální straně distální třetiny tibie secernující píštěl. Pacient docházel ambulantně k ošetření píštěle do spádového chirurgického zařízení a následně byl konzultován na našem pracovišti. Protože se jednalo o pacienta bez závažných komorbidit, autoři se rozhodli pro léčbu této chronické osteomyelitidy. Kultivace sekretu z píštěle prokázala infekci kmeny Klebsibella oxytoca, Enterococcus species, Bacteorides thetaiotaomicron a Pseudomonas aeruginosa a podle výsledku citlivosti byla zahájena cílená intravenózní antibiotická terapie (Cefuroxim 4,5g/den, 30 dnů). Chirurgická terapie byla zahájená debridementem, exkochleací fistuly (provedené histologické vyšetření neprokázalo přítomnost nádorových změn), proplachem intramedulární dutiny pomocí tryskové laváže (Inter-Pulse, výrobce Instruments, Kalamazo, USA) a zavedením proplachové drenáže. Předoperační hodnota CRP byla 119,4 mg/l.
Pro zhoršení klinického (obr. 1) a laboratorního nálezu byla provedena operační revize s nálezem intramedulárního abscesu v celé dřeňové dutině, který byl ošetřen exkochleací celé proximální metafýzy tibie a saucerizací (otevření místa infikované kostní léze přímo – incize měkkých tkání a následně otevření dřeňové dutiny s odstraněním části kortikální kosti) distální metafýzy tibie.
Image 1. CT před operační revizí 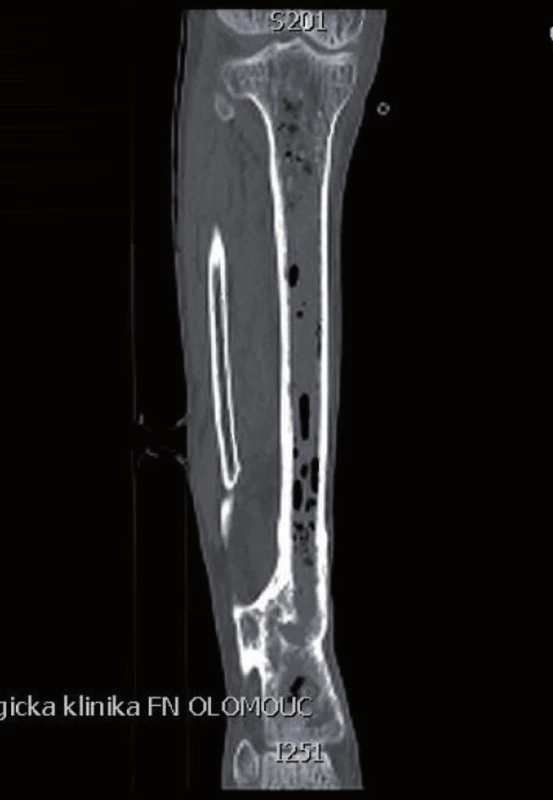
Po následném vyfrézování dřeňové dutiny byl proveden výplach Pamyconem (Neomycini sulfas 33 000 IU+ Bacitracinum 2 500 IU, Biotika a.s., Slovenská Ľupča, Slovenská republika), nekrektomie okolní měkké tkáně a resekce ligamentum proprium patellae při jeho úponu na tuberositas tibie. Celá dřeňová dutina byla vyplněná kostním cementem s antibiotiky – Vancogenx (PMMA + Vankomycin + Gentamicin, výrobce Tecres S.P.A., Verona, Italy). Část Vancogenxu byla nanesena na Prevotův prut a zbytek byl aplikován ve formě ručně vymodelovaných kuliček (obr. 2).
Image 2. RTG po aplikaci Vancogenxu 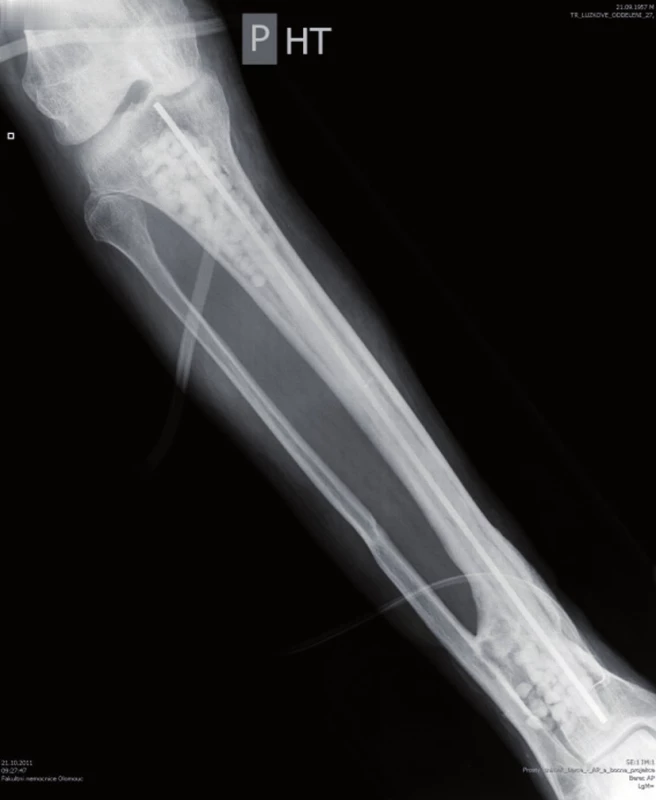
Množství kostního cementu, které bylo naneseno na Prevotův prut, jsme zvolili podle velikosti vyfrézované dřeňové dutiny tibie. Ke kosti byl zaveden Redonův drén a defekt měkkých částí byl kryt pomocí V.A.C. systému (Vacuum Assisted Closure, Hartmann-Rico a.s.). Pooperačně došlo k poklesu hodnoty CRP v krevní plazmě na 73,0 mg/l. Za pět dní byl defekt měkkých tkání kryt rotačním svalovým lalokem s užitím caput mediale musculi gastrocnemii. V okolí laloku jsme nalezli ještě nejasně ohraničené nekrotické zbytky ligamentum proprium patellae a povrchovou část Hoffova tělesa. K odstranění této nekrotické tkáně byla použita larvální terapie, protože minimalizuje případné porušení bariéry kloubního pouzdra. Po celou dobu hospitalizace (64 dnů) byla pacientovi podávána intravenózně antibiotika podle výsledku kultivace a citlivosti (Amoxicilinum 3,6g/den + Ciprofoxacín 800mg/den 23 dnů, pak Amikacin 1,5g/den osm dnů). Před dimisí pacienta do domácí péče byla antibiotická terapie ukončena. Při následné hospitalizaci za tři měsíce bylo provedeno vyšetření 18F-FDG (18F-fluorodeoxyglucose) PET/CT a vyšetření značenými leukocyty Le 99mTc-HMPAO (hexametylpropylen amin oxim) SPECT/CT, která ještě prokazovala přítomnost aktivního zánětlivého procesu v proximálních 2/5 intramedulárního kanálu tibie. Proto byl Vancogenx extrahován a po provedení masivního výplachu dřeňové dutiny roztokem Pamyconu byla dutina opět vyplněna Vancogenxem. Během hospitalizace byla pacientovi podávána nitrožilně antibiotika podle kultivace a citlivosti v délce 10 dnů (Tazobactamum 1,5g + Piperacilinum 12g/den ) a stejnou dobu pak užíval perorální formu ( Sulfamicillium 1,125g/den) – to již během domácí léčby. Za další tři měsíce bylo vyšetření opakováno 18F-FDG PET/CT a vyšetření značenými Le 99mTc-HMPAO SPECT/CT, která již neprokázala přítomnost infektu, a proto byl Vancogenx extrahován a dřeňová dutina byla vyplněna pomocí kortikospongiózních kostních štěpů odebraných z lopat kyčelních kostí pacienta, smíchaných se směsí syntetické kostní náhrady PerOssal (Nanocrystalline Calcium Phosphate, výrobce Biomaterials GmbH, Dieburg, Germany) a 750 mg Vankomycinu v poměru 1 : 2 (obr. 3, 4).
Image 3. RTG po spongioplastice a aplikaci PerOssalu 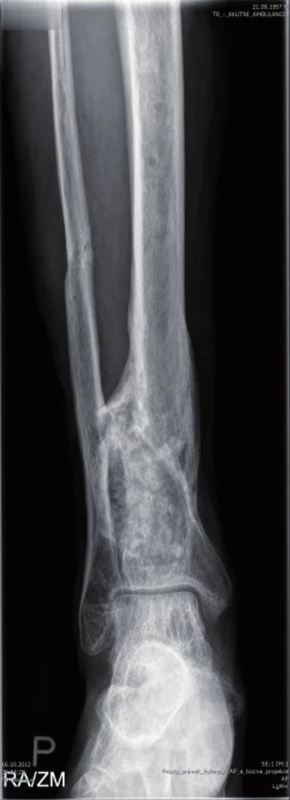
Image 4. RTG po spongioplastice a aplikaci PerOssalu 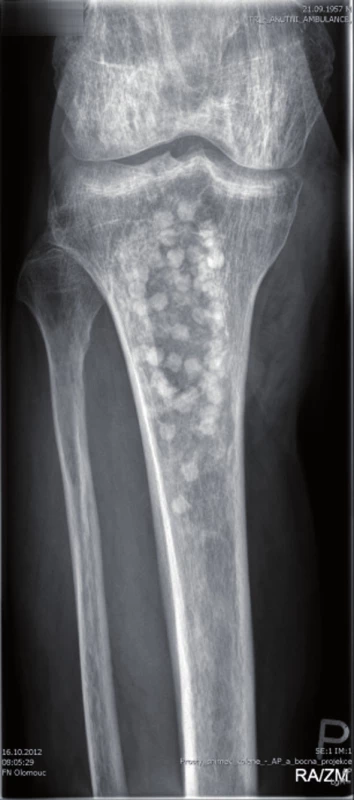
Pooperační antibiotická terapie (Tazobactamum 1,5g + Piperacilinum 12g/den ) nitrožilní cestou byla po dimisi upravena na perorální formu léku Clindamycin 900mg/den, kterou pacient užíval po dobu šesti týdnů. Nyní je pacient 19 měsíců po posledním chirurgickém výkonu laboratorně (CRP 5 mg/l), klinicky i radiologicky bez známek eventuální reinfekce. Postiženou končetinu plně zatěžuje a rozsahy pohybu v kolenním kloubu jsou bez výraznějšího omezení – S 0-0-130 (obr. 5, 6). Kontrolní vyšetření 18F-FDG PET/CT a vyšetření značenými Le 99mTc-HMPAO SPECT/CT neprokázala přítomnost infekce ani vznik pakloubu a rentgenové vyšetření ukázalo částečnou resorbci PerOssalu.
Image 5. Pacient s plnou zátěží končetiny 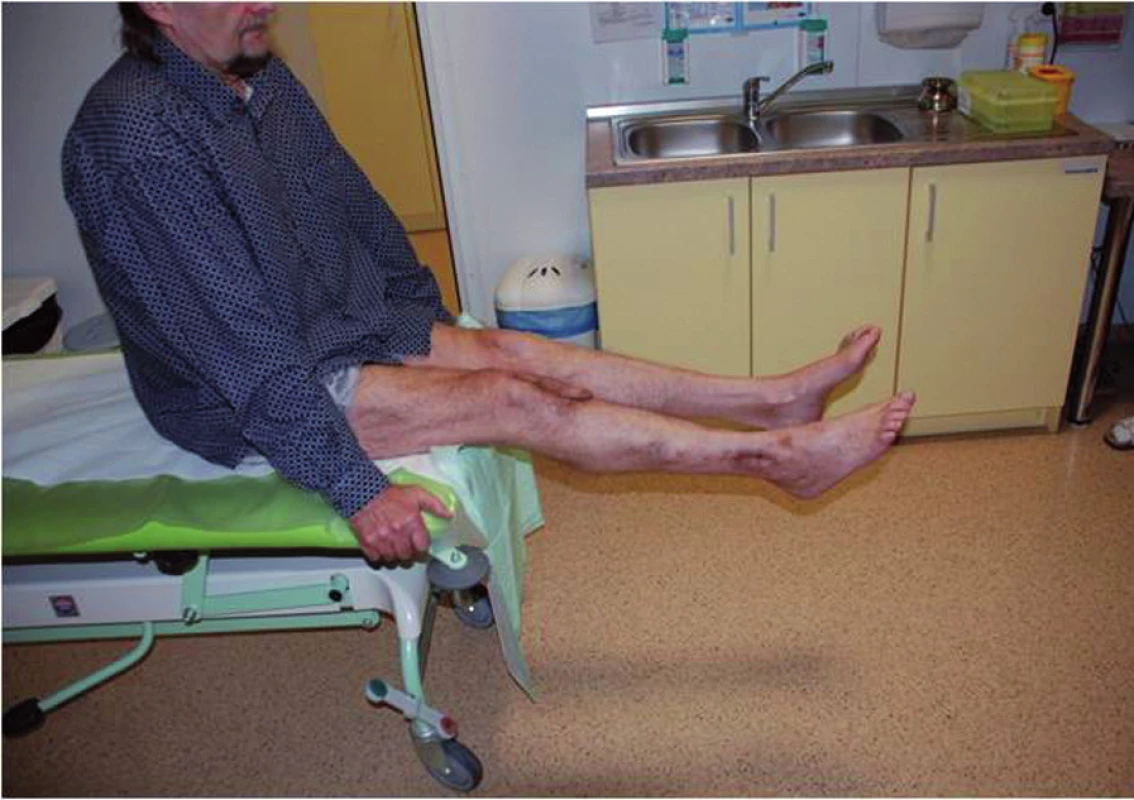
Image 6. Pacient s plnou zátěží končetiny 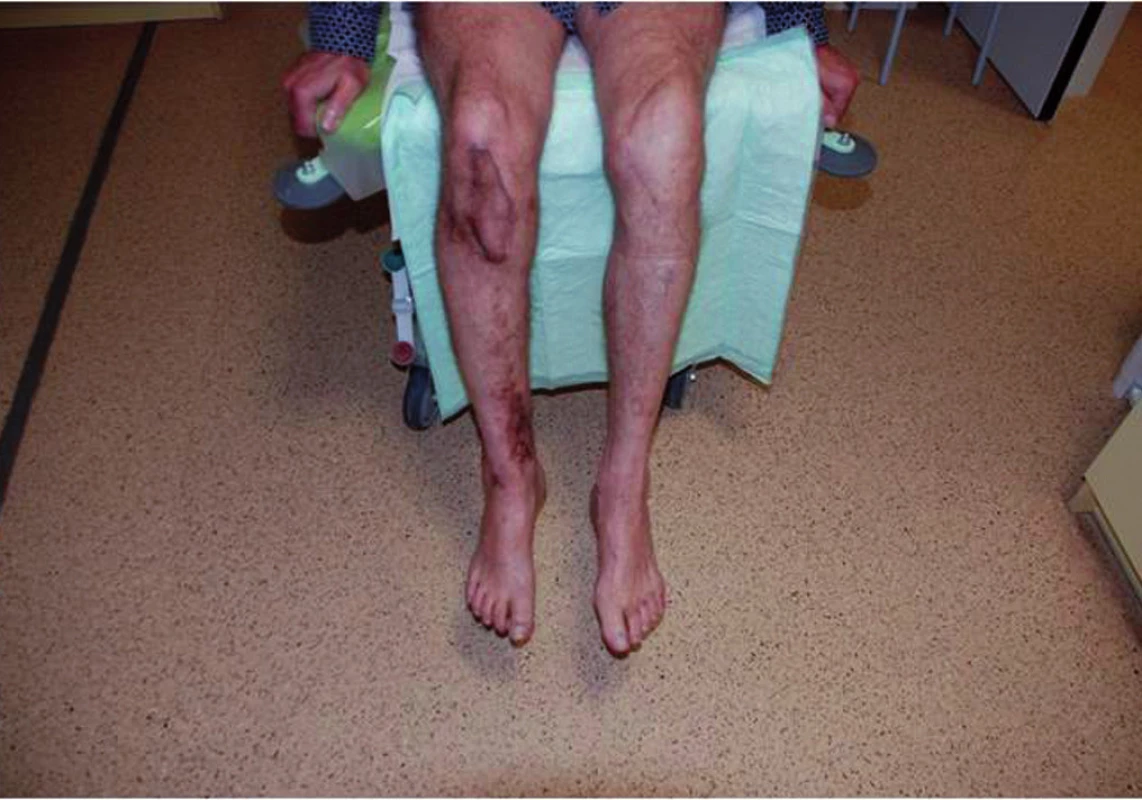
DISKUZE
Klíčovým momentem léčby chronické osteomyelitidy je její správná diagnostika. Autoři klinické, laboratorní, rentgenologické a CT vyšetření doplnili vyšetřením 18F-FDG PET/CT a vyšetřením značenými Le 99mTc-HMPAO SPECT/CT. Literární prameny uvádějí, že vyšetření 18F-FDG PET/CT je vysoce senzitivní a specifická metoda vhodná ke zhodnocení chronické infekce zejména axiálního skeletu. Umožňuje precizní anatomickou lokalizaci infekčního fokusu a demonstruje rozsah chronické osteomyelitidy s vysokým stupněm přesnosti [1, 8, 11]. Vyšetření značenými leukocyty pomocí SPECT/CT má, oproti tomu, vyšší diagnostickou výtěžnost při postižení periferního skeletu [4, 11]. Výhodou obou zmíněných zobrazovacích metod je skutečnost, že vyšetření není limitováno přítomností osteosyntetického materiálu [6].
Sekret ke kultivaci byl odebrán z píštěle a na základě výsledků byla pacientovi nasazena antibiotická terapie. Tento postup je však diskutabilní. Obecně se nedoporučuje volit antibiotickou terapii podle výsledků stěrů z píštěle pro povrchovou kontaminaci, která neodráží hloubkovou kolonizaci rány. Navíc je většina patogenů součástí biofilmu [10]. Proto se za nejcennější pokládá vzorek tkáně z hloubky rány a podle něj se má i volit antibiotická terapie [3,13].
Proplach Pamyconem autoři zvolili ještě ze starších doporučení, která jsou ale v dnešní době změněná.
Po radikálním chirurgickém debridementu byl tzv. mrtvý prostor vyplněn antibiotickým kostním cementem. Při jeho použití je lokální koncentrace antibiotik 1000krát vyšší, než potřebná minimální inhibiční koncentrace pro většinu patogenů, navíc bez výraznějšího uvolňování do systémové cirkulace [12]. Autoři použili Vancogenx, což je v korelaci s literárním doporučením. Také se uvádí i možnost použití PMMA bez přidaných antibiotik [13]. Část Vancogenxu byla nanesena na Prévotův prut. Výhodu této modifikace vidíme v tom, že se tak významně zjednodušuje aplikace i následná extrakce cementu z dřeňové dutiny dlouhých kostí. Kuličky z Vankogenxu si vyrábíme sami těsně před aplikací do nitrodřeňové dutiny na operačním sále.
Po primárním krytí defektů měkkých tkání pomocí V.A.C. systému byl za pět dní defekt kryt rotačním lalokem z mediální hlavy musculi gastrocnemii, což je ve shodě s literárním doporučením. Za ideální čas definitivního krytí defektu měkkých tkání svalovými laloky se uvádí období mezi 6. a 8. dnem od primárního krytí poté, co klinicky a laboratorně došlo k zastavení infekce [13].
Pro nejasné ohraničení nekrotických částí ligamentum proprium patellae byla použita larvální terapie - pomocí larev Lucilia sericata (bzučivka zelená). Larvy svými trávicími šťávami selektivně rozrušují nekrotický materiál, kterým se následně živí. Zdravé tkáně, granulační tkáň i spodina rány zůstávají nepoškozené. Spodina rány je larvami stimulována, dochází k jejímu lepšímu prokrvení a stimulaci tvorby granulační tkáně. Za pět dnů byly larvy odstraněny. Spodina rány byla růžová, bez nekrotických částí. Použití larev pro biochirurgický debridement akutních i chronických ran je možností volby [3]. Sekret, který larvy produkují, je alkalický a obsahuje látky s baktericidními účinky. Ty jsou účinné i u kmenů, které jsou rezistentní vůči léčbě antibiotiky - např. MRSA [2].
Kromě první operační revize, po které se pacientovi nepodávala perorální antibiotika, byla u něj po dalších operačních zákrocích zahájena antibiotická terapie v délce trvání šesti týdnů, což je v korelaci s literárním doporučením [5, 13]. Nezaznamenali jsme žádné komplikace při dlouhodobém užívaní antibiotik. Při osteomyelitidě je doporučováno dlouhodobé podávání antibiotik.
MUDr. Eva Čurlejová
curlejova@yahoo.comw
Sources
1. AKTEKIN , C.M., OZTURK, A.M., TABAK, A.Y. et al. A different perspective for radiological evaluation of experimental osteomyelitis. Skeletal radiol. 2007, 36, 945–950.
2. BAER, W. S. The treatment of chronic osteomyelitis with the Maggot (Larva of the Blow Fly). Clin Orthop Relat Res. 2011, 469, 920–944.
3. BOWLER,P.G., DUERDEN, B.I., ARMSTRONG, D.G. Wound mikrobiology and associated approaches to wound management. Clin Microbiol Rev. 2001, 14, 244-269.
4. CLIMIC, A. Disease of skeletal muscle. In: Kissane, J., editor. Andersons pathology. Vol 2: Mosby. 1985, 1763–1764.
5. FORSBERG, J.A., POTTER, B.K., CIERNY III, G., WEBB, L. Diagnosis and management of chronic infection. J Am Acad Orthop Surg. 2011, 19, 8–19.
6. GOTTHARDT, M., BLEEKER-ROVERS, CH. P., BOERMAN, O. C., OYEN, W. J. G. Imaging of inflamation by PET, conventional scintigraphy, and other imaging techniques. The journal of nuclear medicine. 2010, 51, 1937–1949.
7. GUSTILO, R.B., ANDERSON, J.T. Prevention of infection in the management of one thousand and twenty-five open fractures of long bones. J Bone Joint Surg. 1976, 4, 453–458.
8. HARTMANN, A., EID, K., DORA, C. et al. Diagnostic value of 18F-FDG PET/CT in trauma patiens with suspected chronic osteomyelitis. Eur J Nucl Med Mol Imaging. 2007, 34, 704–714.
9. LABLER, L., KEEL, M., TRENTZ, O. Vacuum-Assisted Closure (V.A.C.) for temporary coverage of soft-tissue injury in type III open fracture of lower extremities. Eur J Trauma. 2004, 30, 305–312.
10. RAO, N., ZIRAN, B. H., LIPSKY, B. A. Treating osteomyelitis: Antibiotics and surgery. Plast Reconstr Surg. 2011, 127, 177–187.
11. TERMAAT, M.F., RAIJMAKERS, P.G.H.M., SCHOLTEN, H.J. The accuracy of diagnostic paging for the assessment of chronic osteomyelitis: A systematic review and Meta-analysis. J Bone Joint Surg Am. 2005, 87, 2464–2471.
12. UÇKAY, I., JUGUN, K., GAMULIN, A. et al. Chronic osteomyelitis. Curr Infect Dis Rep. 2012, 14, 566–575.
13. WALTER, G., KEMMERER, M., KAPPLER, C., HOFFMANN, R. Treatment algorithms for chronic osteomyelitis. Dtsch Arztebl Int. 2012, 109, 257–264.
Labels
Surgery Traumatology Trauma surgery
Article was published inTrauma Surgery

2014 Issue 1-
All articles in this issue
- Možnosti prevence komplikací dlahových osteosyntéz nitrokloubních zlomenin distálního radia
- Využití podtlakové terapie rány při léčbě otevřených zlomenin III. stupně na Traumatologickém centru FN Ostrava
- LÉČBA CHRONICKÉ OSTEOMYELITIDY TIBIE S POUŽITÍM DOČASNÉHO ANTIBIOTICKÉHO SPACERU, ROTAČNÍHO SVALOVÉHO LALOKU, TERAPIE LARVAMI A SPONGIOPLASTIKY S PEROSSALEM – KAZUISTIKA
- JE TLAK V OSE DOLNÍ KONČETINY DOSTAČUJÍCÍ PRO IMITACI ZÁTĚŽE PŘI IMPLANTACI TEP KOLENA?
- Trauma Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Možnosti prevence komplikací dlahových osteosyntéz nitrokloubních zlomenin distálního radia
- LÉČBA CHRONICKÉ OSTEOMYELITIDY TIBIE S POUŽITÍM DOČASNÉHO ANTIBIOTICKÉHO SPACERU, ROTAČNÍHO SVALOVÉHO LALOKU, TERAPIE LARVAMI A SPONGIOPLASTIKY S PEROSSALEM – KAZUISTIKA
- JE TLAK V OSE DOLNÍ KONČETINY DOSTAČUJÍCÍ PRO IMITACI ZÁTĚŽE PŘI IMPLANTACI TEP KOLENA?
- Využití podtlakové terapie rány při léčbě otevřených zlomenin III. stupně na Traumatologickém centru FN Ostrava
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

