-
Medical journals
- Career
Hodnocení bolesti operačních ran po angiochirurgických výkonech
Authors: P. Juřeníková 1; T. Novotný 2; R. Staffa 2; M. Krejčí 2
Authors‘ workplace: Katedra ošetřovatelství a porodní asistence, LF MU, Brno 1; II. chirurgická klinika, Centrum cévních onemocnění, LF MU a FN u sv. Anny v Brně 2
Published in: Cesk Slov Neurol N 2019; 82(Supplementum 1): 44-46
Category: Original Paper
doi: https://doi.org/10.14735/amcsnn2019S44Overview
Cíl: Cílem prospektivní studie bylo zjistit intenzitu pooperační bolesti, vnímání nepříjemnosti pooperační bolesti a celkového životního pocitu v souvislosti s operační léčbou.
Soubor a metodika: Soubor tvořilo 76 pacientů, kteří byli přijati a podstoupili operační intervenci z důvodu aneuryzmatu břišní aorty / pánevní tepny (21,05 %), aneuryzmatu stehenní/ podkolení tepny (23,68 %), aortoilického okluzivního onemocnění (3,95 %) a infraguinálního okluzivního onemocnění (51,32 %). Pacienti hodnotili intenzitu bolesti, nepříjemnost bolesti a celkový životní pocit na Vizuální analogové škále. Hodnocení na škále bylo testováno pro 0. – 7. pooperační den Fisherovým exaktním testem, testem chí-kvadrát pro pohlaví, věk, diagnózu, typ operace, anesteziologické riziko, komorbidity související s operačním výkonem. Pro testování byla stanovena 5% hladina významnosti.
Výsledky: V hodnocení intenzity bolesti, nepříjemnosti bolesti a vnímání celkového životního pocitu byl zjištěn signifikantní rozdíl ve vztahu k typu operačního zákroku, diagnóze.
Závěr: Léčba bolesti je významnou součástí péče o pacienty s pooperační ránou. Pro adekvátní léčbu bolesti je nutné provádět systematické hodnocení bolesti. Nejhůře hodnotili intenzitu bolesti pacienti po revizních operacích, nepříjemnost bolesti a celkový životní pocit pacienti po resekci aneuryzmatu břišní aorty / pánevní tepny, přičemž nejhorší hodnocení bolesti a celkového životního pocitu uvedli pacienti v prvních dnech po operaci. Následně měly hodnoty klesající tendenci.
Tato práce byla podpořena z programového projektu Ministerstva zdravotnictví ČR s reg. č. 15 – 33437A „Vliv edukace na vybrané psychosomatické faktory u pacientů indikovaných k implantaci cévní protézy“. Veškerá práva podle předpisů na ochranu duševního vlastnictví jsou vyhrazena.
Klíčová slova:
hodnocení bolesti – bolest po operaci – operační rána – angiochirurgický výkon
Úvod
Intervence na tepenném systému jsou principiálně dvojího typu – endovaskulární a chirurgické. Předností endovaskulárních metod je menší periprocedurální morbidita, kratší pobyt v nemocnici, menší periprocedurální bolestivost, nevýhodou jsou především horší dlouhodobé výsledky. Nejčastěji jsou léčeny dvě základní skupiny onemocnění – ischemická choroba končetin a tepenná aneuryzmata. Ischemická choroba dolních končetin je onemocnění, kdy z důvodu zúžení nebo uzávěru tepen dochází k nedostatečnému zásobení tkání krví a kyslíkem pro pokrytí jejich potřeb. Důsledkem může být až odumírání jejich částí. Aneuryzma je rozšíření tepny na nejméně 1,5× očekávané normální velikosti. Důsledkem může být prasknutí aneuryzmatu a až život ohrožující krvácení nebo naopak jeho uzávěr s těžkou poruchou prokrvení zásobované části těla [1].
Chirurgický zákrok je vždy ve větší či menší míře spojen s bolestí a její léčba je významnou součástí pooperační péče. Některé studie poukazují na to, že přibližně 20 – 80 % pacientů po operaci trpí mírnou až těžkou pooperační bolestí a prevalence zůstává v posledních dvou desetiletích konzistentně vysoká [2,3]. Systematické hodnocení a dokumentace bolesti pomáhá přesně určit intenzitu a charakter bolesti u jednotlivých pacientů a nastavit účinnou léčbu [4,5]. K hodnocení bolesti lze užívat objektivizující škály. K nejčastěji používaným patří Vizuální analogová škála měření intenzity bolesti (Visual Analogue Scale – Intensity; VAS – I) [6], Vizuální analogová škála nepříjemnosti bolesti (Visual Analogue Scale – Unpleasantness; VAS – U) [7], Numerická vizuální analogová škála (Numeric Rating Scale; NRS) [8], zkrácená verze McGillského dotazníku bolesti (Short-form Mc Gill Pain Questionnaire; SFMPQ) [9].
Léčba bolesti má význam pro hojení ran. Bolest operačních ran vede ke změnám v neuroendokrinních a imunitních funkcích a řada studií prokazuje, že tyto dysregulace mohou přispívat k protrahovanému hojení ran [10 – 15].
Soubor a metodika
Kritériem pro zařazení pacientů do výzkumu bylo dosažení minimálně 24 bodů Mini Mental State Examination a splnění stanovených indikačních kritérií k operaci. S výzkumem souhlasila etická komise zdravotnického zařízení i všichni pacienti, kteří byli do výzkumu zařazení a byli informováni o účelech výzkumného šetření. Soubor tvořilo 76 pacientů, kteří byli přijati a podstoupili intervenční léčbu z důvodu aneuryzmatu břišní aorty / pánevní tepny 21,05 %, aneuryzmatu stehenní/ pokolenní tepny 23,68 %, aortoilického okluzivního onemocnění 3,95 % a infrainguinálního okluzivního onemocnění 51,32 % v období od března 2017 do listopadu 2018 na II. chirurgické klinice FN u sv. Anny v Brně. Pacienti hodnotili intenzitu bolesti, nepříjemnost bolesti a celkový životní pocit na Vizuální analogové škále na speciálně připraveném formuláři. Intenzita bolesti byla hodnocena minimálně 4× denně, nepříjemnost bolesti a celkový životní pocit byly hodnoceny 1× denně. Hodnota byla následně odečtena pomocí pravítka. Hodnocení bolesti na škále bylo testováno pro 0. – 7. pooperační den Fisherovým exaktním testem, testem chí-kvadrát pro pohlaví, věk, diagnózu, typ operace, anesteziologické riziko, komorbidity a komplikace související s operačním výkonem. Pro testování byla stanovena 5% hladina významnosti.
Výsledky
Výzkumu se zúčastnilo 22,37 % (n = 17) žen a 77,63 % (n = 59) mužů. Z celkového počtu 76 pacientů byl proveden u 19,74 % (n = 15) bypass v aorto-ilicko-femorální oblasti, u 32,90 % (n = 25) endarterektomie a plastika tepny, u 18,41 % (n = 14) infrainguinální bypass, u 7,90 % (n = 6) operační revize a u 21,05 % (n = 16) resekce aneuryzmatu a náhrada. Anesteziologickým rizikem dle American Society of Anesthesiologists bylo ve třídě 1 a 2 zařazeno 46,05 % (n = 35) pacientů a ve třídě 3 celkem 53, 95 % (n = 41) pacientů. Nejčastější komorbiditou byla hypertenze u 85,53 % (n = 65) pacientů, hyperlipidémie u 60,53 % (n = 46) pacientů, kuřáků bylo v souboru 35,53 % (n = 27), bývalých tzv. stop kuřáků 47,37 % (n = 36), diabetem mellitem trpělo 32,90 % (n = 25) pacientů. U 10,53 % (n = 8) pacientů se vyskytly komplikace hojení operačních ran (tab. 1).
Table 1. Průměrná hodnota intenzity, nepříjemnosti bolesti a celkového životního pocitu (n = 76 pacientů). 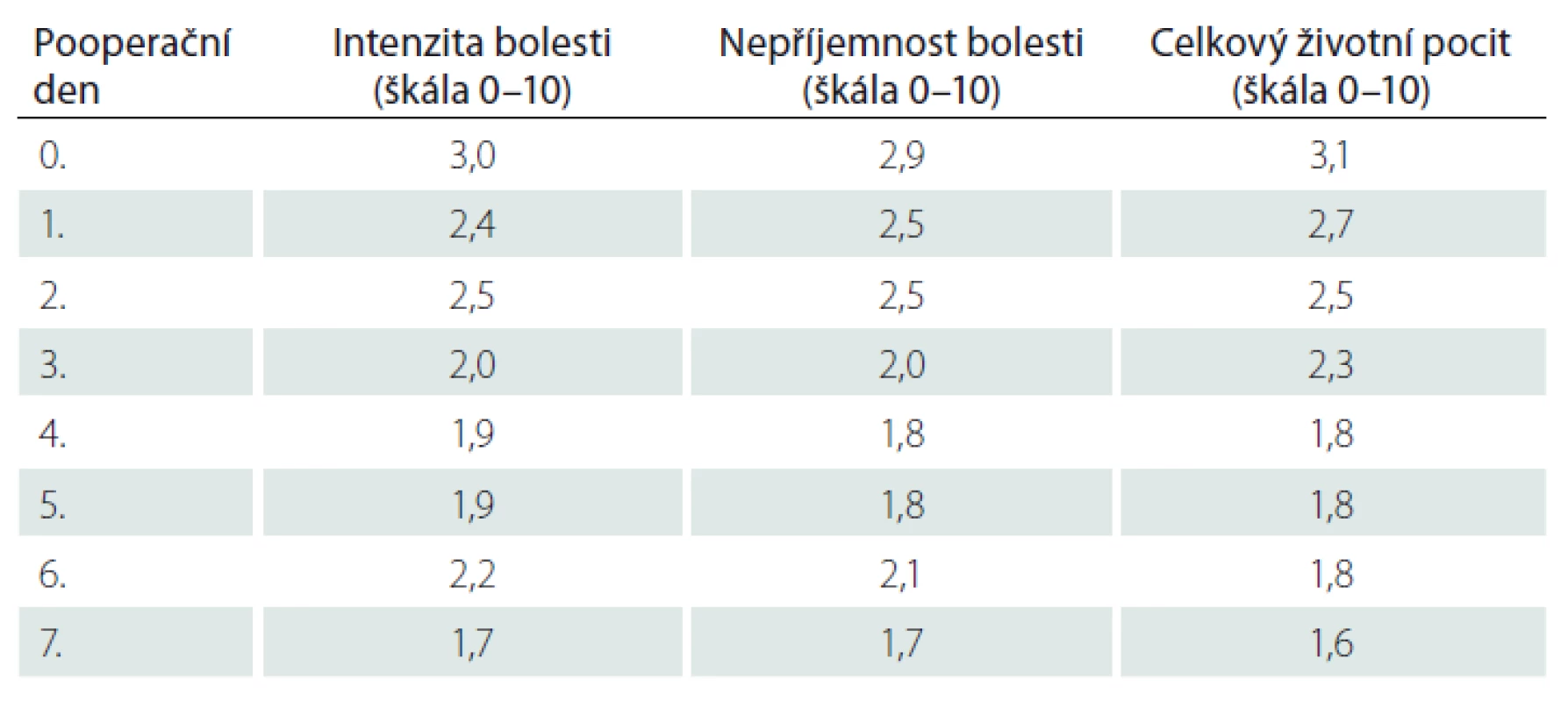
Šestý den se navýšily průměrné hodnoty intenzity a nepříjemnosti bolesti o 0,3 oproti předcházejícímu dni. Ke zvýšení hodnot bolesti došlo z důvodu zintenzivnění mobilizace a rehabilitace.
Signifikance byla zjištěna u hodnocení intenzity bolesti ve vztahu k důvodu operace ve 2. – 5. pooperační den (2. den p = 0,005; 3. den p = 0,000; 4. den p = 0,013; 5. den p = 0,000), přičemž intenzitu bolesti nejhůře hodnotili pacienti přicházející s aneuryzmatem břišní aorty / pánevní tepny. Signifikance byla zjištěna i u hodnocení intenzity bolesti ve vztahu k typu operace ve 2., 3. a 5. pooperační den (2. den p = 0,014; 3. den p = 0,000; 5. den p = 0,013). Nejhůře hodnotili intenzitu bolesti pacienti po revizních operacích.
Signifikance byla zjištěna u hodnocení nepříjemnosti bolesti ve vztahu k důvodu operace ve 2., 3. a 5. pooperační den (2. den p = 0,000; 3. den p = 0,000; 5. den p = 0,009), přičemž nepříjemnost bolesti nejhůře hodnotili pacienti přicházející k operaci z důvodu aortoilického okluzivního onemocnění. Signifikance byla zjištěna i u hodnocení nepříjemnosti bolesti ve vztahu k typu operace 1. – 3. a 5. pooperační den (1. den p = 0,047; 2. den p = 0,000; 3. den p = 0,001; 5. den p = 0,001), přičemž nejhůře hodnotili nepříjemnost bolesti pacienti po resekci aorty.
Signifikance byla zjištěna u hodnocení celkového životního pocitu ve vztahu k důvodu operace 1. – 3. a 5. pooperační den (1. den p = 0,033; 2. den p = 0,000; 3. den p = 0,006; 5. den p = 0,007), vnímání celkového životního pocitu nejhůře hodnotili pacienti přicházející s aneuryzmatem břišní aorty / pánevní tepny. Signifikance byla zjištěna i u hodnocení celkového životního pocitu ve vztahu k typu operace 2., 3. a 5. pooperační den (1. den p = 0,047; 2. den p = 0,000; 3. den p = 0,001; 5. den p = 0,001), přičemž nejhůře hodnotili nepříjemnost bolesti pacienti po resekci aneuryzmatu aorty.
Diskuze
Objevují se důkazy, že bolest hraje důležitou roli v pooperačním hojení ran, kdy bolest je klíčovou proměnnou v pooperačním zotavení [16]. Z těchto důvodů je nutno k léčbě bolesti přistupovat zodpovědně tak, aby byla bolest minimalizována. Případné nedostatečné zvládnutí pooperační bolesti ovlivňuje několik faktorů, a to zejména nedostatečně proškolený personál, nedostatečné znalosti ze strany sester a lékařů, neochotné postoje personálu k pacientům, strach z vedlejších účinků analgetik, nedostatek odpovědnosti při nesprávném hodnocení bolesti [17]. V našem výzkumu se průměrné hodnoty intenzity bolesti pohybovaly od 1,7 do 3,0 (na 10cm škále), přičemž nejhorší hodnocení intenzity bolesti uvedli pacienti v prvních dnech po operaci a následně měly hodnoty klesající tendenci a lze je považovat za uspokojivé. Jako rozhodující pro snížení intenzity bolesti se ukazuje četnost hodnocení bolesti pro získání informací, na jejímž základě se rozhodne o léčbě bolesti [18]. Optimální frekvence měření bolesti není známa a měla by záviset na individuálních potřebách pacienta. Důležité je, že intenzita bolesti se pravidelně vyhodnocuje pomocí standardizovaného měřicího nástroje [19]. V našem případě byla použita VAS – I a VAS – U a měření intenzity bolesti bylo realizováno minimálně 4× denně, což mělo vliv na rozhodnutí o léčbě bolesti. Naše zkušenosti s využitím škály VAS – I, VAS – U ukazují, že jsou vhodné pro identifikaci bolesti, přičemž určitou alternativou může být NRS. Zahraniční studie ukázala vysokou korelaci mezi NRS a VAS – I (rs = 0,84, p < 0,001) [20].
Závěr
Léčba bolesti je významnou součástí pooperační péče. Pro adekvátní léčbu bolesti je nutné provádět systematické hodnocení bolesti s frekvencí odpovídající individuální potřebě pacienta. V našem souboru nejhůře hodnotili intenzitu bolesti pacienti po revizních operacích, nepříjemnost bolesti a celkový životní pocit vnímali nejhůře pacienti po resekci aneuryzmatu břišní aorty / pánevní tepny, přičemž nejhorší hodnocení bolesti a celkového životního pocitu uvedli pacienti v prvních dnech po operaci a následně měly hodnoty klesající tendenci. Správná léčba bolesti přispívá k rychlejšímu hojení operačních ran.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Přijato k recenzi: 30. 6. 2019
Přijato do tisku: 11. 7. 2019
Mgr. Petra Juřeníková, Ph.D.
Ústav zdravotnických věd FHS UTB ve Zlíně
Štefánikova 5670, 760 01 Zlín
e-mail: jurenikova@utb.cz
Sources
1. Juřeníková P, Novotný T, Staffa R et al. Vybraná perioperační problematika cévněchirurgických pacientů. 1. vyd. Brno: Masarykova univerzita 2018.
2. Gan TJ, Habib TE, Miller W et al. Apfelbaum incidence, patient satisfaction, and perceptions of post-surgical pain: results from a US national survey. Curr Med Res Opin 2014; 30(1): 149 – 160. doi: 10.1185/ 03007995.2013.860019.
3. Gerbershagen HJ, Aduckathil S, van Wijck AJ et al. Meissner pain intensity on the first day after surgery: a prospective cohort study comparing 179 surgical procedures. Anesthesiology 2013; 118(4): 934 – 944. doi: 10.1097/ ALN.0b013e31828866b3.
4. Castle NG, Engberg J. Further examination of the influence of caregiver staffing levels on nursing home quality. Gerontologist 2008; 48(4): 464 – 476. doi: 10.1093/ geront/ 48.4.464.
5. Chapman RC, Donaldson WG, Davis JJ et al. Improving individual measurement of postoperative pain: the pain trajectory. J Pain 2011; 12(2): 257 – 262. doi: 10.1016/ j.jpain.2010.08.005.
6. Huskisson EC. Measurement of pain. Lancet 1974; 2 : 1127 – 1131. doi: 10.1016/ s0140-6736(74)90884-8.
7. Price DD, Harkins SW. The affective-motivational dimension of pain: a two stage model. Am Pain Soc J 1992; 1 : 229 – 239.
8. Childs JD, Piva SR, Fritz JM. Responsiveness of the numeric pain rating scale in patients with low back pain. Spine (Phila Pa 1976) 2005; 30(11): 1331 – 1334.
9. Knotek P, Šolcová I, Žalský M. Česká verze krátké formy Dotazníku bolesti McGillovy Univerzity: restandardizace. Bolest 2002; 5(3): 169 – 172.
10. Hlinková1 E, Nemcová J, Simová A et al. The factors of pressure ulcer’s healing in critically ill patients. Cesk Slov Neurol N 2018; 81/ 114 (Suppl 1): S13 – S18. doi: 10.14735/ amcsnn2018S13.
11. Glaser R, Kiecolt-Glaser JK, Marucha PT et al. Stress--related changes in proinflammatory cytokine production in wounds. Arch Gen Psychiatry 1999, 56(5): 450 – 456.
12. Kiecolt-Glaser JK, Marucha PT, Malarkey WB et al. Slowing of wound healing by psychological stress. Lancet 1995; 346(8984): 1194 – 1196. doi: 10.1016/ s0140-6736(95)92899-5.
13. Marucha PT, Kiecolt-Glaser JK, Favagehi M. Mucosal wound healing is impaired by examination stress. Psychosom Med 1998; 60(3): 362 – 365.
14. Padgett DA, Marucha PT, Sheridan JF. Restraint stress slows cutaneous wound healing in mice. BrainBehav Immun 1998; 12(1): 64 – 73. doi: 10.1006/ brbi.1997.0512.
15. Page GG, Ben-Eliyahu S. The immune-suppressive nature of pain. Semin Oncol Nurs 1997; 13(1): 10 – 15.
16. McGuire L, Heffner K, Glaser R et al. Pain and wound healing in surgical patients. Ann Behav Med 2006; 31(2): 165 – 172. doi: 10.1207/ s15324796abm3102_8.
17. Taylor A, Stanbury L. A review of postoperative pain management and the challenges. Curr Anaesth Crit Care 2009; 20(4): 188 – 194. doi: 10.1016/ j.cacc.2009.02.003.
18. van Dijk, WJ, Vervoort SC, van Wijck AJ et al. Postoperative patients’ perspectives on rating pain: a qualitative study. J Nurs Stud 2016; 53 : 260 – 269. doi: 10.1016/ j.ijnurstu.2015.08.007.
19. Meissner W, Coluzzi F, Fletcher D et al. Improving the management of post-operative acute pain: priorities for change. Curr Med Res Opin 2015; 31(11): 2131 – 2143. doi: 10.1185/ 03007995.2015.1092122.
20. Ahlers SJ, van Gulik L, van der Veen AM et al. Comparison of different pain scoring systems in critically ill patients in a general ICU. Crit Care 2008; 12(1): R15. doi: 10.1186/ cc6789.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2019 Issue Supplementum 1-
All articles in this issue
- Znalosti a zvyklosti všeobecných sester v prevenci ran v souvislosti se zdravotnickými prostředky v intenzivní péči – dotazníkový průzkum
- Účinnost komprehenzivního managementu bolesti u obtížně se hojících ulcerací – protokol systematického review
- Podtlaková léčba u pacienta s dekubitem a paraplegií
- Využití podtlakové terapie k řešení ranných komplikací po angiochirurgických výkonech
- Mapování dekubitů a nehojících se ran v medicínském kurikulu
- Kvalita života pacientů s nehojící se ranou
- Hodnocení bolesti operačních ran po angiochirurgických výkonech
- Účinnost hyperbarické oxygenoterapie u obtížně se hojících ulcerací – meta-review
- Hyperbarická oxygenoterapie u obtížně se hojících ulcerací – mechanizmy účinku, současná evropská doporučení a kazuistika
- Využití svalového laloku v rekonstrukci recidivy ischiadického dekubitu
- Role oxidativního stresu v hojení ran – současné poznatky
- Multidisciplinární přístup v chirurgické léčbě dekubitů u pacientů s míšní lézí
- Rizikové faktory u pacientů s dekubity na chirurgickém oddělení
- Pilotní analýza počtu dekubitů – celostátní data v centrálním systému hlášení nežádoucích událostí
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Kvalita života pacientů s nehojící se ranou
- Znalosti a zvyklosti všeobecných sester v prevenci ran v souvislosti se zdravotnickými prostředky v intenzivní péči – dotazníkový průzkum
- Využití podtlakové terapie k řešení ranných komplikací po angiochirurgických výkonech
- Podtlaková léčba u pacienta s dekubitem a paraplegií
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

