-
Medical journals
- Career
Optimalizace léčebného postupu u kožního trofického defektu bérce − pilotní studie chirurgické metody
Authors: I. Slaninka 1,2; L. Klein 1,2; R. Čáp 2,3; F. Hošek 2; I. Guňka 1,2; O. Šedivý 1,2; S. Jiška 1,2; M. Kaška 1,2
Authors‘ workplace: Katedra chirurgie, LF UK v Hradci Králové, vedoucí katedry: doc. MUDr. RNDr. M. Kaška, Ph. D. 1; Chirurgická klinika LF UK a FN Hradec Králové, přednosta kliniky: prof. MUDr. A. Ferko, CSc. 2; Katedra válečné chirurgie, Fakulta vojenského zdravotnictví UO, Hradec Králové vedoucí katedry: doc. MUDr. J. Páral, Ph. D. 3
Published in: Rozhl. Chir., 2015, roč. 94, č. 2, s. 69-73.
Category: Original articles
Overview
Úvod:
Současné medicínské poznatky nám nabízejí široké spektrum možností, jak pečovat o chronickou ránu. Zejména v posledních desetiletích došlo k významnému pokroku na poli jejich léčby. Autoři prezentují svoje poznatky o postupech při péči o pacienta s chronickou ránou a vymezují roli chirurga v procesu její léčby.Metody:
Do pilotní randomizované prospektivní studie byli zařazeni 4 pacienti s chronickou ránou v oblasti bérce po předchozí neúspěšné konzervativní terapii, kteří byli indikováni k autotransplantaci kůže. Po předchozí aplikaci podtlakové terapie (VAC – vacuum asisted closer) byli pacienti podstupující kožní transplantaci pro chronickou ránu v oblasti bérce prospektivně randomizováni do dvou skupin. U jedné skupiny byla použita k podpoře hojení autologní plazma bohatá na trombocyty (PRP) a ve druhé – kontrolní – skupině byla provedena autotransplantace kůže standardně bez její aplikace.Výsledky:
Ve skupině s použitím PRP bylo 15. pooperační den zhojeno v průměru 99 % ranné plochy. Ve skupině bez užití PRP bylo 15. pooperační den zhojeno v průměru 90 % ranné plochy. Ve skupině s použitím PRP došlo u pacientů k úplnému zhojení defektu za 15, resp. 20 dnů po výkonu. Ve skupině bez aplikace PRP došlo u jednoho pacienta k úplnému zhojení za 28 dnů a jednoho k úplnému zhojení nedošlo ani za 3 měsíce po operaci a přetrvávala zbytková nezhojená plocha 10 %.Závěr:
V případě využití metod chirurgické léčby se hojí chronické rány během relativně krátké doby. Na základě prvních zkušeností lze předpokládat, že tuto dobu můžeme ještě zkrátit použitím PRP. Z užití chirurgické léčby a podpory hojení chronických ran pomocí PRP by mohli profitovat pacienti, u kterých selhaly jiné dostupné metody celkové i lokální terapie.Klíčová slova:
plazma bohatá na trombocyty – trombocyty − hojení ran − chronická ránaÚvod
Široké spektrum možností, jak pečovat o chronickou ránu, a odlišný pohled různých specialistů na léčbu pacienta s chronickou ránou ztěžují orientaci v této složité problematice. Chronické rány léčí hlavně chirurgové, dermatologové, praktičtí lékaři, internisté a při domácí péči i střední a nižší zdravotnický personál. Každá specializace je v procesu léčby nezastupitelná a důležitá a optimálního výsledku v léčbě lze dosáhnout často jen na základě mezioborové spolupráce. Doménou chirurgických oborů by měla být hlavně chirurgická léčba a správná lokální terapie.
Pod pojmem lokální terapie ran rozumíme především účelné provádění převazů. Základem je aseptický přístup, kdy po toaletě (ošetření okolí rány a jejím opláchnutí k tomu určeným roztokem) provedeme débridement. Přítomnost nekrotických tkání, buněčného detritu, cizích těles a tekutinových kolekcí je zásadní překážkou pro hojení. Nekrotická tkáň jednak brání granulaci a epitelizaci, jednak je živným médiem pro růst bakterií a rozvoj bakteriální kolonizace rány. Z toho vyplývá, že débridement a nekrektomie jsou pro lokální terapii zásadní. Débridement nejčastěji provádíme i v ambulantních podmínkách mechanicky exkochleací. V případě rozsáhlejší rány s nutností débridement se nevyhneme místní či celkové anestezii. Každá rána má i schopnost samočištění a pomocí proteolytických enzymů může být nekrotická tkáň rozpuštěna. V případě, že pro hojení rány vytvoříme vhodné podmínky podle zásad vlhkého hojení, je možné tímto pro pacienta nejpřijatelnějším způsobem provádět débridement i extenzivněji. Nevýhodou tohoto konzervativního přístupu je delší doba potřebná k vyčištění rány. K podpoře autolytického čištění rány je vhodná mj. i podtlaková terapie (VAC). Ta kromě akcelerace débridement výrazně urychluje i tvorbu granulační tkáně. Podle našich zkušeností je použití podtlakové terapie vhodné hlavně po mechanickém radikálním débridement k podpoře tvorby granulační tkáně jako podkladu pod kožní transplantát.
V současnosti jsou na trhu desítky variant krycích materiálů. Z toho může ale vzniknout problém, jaký materiál použít v dané situaci k léčení konkrétní rány. Při volbě krycího materiálu bychom se měli opírat hlavně o své zkušenosti a možnosti. Stejně důležité je správné vyhodnocení stadia hojení, v němž se rána momentálně nachází, a zhodnocení případné ranné infekce. Závažnost přítomnosti bakterií v chronické ráně se hodnotí dle množství přítomných mikroorganismů a jejich projevů od kontaminace přes kolonizaci až k pokročilému infekčnímu zánětu [1]. U chronické rány dojde v čase téměř vždy k mikrobiální kontaminaci.
Jednou z možností, jak urychlit přihojení kožního transplantátu, je použití plazmy bohaté na trombocyty jako zdroje růstových faktorů. Platelet-rich plasma – PRP je definována jako frakce autologní krve s koncentrací trombocytů, která je vyšší než jejich koncentrace v periferní krvi. V experimentech in vitro se neprokázalo, že vyšší lokální koncentrace trombocytů vede k lepšímu efektu. Za jejich optimální koncentraci v klinické praxi se považují hodnoty asi 2,5 až 5x vyšší, než jaká je standardně tato hodnota v periferní krvi [2]. Terapeuticky se využívá od 80. let 20. století [3]. Za tuto dobu se začala používat v mnoha medicínských oborech, jako jsou maxilo-faciální chirurgie, stomatochirurgie [4,5], ortopedie [6], estetická a rekonstrukční chirurgie [7], popáleninová medicína a další [8]. Stejně tak se opakovaně potvrdil i její příznivý efekt na hojení měkkých i tvrdých tkání.
Významnou metodou léčby chronické rány je terapie celková. I chronické rány mohou mít tendenci ke spontánnímu zhojení při správné celkové terapii – kompenzaci významných systémových onemocnění, ale většina z nich by se bez kombinace s adekvátní lokální terapií hojila velmi dlouho, nebo by se vůbec nezhojila.
Metody
K optimalizaci léčby pacienta s chronickým kožním defektem v oblasti dolní končetiny jsme vypracovali následující léčebný postup. U každého pacienta byla nejdříve zahájena konzervativní terapie spočívající ve správné lokální i celkové léčbě a vyhodnocení etiologie chronické rány. V období 8 měsíců (únor–srpen 2014) jsme zařadili do našeho souboru 4 nemocné. Pacienti byli randomizováni do dvou skupin, přičemž u poloviny z nich byla použita PRP. Při zjištění cévní etiologie defektu nebo v případě neúspěchu konzervativní léčby byl pacient vyšetřen angiologem, resp. cévním chirurgem a při splnění indikačních kritérií byla provedena nejprve cévní intervence. Ta spočívala buď v operaci pro chronickou žilní insuficienci, nebo ischemickou chorobu dolních končetin (operace/PTA). V případě jiné než cévní etiologie bylo přistoupeno k adekvátní kauzální celkové a místní léčbě příslušným specialistou. K urychlení zhojení chronického defektu byl u pacientů proveden za hospitalizace débridement většinou v krátké celkové anestezii a naložena podtlaková terapie (Obr. 1). Po nárůstu granulační tkáně (v průběhu několika dnů) bylo přistoupeno k transplantaci kůže – „meshovaným“ dermo-epidermálním štěpem v poměru 1 : 1,5 (Obr. 2). V prezentovaném souboru byly u dvou pacientů poprvé použity k přípravě PRP plazmy zkumavkový set a centrifuga (TropoCellsTM, Estar Technologies Ltd., Israel). Příprava PRP začínala odběrem venózní krve. Z 10 ml venózní krve lze získat cca 3 ml PRP. Venózní krev byla odebrána do vakuové trubice s antikoagulantem (ACD – Adenine Citrate Dextrose) a separačním gelem (velikost pórů 10 µm). Po 10 minutách odstřeďování při 3600 ot./min. docházelo k separaci erytrocytů, plazmy chudé na trombocyty (PPP – platelet-poor plasma) a trombocytů. Přebytečná plazma (asi 3 ml) byla odebrána a zbylá následně rozmíchána s trombocyty. Tím vznikla PRP, která byla oddělena speciální filtrační trubicí a aplikována v objemu 2–5 ml injekční stříkačkou s tupou jehlou na povrch rány.
Image 1. Pacient č. 3 − chronický kožní defekt po débridement a VAC péči trvající 6 dnů Fig. 1: Patient No. 3 − chronic wound after debridement and 6 days of VAC therapy 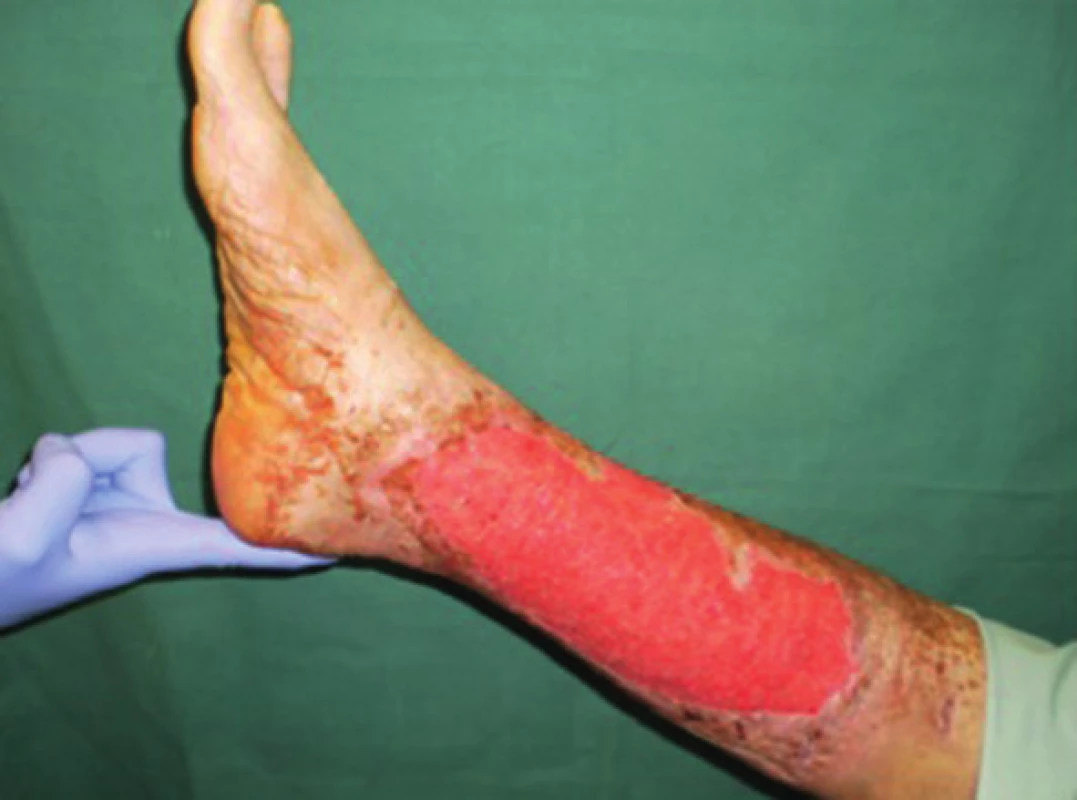
Image 2. Pacient č. 3 − dermoepidermální autotransplantace s použitím autologní PRP Fig. 2: Patient No. 3 − split-thickness skin graft and autologous PRP 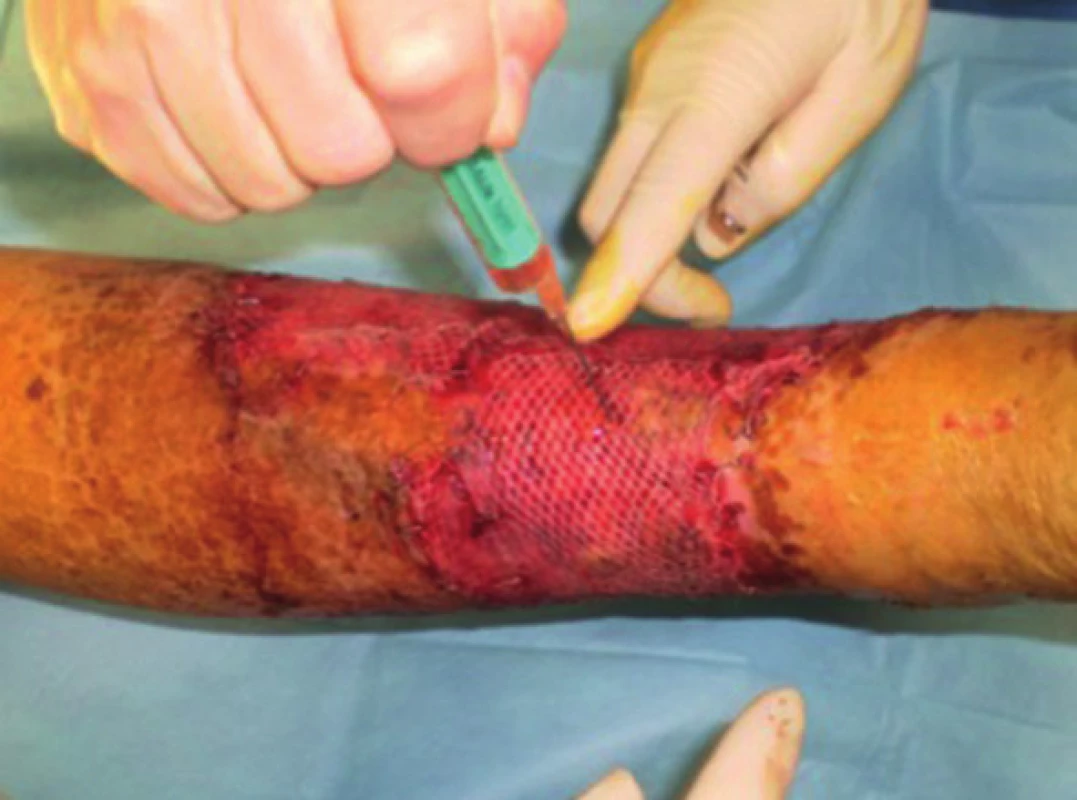
Výsledky
Do studie byli zařazeni celkem 4 pacienti. U dvou pacientů byla k podpoře hojení kožního transplantátu použitá vlastní PRP a u dvou pacientů v kontrolní skupině probíhala operace standardním způsobem bez jejího užití. Sledovali jsme procento zhojené plochy 15. den od výkonu a v dalším období (Tab. 1). Ve skupině s použitím PRP bylo 15. pooperační den zhojeno v průměru 99 % plochy. Ve skupině bez aplikace PRP bylo 15. pooperační den zhojeno v průměru 90 % plochy. Ve skupině s PRP došlo u obou pacientů k úplnému zhojení defektu za 15 a 20 dnů po výkonu (Obr. 3). Ve skupině bez aplikace PRP plazmy došlo u jednoho pacienta k úplnému zhojení za 28 dnů a u druhého nedošlo k úplnému zhojení ani během období 3 měsíců po operaci a přetrvávala zbytková nezhojená plocha 10 % (Obr. 4, 5).
Table 1. Hojení trofického defektu v jeho ploše a v čase Tab. 1: Healing of a trophic defect in its area and time period 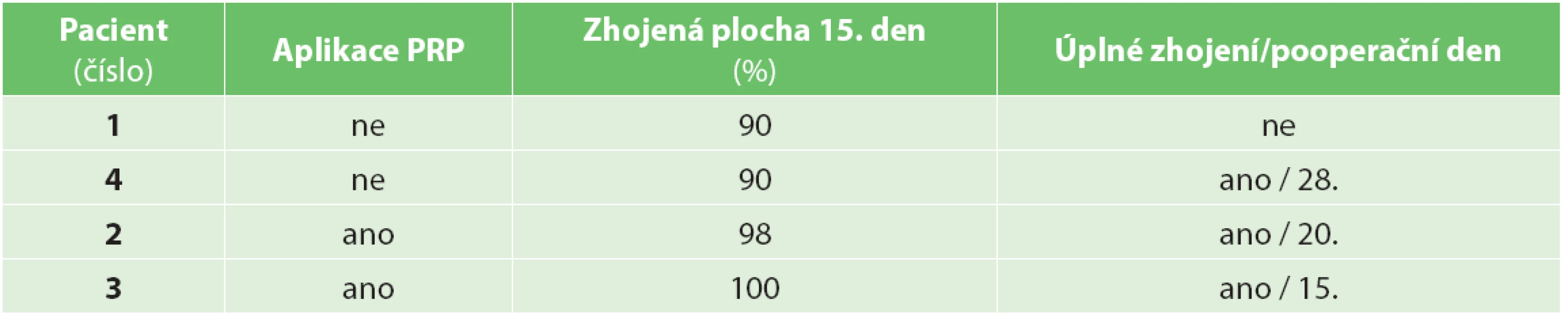
Image 3. Pacient č. 3 − 15. den po operaci s použitím PRP – kompletně zhojeno Fig. 3: Patient No. 3 − 15 days after surgery with PRP – wound completely healed 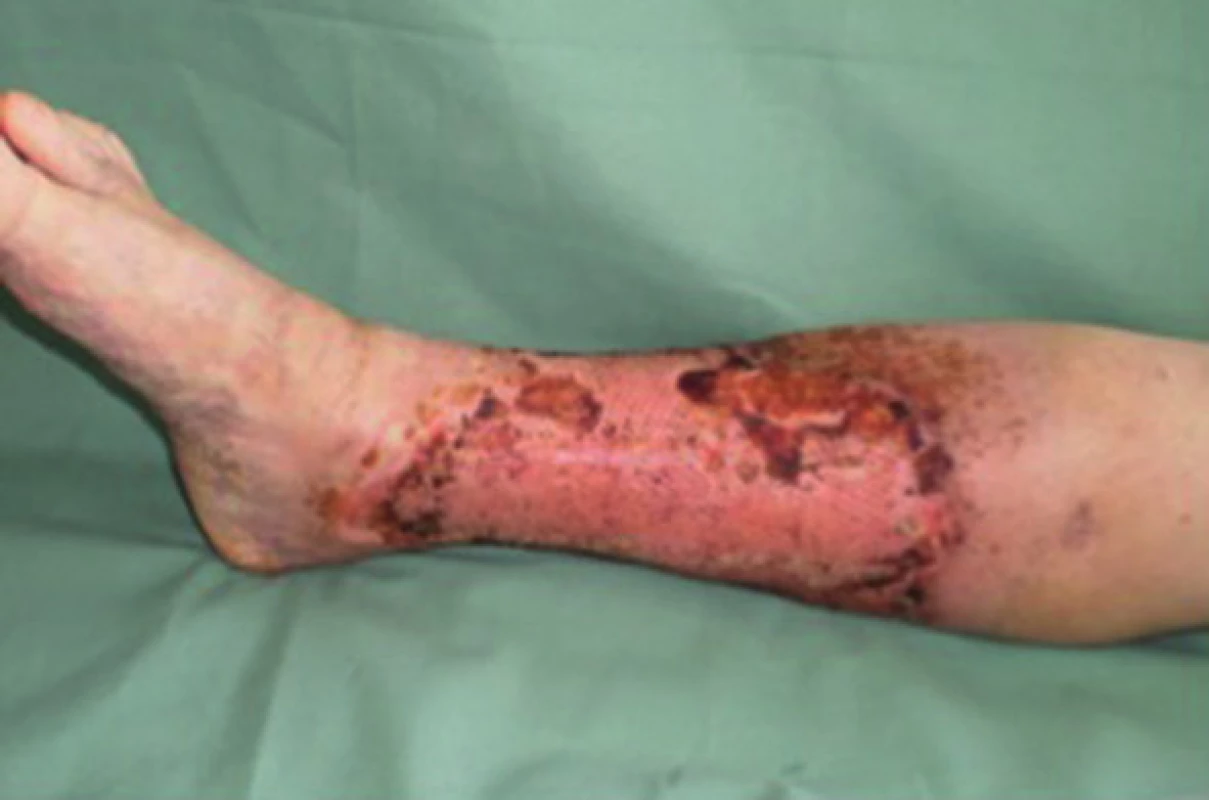
Image 4. Pacient č. 1 − chronický kožní defekt po débridement a VAC terapii trvající 7 dnů Fig. 4: Patient No. 1 − chronic wound after debridement and 7 days of VAC therapy 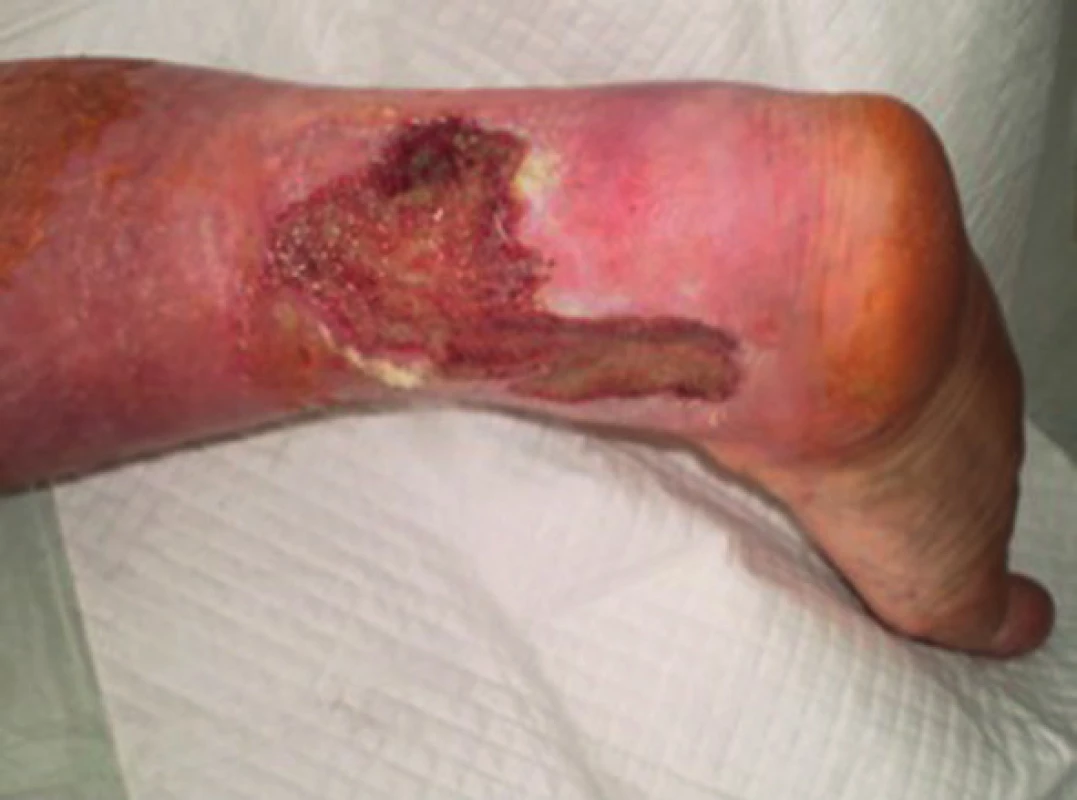
Image 5. Pacient č. 1 −15. den po dermoepidermální transplantaci bez PRP – 90 % defektu zhojeno Fig. 5: Patient No. 1 − 15 days after transplantation without PRP – 90% of the defect healed 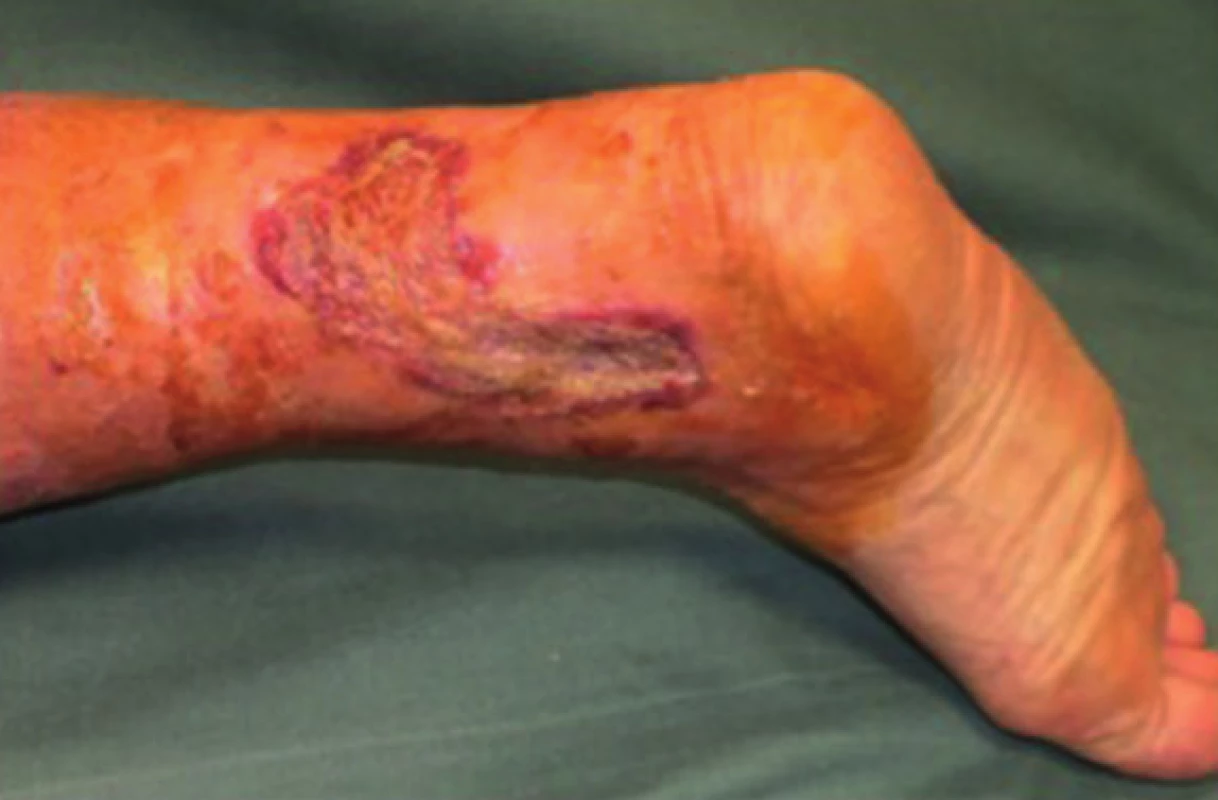
Diskuze
Podstatou účinku PRP je přítomnost vitálních trombocytů v ní. Kromě jejich dobře známé funkce v procesu hemostázy mají ještě významné funkce v angiogenezi, reparaci a hojení tkání. Jsou to první elementy, které se účastní časné zánětové reakce v procesu hojení [9]. Alfa granule, denzní granule a lysozomy obsahují celou řadu nezbytných růstových faktorů, cytokinů, signálních a jiných molekul [10]. Pro hojivý proces se ukazuje jako nejdůležitější přítomnost alfa granulí, ve kterých jsou obsaženy růstové faktory jako například platelet-derived growth factor (PDGF), insulin-like growth factor (IGF1), transforming growth factor-beta 1 (TGF-β1), vascular endothelial growth factor (VEGF), basic fibroblastic growth factor (bFGF) a epidermal growth factor (EGF) [11]. Nemalou úlohu v procesu hojení hrají též katecholaminy, histamin, serotonin, dopamin a ionty kalcia rovněž obsažené v trombocytech. Jejich role spočívá hlavně ve zvýšení permeability kapilár a aktivaci zánětové reakce [12]. Aby mohlo dojít k procesu vyplavení všech výše uvedených faktorů, musejí být trombocyty aktivovány [13]. K aktivaci dochází buď a) adhezí a kontaktem s molekulami endotelu (jako například von Willebrandův faktor, kolagen, fibronektin a laminin), nebo b) kontaktem s trombinem a tromboxanem A2 [14]. Po aktivaci trombocytů dojde k vyplavení přibližně 95 % předsyntetizovaných růstových faktorů do 10 minut, zbylých 5 % se následně syntetizuje a vyplavuje v průběhu jejich dalšího života (5−10 dnů) [13,15].
Právě díky přítomnosti růstových faktorů v procesu hojení ran se ukazuje užití PRP jako jedna z možností, jak urychlit hojení rány, nebo jak umožnit zhojení tam, kde je proces hojení zpomalen nebo zastaven. Její použití vidíme jako optimální tam, kde lze očekávat zpomalené hojení operačních, traumatických ran a popálenin. Během několika desítek let používaní PRP se v mnoha studiích prokázal její příznivý efekt na hojení nejen tvrdých, ale i měkkých tkání [16,17,18]. Stejně tak i řada studií in vitro prokázala jednoznačný příznivý efekt PRP v procesu hojení [19, 20]. Na druhou stranu existují i studie in vivo, které tuto skutečnost nakonec částečně zpochybnily [21,22]. Jako jeden z hlavních faktorů těchto nejednoznačných závěrů vidíme fakt, že proces hojení ran je natolik složitý děj, že pouhé zvýšení koncentrace přítomných růstových faktorů nemusí znamenat i rychlejší hojení, ale může ke zhojení přispět jako jeden z mnoha dalších faktorů.
V naší malé skupině pacientů došlo u skupiny pacientů s použitím PRP nejen k signifikantně urychlenému hojení, ale i k úplnému zhojení chronické rány v poměrně kratším časovém období.
Závěr
Cílem sdělení bylo poukázat na opodstatněnost a efektivitu chirurgické léčby chronických ran a určit význam využití PRP v urychlení a zkvalitnění hojení dermo-epidermálních štěpů u rizikové skupiny starších pacientů. Užití PRP je experimentálně a klinicky zkoušená metoda využívající aplikaci autologních trombocytů a v nich obsažených růstových faktorů a dalších látek s příznivým efektem na hojivý proces a hemostázu. Trombocyty lze získat z venózní krve buď použitím separátoru, nebo její centrifugací. Ta představuje dostupnější a finančně méně náročný způsob jejich selekce. Naše první zkušenosti potvrzují příznivý efekt PRP jednak na rychlejší hemostázu a jednak na akceleraci základních mechanismů hojení rány. Nezanedbatelný je i její příznivý efekt na redukci intenzity bolesti v ráně, do které byla PRP aplikována [20]. Časový faktor při přípravě není zanedbatelný, ale příprava PRP je nyní už finančně i provozně dostupná metoda s ohledem na benefit, který pro pacienta v určitých indikacích může nabídnout.
Tento fakt potvrzují i naše první dílčí zkušenosti. Pro jednoznačný průkaz výše uvedených výhod metodiky s použitím PRP a pro její zavedení do běžné klinické praxe bude zapotřebí ještě zhodnotit výsledky této metody u vyššího počtu pacientů.
Práce je dedikována výzkumnému programu UK PRVOUK P37/04.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
MUDr. Igor Slaninka
Sokolská 581
500 05 Hradec Králové
e-mail: igor.slaninka@fnhk.cz
Sources
1. Wysocki AB. Evaluating and managing open skin wounds: colonization versus infection. AACN Clin Issues 2002;13 : 382−97.
2. Graziani F, Ivanovski S, Cei S, et al. The in vitro effect of different PRP concentrations on osteoblasts and fibroblasts. Clin Oral Implants Res 2006;17 : 212−9.
3. Driver VR, Hanft J, Fylling CP, et al. Autologel Diabetic Foot Ulcer Study Group. A prospective, randomized, controlled trial of autologous platelet-rich plasma gel for the treatment of diabetic foot ulcers. Ostomy Wound Manage. 2006;52 : 68−70.
4. PietrzakWS, Eppley BL. Platelet rich plasma: biology and new technology. J Craniofac Surg 2005;16 : 1043−54.
5. Lindeboom JA, Mathura KR, Aartman IH, et al. Influence of the application of platelet-enriched plasma in oral mucosal wound healing. Clin Oral Implants Res 2007;18 : 133−9.
6. Wrotniak M, Bielecki T, Gazdzik TS. Current opinion about using the platelet-rich gel in orthopaedics and trauma surgery. Ortop Traumatol Rehabil 2007;9 : 227−38.
7. Frechette JP, Martineau I, Gagnon G. Platelet-rich plasmas: growth factor content and roles inwound healing. JDent Res 2005;84 : 434−9.
8. Bhanot S, Alex JC. Current applications of platelet gels in facial plastic surgery. Facial Plast Surg 2002;18 : 27−33.
9. Nachman RL, Rafii S. Platelets, petechiae, and preservation of the vascular wall. The New England Journal of Medicine 2008;359 : 1261−70.
10. Rendu F, Brohard-Bohn B. The platelet release reaction: granules’ constituents, secretion and functions. Platelets 2001;12 : 261−73.
11. Anitua E, Andia I, Ardanza B, et al. Autologous platelets as a source of proteins for healing and tissue regeneration. Tromb Haemost 2004;91 : 4−15.
12. Qureshi AH, Chaoji V, Maiguel D, et al. Proteomic and phospho-proteomic profile of human platelets in basal, resting state: insights into integrin signaling. PLoS One 2009;4:e7627.
13. Sánchez-González DJ, Méndez-Bolaina E, Trejo-Bahena NI. Platelet-rich plasma peptides: key for regeneration. Int J Pept 2012;2012 : 532519.
14. Borregaard N, Cowland JB. Granules of the human neutrophilic polymorphonuclear leukocyte. Blood 1997;89 : 3503−21.
15. Cole BJ, Seroyer ST, Filardo G, et al. Platelet-rich plasma: where are we now and where are we going? Sports Health 2010;2 : 203−10.
16. Stryja J. The use of platelet-rich fibrin in the complex treatment of crural ulcer – case report. Hojení ran 2012;6 : 17−21.
17. Dionyssiou D, Demiri E, Foroglou P, et al. The effectiveness of intralesional injection of platelet-rich plasma in accelerating the healing of chronic ulcers. An experimental and clinical study. Int Wound J 2012;10 : 1111 : 17.
18. Sakata J, Sasaki S, Handa K, et al. A retrospective, longitudinal study to evaluate healing lower extremity wounds in patients with diabetes mellitus and ischemia using standard protocols of care and platelet-rich plasma gel in a Japanese wound care program. Ostomy Wound Manage 2012;58 : 36−49.
19. Shengyun H, Zuolin W. Platelet-rich plasma-derived growth factors promotes osteogenic differentiation of rat muscle satellite cells: in vitro and in vivo studies. Cell Biol Int 2012;36 : 1195−1205.
20. Klosová H. Operační léčba hlubokých popálenin kombinací dermoepidermální autotransplantace a lokální transplantace koncentrátu autologních trombocytů. Hradec Králové, 2014. Doktorská disertační práce, Univerzita Karlova v Praze, Lékařská fakulta v Hradci Králové.
21. Abate M, Di Gregorio P, Schiavone C, et al. Platelet rich plasma in tendinopathies: how to explain the failure. Int J Immunopathol Pharmacol 2012;25 : 325−34.
22. Casati MZ, de Vasconcelos Gurgel BC, Gonçalves PF, el al. Platelet-rich plasma does not improve bone regeneration around peri-implant bone defects-a pilot study in dogs. Int J Oral Maxillofac Surg 2007;36 : 132−6.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2015 Issue 2-
All articles in this issue
- Přehled metod primárního uzávěru střední sternotomie
-
Uzávěr laparotomie – víme jak?
(Doporučení Evropské kýlní společnosti) - Transanální totální mezorektální excize pro karcinom distálního rekta – první výsledky
- Optimalizace léčebného postupu u kožního trofického defektu bérce − pilotní studie chirurgické metody
- Zriedkavá náhla brušná príhoda – gangréna kolonu ako komplikácia systémového lupus erythematosus
- Synoviální sarkom jater – kazuistika
- Raritní nález metastázy světlobuněčného karcinomu z renálních buněk v terénu polynodózní strumy
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue-
Uzávěr laparotomie – víme jak?
(Doporučení Evropské kýlní společnosti) - Přehled metod primárního uzávěru střední sternotomie
- Synoviální sarkom jater – kazuistika
- Transanální totální mezorektální excize pro karcinom distálního rekta – první výsledky
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

