-
Medical journals
- Career
Aflibercept v klinickej praxi
Authors: J. Bajaček; A. Bieliková
Authors‘ workplace: Oftalmologická klinika, Ústredná vojenská nemocnica SNP-FN, Ružomberok, prednostka kliniky MUDr. Bieliková Anna, PhD.
Published in: Čes. a slov. Oftal., 71, 2015, No. 2, p. 101-108
Category: Original Article
Overview
V tomto článku sme sa snažili zhodnotiť prvé klinické skúsenosti s účinnosťou a bezpečnosťou afliberceptu v liečbe vlhkej formy vekom podmienenej degenerácie makuly u všetkých typov subretinálnych neovaskulárnych membrán za obdobie prvých 10 mesiacov liečby na našom pracovisku.
Kľúčové slová:
aflibercept, vlhká forma vekom podmienenej degenerácie makuly, subretinálna neovaskulárna membránaÚVOD
Vekom podmienená degenerácia makuly (VPDM), najmä jej pokročilá neovaskulárna forma, je jedna z hlavných príčin ireverzibilnej straty zraku vo vyspelých krajinách a tretia najčastejšia príčina ireverzibilnej straty zraku na celom svete [2, 8]. Väčšina pacientov s neliečenou vlhkou formou VPDM zaznamená progresiu do ťažkej straty centrálnej zrakovej ostrosti na postihnutom oku do 2 rokov od stanovenia diagnózy [1].
Vlhká forma VPDM podstatne znižuje kvalitu života, súvisiacu aj nesúvisiacu, so zrakom a má veľký vplyv na nezávislosť pacienta a na jeho fyzické, emocionálne a sociálne zdravie [13]. Ekonomická záťaž spojená so stratou zraku v dôsledku vlhkej formy VPDM je veľmi veľká, predstavuje oftalmologickú zdravotnú starostlivosť, ale aj náklady, ktoré nesúvisia so zrakom, sú však spojené s pádmi a zlomeninami a z nich vyplývajúceho postihnutia, hospitalizácií, opatrovníctva a domácej ošetrovateľskej starostlivosti [12].
Kľúčovú úlohu pri rozvoji chorioidálnej neovaskularizácie v patogenéze vlhkej formy VPDM zohrávajú podľa najnovších poznatkov dva dôležité proteíny zo skupiny vaskulárnych endoteliálnych rastových faktorov (VEGF): VEGF-A a placentárny rastový faktor (PlGF). Anti-VEGF liečba predstavuje v súčasnosti štandard starostlivosti o pacientov s vlhkou formou VPDM. V klinickej praxi používané anti-VEGF terapie pegaptanib sodný, ranibizumab a bevacizumab (používaný off-label = mimo schválenej indikácie) pôsobia proti rastovému faktoru VEGF-A a umožňujú pacientom vyhnúť sa strate zraku, dokonca u mnohých aj zlepšiť zrakovú ostrosť. Výsledky klinických skúšaní preukázali, že proaktívny prístup k liečbe (fixné mesačné dávkovanie) intravitreálnou anti-VEGF terapiou (ranibizumab alebo bevacizumab) prináša počas prvého roka lepšie výsledky zrakovej ostrosti ako reaktívny prístup (liečba podľa potreby, založená na klinických kritériách) [6].
V minulom roku bol na Slovensku uvedený aflibercept, ide o rozpustný, plne humánny, falošný receptorový fúzny proteín, ktorý je tvorený časťami extracelulárnych domén prirodzených receptorov 1 a 2 pre ľudský VEGF, spojenými s Fc časťou ľudského imunoglobulínu (Ig) G1 [14]. Aflibercept sa viaže na VEGF-A aj PlGF s vyššou afinitou ako ranibizumab [7, 9]. Táto posilnená väzobná afinita naznačuje, že aflibercept môže mať dlhšie trvanie účinku a vyššiu účinnosť v oku, čo umožňuje menej časté dávkovanie a zníženie záťaže pravidelného mesačného monitorovania pacientov s vlhkou formou VPDM.
Na základe pozitívnych výsledkov z registračných štúdií u pacientov s vlhkou formou VPDM, vylepšenému mechanizmu účinku afliberceptu a jeho kategorizovania pre liečbu vlhkej formy VPDM od októbra 2013 v aplikačných centrách na Slovensku, sme sa rozhodli zhodnotiť jeho prínos v klinickej praxi na našom pracovisku. V nasledujúcich kazuistikách uvádzame príklady účinnosti a bezpečnosti afliberceptu po 10 mesiacoch liečby u novodiagnostikovanej vlhkej formy VPDM a tiež u pacientky s refraktérnou subretinálnou neovaskulárnou membránou, ktorá reagovala suboptimálne na predchádzajúcu anti-VEGF liečbu. Centrálna zraková ostrosť bola hodnotená pomocou ETDRS optotypu a centrálnu hrúbku sietnice sme hodnotili pomocou spectral domain OCT.
Dnes je injekčný roztok afliberceptu indikovaný na liečbu vlhkej formy vekom podmienenej makulárnej degenerácie a ďalších sietnicových ochorení – makulárny edém v dôsledku oklúzie centrálnej žily sietnice a diabetický makulárny edém [14].
KAZUISTIKA 1
V septembri 2013 prichádza na našu ambulanciu 77-ročný pacient na OCT vyšetrenie, odoslaný od spádového oftalmológa pre podozrenie na subretinálnu neovaskulárnu membránu (SRNM) na pravom oku. Pacient približne pol roka udáva postupné zhoršovanie zraku na pravom oku a asi mesiac trvajúce metamorfopsie. Pri prvom našom vyšetrení zisťujeme na pravom oku centrálnu zrakovú ostrosť (CZO): 20/80 – 52 písmen ETDRS optotypu, na ľavom oku CZO: 20/25 – 79 písmen ETDRS optotypu a pozitívny test na Amslerovej mriežke. Fundoskopicky vidieť v centrálnej oblasti početné tvrdé i mäkké drúzy, edém aj abláciu neuroretiny v centre makulárnej krajiny (MK) (obr. 1). Na OCT náleze nachádzame subfoveolárne abláciu retinálneho pigmentového epitelu (RPE) aj seróznu abláciu neuroretiny s edémom a výrazné defekty v RPE aj do periférie MK (obr. 2). Pacientovi realizujeme aj FAG vyšetrenie, ktoré nám potvrdzuje predominantne klasickú SRNM (obr. 3a + 3b). Pacienta sme nastavili na intravitreálnu liečbu afliberceptom v dávkovacom režime á 4 týždne počas prvých 3 mesiacov liečby, po ktorých nasledovali ďalšie 3 dávky v intervaloch á 8 týždňov. Na posledné kontrolné vyšetrenie, mesiac po šiestej aplikácii, prichádza pacient v auguste 2014 s CZO 20/63 – 62 písmen ETDRS optotypu, na OCT náleze vidieť miernu regresiu ablácie RPE, výraznú regresiu seróznej ablácie neuroretiny so zbytkovým edémom a viditeľnejšiu foveolárnu depresiu (obr. 4). Pacientovi bolo objednané pokračovanie intrevitreálnej liečby afliberceptom á 8 týždňov.
Image 1. Farebný snímok fundu pravého oka. V makulárnej oblasti sú početné tvrdé i mäkké drúzy s edémom 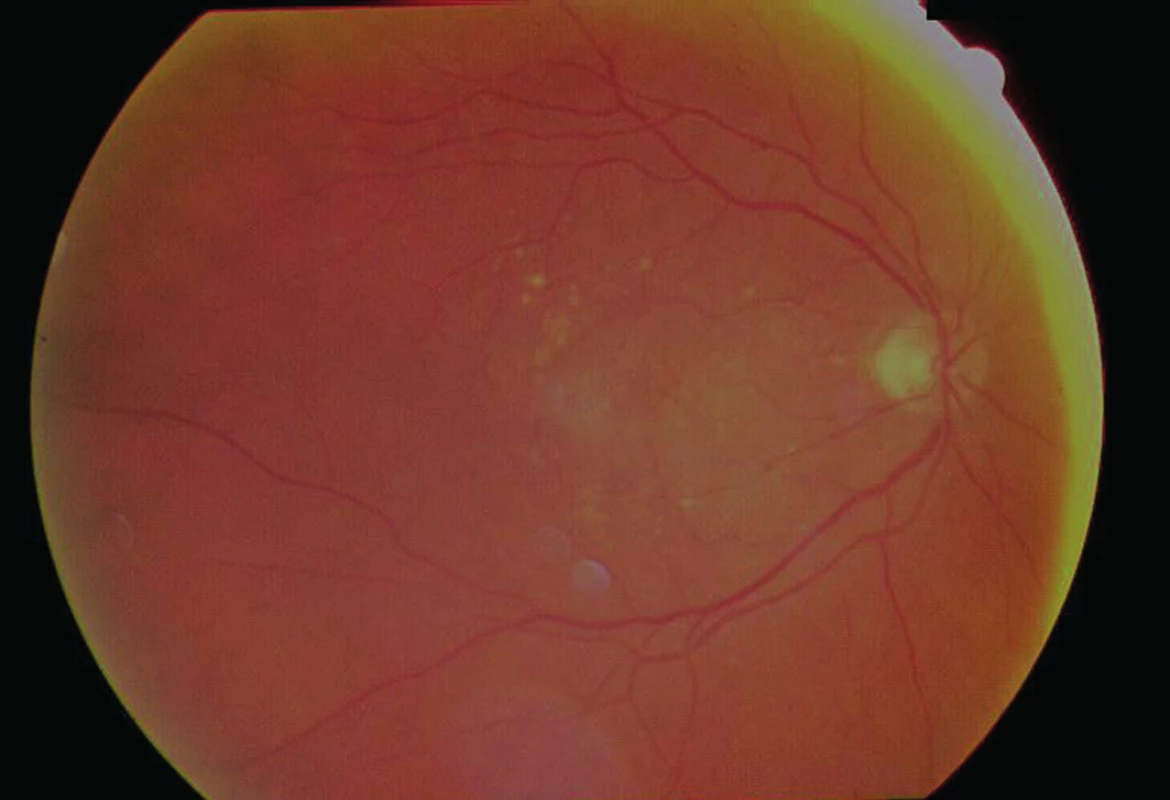
Image 2. OCT snímok (HD cross-line) pravého oka. Subfoveolárne výrazná serózna ablácia neuroretiny s edémom aj s abláciou RPE 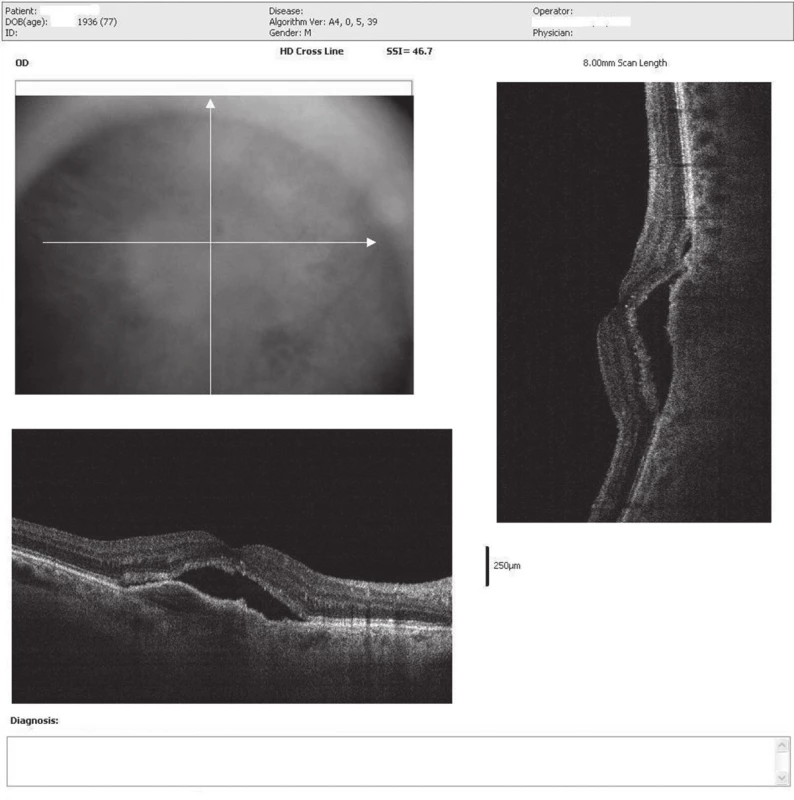
Obr. 3a, b FAG snímky pravého oka. V MK oblasti početné hyperfluorescenčné ložiská pre stázu a presakovanie kontrastnej látky v miestach edému a ablácie neuroretiny. V okolí hyperfluorescenčné drúzy 
Image 3. OCT snímok pravého oka (porovnávacia mapa po 10 mesiacoch od začatia liečby afliberceptom). Výrazná regresia edému aj seróznej ablácie neuroretiny. CHS -205μm. Ablácia RPE pretrváva 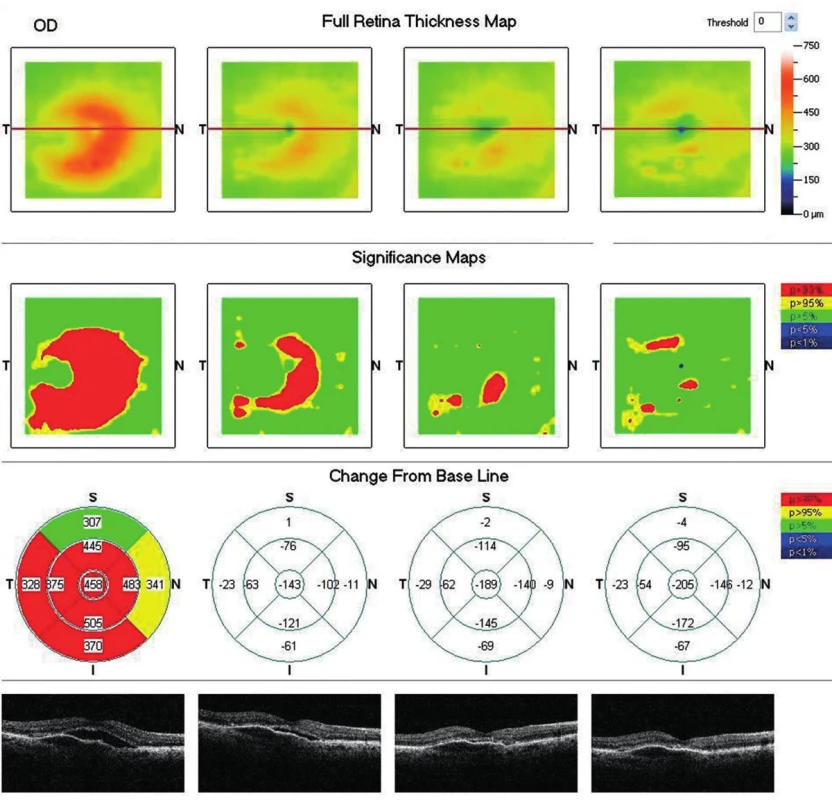
KAZUISTIKA 2
V júni 2011 prichádza na našu ambulanciu 80-ročná pacientka odoslaná z iného aplikačného centra za účelom pokračovania anti-VEGF liečby do ľavého oka. Na primárnom pracovisku bol pacientke pre klasickú SRNM intravitreálne aplikovaný 10x pegaptanib á 6 týždňov so stabilnou centrálnou zrakovou ostrosťou (CZO 20/32 – 72 písmen ETDRS optotypu ) aj hrúbkou sietnice na OCT (obr. 5). Na pravom oku mala pacientka dlhodobo redukovaný vízus - prsty pred okom, pre jazvovité štádium SRNM. Po angiografickom vyšetrení (obr. 6, obr. 7a + 7b) sme pacientku nastavili na intravitreálnu liečbu ranibizumabom á 4 týždne. V priebehu 2 rokov jej bolo aplikovaných celkom 15 dávok ranibizumabu s postupne zhoršujúcou sa CZO až na 20/125 – 41 písmen ETDRS optotypu, pričom na OCT náleze pretrvávali výraznejšie atrofické zmeny v retinálnom pigmentovom epiteli (RPE) s edémom neuroretiny s maximom v dolných nazálnych sektoroch a v mieste fovey až makrocystické zmeny (obr. 8). Vzhľadom na zhoršujúci sa vízus, progresiu nálezu na OCT (obr. 9) a možnosť objednať novú dostupnú anti-VEGF liečbu pre vlhkú formu VPDM, sme po kontrolnom angiografickom vyšetrení pacientku indikovali na intravitreálnu liečbu afliberceptom 2 mg v dávkovacom režime á 4 týždne počas prvých 3 mesiacov liečby, po ktorých nasledovali ďalšie 3 dávky v intervaloch á 8 týždňov. Na poslednom kontrolnom vyšetrení po 6 dávkach afliberceptu má pacientka CZO 20/63 – 62 písmen ETDRS optotypu a na OCT náleze vidieť regresiu edému neuroretiny (obr. 10). Vzhľadom na zlepšenie anatomického aj funkčného nálezu bolo pacientke objednané pokračovanie intravitreálnej liečby afliberceptom v intervale á 8 týždňov.
Image 4. OCT snímok (mapa) ľavého oka. Výrazné defekty, atrofické zmeny RPE prevažne subfoveolárne, s edémom aj seróznou abláciou neuroretiny prevažne v nazálnych sektoroch. Nález po 10 intravitreálnych aplikáciách pagaptanibu 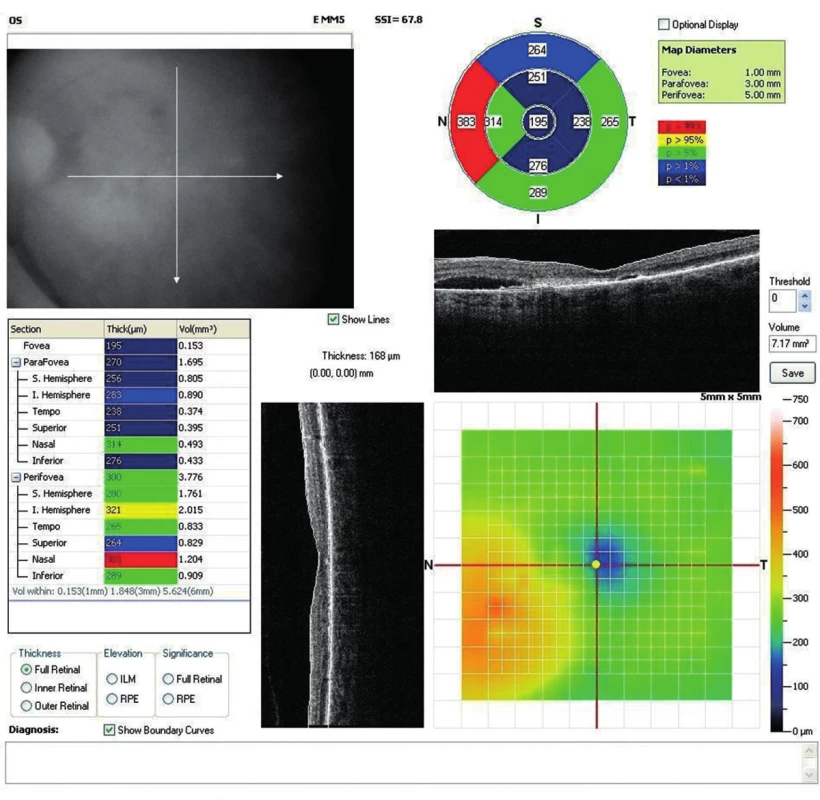
Image 5. Farebný snímok ľavého oka klasickej SRNM 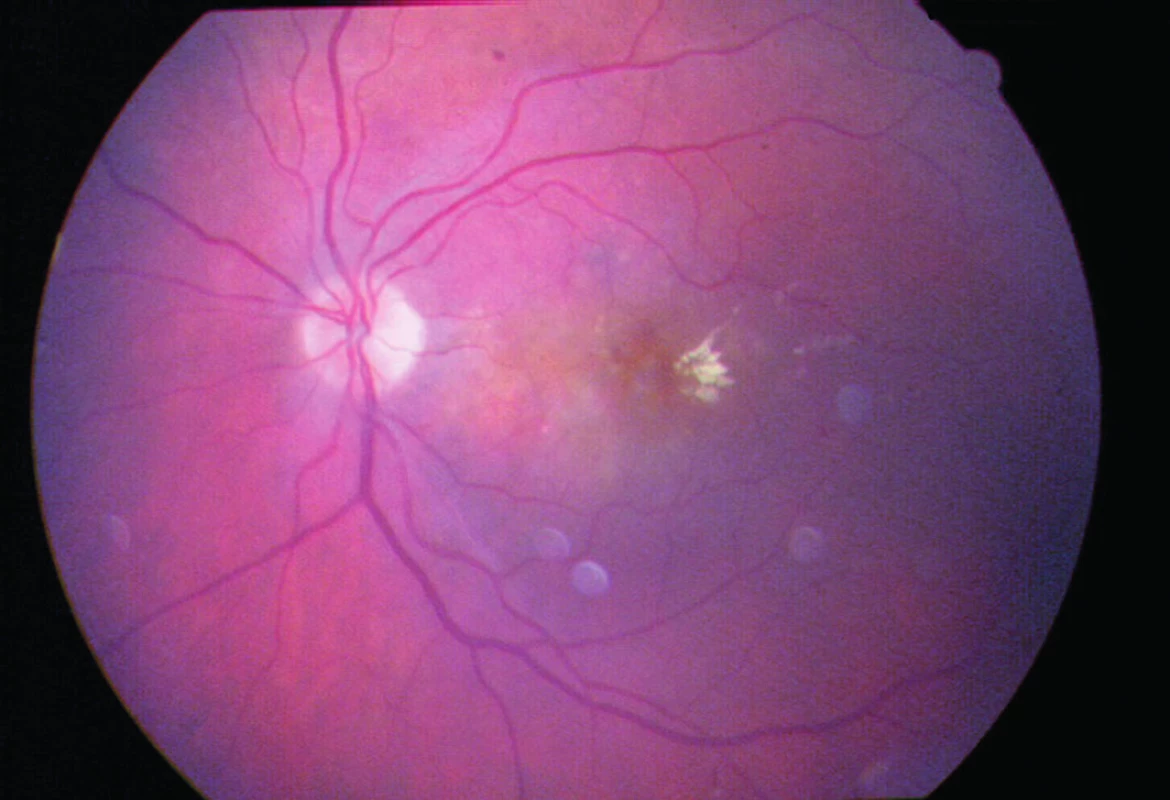
Obr. 7a, b FAG snímky ľavého oka klasickej SRNM 
#obr:7#
Image 6. OCT snímok (mapa) ľavého oka. Výrazný edém neuroretiny s makrocystickou premenou v mieste fovey. Výrazné atrofické zmeny RPE, až počínajúca fibrotická premena. Nález po 15 intravitreálnych dávkach ranibizumabu 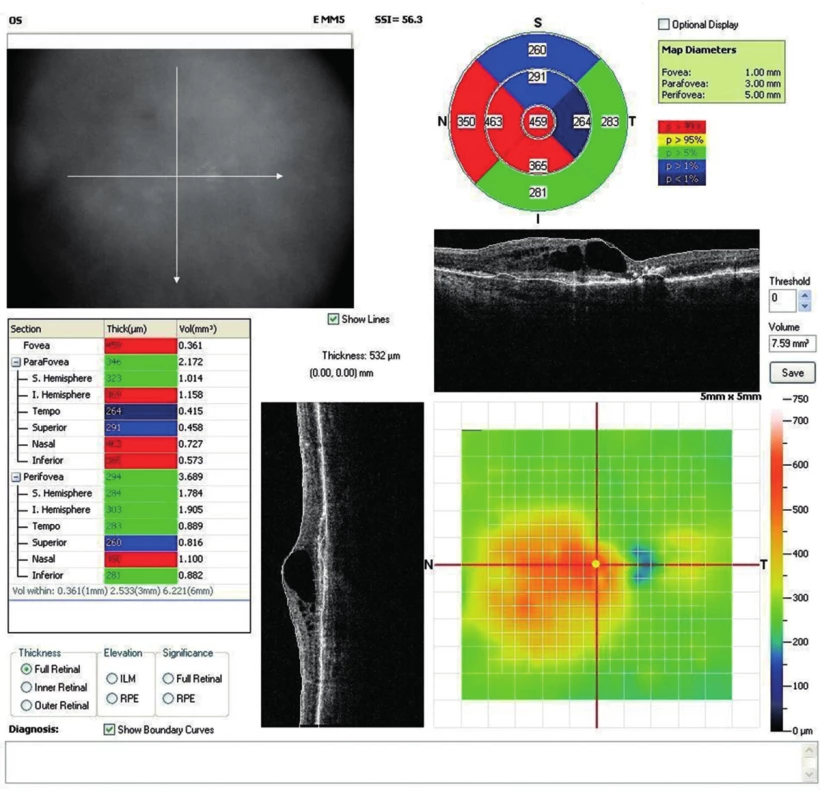
Image 7. OCT snímok (porovnávací – po 2 rokoch liečby ranibizumabom). Progresia edému neuroretiny aj hrúbky sietnice – CHS: +265 μm 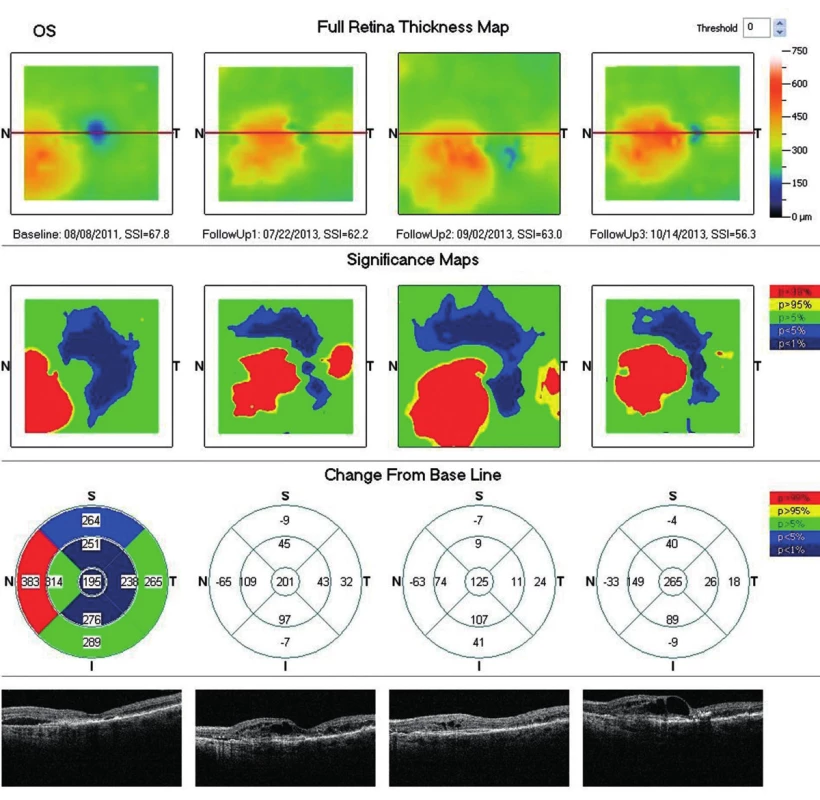
Image 8. OCT snímok (porovnávací – po 10 mesiacoch liečby afliberceptom). Regresia edému neuroretiny aj hrúbky sietnice – CHS: -242 μm 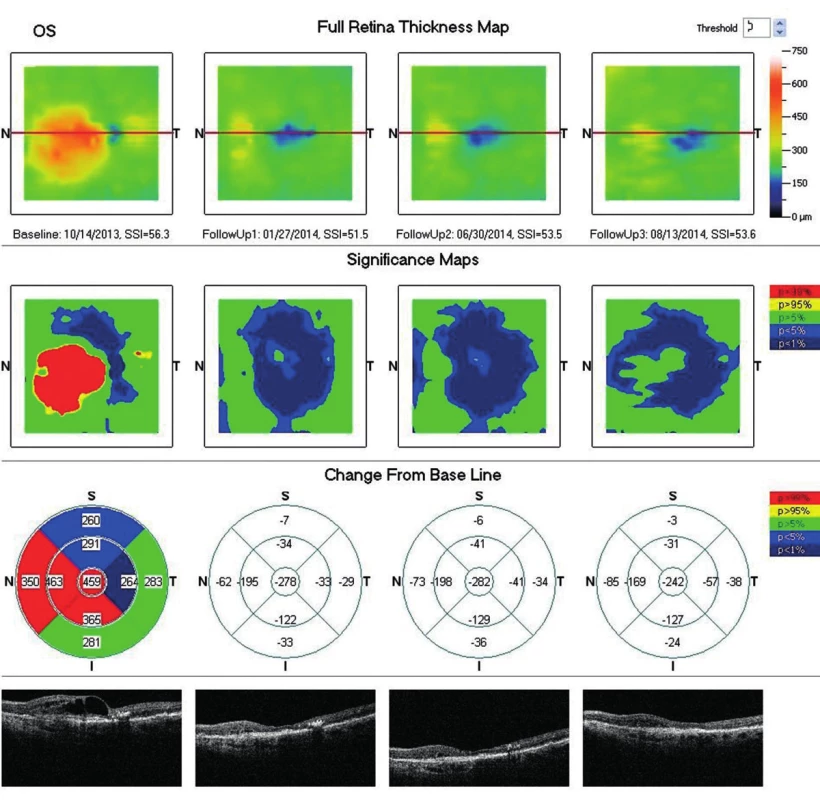
DISKUSIA
Na základe výsledkov klinických skúšaní 3. fázy VIEW1 a VIEW2 u novodiagnostikovaných pacientov s vlhkou VPDM má aflibercept 2 mg podávaný každé 2 mesiace (po 3 úvodných dávkach raz mesačne) štatisticky porovnateľnú a klinicky rovnocennú účinnosť ako ranibizumab 0,5 mg podávaný raz mesačne v zmysle prevencie straty zraku, zlepšenia zrakovej ostrosti, zmenšenia rozsahu chorioidálnej neovaskularizácie, zmenšenia hrúbky sietnice a zmenšenia množstva tekutiny v sietnici po 1 roku [3]. V 52. týždni bola pri liečbe afliberceptom v spomínanom dávkovaní priemerná zmena zrakovej ostrosti +8,4 písmen na ETDRS optotype v porovnaní so vstupnou hodnotou [3]. Funkčné aj anatomické výsledky liečby vlhkej formy VPDM boli dosiahnuté so signifikantne nižším počtom injekcií afliberceptu v prvom roku (7,6 injekcií afliberceptu verzus 12,3 injekcií ranibizumabu) a tieto výsledky boli zachované aj v druhom roku liečby pri významne nižšom počte injekcií afliberceptu (4,2 injekcií afliberceptu verzus 4,7 injekcií ranibizumabu) [14, 11]. Bezpečnosť afliberceptu bola po dvojročnom sledovaní porovnateľná s ranibizumabom [11].
Predložená kazuistika a tiež naše praktické skúsenosti s afliberceptom v liečbe ďalších novodiagnostikovaných pacientov s vlhkou VPDM s okultnými či predominantne klasickými SRNM sú podobné výsledkom účinnosti afliberceptu z klinických skúšaní, v niektorých prípadoch ich dokonca prekonávajú.
V nedávnej dobe boli publikované prvotné dáta z niekoľkých štúdií preukazujúce klinický benefit použitia afliberceptu aj u pacientov so suboptimálnou odpoveďou na predchádzajúcu anti-VEGF liečbu [4, 15, 16]. V snahe dosiahnuť zlepšenie zrakovej ostrosti, liečiť pacientov nereagujúcich alebo nedostatočne reagujúcich na liečbu, rovnako v snahe zvládnuť tachyfylaxiu a redukovanú biologickú účinnosť po opakovanom podávaní intravitreálnych injekcií, sa v praxi skúša zámena (switch) liečebných látok. V porovnaní s ostatnými anti-VEGF látkami používanými v liečbe neovaskulárnej VPDM, aflibercept má vďaka svojej unikátnej štruktúre odlišné väzobné vlastnosti – vyššiu afinitu a širší záber nielen ku všetkým izoformám VEGF-A, ale aj k PlGF [7]. K dispozícii sú dáta preukazujúce klinický benefit, zahrňujúci stabilizáciu alebo zlepšenie zrakovej ostrosti a zlepšenie anatomického nálezu na OCT alebo predĺženie intervalov medzi injekciami po zmene liečby na aflibercept pri suboptimálnej odpovedi na iné anti-VEGF látky [4, 5, 10, 15, 16].
Podľa našich doterajších skúseností, zmena liečby na aflibercept u pacientov suboptimálne reagujúcich na iné anti-VEGF látky na našom pracovisku viedla po prvých 3 úvodných injekciách k zlepšeniu anatomického nálezu a k stabilizácii alebo aj zlepšeniu zrakovej ostrosti. Keďže odporúčaná dvojmesačná dávkovacia schéma (po 3 úvodných mesačných dávkach) v prvom roku liečby VPDM nevyžaduje monitorovanie v období medzi injekciami afliberceptu, pacienti nemusia chodiť na kliniku každý mesiac a tým sa lekárom aj pacientom znižuje záťaž spojená s mesačným monitorovaním a liečbou vlhkej formy VPDM.
ZÁVER
Doterajšie skúsenosti s afliberceptom v liečbe vlhkej formy VPDM preukázali napriek krátkemu sledovaciemu obdobiu dobrú účinnosť i bezpečnosť u novodiagnostikovaných pacientov pri všetkých typoch SRNM, ktorú je potrebné overiť v praxi z dlhodobého hľadiska. U pacientov, ktorým bola predchádzajúca anti-VEGF liečba zmenená na aflibercept, sme sledovali stabilizáciu aj zlepšenie anatomického a funkčného nálezu. Do tejto doby sa pri liečbe s afliberceptom neprejavili žiadne závažné nežiaduce účinky. Dávkovací režim afliberceptu v liečbe vlhkej formy VPDM má výhody v zníženej potrebe monitorovania, vyššom pohodlí pre pacienta i lekára a prináša možnosť menšieho výskytu nežiaducich účinkov súvisiacich s intravitreálnou aplikáciou, čím sa znižuje pracovná a ekonomická záťaž vlhkej formy VPDM na pacientov, lekárov v aplikačných centrách a celý zdravotný systém. Očakávame, že v druhom roku liečby pacientov s VPDM sa vďaka možnosti ďalšieho predlžovania intervalov medzi injekciami afliberceptu táto záťaž ešte viac zredukuje.
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmu a není podpořeno žádnou farmaceutickou firmou.
Do redakce doručeno dne 14. 10. 2014
Do tisku přijato dne 12. 2. 2015
MUDr. Juraj Bajaček
Oftalmologická klinika
Ústredná vojenská nemocnica SNP - FN
Generála Miloša Vesela 21
034 26 Ružomberok
e-mail: jbajacek@yahoo.com
Sources
1. Bressler, S.B., Bressler, N.M., Fine, S.L. et al.: Natural course of choroidal neovascular membranes within the foveal avascular zone in senile macular degeneration. Am J Ophthalmol, 93(2); 1982 : 157–163.
2. Congdon, N., O’Colmain, B., Klaver, C.C. et al.: Causes and prevalence of visual impairment among adults in the United States. Arch Ophthalmol, 122 (4); 2014 : 477–485.
3. Heier, J.S., Brown, M.D., Chong, V. et al.: Intravitreal aflibercept (VEGF Trap-Eye) in wet age-related macular degeneration. Ophthalmology, 119 (12); 2012 : 2537–2548.
4. Chang, A.A., Li, H., Broadhead, G.K. et al.: Intravitreal aflibercept for treatment-resistant neovascular age-related macular degeneration. Ophthalmology, 121; 2014 : 188–192.
5. Cho, H., Weber, M.L., Shah, C.P. et al.: Initial utilization of aflibercept in exudative age related macular degeneration. Eur J Ophthalmol, 24(4); 2014 : 576–581.
6. Martin, D.F., Maguire, M.G., Ying, G.S. et al: Ranibizumab and bevacizumab for neovascular age-related macular degeneration. N Engl J Med, 364(20); 2011 : 1897–1908.
7. Papadopoulos, N., Martin, J., Ruan, Q. et al.: Binding and neutralization of vascular endothelial growth factor (VEGF) and related ligands by VEGF Trap, ranibizumab and bevacizumab. Angiogenesis, 15(2); 2012 : 171–185.
8. Resnikoff, S., Pascolini, D., Etya’ale, D. et al.: Global data on visual impairment in the year 2002, Bull World Health Organ, 82(11); 2004 : 844–851.
9. Rudge, J.S., Holash, J., Hylton, D. et al.: VEGF Trap complex formation measures production rates of VEGF, providing a biomarker for predicting efficacious angiogenic blockade. Proc Natl Acad Sci U S A, 104(47); 2007 : 18363–18370.
10. Sawa, Y. et al.: Short-term outcomes of aflibercept for recurrent neovascular age-related macular degeneration in Japanese patients. E-poster PO-1531, World Ophthalmology Congress 2014, Tokyo, Japan, April 2–6, 2014.
11. Schmidt-Erfurth, U. et al.: Intravitreal aflibercept injection for neovascular age-related macular degeneration. Ninety-six week results of the VIEW studies. Ophthalmology, 121; 2014 : 193–201.
12. Schmier, J.K., Jones, M.L., Halpern, M.T.: The burden of age-related macular degeneration. Pharmacoeconomics, 24(4); 2006 : 319–334.
13. Soubrane, G., Cruess, A., Lotery, A. et al.: Burden and health care resource utilization in neovascular age-related macular degeneration: findings of a multicountry study. Arch Ophthalmol, 125(9); 2007 : 1249–1254.
14. Eylea (aflibercept injekčný roztok v liekovke) Súhrn charakteristických vlastností lieku. Berlin, Nemecko: Bayer Pharma AG: 2014.
15. Wykoff, C.C., Brown, D.M., Maldonado, M.E. et al.: Aflibercept treatment for patients with exudative age-related macular degeneration who were incomplete responders to multiple ranibizumab injections (TURF trial). Br J Ophthalmol, 98(7); 2014 : 951–955.
16. Yonekawa, Y., Andreoli, C., Miller, J.B. et al.: Conversion to aflibercept for chronic refractory or recurrent neovascular age-related macular degeneration. Am J Ophthalmol, 156(1); 2013 : 29–35.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2015 Issue 2-
All articles in this issue
- Retinální tubulace
- Výsledky implantace plného rohovkového kroužku (MyoRing) v léčbě keratokonu
- Zmena spektra primarne indikovaných operácií pre odlúpenie sietnice počas 15 rokov
- Aflibercept v klinickej praxi
- AZOOR: Akútna zonálna okultná vonkajšia retinopatia – kazuistika typu 3 ochorenia so superrýchlym návratom zraku
- Příběh jedné papily
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Příběh jedné papily
- Výsledky implantace plného rohovkového kroužku (MyoRing) v léčbě keratokonu
- AZOOR: Akútna zonálna okultná vonkajšia retinopatia – kazuistika typu 3 ochorenia so superrýchlym návratom zraku
- Aflibercept v klinickej praxi
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career



