-
Medical journals
- Career
Katetrizační ablace akcesorních spojek: vyřešená otázka?
Authors: L. Haman P. Pařízek 1,2 2
Authors‘ workplace: Katedra válečného vnitřního lékařství Fakulty vojenského zdravotnictví Univerzity obrany, Hradec Králové 1; I. interní klinika LF UK a FN Hradec Králové 2
Published in: Kardiol Rev Int Med 2006, 8(Supplementum): 20-23
Overview
Definice:
Akcesorní spojky jsou vrozeným anomálním atrioventrikulárním spojením, které predisponuje k vzniku supraventrikulárních tachyarytmií.Hlavní znaky:
Existují 2 hlavní formy akcesorních spojek – atrioventrikulární (98 %), atriofascikulární (2 %). Klinické projevy se objevují nejčastěji během prvního roku života a na začátku dospívání formou supraventrikulární tachykardie, případně fibrilace síní (30 %). Zhruba 50 % pacientů může být asymptomatických. Vzácně dochází k náhlé srdeční smrti na podkladě fibrilace komor, která je spuštěna fibrilací síní s rychlým převodem spojkou na komory.Terapie:
Preferovanou terapií pro symptomatické pacienty je katetrizační ablace jako metoda s vysokou úspěšností a nízkým rizikem komplikací.Klíčová slova:
preexcitace - akcesorní spojky - katetrizační ablaceÚvod
Vrozené anomální atrioventrikulární spojení – akcesorní spojka (accessory pathway - AP) způsobuje předčasnou depolarizaci komorového myokardu, tzv. komorovou preexcitaci. Nejčastější formou preexcitace je tzv. Wolffův-Parkinsonův-Whiteův (WPW) syndrom, který je označením pro symptomatické paroxyzmy palpitací na podkladě supraventrikulární tachyarytmie a s obrazem komorové preexcitace na klidové křivce. Až 50 % pacientů s komorovou preexcitací nemá symptomy, ale i tito pacienti jsou ohrožení náhlou srdeční smrtí způsobenou fibrilací síní s rychlým převodem na komory přes AP. Za této situace může dojít k vzniku fibrilace komor. Cca 40 % všech AP postrádá kapacitu pro antegrádní vedení – tehdy se jedná o tzv. skryté (pouze retrográdně vedoucí) AP.
V léčbě pacientů s AP došlo k revoluční změně rozvojem katetrizační radiofrekvenční (RF) ablace, která vede u většiny pacientů k eliminaci AP, a tím k definitivnímu vyléčení.
Epidemiologie
Roční incidence nových případů pacientů s WPW syndromem je odhadována na 4 na 100 000 obyvatel a prevalence elektrokardiografických známek WPW je popisována v rozmezí 0,1 % až 0,3 % [1]. Muži jsou postiženi 2krát častěji než ženy a je popisována bimodální věková distribuce manifestace s vrcholy během prvního roku života a na začátku dospívání.
Anatomie a patofyziologie
Atrioventrikulární spojky
Ve starší literatuře jsou nazývány Kentovy svazky. Klasické elektrokardiografické známky preexcitace (obr. 1) jsou u 98 % pacientů výsledkem akcesorního AV-spojení, které je zbytkem reziduální tkáně po segmentaci embryonální srdeční trubice na síňové a komorové oddíly. Histologicky je většina AP tvořena vlákny běžného myokardu, které přemosťují AV-prstenec a přenášejí elektrický signál ze síňového na komorový myokard (obr. 2). Vedení AP je na rozdíl od normálního převodního systému frekvenčně nezávislé. Nejčastější lokalizací AP je volná stěna levé komory – 50-60 %, 20-30 % AP se nachází v posteroseptální oblasti, 10-20 % v oblasti volné stěny pravé komory. Vícečetné AP jsou popisovány u 5-20 % pacientů s preexcitačním syndromem.
Image 1. 12svodové EKG s obrazem preexcitace. Obraz preexcitace (vlna delta, krátký PQ-interval a široký QRS-komplex) u pacienta s akcesorní AV-spojkou na levé volné stěně (negativní delta-vlna ve svodech I, aVL, obraz pseudoblokády pravého Tawarova raménka). 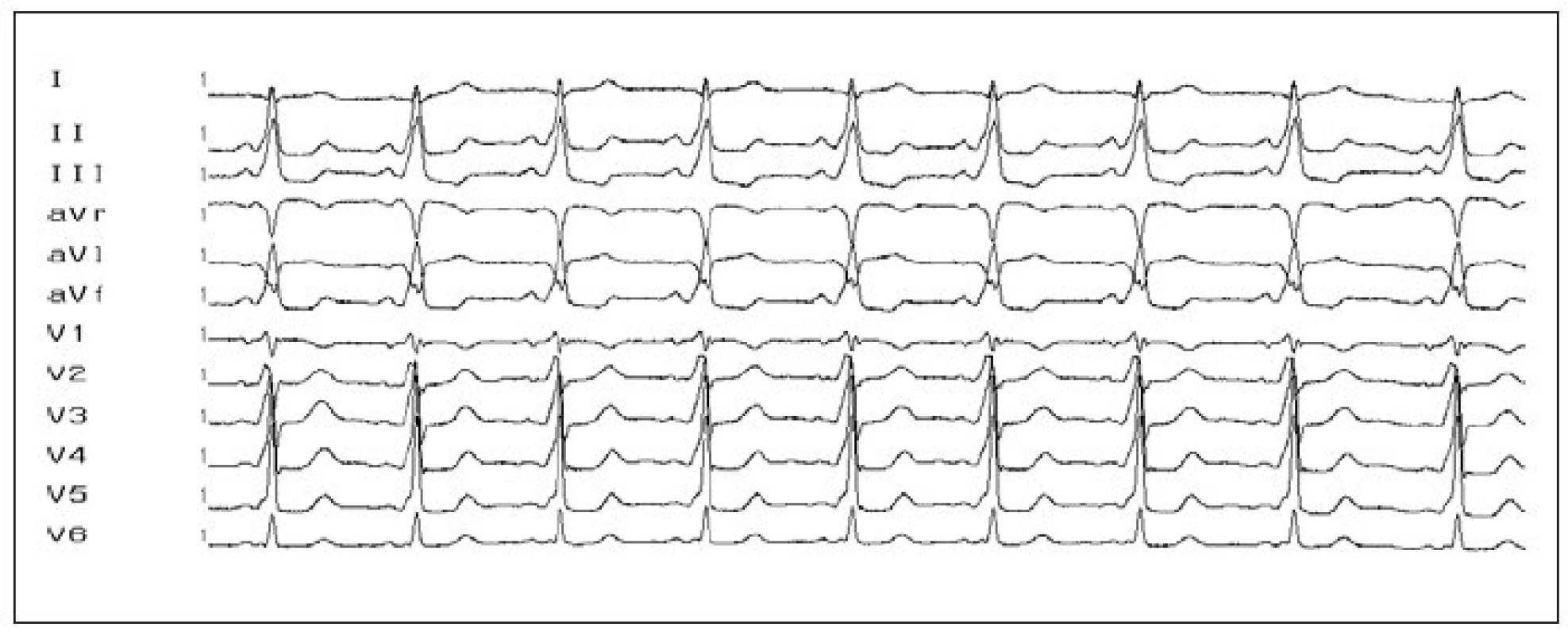
Image 2. Schematické znázornění průběhu akcesorní AV-spojky. 
A – svalovina síně, V – svalovina komor, MV – mitrální chlopeň, FA – fibrózní anulus, CS – koronární sinus, CA – koronární tepna, AP – akcesorní spojky. Skryté (pouze retrográdně vedoucí) akcesorní spojky
Tato varianta AP postrádá kapacitu pro vedení antegrádním směrem. To znamená, že tito pacienti nemají na povrchovém EKG známky preexcitace, ale mohou mít charakteristické ortodromní atrioventrikulární reentry tachykardie (AVRT) s antegrádním vedením AV-uzlem a retrográdním vedením přes AP. Výskyt skrytých AP je pravděpodobně vyšší než spojek s obousměrným vedením a je podhodnocen díky obtížnější diagnostice.
Atriofascikulární a nodofascikulární spojky (tzv. Mahaimova vlákna)
Tyto spojky jsou popisovány u cca 2 % pacientů s preexcitačním syndromem a začínají v myokardu pravé síně nebo v oblasti AV-uzlu a ústí do distální části pravého Tawarova raménka. Spojka vede pouze jedním směrem (antegrádně) s jasně dekrementálními vlastnostmi a tachykardie má díky pravostranné lokalizaci typický obraz blokády levého Tawarova raménka.
Klinické nálezy
Asymptomatické preexcitace
Ačkoliv se jedná o kongenitální abnormalitu, až 50 % pacientů nemá symptomy a tato abnormalita je nalezena pouze náhodně.
Palpitace
Pacienti s AP si nejčastěji stěžují na náhle vznikající a končící palpitace s rychlým bušením srdce, které jsou někdy doprovázeny hrudním diskomfortem, dyspnoí a někdy až synkopou.
Náhlá srdeční smrt
Nejčastěji je důsledkem fibrilace síní s rychlým převodem na komory přes AP, která degeneruje do fibrilace komor, a může být i první manifestací WPW-syndromu u dříve asymptomatických pacientů.
Tachykardie na podkladě přítomnosti AP
Ortodromní AVR-tachykardie
Je nejčastějším typem tachykardie, představuje paroxyzmální, pravidelnou, úzkokomplexovou tachykardii o frekvenci 150-250/min (obr. 3). P-vlna je při ortodromní AVRT lokalizována za komplexem QRS, obvykle v segmentu ST nebo splývá s vlnou T.
Image 3. Ortodromní AVRT. Úzkokomplexová tachykardie (antegrádní šíření přes AV-uzel – viz potenciál Hisova svazku ve svodu HBE). Lokalizace akcesorní spojky – laterální stěna levé komory (v CS 9–10 – potenciály z ústí koronárního sinu – je malý komorový potenciál vzdálený od většího síňového potenciálu, zatímco v CS 1–2 – potenciály z oblasti levé volné stěny – je síňový potenciál nejčasnější a je prakticky splynulý s komorovým potenciálem). 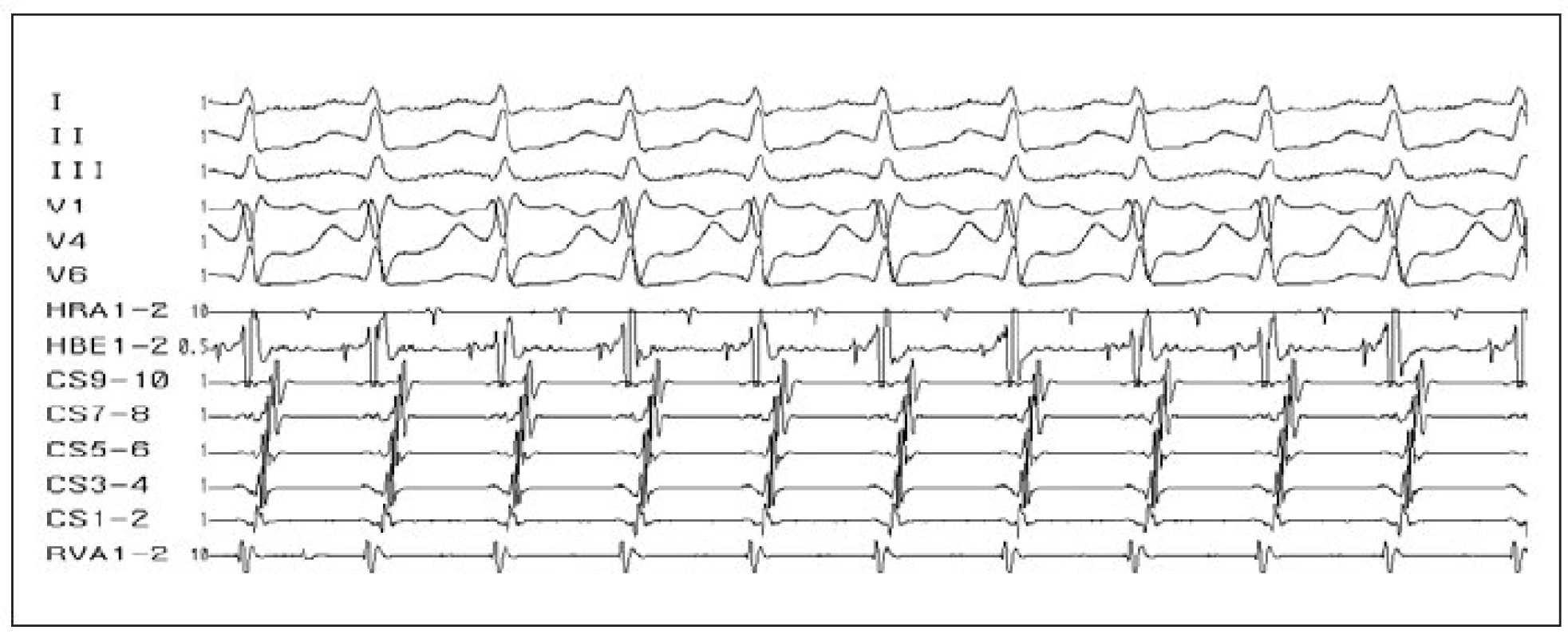
I–III, V1–V6 – svody povrchového EKG, HRA – potenciály z horní pravé síně, HBE – záznam katétru v oblasti Hisova svazku, CS 1–10 – multipolární záznam z koronárního sinu, RVA – potenciály z hrotu pravé komory. Antidromní AVR-tachykardie
V průběhu antidromní AVRT je AP antegrádní větví okruhu reentry a k retrográdní aktivaci síní dochází přes komplex AV-uzel – Hisův svazek. Tato arytmie je méně častá (cca 5 % pacientů). Komplexy QRS mají tvar maximální preexcitace díky aktivaci komor probíhající výlučně přes AP (obr. 4).
Image 4. Antidromní AVRT. Širokokomplexová tachykardie (antegrádní vedení přes akcesorní spojku). Lokalizace akcesorní spojky – laterální stěna levé komory (v CS 9–10 – potenciály z ústí koronárního sinu – je větší síňový potenciál vzdálený od menšího komorového potenciálu, zatímco v CS 1–2 – potenciály z oblasti levé volné stěny – je komorový potenciál nejčasnější a je prakticky splynulý se síňovým potenciálem). 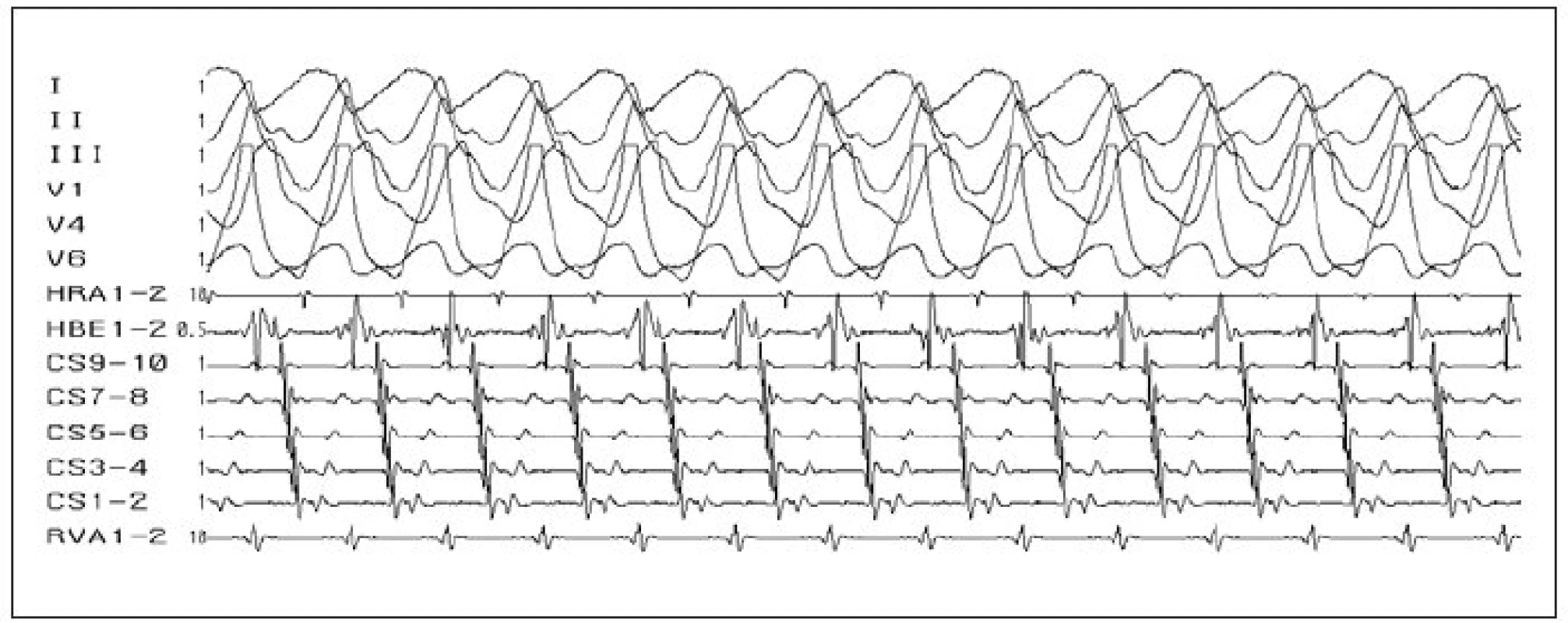
I–III, V1–V6 – svody povrchového EKG, HRA – potenciály z horní pravé síně, HBE – záznam katétru v oblasti Hisova svazku, CS 1–10 – multipolární záznam z koronárního sinu, RVA – potenciály z hrotu pravé komory. Fibrilace síní
Fibrilace síní se může objevit u více než 1/3 pacientů s WPW-syndromem (obr. 5). Patogeneze fibrilace síní u WPW-syndromu není zcela známa.
Image 5. Fibrilace síní. Fibrilace síní (rychlé a nepravidelné, chaotické, síňové potenciály ve svodech HRA, HBE a CS), v povrchových svodech s různě vyjádřeným stupněm preexcitace (různě široké QRS-komplexy) u pacienta s akcesorní spojkou v posteroseptální oblasti (negativní delta-vlna ve svodech II, III). 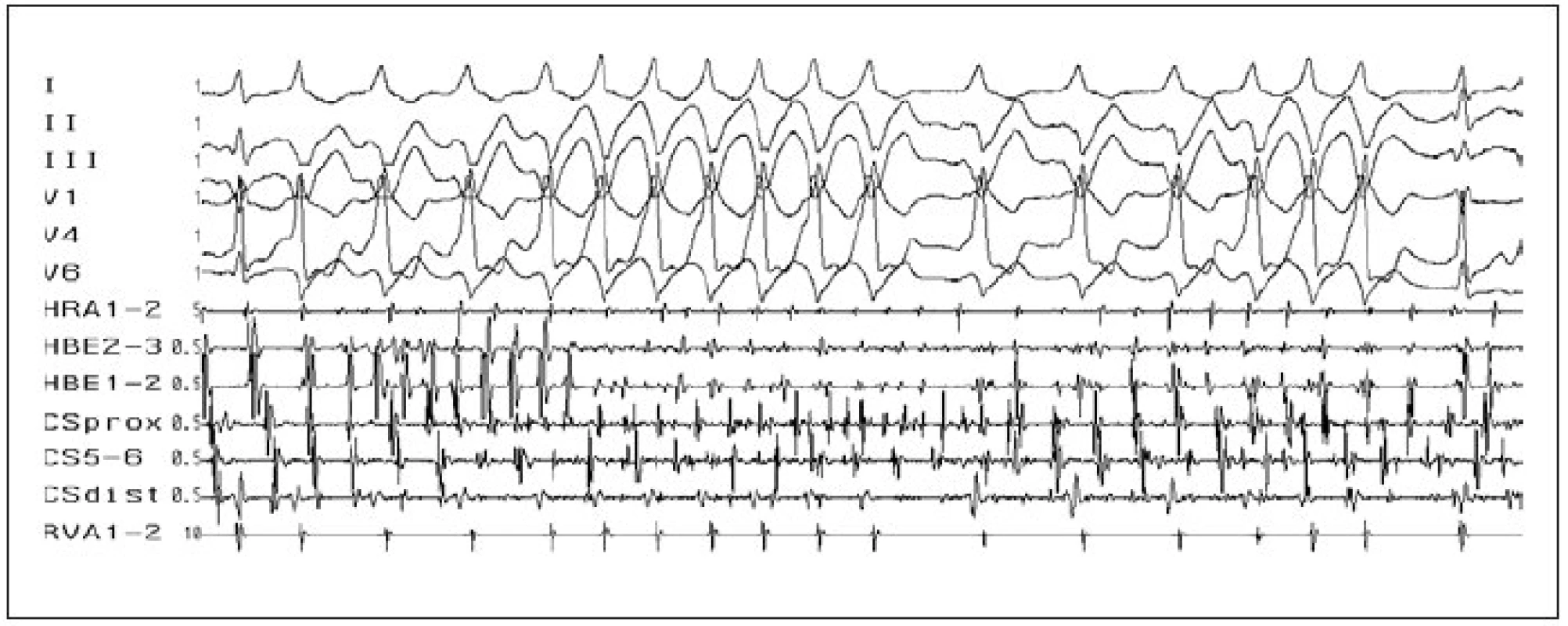
I–III, V1–V6 – svody povrchového EKG, HRA – potenciály z horní pravé síně, HBE – záznam katétru v oblasti Hisova svazku, CS 1–10 – multipolární záznam z koronárního sinu, RVA – potenciály z hrotu pravé komory. Permanentní forma junkční reciproční tachykardie
Patří mezi vzácné nálezy. Bývá nepřetržitá (incesantní) a může vést k rozvoji tachykardické kardiomyopatie. Mechanizmem tachykardie je AV reentry používající skrytou AP jako retrográdní větve reentry okruhu. Tato AP má dekrementální vlastnosti a lokalizována je většinou posteroseptálně.
Stratifikace rizika
Fibrilace síní představuje u pacientů s WPW-syndromem a rychle vedoucí AP s ohledem na možnost degenerace do fibrilace komor život ohrožující arytmii [2]. Incidence náhlé smrti u pacientů s WPW-syndromem se odhaduje na 0,15-0,40 % a asi polovina náhlých smrtí je prvním projevem tohoto syndromu. Ukazatele zvýšeného rizika náhlé smrti zahrnují nejkratší preexcitovaný RR-interval při fibrilaci síní menší než 250 ms, anamnézu symptomatických tachykardií a mnohočetné AP. Vysoká incidence náhlé smrti je také popsána u familiárního WPW-syndromu, který je však velmi vzácný [3].
Neinvazivní vyšetřovací metody jsou v rizikové stratifikaci nespolehlivé a zlatým standardem k hodnocení rizika u všech pacientů s AP se stalo elektrofyziologické vyšetření.
Katetrizační ablace
Katetrizační ablace znamená lokalizaci AP za pomoci zaznamenávání elektrické aktivace okolo AV-prstenců (obr. 6) a následnou aplikaci RF-energie do místa spojky za použití ablačního katétru (obr. 7). Jako první referovali o úspěšné ablaci AP za použití RF-energie Borggrefe et al [4] již v roce 1987. Výhodou RF-energie je dobrá řiditelnost aplikace a výsledná malá, dobře ohraničená nekróza srdeční tkáně.
Image 6. Lokalizace akcesorní spojky. Potenciál akcesorní spojky (šipka) na ablačním katétru (USER 1) v optimálním místě k RF-ablaci (prakticky splynulý síňový a komorový potenciál, nejčasnější komorový potenciál). 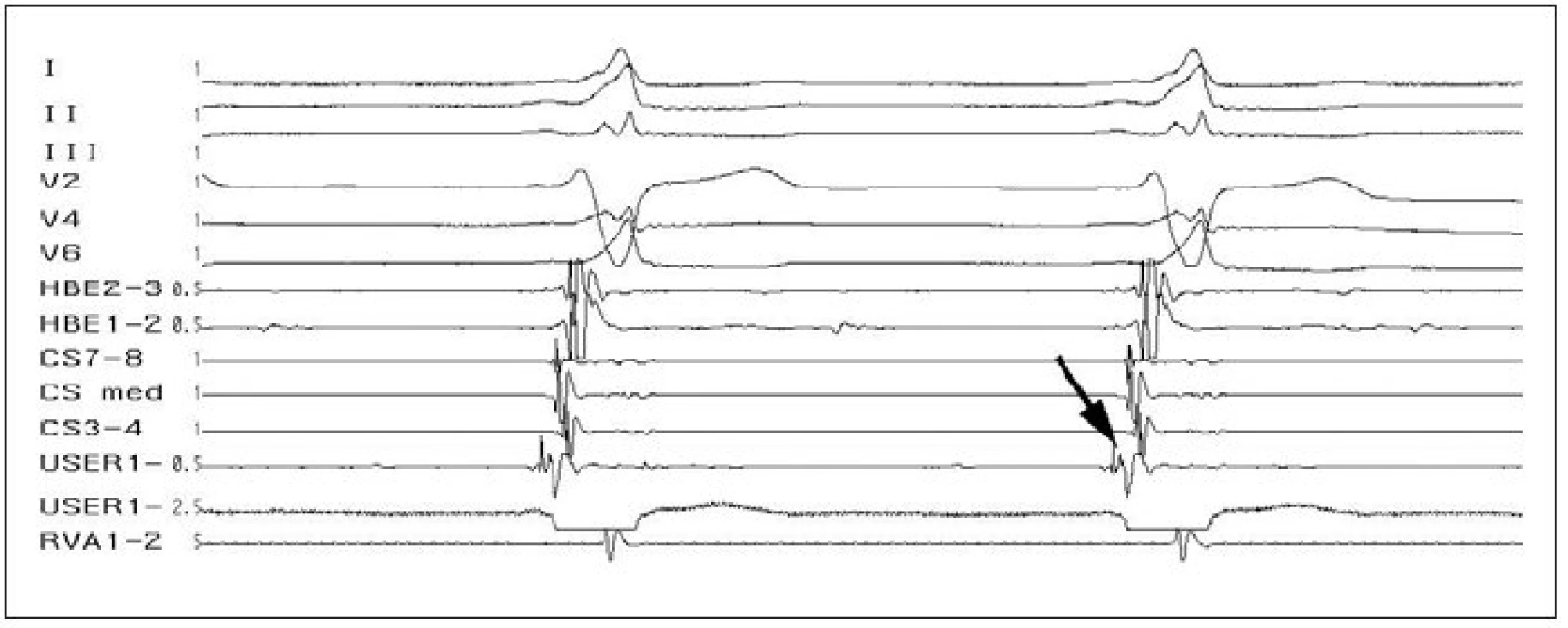
Image 7. Úspěšná ablace akcesorní spojky. Obraz preexcitace na povrchovém EKG, akcesorní spojka lokalizována na levé volné stěně (splynulý potenciál síní a komor v koronárním sinu z oblasti levé volné stěny – CSdist). Začátek aplikace RF-energie (černá šipka), v průběhu 3. sekundy aplikace RF-energie (šedá šipka) přerušení vedení akcesorní spojkou se změnou tvaru QRS-komplexu na povrchovém EKG a změnou aktivace v koronárním sinu – odpojení potenciálu síní a komor. 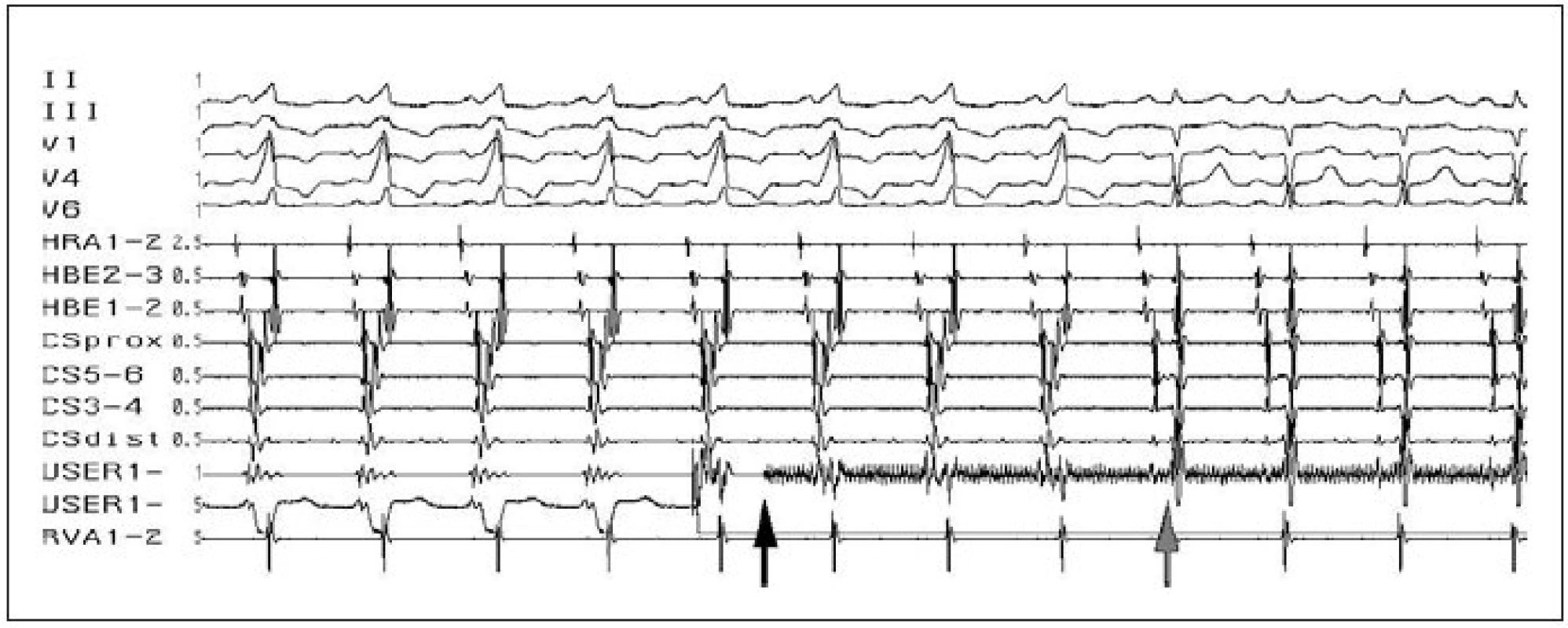
I–III, V1–V6 – svody povrchového EKG, HRA – potenciály z horní pravé síně, HBE – záznam katétru v oblasti Hisova svazku, CS 1–10 – multipolární záznam z koronárního sinu, USER – záznam z ablačního katétru, RVA – potenciály z hrotu pravé komory. K dosažení AP lokalizovaných v pravé části srdce je mapovací/ablační katétr zaváděn do pravé síně nejčastěji femorálním transvenózním přístupem. K dosažení AP lokalizované v levé části srdce je mapovací/ablační katétr obvykle zaváděn do levé komory retrográdním transaortálním přístupem přes femorální tepnu. Alternativou je dosažení levé síně z pravé síně, buď pomocí foramen ovale patens nebo transseptální punkcí.
Výsledky RF-ablací u pacientů s AP
Celková úspěšnost ve velkých souborech je přibližně 95% [5-7]. U levostranných AP se transseptální a retrográdní přístup neliší účinností, délkou výkonu a dobou vystavení rentgenovému záření ani počtem komplikací a kombinací těchto přístupů lze dosáhnout až 100% úspěšnosti. Většinu epikardiálně umístěných AP se podaří úspěšně přerušit přístupem z koronárního sinu [8]. Nižší úspěšnost a častější recidivy jsou u posteroseptálních spojek a u všech pravostranných AP. Recidivy vedení AP se v jednotlivých souborech různí, ale nepřesahují 5 % [5,6]. Většinou jsou tyto AP úspěšně odstraněny při opakovaném výkonu, pokud u nich nedojde k pozdnímu přerušení vedení AP s odstupem od výkonu, které se přičítá procesu hojení v místě poškození RF-energií. Kvalita života (zejména subjektivní pocit zdraví, schopnost fyzické zátěže, práce a řízení motorových vozidel) se po ablaci zlepšuje [9]. Kvalita života a tolerance zátěže jsou po úspěšné ablaci vyšší proti skupině nemocných s medikamentózní léčbou [10]. Někteří pacienti ale mají po úspěšné ablaci zbytkové příznaky či tzv. pseudorecidivy, jejichž příčinou bývají síňové a komorové extrasystoly nebo paroxyzmy fibrilace síní.
Komplikace radiofrekvenční ablace
Celkový počet komplikací ablační RF-procedury se pohybuje okolo 5 % a zahrnuje komplikace vzniklé při manipulaci s katétry a při aplikaci RF-energie. Incidence komplikací ve velké multicentrické evropské radiofrekvenční studii [7] činila 4,4 % a v jedné z posledních studií, publikované Calkinsem et al [5] byly popsány velké komplikace u 3 % a malé komplikace u 8,2 % pacientů. Mortalita v důsledku výkonu kolísá od 0 do 0,2 % [5-7]. Srdeční tamponáda se ve větších souborech pacientů vyskytuje do 1 % a v naprosté většině byla vyřešena perikardiocentézou bez chirurgické intervence. Výskyt tromboembolických komplikací je podle prospektivních studií kolem 1 %, ale pro pacienty bez rizikových faktorů (fibrilace síní atd) byl významně nižší [11]. Incidence kompletní AV-blokády se pohybuje od 0,17 do 1,0 %, je však relativně častou komplikací (36 %) při ablacích parahisálních a paranodálních drah [12]. Vzhledem k této skutečnosti by ablace v této lokalizaci měly být rezervovány pro pacienty s rizikovými a výrazně symptomatickými tachyarytmiemi, nebo by měly být ablace v této lokalizaci prováděny jiným druhem energie, jako např. technikou kryoablace.
Solomon et al [13] neprokázali vliv RF-energie na věnčité tepny při ablaci z endokardiálního přístupu u skupiny pacientů, u kterých byla provedena koronarografie bezprostředně před a po ablaci a poté 2 měsíce po ablaci. Při ablaci z větve koronárního sinu byl popsán asymptomatický přechodný spazmus posterolaterální větve (klinicky, laboratorně i echokardiograficky) a byl popsán infarkt myokardu při nepoznané aplikaci RF-energie do ramus circumflexus s kompletním uzávěrem tepny při koronarografii o 30 min později, který byl řešen angioplastikou.
Nejčastějšími malými komplikacemi jsou obecně katetrizační komplikace, jako jsou trombózy či hematomy v třísle, arteriovenózní píštěle atd.
Indikace ke katetrizační ablaci AP
Symptomatičtí pacienti
Katetrizační ablace akcesorní spojky je u symptomatických pacientů první léčebnou možností [14].
Asymptomatičtí pacienti
U asymptomatických pacientů není stratifikace rizika a indikace k invazivnímu vyšetření a terapii dosud vyřešena definitivně. Asi u 1/3 pacientů s asymptomatickou preexcitací se nakonec rozvinou symptomy tachykardií a jen asi 20 % pacientů má AP s vysokou antegrádní převodní kapacitou. Katetrizační ablace byla proto indikována jen u asymptomatických osob s rizikovým povoláním (letci, řidiči apod). Podle nedávné studie [15] je ale elektrofyziologické testování u asymptomatických nemocných významné pro předpověď dalších arytmických příhod (212 pacientů, z nichž při více než 3letém sledování mělo 33 pacientů symptomy tachyarytmie a u 3 z nich došlo ke vzniku fibrilace komor včetně jedné náhlé smrti). Nejdůležitějšími faktory pro stratifikaci rizika byly vyvolatelnost AVRT nebo fibrilace síní a přítomnost více AP. Dle další studie [16] redukuje profylaktická katetrizační ablace riziko život ohrožujících arytmií u asymptomatických, rizikových dětí s WPW-syndromem (z 27 dětí bez RF-ablace mělo 44 % arytmickou příhodu, 2 fibrilaci komor a 1 náhle zemřelo).
Závěr
Katetrizační ablace AP je jistě vyřešenou otázkou pro symptomatické nemocné, u nichž je léčba RF-ablací metodou volby. U asymptomatických nemocných je odpověď zatím stále nejednoznačná, i když v poslední době se miska vah přiklání na stranu elekrofyziologického vyšetření a následné katetrizační ablace. I nadále je asymptomatické pacienty nutno posuzovat individuálně, ale při souhlasu nemocného doporučujeme u všech elektrofyziologické vyšetření ke zhodnocení rizika náhlé srdeční smrti s případnou návazností katetrizační ablace AP.
MUDr. Luděk Haman, Ph.D.1,2
MUDr. Petr Pařízek, Ph.D.2
1Katedra válečného vnitřního lékařství Fakulty vojenského zdravotnictví Univerzity obrany, Hradec Králové
21. interní klinika FN Hradec Králové
MUDr. Luděk Haman, Ph.D. (1971)
Promoval na LF Univerzity Karlovy a Vojenské lékařské akademie Jana Evangelisty Purkyně v Hradci Králové (1995). Složil atestaci 1. stupně v oboru vnitřní lékařství (1998) a nadstavbovou atestaci z kardiologie (2002). Pracuje na I. interní klinice FN Hradec Králové jako odborný lékař se specializací na elektrofyziologii a katetrizační ablace. Je autorem či spoluautorem více než 50 českých a zahraničních publikací.
Sources
1. Munger TM, Packer DL, Hammill SC et al. A population study of the natural history of Wolff-Parkinson-White syndrome in Olmsted County, Minnesota, 1953-1989. Circulation 1993; 87 : 866-873.
2. Priori SG, Aliot E, Blomstrom-Lundquist C et al. Task force on sudden cardiac death of the European Society of Cardiology. Eur Heart J 2001; 22 : 1374-1450.
3. Gollob MH, Green MS, Tang AS et al. Identification of a gene responsible for familial Wolff-Parkinson-White syndrome. N Engl J Med 2001; 344 : 1823-1831.
4. Borggrefe M, Budde T, Podczek A et al. High frequency alternating current ablation of an accessory pathway in humans. J Am Coll Cardiol 1987; 10 : 576-582.
5. Calkins H, Yong P, Miller JM, et al. Catheter Ablation of Accessory Pathways, Atrioventricular Nodal Reentrant Tachycardia, and the Atrioventricular Junction: Final Results of a Prospective, Multicenter Clinical Trial. Circulation 1999; 99 : 262-270.
6. Scheinman MM, Huang S. The 1998 NASPE prospective catheter ablation registry. Pacing Clin Electrophysiol 2000; 23 : 1020-1028.
7. Hindricks G. Multicentre European Radiofrequency Survey (MERFS): Complications of radiofrequency catheter ablation of arrhythmias. Eur Heart J 1993; 14 : 1644-1653.
8. Langberg JJ, Ching Man K, Vorperian VR et al. Recognition and catheter ablation of subepicardial accessory pathways. J Am Coll Cardiol 1993; 22 : 1100-1104.
9. Bubien RS, Knotts-Dolson SM, Plumb VJ et al. Effect of Radiofrequency Catheter Ablation on Health-Related Quality of Life and Activities of Daily Living in Patients With Recurrent Arrhythmias. Circulation 1996; 94 : 1585-1591.
10. Lau CP, Tai YT, Lee PWH. The effects of radiofrequency ablation versus medical therapy on the quality-of-life and excercise capacity in patients with accessory pathway-mediated supraventricular tachycardia: a treatment comparison study. PACE 1995; 18 : 424-432.
11. Saul PS, Epstein MR, Triedman JK et al. Embolic complications associated with RF ablation procedures: Does the risk extend beyond the procedure? (abstract) Pacing Clin Electrophysiol 1995; 18 : 818 II.
12. Yeh SJ, Wang CC, Wen MS et al. Characteristics and radiofrequency ablation therapy of intermediate septal accessory pathway. Am J Cardiol 1994; 73 : 50-56.
13. Solomon AJ, Tracy CM, Swartz JF et al. Effect on coronary artery anatomy of radiofrequency catheter ablation of atrial sites of accessory pathways. J Am Coll Cardiol 1993; 21 : 1440-1444.
14. Fiala M. Doporučené postupy pro diagnostiku a léčbu supraventrikulárních tachyarytmií. Cor Vasa 2005; 47(9, Suppl K):18-39.
15. Pappone C, Santinelli V, Rosanio S et al. Usefulness of invasive electrophysiologic testing to stratify the risk of arrhythmic events in asymptomatic patients with Wolff-Parkinson-White pattern. J Am Coll Cardiol 2003; 41 : 239-244.
16. Pappone C, Manguso F, Santinelli R et al. Radiofrequency ablation in children with asymptomatic Wolff-Parkinson-White syndrome. N Engl J Med 2004; 351 : 1197-1205.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2006 Issue Supplementum-
All articles in this issue
- Katetrizační ablace srdečních arytmií v České republice – současný stav
- Neselektivní ablace AV-uzlu: nové aspekty v době kurativní léčby fibrilace síní a srdeční resynchronizační terapie
- Katetrizační ablace atrioventrikulární nodální reentry tachykardie: léčba první volby?
- Katetrizační ablace akcesorních spojek: vyřešená otázka?
- Katetrizační léčba typického flutteru síní včera a dnes
- Katetrizační ablace fibrilace síní: naděje pro všechny výrazně symptomatické pacienty
- Katetrizační ablace postincizionálních tachykardií: konečné řešení nebo paliativní léčba?
- Katetrizační ablace komorových tachykardií
- Katetrizační ablace fibrilace komor: realita nebo fikce?
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Katetrizační ablace atrioventrikulární nodální reentry tachykardie: léčba první volby?
- Katetrizační léčba typického flutteru síní včera a dnes
- Katetrizační ablace akcesorních spojek: vyřešená otázka?
- Neselektivní ablace AV-uzlu: nové aspekty v době kurativní léčby fibrilace síní a srdeční resynchronizační terapie
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


